'Dùng Thuốc Theo Cá Thể' đối với thuốc điều trị đái tháo đường

Trungtamthuoc.com - Chương 11 "Dùng thuốc theo cá thể đối với thuốc điều trị đái tháo đường" sẽ phân tích được khả năng ứng dụng của gen được trong dùng thuốc theo cá thể đối với các thuốc điều trị đái tháo đường.
Trường Đại học Dược Hà Nội, Bộ môn Hóa Sinh - Khoa Công Nghệ Sinh Học
CHƯƠNG 11, Trang 139-151, Giáo trình GEN DƯỢC HỌC - ẢNH HƯỞNG CỦA GEN ĐẾN ĐÁP ỨNG THUỐC, Tải PDF sách TẠI ĐÂY
CHỦ BIÊN
PGS.TS. Phùng Thanh Hương
PGS.TS. Đỗ Hồng Quảng
CÁC TÁC GIẢ THAM GIA BIÊN SOẠN
PGS.TS. Phùng Thanh Hương
PGS.TS. Đỗ Hồng Quảng
PGS.TS. Nguyễn Văn Rư
PGS.TS. Nguyễn Thị Lập
TS. Nguyễn Quốc Bình
Cho đến nay, điều trị đái tháo đường (ĐTĐ) typ 1 vẫn chủ yếu dựa vào Insulin với nhiều dạng bào chế khác nhau. Các nghiên cứu về gen trong ĐTĐ typ 1 hầu hết tập trung vào các gen liên quan đến bệnh sinh ĐTĐ, hầu như chưa có những nghiên cứu về ảnh hưởng của đa hình gen đến đáp ứng điều trị với insulin. Các nghiên cứu về dùng thuốc theo cá thể chủ yếu tập trung vào thuốc điều trị ĐTĐ typ 2.
Bên cạnh những biện pháp điều trị thông qua thay đổi chế độ ăn uống, sinh hoạt, cho đến nay, đã có nhiều thuốc hạ Glucose máu đường uống được sử dụng trong điều trị ĐTĐ typ 2. Tuy nhiên, nhiều nghiên cứu cho thấy chỉ khoảng 53% bệnh nhân ĐTĐ typ 2 dùng các thuốc hạ glucose đường uống có đáp ứng điều trị tốt, giảm được HbA1c xuống dưới 7%. Có sự dao động về cả hiệu quả điều trị và tác dụng không mong muốn giữa các bệnh nhân. Thực tế này do nhiều nguyên nhân khác nhau, bao gồm cả các yếu tố phi sinh học như khả năng tiếp cận với dịch vụ y tế, nghiệp vụ kê đơn của thầy thuốc và các yếu tố sinh học như tuổi, giới, trọng lượng cơ thể, sự khác biệt về chức năng gan, thận, ruột... cũng như sự khác biệt về di truyền. Dưới đây là tổng hợp những kết quả nghiên cứu về cá thể hóa điều trị liên quan đến một số thuốc điều trị ĐTĐ typ 2 phổ biến nhất.
1 Metformin
Metformin là thuốc được dùng rộng rãi trong điều trị ĐTĐ typ 2. Tuy nhiên, có khoảng 1/3 người dùng metformin không đạt được mức kiểm soát glucose máu cần thiết. Bên cạnh đó, gần 63% bệnh nhân gặp rối loạn tiêu hóa, khoảng 5 - 10% phải ngưng dùng thuốc.
Ở pH sinh lý của cơ thể, metformin tích điện dương, do đó, khó qua được các màng sinh học mà phải nhờ các protein vận chuyển. Ở gan, mô đích quan trọng của metformin, thuốc vào tế bào gan thông qua organic cation transporter 1 (OCT1), một protein vận chuyển ở tế bào gan (Hình 11.1). Một số nghiên cứu đã chứng minh có sự liên quan giữa những kiểu gen mang biến thể của gen SLC22C1 (gen mã hóa OCT1) với đáp ứng điều trị bởi metformin, tùy từng loại đa hình sẽ có thể làm thay đổi đáp ứng điều trị theo một cách khác nhau. Một nghiên cứu sử dụng test dung nạp glucose đường uống với các bệnh nhân điều trị bằng metformin cho thấy những người mang biến thể gen mã hóa OCT1 làm giảm chức năng bơm vận chuyển này có AUC glucose cao hơn đáng kể những người mang kiểu gen bình thường. Trong nghiên cứu này, vai trò của biến thể hóa OCT1 đối với đáp ứng điều trị bởi metformin không chỉ làm giảm hiệu quả kiểm soát glucose máu mà còn làm tăng nguy cơ tác dụng không mong muốn khi dùng thuốc. Một nghiên cứu khác tiến hành trên 2166 bệnh nhân ĐTĐ typ 2 dùng metformin cho thấy các bệnh nhân có kiểu gen mang alen biến thể làm giảm chức năng OCT1 có nguy cơ bị tác dụng không mong muốn trên hệ tiêu hóa cao gấp 2,4 lần những người mang kiểu gen bình thường.
Bên cạnh OCT1, OCT2 là bơm vận chuyển biểu hiện nhiều ở màng đáy của tế bào ống thận, đóng vai trò quan trọng (80%) trong thanh thải của metformin qua thận. Một số nghiên cứu trên người khỏe mạnh cũng như bệnh nhân ĐTĐ cho thấy, mối liên quan giữa biến thể gen làm giảm chức năng OCT2 với hiện tượng tăng nồng độ huyết tương và giảm độ thanh thải của metformin. Một nghiên cứu trên 209 bệnh nhân ĐTĐ ở Trung Quốc, dùng metformin hàng ngày với liều 1500 mg/ngày trong vòng 1 năm cho thấy mục tiêu điều trị làm giảm HbA1c ở những người mang kiểu gen OCT2 mang cả 2 alen làm giảm chức năng của bơm này đạt được tốt hơn so với người mang kiểu gen bình thường.
Ngoài các OCT, MATE1 (Multidrug and toxin extrusion 1) là một loại protein vận chuyển biểu hiện nhiều ở màng đỉnh của tế bào biểu mô thận, cũng đóng vai trò quan trọng trong sự bài xuất của metformin ra đường nước tiểu. Một nghiên cứu đã ghi nhận những người mang cả 2 alen biến thể làm giảm chức năng MATE1 (rs2289669G>A) đều xuất hiện giảm thanh thải metformin. Một vài nghiên cứu khác đã khẳng định mối liên quan giữa biến thể này với sự tăng hiệu quả giảm HbA1c bởi metformin.
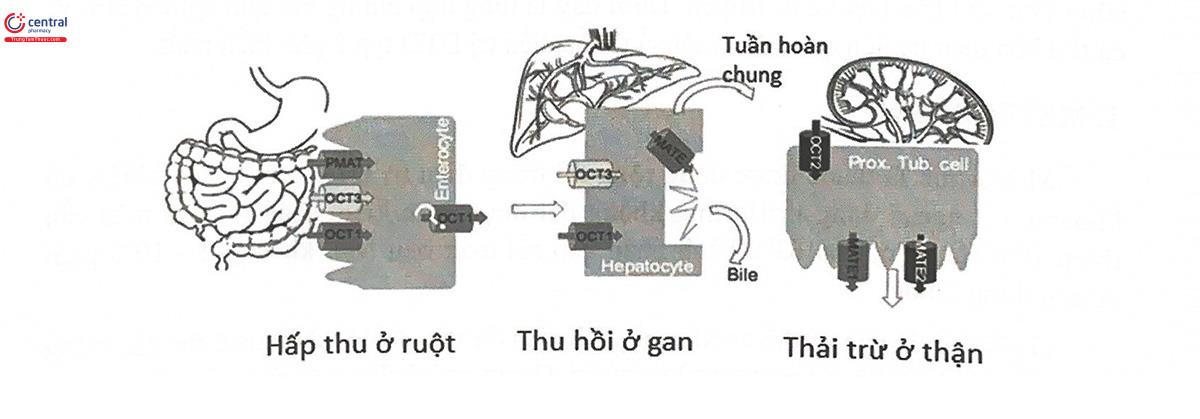
Mức độ ảnh hưởng của các biến thể gen liên quan đến sự vận chuyên, phân bố, đào thải metformin càng thể hiện rõ khi có sự xuất hiện đồng thời các alen biến thể của các gen đó trong cùng một cá thể. Trong một nghiên cứu năm 2013, trong khi biến thể c.808 (rs316019) của gen mã hóa OCT2 không ảnh hưởng đáng kể đến sự đào thải metformin qua thận thì những người mang Haplotype gồm cả alen biến thể này và alen biến thể rs2252281 của gen MATE1 có độ thanh thải tăng rõ rệt. Hiện tượng tương tự được ghi nhận với những người mang Haplotype gồm cả alen biến thể rs2252281 của gen MATE1 và alen biến thể rs2289669 hoặc rs622342 của gen mã hóa OCT1, có mức độ giảm glucose máu sau dùng metformin tốt hơn những người mang kiểu gen bình thường. Một nghiên cứu khác phát hiện sự tương tác giữa hai biến thể của gen MATE1 và MATE2 làm tăng đáng kể bài xuất metformin qua thận. Như vậy, tùy từng loại alen biến thể và tương tác giữa các biến thể của các gen khác nhau mà sự ảnh hưởng đến đáp ứng điều trị bởi metformin rất khác biệt và phức tạp.
Trong khi đã có những bằng chứng về sự liên quan giữa kiểu gen của các gen tham gia vào quá trình dược động học với đáp ứng điều trị của metformin thì với các gen tham gia vào quá trình được lực học, các kết quả còn gây nhiều tranh cãi. Cho đến nay, gen duy nhất được chứng minh trong một số nghiên cứu là có ảnh hưởng đến dược lực học của metformin là gen ATM (ataxia telangiectasia mutated). Sự thay đổi hoạt tính ATM làm thay đổi hoạt tính AMPK - đích phân tử của metformin. Ngoài ra, các nghiên cứu trên chuột chuyển gen còn cho thấy vai trò của ATM đối với quá trình truyền tín hiệu của insulin và chức năng sản xuất insulin của tế bào beta. Một nghiên cứu trên 1.024 bệnh nhân ĐTĐ typ 2 cho thấy có liên quan giữa alen biến thể rs11212617 của gen ATM với đáp ứng điều trị bởi metformin. Kết quả này được tái khẳng định với hai nghiên cứu cohort của Scotland (trên 1.783 người) và Anh (trên 1.113 người).
|
Bảng 11.1. Tổng hợp các biến thể gen có ảnh hưởng đến đáp ứng điều trị bởi metformin |
||||
| Gen | Loại đa hình | Quy mô nghiên cúru | Sự thay đổi trong đáp ứng lâm sàng | Tác giả |
| OCT1/SLC22A1 | R61C (rs12208357) | 1531 bệnh nhân dùng metformin (GO-DARTS quả điều trị cohort) | Không ảnh hưởng tới kết quả điều trị | Zhou |
| 420del (rs72552763) | 159 bệnh nhân điều trị metformin trong 9 tháng | Giảm nồng độ thuốc trong huyết tương | Christensen | |
| G401S (rs3413095) | Giảm HbA1c |
Christensen |
||
| Rs461473 | ||||
| OCT2/SLC22A2 | c.808G>T (rs316019) | 400 bệnh nhân Trung Quốc dùng metformin | Nồng độ Acid Lactic huyết tương tăng | Li |
| A270S | Người khỏe mạnh dùng liều đơn | Tăng thanh thải qua thận | Christensen | |
| T201M (rs145450955) | 40 bệnh nhân điều trị bằng metformin | Tăng glucose máu, HbA1c, tăng kháng insulin | Kashi | |
| MATE1/SCL47A1 | Rs2289669 G>A | 116 bệnh nhân dùng metformin | Tăng hiệu quả giảm HbA1c | Becker |
| 220 người da trắng điều trị bằng metformin trong 12 tháng |
Tăng hiệu quả giảm HbA1c Tăng nồng độ thuốc trong huyết tương Giảm thanh thải qua thận |
He | ||
| 103 người da trắng khỏe mạnh dùng liều đơn | Không khác biệt về độ thanh thải qua thận | Tzvetkov | ||
| 159 bệnh nhân dùng metformin trong 9 tháng | Không khác biệt về nồng độ thuốc trong huyết tương và nồng độ HbA1c | Christensen | ||
| Rs8065082G>A | 900 người tiền đái tháo đường dùng metformin | Giảm hiệu quả giảm glucose máu và dung nạp glucose | Jablonski | |
| 148 bệnh nhân điều trị bằng metformin trong 6 tháng | Tăng hiệu quả giảm HbA1c | Tkas | ||
| g.66T>C | 249 bệnh nhân da trắng và da đen dùng metformin | Tăng hiệu quả giảm HbA1c | Stocker | |
| 57 người khỏe mạnh dùng 2 liều metformin | Tăng hiệu quả tăng dung nạp glucose | Stocker | ||
| MATE1/SCL47A1 | g.130G>A | 57 người khỏe mạnh dùng 2 liều metformin |
Tăng thanh thải qua thận Giảm hiệu quả về dung nạp glucose |
Stocker |
| 253 bệnh nhân da trắng và da đen dùng metformin | Giảm hiệu quả về HbA1c | Choi | ||
| ATM | Rs11212617 | 3920 bệnh nhân dùng metformin | Tăng đáp ứng với metformin | Zhou |
| 929+182+254 bệnh nhân dùng metformin | Tăng đáp ứng với metformin | Van Leeuwen | ||
2 Sulfonylurea
Sự dao động về đáp ứng với các sulfonylurea cũng đã được ghi nhận từ lâu, với khoảng 10 - 20% bệnh nhân không đạt hiệu quả giảm glucose máu tối thiểu 20 mg/dL. Bên cạnh ảnh hưởng của các yếu tố lâm sàng như mức glucose máu trước khi điều trị, thời gian mắc bệnh, chức năng tế bào beta, mức độ kháng insulin của bệnh nhân, sự khác biệt về gen di truyền cũng là một yếu tố ảnh hưởng đáng kể tới cả dược động học và dược lực học của thuốc.
Các sulfonylurea được chuyển hóa chủ yếu ở gan bởi CYP2C9, do đó, kiểu gen CYP2C9 của bệnh nhân có ảnh hưởng đáng kể tới nồng độ thuốc trong máu. Một nghiên cứu trên người tình nguyện khỏe mạnh mang kiểu gen đồng hợp tử CYP2C9*3/*3 hoặc CYP2C9*2/*2 làm giảm độ thanh thải glyburid lần lượt là 50% và 10%, đi kèm với tăng rõ rệt AUC và T1/2. Một nghiên cứu với tolbutamid cũng cho kết quả tương tự. Đối với sulfonylurea thế hệ 2, những bệnh nhân mang kiểu gen CYP2C9 *3/*3 hoặc *3/*1 có AUC glimepirid tăng lần lượt 40% và 30% so với kiểu gen *1/*1. Những ảnh hưởng trên chuyển hóa và thải trừ của sulfonylurea thông qua biến thể gen CYP2C9 đã dẫn đến những thay đổi về đáp ứng thuốc trên lâm sàng. Một nghiên cứu quy mô lớn trên 1073 bệnh nhân dùng sulfonylurea cho thấy những người mang kiểu gen chứa alen CYP2C9*2 hoặc CYP2C9*3 dễ đạt được mục tiêu điều trị hơn gấp 3 - 4 lần, HbA1c giảm nhiều hơn 0,5% so với người mang kiểu gen bình thường. Một nghiên cứu khác với 172 bệnh nhân dùng tolbutamid đã chỉ ra những người mang alen CYP2C9*3 trong kiểu gen cần liều tolbutamid thấp hơn để đạt được cùng một mức độ kiểm soát glucose máu. Một báo cáo tương tự thu được từ nghiên cứu trên người Nhật Bản dùng glimepirid. Những kết quả này có thể giúp CYP2C9 trở thành một marker giúp lựa chọn thuốc phù hợp cho bệnh nhân ĐTĐ typ 2.
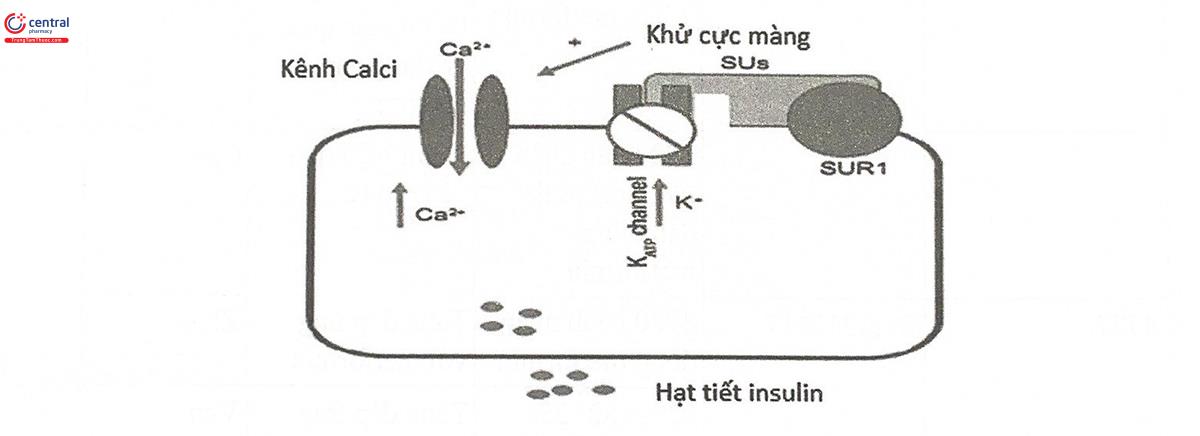
Bên cạnh các yếu tố dược động học, ảnh hưởng của các gen và protein liên quan đến dược lực học của sulfonylurea đối với đáp ứng điều trị cũng được quan tâm nghiên cứu. Sulfonylurea làm tăng giải phóng insulin phụ thuộc glucose bằng cách gắn vào kênh Kali nhạy cảm với ATP (kênh KATP) (Hình 11.2). Kênh này gồm 4 tiểu đơn vị SUR1 (sulfonylurea receptor) và 4 tiểu đơn vị Kir 6.2 (Potassium inward rectifier channel). Để phát huy tác dụng, thuốc gắn vào cả hai loại protein đích này, ức chế kênh kali, gây khử cực màng dẫn đến mở kênh Ca phụ thuộc điện thế. Dòng Ca++ đi vào tế bào làm tăng nồng độ Ca++ nội bào, đây là tín hiệu kích thích giải phóng insulin dự trữ trong các hạt tiết của tế bào beta.
Sau khi phát hiện vai trò quan trọng của SUR1 và Kir6.2 trong cơ chế hoạt động của sulfonylurea, người ta tiếp tục tìm hiểu vai trò của các gen mã hóa hai protein này đối với đáp ứng điều trị. Một nghiên cứu trên 115 người Trung Quốc dùng gliclazid trong 8 tuần cho thấy kiểu gen mang SNP rs757110 (A1369S) của gen ABCC8 (mã hóa SUR1) đạt hiệu quả giảm HbA1c tốt hơn so với kiểu gen bình thường. Một nghiên cứu khác cũng cho kết quả tương tự khi đánh giá hiệu quả điều trị với gliclazid bằng mức glucose máu lúc đói và test dung nạp glucose đường uống. Một biến thể thường gặp của gen KCNJ11 (mã hóa Kir6.2) là rs5219 (E23K) cũng được chứng minh là có ảnh hưởng đến đáp ứng của sulfonylurea. Một nghiên cứu trên 101 bệnh nhân ĐTĐ typ 2 da trắng dùng sulfonylurea sau khi dùng metformin cho thấy sau 6 tháng điều trị, người mang gen gồm cả 2 alen biến thể (KK) có mức giảm HbA1c tốt hơn người mang kiểu gen bình thường (EE). Một nghiên cứu trên 108 bệnh nhân ĐTĐ typ 2 Trung Quốc cũng cho kết quả tương tự với gliclazid MR sau 16 tuần điều trị.
| Bảng 11.2. Tổng hợp các biến thể gen có ảnh hưởng đến đáp ứng điều trị bởi sulfonylurea | ||||
| Gen | Loại đa hình | Quy mô nghiên cứu | Sự thay đổi trong đáp ứng lâm sàng | Tác giả |
| KCNJ11 | E23K |
101 bệnh nhân điều trị bằng metformin+ sulfonylurea trong 6 tháng |
Tăng hiệu quả về HbA1c | Javorsky |
| 525 bệnh nhân dùng glibenclamid hoặc glibenclamid +metformin | Giảm hiệu quả điều trị | Sesti | ||
| 278 bệnh nhân không béo phì dùng metformin + sulfonylurea | Giảm hiệu quả điều trị | Shimajiri | ||
| ABCC8 | S1369A | 1268 bệnh nhân dùng gliclazid trong 8 tuần | Tăng hiệu quả về HbA1c, glucose máu và dung nạp glucose | Feng |
| 115 bệnh nhân dùng gliclazid trong 8 tuần | Tăng hiệu quả về HbA1c | Zhang | ||
| TCF7L2 | Rs12255372 | 901 bệnh nhân dùng sulfonylurea | Giảm hiệu quả điều trị ở nhóm đồng hợp tử TT | Pearson |
| Rs7903146 | 189 bệnh nhân dùng sulfonylurea | Giảm hiệu quả điều trị ở nhóm đồng hợp tử TT | Holstein | |
| CYP2C19 | Rs16889462 (*2) | 1.073 bệnh nhân dùng sulfonylurea, chủ yếu là gliclazid | Tăng hiệu quả điều trị ở nhóm mang kiểu gen biến thể | Zhou |
| Rs1057910 (*3) | 475 bệnh nhân dùng sulfonylurea | Tăng hiệu quả điều trị ở nhóm mang kiểu gen biến thể | Becker | |
3 Thiazolidindion
Đây là nhóm thuốc điều trị ĐTĐ typ 2 tác động theo cơ chế tăng cường nhạy cảm với insulin của 3 mô đích chính là gan, cơ và mỡ. Các thiazolidindion (TZD) được chuyển hóa ở gan chủ yếu bởi CYP2C8. Do đó, enzym này và gen mã hóa nó có ảnh hưởng tới nồng độ thuốc trong huyết tương. Một nghiên cứu trên người tình nguyện khỏe mạnh cho thấy người mang kiểu gen đồng hợp tử chứa 2 alen biến thể CYP2C8*3 có nồng độ Rosiglitazon huyết tương thấp hơn 36%. Hai nghiên cứu khác với pioglitazon cũng cho kết quả tương tự.
Đích phân tử của TZD là receptor PPAR-γ, bằng cách gắn và hoạt hóa receptor này, TZD điều hòa phiên mã các gen tham gia chuyển hóa glucid và lipid. Do vậy, gen PPARG (gen mã hóa PPAR-γ) cũng là một gen được quan tâm trong các nghiên cứu gen dược liên quan đến TZD (Hình 11.13). Biến thể thường gặp nhất của gen này là SNP rs1801282 (P12A), dẫn đến thay thế Pro bằng Ala ở vị trí 12 trong chuỗi peptid của receptor, làm thay đổi cấu trúc và chức năng của PPAR. Biến thể này đã được ghi nhận mối liên quan với đáp ứng điều trị của 250 bệnh nhân dùng pioglitazon trong vòng 24 tuần. Những người mang alen P12A có đáp ứng tốt hơn trong mục tiêu giảm HbA1c và glucose máu lúc đói gấp hơn 2 lần so với người mang kiểu gen thông thường. Một nghiên cứu khác trên 67 bệnh nhân dùng pioglitazon và 198 bệnh nhân dùng rosiglitazon cũng cho thấy mối liên quan theo cùng xu hướng.
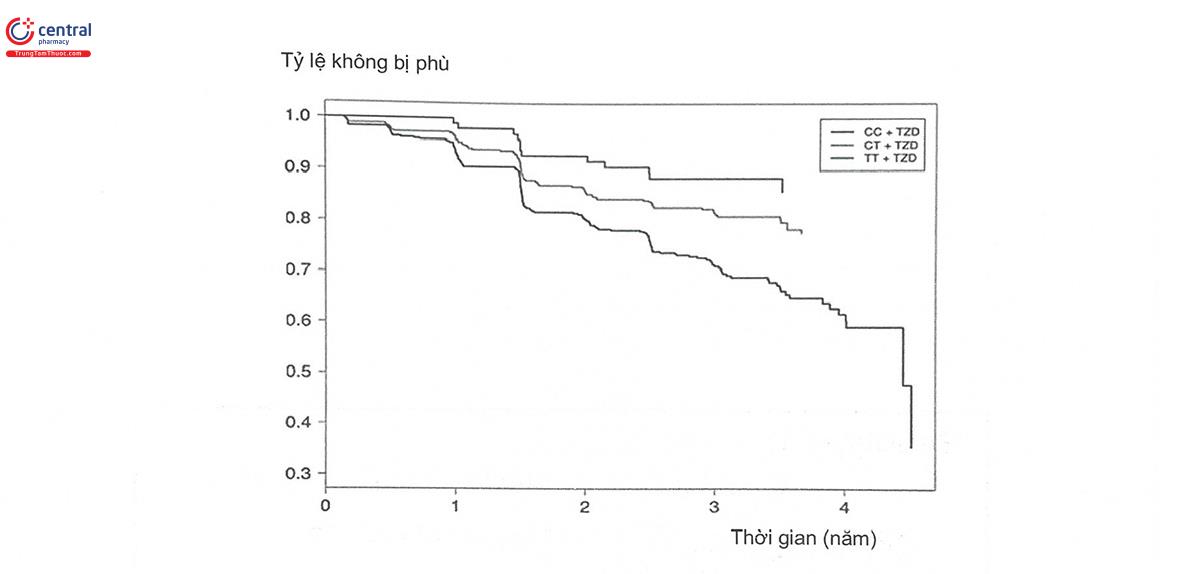
Một trong những vấn đề đáng chú ý khi dùng TZD là tác dụng không mong muốn đáng kể. Năm 2000, troglitazon bị rút khỏi thị trường toàn thế giới do độc tính trên gan, rosiglitazon cũng đã bị rút khỏi châu Âu và giám sát chặt chẽ ở Mỹ do liên quan đến nguy cơ tim mạch. Thậm chí, Pháp và Đức cũng đang nghi ngờ pioglitazon có liên quan đến tăng nguy cơ ung thư bàng quang. Vì vậy, đã có nhiều nghiên cứu về ảnh hưởng của kiểu gen khác nhau đến nguy cơ tác dụng không mong muốn khi dùng TZD. Một nghiên cứu sàng lọc 68 SNP của 51 gen nghi ngờ liên quan đến TDKMM trên 110 bệnh nhân Nhật Bản cho thấy kiểu gen mang cả hai alen giảm chức năng của hai gen glutathion-S- transferase theta-1 và glutathion-S-transferase mu-1 có liên quan đến độc tính trên gan do troglitazon. Đây là hai gen mã hóa cho các enzym tham gia vào quá trình giải độc ở gan. Một nghiên cứu khác của Nhật đã ghi nhận sự liên quan của biến thể gen CYP2C19 với nguy cơ tổn thương gan do troglitazon. Năm 2010, một nghiên cứu của Canada trên 4197 bệnh nhân dùng rosiglitazon, sau khi sàng lọc 32088 SNP đã phát hiện SNP rs6123045 của gen NFATC2 có liên quan đến nguy cơ phù ngoại vi do rosiglitazon. NFATC2 (Nuclear Factor of Activated T-cells, Cytoplasmic, Calcineurin-Dependent 2) là một gen liên quan đến hoạt động của hệ miễn dịch. Kiểu gen mang ít nhất một alen biến thể của NFATC2 (CC hoặc TT) có nguy cơ phù cao hơn kiểu gen wildtype (TT) (Hình 11.4)
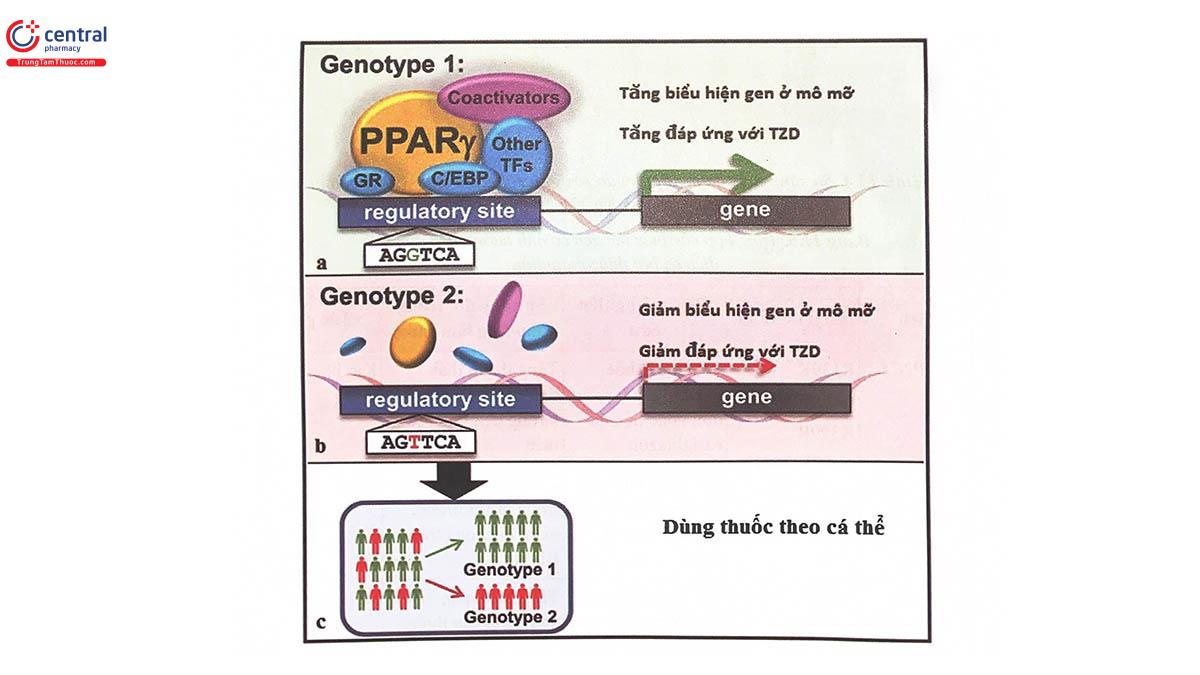
a) Kiểu gen bình thường: Thuốc gắn được vào receptor PPARγ dẫn đến điều hòa biểu hiện gen ở mô mỡ theo hướng làm giảm kháng insulin; b) Kiểu gen mang SNP: Thuốc không gắn được vào receptor PPARγ, giảm đáp ứng điều trị; c) Sàng lọc kiểu gen PPARG có thể lựa chọn được những người đáp ứng tốt với TZD
| Bảng 11.3. Tổng hợp các biến thể gen có ảnh hưởng đến đáp ứng điều trị bởi thiazolidindion | ||||
| Gen | Loại đa hình | Quy mô nghiên cứu |
Sự thay đổi trong đáp ứng lâm sàng |
Tác giả |
| CYP2C8 |
R139K (rs11572080) K399R (rs10509681) |
31 người khỏe mạnh dùng liều đơn hoặc liều đa rosiglitazon | Tăng thanh thải thuốc, không ảnh hưởng đến glucose máu | Kirchheiner |
| 187 bệnh nhân dùng rosiglitazon + insulin trong 24 tháng | Giảm nồng độ thuốc trong huyết tương, giảm hiệu quả trên HbA1c | Stage | ||
| UGT2B15 | D85Y |
644 bệnh nhân dùng sipoglitazar hoặc rosiglitazon trong 3 tháng |
Tăng hiệu quả, giảm liều dùng cần thiết | Stringer |
| PPARY | P12A (rs1801282) | 189 bệnh nhân dùng rosiglitazon trong 12 tháng | Tăng hiệu quả điều trị về HbA1c và glucose máu | Kang |
| 250 bệnh nhân Trung Quốc dùng pioglitazon trong 24 tháng | Tăng hiệu quả điều trị về glucose máu | Hsieh | ||
| 101 bệnh nhân Iran dùng | Tăng hiệu quả điều trị | Namvaran | ||
| ACDC | 45T>G (rs2241766) | Trung Quốc dùng pioglitazon trong 12 tuần | Giảm hiệu quả điều trị về HbA1c và glucose máu (chủ yếu ở người đồng hợp tử) | Yang |
| 101 bệnh nhân Iran dùng pioglitazon trong 12 tuần | Không thay đổi đáp ứng điều trị | Namvaran | ||
| 276G>T | 166 bệnh nhân dùng pioglitazon trong 12 tuần | Giảm hiệu quả về HbA1c và glucose máu | Kang | |
| PGC-1α | G4825S (rs8192678) | 41 bệnh nhân dùng rosiglitazon trong 12 tuần | Giảm hiệu quả về HbA1c và tăng kháng insulin | Zhang |
| UCP2 | 866G>A | 199 bệnh nhân Trung Quốc dùng rosiglitazon trong 12 tuần | Tăng hiệu quả về HbA1c | Yang |
4 Các thuốc hạ Glucose máu đường uống khác
Bên cạnh các nhóm thuốc kể trên, hiện nay đã có một số nhóm thuốc hạ glucose máu đường uống mới. Mặc dù thời gian sử dụng trên lâm sàng chưa nhiều nhưng đã có những nghiên cứu bước đầu về ảnh hưởng của gen di truyền đến đáp ứng với các nhóm thuốc mới này.
Một trong những hướng điều trị ĐTĐ theo cơ chế tăng insulin nội sinh là thông qua hiệu ứng incretin. Các chất đồng vận trên thụ thể Glucagon-like peptide-1 (GLP-1) có tác dụng tương tự GLP-1 nội sinh, làm tăng tiết insulin phụ thuộc nồng độ glucose từ tuyến tụy. Một nghiên cứu trên người tình nguyện châu u cho thấy có sự khác biệt đáng kể trong đáp ứng tiết insulin với các chất chủ vận GLP-1 ngoại sinh giữa những người mang 2 alen biến thể của gen GLP-1R (mã hóa receptor của GLP-1). Cụ thể là với SNP rs6923761 G>A (được tìm thấy ở 29% người da trắng châu u), những người mang kiểu gen đồng hợp tử wildtype có lượng insulin sản xuất từ tế bào beta tăng 15% so với kiểu gen mang ít nhất 1 alen rs6923761 G>A. Ngược lại, với SNP rs3765467C>T, kiểu gen đồng hợp tử hoặc dị hợp tử mang alen biến thể này có lượng insulin nội sinh tăng 100% so với kiểu gen bình thường. Không chỉ ảnh hưởng đến đáp ứng điều trị của các chất chủ vận receptor GLP-1, SNP rs6923761 G>A còn làm thay đổi hiệu quả điều trị với một nhóm thuốc có liên quan đến hiệu ứng incretin là các chất ức chế DPP4. Trong một nghiên cứu trên 246 bệnh nhân ĐTĐ typ 2 tại Hàn Quốc điều trị trong vòng 24 tuần, những người có kiểu gen mang ít nhất 1 alen biến thể rs6923761 G>A có HbA1c cao hơn hẳn những người mang kiểu gen widltype (GG).
5 Kết luận
Việc ứng dụng gen dược trong cá thể hóa điều trị bệnh đái tháo đường còn rất hạn chế, chủ yếu mới dừng ở giai đoạn nghiên cứu. Các kết quả nghiên cứu cho thấy chưa có một cặp gen - thuốc nào thực sự có liên quan đáng kể. Rất có thể đáp ứng điều trị của các thuốc đái tháo đường không phụ thuộc vào một gen mà vào nhiều gen khác nhau cũng như phụ thuộc vào nhiều yếu tố lâm sàng khác.
6 Tài liệu tham khảo
1. Mannino GC, Andreozzi F, Sesti G (2019), Pharmacogenetics of type 2 diabetes mellitus, the route toward tailored medicine, Diabetes Metab Res Rev. 2019 Mar;35(3).
2. Nisa M. Maruthur, The Pharmacogenetics of Type 2 Diabetes: A Systematic Review, Diabetes Care 2014 Mar; 37(3): 876-886.
3. Lam F. (2019), Chapter 9 The Role of Pharmacogenomics in Diabetes, Pharmacogenomics (Second Edition) Chalenges and Opportunities in Therapeutic Implementation 2019, Pages 247-269.

