Kyongbo Pharmaceutical
9 sản phẩm
 Dược sĩ Thu Hà
Dược sĩ lâm sàng
Dược sĩ Thu Hà
Dược sĩ lâm sàng
Ước tính: 5 phút đọc,
Ngày đăng:
Cập nhật:
Nếu phát hiện nội dung không chính xác, vui lòng phản hồi thông tin cho chúng tôi tại đây

KyongBo Pharmaceuticals được thành lập năm 1987 tại Hàn Quốc, là công ty sản xuất và phát triển dược phẩm hàng đầu thế giới chịu trách nhiệm về sức khỏe con người. Trong bài viết này, Trung Tâm Thuốc Central Pharmacy sẽ cung cấp cho bạn đọc những thông tin về thương hiệu KyongBo Pharmaceuticals.
1 Tổng quan
1.1 Thông tin chung
Tên công ty: Kyongbo Pharmaceutical LTD.
Thành lập: Ngày 31 tháng 3 năm 1987
Ngày niêm yết: Ngày 29 tháng 6 năm 2015
Ngành nghề kinh doanh: Sản xuất/Bán thành phần dược phẩm hoạt động, Sản xuất/Bán thuốc thành phẩm
Trụ sở chính: 174, Sirok-ro, Asan-si, Chungcheongnam-do, Hàn Quốc
Kyongbo Pharmaceutical được thành lập vào năm 1987 với Cam kết phát triển các hoạt chất có chất lượng cao nhất thông qua những đổi mới trong công nghệ sản xuất.
Là công ty đầu tiên ở Hàn Quốc phát triển kháng sinh Cefaclor.
Nỗ lực liên tục của KyongBo nhằm nâng cao các tiêu chuẩn sản xuất và quản lý chất lượng của riêng mình.
Nhờ các khoản đầu tư liên tục vào các cơ sở và R&D, công ty đang xuất khẩu các sản phẩm trị giá 85.000.000 đô la như kháng sinh cephalosporin, thuốc chống tăng lipid máu và thuốc chống ung thư đến hơn ba mươi quốc gia trên thế giới và nhanh chóng trở thành một tập đoàn toàn cầu thực sự.
Từ năm 2001, Kyongbo Pharmaceutical đã sản xuất nhiều thành phẩm khác nhau bao gồm thuốc gây mê, tim mạch, tiêu hóa và kháng sinh. Kyongbo Pharmaceutical cam kết phát triển thành một tập đoàn nhân đạo cung cấp dược phẩm chất lượng cao giúp cải thiện sức khỏe và cuộc sống của nhân loại.

2 Lịch sử hình thành và phát triển
| Mốc thời gian | Sự kiện |
|---|---|
| 1987 |
Giấy phép xuất khẩu dược phẩm được mua từ Bộ Y tế và Phúc lợi Hoạt động nhà máy đầu tiên (Nhà máy 1) Đăng ký là một nhà xuất khẩu Công ty TNHH Dược phẩm Kyongbo được thành lập với vốn thanh toán 100 triệu ₩ |
| 1988 |
Vốn thanh toán tăng lên ₩500 triệu Tháp xuất khẩu 1 triệu đô la đã nhận được Hoàn thành xây dựng phòng sạch Trung tâm nghiên cứu trung tâm đã được mở Khu vực nhà máy được mở rộng đến 7,253 m2 |
| 1989 | Được chọn là một công ty vừa và nhỏ đầy hứa hẹn |
| 1990 |
Vốn trả góp tăng lên ₩1.4 tỷ Nhận được tấm bảng Sản xuất Hứa hẹn từ Ngân hàng Công nghiệp Hàn Quốc Vốn thanh toán tăng lên ₩1.2B |
| 1993 |
Vốn thanh toán tăng lên ₩2.4B Sản xuất Cephalosporin (exc. Cefaclor) đã bắt đầu Việc xây dựng nhà máy thứ hai đã hoàn thành (Nhà máy 2) |
| 1994 | Tháng Hai. Khai mạc xuất khẩu Cefaclor sang Nhật Bản (lần đầu tiên ở Hàn Quốc) |
| 1995 |
Tháp xuất khẩu 10 triệu đô la đã nhận được Giấy phép KGMP được mua lại |
| 1996 |
Đã hoàn thành bảo trì, sửa chữa và mở rộng nhà máy 1, nhà máy 2 và phòng sạch Khu vực nhà máy được mở rộng lên 8.875m2 Được thêm vào như một thành viên của công ty gia đình Chong Kun Dang |
| 1997 |
Đạt được chứng nhận ISO 9001 (Đăng ký Hiệp hội Quản lý Hàn Quốc) Địa điểm nhà máy được mở rộng lên 22,478m2 |
| 1998 |
Đạt được chứng nhận ISO 14001 (Đăng ký Hiệp hội Quản lý Hàn Quốc) Vốn trả góp tăng lên ₩7.4B |
| 1999 |
Jeong-woo, Kim được bổ nhiệm làm Giám đốc điều hành Chứng nhận BGMP được mua lại (Bộ An toàn Thực phẩm và Dược phẩm) Khen thưởng về Bằng khen Xuất khẩu đã nhận được (Bộ trưởng Bộ Y tế và Phúc lợi |
| 2001 |
Đã đăng ký là một công ty liên doanh (Quản trị doanh nghiệp vừa và nhỏ) Vốn thanh toán giảm xuống còn ₩4.4B Lực lượng đặc nhiệm đăng ký DMF được khánh thành |
| 2002 |
Bắt đầu xây dựng nhà máy sản xuất thuốc thành phẩm được chứng nhận KGMP Tên thương mại được đổi thành Công ty TNHH Dược phẩm Kyongbo. Giấy phép bán buôn dược phẩm tổng hợp có được |
| 2003 |
Nhận được khen ngợi của Bộ trưởng Bộ Thương mại, Công nghiệp và Năng lượng (Phát triển công nghệ sản xuất Cefixime) Phê duyệt cho Bacampicillin Hcl bởi COS của Châu u Giấy phép KGMP được mua lại Vốn thanh toán tăng lên ₩17.2B Yeong-eun, Kim được bổ nhiệm làm Giám đốc điều hành Giấy phép sản xuất dược phẩm có được Chứng nhận kiểm toán cho axit Cefuroxime bởi FDA Hoa Kỳ |
|
2004 |
Chứng nhận hệ thống quản lý môi trường (ISO 14001) được mua lại Vốn trả góp tăng lên ₩27.2B Phê duyệt cho Ceftizoxime natri bởi IDL của Trung Quốc |
| 2005 | Vốn đã trả tăng lên ₩28.6B |
| 2006 |
Vốn thanh toán giảm xuống còn ₩7.4B Chứng nhận nhà sản xuất nước ngoài được mua lại từ Bộ Y tế, Lao động và Phúc lợi Nhật Bản (Nhà máy tiêm 2) |
| 2007 |
Bắt đầu xây dựng cánh mới của trung tâm nghiên cứu trung tâm Tháp xuất khẩu 30 triệu đô la đã nhận được Tên thương mại được đổi thành Công ty TNHH Dược phẩm Kyongbo |
| 2008 |
Vốn trả góp tăng lên ₩10.7B QC tách Cephalosporin và các API chung khác Việc xây dựng cánh mới của trung tâm nghiên cứu trung tâm đã hoàn thành Được chọn là Tập đoàn Tự kiểm tra Tuyệt vời năm 2007 (Văn phòng Daejeon của Cục Quản lý Thực phẩm & Dược phẩm Hàn Quốc) Chứng nhận GMP được mua từ EDQM của Châu u |
|
2009 |
Chứng nhận Hệ thống Quản lý An toàn và Sức khỏe đã đạt được (KOSHA 18001) Chứng nhận KGMP được mua cho thuốc tiêm Phê duyệt cho Cefaclor bởi EDQM của Châu u Kiểm tra PMDA (Ceftriaxone, Cefmetazole) Hoàn thành việc xây dựng dây chuyền chiết rót tiêm Cephalosporin |
| 2010 |
Được chọn là nhà tuyển dụng vừa và nhỏ được tìm kiếm Chứng nhận Người tạo Việc làm Xuất sắc đã đạt được Giải thưởng lớn tại Hội nghị Công nghiệp Chungcheongnamdo lần thứ 17 ₩Giải thưởng Công ty Liên doanh 100B từ Hiệp hội Doanh nghiệp Liên doanh Hàn Quốc và Quản trị Doanh nghiệp vừa và |
| 2011 |
Giải thưởng Tháp Xuất khẩu trị giá 50 triệu đô la đã nhận được Giải thưởng Bộ trưởng Kinh tế Tri thức nhận được tại Giải thưởng Công nghệ Công nghiệp Hàn Quốc GMP và sự chấp thuận cơ sở của FDA Hoa Kỳ Phê duyệt kiểm tra theo lịch trình của Cephalosporin bởi EDQUM của Châu u Sự chấp thuận của Atorvastatin Ca bởi PMDA của Nhật Bản |
| 2012 |
Sự chấp thuận cho Meropenem và Mosapride bởi PMDA của Nhật Bản Tae Won, Kang được bổ nhiệm làm Giám đốc điều hành |
| 2013 |
Phê duyệt cho Ceftazidime pentahydrate vô trùng bởi EDQM của Châu u Giải thưởng Tháp Xuất khẩu trị giá 70 triệu đô la đã nhận được |
| 2014 |
Cơ sở sản xuất thuốc chống ung thư gây độc tế bào đã được phê duyệt (Cơ quan Quản lý Thực phẩm & Dược phẩm Hàn Quốc) Hoàn thành xây dựng nhà máy High-Potency 1 (thuốc chống ung thư) |
| 2015 |
Hoàn thành xây dựng nhà máy General APIs 3 Được liệt kê trên KOSPI |
| 2016 |
Được công nhận là Tập đoàn Văn hóa Quản lý Lao động xuất sắc năm 2016 Cơ sở sản xuất GMP vô trùng được FDA Hoa Kỳ phê duyệt Hoàn thành xây dựng nhà máy High-Potency Plant 2 Phê duyệt Ceftriaxone Sodium bởi EDQM của Châu u |
| 2017 |
Được trao tặng bởi Bộ trưởng Bộ Việc làm và Lao động Điều tra GMP kiểm tra PMDA Nhật Bản (Olmesartan Medoxomil) Đạt được sự phù hợp với các tiêu chuẩn sản xuất dược phẩm và kiểm soát chất lượng |
| 2018 |
Chứng nhận GMP của FDA Hoa Kỳ (Ceftriaxone Sodium Sterile) Chứng nhận ANSM GMP của Pháp (Ceftriaxone Sodium, Cefotaxime Sodium |
| 2019 |
Mục đích được thêm vào của các điều khoản thành lập (Bán thiết bị y tế, Bán thực phẩm chức năng sức khỏe) Thành lập Trung tâm Nghiên cứu Thuốc Mới ở Yongin TechnoValley |
3 Tầm nhìn sứ mệnh và giá trị cốt lõi
3.1 Tầm nhìn sứ mệnh
Sứ mệnh: cải thiện sức khỏe và cuộc sống của nhân loại.
Kyongbo Pharmaceutical cam kết phát triển vượt ra ngoài việc trở thành người vĩ đại nhất và công ty API lớn nhất ở Hàn Quốc để trở thành một nhà lãnh đạo toàn cầu trong ngành công nghiệp hóa học dựa trên dược phẩm
3.2 Giá trị cốt lõi
Quyền tự trị
Sự tôn trọng
Giao tiếp
Luyện tập
4 Tiêu chuẩn và chứng nhận chất lượng
Dược phẩm KyongBo đã nhận được chứng nhận cGMP từ nhiều cơ quan chức năng khác nhau như FDA ở Hoa Kỳ, EDQM ở Châu u, PMDA ở Nhật Bản và CFDA ở Trung Quốc; Tiêu chuẩn ISO14001 Mã số KOSHA1800
Được cấp giấy phép sản xuất hoạt chất. nguyên liệu cho thuốc tiêm vô trùng và thuốc generic đầu tiên .
5 Các chi nhánh và công ty con
5.1 Lĩnh vực y tế
Dược phẩm CKD: công ty dược phẩm đầu tiên ở Hàn Quốc nhận được sự chấp thuận từ FDA Hoa Kỳ, đánh dấu sự khởi đầu xuất khẩu dược phẩm của Hàn Quốc.
CKD bio: kinh doanh nguyên liệu sinh học dựa trên công nghệ lên men cấp quốc tế

Dược phẩm KB: công ty chuyên sản xuất nguyên liệu dược phẩm thô và hóa chất tinh khiết
CKDHC: Chong Kun Dang Health là công ty thực phẩm sức khỏe, sản xuất và bán nhiều loại thực phẩm tốt cho sức khỏe và đồ uống chức năng. đáp ứng nhanh chóng nhu cầu sức khỏe của người tiêu dùng.
5.2 Các lĩnh vực khác
CKD holding: tập trung năng lực vào phát triển kinh doanh mới và đầu tư mới để tối đa hóa giá trị doanh nghiệp của Chong Kun Dang và các công ty kinh doanh khác
CKD Industries: công ty quản lý tài sản được thành lập năm 1979 với mục đích tham gia vào lĩnh vực cho thuê bất động sản và các hoạt động kinh doanh phụ trợ có liên quan
Bell E&C: sản xuất và lắp đặt cơ sở sản xuất và thiết bị sản xuất cần thiết cho từng ngành, bao gồm thiết bị công nghiệp, máy móc công nghiệp, nhà máy hóa chất và lĩnh vực môi trường
Bell SM: quản lý tòa nhà toàn diện, gia công phần mềm (an ninh an ninh, vệ sinh môi trường, điều động công nhân, v.v.), hậu cần và kinh doanh vận tải
Bell Communications: Belcom là một 'công ty giải pháp kỹ thuật số' dựa trên dữ liệu; hoạt động truyền thông quảng cáo, từ việc thiết lập chiến lược tiếp thị của công ty đến sản xuất quảng cáo
Bell I&S: một công ty chuyên về CNTT hoạt động trong lĩnh vực tư vấn, xây dựng và bảo trì hệ thống CNTT của doanh nghiệp
6 Vật chất trang thiết bị tại Kyungbo Pharmaceutical
6.1 Cơ sở sản xuất
KB Pharmaceutical vận hành các cơ sở sản xuất có khả năng sản xuất nhiều loại dược phẩm từ hoạt chất dược phẩm đến thành phẩm và đã tạo dựng được danh tiếng trên thế giới về chất lượng và chuyên môn
Nhà máy API chung 1 và 3: Hoạt chất dược phẩm tổng hợp
Nhà máy API chung 2: Hoạt chất dược phẩm của thuốc cephalosporin/thuốc tiêm trung gian
Nhà máy sản xuất thuốc uống dạng rắn: Thuốc dạng rắn uống thành phẩm
Nhà máy tổng hợp API 4, 5: API tổng hợp Nhà máy 4, 5
Nhà máy API vô trùng 1 và 2: API chống ung thư, hiệu lực cao
Nhà máy lọ y tế vô trùng: Thuốc tiêm cephalosporin thành phẩm

6.2 Đảm bảo chất lượng QA/QC
6.2.1 Chính sách chất lượng
Kyongbo Pharmaceutical là nhà sản xuất dược phẩm hàng đầu thế giới chịu trách nhiệm về sức khỏe của nhân loại, cam kết thực thi chính sách chất lượng của mình trong toàn bộ tổ chức.
- Tuân thủ luật pháp và quy định trong và ngoài nước cũng như tuân thủ các tiêu chuẩn cGMP quốc tế với tư cách là đơn vị chủ động tham gia sản xuất và phân phối các sản phẩm dược phẩm chất lượng cao.
- Tuân theo các biện pháp đảm bảo chất lượng nghiêm ngặt từ nguyên liệu thô và nguyên liệu đóng gói đến khi xuất xưởng thành phẩm như một phần của chính sách quản lý chất lượng có trách nhiệm
- Với khẩu hiệu “Cuộc sống tốt đẹp hơn thông qua y học tốt hơn”, KB Pharmaceutical cung cấp API và thành phẩm có chất lượng cao nhất để mang lại sự hài lòng cho khách hàng và cam kết thực hiện mọi trách nhiệm xã hội của mình với tư cách là một tập đoàn ưu tú sản xuất các sản phẩm dược phẩm chất lượng cao giúp cải thiện sức khỏe và cuộc sống của loài người.
6.3 Đơn vị chất lượng
| Đội QA 1 |
Quản lý GMP cho API MF cho API Phát hành sản phẩm & Khiếu nại của khách hàng |
| Đội QA 2 |
Quản lý GMP cho thuốc thành phẩm MF cho thành phẩm Xác nhận & Chứng nhận |
| Đội QA 3 |
Đăng ký sản phẩm Kiểm soát thay đổi và sai lệch Đào tạo SOP & GMP |
| Đội QC 1 |
Phân tích sản phẩm chung Phân tích API hiệu lực cao Xác thực phương pháp phân tích |
|
Đội QC 2 |
Phân tích sản phẩm Cephalosporin Kiểm tra vi sinh vật & vô trùng Giám sát môi trường |
6.4 Nhiệm vụ QA
Hệ thống đảm bảo chất lượng của Kyongbo Pharmaceutical hướng tới trở thành một hệ thống chuyên biệt có khả năng sản xuất các sản phẩm chất lượng cao theo yêu cầu của khách hàng và cung cấp kịp thời. Hơn nữa, hệ thống QA đảm bảo sản xuất các hoạt chất dược phẩm và thuốc thành phẩm chất lượng cao thông qua quá trình xác nhận.
Kyongbo Pharmaceutical đã đăng ký các sản phẩm dược phẩm đang hoạt động của mình với MFDS của Hàn Quốc, PMDA của Nhật Bản, EDQM của Châu u, FDA của Hoa Kỳ, CFDA của Trung Quốc và với các cơ quan hữu quan ở Đông Nam Á và các quốc gia khác để mở rộng sự hiện diện trong nước và toàn cầu.
Bộ phận đảm bảo có những hiểu biết vô giá thu được từ các cuộc kiểm tra của các cơ quan quản lý khác nhau và kiểm toán khách hàng hàng năm, cũng như các cuộc tham vấn thường xuyên về GMP với các chuyên gia bên ngoài, để liên tục cải tiến và phát triển hệ thống GMP và QA của chúng tôi.
6.5 Hoạt động QC
Hệ thống kiểm soát chất lượng của Kyongbo Pharmaceutical bao gồm các phòng thí nghiệm thử nghiệm riêng biệt và độc lập cho các loại sản phẩm khác nhau như sản phẩm có hiệu lực cao, sản phẩm thông thường và cephalosporin.
Các phòng thí nghiệm được trang bị các thiết bị phân tích mới nhất (NMR, XRD, ICP, DSC, v.v.) đảm bảo tính chính xác và chính xác của kết quả từ mỗi lần kiểm tra. Các biện pháp kiểm soát chất lượng nghiêm ngặt của Dược phẩm Kyungbođảm bảo cho ra đời các sản phẩm chất lượng cao.
7 Nghiên cứu và phát triển
7.1 Viện nghiên cứu và phát triển
Kyongbo sẽ phát triển thành một công ty cung cấp các loại thuốc chất lượng cao cho sức khỏe con người và một cuộc sống tốt đẹp hơn.
Kể từ khi thành lập Viện Nghiên cứu vào năm 1988, Dược phẩm Kyungbođã phát triển các API với những phẩm chất tuyệt vời dựa trên các công nghệ và bí quyết tích lũy của Dược phẩm Kyungbotrong nhiều thập kỷ.
Là Viện nghiên cứu tốt nhất trong lĩnh vực API, Dược phẩm Kyungbođã đạt được sự tiến bộ chắc chắn và ổn định và đóng vai trò hàng đầu tại Hàn Quốc.
Dược phẩm Kyungbođã cố gắng hết sức để nâng cao khả năng cạnh tranh của mình trên thị trường thế giới. Dược phẩm Kyungbođã xây dựng cơ sở hạ tầng nghiên cứu tốt nhất thông qua các khoản đầu tư R&D liên tục và phát triển nguồn nhân lực và Dược phẩm Kyungbođã cống hiến để phát triển các sản phẩm dược phẩm sáng tạo thông qua các hoạt động nghiên cứu chung.
Trung tâm Nghiên cứu R&D cho APIs Số 1 của Hàn Quốc
Công ty đang thiết lập cơ sở hạ tầng nghiên cứu ở mức cao nhất thông qua đầu tư liên tục vào các nỗ lực R & D và nuôi dưỡng tài năng nghiên cứu xuất sắc.
Thúc đẩy sự phát triển của các loại thuốc cải tiến thông qua nghiên cứu chung sâu rộng.
7.2 Chiến lược R&D
Tầm nhìn
Viện nghiên cứu hàng đầu toàn cầu với chuyên môn.
Giá trị cốt lõi
Sự đổi mới
Sáng tạo
Đam mê
Giao tiếp
Sứ mệnh
Tiến hành ba lĩnh vực nghiên cứu để đạt được mục tiêu tầm nhìn:
|
Thống trị thị trường API Phát triển API chung lần đầu tiên Phát triển API thách thức bằng sáng chế Các loại thuốc có khả năng tiếp thị lớn trong tương lai (bệnh chuyển hóa, thuốc kháng vi-rút) Thuốc chống ung thư, thuốc hiệu lực cao |
Tham gia lĩnh vực kinh doanh mới và phát triển thuốc mới Đổi mới mở Thiết lập cơ sở hạ tầng phát triển thuốc mới kinh doanh CDMO |
Phát triển dược phẩm thành phẩm thông qua chọn lọc và tập trung Phát triển công thức khác biệt mới Phát triển công nghệ xây dựng nền tảng |
7.3 Nhiệm vụ R&D
Dược phẩm Kyungbo không ngừng cố gắng đạt được tầm nhìn của mình "Viện nghiên cứu hàng đầu toàn cầu với chuyên môn" thông qua các hoạt động nghiên cứu khác nhau.
Tập trung nỗ lực vào việc phát triển API chung thứ nhất và API thách thức bằng sáng chế, đặc biệt tập trung ứng dụng các thuốc tim mạch, tăng huyết áp, chuyển hóa, kháng virus, chống ung thư và các loại thuốc có hiệu lực cao.
Tập trung phát triển các công nghệ Nền tảng và xây dựng cơ sở hạ tầng cho các loại thuốc mới.
Nỗ lực trong việc đầu tư mạo hiểm, kết nối mạng lưới nghiên cứu và các hoạt động nghiên cứu chung thông qua đổi mới mở.
Phát triển thành phẩm thông qua các chiến lược lựa chọn và tập trung.
Cống hiến để phát triển công thức mới chuyên biệt và các công nghệ chuẩn bị nền tảng.
7.4 Pipeline
7.5 Thành tích đã đạt được
Kyongbo Pharmaceuticald đã được cấp bằng sáng chế cho 85 API tại Hàn Quốc; 49 hoạt chất được cấp phép ở Nhật; 2 hoạt chất tại Mỹ và 7 chất được công nhận tạ CEP.
8 Sản xuất tại Dược Phẩm KyongBo
8.1 Sản xuẩt API
KyongBo hiện đã được cấp phép công nhận sản xuất 99 API bao gồm các API chung; API Cefalosporin đường uống; API Cefalosporin vô trùng và API chống ung thư
8.2 Thuốc thành phẩm
Thuốc kê đơn; OTC và các phân loại khác
8.3 Kinh doanh CDMO
8.3.1 Đặc điểm
Cơ sở vật chất chuyên dụng và hệ thống chất lượng của Dược phẩm Kyungbohài lòng với các tiêu chuẩn cGMP và đã được chứng minh qua nhiều cuộc kiểm tra từ USFDA, EDQM, PMDA và KFDA.
Kể từ khi thành lập Kyongbo vào năm 1987, với nhiều năm kinh nghiệm sản xuất nhiều loại API về quy mô lô và phân loại, Kyongbo đã trở thành nhà sản xuất API hàng đầu tại Hàn Quốc.
Hiện tại, 7 nhà máy API đang hoạt động tại địa điểm Kyongbo. Kyongbo đã tích lũy kiến thức chuyên môn và kinh nghiệm chuyên sâu về các quy trình API cần thiết để hoàn thành các dự án CRMO từ giai đoạn tiền lâm sàng đến giai đoạn thử nghiệm lâm sàng Ⅰ,Ⅱ,Ⅲ.
Đội ngũ nhân viên lành nghề và đầy đủ kinh nghiệm từ Đơn vị Kinh doanh CRMO (CBU) tại Kyongbo được thành lập để tập trung vào dự án và mở rộng kinh doanh ra nước ngoài, điều này sẽ tạo điều kiện thuận lợi cho việc liên lạc chặt chẽ và phản hồi nhanh chóng với khách hàng.
Có sẵn nhiều cơ sở sản xuất và thiết bị phân tích (NMR, XRD, FT-IR, UV-Vis, LC (GC), ICP, DSC, TGA, PSD, SEM, Kính hiển vi điện tử, v.v.) nên Dược phẩm Kyungbocó đủ khả năng xây dựng quy trình, nhận dạng và phân lập tạp chất
8.4 Dịch vụ
| Phát triển và sản xuất quy trình |
01. Nghiên cứu khả thi 02. Phát triển quy trình
03. Thanh lọc 04. Tối ưu hóa quy trình 05. Cải tiến quy trình 06. Quy mô thí điểm 07. Chuyển quy trình (đến nơi sản xuất) 08. Chuyển giao quy trình (tài liệu GMP)
09. Sản xuất cGMP (Thí điểm, Toàn quy mô) 10. Xác nhận làm sạch 11. Trình độ chuyên môn và quản lý 12. Đánh giá rủi ro 13. Cải tiến hơn nữa |
|
Phát triển phương pháp thử nghiệm. Nguyên liệu thô, sản phẩm trung gian, API |
01. Phát triển phương pháp thử nghiệm (Nguyên liệu thô, Sản phẩm trung gian, API) 02. Chuyển giao phương pháp thử nghiệm (R&D → QC) 03. Chuyển giao phương pháp thử nghiệm (cho khách hàng) 04. Xác nhận phương pháp thử nghiệm (HPLC) 05. Xác nhận phương pháp thử nghiệm (ICP) 06. Xác nhận phương pháp thử nghiệm (GC) 07. Xác nhận phương pháp thử nghiệm (Tài liệu trung cấp & ban đầu) 08. Nghiên cứu độ ổn định |
| Xác nhận quá trình | |
| Tài liệu và đăng ký CMC | |
8.4.1 Công nghệ chủ chốt
01. Phạm vi rộng của phản ứng hóa học hữu cơ & sản xuất cGMP
02. Phản ứng ở nhiệt độ thấp -80oC, STS 316L, 500 ~ 8000L
Phản ứng Grignard (Halide hữu cơ, -80oC)
Phản ứng Reformatsky (Thuốc thử Organozinc, -80oC)
Giảm thiểu có kiểm soát chelation chọn lọc lập thể (Et2BOMe, NaBH4, -80oC)
03. Phản ứng hydro hóa và áp suất cao
Bình phản ứng 10 bar, STS 316L, 1L cách ly, 2.500L
Khử bằng Pd (khí H2)
Khử benzen bằng Pd (khí H2)
04. Độ phân giải động học có tính chọn lọc cao
05. Hiệu lực cao
API gây độc tế bào và không gây độc tế bào, phân loại OEL của Safebridge 4, 10~2.000L
Hệ thống cách ly hiện đại
Hệ thống HVAC 100% một lượt
Phòng thí nghiệm QC riêng biệt tại cơ sở có hiệu lực cao
8.4.2 Dịch vụ CDMO thuốc mới (NCE)
Dựa trên công nghệ sản xuất API có độ tinh khiết cao và kiểm soát chất lượng nghiêm ngặt, Kyongbo thường xuyên được các cơ quan quản lý Hàn Quốc và nước ngoài từ Nhật Bản, Mỹ, Châu u, v.v. kiểm tra thường xuyên và được chứng nhận cGMP.
Kyongbo bắt đầu hoạt động kinh doanh CDMO cho NCE (Thực thể hóa học mới) của CKD Pharm và Crystalgenomics và bắt đầu từ những kinh nghiệm này, giờ đây Dược phẩm Kyungbocó công nghệ chuyên biệt trong nghiên cứu thuốc mới từ giai đoạn đầu đến quá trình phát triển và cải tiến cho đến thương mại hóa.
Kyongbo có các cơ sở riêng biệt có khả năng sản xuất các API thông thường, kháng sinh cephalosporin và carbapenem, API chống ung thư gây độc tế bào và API có hiệu lực cao. Việc kiểm soát chất lượng cũng được tách ra.
Gần đây, Kyongbo đóng vai trò là đối tác phát triển API NCE trong và ngoài nước và thông qua bí quyết dựa trên kinh nghiệm lâu năm từ bộ phận R&D, sản xuất và chất lượng, Kyongbo cung cấp các kỹ năng giải quyết vấn đề và tài liệu liên quan đến CMC dành riêng cho khách hàng theo yêu cầu của chính phủ cơ quan quản lý.
Kyongbo Pharm sẽ tiếp tục đóng góp vào việc phát triển các loại thuốc mới cả trong và ngoài nước thông qua việc hợp tác kịp thời và hiệu quả với tư cách là đối tác phát triển thuốc mới.
9 Sản phẩm tiêu biểu
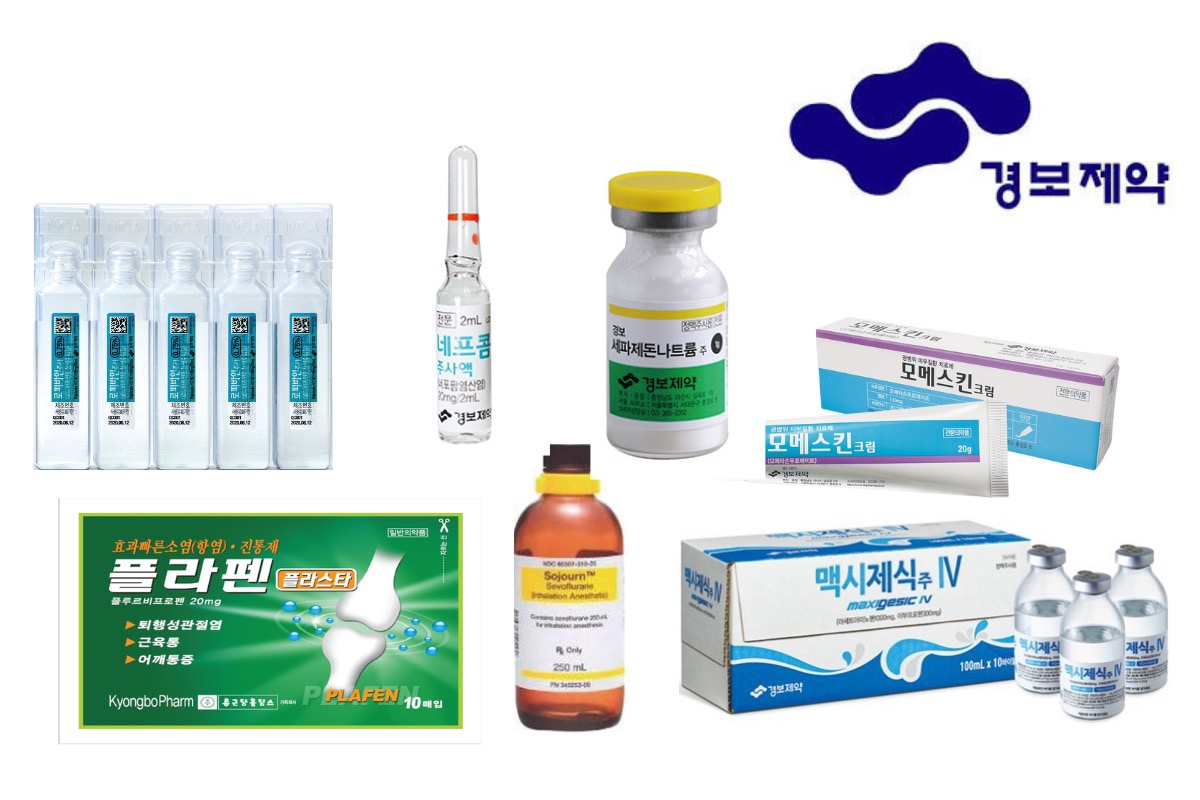
10 Thông tin liên hệ
Địa chỉ: 174, Sirok-ro, Asan-si, Chungcheongnam-do, Hàn Quốc
Liên hệ; 1900888633 hoặc 0868552633