'Dùng Thuốc Theo Cá Thể' đối với thuốc chống đông và chống kết tập tiểu cầu

Trungtamthuoc.com - Chương "Dùng Thuốc Theo Cá Thể' đối với thuốc chống đông và chống kết tập tiểu cầu" sẽ phhân tích được khả năng ứng dụng của gen dược trong cá thể hóa điều trị đối với các thuốc chống động và chống kết tập tiểu cầu.
Trường Đại học Dược Hà Nội, Bộ môn Hóa Sinh - Khoa Công Nghệ Sinh Học
CHƯƠNG 10, Trang 128-138, Giáo trình GEN DƯỢC HỌC - ẢNH HƯỞNG CỦA GEN ĐẾN ĐÁP ỨNG THUỐC, Tải PDF sách TẠI ĐÂY
CHỦ BIÊN
PGS.TS. Phùng Thanh Hương
PGS.TS. Đỗ Hồng Quảng
CÁC TÁC GIẢ THAM GIA BIÊN SOẠN
PGS.TS. Phùng Thanh Hương
PGS.TS. Đỗ Hồng Quảng
PGS.TS. Nguyễn Văn Rư
PGS.TS. Nguyễn Thị Lập
TS. Nguyễn Quốc Bình
Thuốc chống đông và thuốc chống kết tập tiểu cầu đều là các thuốc tác động lên hệ thống đông máu, có thể giúp ngăn ngừa và điều trị nhiều bệnh lý phức tạp và nguy hiểm, giúp bảo vệ tính mạng người bệnh. Mặt khác, đây cũng là hai nhóm thuốc có phạm vi điều trị hẹp, có thể dẫn đến nhiều tai biến nguy hiểm khi dùng thuốc. Do vậy, việc sử dụng các thông tin về cá thể người bệnh để lựa chọn được đúng thuốc phù hợp với liều phù hợp có ý nghĩa rất quan trọng đối với việc sử dụng hai nhóm thuốc này.
1 Dùng thuốc theo cá thể đối với các thuốc chống đông
1.1 Warfarin
Trong các thuốc chống đông, một trong những thuốc được dùng nhiều nhất và cũng “nổi tiếng” nhất về sự dao động đáp ứng điều trị là warfarin. Sự dao động về đáp ứng điều trị này càng đặc biệt đáng chú ý bởi warfarin là một thuốc có phạm vi điều trị hẹp, nếu không đạt hoặc vượt quá phạm vi điều trị đều có thể gây những tai biến nghiêm trọng. Liều dùng thích hợp của warfarin giữa các bệnh nhân khác nhau có thể chênh lệch nhau tới hơn 15 lần (Hình 10.1). Chính vì vậy, các biến chứng do liều warfarin không hợp lý là loại biến chứng thường được báo cáo về FDA nhiều nhất và cũng là một trong những nguyên nhân hàng đầu trong các trường hợp cấp cứu do tai biến dùng thuốc ở Mỹ.
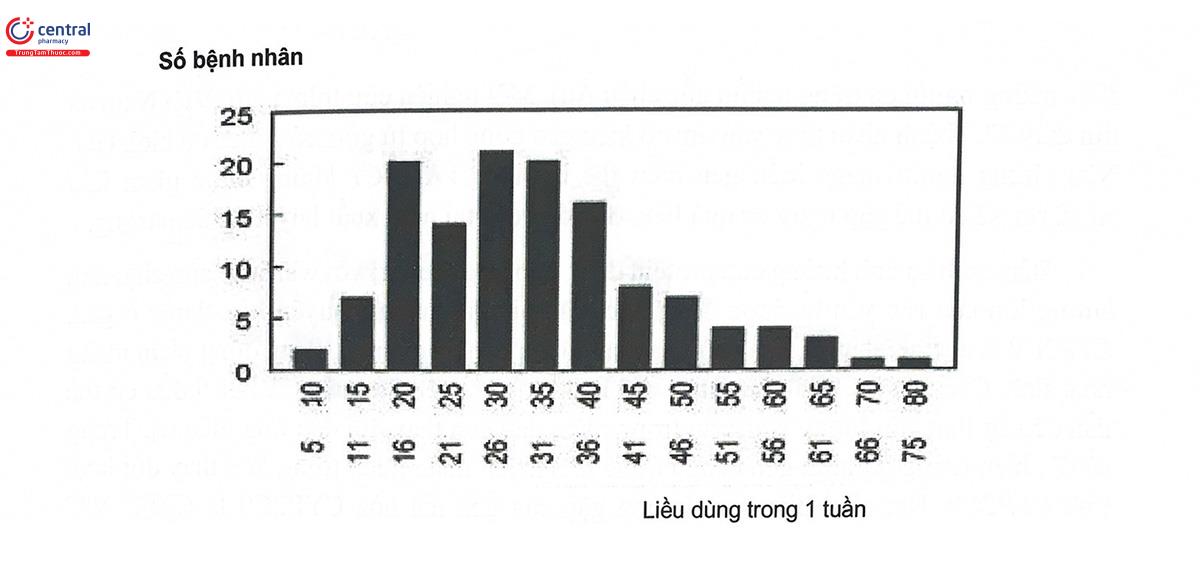
Bên cạnh sự khác biệt giữa các cá thể về giới, tuổi, trọng lượng cơ thể... dẫn đến sự dao động về đáp ứng thuốc, trong điều trị bằng warfarin có sự ảnh hưởng quan trọng của hai loại protein: CYP2C9 và VKOR. Một số phân tích gộp đã cho thấy nguyên nhân từ sự đa hình của hai gen CYP2C9 và VKORCI chiếm khoảng 50% các nguyên nhân gây ra hiện tượng dao động về đáp ứng điều trị với warfarin (Hình 10.2).
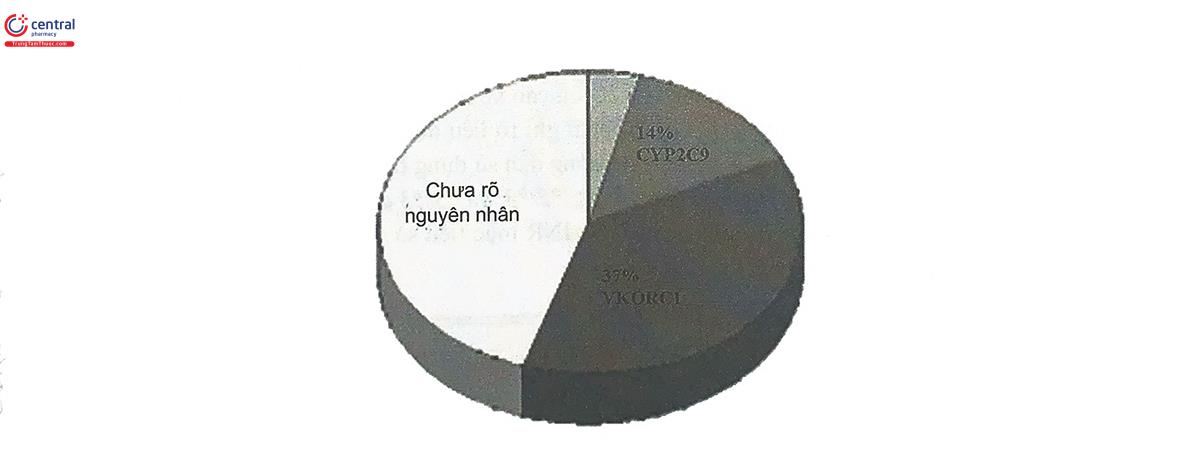
VKOR (vitamine K epoxide reductase) là enzym xúc tác phản ứng khử hóa vitamin K. Đây chính là đích tác dụng của warfarin, bằng cách ức chế VKOR, warfarin ức chế sự tạo thành vitamin K dạng khử và từ đó làm giảm tổng hợp các yếu tố đông máu. Vì vậy, ở những người có số lượng VKOR giảm, thường do nguyên nhân biến đổi trình tự gen mã hóa enzym VKOR, liều dùng cần thiết của warfarin sẽ thấp hơn những người bình thường. Gen mã hóa cho VKOR có tên là VKORC1, loại biến đổi thường gặp của gen này là sự thay thế một nucleotid trong trình tự gen (G1639A). Hiện tượng đa hình này của gen VKORC1 xuất hiện với tần suất khá cao (91% những người có nguồn gốc châu Á và 37% những người da trắng nguồn gốc châu Âu). Một nghiên cứu trên người Việt Nam đã tìm thấy 87,3 bệnh nhân thay van tim có kiểu gen đồng hợp tử gồm cả 2 alen đa hình GG. Nếu những người mang kiểu gen biến thể của gen VKORC1 không được giảm liều warfarin, sẽ có thể gặp nguy cơ quá liều, dẫn đến các tai biến xuất huyết nghiêm trọng.
Bên cạnh sự ảnh hưởng của protein đích, đáp ứng điều trị với warfarin còn chịu ảnh hưởng lớn của các yếu tố dược động học, đặc biệt là enzym chuyển hóa thuốc ở gan. CYP2C9 là enzym chuyển hóa chủ yếu của đồng phân warfarin S, dạng đồng phân mang hoạt tính. Các nguyên nhân làm thay đổi hoạt tính chuyển hóa của CYP2C9 đều có thể dẫn đến sự thay đổi lượng warfarin trong máu, dẫn đến thay đổi đáp ứng điều trị. Trong số đó, hiện tượng đa hình gen cũng có thể là nguyên nhân quan trọng làm thay đổi hoạt tính CYP2C9. Hai alen biến thể thường gặp của gen mã hóa CYP2C9 là CYP2C9*2 (c.430C>T; p.Arg144Cys; rs1799853) và CYP2C9*3 (c.1075A>C; p.I1e359Leu; rs1057910), trong đó có sự thay đổi một nucleotid trong trình tự ADN. Khi kiểu gen của một người xuất hiện ít nhất một trong hai alen CYP2C9*2 hoặc CYP2C9*3, hoạt tính chuyển hóa của enzym CYP2C9 giảm, dẫn đến nồng độ warfarin trong máu cao hơn nồng độ cần thiết để đạt hiệu quả điều trị. Hậu quả là tai biến xuất huyết có thể xảy ra. Tần suất xuất hiện của hai alen đa hình nói trên vào khoảng 20% ở người da trắng châu Âu và khoảng 2 - 4% ở người châu Á và châu Phi.
Từ các kết quả nghiên cứu về ảnh hưởng của hiện tượng đa hình hai gen VKORC1 và CYP2C9, năm 2010, FDA đã đưa ra khuyến cáo về nhãn thuốc đối với warfarin, theo đó, trên tờ hướng dẫn sử dụng của thuốc phải ghi rõ liều dùng tương ứng với từng kiểu gen của hai gen này (Hình 10.3). Trên tờ hướng dẫn sử dụng theo FDA cũng ghi rõ: Các bệnh nhân có kiểu gen CYP2C9 *1/*3, *2/*2, *2/*3, và *3/*3 có thể cần nhiều thời gian hơn (nhiều hơn 2 - 4 tuần) để đạt tới ngưỡng INR mục tiêu so với người mang kiêu gen CYP khác dùng cùng một liệu trình warfarin.
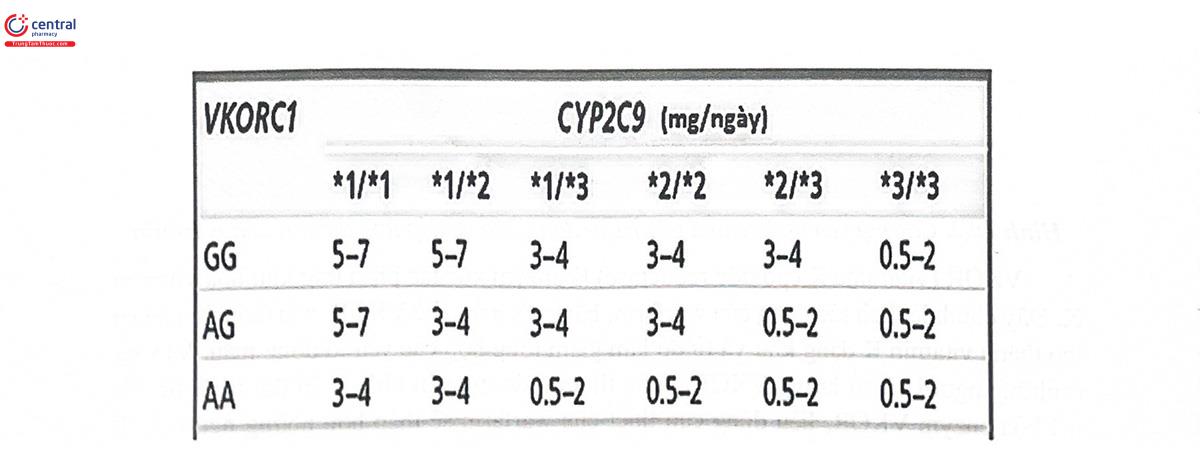
Trong khi đó, Ủy ban Thực hành gen dược trong lâm sàng (CPIC) cho rằng bảng hướng dẫn điều chỉnh liều của FDA chỉ nên dùng khi không thể tiếp cận với internet bởi ủy ban này đã đưa ra những thuật toán cho phép tính toán liều dùng tối ưu của warfarin dựa trên kiểu gen. Các thuật toán này được chia sẻ công khai trên trang web http://www.warfarindosing.org.
Năm 2017, Ủy ban CPIC cũng đưa ra các hướng dẫn về liều dùng warfarin dựa trên kiểu gen cho các bệnh nhân người lớn và bệnh nhi, trong đó, không chỉ dựa trên dữ liệu về các alen biến thể thường gặp của gen VKORC1 và CYP2C9 mà còn dựa trên một số alen khác như CYP2C9*5, *6, *8, *11 hoặc CYP2F4 rs 2108622T, gen mã hóa cho một enzym chuyển hóa khác của warfarin (Hình 10.4).

Cho đến nay, đã có một số thử nghiệm lâm sàng lớn, chủ yếu ở châu Âu, được tiến hành để đánh giá hiệu quả của việc lựa chọn liều warfarin dựa trên kiểu gen. Năm 2013, nghiên cứu về gen dược trong dùng thuốc chống đông (EU-PACT) đã cho thấy hiệu quả của các thuật toán xác định liều dựa trên kiểu gen trong giảm thời gian cần thiết để ổn định liều, tăng khoảng thời gian đạt ngưỡng điều trị, giảm số lần có INR quá cao (>4) so với dùng liều theo cách thông thường, dựa trên đáp ứng lâm sàng. Trong khi đó, cùng trong năm 2013, nghiên cứu Xác định liều dùng tối ưu của thuốc chống đông dựa trên gen di truyền (COAG) không ghi nhận sự khác biệt về hiệu quả điều trị giữa hai nhóm thử nghiệm. Sự khác nhau về kết luận của hai nghiên cứu này có thể do đối tượng của nghiên cứu EU-PACT khá đồng nhất, trên chủ yếu là người da trắng châu Âu, trong khi đối tượng của nghiên cứu COAG có sự đa dạng về nguồn gốc chủng tộc, bao gồm 27% là người gốc Phi. Những người này có thể mang alen CYP2C9*5, *6, *8 và *11, những alen cũng có ảnh hưởng đến đáp ứng điều trị của warfarin nhưng đã không được sàng lọc trong nghiên cứu COAG.
Cuối năm 2016, một nghiên cứu lâm sàng ngẫu nhiên có đối chứng mang tên GIFT đã đánh giá hiệu quả và độ an toàn của việc áp dụng thuật toán xác định liều warfarin cho các bệnh nhân phẫu thuật chỉnh hình. Với cỡ mẫu là 1597, các alen được sàng lọc trong nghiên cứu này gồm CYP2C9*2 và *3, CYP4F2*3, VKORC1-1639. Kết quả cho thấy, việc xác định liều nhờ thuật toán làm giảm 27% các tai biến so với liệu trình thông thường, giúp kiểm soát INR tốt hơn.
1.2 Các thuốc chống đông đường uống mới
Trong những năm gần đây, bên cạnh warfarin, các thuốc chống đông đường uống mới đã được dùng ngày càng phổ biến hơn, nhờ những ưu điểm so với warfarin, đặc biệt là sự ít dao động hơn về đáp ứng điều trị giữa các cá thể, dẫn đến không phải theo dõi chặt chẽ và có thể sử dụng liều dùng cố định. Tuy nhiên, đã có những ghi nhận về vai trò của yếu tố di truyền ảnh hưởng đến đáp ứng điều trị của dabigatran, một thuốc chống đông đường uống mới. Mới đây, một nghiên cứu của châu Âu (RE-LY) xác định các SNP liên quan đến nồng độ đáy và nồng độ đỉnh của dabigatran trong số 1490 bệnh nhân gốc châu Âu. Kết quả cho thấy, 1 SNP ở gen CES1 và 1 SNP ở gen ABCB1 liên quan đến nồng độ đỉnh và 2 SNP ở gen CES1 liên quan đến nồng độ đáy của dabigatran. Những người mang biến thể của cả hai gen này có nồng độ dabigatran dao động từ +29,6% đến -20,2%% so với những người không mang gen biến thể. Tuy nhiên, người ta chưa tìm thấy sự liên quan giữa các SNP này với sự gia tăng nguy cơ tai biến ở người dùng dabigatran.
2 Dùng thuốc theo cá thể đối với các thuốc chống kết tập tiểu cầu
2.1 Clopidogrel
Với ưu điểm về hiệu quả điều trị và giá thành rẻ, cho đến nay, clopidogrel vẫn đang là một trong những thuốc chống kết tập tiểu cầu được kê đơn rộng rãi nhất để phòng các biến chứng ở bệnh nhân hội chứng mạch vành cấp, nhồi máu cơ tim, những bệnh nhân đang dùng can thiệp mạch vành qua da. Tuy nhiên, khoảng 30 - 40% bệnh nhân không đáp ứng tốt với thuốc hoặc có phản ứng tiểu cầu cao trong điều trị (high on-treatment platelet reaction - HTPR), dẫn đến các biến chứng tim mạch. Bên cạnh các yếu tố ảnh hưởng như tuổi, BMI, bệnh mắc kèm, tương tác thuốc..., người ta đã phát hiện ra một số gen ảnh hưởng đáng kể đến đáp ứng với clopidogrel.
Clopidogrel là một tiền thuốc của nhóm thienopyridin thế hệ 2, phải qua chuyển hóa ở gan, chủ yếu nhờ CYP2C19, để khoảng 15% biến đổi thành sản phẩm thiol có hoạt tính. Số còn lại được thoái hóa nhờ các enzym esterase, mà chủ yếu là carboxyesterase 1 (CES1) thành các dẫn chất của acid carboxylic không có hoạt tính.
Trong các enzym chuyển hóa pha I của clopidogrel, CYP2C19 là enzym chủ chốt và cũng là enzym mà gen mã hóa có tính đa hình cao. Alen biến thể gây giảm chức năng phổ biến nhất của gen mã hóa CYP2C19 là CYP2C19*2 (rs4244285), sự thay thế chỉ một nucleotid ở exon 5 đã dẫn đến tạo thành mã kết thúc sớm nghĩa là thay đổi cấu trúc và chức năng của protein tương ứng. Alen biến thể này chiếm khoảng 20 - 30% ở người châu Âu và châu Phi, 60% ở người châu Á.
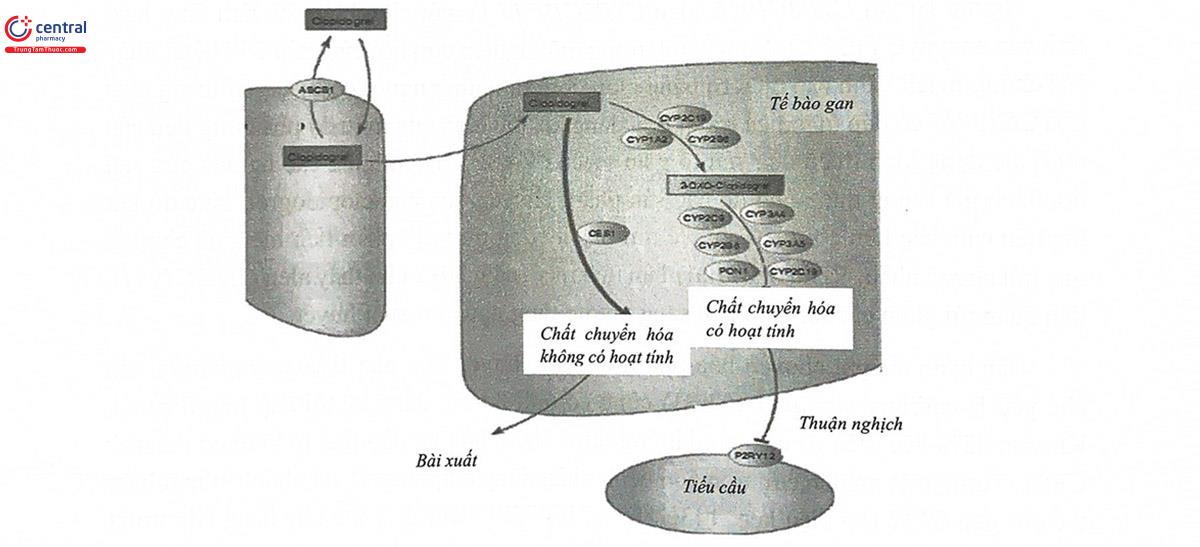
Có nhiều bằng chứng về ảnh hưởng của alen CYP2C19*2 tới dược động học và dược lực học của clopidogrel. Năm 2006, lần đầu tiên, Hulot công bố kết quả trên 28 người tình nguyện khỏe mạnh cho thấy những người mang alen biến thể này có đáp ứng kém hơn với clopidogrel, thông qua phản ứng hoạt hóa tiểu cầu dưới tác dụng của ADP. Kết quả này được giải thích do giảm hoạt tính CYP2C19, giảm số lượng sản phẩm chuyển hóa có hoạt tính của thuốc. Trong những năm gần đây, có nhiều nghiên cứu ghi nhận ảnh hưởng của alen CYP2C19*2 tới hiệu quả điều trị về tim mạch. Những bệnh nhân mà kiểu gen mang ít nhất 1 alen CYP2C19*2 có nguy cơ tai biến tim mạch cao hơn đáng kể so với những người mang kiểu gen đồng hợp tử wildtype, cụ thể là nguy cơ huyết khối stent tăng 2 - 3 lần. Hầu hết các phân tích meta đều cho thấy alen này ảnh hưởng nhiều nhất ở những bệnh nhân can thiệp mạch vành qua da là những người có nguy cơ cao bị huyết khối stent.
Đáng chú ý là tại Việt Nam cũng đã có những kết quả nghiên cứu bước đầu về đa gen CYP2C19 trong điều trị hội chứng mạch vành cấp. Trong 116 bệnh nhân hội chứng mạch vành cấp dùng clopidogrel, số người mang alen CYP2C19*2 và *3 lần lượt là 40,5% và 16,4%, trong đó, phân tích hồi quy đa biến cho thấy chỉ kiểu gen mang CYP2C19*2 có ảnh hưởng tới độ kết tập tiểu cầu và tỷ lệ kháng clopidogrel. Bên cạnh alen đa hình này, có thêm một yếu tố ảnh hưởng tới mức độ kháng clopidogrel là tiền sử hút thuốc lá. Với tỷ lệ CYP2C19*2 lên tới 20,5% ở người Kinh Việt Nam, rất cần có những lưu ý về yếu tố di truyền trong sử dụng clopidogrel cho người Việt Nam.
Ngược lại với CYP2C19*2, alen CYP2C19*17 là một alen biến thể làm tăng hoạt tính của enzym CYP2C19. Năm 2009, trong một nghiên cứu hồi cứu trên 598 bệnh nhân hội chứng mạch vành cấp điều trị bằng clopidogrel, những người có kiểu gen mang alen CYP2C19*17 có đáp ứng điều trị tốt hơn đáng kể, thể hiện qua mức độ phản ứng tiểu cầu dưới tác dụng kích thích của yếu tố giãn mạch (VASP). Tuy nhiên, các nghiên cứu sau đó, đánh giá thông qua nồng độ các sản phẩm chuyển hóa của clopidogrel, mức độ kết tập tiểu cầu, các tiêu chí hiệu quả về tim mạch cũng như các phân tích meta đã cho kết quả trái ngược nhau. Ví dụ như: Hai phân tích meta năm 2012 cho thấy alen CYP2C19*17 liên quan tới giảm các tai biến lâm sàng nhưng tăng nguy cơ xuất huyết.
Bên cạnh enzym chuyển hóa pha I, enzym chuyển hóa pha II của clopidogrel mà chủ yếu là carboxyesterase 1 (CES1) cũng có ảnh hưởng đáng kể tới đáp ứng điều trị. Khoảng 85% liều điều trị của clopidogrel được thoái hóa và đào thải ra khỏi cơ thể nhờ CES1. Trong một nghiên cứu trên 566 bệnh nhân dùng clopidogrel, đã ghi nhận một biến thể của gen CES1 (ký hiệu là p. 143G>E, rs71647871) làm thay thế Gly bằng Glu trong chuỗi acid amin, đã ảnh hưởng đến dược động học và dược lực học của thuốc. Những người mang kiểu gen 143E đồng hợp tử có nồng độ các sản phẩm chuyển hóa có hoạt tính của clopidogrel cao hơn đáng kể so với kiểu gen wildtype, kèm theo hoạt tính kết tập tiểu cầu dưới tác dụng của ADP cao hơn. Một ghi nhận khác trên 350 bệnh nhân mạch vành cho thấy, người mang alen CES1 143E có đáp ứng với clopidogrel tốt hơn, thể hiện qua hoạt tính kết tập tiểu cầu, 0% những người mang alen này bị tai biến tim mạch trong vòng 1 năm theo dõi. Các kết quả này tương đồng với một kết quả nghiên cứu trên gan người, trong đó phản ứng thủy phân clopidogrel và 2-oxo-clopidogrel bị ức chế ở những người mang alen 143E.
Ngoài các gen liên quan đến dược động học của clopidogrel, đã có một số nghiên cứu quan tâm đến các gen liên quan đến dược lực học của thuốc này. Khi vào máu, các sản phẩm chuyển hóa có hoạt tính của clopidogrel gắn không thuận nghịch và ức chế receptor P2Y12 trên bề mặt tiểu cầu, dẫn đến giảm sự hoạt hóa và kết tập tiểu cầu dưới tác dụng của ADP. Điều đó có nghĩa là P2Y12 là protein đích của clopidogrel. Có 1 Haplotype gồm các SNP thường đi kèm nhau trên gen P2RY12 (gen mã hóa receptor P2Y12), dẫn đến tăng biểu hiện gen, tăng hoạt tính tiểu cầu khi dùng clopidogrel. Tuy nhiên, các kết quả về ảnh hưởng của Haplotype này trên đáp ứng với clopidogrel trên lâm sàng cho kết quả khá mâu thuẫn.
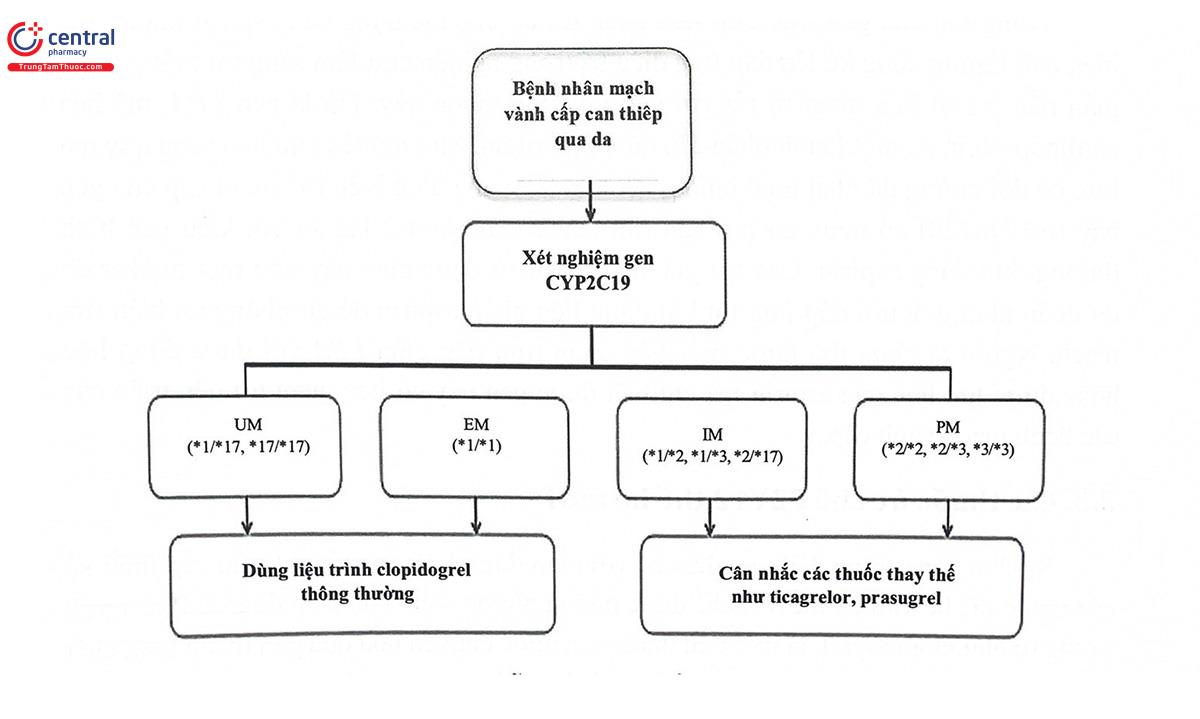
Như vậy, trong các gen liên quan đến đáp ứng với clopidogrel, gen CYP2C19 có nhiều bằng chứng lâm sàng về ảnh hưởng tới đáp ứng điều trị. Vì vậy, clopidogrel cũng là thuốc được FDA khuyến cáo về việc ghi nhãn thuốc cần có thông tin hướng dẫn sử dụng dựa trên kiểu gen. Cụ thể là những người mang alen CYP2C19 làm giảm hoạt tính enzym chuyển hóa cần cân nhắc thay clopidogrel bằng một thuốc ức chế P2Y12 khác. Bên cạnh đó, Ủy ban áp dụng gen dược trong lâm sàng (CPIC) cũng đưa ra phác đồ hướng dẫn dùng thuốc chống kết tập tiểu cầu đối với các kiểu gen khác nhau của gen CYP2C19 (Hình 10.6).
2.2 Aspirin
Aspirin là một thuốc chống kết tập tiểu cầu được dùng phổ biến để ngăn ngừa nhồi máu cơ tim, đột quỵ... với cơ chế ức chế prostaglandin synthase 1 (PTGS1) hay còn gọi là cyclooxygenase 1 (COX1). Hiện tượng kém đáp ứng với aspirin đã được báo cáo trong 6 - 60% các trường hợp. Nhiều nghiên cứu về liên quan kiểu gen trong quần thể (GWAS) đã thống kê một loạt gen liên quan đến đáp ứng của aspirin, từ những gen liên quan đến enzym chuyển hóa thuốc như butyrylcholinesterase (BCHE) cho đến các gen liên quan đến tiểu cầu, tế bào đích của thuốc. Thậm chí, một nghiên cứu đã thống kê một nhóm 62 gen được gọi chung là “chữ ký đáp ứng với aspirin” (Aspirin response signature - ARS) gồm các gen mà biểu hiện của chúng liên quan chặt chẽ đến chức năng của tiểu cầu dưới tác dụng của aspirin. Mặc dù đã được khẳng định qua các nghiên cứu in vitro và ex vivo, ý nghĩa lâm sàng của các gen này còn là vấn đề gây nhiều tranh cãi qua các thử nghiệm lâm sàng gần đây. Trong số đó, chỉ có một số ít gen được chứng minh vai trò bởi nghiên cứu lâm sàng, ví dụ như gen PEAR1, thường biểu hiện ở tiểu cầu, tham gia vào sự hoạt hóa tiểu cầu. Một alen biến thể của gen này (rs12041331) làm giảm chức năng tiểu cầu trong đáp ứng với aspirin. Nghiên cứu lâm sàng cho thấy những người mang alen này có nguy cơ tai biến tim mạch trong điều trị bằng aspirin cao hơn người mang kiêu gen bình thường.
Trong khi các gen trực tiếp liên quan tới cơ chế tác dụng của aspirin không thể hiện ảnh hưởng đáng kể lên đáp ứng điều trị trong nghiên cứu lâm sàng thì một gen rát gián tiếp lại có liên quan rõ rệt với đáp ứng của thuốc này. Đó là gen LPA, mã hóa apolipoprotein A, một thành phần cấu tạo lipoprotein. Một nghiên cứu lâm sàng quy mô lớn, có đối chứng đã phát hiện những bệnh nhân mang alen biến thể hiếm gặp của gen này (rs3798220) có nguy cơ tai biến tim mạch giảm hơn 2 lần so với kiểu gen bình thường, khi dùng aspirin. Các tác giả đã đề xuất sử dụng alen này như một marker để dự đoán những người đáp ứng tốt khi dùng liệu pháp aspirin để dự phòng tai biến tim mạch. Người ta chưa tìm được mối liên quan trực tiếp giữa LPA với dược động học hoặc dược lực học của aspirin mà chỉ biết được gen này có liên quan tới tiến triển của các bệnh mạch vành cấp.
2.3 Các thuốc ức chế P2Y12 thế hệ mới
Sự dao động trong đáp ứng điều trị với clopidogrel đặt ra một nhu cầu cấp thiết về các thuốc thế hệ mới có thể hạn chế được những nhược điểm của clopidogrel. Prasugrel, tương tự như clopidogrel, là một tiền thuốc cần được chuyển hóa qua gan thành hoạt chất ức chế receptor P2Y12 ở tiểu cầu. Tuy nhiên khác với clopidogrel, phần lớn lượng prasugrel đưa vào đều được chuyển thành hoạt chất, do đó, hoạt tính ức chế tiểu cầu mạnh hơn. Một chất ức chế P2Y12 mới khác là ticagrelor là dạng chất có hoạt tính, không cần qua giai đoạn hoạt hóa ở gan.
Mặc dù có những ưu điểm như vậy nhưng cả prasugrel và ticagrelor vẫn có hiện tượng dao động về đáp ứng điều trị, đánh giá qua hoạt tính tiểu cầu ex vivo và các tai biến tim mạch khi dùng thuốc. Một số tác giả đề xuất dùng test chức năng tiểu cầu ex vivo làm biomarker để dự đoán bệnh nhân nào đáp ứng tốt với thuốc. Cho đến nay, mặc dù chưa có các nghiên cứu GWAS về đáp ứng với prasugrel nhưng đã xác định được một số gen liên quan. Một số nghiên cứu đã cho thấy alen CYP2C19* và CYP2C19*17 có ảnh hưởng đáng kể tới hoạt động tiểu cầu ở bệnh nhân đặt stent mạch vành dùng prasugrel. Ticagrelor không cần qua chuyển hóa ở gan để trở thành dạng có hoạt tính, do đó, đáp ứng với thuốc này ít chịu ảnh hưởng của đa hình các CYP. Tuy nhiên, một số gen mã hóa các protein có liên quan tới dược động học của ticagrelor đã được xác định là ảnh hưởng tới nồng độ của thuốc trong máu. Ví dụ như: Một alen biến thể gây giảm chức năng (SLC01B1*5) của gen mã hóa protein vận chuyển SCL01B1 và một alen biến thể (rs61361928) của gen UGT2B7 mã hóa enzym UDP-Glucuronosyltransferase-2B7, enzym chuyển hóa pha II của ticagrelor liên quan tới hiện tượng tăng nồng độ ticagrelor và các chất chuyển hóa có hoạt tính của nó trong máu của bệnh nhân dùng thuốc. Tuy nhiên, chưa tìm thấy các bằng chứng lâm sàng của việc tăng nồng độ thuốc đi kèm theo tăng các biến chứng xuất huyết hoặc nhồi máu ở người dùng ticagrelor.
3 Kết luận
Trong các thuốc chống đông và chống kết tập tiểu cầu, mới chỉ hai thuốc kinh điển là warfarin và clopidogrel có nhiều dữ liệu về ảnh hưởng của đa hình gen tới đáp ứng điều trị, bao gồm cả dữ liệu nghiên cứu trên người Việt Nam. Các dữ liệu này đã đưa tới các hướng dẫn về lựa chọn thuốc và điều chỉnh liều trong lâm sàng cũng như những khuyến cáo cần thiết trên nhãn thuốc.
Với các thuốc còn lại trong hai nhóm điều trị này chủ yếu mới chỉ dừng ở mức độ nghiên cứu cơ bản, các kết quả nghiên cứu cho đến nay vẫn chưa chứng minh được mức độ ảnh hưởng đáng kể của đa hình gen lên đáp ứng điều trị.
4 Tài liệu tham khảo
1. Đào Văn Đôn (2019), Ảnh hưởng của đa hình CYP2C19 tới độ ngưng tập tiểu cầu trên bệnh nhân sử dụng clopidogrel điều trị nhồi máu cơ tim cấp có ST chênh tại Bệnh viện Quân y 103, Tạp chí Y học Việt Nam 1(481), 210-213.
2. Nhung Phuong Vu (2019), CYP2C19 genetic polymorphism in the Vietnamese population, Annals Of Human Biology. 2019, Vol. 46, No. 6, 491-497.
3. Thuy Thi Pham (2019), VKORC1 and CYP2C9*3 Polymorphisms and Their Impacts to Acenocoumarol Dosage in Vietnamese Heart Valve Replacement Patients†1, Walailak J Sci & Tech. 2019; 16(3): 207-215.
4. Johnson JA et al (2017), Clinical Pharmacogenetics Implementation Consortium (CPIC) Guideline for Pharmacogenetics-Guided Warfarin Dosing: 2017 Update, Clin Pharmacol Ther. 2017 Sep;102(3):397-404.
5. Melissa D. Klein (2019), Clinical Utility of CYP2C19 Genotyping to Guide Antiplatelet Therapy in Patients With an Acute Coronary Syndrome or Undergoing Percutaneous Coronary Intervention, Arterioscler Thromb Vasc Biol, DOI: 10.1161/ATVBAHA.118.311963.

