Ý nghĩa và điều kiện cần thiết để triển khai 'Dùng Thuốc Theo Cá Thể'

Trungtamthuoc.com - Chương "Đại cương về dùng thuốc theo cá thể" này sẽ trình bày được các khái niệm cơ bản liên quan đến dùng thuốc theo cá thể, ý nghĩa và điều kiện cần thiết để triển khai dùng thuốc theo cá thể, các lĩnh vực lâm sàng đang áp dụng dùng thuốc theo cá thể.
Trường Đại học Dược Hà Nội, Bộ môn Hóa Sinh - Khoa Công Nghệ Sinh Học
CHƯƠNG 9, Trang 120-127, Giáo trình GEN DƯỢC HỌC - ẢNH HƯỞNG CỦA GEN ĐẾN ĐÁP ỨNG THUỐC, Tải PDF sách TẠI ĐÂY
CHỦ BIÊN
PGS.TS. Phùng Thanh Hương
PGS.TS. Đỗ Hồng Quảng
CÁC TÁC GIẢ THAM GIA BIÊN SOẠN
PGS.TS. Phùng Thanh Hương
PGS.TS. Đỗ Hồng Quảng
PGS.TS. Nguyễn Văn Rư
PGS.TS. Nguyễn Thị Lập
TS. Nguyễn Quốc Bình
Sử dụng thuốc theo cá thể hay cá thể hóa điều trị là quan điểm trị liệu đã tồn tại từ hàng ngàn năm trước, được làm sáng tỏ và ngày càng được áp dụng rộng rãi từ cuối thế kỷ 20, đầu thế kỷ 21.
Y học phương Đông nguồn gốc Trung Quốc và Ấn Độ, ngay từ trước công nguyên đã nhấn mạnh tầm quan trọng của việc xem xét các đặc điểm của mỗi cá thể bệnh nhân trong chữa bệnh, bởi quan niệm dùng thuốc và y thuật để lập lại cân bằng trong cơ thể, từ đó loại trừ bệnh tật.
Hippocrates, ông tổ của ngành y hiện đại cũng đã kết luận: “Điều quan trọng là phải hiểu được bệnh này do người nào mang hơn là người này mang bệnh nào”. Đầu thế kỷ 20, Sir William Osler, người được coi là cha đẻ của ngành phẫu thuật thần kinh hiện đại cũng đã có một câu nói nổi tiếng: “Người thầy thuốc tốt chữa bệnh, người thầy thuốc vĩ đại chữa người mang bệnh”.
Như vậy, ý tưởng về “Cá thể hóa điều trị” đã có từ rất lâu đời, nhưng mãi tới giữa thế kỷ 20, với sự phát triển của y dược học, di truyền học, của công nghệ chẩn đoán hình ảnh và công nghệ khai thác dữ liệu, những nghiên cứu về sự khác biệt trong đáp ứng thuốc giữa các cá thể khác nhau, tập trung chủ yếu vào các enzym chuyển hóa thuốc mới được quan tâm. Đặc biệt, từ đầu thế kỷ 21, khi những thông tin về hệ gen người ngày càng sáng tỏ cùng với sự phát triển nhanh chóng của công nghệ genomics, công nghệ tin sinh học, đã có sự thay đổi mạnh mẽ, giúp các nhà khoa học có những công cụ hiệu quả để đưa “Cá thể hóa điều trị” từ ý tưởng trở thành hiện thực, phát triển thực sự trong thực tế lâm sàng.
1 "Dùng thuốc theo cá thể" và các khái niệm liên quan
Thực ra chưa có một định nghĩa chính thức về “Dùng thuốc theo cá thể” (Personalized medicine) hay “Cá thể hóa điều trị” (Personalized therapy). Khái niệm này được sử dụng lần đầu tiên trong một chuyên luận năm 1998 và bắt đầu xuất hiện trên MEDLINES từ năm 1999. Đến nay, có nhiều định nghĩa khác nhau về “Dùng thuốc theo cá thể”, tùy theo quan điểm của từng tổ chức. Một cách ngắn gọn, quan điểm của châu Âu, “Cá thể hóa điều trị” là “Đưa ra đúng liệu pháp điều trị cho đúng người, dùng đúng liều, vào đúng thời điểm”. Theo Hiệp hội Y học Hoa Kỳ, “Cá thể hóa điều trị” là “Toàn bộ các hoạt động chăm sóc y tế dựa trên thông tin cụ thể của từng bệnh nhân về lâm sàng, di truyền và môi trường”. Theo Viện Ung thư Hoa Kỳ, thuốc cá thể hóa là “Thuốc sử dụng thông tin của cá nhân về gen, protein và môi trường để phòng, chẩn đoán và điều trị một bệnh”.
Bên cạnh đó, có một số khái niệm thường được dùng đồng thời hoặc thay thế cho khái niệm “Dùng thuốc theo cá thể”. Y học chính xác (precision medicine) là thuật ngữ được Viện Hàn lâm Khoa học Hoa Kỳ dùng đề chỉ: “Việc sử dụng các dữ liệu genomic, epigenomic và các dữ liệu khác để thiết lập những mô hình cá nhân của một bệnh, nhằm đạt được những phương pháp điều trị tốt hơn cho cá nhân đó”. Y học phân tầng (stratified medicine) là khái niệm chỉ sự phân chia quần thể bệnh nhân thành những nhóm nhỏ, dựa trên một số đặc điểm chung, mỗi nhóm sẽ đáp ứng tốt hơn với một thuốc nhất định hoặc một liệu pháp điều trị nhất định. Y học phân tầng được coi là cốt lõi của “Cá thể hóa điều trị”, cho phép có những biện pháp chiến lược để chẩn đoán, điều trị phù hợp và hiệu quả cho từng bệnh nhân hoặc nhóm bệnh nhân.
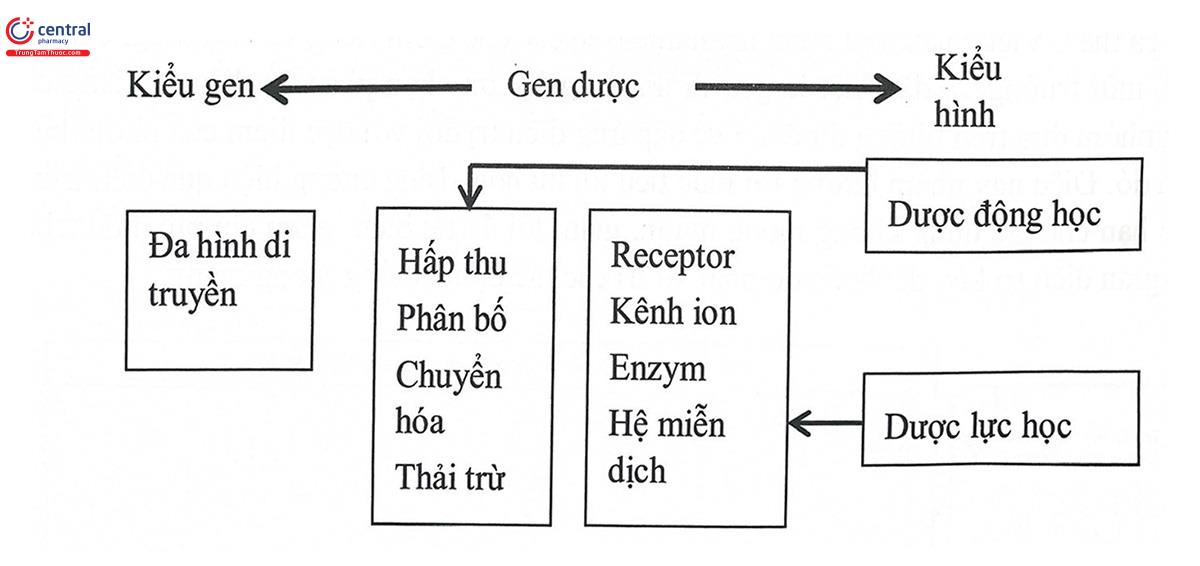
Bên cạnh đó, một khái niệm được coi là quan trọng đặc biệt trong “Dùng thuốc theo cá thể”, giúp cho nó từ một ý tưởng trở thành một lĩnh vực phát triển nhanh chóng trong thế kỷ 21 là khái niệm Gen dược/ Hệ gen dược (Pharmacogenetics/ Pharmacogenomics). Việc nghiên cứu các thông tin về ADN, ARN với các kỹ thuật sinh học phân tử và công nghệ sinh học hiện đại, cho phép sử dụng các thông tin về di truyền của bệnh nhân để đưa ra những quyết định điều trị phù hợp nhất nhờ dự đoán được đáp ứng thuốc ở mỗi bệnh nhân thông qua các yếu tố dược động học và dược lực học.
2 Ý nghĩa của dùng thuốc theo cá thể
Trước kia, phần lớn các thuốc được thiết kế và phát triển để điều trị tất cả bệnh nhân mắc cùng một bệnh nhất định. Một thực tế được thừa nhận rộng rãi là một thuốc cho dù có chất lượng tốt nhất, được thử nghiệm chặt chẽ, thận trọng trước khi đưa ra thị trường đều có thể không đạt hiệu quả hoặc có nhiều tác dụng không mong muốn đối với một số bệnh nhân. Đối với những bệnh có nhiều lựa chọn về thuốc điều trị, việc quyết định dùng thuốc nào thường do kinh nghiệm và thói quen của thầy thuốc. Y học bằng chứng thường đưa ra một phác đồ điều trị chuẩn mà không tính đến sự khác biệt về đáp ứng thuốc giữa các cá thể bệnh nhân khác nhau. Các thử nghiệm lâm sàng thường dựa trên các phân tích thống kê với cỡ mẫu lớn trên cả quần thể nói chung để đưa ra kết luận và hướng dẫn sử dụng áp dụng cho từng người bệnh. Trong khi đó, một thực tế là các cá thể có đặc điểm khác nhau thường có đáp ứng rất khác biệt với từng thuốc nhất định. Thông thường trước kia, các trường hợp không đáp ứng tốt sau khi dùng một phác đồ điều trị nào đó sẽ được thay thế bằng phác đồ khác. Tuy nhiên, đôi khi đáp ứng thuốc kém có thể dẫn đến những hậu quả nghiêm trọng cho bệnh nhân, nhiều trường hợp không cho phép có cơ hội sửa sai.
Tất cả các vấn đề nói trên có thể được khắc phục bằng cách tiếp cận “Dùng thuốc theo cá thể”. Việc phân loại bệnh nhân dựa trên các đặc điểm riêng về lâm sàng, cận lâm sàng, môi trường và đặc biệt là gen di truyền giúp lựa chọn phác đồ điều trị riêng cho từng nhóm dựa trên những dự đoán về đáp ứng điều trị đối với đặc điểm của nhóm bệnh nhân đó. Điều này nhằm hướng tới mục tiêu tối ưu hóa: Tăng cường hiệu quả điều trị và hoặc hạn chế tác dụng không mong muốn, giảm tối đa tai biến, giảm chi phí điều trị do thời gian điều trị kéo dài hoặc do phải xử trí các tác dụng không mong muốn.
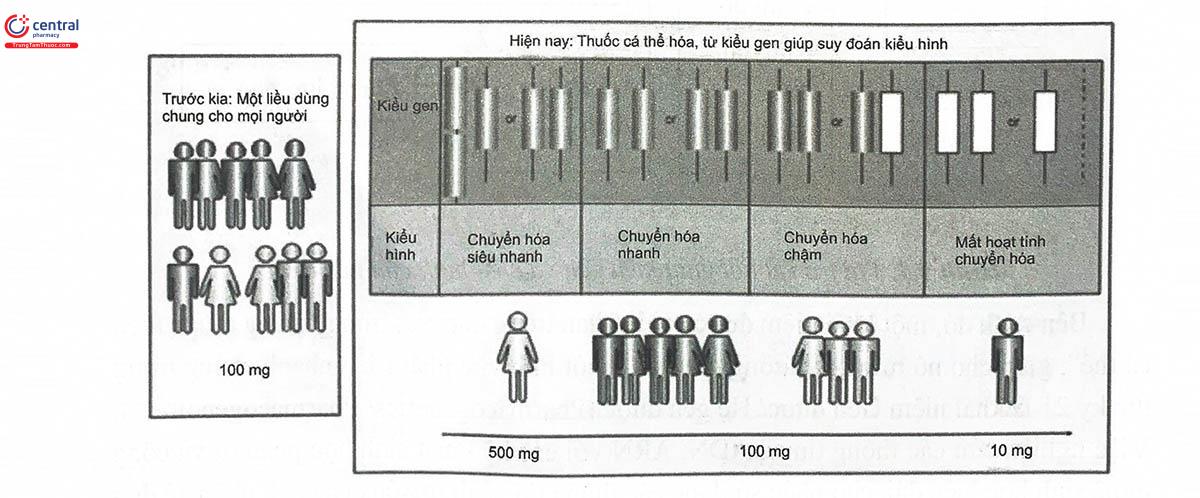
Bên trái: Mọi người đều dùng cùng 1 thuốc, cùng 1 liều; Bên phải: Lựa chọn liều của thuốc dựa trên thông tin di truyền về kiểu gen, kiểu hình.
3 Các điều kiện cần thiết để triển khai việc dùng thuốc theo cá thể
Với mục tiêu lựa chọn được đúng thuốc, đúng liều, dùng đúng thời điểm cho đúng người, cá thể hóa điều trị thường liên quan đến sử dụng kết hợp hai sản phẩm y học, thông thường là một công cụ chẩn đoán/ xét nghiệm và một thuốc điều trị. Các công cụ chẩn đoán bao gồm cả chẩn đoán in vitro (ví dụ: xét nghiệm một đột biến gen di truyền, xác định sự có mặt, vắng mặt hoặc định lượng một marker sinh học) và chẩn đoán in vivo (ví dụ: điện não đồ, điện tâm đồ, chẩn đoán hình ảnh). Mức độ của các chẩn đoán có thể đi từ những thông số đơn giản như trọng lượng cơ thể, diện tích bề mặt da, huyết áp đến những thông số xét nghiệm hóa sinh, huyết học như độ thanh thải creatinin, thời gian đông máu và gần đây là các xét nghiệm di truyền như đột biến làm giảm hoạt tính của một enzym chuyển hóa thuốc hay sự có mặt của một receptor đặc hiệu... Rất nhiều các công cụ chẩn đoán khác nhau đã được phát triển nhằm cung cấp những thông tin về đặc điểm cá thể của từng bệnh nhân.
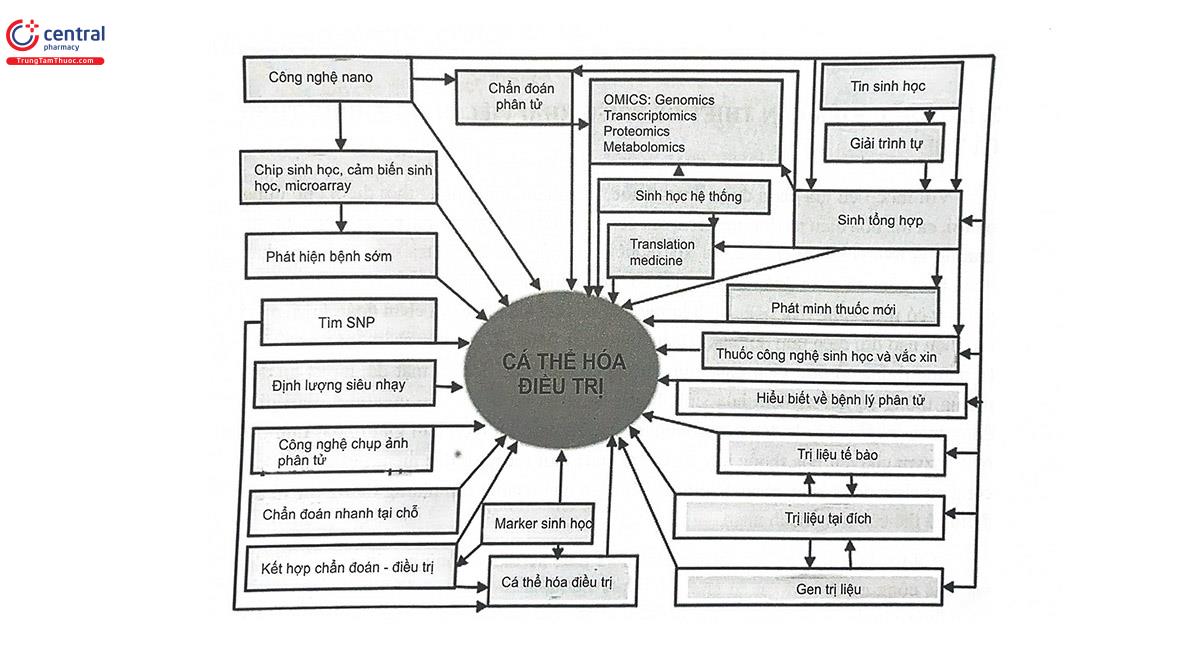
“Cá thể hóa điều trị” có thể phát triển và thực sự thành công hay không phụ thuộc vào các công cụ chẩn đoán có cho các thông tin đáng tin cậy hay không. Nếu công cụ chẩn đoán cho kết quả không chính xác có thể dẫn đến những quyết định sai lầm dựa trên các kết quả đó. Ví dụ: Dựa trên một chẩn đoán không chính xác, có thể lựa chọn thuốc không phù hợp cho một bệnh nhân dẫn đến không đạt hiệu quả điều trị và/ hoặc có tác dụng không mong muốn. Để có các công cụ chẩn đoán chính xác, đáng tin cậy, điều kiện cốt lõi là trình độ công nghệ. Điều đó giải thích vì sao “Cá thể hóa điều trị” thực sự phát triển và đi vào thực tế từ đầu thế kỷ 21, với sự phát triển vượt bậc của nhiều công nghệ tiên tiến. Hình 9.3 thể hiện mối quan hệ của “Cá thể hóa điều trị” với các ngành công nghệ khác nhau.
Bên cạnh yếu tố công nghệ, để phát triển những ứng dụng của “Cá thể hóa điều trị”, thực sự đem lại những lợi ích cho bệnh nhân, thì các yếu tố về truyền thông và chính sách cũng đóng vai trò hết sức quan trọng. Minh chứng rõ nhất là Hoa Kỳ, một trong những nước có “Cá thể hóa điều trị” phát triển mạnh nhất, Cơ quan Quản lý Dược và An toàn thực phẩm (FDA) có nhiều chính sách, quy định, hướng dẫn hỗ trợ việc triển khai áp dụng “Dùng thuốc theo cá thể” vào thực tế lâm sàng.
| Bảng 9.1. Một số thuốc được FDA khuyến cáo cần cân nhắc thông tin về di truyền của bệnh nhân khi dùng | |||
| Thuốc | Gen | Thuốc | Gen |
| Clopidogrel | CYP2C19 | Azathiopurin |
TPMT |
| Atomoxetin | CYP2D6 | Irinotecan | UGT1A1 |
| Codein | CYP2D6 | Cetuximab | EGFR |
| Tamoxifen | CYP2D6 | Erlotinib | EGFR |
| Warfarin | CYP2C9, VKORC1 | Imatinib mesylate | C-KIT |
| Abacavir | HLA-B*5701 | Panitumumab | KRAS |
| Carbamazepin | HLA-B*1502 | Trastuzumab | Her2/neu |
Chỉ tính riêng trong 2 năm 2017 - 2018, 1/3 số thuốc được FDA phê duyệt đã đưa các thông tin cá thể hóa điều trị vào nhãn thuốc và tờ hướng dẫn sử dụng nhằm làm tăng hiệu quả điều trị/ giảm thiểu TDKMM (Bảng 9.1).
Tại Việt Nam, việc áp dụng “Dùng thuốc theo cá thể” dựa trên biểu hiện của marker sinh học cũng đã được áp dụng. Thông tư số 40/2014/TT-BYT về danh mục các thuốc tân dược được BHYT chi trả cũng đã đưa ra quy định về bằng chứng cần thiết để chỉ định, thanh toán cho một số thuốc điều trị ung thư khi và chỉ khi bệnh nhân dương tính với marker sinh học như EGFR, KRAS, Her2. Thông tư số 37/2015/TTLT-BYT-BTC quy định chi trả chi phí xét nghiệm phát hiện đột biến gen EGFR, KRAS và BRAS.
4 Các lĩnh vực lâm sàng đang áp dụng dùng thuốc theo cá thể
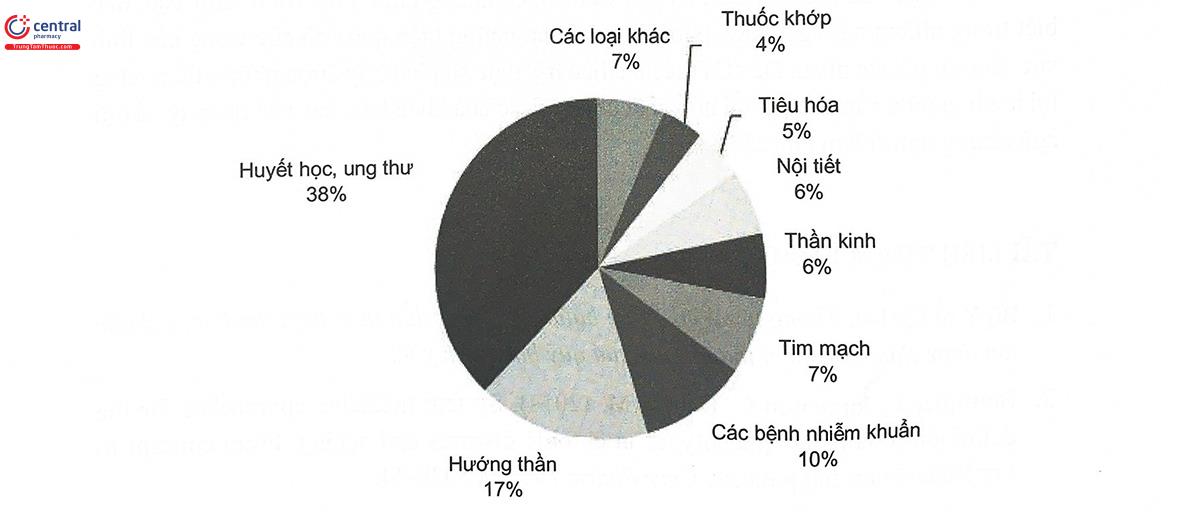
“Dùng thuốc theo cá thể” đã và đang được áp dụng trong nhiều lĩnh vực điều trị khác nhau, bước đầu đem lại những kết quả khả quan, cải thiện đáp ứng điều trị, trong một số trường hợp tạo ra những ý nghĩa lâm sàng đáng kể. Một trong những sự thể hiện rõ nhất của “Dùng thuốc theo cá thể” trong lâm sàng là những thay đổi trên nhãn thuốc và tờ hướng dẫn sử dụng. Cho đến nay, đã có hơn 150 thuốc được lưu hành với thông tin trên nhãn có nội dung liên quan đến marker sinh học và di truyền (ví dụ như: các biến thể gen, các thiếu hụt chức năng, thay đổi biểu hiện gen, các bất thường nhiễm sắc thể..). Trong số đó, một số thuốc trên nhãn có cả thông tin về những điều chỉnh cần thiết dựa trên thông tin di truyền của bệnh nhân. Các thông tin này có thể xuất hiện trên nhãn thuốc ở mục chỉ định hoặc mục thận trọng, cảnh báo... Trong các nhóm điều trị, điều trị ung thư là lĩnh vực phát triển “Cá thể hóa điều trị” mạnh mẽ nhất. Bên cạnh đó, “Dùng thuốc theo cá thể” cũng đang bước đầu được áp dụng trong các lĩnh vực điều trị khác như: Điều trị bệnh về huyết học, nhiễm khuẩn, điều trị rối loạn thần kinh, rối loạn tâm thần, điều trị các bệnh tim mạch, các bệnh phổi, các bệnh di truyền, các bệnh miễn dịch... (Hình 9.4).
Một trong các lĩnh vực đang có những thay đổi mạnh mẽ, tích cực nhờ áp dụng “Cá thể hóa điều trị” là lĩnh vực thử nghiệm lâm sàng trong phát triển thuốc mới. Trước kia, các thử nghiệm lâm sàng thường tiến hành trên một số lượng lớn bệnh nhân với nhóm thử nghiệm, nhóm placebo, kết luận về đáp ứng điều trị được rút ra sau những phân tích thống kê. Trong nhiều trường hợp, sau khi bỏ ra một lượng tiền lớn cùng thời gian dài để thử nghiệm, thuốc không cho kết quả mong muốn và không được lưu hành. Từ thực tế đó, ý tưởng về việc áp dụng “Cá thể hóa điều trị”, phân tầng bệnh nhân trước khi lựa chọn đưa vào thử nghiệm lâm sàng đã được triển khai nhằm mục đích rút ngắn thời gian, giảm số người tham gia thử nghiệm và giảm thiểu chi phí để rút ra kết luận, tăng tỷ lệ thành công của thử nghiệm lâm sàng. Ví dụ như crizotinib, một thuốc chống ung thư theo cơ chế ức chế tạo thành phức hợp ALK-EMLA, vốn chỉ xuất hiện ở 4% bệnh nhân ung thư phổi. Thử nghiệm lâm sàng được tiến hành chỉ trên 82 bệnh nhân ung thư mang đột biến ALK thay vì hàng nghìn bệnh nhân ung thư như những thử nghiệm khác. Tuy nhiên, các kết luận về hiệu quả điều trị của crizotinib được rút ra với ý nghĩa thống kê rất cao. Crizotinib được FDA cấp phép lưu hành chỉ sau 2 năm, trở thành kỷ lục trong phát triển thuốc cho đến nay. Các nhà khoa học thậm chí đã bắt đầu đưa ra khái niệm “Thử lâm sàng đơn bệnh nhân” (single person trial). Kết hợp kết quả của nhiều thử nghiệm lâm sàng đơn bệnh nhân (tiến hành theo cùng một cách) sẽ cho những thông tin về các cách điều trị tối ưu cho một nhóm đối tượng trong quần thể hoặc thậm chí cho cả quần thể.
5 Kết luận
Như vậy, “Cá thể hóa điều trị” đã và đang có những bước phát triển vượt bậc, đặc biệt trong những năm gần đây, bước đầu đem lại những hiệu quả tích cực trong các lĩnh vực lâm sàng khác nhau. Để “Cá thể hóa điều trị” thực sự phát huy được những tiềm năng lợi ích hơn nữa, cần có sự phối hợp chặt chẽ của các nhà khoa học, các nhà quản lý và đội ngũ những người làm lâm sàng.
6 Tài liệu tham khảo
1. Bộ Y tế (2014), Thông tư số 40 - Ban hành và hướng dẫn thực hiện danh mục thuốc tân dược thuộc phạm vi thanh toán của quỹ bảo hiểm y tế.
2. Bousquet J., Jorgensen C. Dauzat M. (2014), System medicine approaches for the definition of complex phenotypes in chronic diseases and ageing. From concept to implementation and policies. Curr Pharm Des 20, 5928-44.
3. FDA (2013), Paving the Way for Personalized Medicine - FDA's Role in a New Era of Medical Product Development.
4. Garassino M. (2013), ESMO Patients Guide Series: ESMO Personalised Medicine, European Society for Medical Oncology EMSO Press.
5. Jain KK. (2015), Textbook of Personalized Medicine, Humana Press.
6. Rodriguez C., Taron M. (2014), Pharmacogenomic biomarkers for personalized cancer treatment, J Intern Med 277, 201-217.
7. Toshihisa Ishikawa (2012), Emerging New Technology to Advance Personalized Medicine, J Pharmacogenomics Pharmacoproteomics 3:e113.

