Xác định công hiệu thành phần ho gà toàn tế bào trong vắc xin phối hợp, hấp phụ
Nếu phát hiện nội dung không chính xác, vui lòng phản hồi thông tin cho chúng tôi tại đây
 Dược sĩ Hoàng Mai Dược sĩ lâm sàng
Dược sĩ Hoàng Mai Dược sĩ lâm sàng
Ước tính: 2 phút đọc, Ngày đăng:
Cập nhật:
Tóm tắt nội dung
Bài viết biên soạn theo Dược Điển Việt Nam V
Do Bộ Y tế ban hành quyết định số 5358/QĐ-BYT ngày 28 tháng 11 năm 2017
Công hiệu của vắc xin ho gà trong vắc xin được xác định bằng cách so sánh liều hữu hiệu 50 % (ED50) của vắc xin mẫu chuẩn so với vắc xin mẫu thử. Kết quả được tính bằng phương pháp Probit analysis (phần mềm WHO program).
1 Pha vắc xin
Sử dụng ít nhất 3 độ pha loãng bậc 5 nhưng không quá 5 độ pha cho cả vắc xin chuẩn và vắc xin thử. Pha vắc xin trong một loại dung dịch đệm sinh lý (dung dịch Natri clorid 0,85 %). Các độ pha vắc xin được chọn dựa vào các số liệu trước đó và tùy thuộc vào chủng loại chuột thí nghiệm, nhưng phải dựa trên nguyên tắc ED50 không được lệch ngoài khoảng giữa độ pha loãng cao nhất và độ pha loãng thấp nhất.
Nếu không có sẵn số liệu trước đó có thể pha 3 độ pha bậc 5 của vắc xin chuẩn và vắc xin thử như ví dụ dưới đây:
1.1 Vắc xin mẫu chuẩn
A = 1/30 = 1 ống mẫu chuẩn + 30 ml NMSL
B = 1/150 = 5 ml A + 20 ml NMSL
C = 1/750 = 5 ml B + 20 ml NMSL
1.2 Vắc xin DTwP mẫu thử
A = 1/5 = 5 ml vắc xin mẫu thử + 20 ml NMSL
B = 1/25 = 5 ml dung dịch A + 20 ml NMSL
C = 1/125 = 5 ml dung dịch B + 20 ml NMSL
2 Tiêm miễn dịch
Chọn chuột nhắt trắng có cân nặng từ 10 g đến 18 g, nhưng các chuột trong một thí nghiệm không được chênh lệch khối lượng quá 4 g. Dùng chuột cùng giới; nếu khác giới phải chia đều số chuột đực, cái vào các nhóm và nhốt riêng. Chuột được tiêm miễn dịch sau khi đã được ăn uống đầy đủ 1 giờ. Tiêm ổ bụng 0,5 ml/chuột. Mỗi độ pha vắc xin tiêm cho một nhóm chuột, số lượng chuột trong mỗi nhóm tùy theo kết quả thẩm định thử nghiệm nhưng không được ít hơn 20 chuột. Tiêm miễn dịch theo thứ tự từ độ pha loãng nhất (từ độ pha C đến A) cho cả loạt vắc xin mẫu thử và mẫu chuẩn.
Bốn nhóm chuột đối chứng: Mỗi nhóm 10 con, được nuôi song song với nhóm chuột miễn dịch dùng để kiểm chứng độc lực của chủng thử thách.
Trong thời gian miễn dịch (14 ngày đến 17 ngày), chuột phải khỏe và tăng trọng bình thường. Ít nhất 94 % số chuột đã được miễn dịch ở mỗi độ pha của cả vắc xin mẫu chuẩn và vắc xin thử nghiệm phải được sống sót và khỏe mạnh cho đến ngày thử thách.
3 Tiêm thử thách
Sau 14 ngày đến 17 ngày miễn dịch, chuột được thử thách với chủng B. pertussis 18323. Chủng thử thách có thể dùng chủng tươi hoặc chủng ở dạng huyền dịch đông băng (10 tỷ vi khuẩn ho gà) được bảo quản trong nitơ lỏng. Chủng thử thách được pha trong dung dịch Casein 1 %. LD50 của chủng thử thách phải nằm trong khoảng 100 đến 1000 vi khuẩn.
3.1 Cách pha dung dịch casein 1 %
Hòa tan 10 g bột casein trong 1000 ml nước cất 2 lần, cho thêm 2,3 g natri clorid. Điều chỉnh đến pH 7 - 7,2 bằng dung dịch natri hydroxyd hoặc acid hydrocloric loãng. Hấp 121 °C trong 30 phút.
Dung dịch casein 1 % phải được kiểm tra an toàn bằng cách tiêm vào não cho 5 chuột nhắt, mỗi con 0,02 ml. Theo dõi 3 ngày, toàn bộ chuột thí nghiệm phải sống. Nếu có 1 chuột chết phải pha lại dung dịch.
3.2 Cách pha hỗn dịch vi khuẩn để kiểm tra liều LD50 và để thử thách
Chủng B. pertussis 18323 được cấy truyền đời 2 hoặc đời 3 trên môi trường Bordet - Gengou có chứa 15 % máu cừu hoặc ngựa. Huyền dịch vi khuẩn ho gà gặt từ nuôi cấy 20 giờ đến 22 giờ được dùng để pha thành hỗn dịch thử thách hoặc sử dụng huyền dịch vi khuẩn ho gà đậm độ 10 tỷ vi khuẩn/ml đã bảo quản trong nitrogen lỏng để pha dung dịch thử thách.
Trong khi pha cũng như trong khi tiêm thử thách, hỗn dịch vi khuẩn ho gà phải giữ trong đá lạnh. Thời gian từ bắt đầu pha đến khi tiêm xong hỗn dịch vi khuẩn thử thách không được quá 150 phút. Xác định đậm độ vi khuẩn ho gà bằng mắt thường khi so với ống độ đục chuẩn quốc tế 10¹⁰ hoặc đo OD bằng máy quang phổ kế để tính số vi khuẩn ho gà trong hỗn dịch gặt. Pha loãng huyền dịch vi khuẩn ho gà bằng casein 1 % để có nồng độ là 10 x 10⁶ vi khuẩn/ml (*). Nếu sử dụng chủng ho gà được bảo quản trong nitơ lỏng thì phải làm tan băng nhanh trước khi thử thách. Các độ pha loãng của chủng ho gà được pha theo sơ đồ dưới đây (Ví dụ 1) trong dung dịch casein 1 %.
Ví dụ 1: Sơ đồ các độ pha loãng của chủng ho gà trong dung dịch casein 1 %
Chủng B. pertussis 18323 giữ trong nitrogen lỏng là 10 x 10⁹/ml (*) = A0
A1 = 1/2 = 5 x 109/ml = 1 ml A0 + 1 ml đệm casein 1 %
A2 = 1/4 = 5 x 109/2ml = 1 ml A1 + 1 ml đệm casein 1 %
A3 = 1/40 = 5 x 10⁶/0,02ml = 1 ml A2 + 9 ml đệm casein 1 %
A4 = 1/400 = 5 x 103/0,02ml = 1 ml A3 + 9 ml đệm casein 1 %
A5 = 1/2000 = 100 000/0,02ml = 3 ml A4 + 12 ml đệm casein 1 %
A6 = 1/20000 = 10 000/0,02ml = 1 ml A5 + 9 ml đệm casein 1 %
A7 = 1/100000 = 2000/0,02ml = 1 ml A6 + 4 ml đệm casein 1 %
A8 = 1/500000 = 400/0,02ml = 1 ml A7 + 4 ml đệm casein 1 %
A9 = 1/2500000 = 80/0,02ml = 1 ml A8 + 4 ml đệm casein 1 %
4 Tiêm chuột
Sau 14 đến 17 ngày, toàn bộ chuột đã miễn dịch bởi vắc xin mẫu chuẩn và mẫu thử được tiêm thử thách vào não, mỗi con nhận 0,02 ml hỗn dịch chứa 100 000 vi khuẩn (độ pha A5) bằng một bơm tiêm bán tự động Hamilton.
Nhóm chuột đối chứng, mỗi nhóm 10 con, được tiêm với các độ pha từ A6 đến A9, tương ứng với hỗn dịch chứa 10 000 vi khuẩn, 2000 vi khuẩn, 400 vi khuẩn và 80 vi khuẩn.
Độ pha hỗn dịch chứa 80 vi khuẩn sẽ được cấy ít nhất trên 2 đĩa thạch Bordet - Gengou sau khi pha xong hỗn dịch và sau khi kết thúc tiêm thử thách, ủ đĩa thạch ở 35°C trong 3 đến 4 ngày, sau đó đếm số khuẩn lạc mọc. Thông thường, số khuẩn lạc đạt khoảng 30 %.
Lưu ý:
Trong quá trình pha và tiêm thử thách, dung dịch chủng phải luôn giữ trong đá lạnh.
Thời gian tính từ khi bắt đầu pha chủng đến khi kết thúc thử nghiệm không được quá 2,5 giờ.
Tất cả vật liệu chứa chủng ho gà đều phải tiệt trùng bằng nồi hấp 121°C trong 15 đến 20 phút hoặc luộc sôi trong 30 phút trước khi rửa dụng cụ.
Những chuột chết trong 3 ngày đầu sau tiêm thử thách được coi là chuột chết không mang tính đặc hiệu của ho gà. Do đó, chỉ những chuột chết từ ngày thứ 4 đến ngày thứ 14 mới được tính kết quả.
Ngày thứ 14 sau thử thách: Tất cả những chuột chết hoặc có dấu hiệu liệt rõ và sưng phồng tấy đỏ đều được tính là chuột chết.
5 Tính kết quả
Dựa vào số chuột sống sót trong mỗi nhóm chứng, dùng phương pháp Reed-Muench để tính LD50 của chủng thử thách. Xem ví dụ 2.
Ví dụ 2:
| Số vi khuẩn | Số Chuột | Số sống | Số chết | Số tích luỹ Sống Chết | Tổng số | %Chết | |
| 10 000 | 10 | 1 | 9 | 1 | 22 | 23 | 95 |
| 2 000 (B) | 10 | 3 | 7 | 4 | 13 | 17 | 76(b) |
| 400 (A) | 10 | 6 | 4 | 10 | 6 | 16 | 37(a) |
| 80 | 10 | 8 | 2 | 18 | 2 | 20 | 10 |
Theo ví dụ trên, LD₅₀ nằm trong khoảng giữa 2 liều 2000 và 400 vi khuẩn. Tỷ lệ % chuột chết tương ứng với liều sát trên 50% là 76%, và tỷ lệ % chuột chết tương ứng với liều sát dưới 50% là 37%.
Tính LD₅₀ bằng công thức sau:
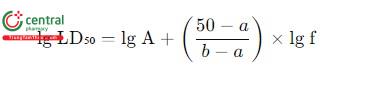
Trong đó:
A là liều gây chết vừa sát dưới 50% (trong ví dụ trên là 400),
a là % chết tương ứng với A (trong ví dụ trên là 37%),
B là liều gây chết vừa sát trên 50% (trong ví dụ trên là 2000),
b là % chết tương ứng với B (trong ví dụ trên là 76%),
f là hệ số pha loãng (trong thử nghiệm này là pha loãng bậc 5).
Thay bằng con số cụ thể:
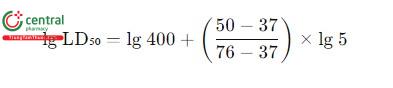
Kết quả: LD₅₀ ≈ 680 vi khuẩn.
Dùng phần mềm Probit analysis của WHO để tính công hiệu của vắc xin ho gà.
Thử nghiệm được coi là có giá trị khi:
ED₅₀ của vắc xin chuẩn và ED₅₀ của vắc xin thử nghiệm nằm giữa độ pha loãng nhất và độ pha đặc nhất của các vắc xin đó.
Trong suốt thời gian miễn dịch cho đến ngày thử thách, số chuột trong mỗi độ pha không được chết quá 6%.
Liều thử thách phải chứa 100 đến 1000 LD₅₀, như vậy liều LD₅₀ phải chứa 100 đến 1000 vi khuẩn.
Thử nghiệm phải đạt được tiêu chuẩn của chương trình Probit Analysis, thể hiện sự tương quan giữa liều miễn dịch và đáp ứng trên chuột (tính tuyến tính), và tương quan giữa vắc xin chuẩn và vắc xin thử (tính song song).
6 Tiêu chuẩn chấp thuận
Vắc xin đạt yêu cầu nếu công hiệu không ít hơn 4 IU trong một liều đơn vắc xin cho người và giới hạn dưới của 95% khoảng tin cậy của công hiệu tìm được không ít hơn 2 IU trong một liều đơn vắc xin cho người.
Nếu thử nghiệm lần 1 có giá trị (valid) và đạt tiêu chuẩn chấp thuận thì vắc xin đó coi như đạt yêu cầu về công hiệu. Nhưng nếu không đạt tiêu chuẩn chấp thuận, thì thử nghiệm đó phải được làm lại.
Công hiệu vắc xin đạt tiêu chuẩn chấp thuận khi kết quả trung bình nhân của các lần thử nghiệm có giá trị không thấp hơn tiêu chuẩn chấp thuận cho phép.
Nếu lần 1 không đạt yêu cầu và thử nghiệm không có giá trị (invalid), thì phải làm lại thử nghiệm. Kết quả lần thử nghiệm đầu sẽ không được dùng để xem xét. Nếu kết quả lần thử nghiệm nhắc lại có giá trị và đạt tiêu chuẩn chấp thuận, thì loạt vắc xin đó coi như đạt yêu cầu về công hiệu. Nếu không đạt yêu cầu, thì phải làm lại như trên.

