Các Kỹ Thuật Tách Sắc Ký
Nếu phát hiện nội dung không chính xác, vui lòng phản hồi thông tin cho chúng tôi tại đây
 Dược sĩ Thùy Dung Dược sĩ lâm sàng
Dược sĩ Thùy Dung Dược sĩ lâm sàng
Ước tính: 30 phút đọc, Ngày đăng:
Cập nhật:
Tóm tắt nội dung
- Các kỹ thuật tách sắc ký
- Định nghĩa
- Sắc ký đồ
- Thời gian lưu (tR)
- Pic
- Thể tích lưu (VR)
- Thời gian chết (tM) (hold-up time)
- Thể tích chết (VM) (hold-up volume)
- Hệ số phân bố khối lượng
- Thời gian toàn bộ của pha động (tt)
- Thể tích toàn bộ của pha động (Vt)
- Thời gian lưu của chất không bị lưu giữ (t0)
- Thể tích lưu của chất không bị lưu giữ (V0)
- Hằng số phân bố (K0)
- Thừa số chậm (RF)
- Số đĩa lý thuyết (N)
- Thể tích lưu trú (D) (Dwell volume)
- Hệ số đối xứng (As)
- Độ phân giải (RS)
- Tỷ số đỉnh - hõm (p/v)
- Độ lưu giữ tỷ đối (r)
- Tỷ số tín hiệu trên nhiễu (S/N)
- Độ lặp lại
- Phương pháp sắc ký giấy
- Phương pháp sắc ký khí
- Phương pháp sắc ký lỏng
- Sắc ký lớp mỏng
- Phương pháp sắc ký rây phân tử
- Thiết bị
- Hiệu năng
- Xác định tỷ lệ thành phần tương đối
- Xác định khối lượng phân tử
- Sự phân bố polymer theo kích thước phân tử
- Phân bố khối lượng phân tử trong dextran
- Chuẩn hóa hệ thống sắc ký
- Tính phù hợp của hệ thống
- Khối lượng phân tử trung bình của chất đối chiếu hóa học dextran dùng cho thử hiệu năng
- Khối lượng phân tử trung bình của dextran phân đoạn cao 10%
- Khối lượng phân tử trung bình của dextran phân đoạn thấp 10%
- Sự phân bố khối lượng phân tử của dextran được phân tích
- Phương pháp điện di
- Ảnh hưởng của điện tích, kích thước tiểu phân, độ nhớt của chất điện giải và biến thiên điện thể
- Ảnh hưởng của pH
- Ảnh hưởng của lực ion và nhiệt độ
- Ảnh hưởng của môi trường nền, dòng điện thẩm
- Sự rây phân tử
- Điện di gel
- Thiết bị cho điện di gel
- Điện di đĩa
- Cơ sở của điện di đĩa
- Linh độ tương đối
- Quan sát các vùng phân tách
- Những điều an toàn cần chú ý
- Phương pháp điện di mao quản
- Nguyên lý của điện di mao quản vùng
- Nguyên lý của sắc ký mixen điện động
- Các điều chú ý đối với thiết bị
- Các loại mao quản và cấu hình thiết bị
- Kỹ thuật đưa mẫu và tiêm mẫu
- Cung cấp nguồn điện
- Các kiểu detector
- Những điểm cần chú ý khi phân tích mẫu
- Kích thước mao quản
- Ảnh hưởng điện thế
- Ảnh hưởng của lực ion
- Các thông số vận hành
- Thiết lập hệ thống
- Quy trình rửa mao quản
- Tiến hành phân tích mẫu
- Tính phù hợp của hệ thống
- Phân tích mẫu
- Xử lý dữ liệu
- Tắt hệ thống
Bài viết biên soạn theo Dược Điển Việt Nam V
Do Bộ Y tế ban hành quyết định số 5358/QĐ-BYT ngày 28 tháng 11 năm 2017
1 Các kỹ thuật tách sắc ký
Các kỹ thuật tách sắc ký là những phương pháp tách trong đó các thành phần của mẫu được phân bố vào hai pha: một pha tĩnh và một pha động. Pha tĩnh có thể là một chất rắn, cũng có thể là một chất lỏng được giữ trên một chất rắn hay một gel. Pha tĩnh có thể được nhồi vào cột, hoặc trải thành một lớp, hay phân tán thành một lớp phim v.v... Pha động có thể là chất khí, chất lỏng hay chất lưu siêu tới hạn (còn được gọi là chất lỏng siêu tới hạn). Sự tách sắc ký có thể dựa trên các cơ chế khác nhau như hấp phụ, phân bố khối lượng (hay phân chia), trao đổi ion, hoặc dựa trên sự khác nhau về tính chất lý hóa của các phân từ như kích thước, khối lượng, thể tích v.v...
Phụ lục này chỉ đề cập đến các định nghĩa và phép tính các thông số thông thường trong kỹ thuật sắc ký, các yêu cầu thường được áp dụng cho sự phù hợp của hệ thống sắc ký. Nguyên lý, thiết bị và phương pháp tách được trình bày trong các phép thử chung sau đây:
Phương pháp sắc ký giấy (Phụ lục 5.1)
Phương pháp sắc ký khí (Phụ lục 5.2)
Phương pháp sắc ký lỏng (Phụ lục 5.3)
Phương pháp sắc ký lớp mỏng (Phụ lục 5.4)
Phương pháp sắc ký rây phân tử (Phụ lục 5.5)
1.1 Định nghĩa
Các định nghĩa sau đây được dùng trong các chuyên luận để tính toàn các thông số về tỉnh phù hợp của hệ thống và các tiêu chuẩn chấp nhận. Một số thiết bị có phần mềm của nhà sản xuất dùng để tính toán một vài thông số như tỷ số tín hiệu trên nhiều và độ phân giải có thể được sử dụng. Trong trường hợp này, người sử dụng có trách nhiệm đảm bảo rằng các phương pháp dùng trong phần mềm đó phù hợp với yêu cầu của hộ tiêu chuẩn này; nếu không, phải điều chỉnh cho phù hợp.
1.2 Sắc ký đồ
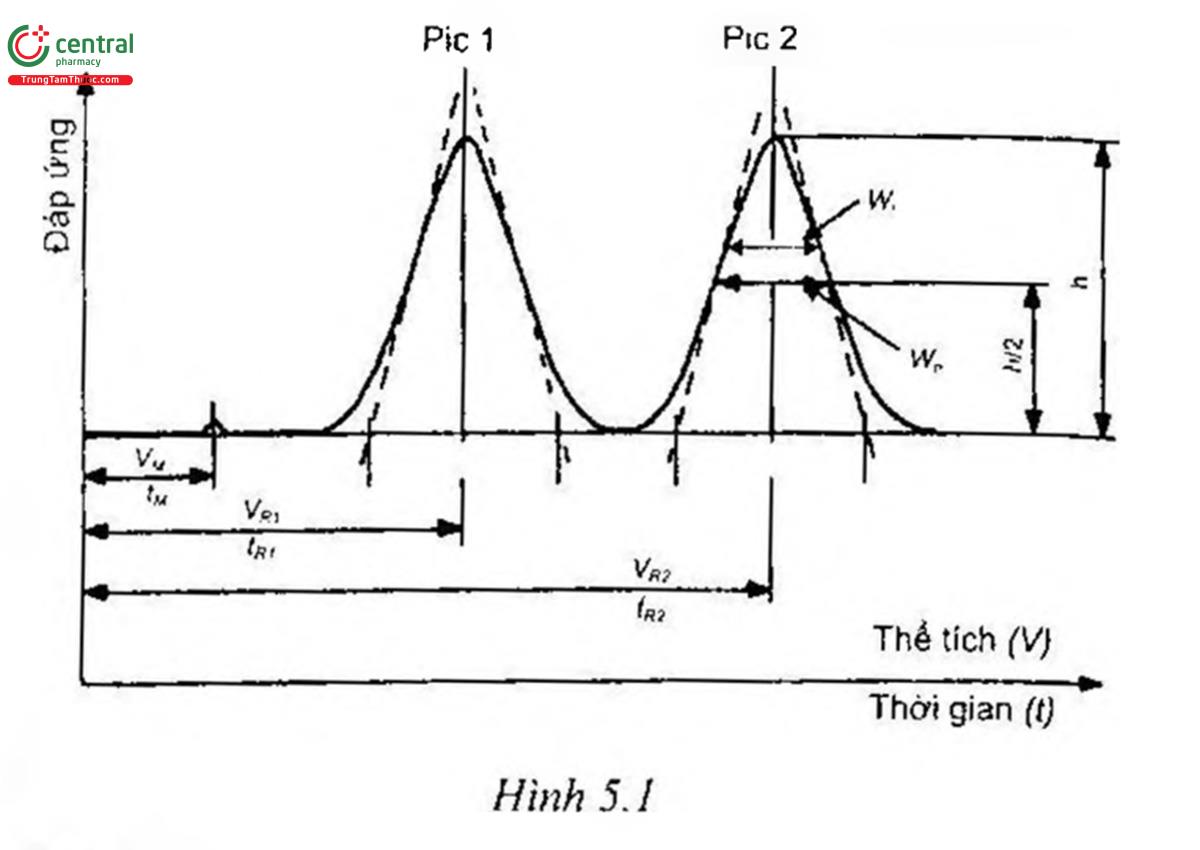
Sắc ký đồ là một đồ thị hay một cách trình bày khác mô tả sự thay đổi đáp ứng của detector (hay nồng độ của chất hay một đại lượng khác làm thước đo nồng độ của chất) theo thời gian, thể tích hay khoảng cách. Một sắc ký đồ lý tưởng có dạng một chuỗi các pic kiểu Gauss trên một đường nền (Hinh 5.1).
1.3 Thời gian lưu (tR)
Là thời gian cần thiết để rửa giải một chất (Hình 5.1, đường nền biểu thị bằng phút).
1.4 Pic
Pic, hay còn gọi là đỉnh, là phần sắc ký đồ ghi lại đáp ứng của detector khi một chất (hoặc 2 hay nhiều chất không tách ra khoi nhau) được rửa giải khỏi cột.
Pic có thể được xác định bằng diện tích pic, hoặc chiều cao pic (h) và chiều rộng pic ở nửa chiều cao (wi), hoặc chiều cao pic (h) và chiều rộng pic giữa các điểm uốn (wh). Ở các pic có dạng hình Gauss (Hình 5.1), có mối quan hệ biểu thị bằng phương trình sau:
wh = 1,18 x wi
1.5 Thể tích lưu (VR)
Là thể tích pha động cần thiết để rửa giải một chất. Thể tích lưu có thể tính được từ thời gian lưu và tốc độ dòng (ml/min) theo công thức:
VR = IR X F
Trong đó:
F là lưu lượng dòng (hay tốc độ dòng) của pha động (ml/min).
1.6 Thời gian chết (tM) (hold-up time)
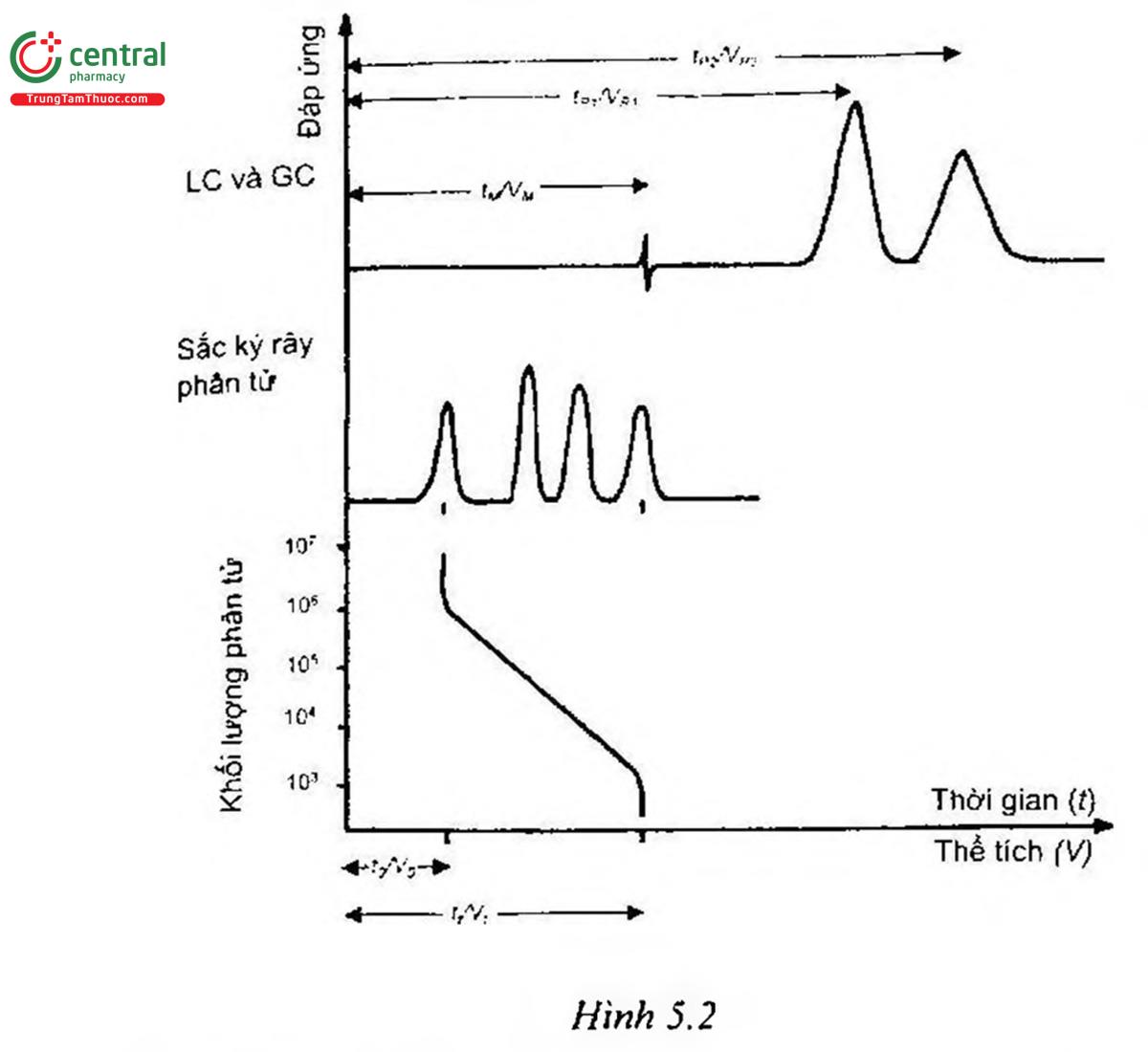
Là thời gian cần thiết để rửa giải một chất không bị lưu giữ (Hình 5.1, đường nền biểu thị bằng phút). Trong phương pháp Sắc ký rây phân từ (xem Hình 5.2), thời gian chết được ký hiệu là to
1.7 Thể tích chết (VM) (hold-up volume)
Là thể tích pha động cần thiết để rửa giải một chất không bị lưu giữ. Nó có thể được tính từ thời gian chết (t) và tốc độ dòng F (số ml pha động trong 1 min) theo công thức sau:
VM = tM x F
Trong phương pháp Sắc ký rây phân từ (xem Hình 5.2), thể tích chết được ký hiệu là Vo.
1.8 Hệ số phân bố khối lượng
Hệ số phân bố khối lượng (Dm) hay còn gọi là thừa số dung lượng (k'), hoặc thừa số lưu giữ (k), được định nghĩa và tính theo công thức sau:
Dm = k’ = k = mS /mM = Kc x VS/VM
Trong đó:
Kc là hãng số phân bố hay còn gọi là hệ số phân bố cân bằng;
VS là thể tích pha tĩnh;
VM là thể tích pha động;
mS là lượng chất trong pha tĩnh; mM là lượng chất trong pha động.
Thừa số lưu giữ k của một chất có thể được xác định trên sắc ký đồ theo công thức:
k= (tR - tM) x tM
1.9 Thời gian toàn bộ của pha động (tt)
Trong phương pháp Sắc ký rây phân tử, thời gian toàn bộ của pha động là thời gian lưu của một chất mà kích thước phân tử nhỏ hơn kích thước các lỗ nhỏ nhất của gel (Hình 5.2).
1.10 Thể tích toàn bộ của pha động (Vt)
Trong phương pháp Sắc ký rây phân tử, thể tích toàn bộ của pha động là thể tích lưu của một chất mà kích thước phân tử nhỏ hơn kích thước các lỗ nhỏ nhất của gel. Nó có thể được tỉnh từ thời gian toàn bộ của pha động (1) và tốc độ dòng F (mlmin) theo công thức sau:
Vt = tt × F
1.11 Thời gian lưu của chất không bị lưu giữ (t0)
Trong phương pháp Sắc ký rây phân tử, thời gian lưu của chất không bị lưu giữ là thời gian lưu của một chất mà kích thước phân từ lớn hơn kích thước các lỗ lớn nhất của gel (Hình 5.2).
1.12 Thể tích lưu của chất không bị lưu giữ (V0)
Trong phương pháp Sắc ký rây phân tử, thể tích lưu của chất không bị lưu giữ là thể tích lưu của một chất mà kích thước phân từ lớn hơn kích thước các lễ lớn nhất của gel. Có thể tính thể tích lưu của chất không bị lưu giữ từ thời gian lưu của chất không bị lưu giữ (to) và tốc độ dòng F (ml/min) theo công thức sau:
V=t0x F
1.13 Hằng số phân bố (K0)
Trong phương pháp Sắc ký rây phân tử, đặc tính rửa giải của một chất có thể được biểu thị dưới dạng hằng số phân bố (còn gọi là hệ số phân bố) K0 và được tính theo công thức:
.png)
1.14 Thừa số chậm (RF)
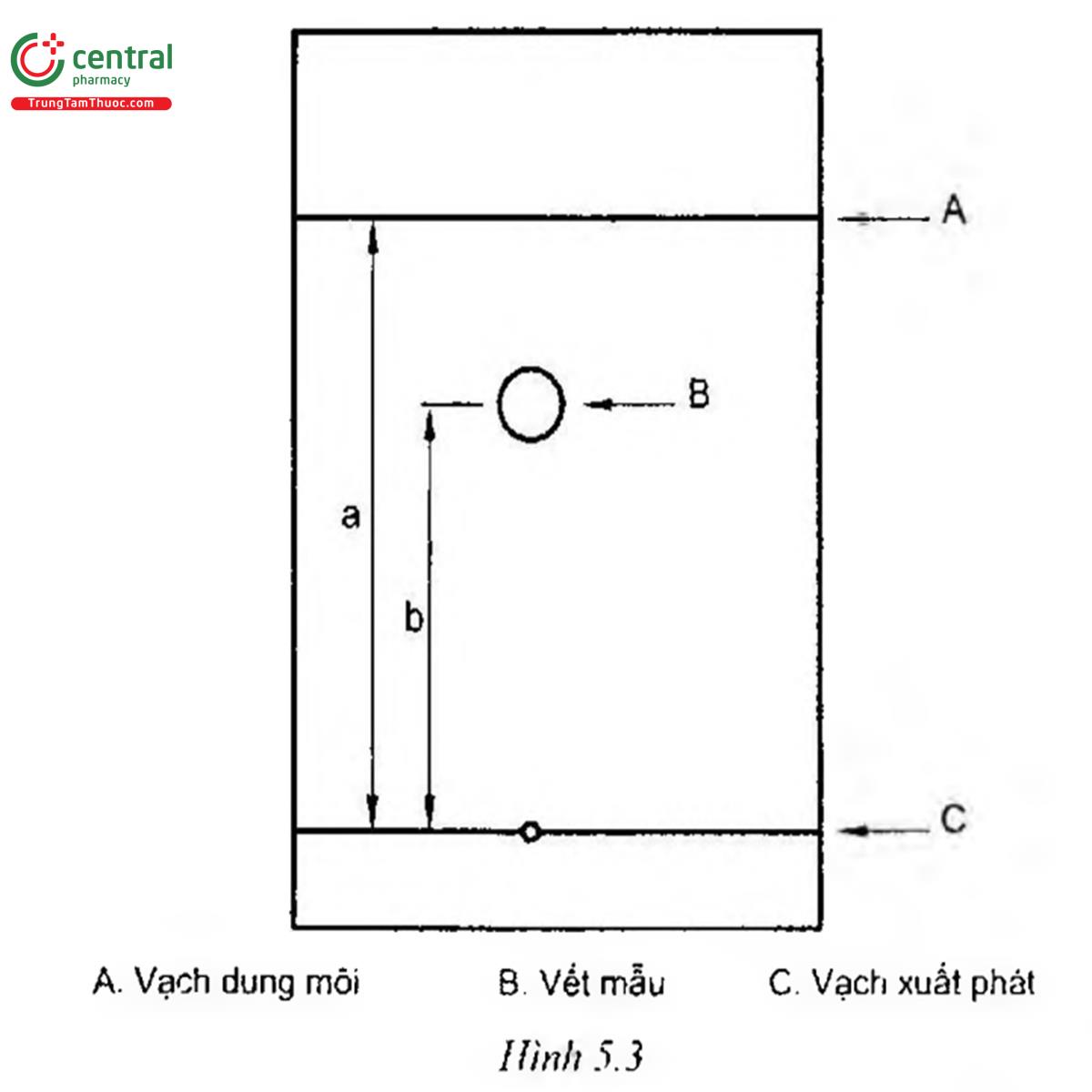
Thừa số chậm RF, hay còn gọi là hệ số di chuyển Rf, được dùng trong sắc ký trên mặt phẳng (sắc ký lớp mỏng, sắc ký giấy) là tỷ số giữa khoảng cách từ điểm chấm mẫu đến tâm của vết sắc ký và khoảng cách di chuyển của dung môi tính từ điểm chấm mẫu (Hình 5.3).
.png)
Trong đó:
b là quãng đường di chuyển của chất phân tích;
a là quãng đường di chuyển của tuyến dung môi.
1.15 Số đĩa lý thuyết (N)
Tùy thuộc vào kỹ thuật sử dụng, hiệu năng của cột (hay hiệu lực biểu kiến của cột) biểu thị dưới dạng số đĩa lý thuyết. có thể tính được từ những dữ liệu thu được dưới điều kiện đằng nhiệt, đăng dòng hoặc đăng mật độ (isodense), theo công thức sau, trong đó các giá trị tR và wh có cùng đơn vị đo:
.png)
Trong đó:
tR là thời gian lưu của pic tương ứng với chất phân tích;
wh là chiều rộng pic ở nửa chiều cao pic.
Số đĩa lý thuyết thay đổi theo chất, theo cột, nhiệt độ cột, pha động và thời gian lưu.
1.16 Thể tích lưu trú (D) (Dwell volume)
Thể tích lưu trú (còn gọi là thể tích trễ gradient) là thể tích giữa điểm mà các chất rửa giải của pha động gặp nhau và đình của cột. Nó có thể được xác định bằng cách sau:
Cột: Thay cột sắc ký bằng một ống mao quản thích hợp (ví dụ ống 1 m × 0,12 mm).
Pha động: Pha động A: Nước cất;
Pha động B: Dung dịch aceton 0,1% (tt/tt).
Thời gian (min) | Pha động A (% tt/tt) | Pha động B (% tt/tt |
0-20 | 100 ⮕ 0 | 0 ⮕ 100 |
20-30 | 0 | 100 |
Tốc độ dòng: Đặt tốc độ đòng sao cho có áp suất ngược thích hợp (back-pressure) (ví dụ 2 ml/min).
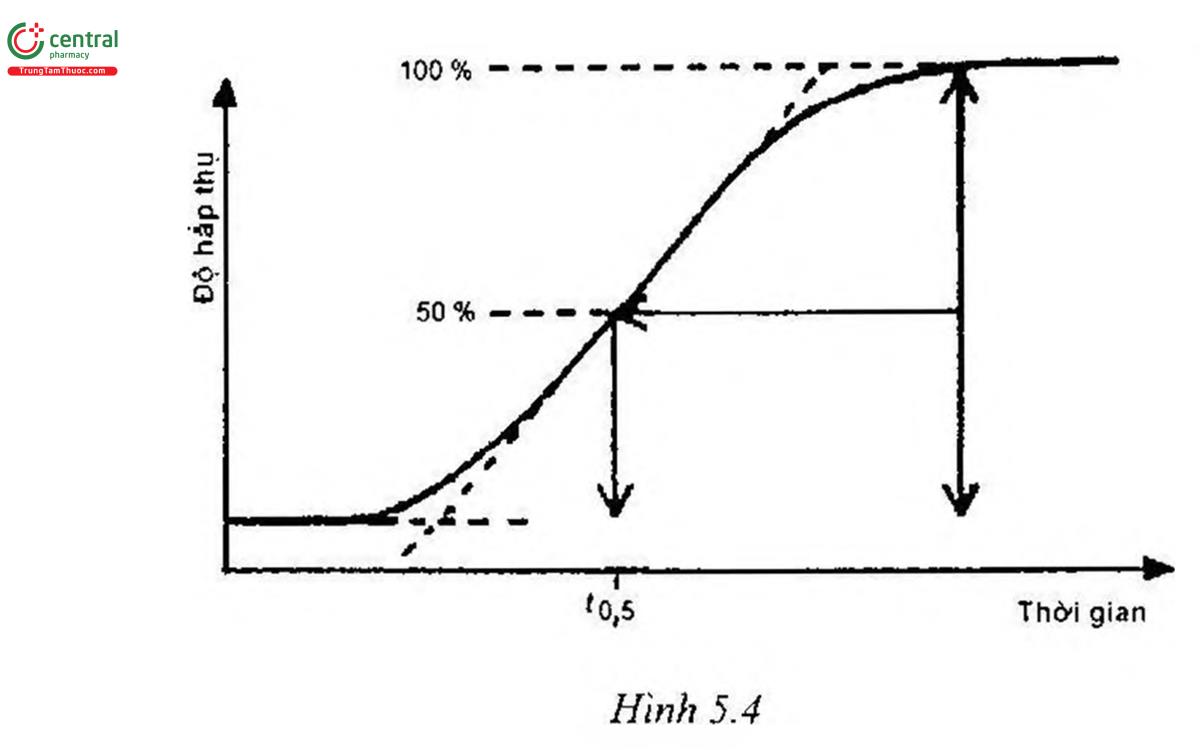
Phát hiện: Quang phổ tử ngoại đặt ở bước sóng ở 265 nm. Xác định thời điểm (105) tính bằng phút khi độ hấp thụ tăng lên đạt 50% (Hình 5.4).
D = tD x F
Trong đó:
tD = t0,5 0,5tG (tính bằng phút);
tG là thời gian gradient đã xác định trước (= 20 min);
F là tốc độ dòng (tính bằng ml/min).
1.17 Hệ số đối xứng (As)
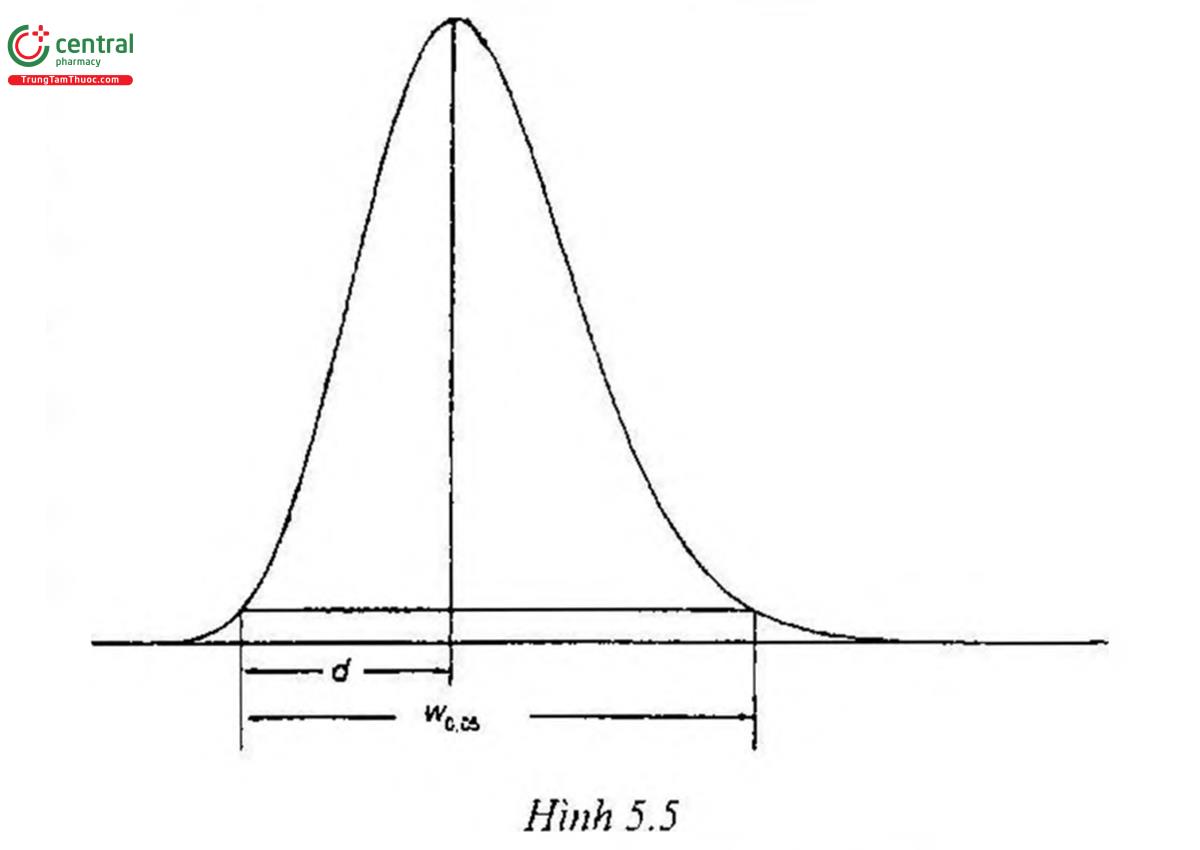
Hệ số đối xứng của một pic (Hình 5.5) được tính theo công thức sau:
.png)
Trong đó:
w0,05 là chiều rộng của pic ở 1/20 chiều cao của pic;
d là khoảng cách tính từ đường thẳng đứng đi qua đỉnh pic đến cạnh phía trước của pic ở 1/20 chiều cao của pic. Khi AS = 1,0 thì pic hoàn toàn đối xứng.
Khi AS > 1,0 thì pic bị kéo đuôi. Khi AS < 1,0 thì pic bị doãng về phía trước.
1.18 Độ phân giải (RS)
Độ phân giải (RS) giữa hai pic của hai chất (Hình 5.5) được tính theo công thức sau:
.png)
Trong đó:
tR2 > tR1
tR1 tR2 là thời gian lưu của các pic tương ứng;
Wh1, Wh2 là chiều rộng pic ở nửa chiều cao pic.
Trong phương pháp định lượng bằng sắc ký trên mặt phẳng dùng phép đo mật độ, khoảng cách di chuyển được dùng thay cho thời gian lưu và độ phân giải giữa các pic của 2 chất có thể được tính theo công thức sau:
.png)
Trong đó:
RF1, RF2 là thừa số chậm của các pic tương ứng;
Wh1 wh2 là chiều rộng pic ở nữa chiều cao pic;
a là khoảng cách di chuyển của tuyến dung môi.
1.19 Tỷ số đỉnh - hõm (p/v)
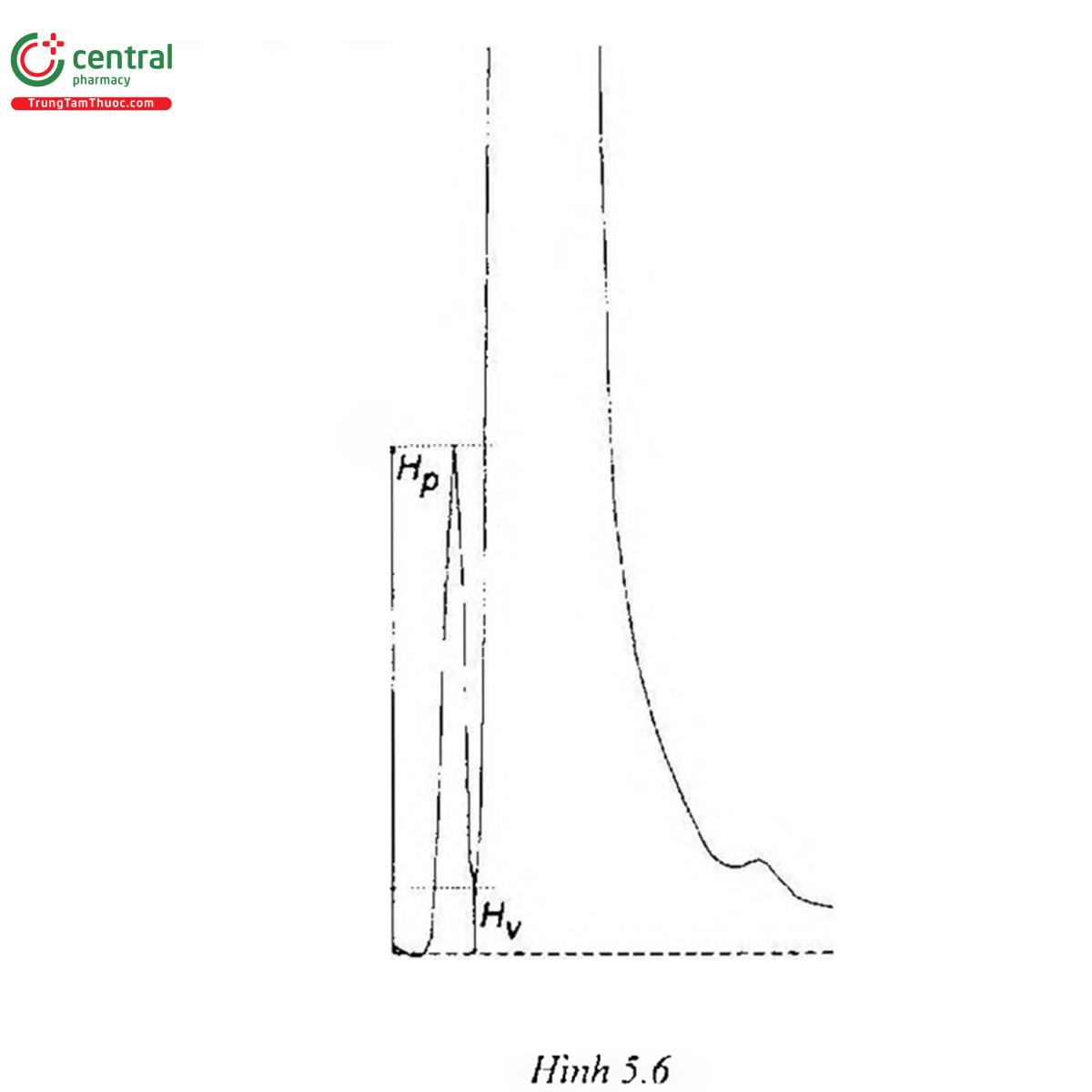
Tỷ số đình - hõm (p/v) có thể được dùng như một thông số về tính phù hợp của hệ thống trong phép thử các tạp chất liên quan khi hai pic không được tách đến đường nền (Hình 5.6).
.png)
Trong đó: Hp là chiều cao của đỉnh pic nhỏ so với đường nên ngoại suy,
Hv là chiều cao của đáy hồm tách hai pic lớn và nhỏ so với đường nên ngoại suy.
1.20 Độ lưu giữ tỷ đối (r)
Độ lưu giữ tỷ đối (r) có thể ước lượng theo công thức sau:
.png)
Trong đó:
tri là thời gian lưu của pic chất được quan tâm;
TRst là thời gian lưu của pic chất đối chiếu (thường là pic tương ứng với chất cần thử);
tM là thời gian chết.
Độ lưu giữ tỷ đối chưa hiệu chỉnh (r) được tính theo công thức:
.png)
Trừ khi có hướng dẫn khác, các giá trị độ lưu giữ tỷ đối cho trong các chuyên luận là độ lưu giữ tỷ đổi chưa hiệu chỉnh. Trong sắc ký trên mặt phẳng, các thừa số chậm RFst và RFi được dùng thay cho các thời gian lưu tRst và tRi
1.21 Tỷ số tín hiệu trên nhiễu (S/N)
Nhiễu có ảnh hưởng đến độ chụm của phép định lượng. Tỷ số tín hiệu trên nhiều được tính theo công thức:
.png)
Trong đó:
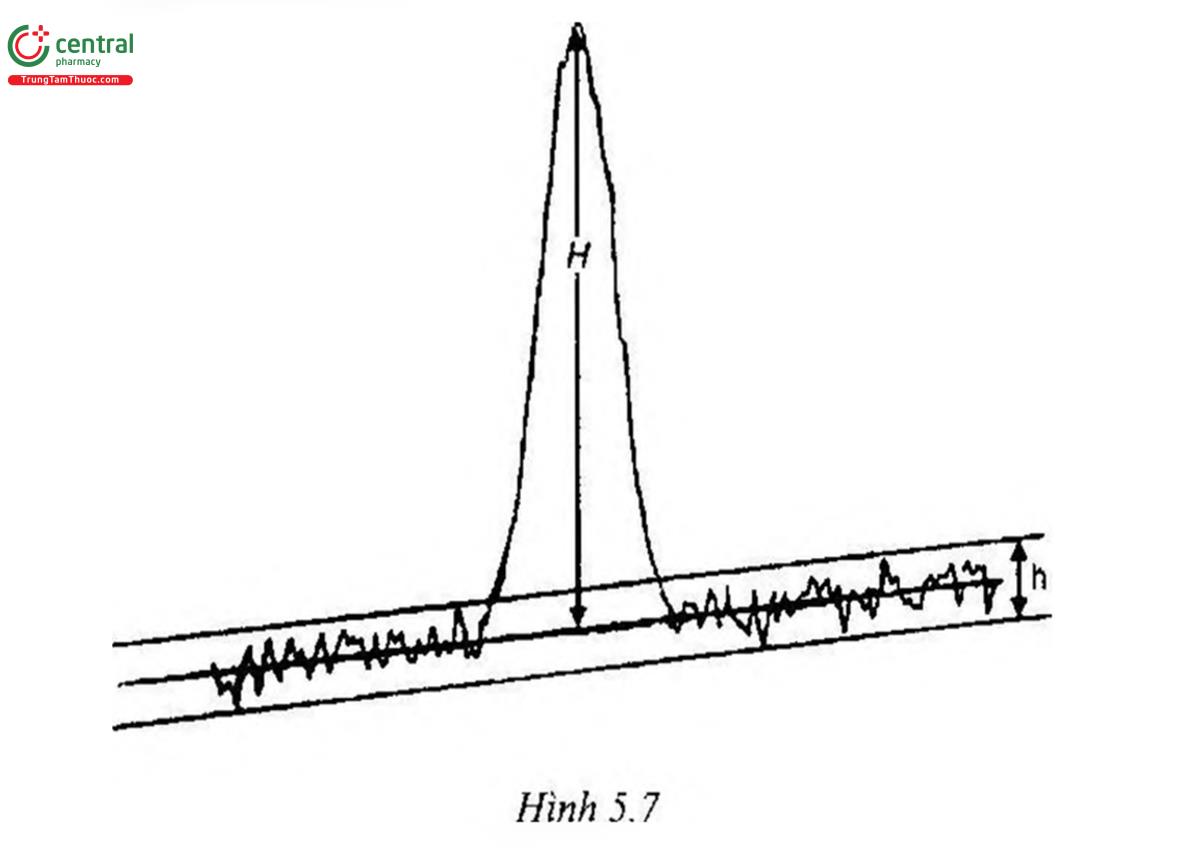
H là chiều cao pic (Hình 5.7) tương ứng với chất được khảo sát trên sắc đồ thu được với dung dịch chất đối chiếu đã định; chiều cao này đo từ đình pic đến đường nên ngoại suy được xác định trên một khoảng bằng ít nhất 5 lần chiều rộng của pic ở nửa chiều cao pic;
h là khoảng dao động của nhiều đường nền trên sắc đồ thu được sau khi tiêm một mẫu trắng: khoảng dao động này được xác định trên một quãng đường bằng ít nhất 5 lần chiều rộng của pic ở nửa chiều cao pic trên sắc đồ thu được khi tiêm dung dịch chất đối chiếu đã định và nếu có thể thì quãng đường này phân bố đều hai bên vị trí của pic của chất khảo sát.
2 Độ lặp lại
Độ lập lại của đáp ứng được biểu thị dưới dạng phần trăm độ lệch chuẩn tương đối (RSD %) của một dãy kết quả của ít nhất 3 lần tiêm hoặc nạp liên tiếp dung dịch chất đối chiều và được tính theo công thức:
.png)
Trong đó:
yi là các giá trị cá thể dưới dạng diện tích pic, hay chiều cao pic, hoặc tỷ số các diện tích trong phương pháp nội chuẩn;
y- là trung bình của các giá trị cá thể;
n là số các giá trị cá thể.
2.1 Tính phù hợp của hệ thống
Các bộ phận khác nhau của thiết bị sắc ký cần phải được kiểm tra hiệu chỉnh để có thể đạt được hiệu năng theo yêu cầu khi tiến hành phép thử hay định lượng.
Các phép thử tính phù hợp của hệ thống là phần không thể thiếu của một phương pháp và được dùng để đảm bảo hệ thống sắc ký có hiệu năng phù hợp. Hiệu lực biểu kiến, thừa số lưu giữ (hệ số phân bổ khối lượng), độ phân giải, độ lưu giữ tỷ đối và hệ số đối xứng là những thông số thường được dùng để đánh giá hiệu năng của cột. Các yếu tố có thể ảnh hưởng đến đặc tính sắc ký bao gồm: Thành phần, nồng độ ion, nhiệt độ và pH biểu kiến của pha động:
Tốc độ dòng, kích thước cột, nhiệt độ cột và áp suất; Các đặc tính của pha tĩnh bao gồm loại chất mang, dộ xốp (cỡ lỗ), cỡ hạt, kiểu các hạt, diện tích bề mặt riêng, Pha đào và các pha tĩnh có biển đối bề mặt khác như biên đôi hoá học (được biêu thị bởi end-capping, carbon loading v.v...].
Các yêu cầu sau đây và các yêu cầu bổ sung trong chuyên luận cụ thể phải được đáp ứng, trừ khi có chỉ dẫn khác: Trong phép thử các tạp chất liên quan hay định lượng, hệ số đối xứng của pic chính trên sắc ký đồ thu được từ dung dịch đối chiếu phải trong khoảng từ 0,8 đến 1,5, trừ khi có chỉ dẫn khác;
Trong phép định lượng hoạt chất mà giá trị xác định là 100% chất tinh khiết, độ lệch chuẩn tối đa được phép [RSD(%)max] cho các lần tiêm lập lại của dung dịch đối chiếu dược tính theo công thức sau:
.png)
Trong đó:
K là một hằng số (-0,349) thu được từ biểu thức
.png)
mà ![]() biểu thị độ lệch chuẩn tương đối yêu cầu cho 6 lần tiêm với B = 1,0.
biểu thị độ lệch chuẩn tương đối yêu cầu cho 6 lần tiêm với B = 1,0.
B là giới hạn trên được cho trong chuyên luận riêng trừ đi 100%;
n là số lần tiêm lặp lại dung dịch đổi chiều (3 ≤ n ≤ 6);
t190%, n-1 là giá trị t-Student ở mức xác xuất 90% (hai phía) với bậc tự do n - 1.
Nếu không có chỉ dẫn gì khác, độ lệch chuẩn tương đối được phép tối đa không được vượt quá giá trị tương ứng ghi trong Bảng 5.1. Yêu cầu này không áp dụng cho phép thử các tạp chất liên quan.
Bảng 5.1 - Yêu cầu về độ lặp lại
Số lần tiêm lặp lại | ||||
3 | 4 | 5 | 6 | |
B (%) | Độ lệch chuẩn tương đối được phép tối đa | |||
2,0 | 0,41 | 0,59 | 0,73 | 0,85 |
| 2,5 | 0,52 | 0,74 | 0,92 | 1,06 |
| 3,0 | 0,62 | 0,89 | 1,10 | 1,27 |
Trong phép thử các tạp chất liên quan, giới hạn định lượng (tương ứng với tỷ số tín hiệu trên nhiễu bằng 10) phải bằng hoặc nhỏ hơn giới hạn được bỏ qua.
Yêu cầu về tính phù hợp của hệ thống là đòi hỏi cho quá trình tiến hành sắc ký. Tùy thuộc vào các yếu tố khác nhau như tần suất sử dụng và kinh nghiệm với hệ thống sắc ký, người phân tích sẽ lựa chọn một quy trình kiêm chứng thích hợp về tính phù hợp này.
2.2 Điều chỉnh các điều kiện sắc ký
Mức độ điều chỉnh các thông số khác nhau để thỏa mãn tính phù hợp của hệ thống sắc ký mà không làm thay đổi căn bản phương pháp được liệt kê dưới đây. Việc điều chỉnh các điều kiện rửa giải gradient thì khắt khe hơn so với rửa giải đăng dòng vì nó có thể dẫn tới sự chuyển dịch các píc đến một bước khác của quá trình gradient. Điều này dẫn đến việc xác định không đúng vị trí các pic, làm che lấp pic hoặc làm chuyển dịch pic tới mức chất phân tích được rửa giải ra sau thời gian đã định. Những thay đổi khác với những điểm đã được qui định đòi hỏi phải thẩm định lại phương pháp. Những điều kiện sắc ký được mô tả đều đã được thẩm định khi biên soạn xây dựng chuyên luận.
Các phép thử tính thích hợp của hệ thống được đưa vào để đảm bảo yêu cầu chia tách cho phép thử hay phép định lượng đạt chất lượng mong muốn. Tuy nhiên, vì pha tĩnh chỉ được mô tả một cách chung chung và trên thị trường lại có nhiều loại pha tĩnh có những đặc tính sắc ký khác nhau, nên có thể cần điều chỉnh một số điều kiện sắc ký để đạt yêu cầu của tính phù hợp hệ thống. Đặc biệt trong phương pháp sắc ký pha đào, việc thay đổi các thông số sắc ký không phải lúc nào cũng cho kết quả thỏa đáng. Trong trường hợp này, có thể phải thay cột khác cùng loại, ví dụ cột silica gel gắn với nhóm octadecylsilyl (C18) khác mà có thể cho kết quả mong muốn. Với các thông số quan trọng, việc điều chỉnh được xác định rõ ràng trong chuyên luận để đảm bảo tính phù hợp của hệ thống.
2.3 Sắc ký lớp mỏng và sắc ký giấy
Thành phần của pha động: Lượng thành phân dung môi nhỏ có thể điều chỉnh = 30% nồng độ tương đối hay - 2% nồng độ tuyệt đối tùy theo khoảng giá trị nào lớn hơn. Ví dụ với dung môi thành phần nhỏ là 10% của pha động thì thay đổi 30% tương đối nghĩa là nông độ trong khoảng 7% đến 13% trong khi thay đổi 2% nồng độ tuyệt đối nghĩa là nồng độ trong khoảng 8% đến 12%; như vậy, khoảng theo nồng độ tương đối lớn hơn: nếu thành phần dung môi nhỏ là 5% thì thay đôi 30% tương đối nghĩa là trong khoảng 3,5% đến 6,5% và thay đổi 2 % nồng độ tuyệt đối nghĩa là trong khoảng 3% đến 7%, trong trường hợp này khoảng theo nồng độ tuyệt đối lớn hơn. Không thành phần đung môi nào được thay đổi lớn hơn 10% nồng độ tuyệt đối.
pH của thành phần nước trong pha động được thay đổi ± 0,2 đơn vị pH trừ khi có chỉ dẫn khác trong chuyên luận, hoặc thay đổi = 1,0 đơn vị pH khi nghiên cứu các chất không ion hóa.
Nồng độ muối trong thành phần đệm của pha động được thay đổi + 10%.
Thể tích mẫu chấm sắc ký điều chỉnh trong khoảng 10% đến 20% của thể tích quy định nếu sử dụng bản mỏng cỡ hạt nhỏ (2 µm đến 10 µm).
Khoảng dịch chuyển của tuyển dung môi không được dưới 50 mm và với bản mỏng hiệu năng cao thì không được dưới 30 mm.
2.4 Sắc ký lỏng rửa giải đẳng dòng
Thành phần pha động: Lượng thành phần dung môi nhỏ có thể điều chỉnh ± 30% nồng độ tương đối hay ± 2% nồng độ tuyệt đối tùy theo khoảng giá trị nào lớn hơn (xem ví dụ ở trên). Không thành phần dung môi nào được thay đổi lớn hơn 10% nồng độ tuyệt đối.
pH của thành phần nước trong pha động: Chỉ điều chỉnh thay đổi ± 0,2 đơn vị pH trừ khi có chỉ dẫn khác trong chuyên luận, hoặc thay đổi ± 1,0 đơn vị pH khi nghiên cứu các chất không ion hóa.
Nồng độ muối trong thành phần đệm của pha động được thay đổi ± 10%.
Tốc độ dòng: ± 50%; có thể chấp nhận một sự điều chỉnh lớn hơn khi thay đổi kích thước cột (xem công thức ở dưới).
Các thông số cột:
Pha tĩnh:
Không thay đổi bản chất của nhóm thế trong pha tĩnh (ví dụ không thay C18 bằng C8);
Kích thước hạt: Cho phép giảm tối đa 50%; không được phép tăng.
Kích thước cột:
Chiều dài: ± 70%;
Đường kính trong: ± 25%.
Khi kích thước cột thay đổi, tốc độ dòng có thể phải điều chinh theo công thức sau:
.png)
Trong đó:
F1 là tốc độ dòng được chỉ ra trong chuyên luận, tính theo ml/min;
F2 là tốc độ dòng hiệu chỉnh, tính theo ml/min;
l1 là chiều dài cột ghi trong chuyên luận, tính bằng mm;
l2 là chiều dài cột được sử dụng, tính bằng mm;
d1 là đường kính trong của cột ghi trong chuyên luận, tính bằng mm;
d2 là đường kính trong của cột được sử dụng, tính bằng mm.
Nhiệt độ: Được điều chỉnh = 10 °C khi có quy định nhiệt độ tiến hành sắc ký, trừ khi có chỉ dẫn khác.
Bước sóng của detector phát hiện: Không được điều chỉnh.
Thể tích tiêm: Có thể giảm đi miễn là khả năng phát hiện và độ lập lại của pic cần xác định thỏa mãn yêu cầu; không cho phép tăng thể tích tiêm.
2.5 Sắc ký lỏng rửa giải gradient
Việc điều chỉnh các điều kiện cho hệ thống sắc ký rửa giải gradient đòi hỏi cần cẩn thận hơn so với hệ thống sắc ký đăng dòng.
Thành phần của pha động dùng rửa giải gradient: Những điều chỉnh nhỏ về thành phần của pha động và chương trình dung môi có thể được chấp nhận, miễn là:
Các yêu cầu về tính phù hợp của hệ thống được thỏa mãn,
Các pic chính được rửa giải trong vòng ± 15% của thời gian lưu quy định;
Thành phần cuối cùng của pha động không yếu hơn về lực rửa giải so với thành phần quy định.
Khi không thể đạt được thỏa mãn các yêu cầu về tính phù hợp của hệ thống thì nên xem xét về thể tích lưu trú (dwell volume) hoặc thay đổi cột tách.
Thể tích lưu trú (Dwell volume): Cấu hình của thiết bị dùng có thể làm thay đổi đáng kể độ phân giải, thời gian lưu và thời gian lưu tỷ đổi được quy định; đó là do thể tích lưu trú quá lớn. Các chuyên luận thường đưa vào một giai đoạn đẳng dòng trước khi bắt đầu chương trình gradient để làm thích ứng với các thời điểm gradient; điều này giúp xem xét sự khác nhau giữa thể tích lưu trú của hệ thống thiết bị được sử dụng để phát triển phương pháp và hệ thống đang được sử dụng. Người sử dụng có trách nhiệm điều chỉnh khoảng thời gian của giai đoạn đãng dòng cho phù hợp với thiết bị được sử dụng. Nếu thể tích lưu trú được dùng khi xây dựng chuyên luận được chỉ ra trong chuyên luận, các thời điểm (t min) ghi trong bảng chương trình dung môi có thể được thay thế bằng các thời điểm điều chỉnh (t, min) và được tính bằng công thức sau:
.png)
Trong đó:
D là thể tích lưu trú, tính bằng ml;
D0 là thể tích lưu trú khi phát triển phương pháp, tỉnh bằng ml;
F là tốc độ dòng tính bằng ml/min.
Giai đoạn đẳng dòng bổ sung cho mục đích trên đây có thể bỏ qua nếu các số liệu thẩm định để áp dụng phương pháp không có giai đoạn này.
pH của thành phần nước trong pha động không được phép điều chỉnh.
Nồng độ muối trong thành phần đệm của pha động cũng không được phép điều chỉnh.
Tốc độ dòng: Có thể điều chỉnh tốc độ dòng khi kích thước cột tách thay đổi (xem công thức ở dưới).
Các thông số về cột:
Pha tĩnh:
Không thay đổi bản chất của nhóm thế trong pha tĩnh (ví dụ không thay C18 bằng C8);
Kích thước tiểu phân không được thay đổi.
Kích thước cột:
Chiều dài: ± 70%;
Đường kính trong: ± 25%.
Khi kích thước cột tách thay đổi, tốc độ dòng có thê phải điều chỉnh dựa theo công thức sau:
.png)
Trong đó:
F1 là tốc độ dòng ghi trong chuyên luận, tỉnh bằng ml/min;
F2 là tốc độ dòng được điều chỉnh, tỉnh bằng ml/min;
l1 là chiều dài cột ghi trong chuyên luận, tính bằng mm;
l2 là chiều dài cột được sử dụng, tính bằng mm;
d1 là đường kính trong của cột ghi trong chuyên luận, tỉnh bằng mm;
d2 là đường kính trong của cột được sử dụng, tỉnh bằng mm.
Nhiệt độ: Được điều chỉnh ± 5 °C khi nhiệt độ vận hành sắc ký được quy định trong chuyên luận, trừ khi có chỉ dẫn khác. Bước sóng phát hiện của detector: Không được điều chỉnh. Thể tích tiêm: Có thể giảm đi miễn là khả năng phát hiện và độ lặp lại của pic cần xác định thỏa mãn yêu cầu; không cho phép tăng thể tích tiêm.
2.6 Sắc ký khí
Các thông số vẻ cột:
Pha tĩnh:
Kích thước tiểu phân: Có thể giảm tối đa 50%; không được phép tăng lên (cột nhồi);
Bề dày lớp phim: Cho phép thay đổi từ -50% đến +100% (cột mao quản).
Kích thước cột:
Chiều dài: ± 70%;
Đường kính trong: + 50%.
Tốc độ dòng: ± 50%.
Nhiệt độ: 110%.
Thể tích tiêm và thể tích chia dòng: Có thể được điều chỉnh, miễn là khả năng phát hiện và độ lặp lại là thỏa mãn yêu cầu.
2.7 Sắc ký lỏng siêu tới hạn
Thành phần pha động: Đối với cột nhồi, lượng hợp phần dung môi nhỏ có thể được điều chỉnh ± 30% tương đối hay ± 2 % tuyệt đối, tùy theo khoảng giá trị nào lớn hơn; không cho phép thay đổi đối với hệ thống cột mao quản. Bước sóng phát hiện của detector không được thay đổi.
Các thông số về cột:
Pha tĩnh: Kích thước tiểu phân: Có thể giảm tối đa 50%; không được phép tăng lên (cột nhồi).
Kích thước cột:
Chiều dài: ± 70%;
Đường kính trong: ± 25% cho cột nhồi và ± 50% cho cột mao quản.
Tốc độ dòng: ± 50%.
Nhiệt độ: Cho phép ± 5 °C khi nhiệt độ vận hành sắc ký được quy định trong chuyên luận.
Thể tích tiêm: Có thể được điều chỉnh, miễn là khả năng phát hiện và độ lặp lại là thỏa mãn yêu cầu, không được phép tăng lên.
2.8 Định lượng
Các pic của dung môi và thuốc thử hoặc xuất hiện từ pha động hay nền mẫu thì bỏ qua trong quá trình định lượng. Độ nhạy của detector: Độ nhạy của detector là tín hiệu đầu ra tỉnh trên một đơn vị nồng độ hay một đơn vị khối lượng chất có trong pha động đi vào detector. Hệ số đáp ứng tương đối của detetor, thường được gọi là hệ số đáp ứng, biểu thị độ nhạy của một detector đối với một chất chuẩn. Hệ số hiệu chỉnh là nghịch đảo của hệ số đáp ứng.
Phương pháp chuẩn ngoại: Nồng độ các thành phần cần phân tích được xác định bằng cách so sánh (các) đáp ứng pic của dung dịch thử đối với đáp ứng pic của dung dịch chất đối chiếu.
Phương pháp chuẩn nội: Chất chuẩn nội phải là một chất có thể tách khỏi chất khảo sát. Thêm cùng lượng chuẩn nội vào dung dịch thử và dung dịch chất đối chiếu. Chất chuẩn nội không được có phản ứng với chất khảo sát, phải bên và không chứa tạp có thời gian lưu tương tự thời gian lưu chất khảo sát. Nồng độ chất khảo sát được xác định dựa vào việc so sánh tỷ số diện tích pic (hay chiều cao pic) giữa chất khảo sát và chuẩn nội trong dung dịch thủ với tỷ số diện tích pic (hay chiều cao pic) giữa chất khảo sát và chuẩn nội trong dung dịch chất đối chiếu.
Phương pháp chuẩn hóa: Còn gọi là quy trình chuẩn hóa. Hàm lượng phần trăm của một hay nhiều thành phần trong mẫu thử được tính bằng cách xác định diện tích một pic hay nhiều pic dưới dạng phần trăm của tổng diện tích tất cả các pic trừ các pic của dung môi hay thuốc thử và các pic ở mức hay dưới mức có thể bỏ qua.
Phương pháp đường chuẩn: Còn gọi là quy trình hiệu chuẩn. Xác định mối quan hệ giữa tín hiệu đo được hay đánh giá được (y) và lượng (nồng độ, khối lượng, v.v...) của chất (x) rồi tính hàm hiệu chuẩn (phương trình đường chuẩn). Tính kết quả phân tích từ tín hiệu của chất phân tích (được đo hay được đánh giá) theo phương pháp hàm số ngược.
Trong các phép thử tạp chất liên quan, người ta dùng hoặc phương pháp chuẩn ngoại với một dung dịch thử được pha loãng để so sánh, hoặc dùng phương pháp chuẩn hóa, khi hệ số đáp ứng nằm ngoài khoảng 0,8 đến 1,2, thì phải áp dụng những hệ số hiệu chỉnh được chỉ ra trong chuyên luận. Khi trong chuyên luận có quy định phép thử các tạp chất liên quan là tổng các tạp chất hay khi phải định lượng một tạp chất thì điều quan trọng là phải chọn một ngưỡng thích hợp và các điều kiện thích hợp cho việc lấy tích phân các diện tích pic. Trong các phép thử như vậy thì ngưỡng bỏ qua (nghĩa là các diện tích pic bằng hoặc dưới ngưỡng này không phải tính đến) thường là 0,05%. Như vậy, ngưỡng đặt cho hệ thống thu thập dữ liệu ít nhất phải là nửa ngưỡng bỏ qua. Việc lấy tích phân các diện tích pic của các tạp không được tách hoàn toàn khỏi pic chính nên được thực hiện theo phương pháp ngoại suy từ hôm tới hõm (vạch tiếp tuyến).
3 Phương pháp sắc ký giấy
Phương pháp sắc ký giấy, cũng như phương pháp sắc ký lớp mỏng, được áp dụng trong kiểm nghiệm chất lượng thuốc để định tính, thử tinh khiết và đôi khi để bán định lượng và định lượng.
Sự tách các chất bằng phương pháp sắc ký giấy dựa chủ yếu trên sự khác nhau về hệ số phân bố của chúng giữa hai pha lỏng: Một pha tĩnh và một pha động. Pha tĩnh ở đây là nước có sẵn trong sợi celulose của giấy, hoặc thành phần thân nước từ hỗn hợp dung môi của pha động được hút chọn lọc vào giây. Pha động là một hệ dung môi thích hợp cho sự tách đã được quy định trong các chuyên luận.
Mức độ di chuyển của một chất được đặc trưng bởi hệ số di chuyển (R4) và tính bằng tỷ lệ giữa khoảng cách di chuyển của chất đó và khoảng cách di chuyển của dung môi:
Rt = a/b
Trong đó:
a là khoảng cách di chuyển của chất phân tích;
b là khoảng cách di chuyển của dung môi tính từ điểm chấm mẫu.
Giá trị Rr bao giờ cũng nhỏ hơn 1.
Trong trường hợp sắc ký liên tục không còn xác định được giới tuyến của dung môi, người ta dùng hệ số di chuyển Rr. Rr là tỷ số giữa khoảng cách di chuyển của chất phân tích và khoảng cách di chuyển của chất dùng làm chuẩn so sánh. Giá trị Rr có thể nhỏ hơn hay lớn hơn 1.
3.1 Cách tiến hành
Chuẩn bị bình sắc ký: Bình sắc ký là những bình thủy tinh hình trụ hoặc hình hộp dẹt, có kích thước thích hợp, có nắp đậy kín. Nắp có lỗ ở giữa để lắp bình gạn có khóa đựng dung môi. Trong bình có các giá để máng đựng dung môi và treo giấy sắc ký được thiết kế thích hợp cho kiểu sắc ký đi lên hay sắc ký đi xuống.
Chuẩn bị dung môi: Thành phần và tỷ lệ các dung môi được quy định trong các chuyên luận. Việc trộn các thành phần được tiến hành trong bình gạn, sau khi lắc đều, để yên. Nếu có tách lớp thì gạn lấy lớp pha thân nước, thường là lớp dưới, làm dung môi pha tình đề bão hòa giấy sắc ký sau khi đã chấm các chất phân tích, còn lớp trên dùng làm dung môi pha động. Nếu dung môi không tách lớp thì dùng chính dung môi đó để bão hòa giấy sắc ký.
Chuẩn bị giấy: Giấy sắc ký là loại giấy đặc biệt dành riêng cho sắc ký, có bề dày thích hợp. Tùy theo kích thước của bình và số lượng các vết cần chấm mà cắt những khổ giấy hình chữ nhật thích hợp, chiều dài dọc theo thớ giấy. Chiều rộng phải nhỏ hơn chiêu dài của máng dung môi nhưng không được nhỏ hơn 2,5 cm. Bề dài phải tính sao cho khi treo giấy vào bình không được để đầu dưới chạm vào máng dung môi trong khi bão hòa dung môi. Trường hợp bình sắc ký có hình chuông úp thì giấy phải cuộn tròn và cố định bằng móc thủy tinh hoặc khâu bằng chỉ. Đường kính của cuộn giấy phải nhỏ hơn đường kính của đĩa để giấy nhằm tránh giấy chạm vào thành đĩa.
Chấm sắc ký: Kẻ một đường chỉ mảnh song song với mép giấy (đường vạch để chẩm sắc ký) theo chiều rộng và cách mép giấy 3 cm đối với sắc ký đi lên để sao cho các vết chấm không bị ngập vào dung môi, 6 cm đối với sắc ký đi xuống để vạch chấm không trùng với đũa thủy tinh đỡ giấy mà thấp hơn 2 cm khi đặt giấy treo vào máng ở phần trên của bình.
Dùng micropipet chia độ tới 0,001 ml đến 0,002 ml hoặc mao quản có dung tích xác định (2 µl; 5 µl; 10 µl) để chấm các dung dịch chất cần sắc ký thành vệt có đường kinh không quá 8 mm. Muốn giữ đường kính của vết chấm nhỏ, phải chấm nhanh nhiều lần, đợi giọt trước khô mới chấm tiếp. Lượng chấm và nồng độ dung dịch chất thử được quy định trong chuyên luận.
Khi chấm nhiều vết trên một dải giấy thì vết chấm hải cách vết chấm kia ít nhất là 30 mm.
3.2 Triển khai sắc ký
Phương pháp sắc ký đi lên: Rót dung môi làm pha động vào máng dung môi để được một lớp dung môi cao 2.5 cm, và trong trường hợp pha tình được chỉ định (là phần tách lớp phía dưới khi trộn hỗn hợp dung môi) thì rót pha tĩnh vào khe giữa mảng dung môi và thành bình sắc ký. Đậy kín nắp bình, để yên trong 24 h ở nhiệt độ 20 °C đến 25 °C và duy trì ở nhiệt độ này trong quá trình tiếp theo. Sau đó treo giấy đã chuẩn bị vào bình, đậy nắp, để yên tiếp 90 min. Tiếp theo dùng tay vặn ở ngoài bình để hạ tờ giấy sắc ký vào máng dung môi sao cho vạch chấm không ngập vào dung môi. Triển khai sắc ký đến một thời gian hoặc một khoảng cách quy định trong chuyên luận. Lấy giấy ra, đánh dấu ngay giới tuyến dung môi và để khô ngoài không khi hoặc làm khô bằng không khí nóng của máy quạt sấy. Phải chú ý tránh ánh sáng trong suốt quá trình triển khai. Làm hiện vết bằng cách phun thuốc thử màu thích hợp, hoặc soi dưới đèn từ ngoại theo quy định của chuyên luận. Tính giá trị R và đánh giá kết quả.
Phương pháp sắc ký đi xuống: Cũng tiến hành tương tự như sắc ký đi lên, chỉ khác các điểm sau đây:
Rót dung môi làm pha tĩnh vào đáy bình, tạo một lớp cao khoảng 2 cm; đặt giấy vào máng dung môi ở phần trên bình, dùng một đũa thủy tinh để chèn giấy, gác đầu giấy treo qua đũa thủy tinh để không cho giấy chạm vào mép máng và chạm vào thành bình. Sau thời gian để bão hòa bình và giấy theo quy định như trên, rót pha động vào máng đựng dung môi ở phía trên. Thường sắc ký đi xuống được áp dụng cho các hỗn hợp khó tách và phải chạy sắc ký liên tục nên phải tính kết quả theo Rr.
4 Phương pháp sắc ký khí
Sắc ký khí là một phương pháp tách dựa trên sự phân bố khác nhau của các chất giữa hai pha không trộn lẫn vào nhau, trong đó pha động là chất khí (khí mang) đi qua pha tĩnh chứa trong cột. Sắc ký khí được áp dụng để tách những chất hoặc dẫn xuất của chúng mà có thể hóa hơi ở nhiệt độ phân tích. Phương pháp sắc ký khí dựa trên cơ chế hấp phụ, phân bố hoặc loại theo kích thước (dùng rây phân tử).
4.1 Thiết bị
Thiết bị gồm nguồn cung cấp khí, bộ phận tiêm mẫu, cột sắc ký chứa trong buồng ổn nhiệt, hệ thống phát hiện và ghi sắc đổ. Khí mang đi qua cột với tốc độ và áp suất có kiểm soát và đi qua detector. Nhiệt độ của cột hoặc được giữ ở một giá trị không đôổ hoặc thay đổi theo một chương trình quy định trong chuyên luận riêng.
Sự đặc thù về thiết kế của máy sắc ký khí có thể yêu cầu phải thay đổi điều kiện sắc ký đã ghi trong chuyên luận riêng. Trong những trường hợp có thay đổi như thế, phải cho những kết quả tương tự. Nếu cần, điều chỉnh tốc độ dòng khí mang để cải thiện chất lượng sắc ký đồ hoặc để thay đổi thời gian lưu của các pic quan tâm.
4.2 Bộ phận tiêm mẫu
Tiêm mẫu trực tiếp: Là kiểu tiêm mẫu thường dùng trừ khi có chỉ dẫn khác. Có thể tiêm mẫu trực tiếp vào đầu cột bằng bơm tiêm (syringe) hoặc dùng van tiêm mẫu hoặc đưa vào buồng hóa hơi có thể có gắn thêm bộ chia dòng.
Tiêm pha hơi: Có thể thực hiện bằng hệ thống tiêm mẫu head-space tình hay động.
Hệ thống tiêm mẫu head-space động (kỹ thuật bẩy và làm sạch): Bao gồm thiết bị nhúng chìm vào dung dịch cho các chất bay hơi bám vào cột hấp phụ ở nhiệt độ thấp. Các chất lưu giữ được giải hấp phụ vào pha động bằng cách làm nóng nhanh cột hấp phụ.
Hệ thống tiêm mẫu head-space tĩnh: Bao gồm buồng ổn nhiệt mẫu có kiểm soát nhiệt độ trong đó đặt lọ dựng mẫu chứa mẫu rắn hoặc lòng trong thời gian cố định để cho các thành phần bay hơi đạt được trạng thái cân bằng giữa pha hơi và pha lỏng hoặc răn. Sau khi đạt được trạng thái cân bằng, một lượng mẫu khí xác định trước được đưa vào máy sắc ký khí.
4.3 Pha tĩnh
Pha tĩnh chứa trong cột có thể là:
Cột mao quản làm bằng silica nung chảy, pha tĩnh phủ trên thành cột.
Cột nhồi chứa hạt chất mang, trơ tấm pha tĩnh lỏng.
Cột nhồi chứa pha tĩnh rắn.
Cột mao quản có đường kính trong từ 0,1 mm đên 0,53 min và dài từ 5 m đến 60 m. Pha tĩnh là một lớp phim bề dày từ 0,1 µm đến 5,0 µm có thể gắn kết về hóa học vào bề mặt bên trong.
Cột nhồi làm bằng thủy tinh hay kim loại, thông thường dài từ 1 m đến 3 m, đường kính trong từ 2 mm đến 4 mm. Pha tĩnh thường là chất polymer xốp hoặc chất mang rắn phủ pha tĩnh lỏng.
Trong phân tích các hợp chất phân cực ở cột nhồi với pha tĩnh có dung lượng thấp, tính phân cực thấp, chất mang phải trơ để tránh làm cho pic không đối xứng. Hoạt tính chất mang có thể được giảm đi bằng cách silan hóa trước khi phủ pha tĩnh lên. Thường dùng diatomit nung, rửa với acid. Các chất mang thường có các kích thước hạt khác nhau, thường sử dụng nhất các hạt từ 150 µm đến 180 µm và 125 µm đến 150 μm.
4.4 Pha động
Thời gian lưu và hiệu lực cột phụ thuộc vào tốc độ dòng khí mang: Thời gian lưu tỉ lệ thuận với chiều dài cột và độ phân giải tỉ lệ thuận với căn bậc hai chiều dài cột. Đối với cột nhồi, lưu lượng khí mang tính bằng ml/min ở áp suất khi quyển và nhiệt độ phòng. Lưu lượng đo ở đầu ra của detector bằng dụng cụ đo cơ học có chia độ hoặc ống đo tốc độ dòng dùng bọt xà phòng ở nhiệt độ cột đang phân tích. Tốc độ dài của dòng khí mang đi qua cột nhồi tỉ lệ nghịch với căn bậc hai dường kính trong của cột ở một thể tích dòng xác định. Lưu lượng 60 ml/min trong cột đường kinh trong 4 mm và lưu lượng 15 ml/min trong cột đường kính trong 2 mm cùng cho tốc độ dòng như nhau, do đó thời gian lưu tương đương nhau.
Thường dùng heli và nitrogen làm khí mang cho cột nhồi và nitrogen, heli và hydrogen cho cột mao quản.
4.5 Detector
Thường dùng detector ion hóa ngọn lửa, ngoài ra còn dùng detector dẫn nhiệt, nitrogen-phosphor (electron nhiệt hay nhiệt điện từ), cộng kết điện từ, phổ khối, phổ hồng ngoại FTIR và các loại detector khác tùy theo mục đích phân tích.
Các đại lượng đặc trưng cho quá trình sắc ký Xem Phụ lục 5. Các kỹ thuật tách sắc ký.
4.6 Phương pháp tiến hành
Ôn định cột, buồng tiêm và detector ở nhiệt độ và tốc độ dòng khí mang quy định trong chuyên luận cho đến khi đường nền ổn định.
Chuẩn bị các dung dịch thử và đối chiếu theo quy định của chuyên luận. Các dung dịch phải không được có các tiểu phân rắn. Dùng dung dịch chuẩn để xác định các điều kiện đo phù hợp đặt trên thiết bị và thể tích dung dịch mẫu tiêm cần dùng để tạo ra một đáp ứng phù hợp. Tiến hành các lần tiêm lặp lại để kiểm tra độ lặp lại của đáp ứng và kiểm tra sổ đĩa lý thuyết, nếu có yêu cầu.
Tiêm các dung dịch thử và ghi lại sắc ký đồ thu được. Tiến hành tiêm lại nhiều lần để kiểm tra độ lặp lại của đáp ứng. Xác định diện tích pic của các thành phần cần quan tâm khi không có chỉ dẫn khác. Cũng có thể xác định chiêu cao của pic tương ứng với các thành phần chất cân quan tâm khi hệ số đối xứng từ 0,80 đến 1,20. Từ những giá trị thu được tính ra hàm lượng của một thành phần hay nhiều thành phần có trong mẫu đem thử. Khi dùng một chất làm chuẩn nội, pic của chất này không được che phủ pic của mẫu thử. Nếu có pic bị ảnh hưởng cần phải có sự bố chính thích hợp. Trong những áp dụng có yêu cầu chương trình nhiệt độ, phải tính kết quả theo diện tích pic.
Trừ những chỉ dẫn khác quy định trong chuyên luận riêng, dùng nitrogen làm khi mang và detector ion hóa ngọn lửa. Thỉnh thoảng cần tiến hành xác định bằng kỹ thuật tiêm on-column, trong đó mẫu được tiêm trực tiếp vào chất nhồi cột không sử dụng bộ phận nạp mẫu gia nhiệt. Khi mẫu thử là chất không bay hơi được tiêm vào cột, nên dùng tiên cột phù hợp, loại có thể thay đổi được.
4.7 Thuốc thử
Các thuốc thử và các dung môi sử dụng trong việc chuẩn bị các dung dịch khảo sát cần có chất lượng phù hợp cho phân tích trên sắc ký khí. Có rất nhiều chất hóa học được dùng làm pha tĩnh như các polyethylen glycol, các ester và các amid có phân tử lượng cao, các hydrocarbon, các silicon dạng gôm hay dạng lỏng (polysiloxan đã dược thể bằng nhóm methyl, phenyl, nitril, vinyl hoặc fluoroalkyl, hoặc hỗn hợp của chúng) và các vi hạt rỗng cầu tạo đa nhân thơm liên kết chéo. Pha tĩnh phù hợp khi nồng độ của nó, bản chất và bậc của chất mang rắn theo đúng quy định của chuyên luận riêng. Cột phải luyện theo chỉ dẫn của nhà sản xuất. Trong đa số các trường hợp, tên thương mại của cột ghi trong chuyên luận là phù hợp cho mục đích phân tích nhưng có thể dùng cột có tên thương mại khác tương đương.
4.8 Chuẩn nội
Các thuốc thử được dùng làm chuẩn nội không được chứa bất kỳ tạp chất nào gây ra các píc có ảnh hưởng tới việc xác định các thành phần của mẫu thử đã mô tả trong chuyên luận riêng.
4.9 Chuẩn hóa
Trong một số trường hợp, cần tiến hành xác định bằng phương pháp quy về 100% để đánh giá một hoặc nhiều thành phần hoặc các tạp chất liên quan. Trong những trường hợp này, tổng diện tích của một pic hay các pic của các thành phần hoặc các tạp chất liên quan được biểu thị dưới dạng tỷ lệ phần trăm so với tổng diện tích của tất cả các pic thu được từ mẫu đem thử. Trong quá trình xác định, cần sử dụng bộ khuếch đại để mở rộng thang đo và bộ tính tích phân tự động.
4.10 Thể tích tiêm
Khi thể tích tiêm không qui định trong chuyên luận riêng, nên chọn một thể tích phù hợp để áp dụng. Chọn thể tích tiêm phụ thuộc vào đáp ứng của phép phân tích, detector sử dụng, hiệu lực cột và toàn bộ hiệu năng của hệ thống sắc ký. Khi không có chỉ dẫn, thường dùng thể tích tiêm là 1 µl, tuy nhiên cần kiểm tra sự thích hợp trong điều kiện cụ thể.
4.11 Pic phụ (pic thứ cấp)
Có thể cần chất đối chiếu để xác định pic phụ. Píc phụ là một pic có trên sắc ký đồ nhưng không phải là pic chính hay pic chuẩn nội hoặc pic của dung môi và các thuốc thử tạo dẫn xuất.
4.12 Sắc ký khí head-space
Sắc ký khí head-space là phương pháp đặc biệt thích hợp để tách và xác định các chất bay hơi hiện diện trong mẫu rắn hay lòng. Phương pháp dựa trên sự phân tích pha hơi sau khi đạt được trạng thái cân bằng với pha rắn hoặc pha lỏng.
4.13 Thiết bị
Máy sắc ký khí kết nối với bộ phận nạp mẫu tự động có thiết bị kiểm soát nhiệt độ và áp suất. Trong trường hợp cần thiết, có thể gắn thêm bộ phận đuổi dung môi.
Đưa mẫu vào lọ đựng mẫu có nắp đậy gắn với hệ thống van có thể cho phép khí mang đi qua. Đặt lọ đựng mẫu trong buồng ổn nhiệt ở nhiệt độ tùy theo bản chất của mẫu và duy trì nhiệt độ này trong thời gian sao cho đạt được trạng thái cân bằng giữa pha rắn hoặc lòng và pha hơi. Đưa khi mang vào lọ đựng mẫu và sau thời gian quy định, mở van tương ứng để khí khuếch tán vào cột sắc ký mang theo các chất bay hơi cần phân tích.
Nếu không có bộ phận nạp mẫu tự động, có thể dùng bơm tiêm (syringe) mẫu khi đưa mẫu trực tiếp vào cột sau khi đạt được trạng thái cân bằng trong buồng ổn nhiệt đặt riêng. Cần lưu ý tránh những yếu tố làm thay đổi trạng thái cân băng.
4.14 Phương pháp tiến hành
Dùng các dung dịch đối chiếu để xác định tính thích hợp của cài đặt thiết bị để cho đáp ứng đạt yêu cầu.
Định lượng trực tiếp Lần lượt cho mẫu thử và mẫu đối chiếu vào các lọ đựng mẫu đồng nhất như quy định trong chuyên luận riêng. tránh tiếp xúc giữa mẫu thử và thiết bị lấy mẫu. Đậy kín lọ và đặt trong buồng ổn nhiệt đã đặt nhiệt độ và áp suất như trong chuyên luận riêng. Sau khi đạt được trạng thái cân bằng, tiến hành sắc ký theo điều kiện quy định trong chuyên luận riêng.
Phương pháp thêm chuẩn Lần lượt cho cùng một thể tích mẫu thử vào các lọ đựng mẫu đồng nhất. Thêm vào mỗi lọ một lượng thích hợp dung dịch đối chiếu của chất cần xác định có hàm lượng đã biết trước để có một dãy dung dịch có nồng độ tăng dần một cách đều đặn.
Đậy kín lọ và đặt trong buồng ổn nhiệt đã đặt nhiệt độ và áp suất như trong chuyên luận riêng. Sau khi đạt được trạng thái cân bằng, tiến hành sắc ký theo điều kiện quy định trong chuyên luận riêng.
Lập phương trình tuyến tính của đồ thị bằng phương pháp bình phương tối thiểu và tìm được từ đó nồng độ của chất cần xác định trong dung dịch. Theo một cách khác, vẽ đồ thị trung bình các nồng độ xác định được theo lượng dung dịch đối chiếu thêm vào. Kéo dài đường nổi các điểm trên đồ thị cho đến khi gặp trục nồng độ. Khoảng cách giữa điểm này và giao điểm của các trục thể hiện nồng độ chất cân xác định trong dung dịch.
Phương pháp rút ra liên tục
Nếu được quy định, phương pháp rút ra liên tục được mô tả đầy đủ trong chuyên luận riêng.
5 Phương pháp sắc ký lỏng
Sắc ký lỏng là phương pháp tách sắc ký các chất dựa trên sự phân bố khác nhau của chúng giữa hai pha không trộn lẫn, trong đó pha động là một chất lỏng chảy qua pha tĩnh chứa trong cột.
Sắc ký lỏng được tiến hành chủ yếu dựa trên cơ chế hấp phụ, phân bố khối lượng, trao đổi ion, loại trừ theo kích thước hoặc tương tác hóa học lập thể.
5.1 Thiết bị
Thiết bị bao gồm một hệ thống bơm, bộ phận tiêm mẫu, cột sắc ký (bộ phận điều khiển nhiệt độ có thể được sử dụng nếu cần thiết), detector và một hệ thống thu đữ liệu (hay một máy tích phân hoặc một máy ghi đồ thị). Pha động được cung cấp từ một hoặc vài bình chứa và chảy qua cột, thông thường với tốc độ không đổi và sau đó chạy qua detector.
5.2 Hệ thống bơm
Hệ thống bơm trong sắc ký lỏng phải giữ cho pha động luôn chảy với một lưu lượng không đổi. Những biến đổi áp suất sẽ được giảm thiểu, ví dụ cho dung môi chạy qua một thiết bị giảm xung. Ông dẫn và hệ thống nổi phải là loại chịu được áp suất sinh ra do hệ thống bơm. Các bơm có thể được lắp với thiết bị loại bỏ bọt khí.
Hệ thống điều khiển bằng bộ vi xử lý có khả năng cung cấp pha động hoặc hằng định (rửa giải đẳng dòng) hoặc thay đổi tỷ lệ thành phần (rửa giải gradient) theo một chương trình xác định. Trong trường hợp rửa giải gradient, hệ thống bơm lấy các dung môi từ một vài bình chứa và các dung môi có thể được trộn lẫn ở áp suất thấp hoặc áp suất cao.
5.3 Bộ phận tiêm mẫu
Dung dịch mẫu thử được đưa vào dòng pha động hoặc vào vị trí gần đầu hoặc đầu cột nhờ một bộ phận tiêm mẫu có khả năng hoạt động ở áp suất cao. Có thể dùng vòng chửa mẫu thử, có thể tích cố định hoặc thiết bị có thể tích thay đổi, có thể vận hành bằng tay hoặc tự động. Khi tiêm mẫu bằng tay có thể gây ra sai số do thể tích tiêm vào vòng chứa mẫu không đủ.
5.4 Pha tĩnh
Có nhiều loại pha tĩnh có thể được sử dụng trong sắc ký lòng, bao gồm:
Silica (silic dioxyd), nhôm oxyd hoặc than graphit xốp thường được dùng trong sắc ký pha thuận mà quá trình phân tách dựa trên sự khác nhau về khả năng hấp phụ hoặc (và) phân bố khối lượng;
Nhựa hoặc polymer có chứa các nhóm chức acid hoặc base, sử dụng trong sắc ký trao đổi ion mà trong đó sự chia tách được thực hiện dựa trên sự cạnh tranh giữa các ion cần tách và các ion trong pha động;
Silica xốp hoặc polymer, sử dụng trong sắc ký rây phân tử, ở đó sự chia tách dựa trên sự khác nhau về kích thước phân tử, tương ứng với sự loại trừ không gian;
Rất nhiều chất mang biến đổi hóa học được chế tạo từ polymer, silica gel hoặc than graphit xốp được dùng trong sắc ký lỏng pha đảo mà ở đó sự chia tách về nguyên tắc cơ bản dựa trên sự phân bố phân từ các chất giữa pha động và pha tĩnh;
Pha tĩnh loại biến đổi hóa học đặc biệt, ví dụ dẫn xuất của celulose hoặc amylose, protein hoặc peptid, cyclodextrin v.v... dùng để tách các đồng phân đối quang (sắc ký đối quang).
Phần lớn sự chia tách dựa trên cơ chế phân bố, sử dụng silica biến đổi hóa học làm pha tình và các dung môi phân cực làm pha động. Bề mặt của chất mang, ví dụ như các nhóm silanol của silica được phản ứng với các thuốc thừ silan khác nhau tạo thành các dẫn xuất silyl có liên kết cộng hóa trị, che phủ một số lượng khác nhau các vị trí hoạt động trên bề mặt chất mang. Bản chất của các pha liên kết là tham số quan trọng để xác định các tính chất tách của hệ sắc ký.
Các pha liên kết dùng phổ biến là:
Octyl = Si-(CH2)7-CH3 C8
Octadecyl = Si-(CH2)17-CH3 C18
Phenyl = Si-(CH2)n-(C6H5) C6H5
Cyanopropyl = Si-(CH2)3-CN CN
Aminopropyl =Si-(CH2)3-NH2 NH2
Diol = Si-(CH2)3-OCH(OH)-CH2-OH
Trừ khi có tiêu chuẩn riêng của nhà sản xuất, thông thường các cột sắc ký pha đào dựa trên silica được coi là ổn định đối với pha động có pH từ 2,0 tới 8,0. Cột chứa than graphit xốp hoặc các hạt vật liệu polymer như styren divinylbenzen copolymer ổn định ở một khoảng pH rộng hơn. Phân tích sử dụng sắc ký pha thuận với pha tĩnh là silica không bị biến đổi, than graphit xốp hoặc silica biến đổi hóa học làm cho phân cực (ví dụ cyanopropyl hoặc diol) và pha động không phân cực được sử dụng trong một số trường hợp.
Đối với sự tách nhằm mục đích phân tích, kích thước hạt của pha tĩnh phổ biến nhất từ 3 µm đến 10 µm. Các hạt có thể hình cầu hoặc không có hình dạng nhất định, có độ xốp khác nhau và diện tích bề mặt đặc hiệu. Những tham số này cấu thành biểu hiện sắc ký của từng pha tình cụ thể. Trong trường hợp pha đảo, các yếu tố bổ sung như bàn chất của pha tĩnh, mức độ liên kết, ví dụ như độ dài mạch carbon liên kết, hoặc các nhóm hoạt động bề mặt của pha tĩnh có được che phủ hết hay không. Sự kéo đuôi pic, đặc biệt của các chất base, có thể xảy ra khi có mặt các nhóm silanol bề mặt của silica.
Cột được làm bằng thép không gỉ trừ khi có chỉ dẫn khác trong chuyên luận riêng, có chiều dài và đường kính trong (2) khác nhau được sử dụng cho phân tích sắc ký. Cột với đường kính trong nhỏ hơn 2 mm thường được coi là vi cột. Nhiệt độ của pha động và cột phải được giữ ổn định trong suốt thời gian phân tích. Phần lớn quá trình tách được thực hiện ở nhiệt độ phòng, nhưng cột có thể được làm nóng nhằm thu được hiệu quả cao hơn. Tuy nhiên, nhiệt độ cột cũng không được phép vượt quá 60 °C vì khả năng phân hủy của pha tĩnh hoặc sự thay đổi thành phần của pha động có thể xảy ra.
5.5 Pha động
Đối với sắc ký pha thuận, thường sử dụng dung môi ít phân cực. Sự có mặt của nước trong pha động phải được hạn chế và kiểm tra chặt chẽ nhằm thu được kết quả tái lập lại. Đối với sắc ký lỏng pha đảo, sử dụng pha động chứa nước, có hoặc không có dung môi hữu cơ.
Các thành phần của pha động thường được lọc nhằm loại bỏ các tiểu phân lớn hơn 0,45 µm. Pha động chứa nhiều thành phần được chuẩn bị bằng cách đong các thể tích qui định (trừ khi có chỉ định về khối lượng) của các thành phần riêng lẻ rồi sau đó trộn lẫn với nhau. Ngoài ra, dung môi cũng có thể được cấp qua các bơm riêng lẻ, điều khiển bằng các van chia tỷ lệ, để có thể trộn lẫn theo các tỷ lệ mong muốn. Dung môi thường được loại khí trước khi bơm bằng cách sục khí heli, lắc siêu âm hoặc sử dụng hệ thống lọc màng lọc chân không trực tuyến nhằm tránh sự tạo bọt khi trong cốc đo của detector.
Dung môi dùng để chuẩn bị pha động thường không được chứa các chất làm ổn định và phải trong suốt (không hấp thụ quang) ở vùng bước sóng phát hiện, nếu như sử dụng detector tử ngoại. Dung môi và những thành phần khác được dùng phải có chất lượng phù hợp. Khi cần điều chỉnh pH chỉ thực hiện với thành phần nước của pha động mà không điều chỉnh với hỗn hợp. Nếu sử dụng dung dịch đệm, cần phải rửa hệ thống bằng hỗn hợp nước và dung môi hữu cơ (5% tt/tt) nhằm ngăn chặn sự kết tinh muối sau khi kết thúc quá trình sắc ký.
Pha động có thể chứa những thành phần khác, ví dụ một ion trái dầu trong sắc ký tạo cặp ion hoặc một chất chọn lọc đối quang trong trường hợp sắc ký sử dụng pha tĩnh không chọn lọc đối quang.
5.6 Detector
Detector hấp thụ từ ngoại khả kiến gồm cả detector chuỗi diod là được sử dụng phổ biến nhất. Detector huỳnh quang. detector khúc xạ vì sai, detector điện hóa, detector khối phố, detector tán xạ ánh sáng bay hơi, detector phóng xạ hoặc các loại detector đặc biệt khác cũng có thể được sử dụng.
5.7 Các đại lượng đặc trưng cho quá trình sắc ký
Xem phần chung Phụ lục 5. Các kỹ thuật tách sắc ký.
5.8 Phương pháp tiến hành
Làm cân bằng cột với pha động và tốc độ dòng theo qui định, ở nhiệt độ phòng hoặc nhiệt độ qui định trong chuyên luận riêng, cho đến khi đường nền ổn định. Chuẩn bị các dung dịch chuẩn và dung dịch thử theo yêu cầu. Các dung dịch phải không được có các tiêu phân rắn.
5.9 Hiệu năng
Qui định về tính phù hợp của hệ thống được mô tả trong Phụ lục 5. Các kỹ thuật tách sắc ký. Xác định và điều chỉnh các thông số của hệ thống sắc ký có thể được thực hiện nhằm đáp ứng các yêu cầu về tỉnh phù hợp của hệ thống cũng được trình bày trong Phụ lục này.
Thành phần và tốc độ dòng của pha động được qui định trong chuyên luận riêng. Pha động là hỗn hợp dung môi được đuổi khí bằng bơm chân không hoặc bằng một thiết bị đuổi khí khác phù hợp nhưng không ảnh hưởng đến thành phần của hỗn hợp.
Trong quá trình định lượng, khi trong chuyên luận riêng không qui định dùng chuẩn nội, nên sử dụng bộ phận tiêm mẫu có thể tích cố định. Trong một số trường hợp ngoại lệ, khi trong chuyên luận chỉ dẫn tính theo chiều cao pic thi không cần quan tâm đến hệ số đối xứng.
Cột sắc ký thường được làm bằng thép không gì có kích thước (chiều dài × đường kính trong) được qui định trong chuyên luận riêng. Trong chuyên luận riêng. khi pha tĩnh được ký hiệu bằng một chữ cái thì tra cứu ở phần Nguyên vật liệu nêu ở dưới đây. Đường kính danh nghĩa của hạt pha tĩnh dược để trong ngoặc đơn ngay sau ký hiệu chữ cái cụ thể. Nếu không có chỉ dẫn khác trong chuyên luận riêng, quá trình sắc ký được tiến hành ở điều kiện nhiệt độ không đòi trong môi trường phòng thí nghiệm. Khi sử dụng các pha động có pH cao với cột có bản chất là silica nên sử dụng một tiền cột ở trước cột phân tích. Trừ khi có các chỉ dẫn khác trong chuyên luận riêng, hệ thống detector gồm một detector đo quang gắn với một cốc đo có thể tích nhỏ (khoảng 10 µl là phù hợp). Phải đặt bước sóng theo chỉ dẫn trong chuyên luận riêng. Khi dùng một máy sắc ký có thiết kế riêng biệt có thể phải thay đổi các điều kiện sắc ký đã ghi trong chuyên luận riêng. Trong trường hợp này, người phân tích cần đảm bảo rằng những thay đổi đó cho kết quả tương đương.
5.10 Thể tích tiêm
Khi thể tích tiêm không qui định trong chuyên luận riêng, nên chọn một thể tích tiêm phù hợp để áp dụng. Chọn thể tích tiêm phụ thuộc vào đáp ứng của phép phân tích, detector sử dụng, hiệu lực cột và toàn bộ hiệu năng của hệ thống sắc ký. Khi không có chỉ dẫn, thường dùng thể tích tiêm là 20 µl, tuy nhiên cần kiểm tra sự thích hợp trong điều kiện cụ thể.
5.11 Pic phụ (Pic thứ cấp)
Có thể cần chất đối chiếu để xác định pic phụ. Pic phụ là một pic có trên sắc ký đồ nhưng không phải là pic chính hay píc của chuẩn nội hoặc pic của dung môi hay của các thuốc thử tạo dẫn xuất.
5.12 Nguyên vật liệu
Các dung môi và thuốc thử dùng để pha các dung dịch sử dụng trong phân tích phải có chất lượng thích hợp cho sắc ký lỏng.
Khi chuyên luận riêng quy định pha tĩnh được gán với một chữ cái (A hoặc B hoặc C) là muốn nói tới các pha tĩnh như mô tả dưới đây:
Pha tĩnh A, hạt silica;
Pha tĩnh B, hạt silica được biến đổi hóa học, gắn với nhóm octylsilyl (Cs);
Pha tĩnh C, hạt silica được biến đổi hóa học, gắn với nhóm octadecylsilyl (C18).
6 Sắc ký lớp mỏng
Phương pháp sắc ký lớp mỏng được dùng để định tỉnh, thử tinh khiết và đôi khi để bản định lượng hoặc định lượng hoạt chất thuốc.
Sắc ký lớp mỏng là một kỹ thuật tách các chất được tiến hành khi cho pha động di chuyển qua pha tĩnh trên đó đã chấm hỗn hợp các chất cần tách. Pha tĩnh là chất hấp phụ được chọn phù hợp theo từng yêu cầu phân tích, được trải thành lớp mỏng đồng nhất và được cổ định trên các phiến kính hoặc phiến kim loại. Pha động là một hệ dung môi đơn hoặc đa thành phần được trộn với nhau theo tỷ lệ quy định trong từng chuyên luận. Trong quá trình di chuyên qua lớp hấp phụ, các cấu tử trong hỗn hợp mẫu thử được di chuyển trên lớp mỏng, theo hướng pha động, với những tốc độ khác nhau. Kết quả thu được là một sắc kỵ đồ trên lớp mỏng. Cơ chế của sự tách có thể là cơ chế hấp phụ, phân bố, trao đổi ion, sàng lọc phân tử hay sự phối hợp đồng thời của nhiều cơ chế tùy thuộc vào tính chất của chất làm pha tĩnh và dung môi làm pha động.
Đại lượng đặc trưng cho mức độ di chuyển của chất phân tích là hệ số di chuyển R, được tính bằng tỷ lệ giữa khoảng dịch chuyển của chất thử và khoảng dịch chuyển của dung môi:
![]()
Trong đó:
a là khoảng cách di chuyển của chất phân tích;
b là khoảng cách di chuyển của dung môi tính từ điểm chẩm mẫu.
Rf: Chỉ có giá trị từ 0 đến 1.
Ngoài ra, khi sắc ký liên tục không xác định được tuyến dung môi, vị trí vết chất thử trên sắc đồ có thể xác định bằng hệ số dịch chuyển tương đối R, Hệ số dịch chuyển tương đối R, được xác định bằng tỷ số giữa khoảng cách dịch chuyển của vết chất thử và khoảng cách dịch chuyển của vết chất chuẩn đối chiếu được sắc ký trong cùng điều kiện và trên cùng bản mỏng với mẫu thử:
.png)
Trong đó:
a là khoảng cách từ điểm xuất phát đến tâm của vết mẫu thử;
c là khoảng cách từ điểm xuất phát đến tâm của vết chất chuẩn.
Giá trị Rt có thể lớn hay nhỏ hơn 1.
6.1 Cách tiến hành
6.1.1 Dụng cụ
Bình triển khai, thường bằng thủy tinh trong suốt có kích thước phù hợp với các phiến kính cần dùng và có nắp đậy kín.
Đèn tử ngoại, phát các bức xạ có bước sóng ngắn 254 nm và bước sóng dài 365 nm.
Dụng cụ để phun thuốc thử.
Tủ sấy điều nhiệt để hoạt hóa và sấy bản mỏng và sắc ký đồ, hoặc để sấy nóng đối với một số phản ứng phát hiện.
Tủ hút hơi độc.
Máy sấy dùng để sấy khô sắc ký đồ và cho phép chấm nhanh nhiều lần những dung dịch pha loãng chất cần phân tích. Một máy ảnh tốt có thể chụp lưu giữ sắc ký đồ ở ánh sáng ban ngày với khoảng cách 30 cm đến 50 cm.
Tủ lạnh để bảo quản những thuốc thử để hỏng. Micropipet nhiều cỡ từ 1 µl, 2 µl, 5 μl, 10 µl đến 20 µl, các ống mao quản hoặc dụng cụ thích hợp. Bản mỏng tráng sẵn chất hấp phụ có chất phát quang thích hợp.
Trường hợp phòng thí nghiệm không có điều kiện trang bị các loại bản mỏng tráng sẵn thì tự chuẩn bị lấy bán mỏng với các dụng cụ sau đây:
Các tấm kính phẳng có kích thước phù hợp đã được xử lý trước bằng hóa chất rồi rửa sạch bằng nước và sấy khô. Thiết bị trải chất hấp phụ lên tấm kính thành một lớp mỏng đồng đều, có chiều dày thích hợp. Giá để xếp các tấm kính đã trải.
6.1.2 Chuẩn bị bản mỏng
Sắp xếp các bản mỏng và chuẩn bị thiết bị: Các phiến kính phải được lau chùi cẩn thận và tẩy sạch hoàn toàn các chất béo bằng cách ngâm trong dung dịch sulfocromic. Sau đó, rửa dưới tia nước máy rồi tráng nước cất và làm khô trên giá ở nhiệt độ thường hay trong tủ sấy. Đặt lên khung trải 5 phiến kinh 20 cm x 20 cm (hay phiến kính 10 cm × 20 cm) dày bằng nhau. Điều chỉnh độ dày của lớp hấp phụ bằng các thông số trên thiết bị trải.
Điều chế vữa của chất hấp phụ: Chất hấp phụ được chọn lọc sao cho phù hợp với yêu cầu phân tích như: Silica gel G, kieselguhr, celulose, nhôm oxyd, trong số đó silica gel G được dùng thông dụng nhất. Trộn 25 g silica gel G với 50 ml nước cất và nhào trong cối hoặc lắc mạnh trong bình nón có dung tích 200 ml đến 250 ml, nút kín, trong 30 s đến 45 s. Dịch treo tạo được ở dạng lỏng và đồng nhất. Rót ngay vào thiết bị trải đã điều chỉnh độ dày cho bản mỏng khoảng 0,25 mm (nếu không có chỉ dẫn trong chuyên luận riêng). Sau khi rót dịch treo vào thiết bị trải, lật tay đòn 180° về phía trái và chờ cho đến khi dịch treo chảy ra thì bắt đầu trải. Khi đã trải đến phiến cuối cùng lật tay đòn về phía phải để giữ cho dịch treo không chảy xuống.
Đề nguyên các phiến kính tại chỗ khoảng 10 min tới khi mặt trên hết bóng, hoặc để khô tự nhiên tại nhiệt độ phòng. Hoạt hóa: Cho các bản mòng đã khô mặt vào tủ sấy và sấy ở 105 °C đến 110 °C trong 30 min (nếu không có chỉ dẫn ở chuyên luận riêng). Đề nguội rồi bảo quản trong bình hút ẩm. Khi dùng, nếu cần thì hoạt hóa lại bằng cách sấy ở 105 °C đến 110 °C trong 1 h rồi cạo bỏ một dải chất hấp phu dọc hai bên cạnh của tấm kính.
Chuẩn bị bình khai triển: Các bình khai triển thường là bình thủy tinh, hình hộp hay hình trụ, có nắp đậy kín, kích thước thay đổi tùy theo yêu cầu của các bản mỏng sử dụng. Bão hòa hơi dung môi vào khí quyển trong bình bằng cách lót giấy lọc xung quanh thành trong của bình, rồi rót một lượng vừa đủ dung môi vào bình, lắc rồi để giấy lọc thẩm đều dung môi. Lượng dung môi sử dụng sao cho sau khi thấm đều giấy lọc còn lại một lớp dày khoảng 5 mm đên 10 mm ở đáy bình. Đậy kín nắp bình và để yên 1 h ở nhiệt độ 20 °C đến 25 °C. Muốn thu được những kết quả lặp lại, ta chỉ nên dùng những dung môi thật tinh khiết, loại dùng cho sắc ký. Những dung môi dễ bị biến đổi về hóa học chỉ nên pha trước khi dùng. Nếu sử dụng những hệ pha động phức tạp phải chú ý đến những thành phần dễ bay hơi làm thay đổi thành phần của hệ pha động dẫn đến hiện tượng không lặp lại của trị số R
Chấm chất phân tích lên bản mỏng: Lượng chất hoặc hỗn hợp chất đưa lên bản mỏng có ý nghĩa quan trọng đối với hiệu quả tách sắc ký, đặc biệt ảnh hưởng rất lớn đến trị số Rf. Lượng chất quá lớn làm cho vết sắc ký lớn và kéo dài, khi đó, vết của các chất có trị số Rf gần nhau sẽ bị chồng lấp. Lượng chất nhỏ quá có thể không phát hiện được do độ nhạy của thuốc thử không đủ (thông thường độ nhạy của các thuốc thử trên 0,005 µg). Lượng mẫu thông thường cần đưa lên bản mỏng là 0,1 µg đến 50 µg ở dạng dung dịch trong dung môi thích hợp. Thể tích dung dịch từ 0,001 ml đến 0,005 ml đổi với trường hợp đưa mẫu lên bản mỏng dưới dạng điểm và từ 0,1 ml đến 0,2 ml khi đưa mẫu lên bản mỏng dưới dạng vạch như trong trường hợp sắc ký điều chế. Đối với các dung dịch có nồng độ rất loãng thì có thể làm giàu trực tiếp trên bản mỏng bằng cách chấm nhiều lần ở cùng một vị trí và sấy khô sau mỗi lần chấm. Đường xuất phát phải cách mép dưới của bản mỏng 1,5 cm đến 2 cm và cách bề mặt dung môi từ 0,8 cm đến 1 cm. Các vết chấm phải nhỏ, có đường kính 2 mm đến 6 mm và cách nhau 15 mm. Các vết ở bìa phải cách bờ bên của bản mỏng ít nhất 1 cm để tránh hiệu ứng bờ. Khi làm sắc ký lớp mỏng bán định lượng, độ chính xác của kết quả phân tích phụ thuộc rất nhiều vào độ chính xác của lượng chất thử đưa lên bản mỏng, tức là thể tích dung dịch châm lên bản mỏng. Do đó, với những trường hợp phân tích bán định lượng phải dùng các mao quản định mức chính xác. Khi không cần định lượng dùng micropipet hoặc ống mao quản thường.
Triển khai sắc ký: Đặt bản mỏng vào bình triển khai. Chú ý lượng dung môi dùng sao cho để các vết chấm phải ở trên bề mặt của lớp dung môi. Đậy kín bình và để triển khai ở nhiệt độ từ 20 °C đến 25 °C và tránh ánh mặt trời. Nếu không có qui định trong chuyên luận riêng, triển khai sắc ký đến khi dung môi đi được khoảng 3/4 bản mỏng, lấy bản mỏng ra khỏi bình, đánh dấu mức dung môi, làm bay hơi dung môi còn đọng lại trên bản mỏng rồi hiện vết theo chỉ dẫn trong chuyên luận riêng. Quan sát các vết xuất hiện, tính giá trị Rf hoặc Rr và tiến hành định tính, phát hiện tạp chất hoặc định lượng như quy định trong chuyên luận riêng.
CHÚ Ý:
Khi phân tích bằng sắc ký lớp mỏng luôn phải chấm chất đối chiếu bên cạnh vết chất thử với lượng tương tự như dự đoán có trong vết chất thử để so sánh kết quả về màu sắc, kích thước và giá trị Rf hoặc Rr trong cùng điều kiện.
Hiệu năng của bản mỏng được kiểm tra như sau: Chấm một thể tích thích hợp (10 µl) cho lớp mỏng thông thường và 1 µl đến 2 µl cho loại bản mỏng có kích thước hạt mịn dung dịch thử hiệu năng lớp mông gôm lục bromocresol, da cam methyl, đó methyi và sudan G đó (thuốc thử). Tiến hành sắc ký với hệ dung môi methanol - toluen (20 : 80). Kết quả trên sắc ký đồ phải có 4 vết tách rõ ràng có R, như sau: Lục bromocresol: < 0,15; da cam methyl: 0,1 đến 0.25, đô methyl: 0,35 đến 0,55 và sudan G đó: 0.75 đến 0,98.
7 Phương pháp sắc ký rây phân tử
Sắc ký rây phân tử là phương pháp chia tách các phân từ trong dung dịch dựa trên kích thước của chúng. Trong trường hợp pha động là một dung môi hữu cơ, kỹ thuật được gọi là sắc ký thấm qua gel, còn trường hợp pha động là nước thì kỹ thuật được gọi là sắc ký lọc trên gel. Mẫu được đưa vào cột chứa đây gel hoặc một loại vật liệu xốp, và được pha động dẫn chạy qua cột. Sự chia tách theo kích thước được thực hiện nhờ sự trao đổi lặp đi lặp lại các phân tư chất tan giữa dung môi pha động và cùng dung môi đó được pha tình giữ ở trong các lỗ xốp của gel. Khoảng kích thước lỗ của vật liệu nhồi trong cột sẽ xác định khoảng kích thước phân tử được chia tách qua quá trình sắc ký.
Những phân tử có kích thước đù nhỏ để có thể đi vào trong tất cả khoảng không gian của lỗ xốp được rửa giải trong thể tích thấm tổng V1. Các phân từ có kích thước lớn hơn kích thước lỗ xốp lớn nhất chỉ di chuyển dược dọc theo cột qua các khoảng trống giữa các hạt vật liệu nhồi mà không bị giữ lại, được rửa giải trong thể tích loại trừ V0 (thể tích trống). Sự chia tách theo kích thước phân tử xảy ra giữa thể tích trống và tổng thể tích thấm, chia tách hiệu quả thường được thực hiện ở hai phần ba đầu tiên của khoảng này.
7.1 Thiết bị
Thiết bị bao gồm một cột sắc ký có kích thước phù hợp, nếu cần thiết phải khống chế nhiệt độ, được nhồi đầy vật liệu chia tách có thể phân loại theo các khoảng kích thước phân tử phù hợp. Kích thước của cột (chiều cao × đường kính trong) được quy định ở chuyên luận riêng. Pha động chạy qua cột ở tốc độ không đổi dưới tác dụng của trọng lực hoặc nhờ một bơm. Một đầu của cột được nối với một thiết bị phù hợp để cấp mẫu theo kiểu bộ phận điều chỉnh lưu lượng dòng, một bơm tiêm đi qua vách hoặc một van tiêm và có thể được nối với một bơm điều khiển lưu lượng dòng dung dịch rửa giải. Một cách khác là mẫu có thể được tiêm vào trực tiếp trên bề mặt lớp gel hoặc dưới dung dịch rửa giải nếu như mẫu có tỷ trọng lớn hơn dung dịch rửa giải.
Đường ra của cột được nối với một detector có gắn với một máy ghi tự động để theo dõi nồng độ tương đối của các thành phần trong mẫu. Detector thường được thiết kế dựa trên các tính chất hấp thụ quang, khúc xạ ánh sáng hay phát quang. Bộ phận thu hứng phân đoạn tự động có thể được lắp trong trường hợp cần thiết. Vật liệu trong cột có thể là một chất mang mềm như gel nở hay một chất mang cứng cấu tạo từ thủy tinh, silic hoặc một hợp chất cao phân tử liên kết chéo tương thích dung môi. Chất mang cứng thưởng đòi hỏi hệ thống điều áp để tăng tốc độ phân tách. Pha động thường được chọn theo loại mẫu, môi trường phân tách và phương pháp phát hiện. Vật liệu nhồi cần được xử lý và được nạp vào cột như mô tả trong chuyên luận hoặc theo hướng dẫn của nhà sản xuất.
7.2 Hiệu năng
Hệ thống sắc ký phải thỏa mãn qui định về tính phù hợp của hệ thống được mô tả trong phần Các kỹ thuật tách sắc ký (Phụ lục 5). Việc điều chỉnh các thông số của hệ sắc ký có thể được thực hiện nhằm đáp ứng các yêu cầu về sự phù hợp của hệ thống cũng được trình bày trong phụ lục này.
7.3 Xác định tỷ lệ thành phần tương đối
Tiến hành phương pháp theo các điều kiện ghi trong chuyên luận riêng. Nếu có thể, theo dõi quá trình rửa giải một cách liên tục và ghi lại diễn tích của các pic tương ứng. Nếu mẫu được xác định dựa vào tính chất hóa lý mà tất cả các thành phần của mẫu đều cho một đáp ứng tương đương (ví dụ cùng có một hệ số hấp thụ riêng), thì lượng tương đối của mỗi thành phần có thể được xác định bằng cách tính tỷ lệ diện tích mỗi pic thu được trên tổng diện tích pic của những thành phần quan tâm. Nếu sự đáp ứng khác nhau, tính tỷ lệ thành phần tương đối bằng cách dựa vào đường chuẩn của các dung dịch chuẩn được ghi trong chuyên luận riêng hoặc bằng phương pháp khác được ghi trong chuyên luận riêng.
7.4 Xác định khối lượng phân tử
Thực hiện phương pháp với dung dịch thử và các dung dịch chuẩn theo quy trình ghi trong chuyên luận riêng. Xây dựng một đồ thị biểu thị sự phụ thuộc giữa thể tích lưu của các chất chuẩn dùng cho hiệu chuẩn và hàm logarit của khối lượng phân tử của chúng. Đường chuẩn thường xấp xỉ với một đường thẳng nằm giữa giới hạn loại trừ và giới hạn thấm tông thể. Khối lượng phân tử của thành phần quan tâm có thể được ước lượng từ đường chuẩn. Việc xây dựng đường chuẩn chỉ có giá trị đối với một hệ cụ thể trong những điều kiện thí nghiệm xác định.
7.5 Sự phân bố polymer theo kích thước phân tử
Sắc ký rây phân tử có thể được sử dụng để xác định sự phân bố các polymer theo kích thước phân tử. Tuy nhiên, việc so sánh mẫu sẽ chỉ có ý nghĩa nếu kết quả thu được là cùng một điều kiện thí nghiệm. Nguyên liệu sử dụng để xây dựng đường chuẩn và phương pháp xác định sự phân bố dựa theo kích thước phân tử của các polymer được ghi trong chuyên luận riêng.
7.6 Phân bố khối lượng phân tử trong dextran
Kiểm tra bằng phương pháp sắc ký rây phân tử.
Dung dịch thử: Hòa tan 0,200 g mẫu thử vào pha động và pha loãng tới 10 ml bằng pha động.
Dung dịch đánh dấu: Hòa tan 5 mg dextrose chuẩn và 2 mg chất đối chiếu hóa học dextran V trong 1 ml pha động.
Dung dịch hiệu chuẩn: Hòa tan riêng rẽ 15 mg các chất đối chiếu hóa học dextran 4, dextran 10 dùng cho hiệu chuẩn và 20 mg các chất đối chiếu hóa học dextran 40, dextran 70, dextran 250 dùng cho hiệu chuẩn trong 1 ml pha động. Dung dịch kiểm tra tính phù hợp của hệ thống:
Hòa tan 20 mg chất đối chiếu dextran 40 dùng cho chuẩn hiệu năng (đối với dextran 40) hoặc 20 mg dextran 60/70 dùng cho chuẩn hiệu năng (đối với dextran 60 và dextran 70) vào 1 ml pha động.
Điều kiện sắc ký: Cột (0,3 m × 10 mm) nhồi agarose loại liên kết chéo dùng trong sắc ký hoặc một dây các cột (0,3 m × 10 mm) nhồi gel polyether hydroxyl hóa dùng trong sắc ký.
Pha động: Dung địch chứa 7 g natri sulfat khan và 1 g clorobutanol trong 1 lít nước.
Tốc độ dòng: 0,5 ml/min đến 1 ml/min, giữ ổn định với sai số ± 1%/h.
Detector khúc xạ ánh sáng vi sai.
Buồng tiêm mẫu dung tích 100 µl đến 200 µl.
Duy trì hệ thống hoạt động ở nhiệt độ ổn định (+0,1°C).
7.7 Chuẩn hóa hệ thống sắc ký
Tiến hành tiêm lặp lại vài lần một thể tích nhất định dung dịch đánh dấu. Trên sắc ký đồ sẽ xuất hiện 2 pic, pic đầu tương ứng chất đối chiếu dextran V0 và pic thứ 2 là của dextrose. Từ thể tích rửa giải của pic tương ứng với dextran V0, tính thể tích trống V0 và từ pic tương ứng với dextrose, tỉnh được thể tích thấm tổng Vt.
Tiêm một thể tích nhất định các dung dịch chuẩn. Vẽ cẩn thận đường nền của mỗi sắc ký đồ. Phân chia mỗi sắc ký đồ thành p phần (ít nhất là 60) bằng những đường gạch thẳng dọc bằng nhau (tương ứng với những thể tích rửa giải). Trong mỗi phần, i tương ứng với một thể tích rửa giải V, đo chiều cao (2) của đường sắc ký đồ phía trên đường nền và tính hệ số phân bố K, theo công thức:
.png)
Trong đó:
V0 là thể tích trống của cột, được xác định bởi pic tương ứng với chất đối chiếu hóa học dextran V0 trong sắc ký đồ thu được từ dung dịch đánh dấu;
Vt là thể tích thấm tổng của cột, được xác định bởi pic tương ứng với dextrose trong sắc ký đồ thu được từ dung dịch đánh dấu;
Vi là thể tích rửa giải của phần i trong sắc ký đồ thu được với mỗi dung dịch chuẩn.
Tiến hành hiệu chuẩn sử dụng một trong những phương pháp dưới đây:
Vẽ đường cong chuẩn
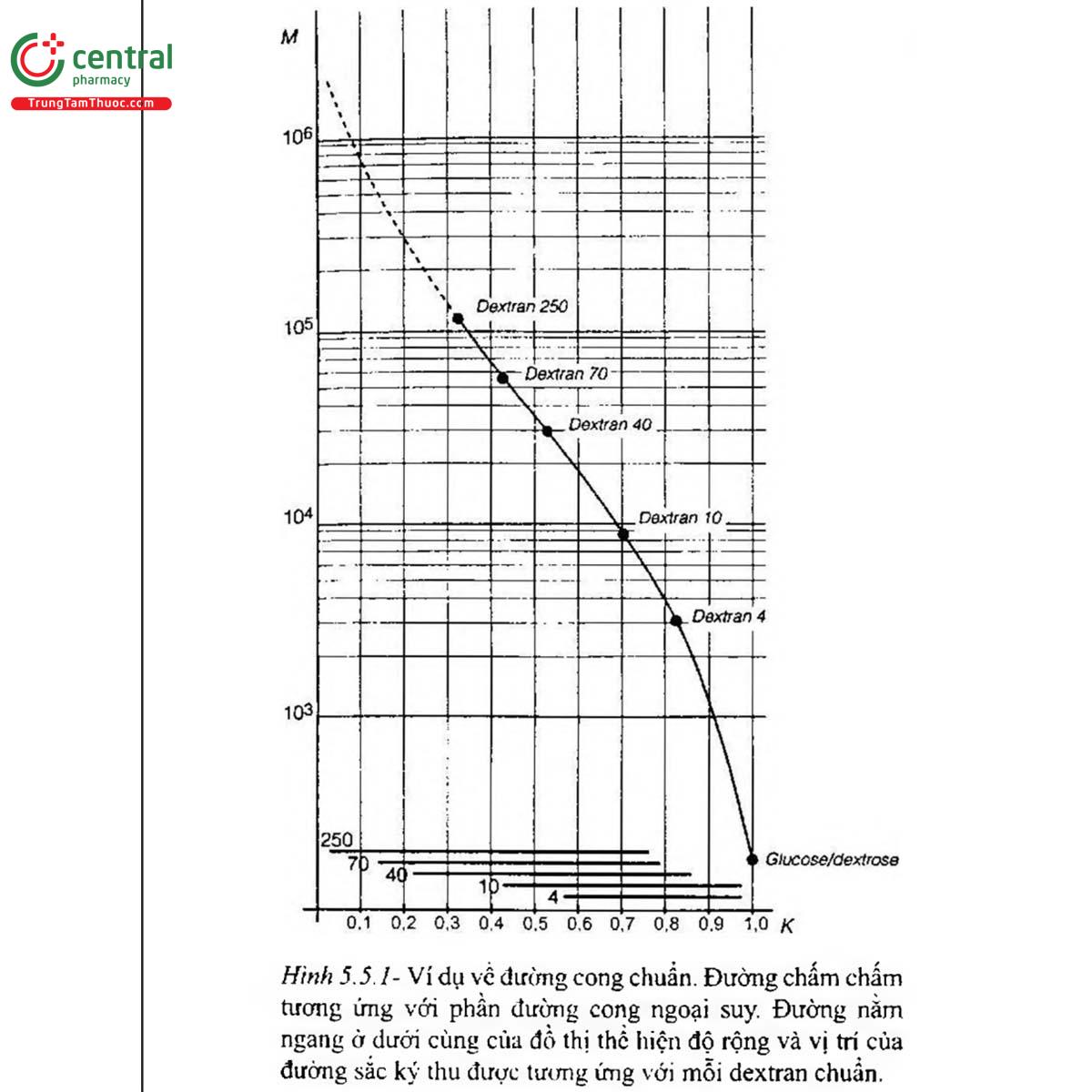
Với mỗi chất đối chiếu hóa học dextran dùng cho hiệu chuẩn, tính hệ số phân bố Kimat tương ứng với chiều cao cực đại của đường sắc ký, sử dụng công thức (1). Trên giấy kẻ ô bán logarit đặt các giá trị của Kmax (trục x) tương ứng với khối lượng phân tử ghi trên nhãn của mỗi chất dextran hiệu chuẩn và của dextrose; những giá trị này được lấy tại điểm cao nhất của đường sắc ký (Mmax). Vẽ đường cong chuẩn đầu tiên qua những điểm thu được, ngoại suy từ điểm K thu được với chất đối chiếu hóa học dextran 250 dùng cho hiệu chuẩn tới giá trị K thấp nhất thu được từ chất đối chiếu hóa học này (xeın Hình 5.5.1). Sử dụng đường cong chuẩn đầu tiên này, chuyển tất cả các giá trị K, ở mỗi sắc ký dồ sang khối lượng phân tử tương ứng M, để thu được sự phân bế khối lượng phân tử. Tính khối lượng phân từ trung bình M, cho mỗi loại dextran đổi chiều hóa học sử dụng phương trình (3) dưới đây. Nếu giá trị thu được đối với Mỹ, không khác hơn 5% so với giá trị công bố của mỗi dextran và mức khác biệt trung bình là ± 3%, đường cong chuẩn được chấp nhận. Nếu không đạt yêu cầu đó, chuyển dịch đường cong chuẩn dọc theo trục y và lặp lại tiến trình này cho tới khi các giá trị M thu được và giá trị công bố không khác nhau lớn hơn 5%.
Tỉnh qua đường cong chuẩn
Tính từ phương trình (2) và (3) dưới đây, sử dụng phương pháp thích hợp, các giá trị b1, b2, b3, b4 và b5 cho phép thu được giá trị Mw, nằm trong khoảng 5% của tất cả những giá trị công bố từ mỗi dextran chuẩn và khối lượng phân tử của dextrose nằm trong khoảng 180 ± 2.
.png) (2)
(2)
.png) (3)
(3)
Trong đó:
p là số phân đoạn chia trong sắc ký đồ;
yi là chiều cao của đường sắc ký phía trên đường nên trong phân đoạn i;
Mi là khối lượng phân từ trong phân đoạn i.
7.8 Tính phù hợp của hệ thống
Tiêm một thể tích nhất định dung dịch thử tỉnh phủ hợp hệ thống thích hợp.
7.9 Khối lượng phân tử trung bình của chất đối chiếu hóa học dextran dùng cho thử hiệu năng
Tính khối lượng phân tử trung bình Mw như đã trình bày trong phần hiệu chuẩn hệ sắc ký, sử dụng đường cong chuẩn hoặc các giá trị thu được ở trên đối với b₁, b2, b3, b4 b5. Phép thử chỉ có giá trị khi Mỹ nằm trong khoảng 41 000 đến 47 000 (chất đối chiếu hóa học dextran 40 dùng cho chuẩn hiệu năng) và 67 000 đến 75 000 (chất đối chiếu hóa học dextran 60/70 dùng cho chuẩn hiệu năng).
7.10 Khối lượng phân tử trung bình của dextran phân đoạn cao 10%
Tính Mw, đối với dextran phân đoạn cao 10% được rửa giải qua phần thứ n sử dụng công thức:
.png) (4)
(4)
Với n được xác định như sau:
.png) (5)
(5)
.png) (6)
(6)
Trong đó:
p là số phần chia trong sắc ký đồ;
yi là chiều cao đường sắc ký phía trên đường nền trong phần i;
Mi là khối lượng phân tử của phần i.
Phép thử chỉ có giá trị khi Mw của dextran phân đoạn cao nằm trong khoảng: 110 000 đến 130 000 (chất đối chiếu hóa học dextran 40 dùng cho hiệu chuẩn) và 190 000 dến 230 000 (chất đối chiếu hóa học dextran 60/70 dùng cho hiệu chuẩn).
7.11 Khối lượng phân tử trung bình của dextran phân đoạn thấp 10%
Tính Mw đối với dextran phân đoạn thấp 10% rửa giải trong và sau phân thứ m theo công thức sau:
.png) (7)
(7)
Trong đó:
m được xác định như sau:
.png) (8)
(8)
.png) (9)
(9)
p là số phần chia trong sắc ký đồ;
yi là chiều cao đường sắc ký phía trên đường nền trong phân i;
Mi là khối lượng phân tử của phần i.
Phép thử chỉ có giá trị khi Mw của dextran phân đoạn thấp 10% là: 6 000 đến 8500 (chất đối chiếu hóa học dextran 40 dùng cho chuẩn hiệu năng) và 7 000 đến 11 000 (chất đối chiếu hóa học dextran 60/70 dùng cho chuẩn hiệu năng).
7.12 Sự phân bố khối lượng phân tử của dextran được phân tích
Tiêm một thể tích nhất định dung dịch (1) và tính Mw, của phân bố tổng khối lượng phân tử, M của dextran phân đoạn cao 10 % và Mw của dextran phân đoạn thấp 10% như chỉ dẫn trong phần thừ tỉnh phù hợp của hệ thống.
Phương pháp lập như phương pháp Gauss - Newton cải tiến bởi Hartley là phù hợp (Xem O Hartley, Tecnometrics, 3 (1961) and G Nilsson and K Nilsson, J. Chromat. 101, 137 (1974)). Một chương trình đường cong thích hợp xử lý tương quan hồi quy không tuyến tính chạy trên máy tính điện tử có thể được sử dụng.
8 Phương pháp điện di
Điện di là hiện tượng liên quan đến sự di chuyển của các protein, các colloid, các phân tử, hay các tiêu phân tích điện hòa tan hoặc phân tán trong dung dịch điện giải khi có dòng điện đi qua.
Điện di được chia thành hai loại tùy theo thiết bị sử dụng: Điện di dung dịch tự do hay điện di với sự chuyển dịch của các lớp biên và điện di vùng.
Trong phương pháp điện di dung dịch tự do, dung dịch đệm của các protein trong một ống hình chữ U dưới tác dụng của dòng điện sẽ hình thành nên các lớp protein có linh độ giảm dần. Chỉ phần di chuyển nhanh nhất của protein sẽ tách rõ rệt khỏi các protein khác, kiểm tra sự dịch chuyển của các lớp biên bằng hệ thống quang học sẽ cung cấp các dữ liệu để tính toán linh độ điện di và các thông tin về mặt định tính và định lượng của thành phần hỗn hợp protein.
Trong điện di vùng, mẫu được đưa vào dưới dạng một dài hẹp hay điểm trong cột, trên tấm phẳng, hay trên một lớp phim chứa đệm. Sự di chuyển của các thành phần trong các dải hẹp cho phép tách hoàn toàn chúng. Có thể tránh sự chồng lấn giữa các dải hẹp do sự đối lưu nhiệt bằng cách đưa chất điện giải vào các nên (matrix) xốp như chất rắn dạng bột, hay nguyên liệu dạng sợi như giây, hay gel như tinh bột, agar hoặc polyacrylamid.
Các phương pháp điện di vùng có ứng dụng rộng rãi. Điện di gel, đặc biệt là điện đi đĩa được sử dụng để tách protein do khả năng cho độ phân giải cao.
Sự di chuyển điện di của các tiểu phân của một chất nhất định phụ thuộc vào tính chất của tiểu phân mà chủ yếu là điện tích, kích thước hay khối lượng phân tử và hình dạng của các tiêu phân cũng như các tính chất và các thông số thực nghiệm của hệ thống. Những thông số này bao gồm: pH, nông độ ion, độ nhớt và nhiệt độ của chất điện giải, mật độ hoặc độ liên kết chéo của các matrix nền như gel và điện thế áp đặt.
8.1 Ảnh hưởng của điện tích, kích thước tiểu phân, độ nhớt của chất điện giải và biến thiên điện thể
Các tiểu phân tích điện sẽ di chuyển về phía điện cực ngược dầu với chúng, sự di chuyển của các phân tử tích cả điện dương và điện âm phụ thuộc vào điện tích mạng. Tốc độ di chuyển tỷ lệ thuận với độ lớn của điện tích mạng trên tiêu phân và tỷ lệ nghịch với kích thước tiêu phân, mà kích thước tiểu phân lại có liên quan trực tiếp với phân tử lượng. Những tiểu phân hình câu lớn, khi định luật Stoke có giá trị, linh độ điện di µo sẽ tỷ lệ nghịch với bán kính của tiều phân theo phương trình:
.png)
Trong đó v là vận tốc của tiểu phân, E là thể đặt lên chất điện giải, Q là điện tích của tiêu phân, r là bán kính tiểu phân và n là độ nhớt của dung dịch chất điện giải. Phương trình này chỉ có giá trị giới hạn ở độ pha loãng nhất định và không có sự hiện diện của các nền như giấy hoặc gel. Các ion và peptid có trọng lượng phân tử lớn hơn 5000, đặc biệt khi có mặt môi trường nền, không tuân theo định luật Stoke và linh độ điện di của chúng được biểu thị bằng phương trình:
.png)
Trong đó A là thừa số hình dạng, thay đổi trong khoảng từ 4 - 6, biểu thị sự phụ thuộc tỷ lệ nghịch của linh độ điện di đối với bình phương bán kính tiều phân. Về mặt khối lượng phân tử, linh độ điện di sẽ tỷ lệ nghịch với căn bậc ba của bình phương khối lượng phân tử.
8.2 Ảnh hưởng của pH
Hướng và tốc độ di chuyển của phân tử có nhiều nhóm chức có thể bị ion hóa như acid amin và protein sẽ phụ thuộc vào pH của dung dịch chất điện giải. Ví dụ: Linh độ điện di của acid amin đơn giản như glycin sẽ thay đổi theo giá trị pH gần đúng như trong Hình 5.6.1.
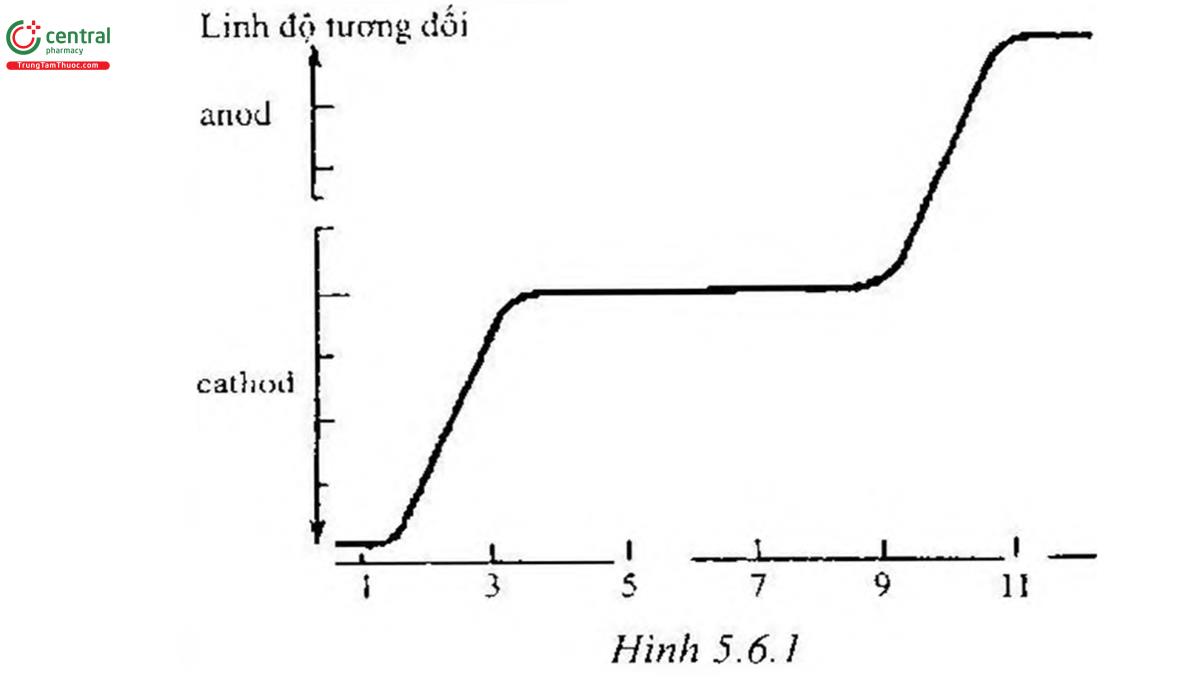
Giá trị pK, bằng 2,2 và 9,9 trùng với điểm uốn trên biểu đồ. Do nhóm chức bị ion hóa 50% ở giá trị pH = pKa, nên linh độ điện di ở những điểm này sẽ bằng 1/2 giá trị quan sát được khi cation và anion bị ion hóa hoàn toàn lần lượt ở pH rất thấp và pH rất cao. Ion lưỡng cực tồn tại ở khoảng pIi trung gian là những chất trung hòa về điện và có linh độ điện dì băng (0.
8.3 Ảnh hưởng của lực ion và nhiệt độ
Linh độ điện di sẽ giảm khi tăng lực ion của chất diện giải nền. Hoạt độ ion ụ được xác định theo phương trình:
.png)
Trong đó C là nồng độ ion (mol/l), Zi là hóa trị và tổng được tính với tất cả các ion trong dung dịch. Đối với dung dịch đệm có cả anion và cation hóa trị 1 thì lực ion được xác định bằng nồng độ mol.
Lực ion của chất điện giải dùng trong điện di nói chung nằm trong dãy từ khoảng 0,01 đến 0,10. Hoạt độ ion thích hợp phụ thuộc một phần vào thành phân của mẫu thử, do đó dung lượng đệm phải đủ lớn để duy trì pH hằng định trên diện tích của các dải hợp phần. Các dải hợp phần trở nên sắc nét hơn và hẹp hơn khi lực ion tăng.
Nhiệt độ ảnh hưởng gián tiếp lên linh độ, vì độ nhớt η của chất điện giải nền phụ thuộc vào nhiệt độ. Độ nhớt của nước sẽ giảm theo tỷ lệ khoảng 3%/ °C trong vùng từ 0 °C đến 5 °C và tỷ lệ giảm này sẽ thấp hơn khi ở nhiệt độ phòng. Bởi vậy, linh độ điện di sẽ tăng cùng với sự tăng nhiệt độ của chất điện giải.
Nhiệt giải phóng là đáng kể khi dòng điện chạy qua chất điện giải. Nhiệt này tăng cùng với sự tăng thể đặt và lực ion tăng. Ở các thiết bị lớn, cho dù có bộ phận làm lạnh, nhiệt giải phóng vẫn tạo nên sự biến thiên về nhiệt độ ở bể điện di, dẫn đến làm biến dạng các dải phân cách. Bởi vậy, cần quan tâm thiết kế các dụng cụ đặc biệt tính đến lực ion và thể đặt.
8.4 Ảnh hưởng của môi trường nền, dòng điện thẩm
Khi dòng điện chạy qua chất điện giải chứa trong ống thủy tinh hoặc chứa giữa các bản thủy tinh hoặc bàn plastic thì xuất hiện dòng chất điện giải hướng về phía đầu một điện cực, gọi là dòng điện thẩm. Dòng điện thẩm được hình thành do điện tích trên bề mặt của thành dụng cụ phát sinh do quá trình ion hóa các nhóm chức trong vật liệu hay do các ion hấp phụ trên thành buồng điện di chứa các chất điện giải. Hiệu ứng này thường tăng khi buồng điện di chứa các chất xốp như gel, được sử dụng để làm ổn định cho chất điện giải nền và đề phòng hiện tượng xáo trộn các dải phân tách do sự đối lưu nhiệt và hiện tượng khuếch tán. Dung dịch ngay sát trên bề mặt sẽ hình thành điện tích bằng nhưng ngược dầu với điện tích trên bề mặt và điện trường đi qua buồng điện di sẽ tạo nên sự chuyển động của dung dịch về phía điện cực ngược dấu. Các chất thường được sử dụng làm môi trường nền trong điện di vùng sẽ tạo điện tích âm trên bề mặt, dòng điện thẩm của chất điện giải sẽ di chuyển về phía cathod. Vì vậy tất cả các vùng, bao gồm cả các chất trung tính sẽ di chuyển về phía cathod trong quá trình điện di. Mức độ thẩm thấu sẽ thay đổi khi các chất nền thay đổi. Độ thẩm thấu thay đổi đáng kể đối với gel agar và thay đối không đáng kể đối với gel polyacrylamid.
8.5 Sự rây phân tử
Khi không có sự hiện diện của môi trường nền hay trong trường hợp môi trường rất xốp thì sự tách điện di của các phân tử là do sự khác nhau về tỷ lệ của điện tích với kích thước phân tử. Nếu có sự hiện diện của chất nền, sự khác nhau về khả năng hấp phụ hay ái lực của phân từ đối với môi trường tạo nên hiệu ứng sắc ký có thể làm tăng hiệu quả tách.
Hiệu ứng rây phân từ sẽ xuất hiện nếu môi trường nền là các loại gel có sự phân nhánh nhiều đến mức tạo thành các lỗ xốp để tách các phân tử theo kích thước. Hiệu ứng này tương đương hiệu ứng thu được trong quá trình tách thẩm thấu gel hay sắc ký rây phân tử, nhưng trong điện di gel hiệu ứng này chồng lên quá trình tách điện di. Có thể nhận thấy sự rây phân từ do cản trở không gian đối với sự di chuyển của các phân tử lớn. Các phân từ nhỏ di chuyển qua các lỗ xốp có kích thước lớn, nên sự điện di qua gel không bị cản trở. Khi kích thước phân tử tăng, một số ít hơn các lỗ xốp cho phép các phân từ đi qua, làm chậm sự di chuyển của các phân tử có trọng lượng phân tử lớn.
8.6 Điện di gel
Quá trình sử dụng một gel như agar (thạch), tinh bột hay polyacrylamid làm môi trường nên được hiểu theo nghĩa rộng là điện di gel. Phương pháp này đặc biệt thuận lợi cho sự tách các protein. Sự tách này đạt được tùy thuộc vào tỷ lệ điện tích đối với kích thước phân tử đi đôi với hiệu ứng rây phân từ phụ thuộc chủ yếu vào khối lượng phân tử.
Gel polyacrylamid được sử dụng nhiều do có một số thuận lợi. Nó có đặc tính ít hấp phụ và tạo nên hiệu ứng dòng điện thẩm không đáng kể. Các gel với dải rộng các lỗ xốp có kích thước khác nhau có thể được điều chế bằng cách thay đổi nồng độ gel tổng cộng (dựa trên monomer kết hợp với các yếu tố tạo mạch nhánh) và phần trăm của chất tạo mạch nhánh dùng để tạo gel. Lượng các chất được biểu thị bằng phương trình sau:
.png)
.png)
Trong đó T là nồng độ gel tổng cộng (%), C là phần trăm tác nhân tạo mạch nhánh dùng để tạo gel, V là thể tích (mL) của đệm dùng điều chế gel, a và b là khối lượng (g) của monomer (acrylamid) và tác nhân tạo mạch nhánh (thường dùng N,N'-methylenbisacrylamid) dùng diều chế gel. Các gel thích hợp có nồng độ trong khoảng 3% - 30%. Tổng tác nhân tạo mạch nhánh thường chiếm khoảng 1/10 đến 1/20 lượng monomer (C = tửừ 10% đến 5%), tỷ lệ phần trăm nhỏ hơn được dùng cho giá trị cao hơn của T.
Trong quá trình điều chế gel, bể của dụng cụ điện di chứa dung dịch nước của monomer và tác nhân tạo mạch nhánh, thường được cân bằng bằng dung dịch đệm đến pH mong muốn trong những lần chạy cuối và được polymer hóa tại chỗ bằng quá trình gốc tự do. Quá trình polymer hóa được kích hoạt bởi quá trình hóa học, thông thường sử dụng amoni persulfat kết hợp với N,N,N',N'- tetramethylendiamin hay quang hóa hỗn hợp Riboflavin và N,N,N',N'-tetramethylendiamin. Quá trình polymer hóa bị cản trở bởi các phân tử oxy và môi trường acid. Lựa chọn thành phần của gel và điều kiện polymer hóa phải bảo đảm chất lượng của gel.
8.7 Thiết bị cho điện di gel
Nói chung bể hay môi trường để thực hiện quá trình điện di có thể được đặt theo phương thẳng đứng hay nằm ngang tùy theo thiết kế của thiết bị. Để so sánh sự tách có thể thực hiện trong một số ống riêng biệt hay đưa các mẫu khác nhau vào các hố kề bên nhau vào khuôn hay cắt vào phiến của gel. Phiến gel thẳng đứng như mô tả trong Hình 5.6.2 thuận lợi cho sự so sánh trực tiếp một số mẫu.
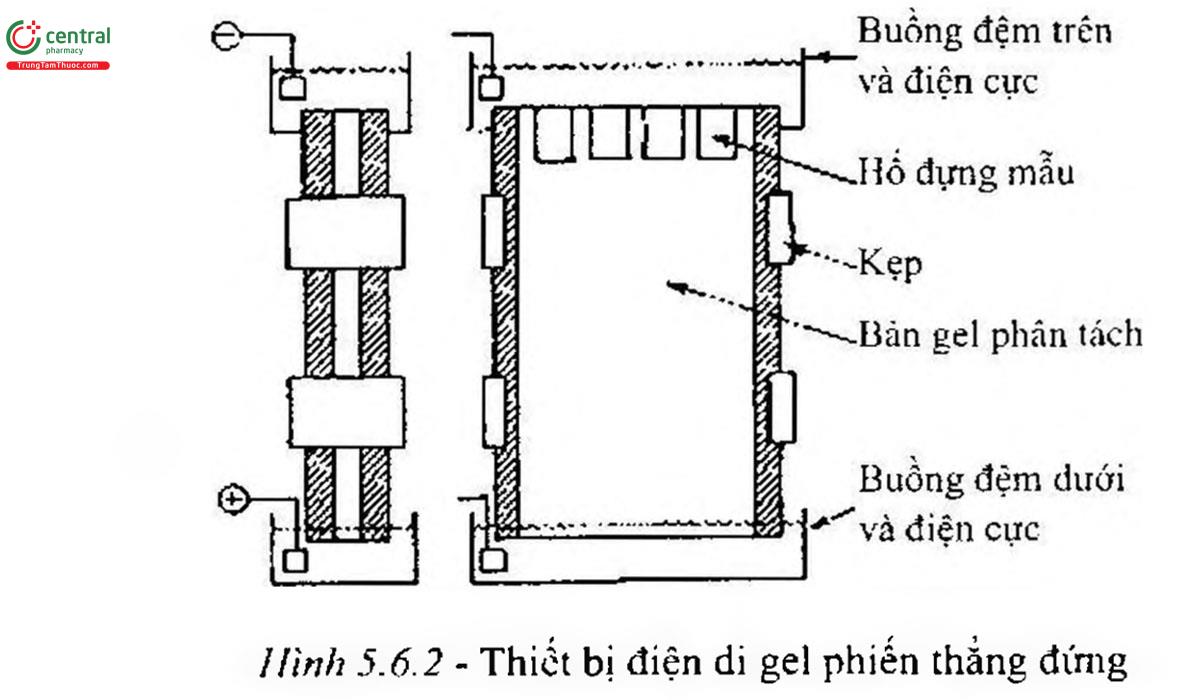
Tốt nhất là sự so sánh các mẫu trong cùng một bản gel, như vậy sẽ đồng nhất hơn về mặt thành phần so với các khuôn gel trong nhiều bề điện di.
Đặc tính của nhiều loại thiết bị là phải hàn kín buồng đệm phía dưới với chân đế của bể điện di, cho phép mức đệm trong buồng đệm phía dưới bằng mức đệm trong buồng đệm phía trên để loại trừ áp suất thùy tĩnh trên gel. Ngoài ra có một vài bộ phận tuần hoàn làm lạnh cả hai mặt bể điện di gel.
Để điều chế gel, buồng gel được đậy bằng nắp thích hợp có chứa dung dịch monomer, tác nhân tạo mạch nhánh và chất xúc tác. Một cái lược có răng với kích thước thích hợp được đặt lên phía trên và cho phép quá trình polymer hóa xảy ra hoàn toàn. Sau khi lấy lược ra sẽ tạo thành các hố trên bản gel được polymer hóa.
Trong điện di gel đơn giản, chỉ sử dụng một dung dịch đệm cho vào buồng đệm phía trên và phía dưới giống nhau. Sau khi cho dung dịch đệm vào buồng đệm, mẫu được hòa tan trong nước đường hay dung dịch đặc và hơi nhớt khác để đề phòng sự khuếch tán. Sau đó mẫu được đưa vào đáy các hồ dựng mẫu bằng bơm tiêm hay micropipet và bắt đầu thực hiện quá trình điện di.
8.8 Điện di đĩa
Điện di gel polyacrylamid sử dụng một dãy không liên tục các đệm và cũng thường sử dụng nhiều lớp gel không liên tục, được gọi là điện di đĩa. Tên của phương pháp xuất phát từ dạng hình dạng đĩa của các dải hẹp được tạo thành. Do tạo thành các dải hẹp, nên kỹ thuật này có độ phân giải đặc biệt cao và thường được sử dụng trong phân tích đặc tinh của hỗn hợp protein và phát hiện tạp chất mà có thể có linh độ gần thành phần chính.
Cơ sở của điện di đĩa được trình bày trong phần sau có liên quan đến các hệ anion thích hợp cho việc phân tách protein mang điện tích âm. Để hiểu được điện di đĩa cần phải có kiến thức chung về điện di và dụng cụ đã được mô tả.
8.9 Cơ sở của điện di đĩa
Độ phân giải cao thu được trong điện di đĩa phụ thuộc vào việc sử dụng hệ đệm không liên tục về pH và thành phần. Thường phối hợp hai hoặc ba gel khác nhau về tỷ trọng. Hệ thống điển hình được mô tả trong Hình 5.6.3.
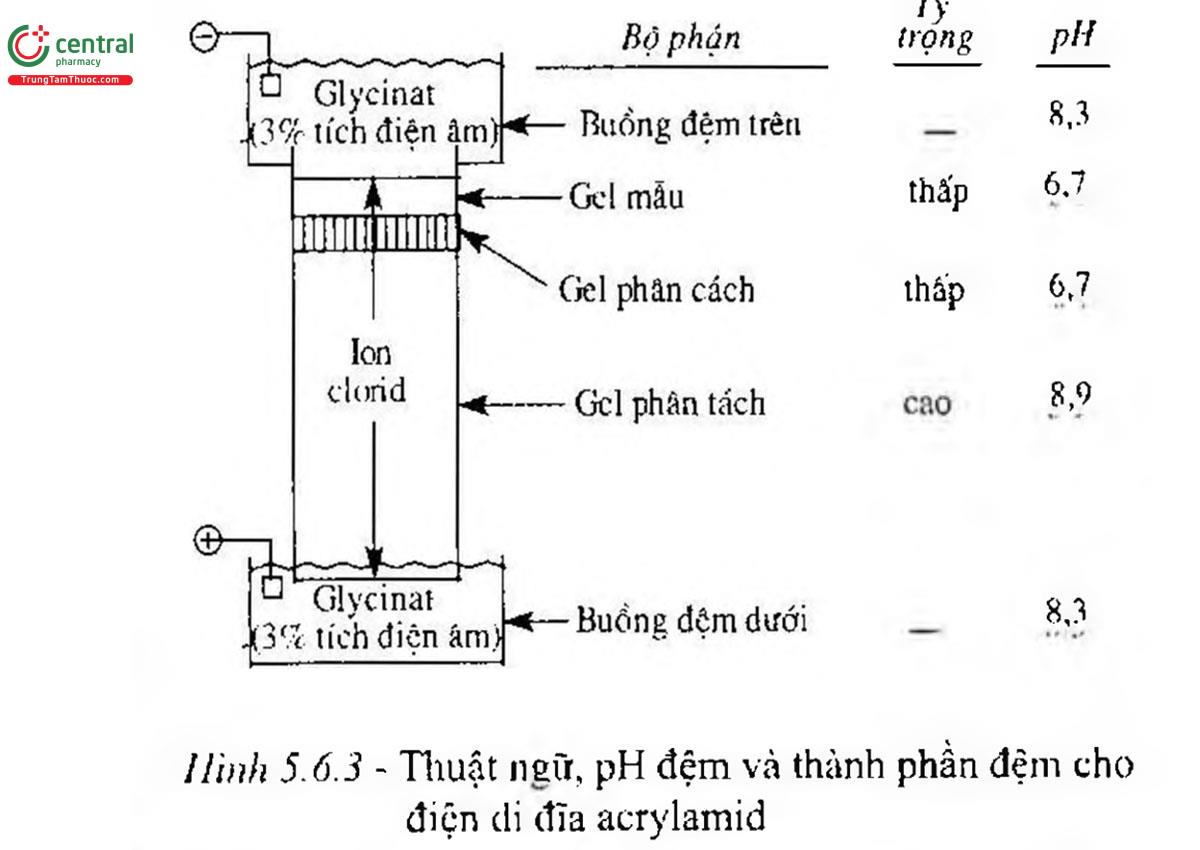
Gel phân tách có chiều cao vài cm với tỷ trọng cao (T = 10% - 30%) được polymer hóa trong đệm tris-clorid trong bể của thiết bị. Trong quá trình polymer hóa đệm được phủ lên một lớp nước mỏng để đề phòng hiện tượng tạo thành mặt khum trên bề mặt của gel. Lớp nước phủ lên sau đó được loại đi, lớp gel mỏng tỷ trọng thấp (T = 3%), có bề dày 3 mm đến 10 mm được gọi là khoảng trống hay gel phân cách, được polymer hóa trong đệm tris-clorid trên mặt của gel phân tách. Lớp nước phủ phía trên lại tiếp tục được sử dụng để tạo mặt phẳng. Mẫu được trộn với một lượng nhỏ dung dịch monomer dùng để tạo gel phân cách, đổ lên mặt của gel phân cách và được polymer hóa. pH của gel phân tách thường là 8,9, trong khi đó pII của gel phân cách và gel chứa mẫu là 6,7. Tất cả ba loại gel này được điều chế dùng clorid làm anion.
Dung dịch đệm chứa trong buồng chứa đệm phía trên và phía dưới có pH là 8,3 và được điều chế từ tris và glycin. Ở pH này khoảng 3% phân tử glycin mang điện tích âm. Khi đặt điện thế lên hệ thống, lớp tiếp giáp glycinat-clorid sẽ di chuyển theo hướng đi xuống và về phía anod. Lớp tiếp giáp bắt đầu ở vị trí lớp tiếp xúc của buồng chứa đệm phía trên và đỉnh của lớp gel chứa mẫu. Tại đây ion clorid do có kích thước nhỏ nên sẽ di chuyển nhanh hơn bất kỳ protein nào hiện diện trong mẫu. pH của lớp gel mẫu và lớp gel phân cách được chọn phải thấp hơn giá trị pKa cao của glycin khoảng 3 đơn vị. Do vậy, khi băng qua các lớp gel này, chỉ có khoảng (0,1% phân tử glycin tích điện âm. Cho nên, glycin sẽ di chuyển chậm hơn clorid. Khuynh hướng dịch chuyển nhanh hơn của clorid khỏi glycinat làm giảm nồng độ nơi tiếp giáp, tạo nên sự giảm thế nhiều hơn ở lớp tiếp giáp, điều này làm cho glycinat bắt kịp ion clorid. Trong điều kiện này, lớp tiếp giáp rất hẹp được duy trì, và khi đó nó di chuyển qua lớp gel mẫu thử và lớp gel phân cách, các protein trong mẫu thử ở lớp tiếp giáp sắp xếp thành lớp rất mỏng theo thứ tự về linh độ. Quá trình này là nguồn gốc của việc các đĩa được phân tách. Các protein được sắp xếp theo trình tự khi tiếp xúc với gel phân tách tỷ trọng cao, chúng sẽ di chuyển chậm lại do quá trình rây phân từ. pH cao hơn trong gel phân tách làm cho glycinat di chuyển nhanh hơn, đến mức độ làm cho lớp tiếp xúc của các đệm không liên tục sẽ vượt qua các protein và cuối cùng sẽ tiếp xúc với đáy của gel phân tách. Trong chu trình này, các đĩa protein tiếp tục phân tách bằng quá trình điện di và quá trình rây phân tử trong gel phân tách. Kết thúc quá trình tách, pH của gel phân tách sẽ tăng từ giá trị ban đầu là 8,9 lên khoảng pH 9,5.
8.10 Linh độ tương đối
Bromophenol xanh thường được sử dụng như là một chuẩn để tính toán linh độ tương đối của các dải phân tách và để quan sát các quá trình tách. Nó có thể được thêm vào trong hồ đựng mẫu hoặc trộn lẫn với mẫu, hoặc đơn giản được thêm vào dung dịch đệm ở buồng chứa đệm phía trên. Lình độ tương đối Mb được tính toán như sau:
.png)
Trong đó:
a là khoảng cách từ mốc xuất phát đến vùng mẫu và b là khoảng cách từ mốc xuất phát đến vùng bromophenol xanh.
8.11 Quan sát các vùng phân tách
Do polyacrylamid trong suốt, nên các dải protein có thể được quan sát bằng đo mật độ quang với ánh sáng UV. Các vùng có thể cố định bằng cách nhúng vào các dung dịch làm tủa protein như acid phosphotungstic hoặc acid tricloracetic 10%. Các thuốc thử hiện màu được sử dụng bao gồm naphthalen đen (amido đen) và Coomassie lam sáng R250. Những vùng được cố định hay có màu có thể được quan sát một cách thuận lợi và được chụp ảnh với ánh sáng truyền qua từ nguồn phát tia X.
8.12 Những điều an toàn cần chú ý
Thế sử dụng trong điện di có thể gây sốc chết người. Nguy cơ này sẽ tăng do sử dụng dung dịch đệm nước và điều kiện môi trường làm việc ẩm ướt.
Bộ phận cung cấp nguồn của thiết bị cần được bao lại trong các lồng kim loại có dây nối đất hoặc cần được chế tạo bằng các vật liệu cách điện, các lồng kim loại này cần có chốt tự cắt nguồn khi mở nắp thiết bị.
Vì sự nguy hiểm của thế cao áp, nhân viên phòng thí nghiệm cần làm quen với thiết bị trước khi sử dụng chúng.
9 Phương pháp điện di mao quản
Điện di là hiện tượng di chuyển của tiều phân tích điện hòa tan hay phân tán trong chất điện giải khi có dòng điện đi qua. Cation di chuyển về phía cực âm (cathod), anion di chuyên về phía cực dương (anod). Các phần tử không tích điện không bị hút về phía hai điện cực.
Trong phương pháp điện di mao quản (CE) việc sử dụng mao quản để làm kênh di chuyển cho phép thực hiện quá trình tách điện di trên một thiết bị có thể so sánh với thiết bị của sắc ký lỏng hiệu năng cao. Tuy nhiên, vẫn còn những khác biệt rõ rệt về cách vận hành, những điểm thuận lợi và không thuận lợi so với sắc ký lỏng hiệu năng cao. Quá trình vận hành của CE điển hình với mao quản mà mặt trong thành mao quản không có lớp bao và mao quản chứa dung dịch “đệm làm việc”, thì nhóm silanol hiện diện trên thành phía trong của mao quản thủy tinh sẽ giải phóng ion hydrogen vào dung dịch đệm và bề mặt thành mao quản sẽ tích điện âm ngay cả ở pH rất thấp. Cation hay các chất hòa tan tích điện dương một phần trong môi trường bị hút tĩnh điện vào thành mao quản tích điện âm tạo nên một lớp điện tích kép. Quá trình điện di bắt đầu bằng cách đặt thế trên chiều dài cột mao quản làm cho phần dung dịch của lớp điện tích kép di chuyển về phía đầu cathod của mao quản kéo theo khối dung dịch. Sự chuyển động của khối dung dịch dưới tác dụng của lực điện trường được gọi là dòng điện thầm (electroosmotic flow - EOF). Mức độ ion hóa của nhóm silanol trên thành mao quản phụ thuộc chủ yếu vào pH của dung dịch đệm làm việc và các chất điều chỉnh được thêm vào chất điện giải. Ở pH thấp, nhóm silanol nói chung có độ ion hóa thấp và dòng EOF nhỏ. Ở pH cao hơn, nhóm silanol bị ion hóa nhiều hơn và dòng EOF tăng. Trong một số trường hợp, các dung môi hữu cơ như methanol hay acetonitril được cho thêm vào dung dịch đệm để làm tăng độ tan của các chất hòa tan và các chất phụ gia hay để ảnh hưởng đến mức độ ion hóa của mẫu. Nói chung, việc thêm các chất điều chỉnh hữu cơ sẽ làm giảm dòng EOF. Detector được đặt về phía đầu cathod của mao quản. Dòng EOF thường lớn hơn linh độ điện di. Do vậy, ngay cả anion cũng bị đẩy về phía cathod và detector. Khi sử dụng đệm phosphat pH 7,0 ở mao quản không có lớp bao, thông thường trình tự xuất hiện các chất tan trong điện di đồ là các cation, các chất trung tính và các anion.
Hiện nay, có 5 loại chủ yếu của điện di mao quản:
Điện di mao quản vùng (capillary zone electrophoresis CZE) còn gọi là điện di dung dịch tự do hay điện di mao quản dòng tự do. Sắc ký mixen điện động, còn gọi là sắc ký điện động mixen (micellar electrokinetic chromatography - MEКС). Diện di mao quản gel (capillary gel electrophoresis - CGE). Điện di mao quản hội tụ đăng điện (capillary isoelectric focusing - CIEF)
Điện di mao quản đẳng tốc (capillary isotachophoresis - CITP). Trong điện di mao quản vùng, quá trình tách được kiểm soát bằng sự khác nhau về linh độ tương đối của từng thành phần trong mẫu thử hoặc dung dịch thử. Linh độ là hàm số của điện tích chất phân tích và kích thước trong điều kiện nhất dịnh của phương pháp. Chúng được tối ưu hóa bằng cách kiểm soát các thành phần của đệm, pH và lực ion.
Trong sắc ký mixen điện động, các chất hoạt động bề mặt được thêm vào dung dịch đệm làm việc ở nồng độ lớn hơn nồng độ mixen tới hạn. Các chất phân tích có thể phân bố trong pha tĩnh giả do mixen tạo thành. Kỹ thuật này thường được ứng dụng để tách các chất trung tính và các ion.
Trong điện di mao quản gel, tương tự như lọc gel, sử dụng các mao quản chứa gel để tách các phân tử, dựa trên cơ sở sự khác nhau tương đối về khối lượng phân tử hay kích thước phân tử. Nó được dùng chủ yếu để tách các protein, peptid và các oligomer. Các gel có ưu điểm là làm giảm dòng EOF và đồng thời làm giảm một cách đáng kể sự hấp phụ protein trên thành phía trong của mao quản, do đó làm giảm đáng kể hiệu ứng bất đối của pic.
Trong điện di mao quản hội tụ đẳng điện, các chất được tách trên cơ sở sự khác nhau tương đối về điểm đẳng điện. Nó được thực hiện bằng cách biến đổi pH đệm để thu được các vùng mẫu thử ở trạng thái bền (pH thấp ở anod và pH cao ở cathod). Quá trình biến đổi được xác lập bằng cách đặt thế vào mao quản chứa hỗn hợp thành phần của các chất mang bao gồm các chất lưỡng cực có giá trị pl khác nhau.
Trong điện di mao quản đẳng tốc sử dụng hai đệm bao quanh các vùng chất phân tích. Cả anion và cation có thể tách thành những vùng rõ rệt. Ngoài ra, nồng độ chất phân tích như nhau trong mỗi vùng. Như vậy, chiều dài của mỗi vùng sẽ tỷ lệ thuận với lượng chất phân tích. Hai kỹ thuật điện di mao quản thường được sử dụng nhiều nhất là điện di mao quản vùng và sắc ký mixen điện động. Chúng được đề cập một cách tóm tắt trong các phân sau.
9.1 Nguyên lý của điện di mao quản vùng
Điện di mao quản vùng sử dụng nguyên lý của điện di và điện thẩm để tách các tiểu phân tích điện.
Linh độ điện đi của ion (up), được biểu diễn bằng phương trình:
.png)
Trong đó q là điện tích của ion, η là độ nhớt dung dịch và r là bán kính của ion hydrat hóa. Từ mối liên hệ này suy ra, chất phân tích kích thước nhỏ, điện tích lớn có linh độ lớn. Chất phân tích kích thước lớn, điện tích nhỏ có linh độ thấp.
Tốc độ di chuyển (Vip), tính bằng cm/s, được biểu thị bằng phương trình:
.png)
Trong đó µEP là lĩnh độ điện di, V là điện thế đặt và L là chiều dài (cm) tổng cộng của mao quản.
Tốc độ của EOF (V10), tính bằng cm/s, được biểu diễn bằng phương trình:
.png)
Trong đó µeo là linh độ của EOF (hệ số của dòng EOF) và các ký hiệu khác được định nghĩa như trên.
Thời gian (t), tính bằng giây, cần thiết cho chất tan di chuyển trên toàn bộ chiều dài hiệu dụng (1) của mao quản (từ đầu vào đến detector), t được biểu thị bằng hệ thức sau:
.png)
Trong đó E là cường độ điện trường và các ký hiệu khác được định nghĩa như ở trên.
Hiệu lực của hệ thống điện di có thể liên quan đến linh độ, dòng EOF và được biểu thị bằng số đĩa lý thuyết (N), được tính bằng phương trình:
.png)
Trong đó D là hệ số khuếch tán của chất hòa tan và các ký hiệu khác được định nghĩa như trên.
Độ phân giải (R) của hai chất hòa tan được rùa giải kế tiếp nhau, có thể xác định bằng phương trình:
.png)
Trong đó: μEP1 νὰ μEP2, là lĩnh độ của hai chất hòa tan,
μ_EP là linh độ trung bình của hai chất tan và các ký hiệu khác được định nghĩa như trên.
9.2 Nguyên lý của sắc ký mixen điện động
Trong MEKC, môi trường chất điện giải nền có chứa chất hoạt động bề mặt ở nồng độ cao hơn nồng độ mixen tới hạn (CMC). Trong môi trường nước, các chất hoạt động bề mặt tự ngưng kết và hình thành mixen gồm nhóm có đầu thân mước tạo nên một lớp áo bên ngoài và nhóm có đuôi không thân nước tạo nhân không phân cực ở bên trong mixen để cho các chất tan có thể phân bố. Nói chung, các mixen có những anion trên bề mặt ngoài, dưới tác dụng của điện thế áp đặt chúng di chuyển theo hướng ngược lại so với dòng EOF. Kiểu phân bố này tương tự với phân bố trong chiết xuất với dung môi hay trong sắc ký lỏng hiệu năng cao pha đảo. Sự phân bố khác nhau của các phân tử trung tính vào pha động nước và pha "tĩnh giả" mixen là cơ sơ duy nhất cho quá trình tách. Dung dịch đệm và các mixen tạo thành hệ thống hai pha, chất tan có thể phân bố giữa hai pha này.
Hệ thống mixen thích hợp cho MEKC phải đáp ứng các tiêu chuẩn sau: Chất hoạt động bề mặt tan tốt trong đệm và dung dịch mixen đồng nhất và trong suốt đối với detector UV. Chất hoạt động bề mặt phổ biến nhất cho MEKC là natri dodecyl sulfat (chất hoạt động bề mặt anion). Những chất hoạt động khác bao gồm cetyltrimethylamoni bromid (chất hoạt động bề mặt cation) và các muối mật (chất hoạt động bề mặt chiral). Độ chọn lọc của hệ thống MEKC chủ yếu tùy thuộc vào bản chất của chất hoạt động bề mặt.
Dung môi hữu cơ thường thêm vào trong đệm MEKC để điều chỉnh hệ số dung lượng, tương tự như trong tách bằng sắc ký lỏng pha đảo. MEKC có thể sử dụng để tách các đồng phân đối quang. Để tách các đồng phân, trong dung dịch đệm được thêm vào các chất phụ gia chiral hoặc chất hoạt động bề mặt chiral như muối mật. Kiến thức chung về sắc ký cột cổ điển sẽ hỗ trợ cho sự hiểu biết nguyên lý MEKC. Tuy vậy, trong MFKC, các mixen không thuần túy là pha tĩnh. Bởi vậy, lý thuyết sắc ký cột cần thiết phải được điều chỉnh. Sự điều chỉnh cơ bàn đối với nguyên lí của MEKC là bản chất xác định của cửa số tách đối với các phân từ trung tính. Thời gian lưu (tr) đối với các chất trung tính được biểu diễn bằng phương trình sau:
.png)
Trong đó, tỷ là thời gian yêu cầu đối với chất không lưu giữ đi qua chiều dài hiệu dụng của cột mao quản, tức là thời gian cần để mixen đi qua mao quản, k' là hệ số dung lượng và từ luôn luôn ở giữa giá trị t0 và tMC. Hệ số dung lượng (k') đối với các chất trung tính được tính theo phương trình:
.png)
Trong đó các ký hiệu được định nghĩa như trên.
Để áp dụng cho mục đích thực tiễn, k' được tính bằng phương trình:
.png)
Trong đó tỷ là thời gian được đo từ thời điểm đặt thế (hoặc điểm bắt đầu tiêm mẫu) đến thời điểm ứng với đỉnh pic tối đa, to được do từ điểm đặt thế (hoặc điểm bắt đầu tiêm mẫu) đến điểm biên phía trước của pic dung môi hay đến tín hiệu của chất không lưu giữ. k' trong MEKC có ý nghĩa nhất định và là đặc trưng của một chất tan nhất định trong hệ MEKC. Những bàn luận khác của k' được trình bày trong phần tính phù hợp hệ thống trong mục các thông số làm việc.
Độ phân giải (R) đối với các chất trung tính được tính bằng phương trình:
.png)
Trong đó a là độ chọn lọc, bằng tỷ số của k'₂ đối với k trong điều kiện cụ thể cho việc tách hai chất tan. Nếu hai chất tan rửa giải gần nhau (a ≤1,1), có thể dùng một trong hai trị giá k'. Phương trình chứng tỏ rằng, cũng như với sắc ký kinh điển, độ phân giải trong MEKC có thể được cải thiện qua việc kiểm soát hiệu lực của hệ thống, độ chọn lọc, sự lưu giữ và bản chất hóa học của các chất hoạt động bề mặt. Hàng từ cuối cùng của phương trình chính là khoảng rửa giải giới hạn. Mặc dầu MEKC đặc biệt hữu hiệu trong tách các chất trung tính, kỹ thuật này cũng có thể được áp dụng cho việc tách các chất tan tích điện. Qui trình sau đây liên quan đến sự phối hợp cơ chế tách giữa sắc ký và điện di. Tương tác giữa chất tan tích điện và mixen có thể được sử dụng để tối ưu hóa sự tách. Cập ion có thể hình thành nếu như điện tích trên chất hoạt động bề mặt và chất tan là trái dấu nhau. Trong trường hợp ngược lại, chất hoạt động bề mặt và chất tan đẩy nhau. Sự khác biệt này có thể ảnh hưởng có ý nghĩa đến sự tách của các phân từ tích điện.
9.3 Các điều chú ý đối với thiết bị
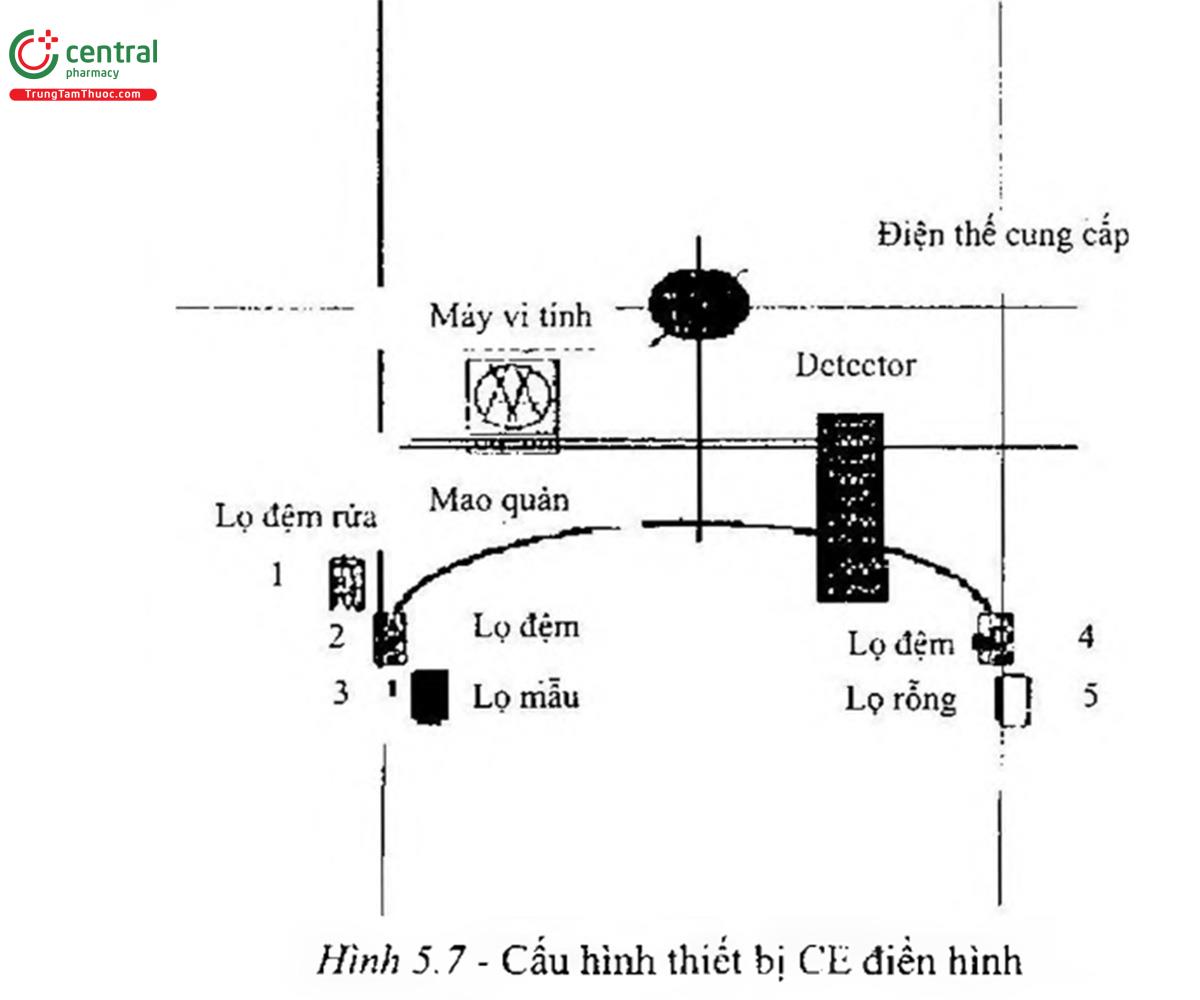
Hệ thống CE điển hình (Hình 5.7) bao gồm một mao quản bằng silica nung chảy có đường kính trong từ 50 µm đến 100 µm và chiều dài từ 20 cm đến 100 cm. Các đầu mao quản được nhúng vào các bình điện giải riêng biệt. Nguồn cung cấp điện một chiều có khả năng tạo điện áp cao từ 0 kV đến 30 kV. Thêm vào đó một detector, bộ phận tiêm mẫu tự động và thiết bị ghi dữ liệu là đủ một hệ thiết bị CE. Hệ thống cung cấp dung dịch đệm tự động và hệ thống kiểm soát bằng máy vi tính, ghi nhận dữ liệu hay kiểm soát nhiệt độ cho cả mao quản và bộ phận tiêm mẫu tự động có thể thấy ở các thiết bị có mặt trên thị trường. Những điều cần quan tâm đầu tiên đối với thiết bị là kiểu mao quản, cấu hình, cách tiêm mẫu, nguồn cung cấp điện và kiểu detector.
9.4 Các loại mao quản và cấu hình thiết bị
Mao quản dùng trong CZE thường được làm bằng silica nung chảy và không có lớp bao mặt trong mao quản. Một vài thiết bị có cấu hình với cột mao quản để tự do, nghĩa là mao quản không đưa vào bên trong hộp chứa. Trong hầu hết các thiết bị trên thị trường, mao quản được đặt vào trong một hộp chứa. Cả hai cấu hình đều có những ưu và nhược điểm riêng. Điều quan trọng là khả năng của thiết bị có thể tương thích được các loại mao quản khác nhau với chiều dài và đường kính mao quản khác nhau. Mao quản với chất bao mặt trong khác nhau hiện nay cũng có mặt trên thị trường. Bởi vậy, khả năng tương thích với các loại cột khác nhau rất quan trọng. Các chất bao mặt trong mao quản có thể được sử dụng để thay đổi cường độ hay hướng của dòng EOF hay làm giảm sự hấp phụ của mẫu. Nếu sử dụng mao quản có chất bao mặt trong, phải có ghi các chi tiết về chất bao và nhà cung cấp trong phương pháp. Mao quản từ nhà cung cấp khác cũng có thể được sử dụng nếu chúng thích hợp.
9.5 Kỹ thuật đưa mẫu và tiêm mẫu
Cách đưa mẫu vào trong mao quản bao gồm tiêm kiểu di chuyển điện (kiểu điện động) và tiêm áp suất âm và tiêm áp suất dương (kiểu thủy tĩnh).
Để tiêm kiểu di chuyển điện, dung dịch mẫu được đưa vào mao quản bằng cách nhúng mao quản và điện cực vào trong lọ mẫu và đặt lên đó một điện thể cao trong thời gian ngắn. Mẫu đi vào mao quản bằng sự phối hợp của điện di và dòng EOF. Bởi vậy, các chất phân tích có linh độ khác nhau đi vào trong mao quản ở mức độ khác nhau. Độ dẫn của mẫu thử và chất chuẩn cũng ảnh hưởng đến dòng EOF và thể tích tiêm.
Tiêm áp suất âm là đặt áp suất âm ở đầu mao quản có detector và hút dung dịch mẫu vào đầu tiêm của mao quản. Tiêm áp suất dương là tạo áp suất lên lọ chứa mẫu, đẩy mẫu vào trong mao quản. Tiêm áp suất có thể đưa tất cả các thành phần của mẫu vào trong mao quản ở cùng một mức độ, nói chung là cho độ tải lặp tốt nhất và là cách tiêm thường được áp dụng nhất. Thể tích mẫu phụ thuộc vào chiều dài và đường kính trong của mao quản và điện thế hay áp suất áp đặt. Thể tích mẫu đặc trưng được tiêm vào trong mao quản khoảng từ 1 nl đến 20 nl.
Mỗi một phương pháp tiêm mẫu có những ưu và nhược điểm riêng, tùy thuộc vào thành phần của mẫu, kiểu tách và áp dụng phương pháp. Không có kiểu tiêm mẫu nào nói trên có độ tái lập như bộ tiêm mẫu của máy sắc ký lỏng hiệu năng cao hiện đang có mặt trên thị trường. Tùy theo hoàn cảnh cụ thể, cần thiết phải sử dụng chất chuẩn nội cho các phương pháp cụ thể khi cần sự tiêm mẫu chính xác.
9.6 Cung cấp nguồn điện
Hầu hết các thiết bị CE có mặt trên thị trường có nguồn điện một chiều, nó có khả năng tạo nguồn điện thay đổi từ từ hay từng nấc đảm bảo duy trì được điện thế mong muốn một cách ổn định. Điều này sẽ đảm bảo có được đường nền tương đối phẳng.
Một đặc điểm thiết yếu khác của nguồn điện là khả năng sử dụng nguồn này để đưa mẫu vào đầu cathod hay anod của mao quản. Bởi vì trên thực tế không thể thay đổi vị trí detector từ đầu này đến đầu kia của thiết bị, mà chỉ có thể ấn định đầu tiêm mẫu ở phía cathod hay anod.
9.7 Các kiểu detector
Nói chung hệ thống CE thường ghép với các detector UV-VIS và detector huỳnh quang cảnm ứng laser. Detector quét phổ UV hay detector dãy diod có thể thấy ở nhiều thiết bị CE hiện có mặt trên thị trường.
Sự ghép nổi CE với phổ khối cho phép thu được thông tin về cấu trúc kết hợp các dữ liệu điện di. Phát hiện bằng detector huỳnh quang sẽ làm tăng độ nhạy phát hiện đối với mẫu chứa một lượng rất nhỏ chất cần phân tích có khả năng hấp thụ UV. Việc ghép một nhóm huỳnh quang với những chất không hấp thụ UV có thể là có ích. Các chất không hấp thụ UV hoặc không phát quang có thể được phát hiện bằng cách thêm trực tiếp vào dung dịch đệm các chất mang màu hay chất có huỳnh quang: Các chất không hấp thụ được phát hiện nhờ sự mất tín hiệu so với chất nên hấp thụ hay huỳnh quang. Detector đo độ dẫn và đo amper có thể được sử dụng, nhưng nói chung chúng không thông dụng ở các thiết bị có mặt trên thị trường.
9.8 Những điểm cần chú ý khi phân tích mẫu
Một vài thông số như kích thước mao quản, điện thế, lực ion và pH được tối ưu hóa để đạt độ phân giải và sự tách phù hợp. Cần tránh sự thay đổi nhiệt độ vì sẽ ảnh hưởng đến độ nhớt của dung dịch đệm và ảnh hưởng cả đến dòng EOF và lính độ của chất tan.
9.9 Kích thước mao quản
Những thay đổi về đường kính và chiều dài mao quản có thể ảnh hưởng đến độ phân giải điện di. Chiều dài mao quản tăng sẽ kéo dài thời gian di chuyển, thông thường sẽ tăng độ phân giải và làm giảm dòng điện. Đường kính mao quản tăng thường làm tăng dòng điện và tạo ra gradient nhiệt độ bên trong cột, dẫn đến làm giảm độ phân giải. Ngược lại, giảm đường kính trong của mao quản sẽ làm giảm sinh nhiệt và cho độ phân giải tốt hơn. Tuy nhiên, ở mao quản có đường kính lớn hơn sẽ có thuận lợi là tiêm được lượng mẫu nhiều hơn và cải thiện được tỷ lệ tín hiệu trên nhiễu.
9.10 Ảnh hưởng điện thế
Khi đặt một điện thế cao hơn, xảy ra sự tăng sinh nhiệt của dung dịch đệm làm việc bên trong mao quản vì có dòng điện đi qua dung dịch đệm. Hiệu ứng nhiệt này còn gọi là nhiệt Jun cần phải được kiểm soát vì trở kháng, hằng số điện môi và độ nhớt phụ thuộc vào nhiệt độ và làm thay đổi tốc độ dòng EOF và linh độ của chất tan. Nói chung, sự tăng điện thể sẽ làm tăng hiệu lực tách và độ phân giải đến điểm mà nhiệt Jun không phát tán được. Độ phân giải tối đa có thể đạt được bằng cách duy trì điện thể ở dưới mức xảy ra sự phát nhiệt Jun và sự khuếch tán trở thành yếu tố giới hạn.
9.11 Ảnh hưởng của lực ion
Kiểm soát lực ion cho phép điều chỉnh độ phân giải, hiệu lực tách và độ nhạy. Tăng lực ion nói chung sẽ cải thiện độ phân giải, hiệu lực tách và hình dạng pic. Độ nhạy có thể được cải thiện do có sự tụ hợp tốt hơn. Tuy nhiên, bởi vì dòng điện sinh ra tỷ lệ thuận với nồng độ đệm, nhiệt sinh ra nhiều hơn khi lực ion của đệm tăng, do đó cần hạn chế tăng lực ion.
9.11.1 Ảnh hưởng của pH
Độ phân giải, độ nhạy và hình dạng pic có thể thay đôi một cách rõ rệt khi có sự thay đổi pH vì thông số này ảnh hường đến mức ion hóa của chất tan và dòng EOF. Dòng EOF cao ở pH cao và thấp ở pH thấp đối với cột mao quản bằng silica nung chảy không có lớp bao mặt trong.
9.12 Các thông số vận hành
Các bước cơ bản trong quá trình vận hành hệ thống CE là thiết lập hệ thống, quy trình rửa cột mao quản, chuẩn bị mẫu, thử tính phù hợp hệ thống, phân tích mẫu, xử lý dữ liệu và tắt hệ thống.
9.13 Thiết lập hệ thống
Cần quan tâm đến khả năng tách, độ phân giải, lực ion của dung dịch đệm và ảnh hưởng pH để chọn cột có kích thước và lớp bao bề mặt cho phù hợp. Điều chế dung dịch đệm có thành phần, lực ion và pH thích hợp, loại khí nếu cần thiết và lọc qua lọc thích hợp. Tất cả dung môi, bao gồm cả nước cần dùng loại tinh khiết dùng cho sắc ký lỏng hay CE.
9.14 Quy trình rửa mao quản
Sự ổn định về thời gian di chuyển và độ phân giải có thể thu được nếu tuân theo quy trình rửa cột mao quản nhất định. Quy trình rửa và cân bằng mao quản phải phù hợp với các chất phân tích, các nền mẫu (matrix) và phương pháp phân tích. Bởi vậy, những qui trình này được xây dựng như là một phần của phương pháp và được quy định trong từng chuyên luận riêng. Rửa cột có thể dùng dung dịch acid phosphoric 0.1 M, nước và dung dịch natri hydroxyd 0,1 M. Trước khi bắt đầu quá trình phân tích mẫu, cột mao quản có thể được rửa với năm lần thể tích cột bằng dung dịch đệm làm việc dùng cho quá trình phân tích. Khi thay đổi thành phần đệm, nên rửa cột mao quản với năm lần thể tích cột bằng dung dịch đệm làm việc mới để làm sạch đệm của lần phân tích trước. Khi sử dụng cột mao quản mới bằng silica nung chảy không có lớp bao, thông thường yêu cầu phải hoạt hóa các nhóm silanol trên bề mặt mao quản. Quá trình này bao gồm việc tráng rửa kỹ với dung dịch natri hydroxyd. Đôi với các loại mao quan có lớp bao bên trong, quy trình rửa cột cần theo sự hướng dẫn của nhà sản xuất vì rửa cột không đúng cách có thể làm phá hủy lớp bao bên trong cột. Cột có thể được chỉ định chuyên dùng cho những loại đệm hay cho những phương pháp phân tích cụ thể để đề phòng nhiễm chéo.
9.15 Tiến hành phân tích mẫu
Để có được độ phân giải, độ nhạy và sự tách tốt với pic có hình dạng dẹp cần phải lựa chọn cột mao quản, chất điện giải và qui trình tiêm mẫu phù hợp. Khi cần thì sử dụng nội chuẩn để có được độ chính xác khi tiêm mẫu. Khi lựa chọn nội chuẩn cần quan tâm đến khả năng tách khỏi chất cân phân tích. Sự hoàn hảo của hệ thống có thể được cải thiện bằng cách rửa mao quản giữa các lần tiêm và cung cấp đệm mới cho hai lọ đệm dùng áp đặt thể trong quá trình tách (lọ . và 4 trong Hình 5.7). Có thể tiêm lặp lại từ cùng lọ mẫu thử miễn là tránh được sự nhiễm chéo. Nếu có sự nhiễm chéo xảy ra, nên rửa đầu mao quản nơi tiêm mẫu bằng cách nhúng nhanh nó vào trong một lọ có chứa đệm trước khi nhúng vào trong lọ chứa mẫu hay lọ chứa chất điện giải.
Các thông số vận hành được quy định cụ thể trong từng chuyên luận nhằm làm giảm ảnh hưởng của điện thế, lực ion và pH. Thiết bị được lắp đặt để phân tích mẫu với cột mao quản và điều kiện tiêm mẫu phù hợp năm trong khoảng tuyến tính động học của detector. Sự chính xác về độ di chuyển có thể đạt được bằng cách chọn chất pha loãng mẫu, chất điện giải và điều kiện xử lý cột mao quản phù hợp. Khi tiến hành phân tích chú ý tránh hiện tượng đưa lượng mẫu quá tải vào cột vì điều này sẽ làm giảm hiệu lực và độ tái lập.
9.16 Tính phù hợp của hệ thống
Các thông số được đo đạc có thể bao gồm độ lặp của bộ phận tiêm mẫu, độ chọn lọc và hiệu lực của hệ thống, và sự đối xứng của pic. Độ phân giải giữa các chất phân tích và các chất khác có thể được xác định bằng cách sử dụng các chất chuẩn hỗn hợp.
Các thông số tiêu biểu dùng để xác định tính phù hợp hệ thống bao gồm độ lệch chuẩn tương đối (RSD), hệ số dung lượng (k'), số đĩa lý thuyết (N), độ nhạy (giới hạn phát hiện và giới hạn định lượng), số đĩa lý thuyết tính trên 1 mét (n), hệ số đối xứng (T) và độ phân giải (R).
Hình dạng pic được kiểm tra chặt chẽ, pic lý tưởng phải đối xứng, không có vai và không kéo đuôi. Nếu những điều kiện này không đạt, cần phải tiến hành điều chỉnh trước khi tiến hành phân tích. Việc tích phân pic cũng phải được kiểm tra chặt chẽ để đảm bảo tín hiệu đáp ứng của pic được định lượng chính xác.
Tiêm lặp lại dung dịch chuẩn với nồng độ biết trước để xác định độ tái lập của hệ thống CE. Dữ liệu tiêm lặp lại từ 5 lần hoặc nhiều hơn được sử dụng để tính toán RSD. Trừ khi có qui định trong chuyên luận riêng, độ lệch chuẩn tương đối cho sự tiêm lặp lại không được quá 3,0%. Giá trị của độ chính xác nhỏ nhất có thể được qui định riêng trong phương pháp CE, đặc biệt khi xác định các thành phần dạng vết. Việc tính toán các thông số điện di trong MEKC, cũng như các phương pháp khác của CE có thể cần đến sự kết hợp các mối quan hệ giữa sắc ký và điện di. Vì vậy, hệ số dung lượng (k') cho sự di chuyển của chất trung tính trong MEKC có thể tính bằng phương trình:
.png)
Trong đó tr, t0 và tMC lần lượt là thời gian di chuyển của chất cần phân tích, của dung dịch (EOF) và của mixen.
Số đĩa lý thuyết (N), là thước đo hiệu lực của hệ thống và được tính bằng phương trình:
.png)
Trong đó W là độ rộng pic của chất cần phân tích do được ở đường nền, W2 là độ rộng pic của chất cần phân tích đo được ở phân nửa chiều cao của pic và từ là thời gian di chuyển của chất phân tích.
Số đĩa lý thuyết tính trên mét (n) là thước đo hiệu lực của cột mao quản được xem như là hàm số về độ rộng pic ở đường nền và có thể tính toán bằng công thức:
.png)
Trong đó L tính bằng cm là chiều dài tổng cộng của mao quản, các ký kiệu khác được định nghĩa như trên. Hệ số đối xứng pic (T) của chất cần phân tích là thước đo sự đối xứng của píc, nó thể hiện độ lệch của pic so với pic đối xứng lý tưởng. Hệ số này được tính bằng phương trình:
.png)
Trong đó W005 là chiều rộng pic đo ở 5% chiều cao của pic tính từ đường nên, f là chiều rộng nửa bên trái của pic đo ở 5% chiều cao pic tính từ đường nền. Hệ số 1,0 chỉ rằng pic là đối xứng. Nếu các hiệu ứng phân tán điện di xảy ra, thì chúng có thể tạo ra pic không đối xứng. Điều này có thể xảy ra khi dùng nồng độ mẫu thử cao như trong phân tích tạp chất. Trường hợp pic bất đối xứng cũng có thể chấp nhận được miễn là đạt được độ lập và chúng không ảnh hưởng đến độ chọn lọc về tách.
Hệ số phân giải (R) đo khả năng của hệ thống CE tách các chất cần phân tích di chuyển kế tiếp nhau. Độ phân giải được xác định cho tất cả các chất cần phân tích, với pH của đệm được điều chỉnh nếu cần thiết để đáp ứng các yêu cầu về tính phù hợp hệ thống. Nó có thể được tính bằng phương trình:
![]()
Trong đó t₂ và t₁ lần lượt là thời gian di chuyển (đo được ở cực đại của pic) của pic đi sau và pic trước. W₂ và W1 lần lượt là chiều rộng của hai pic đo được ở đường nền.
9.17 Phân tích mẫu
Sau khi xác định tính phù hợp hệ thống, có thể tiêm dung dịch mẫu thử và mẫu chuẩn. Mẫu chuẩn có thể tiêm trước hay sau mẫu thử và tiêm xen kẽ trong suốt quá trình phân tích.
9.18 Xử lý dữ liệu
Diện tích pic được chuẩn hóa theo thời gian thường được sử dụng trong định lượng. Các dữ liệu được xác định bằng cách chia diện tích pic đã tích phân được cho thời gian di chuyển của chất phân tích. Điều này làm giảm sai số do trong CE, không giống như trong sắc ký lỏng, mỗi chất cần phân tích di chuyển qua detector với một tốc độ khác nhau. Trừ khi sự chuẩn hóa này được thực hiện, những chất di chuyển chậm hơn sẽ có diện tích lớn bất thường so với diện tích của những thành phần di chuyển nhanh.
9.19 Tắt hệ thống
Sau khi phân tích, cột mao quản được rửa theo sự hướng dẫn được quy định riêng trong từng chuyên luận hay theo khuyến cáo của nhà sản xuất. Ví dụ: Cột mao quản có thể được rửa bằng nước cất để loại các thành phần đệm và sau đó được nạp không khí hoặc khí nitrogen lấy từ lọ rỗng. Thông thường, lọ đích và lọ nguồn (lọ 4 và lọ 2 trong Hình 5.7) là các lọ được bỏ dung dịch đệm đi và được tráng kỹ bằng nước khử khoáng.

