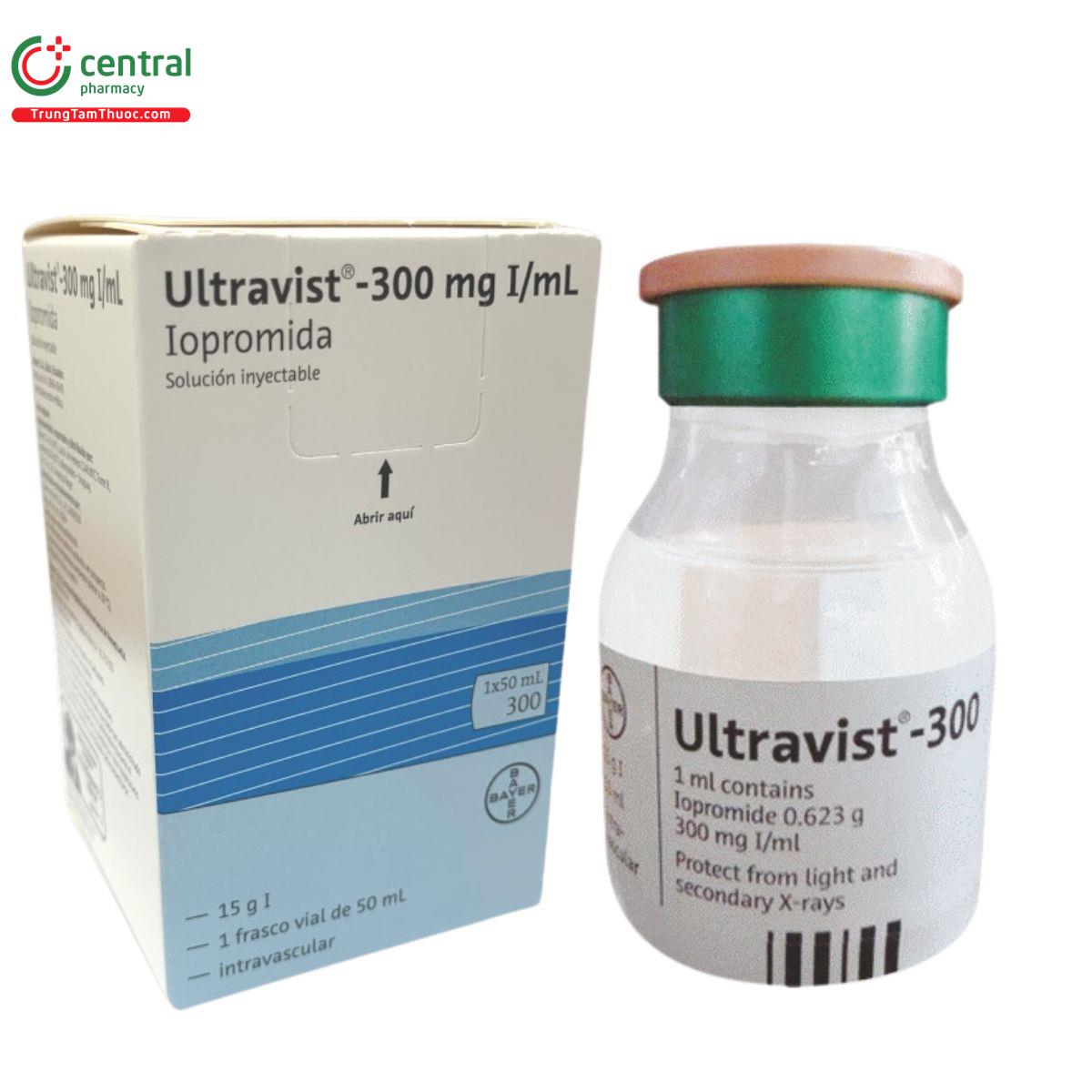
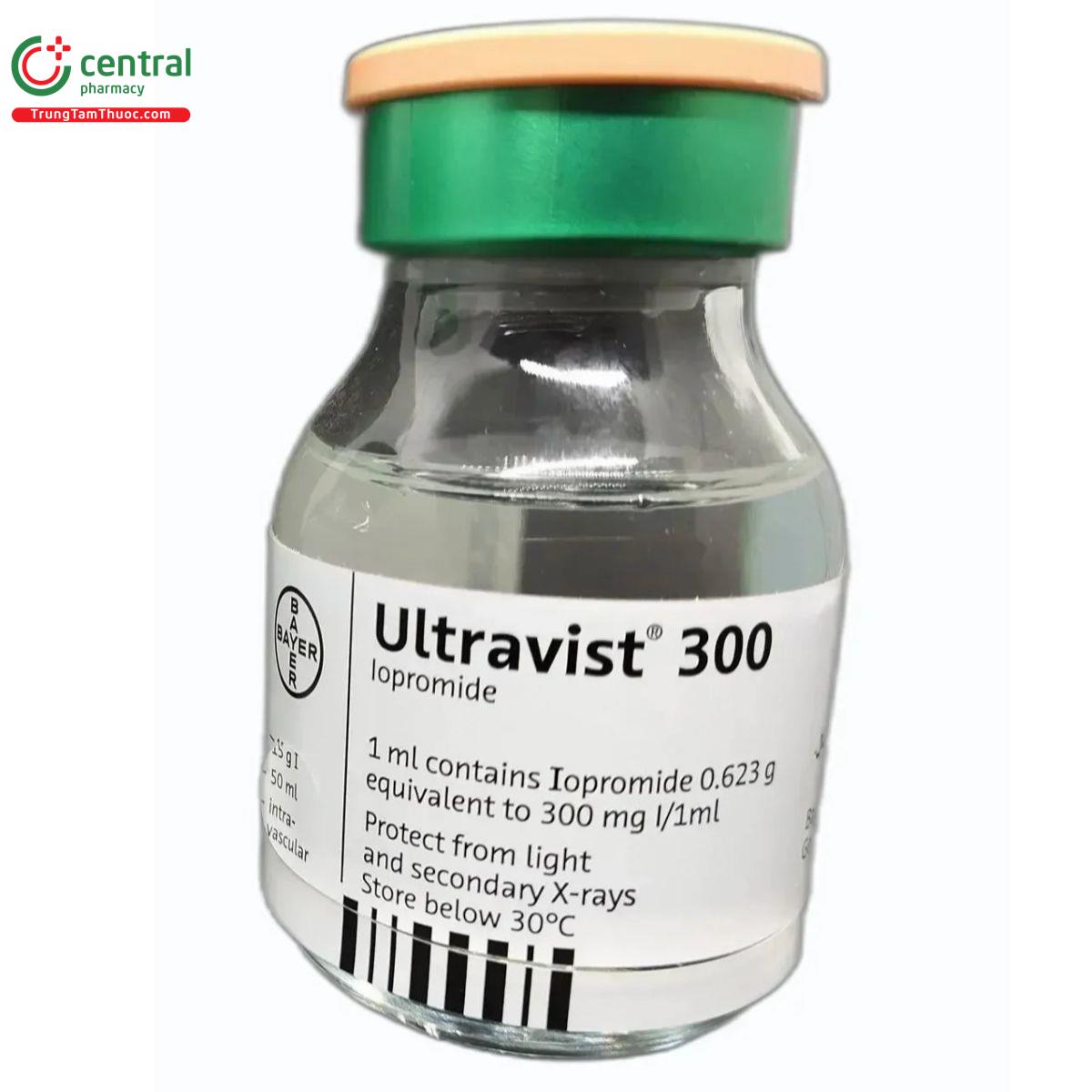
Ultravist - 300 50ml
Thuốc không kê đơn
| Thương hiệu | Tập đoàn Bayer, BAYER PHARMA AG |
| Công ty đăng ký | BAYER PHARMA AG |
| Số đăng ký | VN-14922-12 |
| Dạng bào chế | Dung dịch để tiêm /tiêm truyền |
| Quy cách đóng gói | Hộp 1 lọ 50ml |
| Hoạt chất | Iopromide |
| Xuất xứ | Đức |
| Mã sản phẩm | ak1176 |
| Chuyên mục | Dung Dịch Tiêm Truyền |
Nếu phát hiện nội dung không chính xác, vui lòng phản hồi thông tin cho chúng tôi tại đây
- Chi tiết sản phẩm
- Hỏi & Đáp 0
- Đánh giá 0
1 Thành phần
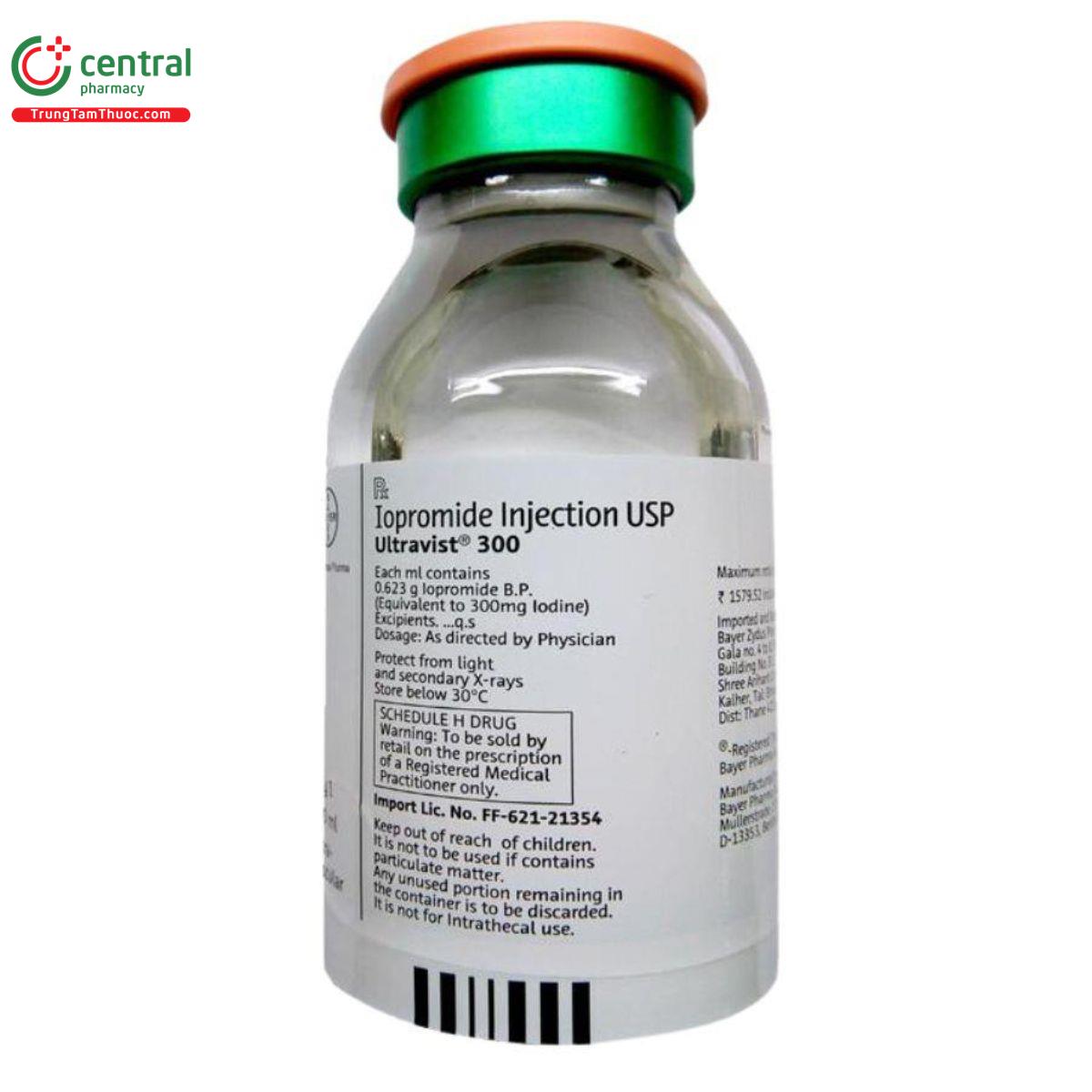
1ml chứa 0,623 g iopromide (tương đương với 300mg iodine)
Tá dược vừa đủ
Dạng bào chế: Dung dịch để tiêm /tiêm truyền. [1]
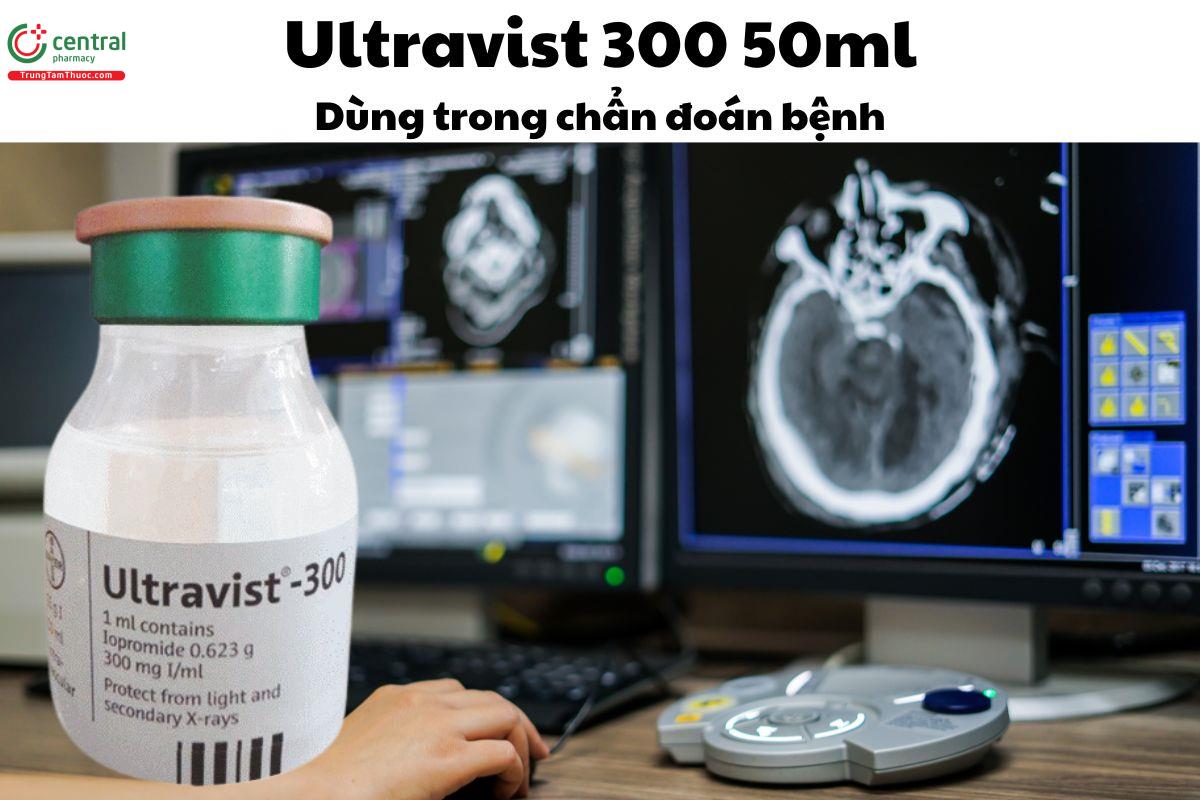
2 Thuốc Ultravist - 300 50ml có tác dụng gì?
Thuốc Ultravist - 300 50ml được dùng để hỗ trợ chẩn đoán qua các kỹ thuật hình ảnh như:
- Chụp cắt lớp (CT), chụp X-quang động mạch và tĩnh mạch.
- Chụp mạch máu số hóa xóa nền (DSA), chụp hệ niệu (UIV).
- Chụp mật tụy ngược dòng (ERCP), X-quang khớp, hoặc các khoang khác.
- Ultravist 370 đặc biệt được dùng trong chụp mạch máu tim.
==>> Xem thêm sản phẩm khác: Dung dịch truyền cung cấp năng lượng Lipofundin MCT/LCT 10%
3 Liều dùng, cách dùng Thuốc Ultravist - 300 50ml
3.1 Liều dùng tham khảo
Chụp mạch máu thông thường:
- Chụp động mạch chủ hoặc các động mạch khác: 50-80 ml Ultravist 300.
- Chụp tĩnh mạch chi trên và chi dưới: 15-60 ml Ultravist 300.
- Chụp mạch máu tim: 5-60 ml Ultravist 370.
Chụp DSA qua tĩnh mạch: Tiêm bolus 30-60 ml Ultravist 300, tốc độ 8-12 ml/giây.
Chụp CT: Liều dùng: 80-150 ml Ultravist 300 (tiêm bolus hoặc truyền chậm).
Chụp sọ não: 1-2 ml/kg (Ultravist 300)
Chụp hệ niệu:
- Trẻ sơ sinh: 4 ml/kg (Ultravist 300)
- Trẻ nhỏ: 3 ml/kg (Ultravist 300)
- Trẻ em: 1,5 ml/kg (Ultravist 300)
- Người lớn: 1 ml/kg (Ultravist 300)
Các chỉ định khác:
- Chụp khớp: 5-15 ml Ultravist 300.
- ERCP và các chụp khác: Liều tùy thuộc vùng chụp và vấn đề lâm sàng.
3.2 Lưu ý đặc biệt
Trẻ sơ sinh và trẻ nhỏ: Cần chú ý cân bằng điện giải và huyết động.
Người cao tuổi: Không cần hiệu chỉnh liều, nhưng cần tuân thủ các khuyến cáo chung.
Bệnh nhân suy gan: Không cần giảm liều, vì iopromide không chuyển hóa qua gan và chỉ thải trừ một phần nhỏ qua phân.
3.3 Thời gian chụp hình ảnh
Sau khi tiêm, độ cản quang của thận cao nhất sau 3-5 phút, còn đường niệu rõ nhất từ 8-15 phút.
Nên chụp phim đầu tiên sau khoảng 2 phút và theo dõi thêm tùy tình trạng bệnh nhân.
4 Chống chỉ định
Hiện tại không có chống chỉ định tuyệt đối đối với Ultravist.
==>> Bạn đọc có thể tham khảo thêm: Thuốc Cefobid 1g có tác dụng điều trị nhiễm khuẩn đường hô hấp
5 Tác dụng phụ
Các tác dụng phụ thường gặp (>4%) bao gồm đau đầu, buồn nôn và giãn mạch.
Các tác dụng phụ nghiêm trọng có thể gặp gồm sốc phản vệ, co thắt phế quản, ngừng thở, hôn mê, đột quỵ, nhồi máu cơ tim, suy tim, và suy hô hấp.
6 Tương tác thuốc
Biguanide (Metformin): Bệnh nhân suy thận cấp hoặc mạn tính có thể gặp rủi ro nhiễm toan lactic do giảm thải trừ Metformin, đặc biệt khi dùng Ultravist, vì thuốc này có thể làm suy thận hoặc làm nặng thêm bệnh thận. Cần thận trọng với bệnh nhân có tiền sử suy thận.
Interleukin-2: Sử dụng Interleukin-2 trong thời gian gần đây có thể làm tăng nguy cơ tác dụng phụ của Ultravist.
Đồng vị phóng xạ: Việc chẩn đoán tuyến giáp bằng phương pháp phóng xạ có thể bị ảnh hưởng sau khi dùng Ultravist do giảm hấp thu chất phóng xạ.
7 Lưu ý khi dùng thuốc và bảo quản
7.1 Lưu ý và thận trọng
Thuốc Ultravist - 300 50ml có thể gây phản ứng dị ứng từ nhẹ đến nặng (bao gồm sốc), thường xảy ra trong vòng 30 phút nhưng cũng có thể xuất hiện muộn.
Những bệnh nhân có tiền sử dị ứng, hen phế quản, hoặc từng phản ứng với thuốc cản quang i-ốt có nguy cơ gặp phản ứng quá mẫn cao hơn khi dùng Thuốc Ultravist - 300 50ml.
Cần chuẩn bị phương tiện cấp cứu sẵn sàng khi dùng thuốc, đặc biệt ở những bệnh nhân có bệnh lý tim mạch, vì phản ứng quá mẫn nặng có thể nguy hiểm hơn ở nhóm này.
Thuốc Ultravist - 300 50ml có thể gây cường giáp hoặc bão giáp, đặc biệt ở người có bướu giáp hoặc rối loạn tuyến giáp trước đó.
Trẻ sơ sinh tiếp xúc với Ultravist (qua mẹ hoặc trực tiếp) cần được theo dõi chức năng tuyến giáp do nguy cơ thiểu năng tuyến giáp.
Thuốc Ultravist - 300 50ml gây nguy cơ biến chứng thần kinh cao hơn ở bệnh nhân có tiền sử động kinh hoặc rối loạn thần kinh trung ương.
Thuốc có thể gây tổn thương thận thoáng qua hoặc suy thận cấp, đặc biệt ở bệnh nhân suy thận, đái tháo đường, mất nước, hoặc sử dụng liều cao.
Thuốc có thể gây thay đổi huyết động hoặc loạn nhịp tim, nguy cơ cao hơn ở bệnh nhân suy tim hoặc bệnh động mạch vành nặng.
7.2 Lưu ý khi dùng cho phụ nữ mang thai và cho con bú
Chưa có đủ nghiên cứu về độ an toàn của Ultravist trong thai kỳ do đó nếu cần thiết, việc sử dụng thuốc cản quang trong thời gian mang thai cần được xem xét kỹ lưỡng, cân nhắc giữa lợi ích và nguy cơ.
Mặc dù chưa có nghiên cứu đầy đủ về tác động của Ultravist đối với trẻ bú mẹ, lượng thuốc cản quang tiết vào sữa mẹ là rất thấp, nên khả năng gây hại cho trẻ là không cao.
7.3 Bảo quản
Thuốc Ultravist - 300 50ml nên được bảo quản nơi khô ráo, tránh ánh sáng trực tiếp từ mặt trời, nhiệt độ < 30oC.
7.4 Xử trí khi quá liều
Các nghiên cứu độc tính trên động vật cho thấy Ultravist không gây ngộ độc cấp tính, tuy nhiên, nếu dùng quá liều qua đường tĩnh mạch, có thể gặp các triệu chứng như rối loạn cân bằng điện giải, suy thận và rối loạn nhịp tim. Khi xảy ra quá liều, cần theo dõi chặt chẽ lượng dịch, điện giải và chức năng thận. Điều trị nên tập trung vào hỗ trợ các chức năng sống. Ultravist có thể được thẩm tách để loại bỏ thuốc ra khỏi cơ thể.
8 Sản phẩm thay thế
Nếu Thuốc Ultravist - 300 50ml hết hàng, quý khách hàng vui lòng tham khảo
Thuốc Diltiazem Stada 60mg do Công ty TNHH LD Stada-Việt Nam sản xuất, bào chế dạng viên nén, chứa Diltiazem Hydrochlorid được chỉ định điều trị bệnh lý tim mạch, tăng huyết áp vô căn
Hoặc Thuốc Tilhasan 60 có chứa Diltiazem Hydrochlorid, bào chế dạng Viên nén bao phim, là sản phẩm đến từ thương hiệu Hasan-Dermapharm, thường được chỉ định điều trị tăng huyết áp, đau thắt ngực
9 Cơ chế tác dụng
9.1 Dược lực học
Ultravist chứa iopromide, một chất không ion, hòa tan trong nước, có khả năng hấp thụ tia X-quang nhờ vào liên kết bền vững với iodine. Thuốc Ultravist giúp hiển thị hình ảnh của các cấu trúc trong cơ thể khi tiêm vào. [2]
9.2 Dược động học
Hấp thu và phân bố: Sau khi tiêm tĩnh mạch, iopromide nhanh chóng phân bổ vào khoang ngoại bào và thải trừ ra ngoài cơ thể. Thể tích phân bố ổn định là khoảng 16 L, và tỷ lệ gắn kết với protein rất thấp (khoảng 1%). Thuốc không qua được hàng rào máu não và chỉ một lượng nhỏ qua nhau thai.
Chuyển hóa: Iopromide không bị chuyển hóa trong cơ thể.
Thải trừ: Thời gian bán hủy cuối cùng của iopromide là khoảng 2 giờ. Hầu hết thuốc được thải trừ qua thận. Khoảng 60% liều dùng thải trừ qua nước tiểu trong vòng 3 giờ, và hơn 93% liều được tái hấp thu trong vòng 12 giờ. Khoảng 2% liều thải trừ qua phân trong vòng 3 ngày.
10 Thuốc Ultravist - 300 50ml giá bao nhiêu?
Thuốc Ultravist - 300 50ml hiện nay đang được bán ở nhà thuốc online Trung Tâm Thuốc Central Pharmacy, giá sản phẩm có thể đã được cập nhật ở đầu trang. Hoặc để biết chi tiết về giá sản phẩm cùng các chương trình ưu đãi, bạn có thể liên hệ với nhân viên nhà thuốc qua số hotline để được tư vấn thêm.
11 Thuốc Ultravist - 300 50ml mua ở đâu chính hãng, uy tín nhất?
Bạn có thể mua Thuốc Ultravist - 300 50ml trực tiếp tại nhà thuốc Trung Tâm Thuốc Central Pharmacy tại địa chỉ: 85 Vũ Trọng Phụng, Thanh Xuân. Hoặc liên hệ qua số hotline/ nhắn tin trên website để được tư vấn sử dụng thuốc đúng cách.
12 Ưu điểm
- Thuốc Ultravist - 300 50ml chứa iopromide là một chất cản quang không ion, có khả năng hấp thụ tia X rất tốt, giúp hiển thị rõ nét các cấu trúc bên trong cơ thể trong các xét nghiệm chẩn đoán hình ảnh như chụp X-quang, CT-scan, và chụp mạch.
- Iopromide có cấu trúc bền vững, không bị chuyển hóa trong cơ thể, giúp thuốc duy trì tác dụng lâu dài và thải trừ hiệu quả qua thận.
13 Nhược điểm
- Thuốc Ultravist - 300 50ml có thể gây tác dụng phụ nghiêm trọng như sốc phản vệ, co thắt phế quản, khó thở, hoặc nhồi máu cơ tim vẫn có thể xảy ra.
Tổng 15 hình ảnh











Tài liệu tham khảo
- ^ Hướng dẫn sử dụng sản phẩm do nhà sản xuất cung cấp, tại đây
- ^ Tác giả W Krause và cộng sự (Cập nhật năm 1994). Preclinical characterization of iopromide, journals. Truy cập ngày 5 tháng 11 năm 2024