Soliris
Thuốc kê đơn
Thuốc kê đơn quý khách vui lòng điền thông tin/ chat vào phần liên hệ này để dược sĩ tư vấn và đặt hàng
| Thương hiệu | Công ty AstraZeneca, Alexion Pharma International Operations Limited |
| Công ty đăng ký | Công ty TNHH AstraZeneca Việt Nam |
| Số đăng ký | 539410440425 |
| Dạng bào chế | Dung dịch |
| Quy cách đóng gói | Hộp 1 lọ chứa 30 ml dung dịch |
| Tá dược | Polysorbate 80 (Tween 80), Disodium Phosphate (Dibasic Sodium Phosphate) |
| Hộp/vỉ | Hộp |
| Xuất xứ | Ireland |
| Mã sản phẩm | na0010 |
| Chuyên mục | Thuốc ức chế miễn dịch |
Nếu phát hiện nội dung không chính xác, vui lòng phản hồi thông tin cho chúng tôi tại đây
- Chi tiết sản phẩm
- Hỏi & Đáp 0
- Đánh giá 0
1 Thành phần
1.1 Thành phần hoạt chất
Eculizumab là một kháng thể đơn dòng nhân hoá (IgG2/4k) được sản xuất trong dòng tế bào NSO bằng công nghệ DNA tái tổ hợp.
Một lọ 30 ml chứa 300 mg eculizumab (10 mg/ mL).
Sau khi pha loãng, nồng độ của dung dịch truyền là 5 mg/ mL.
1.2 Thành phần tá dược
Sodium phosphate monobasic, Sodium phosphate dibasic, Sodium chloride, Polysorbate 80 và nước pha tiêm
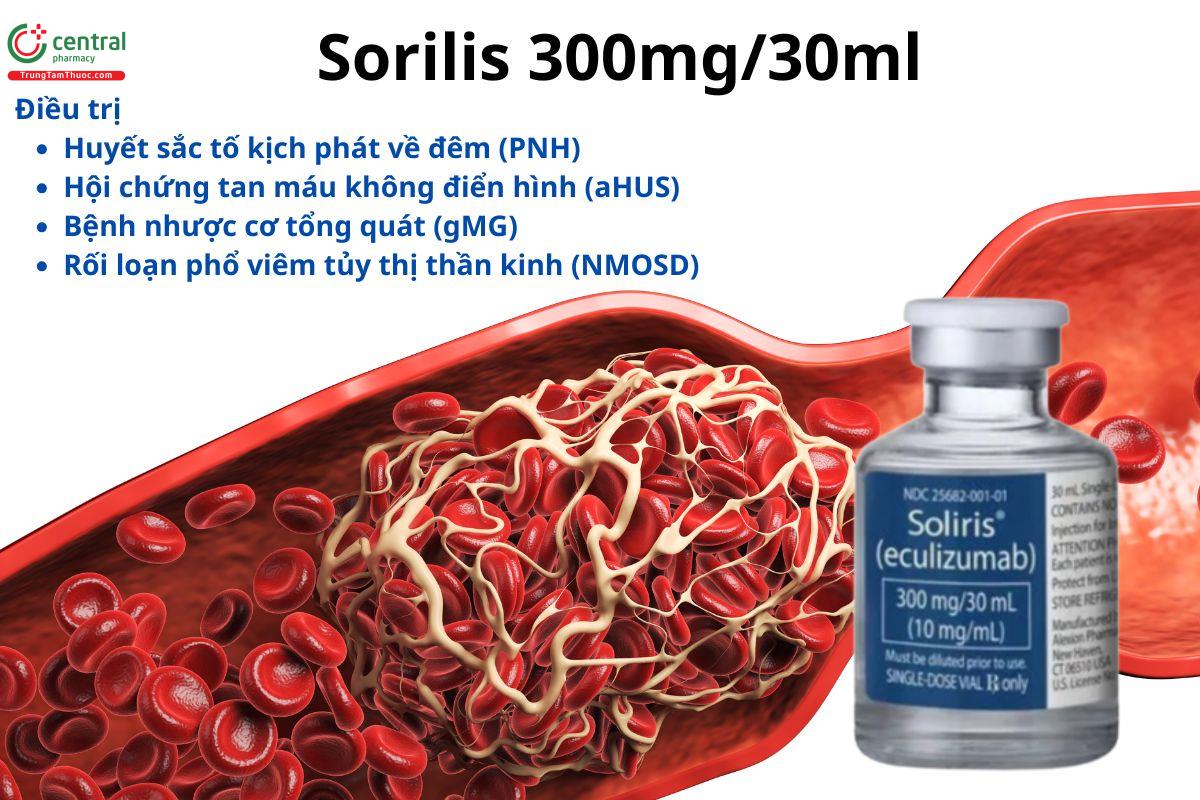
2 Tác dụng - Chỉ định của thuốc Soliris
Thuốc Soliris được sử dụng trong can thiệp lâm sàng đối với các bệnh lý cụ thể sau:
Bệnh tiểu huyết sắc tố kịch phát về đêm (PNH): Mục đích để giảm tình trạng tán huyết.
Hội chứng tán huyết tăng urê máu không điển hình (aHUS): Giúp ức chế các phản ứng bổ thể gây ra huyết khối vi mạch (ngoại trừ trường hợp STEC-HUS do vi khuẩn E. coli).
Bệnh nhược cơ toàn thân (gMG): Dành riêng cho người lớn có kháng thể AChR (+).
Rối loạn phổ viêm tủy thị thần kinh (NMOSD): Chỉ định cho người lớn có kháng thể AQP4 (+).
3 Liều dùng - Cách dùng của thuốc Soliris
3.1 Liều dùng
3.1.1 Nguyên tắc tiêm phòng và điều trị dự phòng
Yêu cầu tiêm chủng: Để hạn chế tối đa nguy cơ nhiễm trùng nặng, bệnh nhân cần tuân thủ việc tiêm vắc-xin theo đúng phác đồ quy định trong hướng dẫn tiêm chủng quốc gia hiện hành.
Sử dụng kháng sinh dự phòng: Trong trường hợp cần can thiệp bằng Soliris khẩn cấp khi bệnh nhân chưa tiêm vắc-xin đủ 14 ngày, phải chỉ định dùng kháng sinh dự phòng trong vòng 2 tuần đầu điều trị.
3.1.2 Phác đồ liều khuyến cáo cho người lớn mắc PNH (từ 18 tuổi)
Việc phân bổ liều lượng cho bệnh nhân được chia thành các giai đoạn cụ thể như sau:
Giai đoạn khởi đầu: Duy trì liều 600 mg/lần/tuần liên tục trong 4 tuần đầu.
Giai đoạn chuyển tiếp: Ở tuần thứ 5, bệnh nhân được chỉ định liều 900 mg.
Giai đoạn duy trì: Kể từ sau liều thứ 5, thực hiện truyền 900 mg định kỳ mỗi 2 tuần.
Lưu ý về thời gian: Để đảm bảo hiệu quả, thuốc nên được sử dụng đúng lịch trình. Trong trường hợp bất khả kháng, cho phép sai lệch thời gian thực hiện trong vòng 48 giờ so với ngày dự kiến.
3.1.3 Phác đồ liều khuyến cáo cho người mắc aHUS
Đối với đối tượng bệnh nhân từ 18 tuổi trở lên, lộ trình sử dụng Soliris được phân bổ cụ thể như sau:
4 tuần đầu tiên: Sử dụng liều khởi đầu 900 mg/lần/tuần.
Tuần thứ 5: Tăng liều lên 1200 mg (cách liều gần nhất 1 tuần).
Giai đoạn duy trì: Tiếp tục truyền 1200 mg định kỳ 2 tuần một lần.
Liều lượng Soliris cho trẻ em và vị thành niên được xác định dựa trên cân nặng thực tế của bệnh nhân. Chi tiết được quy định theo bảng dưới đây:
| Trọng lượng cơ thể | Giai đoạn khởi đầu | Liều duy trì |
| Từ 40 kg trở lên | 900 mg/tuần x 4 tuần | 1200 mg vào tuần thứ 5; sau đó duy trì 1200 mg mỗi 2 tuần |
| Từ 30 kg đến < 40 kg | 600 mg/tuần x 2 tuần | 900 mg vào tuần thứ 3; sau đó duy trì 900 mg mỗi 2 tuần |
| Từ 20 kg đến < 30 kg | 600 mg/tuần x 2 tuần | 600 mg vào tuần thứ 3; sau đó duy trì 600 mg mỗi 2 tuần |
| Từ 10 kg đến < 20 kg | 600 mg x 1 liều duy nhất | 300 mg vào tuần thứ 2; sau đó duy trì 300 mg mỗi 2 tuần |
| Từ 5 kg đến < 10 kg | 300 mg x 1 liều duy nhất | 300 mg vào tuần thứ 2; sau đó duy trì 300 mg mỗi 3 tuần |
Bệnh nhân cần được dùng Soliris đúng theo lịch trình đã nêu. Trong các trường hợp đặc biệt, việc tiêm truyền có thể linh động thực hiện trong vòng 48 giờ (2 ngày) so với thời điểm được chỉ định mà không làm ảnh hưởng đến phác đồ chung.
3.1.4 Phác đồ liều khuyến cáo cho người mắc gMG và NMOSD
Đối với người trưởng thành mắc bệnh nhược cơ toàn thân hoặc rối loạn phổ viêm tủy thị thần kinh, quy trình dùng thuốc được thực hiện theo các giai đoạn sau:
Tháng đầu tiên (Giai đoạn tấn công): Truyền tĩnh mạch liều 900 mg/lần, thực hiện định kỳ mỗi tuần một lần trong suốt 4 tuần đầu.
Giai đoạn chuyển tiếp: Một tuần sau liều cuối cùng của giai đoạn tấn công (tức tuần thứ 5), bệnh nhân sẽ được dùng liều 1200 mg.
Giai đoạn duy trì: Sau đó, duy trì liều 1200 mg với tần suất 2 tuần một lần.
Trong các trường hợp đặc biệt, việc tiêm truyền có thể linh động thực hiện trong vòng 48 giờ (2 ngày) so với thời điểm được chỉ định mà không làm ảnh hưởng đến phác đồ chung.
3.1.5 Hướng dẫn bổ sung liều Soliris khi can thiệp huyết tương (PE/PI)
Đối với các bệnh nhân đang điều trị aHUS (cả người lớn và trẻ em), gMG hoặc NMOSD (người lớn), nếu thực hiện đồng thời các liệu pháp như lọc huyết tương, thay huyết tương hoặc truyền huyết tương tươi đông lạnh, cần phải bổ sung liều Soliris để đảm bảo nồng độ thuốc trong cơ thể.
Quy định bổ sung liều cụ thể được trình bày trong bảng sau:
| Liệu pháp can thiệp | Liều Soliris gần nhất của bệnh nhân | Liều bổ sung cho mỗi lần can thiệp | Thời điểm chỉ định liều bổ sung |
| Lọc hoặc Thay huyết tương (PE) | ≥600 mg | 600 mg cho mỗi lần thực hiện | Thực hiện trong vòng 60 phút sau khi kết thúc lọc/thay huyết tương. |
| Lọc hoặc Thay huyết tương (PE) | 300 mg | 300 mg cho mỗi lần thực hiện | Thực hiện trong vòng 60 phút sau khi kết thúc lọc/thay huyết tương. |
| Truyền huyết tương tươi đông lạnh (PI) | ≥300 mg | 300 mg cho mỗi lần thực hiện | Thực hiện trong vòng 60 phút trước khi bắt đầu truyền huyết tương |
3.2 Quy trình pha loãng và chuẩn bị dung dịch truyền Soliris
Để đạt được nồng độ mục tiêu là 5 mg/mL, việc pha chế cần tuân thủ nghiêm ngặt các bước sau:
Lấy thuốc: Sử dụng bơm tiêm vô trùng để rút chính xác thể tích Soliris cần thiết từ lọ thuốc.
PHA trộn: Chuyển lượng thuốc đã rút vào túi dịch truyền. Sau đó, thêm một lượng dung dịch pha loãng tương ứng (tỉ lệ thể tích 1:1) để đạt nồng độ 5 mg/mL.
Dung dịch tương thích: Chỉ sử dụng các loại dịch truyền sau để pha loãng:
Natri clorid 0,9% hoặc 0,45%.
Dextrose 5%.
Dung dịch Ringer lactate.
Đồng nhất dung dịch: Đảo ngược túi truyền một cách nhẹ nhàng để thuốc và dịch pha loãng hòa quyện hoàn toàn. Tuyệt đối không lắc mạnh.
| Liều lượng chỉ định | Thể tích thuốc nguyên chất | Thể tích dịch pha loãng thêm vào | Tổng thể tích dịch truyền cuối cùng |
| 300 mg | 30 mL | 30 mL | 60 mL |
| 600mg | 60 mL | 60 mL | 120 mL |
| 900mg | 90 mL | 90 mL | 180 mL |
| 1200mg | 120 mL | 120 mL | 240 mL |
3.3 Các lưu ý quan trọng về an toàn và bảo quản
Kiểm soát nhiệt độ: Trước khi bắt đầu truyền, dung dịch phải được để tự cân bằng về nhiệt độ phòng (18°C - 25°C). Không sử dụng lò vi sóng hoặc các thiết bị tạo nhiệt để làm ấm thuốc nhanh.
Kiểm tra cảm quan: Trước khi sử dụng, cần quan sát kỹ dung dịch qua ánh sáng. Nếu phát hiện có vẩn đục, kết tủa hoặc biến màu bất thường, tuyệt đối không được sử dụng
Xử lý thuốc dư: Do Soliris không chứa chất bảo quản, mỗi lọ thuốc chỉ sử dụng một lần. Mọi phần thuốc còn dư sau khi rút liều cần phải bỏ đi.
3.4 Cách dùng
Phương thức thực hiện: Không dùng Soliris để tiêm tĩnh mạch nhanh chỉ được tiêm truyền.
Thời gian truyền sau khi pha dung dịch thuốc Soliris: Với người lớn là tối thiểu 35p và không quá 2 giờ. Còn với trẻ em là 1-4 giờ qua túi cho ăn có trọng lực, bơm tiêm xi-lanh hoặc bơm truyền.
Độ ổn định: Sau khi pha, dung dịch có thể duy trì chất lượng trong vòng 24 giờ nếu được bảo quản ở nhiệt độ phòng hoặc trong tủ lạnh (2°C - 8°C)
Xử trí phản ứng phụ: Nếu có dấu hiệu bất thường trong lúc truyền, bác sĩ có thể chỉ định giảm tốc độ hoặc tạm dừng.
Giám sát sau truyền: Cần theo dõi sát sao tình trạng của bệnh nhân ít nhất 60 phút sau khi kết thúc truyền để kịp thời phát hiện các phản ứng liên quan.
3.4.1 Sử dụng cho trẻ em
Chỉ định: Hiện tại, thuốc mới chỉ được xác nhận an toàn và hiệu quả cho trẻ em mắc aHUS (dựa trên nghiên cứu trên 47 bệnh nhi từ 2 tháng đến 17 tuổi). Các bệnh lý khác như PNH, gMG hay NMOSD vẫn chưa có dữ liệu ứng dụng cho nhóm tuổi này.
Hiệu quả: Kết quả điều trị aHUS ở trẻ em được ghi nhận là tương đương với người trưởng thành.
Yêu cầu phòng ngừa: Trẻ bắt buộc phải được tiêm chủng đầy đủ các loại vắc-xin phòng não mô cầu (N. meningitidis), phế cầu (S. pneumoniae) và vi khuẩn Hib theo quy định y tế quốc gia để hạn chế rủi ro nhiễm trùng.
3.4.2 Sử dụng trên bệnh nhân cao tuổi (trên 65 tuổi)
Dựa trên dữ liệu từ các thử nghiệm lâm sàng đối với các bệnh lý PNH, aHUS, gMG và NMOSD, có 51 trường hợp bệnh nhân từ 65 tuổi trở lên đã tham gia điều trị bằng Soliris.
Kết quả: Chưa ghi nhận sự khác biệt đáng kể về hiệu quả điều trị hay độ an toàn giữa nhóm này và nhóm bệnh nhân trẻ tuổi.
Hạn chế: Do quy mô mẫu ở người cao tuổi còn ít, hiện vẫn chưa thể khẳng định chắc chắn liệu nhóm đối tượng này có phản ứng khác biệt hoàn toàn so với những người trẻ hơn hay không.
4 Chống chỉ định
Tuyệt đối không sử dụng Soliris cho các đối tượng sau:
Nhiễm khuẩn cấp tính: Người đang bị nhiễm não mô cầu (Neisseria meningitidis) ở mức độ nặng mà chưa được điều trị dứt điểm.
Chưa tiêm vắc-xin: Người chưa thực hiện tiêm chủng phòng vi khuẩn não mô cầu.
Ngoại trừ: Trường hợp bác sĩ đánh giá việc chậm trễ dùng Soliris gây nguy hiểm cho tính mạng hơn là rủi ro nhiễm trùng não mô cầu.
Lưu ý: Cần xem xét kỹ các mục Cảnh báo và thận trọng trước khi quyết định điều trị để đảm bảo an toàn cho bệnh nhân.
5 Tác dụng không mong muốn
5.1 Tổng quan về độ an toàn
Dữ liệu an toàn được tổng hợp từ 33 thử nghiệm lâm sàng trên hơn 1.500 bệnh nhân (mắc PNH, aHUS, gMG và NMOSD).
Tác dụng phụ thường gặp nhất: Đau đầu (thường xuất hiện trong giai đoạn đầu trị liệu).
Nguy cơ nghiêm trọng nhất: Nhiễm trùng não mô cầu (viêm màng não).
| Tần suất | Các phản ứng chính |
Rất thường gặp ≥ 1/10 | Đau đầu. |
Thường gặp ≥ 1/100 đến <1/10 | Nhiễm trùng hô hấp (viêm phổi, viêm mũi họng, viêm xoang), rối loạn tiêu hóa (nôn, buồn nôn, tiêu chảy), đau cơ xương khớp, sốt, mệt mỏi, phát ban. |
Ít gặp ≥ 1/1000 đến <1/100 | Nhiễm trùng não mô cầu, sốc nhiễm khuẩn, nhiễm nấm, giảm các dòng tế bào máu (bạch cầu, tiểu cầu), rối loạn tâm thần (lo âu, mất ngủ), rối loạn thị giác, tăng/hạ huyết áp, suy thận. |
Hiếm gặp ≥ 1/10000 đến <1/1000 | Ung thư hắc tố, tan máu, rối loạn đông máu, vàng da, cường giáp (bệnh basedow). |
5.2 Các phản ứng cần lưu ý đặc biệt
Nhiễm trùng Neisseria: Ngoài não mô cầu, bệnh nhân có nguy cơ nhiễm các chủng Neisseria khác (như lậu cầu). Bắt buộc phải theo dõi sát các dấu hiệu nhiễm trùng.
Tính sinh miễn dịch: Một tỷ lệ nhỏ bệnh nhân (2% - 3%) có thể hình thành kháng thể kháng thuốc, tuy nhiên chưa ghi nhận ảnh hưởng lớn đến hiệu quả điều trị.
Hệ quả khi ngưng thuốc: Việc bỏ lỡ hoặc chậm trễ liều có thể gây tái phát tan máu nghiêm trọng (ở bệnh nhân PNH) hoặc biến chứng huyết khối (ở bệnh nhân aHUS).
Nhóm đối tượng đặc thù:
Trẻ em: Hồ sơ an toàn ở trẻ em mắc aHUS tương đồng với người lớn. Chưa có dữ liệu cho trẻ em mắc NMOSD.
Người cao tuổi: Không có sự khác biệt đáng kể về độ an toàn giữa người trên và dưới 65 tuổi.
Khuyến cáo: Nếu gặp bất kỳ triệu chứng bất thường nào, bệnh nhân cần thông báo ngay cho y bác sĩ hoặc cơ quan quản lý dược phẩm để cập nhật dữ liệu an toàn.
6 Tương tác, tương kỵ
Hiện chưa có các nghiên cứu chính thức về tương tác thuốc của Soliris (Eculizumab). Tuy nhiên, dựa trên cơ chế sinh học, cần đặc biệt lưu ý các trường hợp sau:
Rituximab: Eculizumab có khả năng làm giảm hiệu quả dược lực học của Rituximab do ức chế quá trình độc tế bào phụ thuộc vào bổ thể.
Immunoglobulin tiêm tĩnh mạch (IVIg): Việc điều trị IVIg dài hạn có thể làm giảm nồng độ Eculizumab trong máu bằng cách can thiệp vào cơ chế tái sinh thụ thể FcRn. Sự kết hợp này có nguy cơ làm giảm hiệu lực của thuốc.
Thuốc chẹn thụ thể FcRn: Sử dụng đồng thời nhóm thuốc này có thể khiến nồng độ Eculizumab trong hệ thống bị sụt giảm, dẫn đến giảm hiệu quả điều trị.
Khuyến cáo: Cần giám sát chặt chẽ tình trạng lâm sàng của bệnh nhân để kịp thời phát hiện việc giảm hiệu quả của Eculizumab khi phối hợp với các liệu pháp trên.
7 Lưu ý khi sử dụng và bảo quản
7.1 Lưu ý sử dụng thuốc cho phụ nữ có thai và cho con bú
7.1.1 Thời kỳ mang thai
Đánh giá rủi ro
Dữ liệu lâm sàng: Các báo cáo trên hơn 300 sản phụ tiếp xúc với Soliris chưa cho thấy các dấu hiệu bất thường cụ thể về sự phát triển của thai nhi. Tuy nhiên, do quy mô dữ liệu còn hạn chế, chưa thể loại trừ hoàn toàn mọi rủi ro tiềm ẩn.
Rủi ro từ bệnh lý nền: Nếu không được điều trị, hai bệnh lý PNH và aHUS gây nguy hiểm lớn cho cả mẹ và con:
Với PNH: Dễ dẫn đến huyết khối, thiếu máu nặng, nhiễm trùng, sảy thai hoặc tử vong ở mẹ; thai nhi có nguy cơ chết lưu hoặc sinh non.
Với aHUS: Mẹ dễ bị tiền sản giật, sinh non; thai nhi dễ bị chậm phát triển trong tử cung (IUGR) hoặc nhẹ cân.
Thử nghiệm trên động vật: Nghiên cứu trên chuột (với liều gấp 2-8 lần liều người) ghi nhận sự gia tăng tỷ lệ dị sản võng mạc, thoát vị rốn và tử vong ở chuột con. Tuy nhiên, khả năng sinh sản của chuột mẹ không bị ảnh hưởng.
Lời khuyên lâm sàng
Mọi thai kỳ đều có tỷ lệ rủi ro nền tự nhiên (2-4% dị tật và 15-20% sảy thai). Việc sử dụng Soliris cần được bác sĩ cân nhắc kỹ lưỡng giữa lợi ích kiểm soát bệnh cho mẹ và các nguy cơ chưa xác định cho thai nhi.
7.1.2 Thời kỳ cho con bú
Sự bài tiết qua sữa: Các dữ liệu hiện có chưa phát hiện nồng độ Eculizumab trong sữa mẹ, dù kháng thể IgG của mẹ thường được tiết qua đường này.
Ảnh hưởng đến trẻ: Chưa có đủ thông tin về tác động của thuốc đối với trẻ bú mẹ cũng như khả năng tiết sữa của người mẹ.
Quyết định điều trị: Cần dựa trên sự cân bằng giữa:
Lợi ích của việc nuôi con bằng sữa mẹ.
Tình trạng sức khỏe cấp thiết của người mẹ.
Các phản ứng phụ tiềm tàng ở trẻ (nếu có).
7.2 Quá liều và cách xử trí
Chưa ghi nhận bất kỳ sự cố quá liều nào trong suốt quá trình thực hiện các thử nghiệm lâm sàng.
7.3 Ảnh hưởng lên khả năng lái xe và vận hành máy móc
Soliris được đánh giá là an toàn, hầu như không gây ảnh hưởng đến khả năng tập trung, lái xe hay điều khiển các thiết bị máy móc phức tạp.
7.4 Bảo quản
Luôn duy trì thuốc trong môi trường từ 2°C đến 8°C (ngăn mát tủ lạnh). Không được làm đông lạnh sản phẩm.
Giữ lọ thuốc nguyên vẹn trong hộp giấy của nhà sản xuất để tránh tiếp xúc trực tiếp với ánh sáng.
Có thể lấy thuốc (vẫn nằm trong hộp gốc) ra khỏi môi trường lạnh trong một khoảng thời gian duy nhất tối đa là 72 giờ (3 ngày).
Nếu chưa sử dụng trong thời gian này, sản phẩm vẫn có thể được đưa trở lại tủ lạnh để tiếp tục bảo quản.
Sau khi pha loãng cần được sử dụng ngay.
8 Cảnh báo và thận trọng
8.1 Nguy cơ nhiễm trùng đặc biệt nghiêm trọng
Nhiễm não mô cầu: Đây là rủi ro nguy hiểm nhất. Soliris làm tăng nguy cơ mắc bệnh não mô cầu gấp 2.000 lần so với người bình thường. Bệnh có thể tiến triển nhanh dẫn đến tử vong nếu không phát hiện kịp thời.
Yêu cầu tiêm chủng: Bệnh nhân phải tiêm vắc-xin phòng não mô cầu ít nhất 2 tuần trước liều đầu tiên.
Trường hợp khẩn cấp: Nếu phải dùng thuốc ngay, cần tiêm vắc-xin sớm nhất có thể và kết hợp uống kháng sinh dự phòng trong ít nhất 2 tuần đầu.
Lưu ý: Tiêm chủng chỉ làm giảm chứ không loại bỏ hoàn toàn nguy cơ. Cần theo dõi sát các biểu hiện sớm của viêm màng não.
Các nhiễm trùng khác: Bệnh nhân dễ nhạy cảm hơn với các vi khuẩn có vỏ bao (như lậu cầu, phế cầu, Hib) và nấm Aspergillus. Trẻ em cần tiêm thêm vắc-xin phòng S. pneumoniae và Hib.
Theo dõi sau khi ngừng thuốc (Nguy cơ tái phát nặng)
8.2 Việc ngưng hoặc quên liều Soliris có thể gây ra các biến chứng cấp tính nghiêm trọng:
Bệnh nhân PNH: Theo dõi tình trạng tán huyết (phá hủy hồng cầu) trong ít nhất 8 tuần sau khi dừng thuốc.
Bệnh nhân aHUS: Theo dõi các dấu hiệu huyết khối vi mạch (TMA) trong ít nhất 12 tuần.
Dấu hiệu nhận biết: Co giật, đau thắt ngực, khó thở, giảm tiểu cầu (>25%), tăng Creatinine hoặc nồng độ LDH máu.
Xử trí: Cần cân nhắc dùng lại Soliris hoặc can thiệp huyết tương ngay nếu TMA tái phát.
8.3 Quản lý điều trị và Tương tác
Thuốc kháng đông: Không được tự ý thay đổi hay ngưng Thuốc chống đông máu khi đang điều trị bằng Soliris, vì hiệu quả phối hợp này chưa được xác lập rõ ràng.
Phản ứng tiêm truyền: Thuốc có thể gây sốc phản vệ hoặc quá mẫn. Nếu bệnh nhân có dấu hiệu suy hô hấp hoặc bất ổn tim mạch khi đang truyền, phải ngưng thuốc ngay lập tức và cấp cứu kịp thời.
Hạn chế của thuốc: Soliris không có tác dụng điều trị tình trạng thiếu máu do suy tủy (bất sản) ở bệnh nhân PNH.
8.4 Quản lý hồ sơ
Truy xuất nguồn gốc: Luôn ghi chép đầy đủ tên thuốc và số lô sản xuất vào hồ sơ bệnh án để theo dõi an toàn sinh học.
9 Cơ chế tác dụng
Eculizumab là một kháng thể đơn dòng có khả năng gắn kết đặc hiệu và mạnh mẽ với protein bổ thể C5. Bằng cách này, thuốc ngăn chặn quá trình phân tách C5 thành các mảnh C5a và C5b, từ đó ức chế sự hình thành phức hợp tấn công màng (C5b-9) – giai đoạn cuối cùng của hệ thống bổ thể.
Tác dụng cụ thể trên từng bệnh như sau:
Đối với PNH (Tiểu huyết sắc tố kịch phát về đêm): Soliris ngăn chặn sự phá hủy hồng cầu (tán huyết) trong lòng mạch do hệ bổ thể gây ra.
Đối với aHUS (Hội chứng tán huyết tăng urê huyết không điển hình): Thuốc ức chế tình trạng huyết khối vi mạch (TMA) do sự kích hoạt quá mức của bổ thể.
Đối với gMG (Nhược cơ năng nặng): Mặc dù cơ chế chưa được khẳng định hoàn toàn, nhưng hiệu quả của thuốc được cho là nhờ việc giảm tích tụ phức hợp C5b-9 tại điểm nối thần kinh - cơ, giúp bảo vệ dẫn truyền thần kinh.
Đối với NMOSD (Viêm tủy thị thần kinh): Cơ chế tác động được cho là thông qua việc ức chế phức hợp C5b-9 do kháng thể kháng Aquaporin-4 kích hoạt, từ đó giảm thương tổn hệ thần kinh trung ương.
9.1 Dược lực học
Kiểm soát nồng độ LDH (Trên bệnh nhân PNH):Hiệu quả của Soliris được thể hiện rõ rệt thông qua việc giảm nhanh chóng chỉ số LDH huyết thanh - một dấu hiệu đặc trưng của tình trạng tán huyết.
Giai đoạn khởi đầu: Chỉ sau 1 tuần điều trị theo phác đồ khuyến cáo, nồng độ LDH trung bình giảm mạnh từ mức 2200 ± 1034 U/L xuống còn khoảng 700 ± 388 U/L.
Duy trì dài hạn: Hiệu quả này được ghi nhận ổn định xuyên suốt 26 tuần trong các nghiên cứu đối chứng giả dược (327 ± 433 U/L) và kéo dài đến 52 tuần trong các thử nghiệm đơn nhánh.
Ngưỡng phong tỏa bổ thể: Đối với tất cả các chỉ định được phê duyệt (PNH, aHUS, gMG và NMOSD), việc kiểm soát hoạt động của hệ bổ thể cuối phụ thuộc chặt chẽ vào nồng độ thuốc trong máu.
Khi nồng độ C5 tự do được duy trì ở mức dưới 0,5 mcg/mL, hệ thống bổ thể tận cùng sẽ bị phong tỏa hoàn toàn, giúp ngăn chặn các phản ứng miễn dịch gây hại cho tế bào.
9.2 Dược động học
Nồng độ trong huyết thanh ở trạng thái ổn định (Tuần 24-26)
Khi sử dụng liều duy trì định kỳ 2 tuần/lần, các chỉ số nồng độ đỉnh (C max) và nồng độ đáy (C trounh) trung bình (± SD) được ghi nhận như sau
Chỉ định
| Chỉ định | Liều duy trì | Cmax (μg/mL) | Ctrough (μg/mL) |
| PNH | 900 mg | 194 ± 76 | 97 ± 60 |
| aHUS | 1200 mg | - | 242 ± 101 |
| gMG | 1200 mg | 783 ± 288 | 341 ± 172 |
| NMOSD | 1200 mg | 877 ± 331 | 429 ± 188 |
Thuốc đạt trạng thái ổn định sau 4 tuần trị liệu với tỷ lệ tích lũy khoảng 2 lần.
Dược động học của thuốc là tuyến tính theo liều (trong khoảng 600–1200 mg) và không thay đổi theo thời gian.
9.2.1 Phân bố
Thể tích phân bố ở người trưởng thành (khoảng 70 kg) dao động từ 5 L đến 8 L, cho thấy thuốc chủ yếu khu trú trong hệ tuần hoàn.
9.2.2 Thải trừ
Thời gian bán thải : Kéo dài từ 270 giờ đến 414 giờ (khoảng 11–17 ngày).
Ảnh hưởng của can thiệp huyết tương: Việc thay hoặc truyền huyết tương làm tăng tốc độ đào thải thuốc lên 250 lần, rút ngắn T1/2 xuống chỉ còn 1,26 giờ. Do đó, cần bổ sung liều Soliris ngay sau các thủ thuật này.
9.2.3 Các đối tượng đặc biệt
Các yếu tố như tuổi tác (từ 2 tháng đến 85 tuổi), giới tính và chủng tộc không làm thay đổi dược động học của eculizumab.
Suy thận: Chức năng thận không gây ảnh hưởng đến quá trình chuyển hóa và đào thải thuốc, ngay cả ở những bệnh nhân có độ lọc cầu thận (eGFR) rất thấp (5 mL/phút/1,73 m2).
9.2.4 Tương tác dược động học đáng lưu ý
Immunoglobulin tiêm tĩnh mạch (IVIg): Có thể làm giảm nồng độ eculizumab trong máu do cạnh tranh cơ chế tái sinh thụ thể FcRn. Mặc dù chưa có nghiên cứu lâm sàng chuyên biệt, cần thận trọng và theo dõi nồng độ thuốc khi phối hợp hai liệu pháp này.
10 Thuốc Soliris giá bao nhiêu?
Thuốc Soliris hiện đang được bán tại nhà thuốc online Trung Tâm Thuốc Central Pharmacy. Giá sản phẩm có thể đã được cập nhật ở đầu trang. Hoặc để biết chi tiết về giá sản phẩm cùng các chương trình ưu đãi, người dùng có thể liên hệ với dược sĩ đại học của nhà thuốc qua số hotline, nhắn tin trên Zalo, Facebook.
11 Thuốc Soliris mua ở đâu?
Khách hàng có thể mang đơn bác sĩ kê để mua trực tiếp tại nhà thuốc Trung Tâm Thuốc Central Pharmacy (địa chỉ : 85 Vũ Trọng Phụng, Thanh Xuân, Hà Nội) hoặc liên hệ qua hotline/ nhắn tin trên website để được tư vấn sử dụng thuốc đúng cách.
12 Ưu điểm
- Với thời gian bán thải dài (11 - 17 ngày), bệnh nhân chỉ cần truyền thuốc định kỳ 2 tuần một lần, tạo sự thuận tiện hơn so với các thuốc phải dùng hàng ngày.
- Thuốc có thể sử dụng cho cả trẻ em (với chỉ định aHUS) và người cao tuổi mà không cần điều chỉnh liều quá phức tạp theo chức năng thận.
13 Nhược điểm
- Làm tăng nguy cơ viêm màng não do não mô cầu. Bệnh nhân bắt buộc phải tiêm chủng và theo dõi y tế chặt chẽ.
- Thuốc chỉ có dạng truyền tĩnh mạch, yêu cầu bệnh nhân phải đến cơ sở y tế có chuyên môn để thực hiện, không thể tự dùng tại nhà như thuốc uống.
Tổng 7 hình ảnh