Ustekinumab
1 sản phẩm
 Dược sĩ Hoàng Mai Dược sĩ lâm sàng
Dược sĩ Hoàng Mai Dược sĩ lâm sàng
Ước tính: 1 phút đọc, Ngày đăng:
Cập nhật:
Nếu phát hiện nội dung không chính xác, vui lòng phản hồi thông tin cho chúng tôi tại đây
Tên chung quốc tế: Ustekinumab
Biệt dược thường gặp: Stelara
Phân loại: Chất ức chế Interleukin
Mã ATC: L04AC05
1 Dạng thuốc và hàm lượng
Dung dịch truyền tĩnh mạch, tiêm dưới da chứa hàm lượng 45mg/0,5mL, 90mg/1mL, 130mg/26mL Ustekinumab.
2 Dược lực học
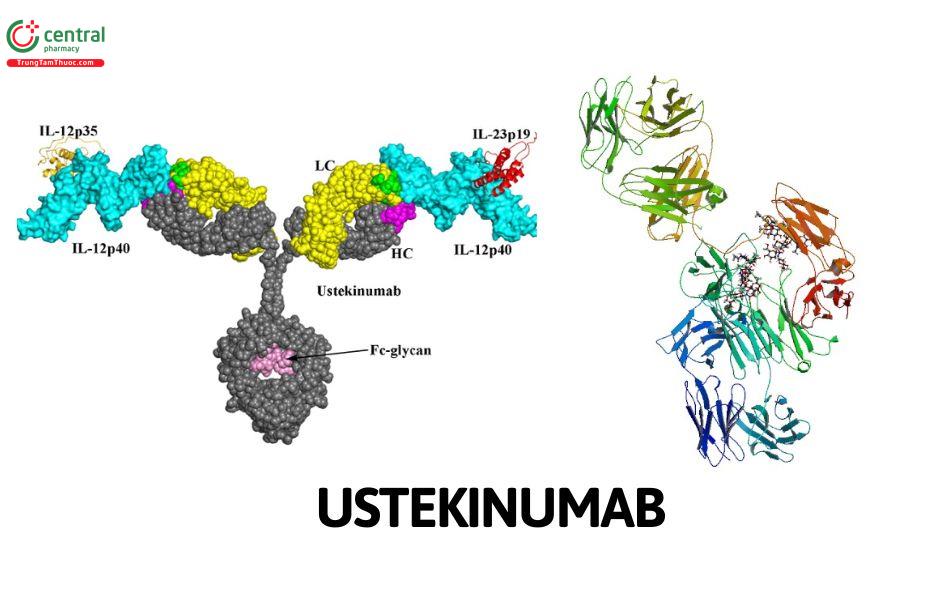
Ustekinumab là kháng thể đơn dòng immunoglobulin (Ig) G1 kappa của người được phát hiện thông qua việc tạo ra các nuôi cấy tế bào lại từ chuột chuyển gen (Tg) immunoglobulin (hu-Ig) của người đã được miễn dịch. Các tế bào lai tiết ra mAb của người có khả năng trung hòa interleukin-12 (IL-12) đã được xác định.
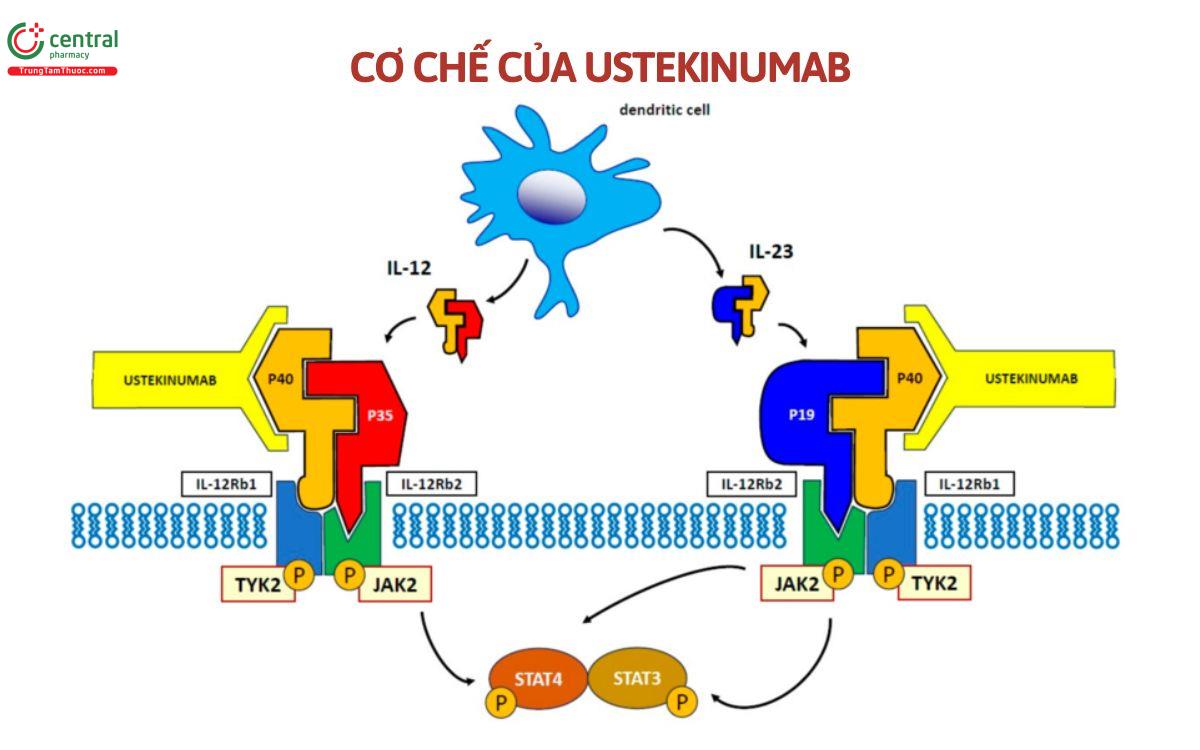
Interleukin (IL)-12 và IL-23 là các cytokine dị hợp tử gây ra phản ứng miễn dịch và viêm, chúng có thể hoạt hoá các tế bào như tế bào NK, tế bào T CD4+ có liên quan đến các bệnh viêm mạn tính như vảy nến, viêm ruột. Việc sử dụng IL-12 làm trầm trọng thêm bệnh ở bệnh vẩy nến ở chuột, viêm đại tràng mãn tính, viêm khớp do Collagen (CIA), viêm não tự miễn thực nghiệm (EAE) trong khi việc sử dụng kháng thể kháng IL-12/23p40 có tác dụng bảo vệ hoặc làm giảm mức độ nghiêm trọng của bệnh.
Ustekinumab là liệu pháp kháng thể nhắm mục tiêu giúp ức chế phản ứng miễn dịch bằng cách liên kết với tiểu đơn vị p40 của interleukin (IL)-12 và IL-23 và ngăn chặn sự tương tác của chúng với thụ thể IL-12Rβ1 trên bề mặt tế bào, sau đó ức chế tín hiệu tế bào, hoạt hóa và sản xuất cytokine do IL-12 và IL-23 trung gian NK, sát thủ tự nhiên. Nó sẽ không ảnh hưởng đến các phản ứng miễn dịch được kích thích thông qua các cytokine hoặc hoạt động của tế bào khác.
3 Dược động học
3.1 Hấp thu
Ustekinumab có thời gian đạt nồng độ trong huyết tương cao nhất khoảng 13,5 ngày và 7 ngày tương ứng với liều 45mg và 90 mg. Giá trị nồng độ cao nhất trong huyết tương lần lượt là 2,4 μg/mL và 5,3 μg/mL ở liều 45mg và 90mg, giá trị AUC lần lượt là 84,9 μg·day/mL và 226,9 μg·day/mL.
3.2 Phân bố
Ustekinumab có Thể tích phân bố ở trạng thái ổn định là 4,62 L ở bệnh nhân viêm ruột và 4,4 L ở người loét đại tràng, các thông tin về liên kết protein chưa rõ ràng.
3.3 Chuyển hoá
Ustekinumab có thể trải qua quá trình phân huỷ protein thông qua dị hoá.
3.4 Thải trừ
Thuốc chủ yếu được cho là đào thải qua thận sau khi phân huỷ, thời gian bán thải khoảng 19,8 ngày và 21,2 ngày với liều dưới da 45 mg hoặc 90 mg.
4 Chỉ định
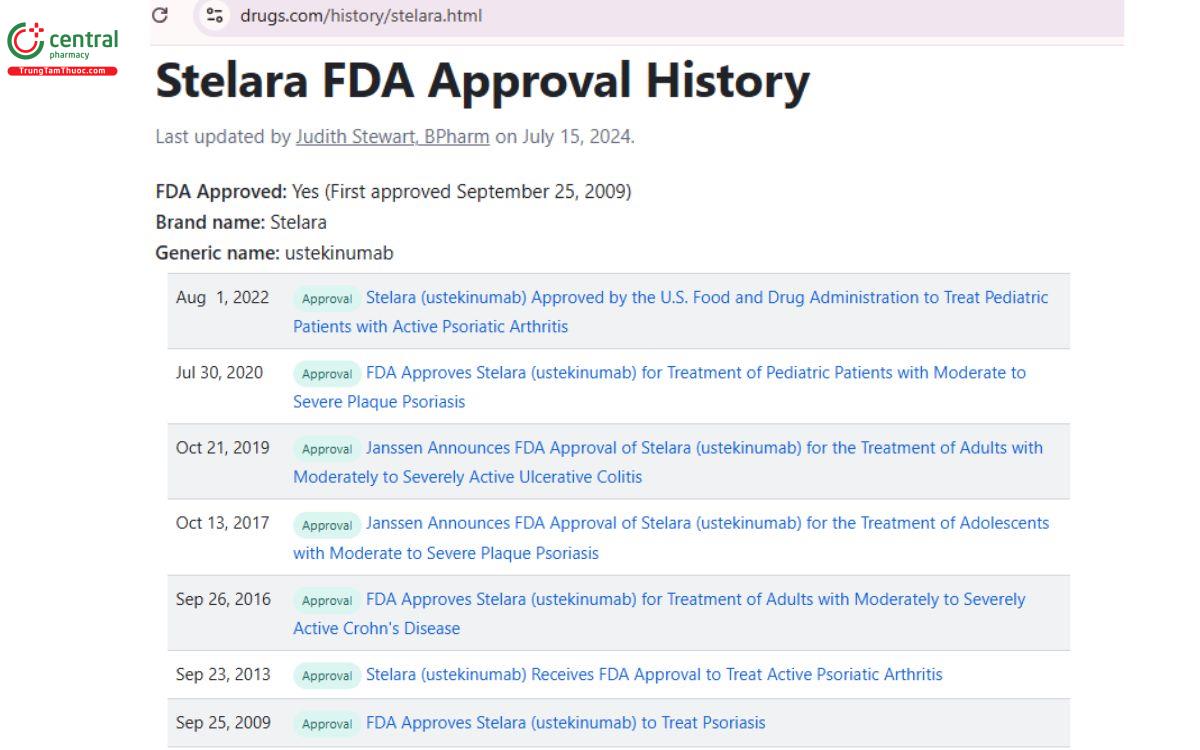
Ustekinumab được chỉ định để điều trị vảy nến mảng bám từ trung bình đến nặng ở người lớn và trẻ em từ 6 tuổi trở lên. Thường sử dụng khi các phương pháp điều trị ưu tiên ban đầu không mang lại hiệu quả mong muốn.
Ustekinumab được chỉ định để điều trị viêm khớp vảy nến kết hợp với Methotrexate, viêm loét đại tràng ,bệnh Crohn từ trung bình đến nặng ở người lớn.
5 Chống chỉ định
Người mẫn cảm với thành phần của Ustekinumab.
6 Liều dùng - Cách dùng
6.1 Liều dùng
Liều dùng khuyến cáo trong từng chỉ định bệnh cụ thể:
6.1.1 Bệnh vẩy nến mảng bám
Sử dụng liều theo cân nặng:
- Dưới 100kg tiêm liều 45mg dưới da và lặp lại sau 4 tuần, sau đó cứ mỗi 12 tuần lặp lại liều.
- Trên 100kg tiêm liều 90mg và lặp lại sau 4 tuần, sau đó cứ mỗi 12 tuần lặp lại liều.
6.1.2 Viêm khớp vảy nến
Sử dụng liều 45mg tiêm dưới da vào tuần 0 và tuần 4, sau đó lặp lại sau 12 tuần. Nếu bệnh nhân nặng hơn 100kg dùng liều 90mg với chu kỳ tương tự.
6.1.3 Bệnh Crohn cấp tính, viêm loét đại tràng
Bắt đầu truyền tĩnh mạch liều duy nhất trong 1 giờ với từng mức liều theo cân nặng:
- ≤55 kg: 260 mg tiêm tĩnh mạch
- >55 kg đến 85 kg: 390 mg tiêm tĩnh mạch
- >85 kg: 520 mg tiêm tĩnh mạch
Sau đó duy trì liều 90mg tiêm dưới da mỗi 8 tuần.
6.2 Cách dùng
Sử dụng đường tiêm dưới da hoặc truyền tĩnh mạch tuỳ vào chỉ định bệnh. Liều lượng và lịch trình tiêm tuân theo hướng dẫn của bác sĩ.
Truyền tĩnh mạch chậm trong 1 giờ, không truyền chung với các dung dịch khác.
7 Tác dụng không mong muốn
7.1 Thường gặp
Nhiễm trùng đường hô hấp trên
7.2 Ít gặp
Viêm mũi họng, đau lưng, viêm mô tế bào, trầm cảm, tiêu chảy, mệt mỏi, đau đầu, ban đỏ tại chỗ tiêm, đau nhức cơ, nghẹt mũi, mề đay, phát ban, ngứa.
7.3 Hiếm gặp
Nhiễm trùng nghiêm trọng, sự ác tính, hội chứng não trắng sau hồi phục.
8 Tương tác thuốc
8.1 Vắc-xin sống
Tránh tiêm vắc-xin sống trong vòng 1 năm trước khi bắt đầu điều trị hoặc sau khi điều trị với ustekinumab.
8.2 Thuốc ức chế miễn dịch
Khi sử dụng đồng thời thuốc ức chế miễn dịch với Ustekinumab có thể làm tăng nguy cơ nhiễm trùng.
9 Thận trọng
Ustekinumab có thể làm giảm khả năng của hệ miễn dịch, làm tăng nguy cơ nhiễm trùng, đặc biệt nhiễm trùng cơ hội, nên thực hiện các xét nghiệm lao tiềm ẩn trước khi dùng thuốc.
Nguy cơ gặp các phản ứng dị ứng nghiêm trọng như sốc phản vệ nên cần ngừng thuốc ngay và cấp cứu kịp thời.
Tăng nguy cơ ung thư ác tính như ung thư da, thận trọng với người có khối u rắn hoặc ung thư.
Các phản ứng nghiêm trọng liên quan đến thần kinh như hội chứng bệnh não trắng sau hồi phục (RPLS), nếu gặp các triệu chứng như yếu cơ, rối loạn thị lực cần thông báo ngay với bác sĩ.
10 Thời kỳ mang thai và cho con bú
Chưa có báo cáo đầy đủ về mức độ an toàn của thuốc, không nên dùng thuốc cho đối tượng đang mang thai. Chỉ nên dùng nếu lợi ích lớn hơn nguy cơ và có sự giám sát của bác sĩ.
Ustekinumab có thể được bài tiết qua sữa mẹ, nên không dùng cho phụ nữ đang cho con bú vì độc tính có thể gặp ở trẻ.
11 Bảo quản
Bảo quản lạnh (từ 2 độ C đến 8 độ C).
Không đông lạnh.
Tránh ánh sáng trực tiếp chiếu vào.
12 Quá liều
Chưa có báo cáo, trong trường hợp quá liều nên ngừng thuốc và cấp cứu.
13 Tài liệu tham khảo
Chuyên gia Drugbank. Ustekinumab. Drugbank. Truy cập ngày 28 tháng 12 năm 2024.
Chuyên gia Drugs.com. Ustekinumab Dosage. Drugs.com. Truy cập ngày 28 tháng 12 năm 2024.
Chuyên gia Pubchem. Ustekinumab. Pubchem.Truy cập ngày 28 tháng 12 năm 2024.
Chuyên gia Drugs.com. Stelara FDA Approval History. Drugs.com. Truy cập ngày 28 tháng 12 năm 2024