Sunitinib
11 sản phẩm
 Dược sĩ Hoàng Mai Dược sĩ lâm sàng
Dược sĩ Hoàng Mai Dược sĩ lâm sàng
Ước tính: 1 phút đọc, Ngày đăng:
Cập nhật:
Nếu phát hiện nội dung không chính xác, vui lòng phản hồi thông tin cho chúng tôi tại đây
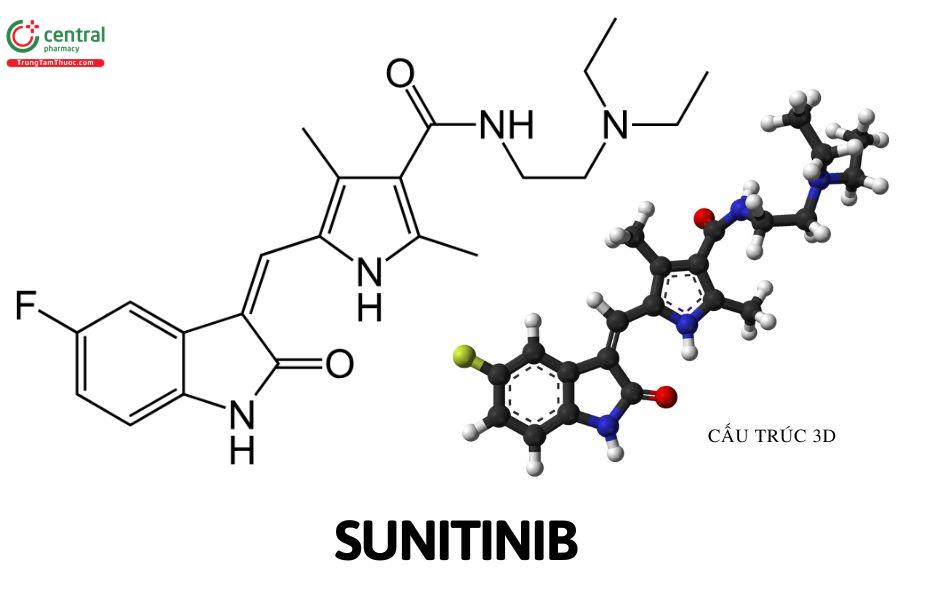
Tên chung quốc tế: Sunitinib
Biệt dược thường gặp: Sutent
Phân loại: Các chất ức chế protein kinase khác
Mã ATC: L01EX01
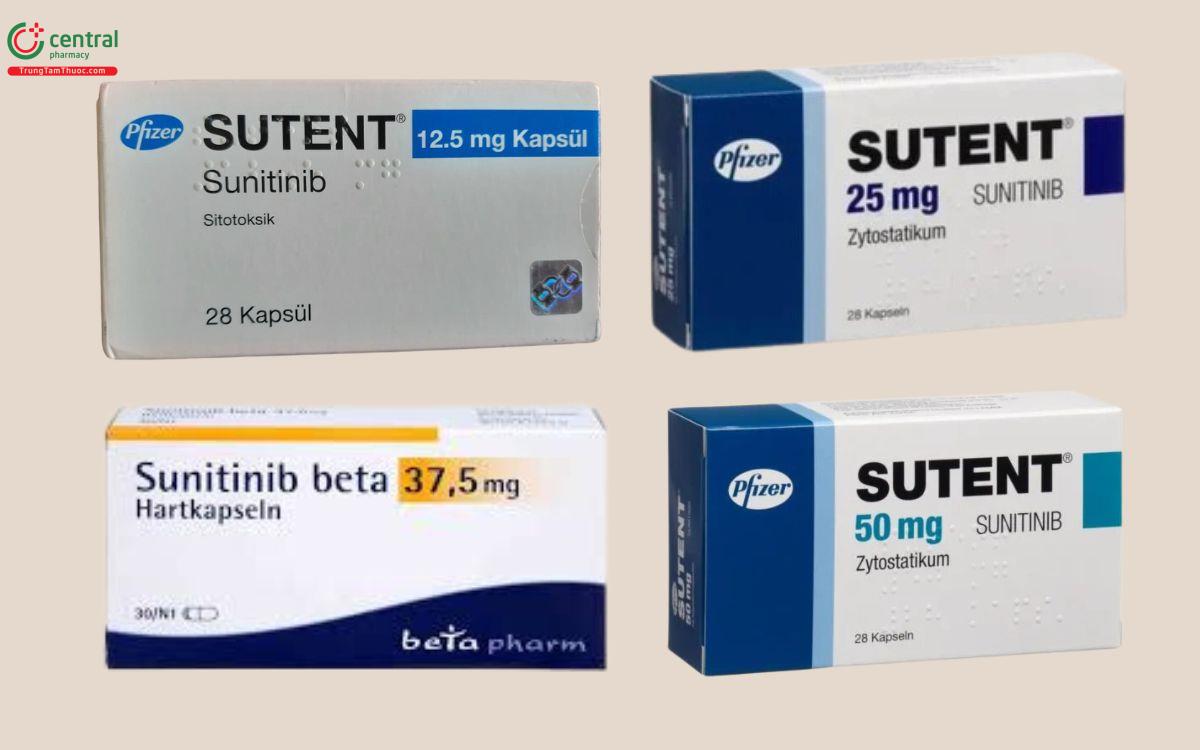
1 Dạng thuốc và hàm lượng
Viên nang chứa hàm lượng 12,5mg, 25mg, 37,5mg, 50mg Sunitinib.
2 Dược lực học
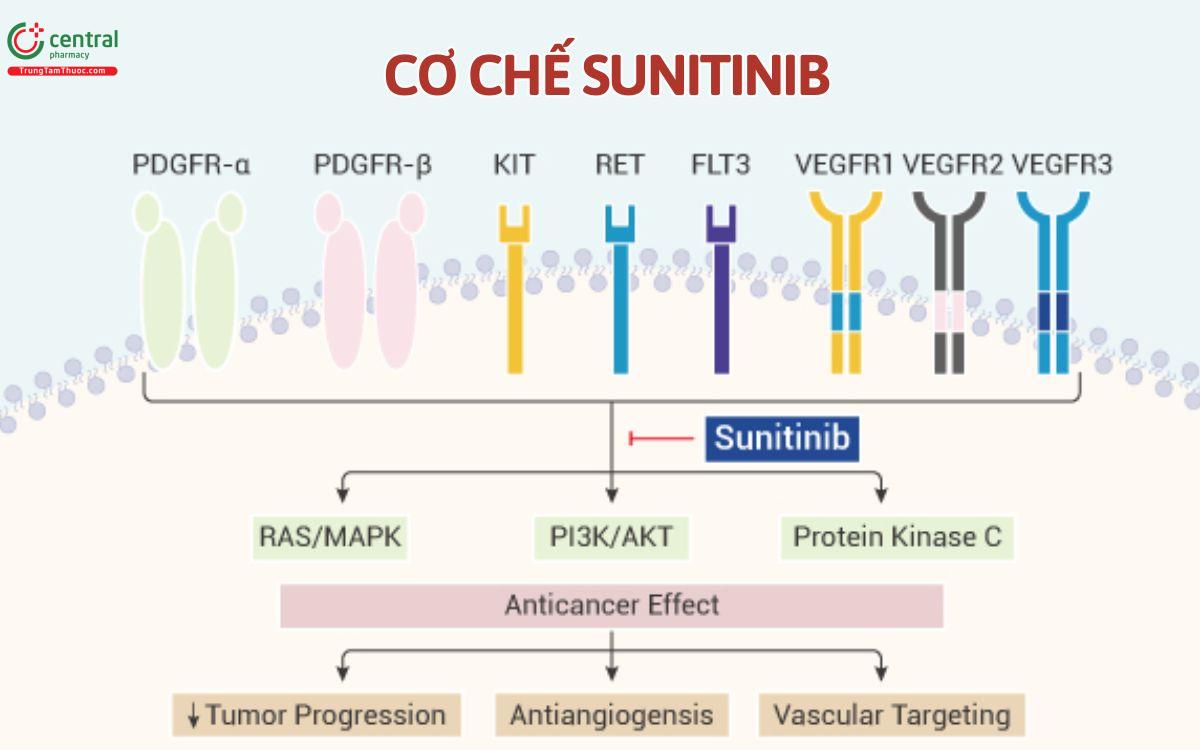
Các thụ thể tyrosine kinase, bao gồm các thụ thể yếu tố tăng trưởng có nguồn gốc từ tiểu cầu (PDGFR), các thụ thể yếu tố tăng trưởng nguyên bào sợi và các thụ thể yếu tố tăng trưởng nội mô mạch máu (VEGFR) và các phối tử của chúng, đã được chứng minh là đóng vai trò quan trọng trong sự phát triển của khối u và quá trình hình thành mạch máu.
Sunitinib là thuốc ức chế nhiều thụ thể tyrosine kinase (RTK) với khoảng hơn 80 kinase, một vài yếu tố quan trọng trong sự phát triển của tế bào ung thư như PDGFRa và PDGFRb, VEGFR1, VEGFR2 và VEGFR3, KIT, FLT3… Chất này ức chế mạnh thụ thể yếu tố tăng trưởng nội mô mạch máu, thụ thể yếu tố tăng trưởng có nguồn gốc từ tiểu cầu và c-Kit ngoài các kinase khác có tác dụng chống hình thành mạch máu và chống khối u đáng kể.
3 Dược động học
3.1 Hấp thu
Sau khi dùng đường uống, nồng độ thuốc sunitinib đật giá trị cao nhất trong huyết tương khoảng từ 6-12 giờ, và thuốc không bị ảnh hưởng bởi thức ăn.
3.2 Phân bố
Sunitinib có Thể tích phân bố khoảng 2230L, tỷ lệ liên kết với protein huyết tương của thuốc và chất chuyển hoá chính lần lượt là 95% và 90%.
3.3 Chuyển hoá
Sunitinib chủ yếu được chuyển hóa chủ yếu qua gan, bởi các con đường P450, CYP3A4.
3.4 Thải trừ
Thuốc và chất chuyển hoá được đào thải chủ yếu qua thận, lượng bài tiết qua phân chiếm 6.1% và qua thận chiêm 16%. Thuốc có thời gian bán thải trung bình khoảng 40-60 giờ.
4 Chỉ định
Sunitinib gần đây đã được chấp thuận trong điều trị một số bệnh, cụ thể:
- Liệu pháp đầu tay cho bệnh nhân ung thư biểu mô tế bào thận (RCC) tiến triển
- Điều trị bệnh nhân u mô đệm Đường tiêu hóa (GIST) sau khi bệnh tiến triển hoặc không dung nạp với liệu pháp ban đầu.
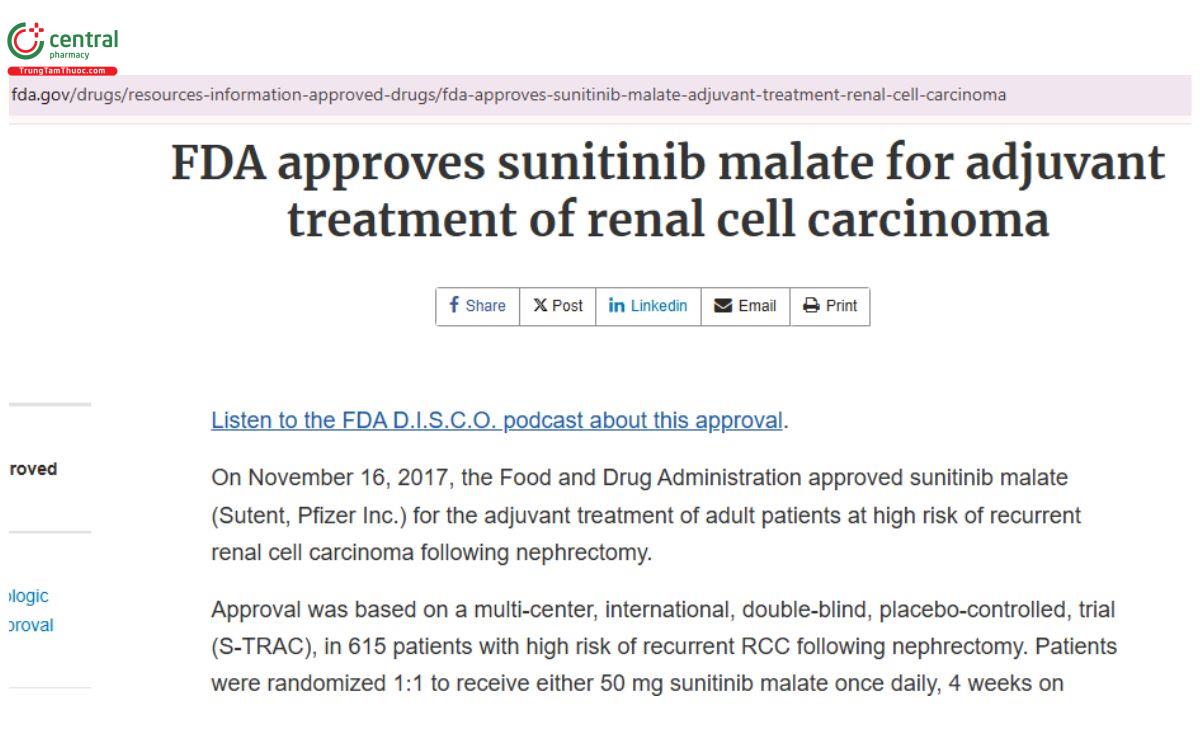
- Điều trị bổ trợ cho bệnh nhân nguy cơ tái phát ung thư biểu mô thận sau phẫu thuật.
- Điều trị khối u thần kinh nội tiết tuyến tụy tiến triển tại chỗ hoặc di căn khắp cơ quan ở người lớn
5 Chống chỉ định
Người mẫn cảm với thành phần của Sunitinib.
6 Liều dùng - Cách dùng
6.1 Liều dùng
Liều dùng khuyến cáo của sunitinib được khuyến cáo trong điều trị các bệnh ung thư như:
6.1.1 U mô đệm đường tiêu hóa
Sử dụng liều uống mỗi ngày 50mg liên tục trong 4 tuần, sau đó ngừng uống 2 tuần rồi lặp lại chu kỳ như trên. Uống thuốc đến khi không còn lợi ích trên lâm sàng cho người bệnh.
6.1.2 Ung thư tế bào thận
Sử dụng liều uống mỗi ngày 50mg liên tục trong 4 tuần, sau đó ngừng uống 2 tuần rồi lặp lại chu kỳ như trên. Uống thuốc đến khi không còn lợi ích trên lâm sàng cho người bệnh.
6.1.3 U thần kinh nội tiết tuyến tụy
Sử dụng liều uống mỗi ngày 37,5mg liên tục và không ngừng cho đến khi không còn lợi ích trên lâm sàng cho người bệnh.
6.2 Cách dùng
Uống trực tiếp viên thuốc với nước, có thể sử dụng chung với thức ăn hoặc không. Nếu quên liều dưới 12 giờ thì uống lại sớm nhất khi nhớ ra, nhưng quên liều trên 12 giờ thì bỏ qua liều và không uống bù vào ngày hôm sau.
7 Tác dụng không mong muốn
7.1 Thường gặp
Rối loạn tiêu hoá, thay đổi vị giác, mệt mỏi, tiêu chảy, phát ban, nôn mửa, táo bón, đổi màu da, đau bụng, buồn nôn, chán ăn, khó thở, tăng bạch cầu trung tính, đau khớp, chảy máu, đau đầu, suy nhược, giảm bạch cầu lympho, sốt, đau tay chân, đau lưng, đau cơ, ho, da khô, thay đổi màu tóc, giảm bạch cầu trung tính, rụng tóc, mất nước, hội chứng bàn tay-chân.
7.2 Ít gặp
Biến cố huyết khối tĩnh mạch, bệnh trĩ, viêm tuỷ, hội chứng giống cúm.
7.3 Hiếm gặp
Độc tính với gan, suy thận cấp, rối loạn chức năng tuyến thượng thận.
8 Tương tác thuốc
8.1 Chất ức chế CYP3A4 mạnh
Tránh dùng đồng thời chất ức chế CYP3A4 mạnh với sunitinib do làm tăng nồng độ sunitinib trong máu, làm tăng tác dụng phụ của thuốc này.
8.2 Chất gây cảm ứng CYP3A4 mạnh
Tránh dùng đồng thời chất gây cảm ứng CYP3A4 mạnh với sunitinib do làm giảm nồng độ sunitinib trong máu, làm giảm hiệu quả điều trị của thuốc này.
8.3 Thuốc kéo dài khoảng QT
Tránh dùng đồng thời với thuốc gây kéo dài khoảng QT vì làm tăng nguy cơ kéo dài khoảng QT gây biến chứng nguy hiểm, cần theo dõi thường xuyên bệnh nhân đang cần phải sử dụng chung.
9 Thận trọng
Không dùng thuốc trong thời kỳ mang thai do có thể gây dị tật bẩm sinh ở thai nhi, phụ nữ trong thời kỳ mang thai nên tránh thai khi điều trị và kéo dài đến 4 tuần sau liều cuối cùng, nam giới nên tránh thai trong 7 tuần sau liều cuối cùng.
Các triệu chứng nôn và buồn nôn có thể xảy ra kéo dài sau khi đã ngừng thuốc, có thể hỏi ý kiến bác sĩ để dùng thuốc giảm triệu chứng.
Các vấn đề nghiêm trọng về gan đã được báo cáo, nếu có triệu chứng như đau dạ dày, chán ăn, buồn nôn, mệt mỏi nên cảnh báo với bác sĩ.
Thận trọng với bệnh nhân có tiền sử bệnh tim mạch, huyết áp, rối loạn nhịp tim do thuốc có thể gây ra các vấn đề nghiêm trọng về tim.
Các phản ứng nghiêm trọng như ban đỏ đa dạng (EM), hội chứng Stevens-Johnson (SJS),hội chứng bệnh não trắng sau hồi phục (RPLS), hội chứng ly giải khối u đã được báo cáo, nếu có bất cứ dấu hiệu cảnh báo nào cần thông báo ngay với bác sĩ.
10 Thời kỳ mang thai và cho con bú
Dựa trên các nghiên cứu trên động vật cho thấy thuốc có thể gây quái thai cho thai nhi, nên không dùng thuốc trong khi có thai, và cần cảnh báo với phụ nữ về nguy cơ tiềm ẩn này. Cả nam và nữ nên thực hiện biện pháp tránh thai an toàn trong khi dùng thuốc.
Các nghiên cứu trên chuột cho thấy thuốc vào được sữa nên khuyến cáo không dùng cho phụ nữ cho con bú khi điều trị và ít nhất 4 tuần sau liều cuối cùng.
11 Bảo quản
Bảo quản ở nhiệt độ tủ phòng dưới 30 độ C, tránh ánh sáng chiếu trực tiếp vào thuốc.
Để xa tầm tay của trẻ nhỏ.
12 Quá liều
Chưa có báo cáo, trong trường hợp quá liều nên ngừng thuốc và cấp cứu.
13 Tài liệu tham khảo
Chuyên gia Drugbank. Sunitinib. Drugbank. Truy cập ngày 11 tháng 12 năm 2024.
Chuyên gia Drugs.com. Sunitinib Dosage . Drugs.com. Truy cập ngày 11 tháng 12 năm 2024.
Chuyên gia Pubchem. Sunitinib. Pubchem.Truy cập ngày 11 tháng 12 năm 2024.
Chuyên gia FDA. FDA approves sunitinib malate for adjuvant treatment of renal cell carcinoma. FDA. Truy cập ngày 11 tháng 12 năm 2024.