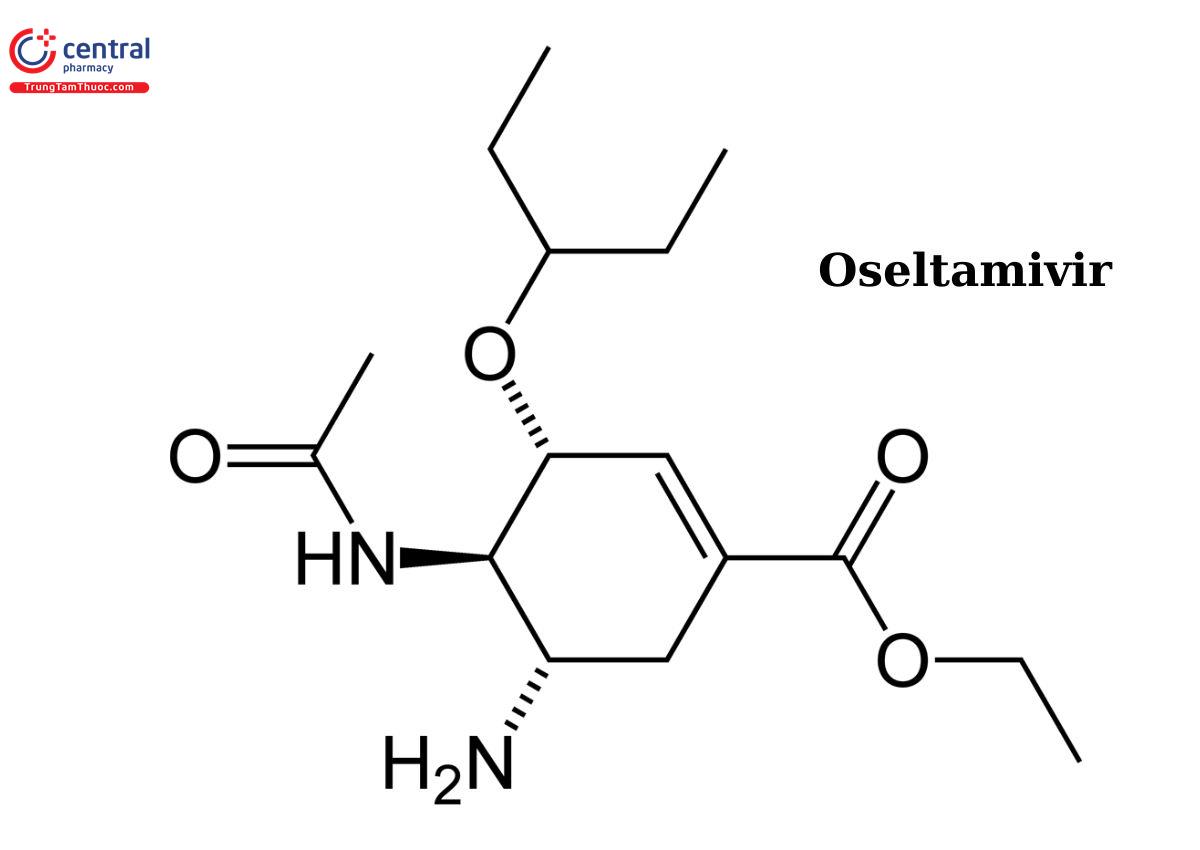
Oseltamivir
4 sản phẩm
 Dược sĩ Nguyễn Trang Dược sĩ lâm sàng - Đại học Dược Hà Nội
Dược sĩ Nguyễn Trang Dược sĩ lâm sàng - Đại học Dược Hà Nội
Ước tính: 5 phút đọc, Ngày đăng:
Cập nhật:
Nếu phát hiện nội dung không chính xác, vui lòng phản hồi thông tin cho chúng tôi tại đây
OSELTAMIVIR
Tên chung quốc tế: Oseltamivir.
Mã ATC: J05AH02.
Loại thuốc: thuốc kháng virus cúm type A và B.
1 Dạng thuốc và hàm lượng
Viên nang: 30mg: 45 mg; 75 mg oseltamivir.
Bột pha hỗn dịch uống: 6 mg/ml.
2 Dược lực học
Oseltamivir phosphate là một tiền thuốc có rất ít hoạt tính trước khi được thủy phân thành chất chuyển hóa có hoạt tính oseltamivir carboxylate. Oseltamivir carboxylate ức chế chọn lọc neuraminidase là một enzym đóng vai trò quan trọng trong quá trình nhân lên của Virus. Vì vậy, các thuốc ức chế enzym neuraminidase làm ngăn cản quá trình giải phóng các hạt virus cúm mới hình thành trong tế bào vật chủ nhiễm bệnh, từ đó hạn chế sự xâm nhập của virus vào tế bào vật chủ mới và ngăn chặn sự phát tán bệnh. Do sự nhân lên của Virus cúm trong đường hô hấp đạt đỉnh sau khi khởi phát bệnh từ 24-72 giờ nên các thuốc ức chế enzyme neuraminidase cần được Sử dụng càng sớm càng tốt. [1]
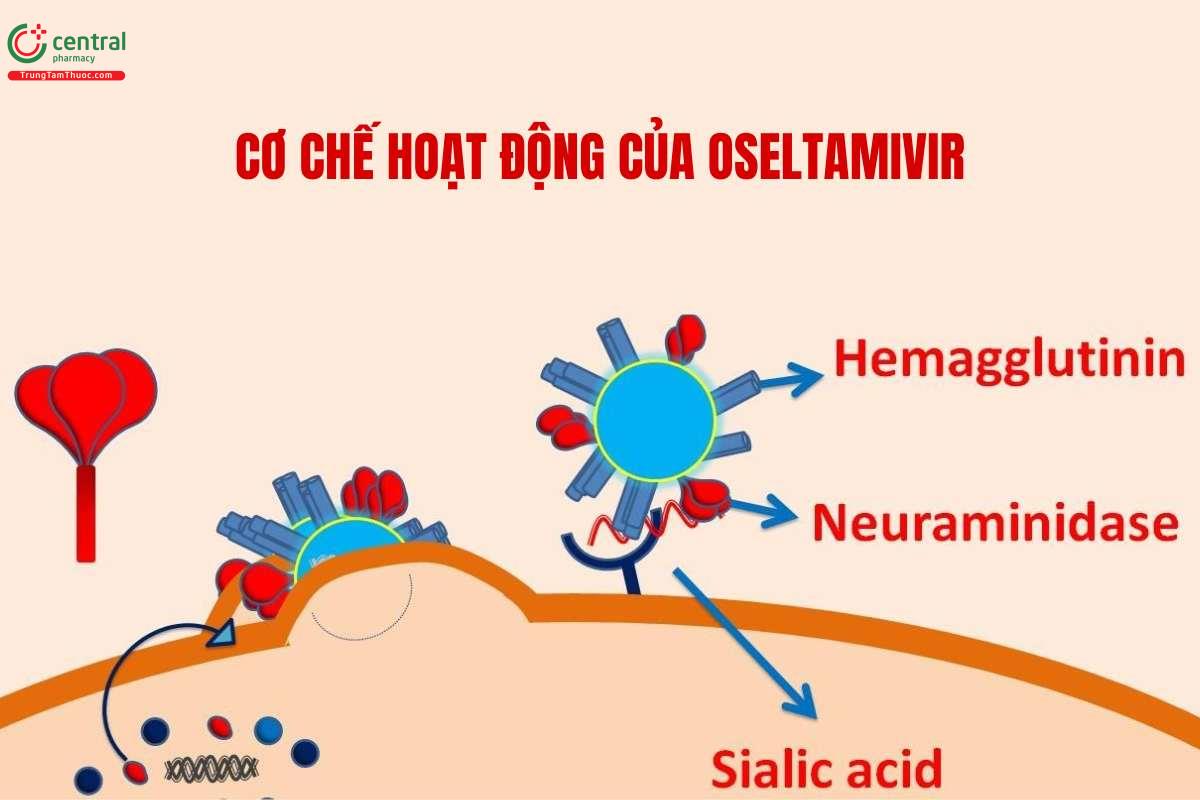
2.1 Phố tác dụng
Các dữ liệu In vitro cho thấy oseltamivir có tác dụng mạnh trên cả virus cúm type A và typ B. Oseltamivir ức chế mạnh và chọn lọc tất cả các subtype của enzyme neuraminidase cúm A (N1-N9) đã được thử nghiệm cho đến nay. Các chủng virus cúm mùa như cúm A (H3N2), cúm AH1N1) và cúm B nhạy cảm với oseltamivir in vitro. Oseltamivir cũng có tác dụng trên cúm gia cầm typ A bao gồm cúm A (H5NI) và một vài chủng virus cúm gia cầm typ A khác như H7N7, H7N9, H9N2, H10N8. Giảm nhạy cảm hoặc đề kháng với oseltamivir đã được ghi nhận với tỷ lệ hiếm gặp. Cơ chế chính khiến virus cúm A và cúm B giảm nhạy cảm với oseltamivir là do đột biến enzyme neuraminidase của virus. Năm 2005, Việt Nam ghi nhận hai trường hợp sử dụng oseltamivir điều trị cúm gia cầm A (H5N1) kháng thuốc. Chủng phân lập từ bệnh nhân cho thầy đột biến tại vị trí acid amin H274Y liên quan đến đề kháng oseltamivir mức độ cao. Cả hai bệnh nhân này sau đó đều tử vong.
2.2 Đề kháng chéo
Đề kháng chéo giữa oseltamivir và các thuốc ức chế enzyme neuraminidase khác như Zanamivir đã được ghi nhận đối với cả virus cúm A và cúm B. Tuy nhiên, do các thuốc này có thể gắn vào các vị trí khác nhau của enzyme neuraminidase hoặc tương tác với vị trí gắn theo các cách khác nhau nên không thể đưa ra kết luận chung về hiện tượng kháng chéo giữa các thuốc. Một số chủng virus cúm có thể giảm nhạy cảm với một thuốc nhưng vẫn nhạy cảm với thuốc còn lại trong nhóm. Ví dụ, chủng phân lập cúm A (H1N1)pdm09 với đột biến ở vị trí H275Y đề kháng với oseltamivir nhưng nhạy cảm với zanamivir. Cúm gia cầm A(H5N') với đột biến ở vị trí H274Y kháng oseltamivir nhưng nhạy cảm với zanamivir in vitro. Loại đột biến thay thế acid amin gây đã kháng chéo giữa các thuốc ức chế enzyme neuraminidase (oseltamivir, zanamivir) và các dẫn xuất adamantan (thuốc chẹn kênh ion M2: Amantadin, rimantadine) chưa được xác định. Tuy nhiên, một số chủng virus cúm có thể đề kháng với cả hai nhóm thuốc kháng virus điều trị cúm nếu có đồng thời cả đột biến neuraminidase gây đề kháng với các thuốc ức chế enzym này và đột biến thay thế M2 gây đề kháng với các thuốc chẹn kênh ion M2.
3 Dược động học
Oseltamivir phosphat được hấp thu tốt qua đường uống. Oseltamivir carboxylate sau khi hấp thu được phân bố khắp toàn cơ thể, bao gồm cả đường, hô hấp trên và dưới. Thể tích phân bố của oseltamivir phosphat dùng đường tĩnh mạch dao động trong khoảng 23 - 26 lít. Cả oseltamivir và oseltamivir carboxylate đều phân bố được vào sữa mẹ. Dữ liệu trên chuột và thỏ ghi nhận oseltamivir carboxylate có thể đi qua nhau thai, tuy nhiên, còn thiếu các dữ liệu về khả năng qua nhau thai của thuốc ở người. Tỷ lệ gắn với protein huyết tương của oseltamivir phosphat và oseltamivir carboxylate lần lượt là 42% và 3%, Sau khi sử dụng oseltamivir phosphat đường uống, oseltamivir carboxylate được phát hiện trong huyết tương trong vòng 30 phút và nồng độ đỉnh của thuốc đạt được trong vòng 3 - 4 giờ. Oseltamivir được chuyên hóa phần lớn (hơn 90%) nhờ enzyme esterase tại gan tạo thành chất chuyên hóa có hoạt tính oseltamivir carboxylate. Sau đó, oseltamivir carboxylate không được chuyển hóa thêm nữa. Oseltamivir phosphat và oseltamivir carboxylate không được chuyển hóa thông qua hệ enzym cytochrom P450. Hơn 99% oseltamivir carboxylate được thải trừ qua thận và dưới 20% liều đường uống oseltamivir đánh dấu phóng xạ được thải trừ qua phân. Nửa đời thải trừ của thuốc là 1- 3 giờ đối với oseltamivir phosphat và 6 - 10 giờ đối với oseltamivir carboxylate.
Sinh khả dụng tuyệt đối của oseltamivir carboxylate là 80% sau khi dùng oseltamivir phosphat đường uống. Thức ăn không ảnh hưởng đến nồng độ đỉnh trong huyết tương hay Diện tích dưới đường cong nồng độ - thời gian (AUC) của Oseltamivir carboxylate.
Ở trẻ sơ sinh và trẻ nhỏ tử 2 tuần đến dưới 1 tuổi, liều oseltamivir 3 mg/kg/lần x 2 lần/ngày cho nồng độ thuốc tương đương hoặc cao hơn so với nồng độ ghi nhận trên người lớn hoặc trẻ trên 1 tuổi dùng liều thông thường. Thải trừ oseltamivir phosphat oseltamivir carboxylate ở trẻ nhỏ mạnh hơn so với người lớn. Thải trừ oseltamivir carboxylate tỉ lệ nghịch với tuổi của trẻ cho đến 12 tuổi. Dược động học của thuốc ở trẻ trên 12 tuổi tương tự như ở người lớn.
Đối với người cao tuổi (6S - 78 tuổi) sử dụng Oseltamivir đường uống, nồng độ oseltamivir carboxylate ở trạng thái ổn định cao hơn 25 - 35% so với người trẻ dùng liều tương đương. Nửa đời thải trừ của thuốc ở người cao tuổi được ghi nhận tương tự như ở người trẻ.
Trên bệnh nhân suy thận ở các mức độ khác nhau sử dụng oseltamivir phosphat 100mg/lần x 2 lần/ngày (1,3 lần liều tối đa khuyến cáo) trong vòng 5 ngày, nồng độ oseltamivir carboxylate tăng lên theo mức độ suy thận của bệnh nhân. Trên bệnh nhân thực hiện thẩm phân phúc mạc liên tục dùng 30mg oseltamivir liều đơn hoặc lều 1 lần/tuần, nồng độ đỉnh của oseltamivir carboxylate cao xấp xỉ gấp 3 lần so với nông độ đỉnh của thuốc trên bệnh nhân có chức năng thận bình thường dùng liều 75mg x 2 lần/ngày. Thải trừ qua thận của oseltamivir carboxylate giảm tuyến tính với Độ thanh thải creatinin.
Dữ liệu hạn chế trên bệnh nhân xơ gan cho thấy hoạt tính của enzyme carboxylesterase trong trường hợp suy gan trung bình vẫn đủ để chuyển hóa oseltamivir phosphat thành oseltamivir carboxylate. Nồng độ oseltamivir carboxylate ở người suy gan mức độ nhẹ và trung bình tương đương với nồng độ thuốc ở người có chức năng gan bình thường dùng liều tương đương.
4 Chỉ định
Điều trị nhiễm cúm A và cúm B cấp, không biến chứng cho người lớn và trẻ em trên 2 tuần tuổi có các triệu chứng nhiễm cúm trong vòng dưới 48 giờ. Hiệu quả của thuốc chưa được thiết lập đối với những trường hợp sử dụng thuốc trong vòng hơn 48 giờ sau khi xuất hiện triệu chứng cúm.
Dự phòng cúm A và cúm B cho người lớn và trẻ trên 1 tuổi có tiếp xúc với người bị nhiễm virus cúm hoặc sinh sống trong cộng đồng hiện đang có virus cúm lưu hành. Trong đợt bùng phát dịch cúm trên diện rộng, thuốc cũng có thể được sử dụng để dự phòng cho trẻ dưới 1 tuổi.
Loại virus cúm, tính nhạy cảm và đề kháng của virus cúm đối với thuốc có thể thay đổi theo thời gian. Do đó, việc sử dụng oseltamivir cần được cân nhắc dựa trên từng cá thể, vùng địa lý và cộng đồng sinh sống, và dựa trên những thông tin hiện có về tính nhạy cảm của virus đối với thuốc và hiệu quả điều trị của thuốc.

5 Chống chỉ định
Tiền sử quá mẫn với thuốc.
6 Thận trọng
Oseltamivir chỉ cho hiệu quả trên virus cúm. Hiện không có bằng chứng về hiệu quả của thuốc trên những tác nhân gây bệnh khác ngoài virus cúm. Các nhiễm khuẩn nặng có thể khởi đầu với những triệu chứng giống cúm, các loại nhiễm khuẩn đồng mắc hoặc biến chứng trong đợt mắc cúm. Hiện không có bằng chứng về hiệu quả của oseltamivir đề ngăn ngừa các biến chứng này, do đó, cán bộ y tế cần nắm được nguy cơ nhiễm khuẩn thứ phát Ở bệnh nhân cúm và cân nhắc liệu pháp điều trị nhiễm khuẩn phù hợp cho bệnh nhân.
Việc sử dụng oseltamivir không thể thay thế việc tiêm phòng vắc xin cúm và không ảnh hưởng đến việc tiêm phòng cúm hàng năm cho từng cá thể. Hiệu quả chống cúm chỉ kéo dài trong thời gian sử dụng oseltamivir. Chỉ nên dùng thuốc để điều trị và dự phòng cúm khi các dữ liệu dịch tễ cho thấy có các virus cúm đang lưu hành trong cộng đồng. Các dữ liệu cho thầy tính nhạy cảm của các chủng virus cúm đang lưu hành với oseltamivir rất dao động. Do đó, cần cân nhắc các thông tin cập nhật về tính nhạy cảm của thuốc với loại virus đang lưu hành để đưa ra quyết định sử dụng thuốc cho bệnh nhân.
Các dữ liệu theo dõi an toàn thuốc sau khi lưu hành trên thị trường đã ghi nhận phản ứng phản vệ và phản ứng trên da nghiêm trọng bao gồm hội chứng hoại tử thượng bì nhiễm độc, hội chứng Stevens-Johnson và hồng ban đa dạng. Trong trường hợp xảy ra các phản ứng dị ứng hoặc nghi ngờ xảy ra các phản ứng dị ứng, bệnh nhân cần ngừng thuốc và được xử trí kịp thời.
Hiệu quả của oseltamivir trên bệnh nhân có tình trạng lâm sàng nặng, không ổn định, bệnh nhân suy giảm miễn dịch, bệnh nhân có bệnh tim mạn tính hoặc bệnh đường hô hấp chưa được thiết lập. Nghiên cứu tiến hành trên bệnh nhân có bệnh tim mạn tính hoặc bệnh đường hô hấp cho thấy không có sự khác biệt về tần suất ghi nhận biến chứng giữa nhóm điều trị và nhóm đối chứng.
Hiện chưa có khuyến cáo về liều dùng của thuốc cho trẻ sinh non (dưới 36 tuần tuổi thai).
Cần hiệu chỉnh liều trên những bệnh nhân người lớn có suy thận mức độ vừa và nặng. Hiện không có đủ dữ liệu lâm sàng trên trẻ nhỏ có suy thận để đưa ra khuyến cáo về liều dùng của thuốc trên đối tượng này.
Dữ liệu về an toàn thuốc sau khi lưu hành trên thị trường đã ghi nhận các biến cố trên thần kinh - tâm thần như: mê sảng và thay đổi hành vi, thậm chí dẫn đến hậu quả tử vong. Hiện không thể ước tính tần suất của các biến cố này dựa trên dữ liệu sử dụng thuốc do những biến cố này được báo cáo một cách tự nguyện từ thực hành lâm sàng. Những biến có trên thần kinh - tâm thần thường khởi phát và hồi phục nhanh, được ghi nhận chủ yếu trên trẻ em và trẻ vị thành niên. Mối liên quan giữa việc sử dụng oseltamivir và các biến cố thần kinh- tâm thần chưa được thiết lập do những biến cố này cũng được ghi nhận trên những bệnh nhân cúm không sử dụng oseltamivir. Cúm có thể đi kèm với các triệu chứng trên thần kinh - tâm thần như: ảo giác, mê sảng, hành vi bất thường. Cần thận trọng theo dõi các bệnh nhân cúm sử dụng oseltamivir để phát hiện các dấu hiệu hành vi bất thường. Trong trường hợp xảy ra các biến cố này, cần cân nhắc lợi ích và nguy cơ của việc tiếp tục sử dụng thuốc trên từng bệnh nhân.
7 Thời kỳ mang thai
Cúm có liên quan đến các biến có bất lợi với người mẹ và thai nhi, bao gồm tử vong thai kỳ, sảy thai, dị tật thai nhi, trong đó có dị tật tim bẩm sinh, trẻ sinh non, nhẹ cân hoặc nhỏ hơn so với tuổi thai.
Ngoài ra, tăng thân nhiệt, một triệu chứng phổ biến của cúm, xảy ra trong vòng 3 tháng đầu thai kỳ làm tăng gấp đôi nguy cơ dị tật thần kinh cho thai nhi. Nếu xảy ra trong quá trình sinh, tăng thân nhiệt ở người mẹ là một yếu tố nguy cơ dẫn đến co giật, bại não và tử vong ở trẻ sơ sinh.
Các nghiên cứu trên động vật cho thấy sự tăng phụ thuộc liều tỷ lệ xảy ra các dị tật xương không nghiêm trọng ở thỏ và chuột khi sử dụng thuốc ở liều tương ứng gấp 50 lần và 100 lần liều dùng ở người. Hiện còn thiếu dữ liệu từ các nghiên cứu trên người về độ an toàn của oseltamivir khi sử dụng trong thai kỳ. Một số nghiên cứu đã được công bố cho thầy thuốc sử dụng ở bất kỳ giai đoạn nào của thai kỳ không làm tăng dị tật thai nhi. Tuy nhiên, các nghiên cứu này có những hạn chế về cỡ mẫu, sử dụng các nhóm so sánh khác nhau và một số nghiên cứu thiếu dữ liệu về liều dùng của thuốc. Các dữ liệu theo dõi độ an toàn của việc sử dụng oseltamivir ở phụ nữ mang thai sau khi thuốc được lưu hành và từ các nghiên cứu quan sát cũng cho thấy thuốc không gây dị tật và các độc tính khác trên thai nhi. Do đó, có thể sử dụng oseltamivir cho phụ nữ mang thai khi cần thiết nếu lợi ích vượt trội so với nguy cơ của thuốc.
8 Thời kỳ cho con bú
Những dữ liệu hiện có cho thấy, oseltamivir và chất chuyển hóa có hoạt tính được bài tiết vào sữa mẹ nhưng ở nồng độ thấp và ít có khả năng gây độc tính trên trẻ sơ sinh bú mẹ. Do đó, oseltamivir có thể được sử dụng trên phụ nữ cho con bú nếu thật cần thiết và thận trọng cân nhắc lợi ích và nguy cơ của thuốc, khả năng gây bệnh của chủng virus cúm đang lưu hành và tình trạng của người mẹ.
9 Tác dụng không mong muốn (ADR)
Nhìn chung ở người lớn và trẻ vị thành niên, ADR phố biến nhất là: buồn nôn và nôn. Các phản ứng này thường xảy ra trong ngày đầu tiên hoặc ngày thử hai dùng thuốc và tự hết sau 1 - 2 ngày. Ở trẻ em, phản ứng thường gặp nhất là nôn. Trong hầu hết các trường hợp. các ADR này không dẫn đến việc phải ngừng thuốc.
Một số ADR nghiêm trọng được ghi nhận với tỷ lệ hiếm gặp sau khi thuốc được lưu hành trên thị trường bao gồm: phản ứng phản vệ và phản ứng kiểu phản vệ, bệnh gan (viêm gan ác tính, rối loạn chức năng gan và vàng da), phù mạch máu - thần kinh, Hội chứng Stevens-Johnson, hội chứng lyell, xuất huyết tiêu hóa và rối loạn thần kinh - tâm thần.
9.1 Rất thường gặp
Thần kinh: đau đầu.
Tiêu hóa: buồn nôn.
9.2 Thường gặp
Nhiễm khuẩn: viêm phế quản, viêm mũi - họng, nhiễm khuẩn đường hô hấp trên, viêm xoang, viêm tai giữa (trẻ em), nhiễm virus Herpes simplex.
Thần kinh: mất ngủ.
Hô hấp: ho, đau họng, chảy nước mũi.
Tiêu hóa: đau bụng, nôn, khó tiêu, tiêu chảy.
Thị giác: viêm kết mạc (trẻ em).
Thính giác: đau tai (trẻ em).
Toàn thân: đau, bao gồm đau tay chân, chóng mặt, mệt mỏi, sốt.
9.3 Ít gặp
Miễn dịch: phản ứng quá mẫn.
Thần kinh: giảm nhận thức, co giật.
Tim mạch: loạn nhịp.
Gan: tăng enzym gan.
Da và mô mềm: eczema, viêm da, ngứa, mày đay.
Thính giác: bệnh màng nhĩ (trẻ em).
9.4 Hiếm gặp
Máu: giảm tiểu cầu.
Miễn dịch: phản ứng phản vệ, phản ứng kiểu phản vệ.
Tâm thần: kích thích, rối loạn hành vi, lo âu, lú lẫn, ảo giác, mê sảng, ác mộng, tự gây tổn thương cho bản thân.
Thị giác: rồi loạn thị giác.
Tiêu hóa: xuất huyết tiêu hóa, viêm đại tràng xuất huyết.
Gan: viêm gan ác tính, suy gan, viêm gan.
Da và mô mềm: phù mạch máu - thần kinh, hồng ban đa dạng, hội chứng Stevens-Johnson, hội chứng Lyell.
9.5 Hướng dẫn cách xử trí ADR
Nhiều ADR ghi nhận khi sử dụng oseltamivir tương tự như triệu chứng. của cúm. Phản ứng đau đầu thường gặp sớm, trong vòng 1 -2 ngày đầu tiên và thường tự hết sau 1 - 2 ngày. Các ADR trên thần kinh - tâm thần đã được ghi nhận ở những bệnh nhân bị cúm dùng thuốc, đặc biệt ở trẻ em và trẻ vị thành niên. Tuy nhiên, phản ứng này cũng được ghi nhận ở những bệnh nhân cúm không dùng oseltamivir. Những phản ứng trên thần kinh - tâm thần này thường diễn ra trong thời gian ngắn và tự hồi phục. Tuy mối liên quan giữa việc dùng thuốc và những phản ứng trên thần kinh - tâm thần chưa được thiết lập, cần thận trọng theo dõi những thay đổi hành vi của bệnh nhân khi sử dụng oseltamivir.
Xem xét kỹ lợi ích và nguy cơ trên từng bệnh nhân đề quyết định việc tiếp tục dùng thuốc cho bệnh nhân.
Ngừng sử dụng thuốc trong trường hợp nghi ngờ hoặc xảy ra các phản ứng dị ứng nghiêm trọng như: phản ứng phản vệ, hội chứng Stevens-Johnson, hội chứng Lyell, hồng ban đa dạng.
10 Liều lượng và cách dùng
10.1 Cách dùng
Oseltamivir có dạng viên nang hoặc dạng bột pha hỗn dịch uống. Dạng bột pha hỗn dịch uống được sử dụng trong trường hợp bệnh nhân không sử dụng được dạng viên nang. Dạng hỗn dịch uống cần được pha chế bởi dược sĩ bằng cách hòa trộn kỹ bột thuốc với nước. Trong trường hợp dạng hỗn dịch thuốc không có sẵn, có thể mở viên nang và trộn với các dung dịch được làm ngọt như siro để pha chế thuốc. Đối với trẻ dưới 1 tuổi, cần cung cấp dụng cụ chia liều phù hợp đề có thể đong chính xác được những thể tích thuốc nhỏ. Thuốc có thể được sử dụng cùng thức ăn hoặc không. Tuy nhiên, việc dùng thuốc cùng thức ăn có thể làm tăng hấp thu thuốc. Cần hiệu chỉnh liều dùng trên bệnh nhân suy thận mức độ vừa và nặng.
10.2 Liều lượng
10.2.1 Điều trị
Bắt đầu dùng thuốc trong vòng 48 giờ sau khi có triệu chứng cúm.
Người lớn và trẻ vị thành niên (trên 13 tuổi): Liều khuyến cáo 75mg/lần x 2 lần/ngày trong vòng 5 ngày.
Trẻ em (2 tuần - 12 tuổi): Xem bảng 1.
10.2.2 Dự phòng
Bắt đầu dùng thuốc trong vòng 48 giờ sau khi tiếp xúc với người bị nhiễm virus hoặc dùng thuốc đề dự phòng khi có dịch bệnh lưu hành.
Người lớn và trẻ vị thành niên (trên 13 tuổi): Liều khuyến cáo là 75mg/lần x 1 lần/ngày trong vòng ít nhất 10 ngày sau khi tiếp xúc với người bị nhiễm virus hoặc trong vòng 6 tuần khi có dịch bệnh lưu hành. Bệnh nhân suy giảm miễn dịch có thể kéo dài thời gian dùng thuốc lên tới 12 tuần. Hiệu quả dự phòng của thuốc kéo dài trong thời gian sử dụng thuốc.
Trẻ em (1 tuổi - 12 tuổi): Xem bảng 1.
Trẻ em được khuyến cáo dùng thuốc để dự vòng trong vòng 10 ngày sau khi tiếp xúc với người bị nhiễm virus hoặc trong vòng 6 tuần khi có dịch bệnh lưu hành.
| Cân nặng | Liều điều trị (trong vòng 5 ngày) | Liều điều trị dự phòng (trong vòng 10 ngày) | Thể tích hỗn dich uống (6mg/ml cho mỗi liều) |
| 2 tuần đến 1 tuổi | |||
| Tất cả các mức cân nặng | 3 mg/kg/lần x 2 lần/ngày | - | 0,5 ml/kg |
| 1 tuổi đến 12 tuổi | |||
| Dưới 15kg | 30 mg/lần x2 lần/ngày | 30 mg/lần x 1 lần/ngày | 5ml |
| 15,1 kg - 23 | 45 mg/lần x 2 lần/ngày | 45 mg/lần x 1 lần/ngày | 7,5 ml |
| 23,1kg-40kg | 60 mg/lần x 2 lần/ngày | 60 mg/lần x 1 lần/ngày | 10 ml |
| Trên 40,1kg | 75 mg/lần x2 lần/ngày | 75 mg/lần x 1 lần/ngày | 12,5 ml |
Bệnh nhân suy thận: Xem Bảng 2.
Thời gian dùng thuốc để dự phòng được khuyến cáo đối với bệnh nhân suy thận tương tự như bệnh nhân có chức năng thận bình thường là trong vòng ít nhất 10 ngày sau khi tiếp xúc với người bị nhiễm virus hoặc trong vòng 6 tuần khi có dịch bệnh lưu hành (hoặc 12 tuần đổi với bệnh nhân suy giảm miễn dịch).
| Mức độ suy thận (độ thanh thải creatinin) | Liều điều trị khuyến cáo | Liều dự phòng khuyến cáo |
| Mức độ nhẹ (60 - 90ml/phút) | 75mg/lần x 2 lần ngày trong vòng 5 ngày | 75mg lần x 1 lần ngày |
| Mức độ trung bình (30 - 60ml/phút) | 30 mg/lần x 2 lần/ngày trong vòng 5 ngày | 30 mg/lần x 1 lần/ngày |
Mức độ nặng (10 - 30 ml/phút) | 30 mg/lần x 1 lần/ngày trong vòng 5 ngày | 30 mg cách ngày |
| Bệnh nhân suy thận giai đoạn cuối có lọc máu (≤ 10ml/phút) | Liều khởi đầu 30mg, sau đó dùng liều 30mg sau mỗi chu kỳ lọc máu (thời gian dùng thuốc không quá 5 ngày) | Liều khởi đầu 30 mg và sau đó dùng liều 30mg cách mỗi chu kỳ lọc máu |
| Bệnh nhân suy thận giai đoạn cuối có thẩm phân phúc mạc liên tục ngoại trú (< 10ml/phút) | Dùng liều duy nhất 30mg | Liều khởi đầu 30mg, sau đó dùng liều 30 mg x 1 lần/tuần |
| Bệnh nhân suy thận giai đoạn cuối không lọc máu | Không khuyến cáo | Không khuyến cáo dùng thuốc |
11 Tương tác thuốc
Do oseltamivir ít gắn vào protein huyết tương, chuyển hóa không phụ thuộc vào cytochrom P450 và glucuronidase nên thuốc ít khả năng tương tác với các thuốc thông qua các cơ chế này. Không cần hiệu chỉnh liều thuốc khi sử dụng đồng thời oseltamivir với các thuốc Amoxicilin, Paracetamol, Aspirin, cimetidin, thuốc kháng acid (Magie và Nhôm Hydroxyd và Canxi cacbonat), rimantadine, amantadine và warfarin (trên bệnh nhân đã sử dụng warfarin ổn định).
Cần thận trọng khi sử dụng đồng thời oseltamivir với các thuốc được thải trừ qua thận và có khoảng điều trị hẹp như: clopropamid, methotrexat và phenylbutazon.
Probenecid: Việc dùng đồng thời oseltamivir và Probenecid có thể làm tăng nồng độ của chất chuyển hóa có hoạt tính của oseltamivir lên khoảng 2 lần do giảm thải trừ qua thận. Tuy nhiên, không cần hiệu chỉnh liều khi dùng phối hợp này ở người có chức năng thận bình thường. Vắc xin cúm sống, giảm hoạt lực: Tương tác khi sử dụng đồng thời oseltamivir và vắc xin cúm sống, giảm hoạt lực chưa được đánh giá. Tuy nhiên, do Oseltamivir có khả năng ức chế sự nhân lên của virut trong vắc xin cúm sống nên thuốc có thể làm giảm hiệu quả của vắc xin. Tránh sử dụng vắc xin cúm sống, giảm hoạt lực trong vòng 2 tuần trước hoặc 48 giờ sau khi dùng oseltamivir, trừ khi có chỉ định.
Vắc xin cúm bất hoạt: Vắc xin cúm bất hoạt có thể được sử dụng ở bắt kỳ thời điểm nào và không bị ảnh hưởng bởi việc sử dụng oseltamivir.
12 Quá liều và xử trí
Dữ liệu từ các thử nghiệm lâm sàng và theo dõi an toàn thuốc sau khi thuốc lưu hành trên thị trường không ghi nhận các biến cố bất lợi liên quan đến quá liều thuốc. Các biến cố bất lợi ghi nhận ở những trường hợp dùng quá liều thuốc có đặc điểm và phân bố tương tự như ở những trường hợp dùng liều điều trị.
13 Tài liệu tham khảo
1. Dược thư quốc gia Việt Nam, lần xuất bản thứ ba. Đây là phiên bản mới nhất của Dược thư Việt Nam do Bộ Y tế ban hành Quyết định số 3445/QĐ-BYT ngày 23 tháng 12 năm 2022. Trang 1239-1242, tải PDF TẠI ĐÂY