Fenofibrate
70 sản phẩm
 Dược sĩ Hương Trà Dược sĩ lâm sàng - Đại học Y Dược Thái Nguyên
Dược sĩ Hương Trà Dược sĩ lâm sàng - Đại học Y Dược Thái Nguyên
Ước tính: 3 phút đọc, Ngày đăng:
Cập nhật:
Nếu phát hiện nội dung không chính xác, vui lòng phản hồi thông tin cho chúng tôi tại đây
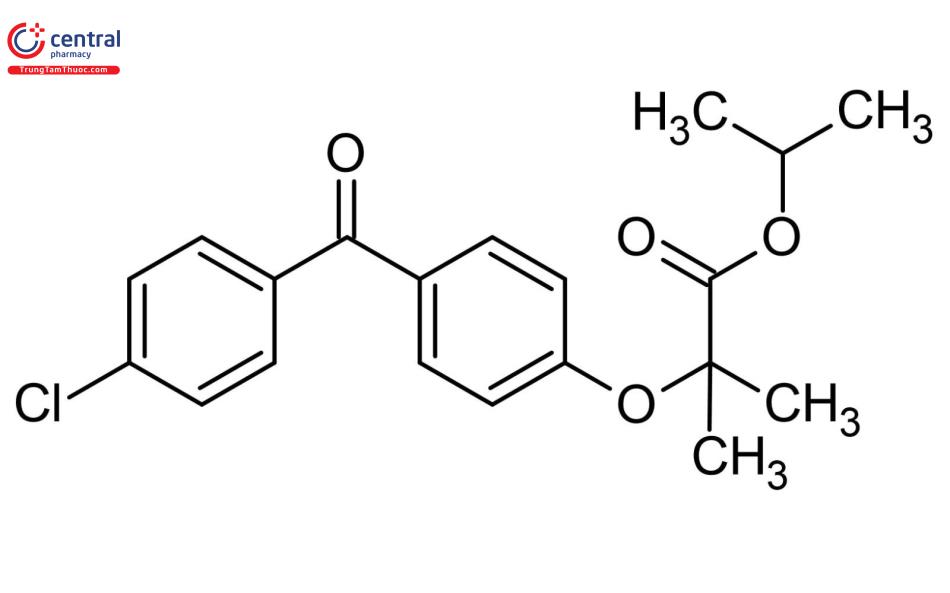
FENOFIBRAT
Tên chung quốc tế: Fenofibrate.
Mã ATC: C10AB05.
Loại thuốc: Thuốc hạ lipid huyết (nhóm fibrat).
1 Dạng thuốc và hàm lượng
Dạng bào chế không vi hạt: Viên nang 100 mg, 200 mg, 300 mg.
Dạng bào chế vi hạt chuẩn: Viên nang 67 mg, 200 mg,
Dạng bào chế có Sinh khả dụng cải tiến (dạng vi hạt hoặc không vi hạt): Viên nang: 43 mg, 130 mg; 30 mg, 90 mg; 50 mg, 150 mg; viên nén: 40mg, 120 mg; 48 mg, 145 mg; viên nén bao phim: 54 mg, 160 mg.
2 Dược lực học
Fenofibrat là một dẫn chất của acid fibric có tác dụng hạ lipid huyết. Có sự giảm cholesterol của các lipoprotein tỷ trọng thấp và rất thấp (LDL, VLDL) là những thành phần gây xơ vữa mạch và tăng cholesterol của lipoprotein tỷ trọng cao (HDL). Mối liên quan giữa tăng cholesterol máu và xơ vữa động mạch đã được xác lập và cả mối liên quan giữa xơ vữa động mạch và nguy cơ mạch vành. Nồng độ HDL hạ có liên quan đến nguy cơ mạch vành cao. Nồng độ triglyceride cao cũng có liên quan đến tăng nguy cơ tim mạch. Mặc dù các fibrat có thể làm giảm nguy cơ các sự cố bệnh mạch vành ở người có HDL-cholesterol thấp hoặc triglyceride cao nhưng các statin (các chất ức chế HMG-CoA reductase) nên được ưu tiên dùng trước. Các fibrat chỉ là thuốc điều trị hàng đầu đối với những người bệnh có nồng độ triglycerid máu cao hơn 10 mmol/lit hoặc người không dung nạp được statin.
Fenofibrat cũng làm giảm acid uric huyết ở người bình thường và người tăng acid uric huyết do làm tăng đào thải acid uric ra nước tiểu. [1]
3 Dược động học
Fenofibrat được hấp thu ngay ở Đường tiêu hóa khi uống cùng với thức ăn. Hấp thu thuốc của một số dạng bào chế có thể bị giảm khi không uống cùng thức ăn. Thuốc nhanh chóng thủy phân thành acid fenofibric là chất có hoạt tính, chất này được gắn tới 99% vào Albumin huyết tương và nồng độ đỉnh trong huyết tương xuất hiện khoảng 5 giờ sau khi uống. Ở người có chức năng thận bình thường nửa đời trong huyết tương của acid fenofibric vào khoảng 20 giờ nhưng thời gian này tăng lên rất nhiều ở người mắc bệnh thận, acid fenofibric tích lũy đáng kể ở người suy thận uống fenofibrat hàng ngày. Acid fenofibric đào thải chủ yếu qua nước tiểu (70% trong vòng 24 giờ), dưới dạng liên hợp glucuronic, dưới dạng khử của acid fenofibric và chất liên hợp glucuronic của nó. Hầu hết các sản phẩm được đào thải trong vòng 6 ngày.
4 Chỉ định
Phối hợp với chế độ ăn và các biện pháp khác để điều trị tăng lipid huyết thể hỗn hợp khi không dung nạp hoặc chống chỉ định với statin.
Phối hợp với chế độ ăn và các biện pháp khác để điều trị tăng triglycerid huyết nặng.
Phối hợp với statin để điều trị tăng lipid hỗn hợp nếu triglycerid và HDL-cholesterol không được kiểm soát đầy đủ ở bệnh nhân có nguy cơ tim mạch cao.
5 Chống chỉ định
Quá mẫn với fenofibrat.
Suy gan (bao gồm xơ gan ứ mật tiên phát và chức năng gan thường dai dẳng không rõ nguyên nhân).
Suy thận nặng (eGFR < 30 ml/phút/1,73 m3).
Tiền sử bệnh túi mật.
Viêm tụy cấp hoặc mạn trừ trường hợp viêm tụy cấp do tăng triglycerid máu nặng.
Có phản ứng dị ứng ánh sáng khi điều trị với các fibrat hoặc Ketoprofen.
6 Thận trọng
Tăng aminotransferase huyết thanh (AST, ALT) vượt quá 3 lần mức bình thường được thông báo ở khoảng 5% người bệnh dùng fenofibrat trong thử nghiệm. Viêm gan hoạt động mạn tính và viêm gan ứ mật xảy ra sớm sau vài tuần hoặc xảy ra muộn sau vài năm kể từ khi bắt đầu dùng fenofibrat; xơ gan kết hợp với viêm gan hoạt động mạn tính cũng được thông báo ở một số hiếm trường hợp. Phải kiểm tra chức năng gan trước khi điều trị và theo dõi chức năng gan định kỳ (3 tháng một lần trong 12 tháng đầu) trong quá trình điều trị.
Nếu nồng độ aminotransferase huyết thanh vượt quá 3 lần mức bình thường thì phải ngừng điều trị fenofibrat. Fenofibrat, cũng như các dẫn chất acid fibric khác (như gemfibrozil) có thể làm tăng bài xuất cholesterol vào mật, dẫn đến bệnh sỏi mật. Nếu kiểm tra túi mật thấy có sỏi thì phải ngừng fenofibrat. Viêm cơ, bệnh cơ và/hoặc tiêu cơ vân đã được thông báo ở người bệnh dùng fenofibrat hoặc các dẫn chất acid fibric khác. Tiêu cơ vân và các biến chứng khác cũng đã được thông báo ở người bệnh dùng fenofibrat cùng với một số thuốc hạ lipid huyết khác, thí dụ các statin (các chất ức chế HMG-CoA reductase). Các bệnh nhân dùng fenofibrat phải được hướng dẫn báo cáo ngay khi thấy đau cơ không rõ nguyên nhân, hoặc nhạy cảm đau, yếu, đặc biệt nếu kèm khó ở hoặc sốt. Phải theo dõi định kỳ enzym creatin kinase (CK hoặc CPK) ở những người bệnh có những tác dụng phụ đó. Phải ngừng điều trị fenofibrat, nếu CPK huyết thanh tăng cao rõ rệt hoặc nghi ngờ hoặc chẩn đoán là viêm cơ hoặc bệnh cơ.
Một số hiếm trường hợp ban da nặng phải nhập viện và dùng liệu pháp corticosteroid, bao gồm hội chứng Stevens-Johnson và hoại tử biểu bì nhiễm độc đã được thông báo khi dùng fenofibrat. Mày đay và ban da cũng được thông báo ở khoảng 1% người bệnh trong các thử nghiệm lâm sàng dùng liệu pháp fenofibrat.
Đã từng gặp viêm tụy ở người bệnh điều trị bằng fenofibrat và các dẫn chất acid fibric khác.
Giảm nhẹ và vừa hemoglobin, hematocrit và bạch cầu đã gặp người bệnh dùng fenofibrat. Những thông số này thường trở nên bình thường trong quá trình điều trị dài hạn. Đã gặp một số hiện trường hợp giảm tiểu cầu và mất bạch cầu hạt trong các đợt kiểm tra sau khi thuốc đã được bán ra thị trường. Cần phải định kỳ đếm huyết cầu trong 12 tháng đầu điều trị fenofibrat.
Ảnh hưởng của fenofibrat đến tỷ lệ mắc bệnh và tỷ lệ tử vong do tim mạch hoặc không do tim mạch chưa được xác định. Tuy nhiên vì fenofibrat về mặt hóa học, dược lý và lâm sàng đều giống các dẫn xuất acid fibric khác, một số tác dụng không mong muốn của clofibrate (hiện không còn bán trên thị trường) và của Gemfibrozil, thí dụ tăng tỷ lệ sỏi mật, viêm túi mật cần phải mổ, biến chứng sau cắt bỏ túi mật, ung thư, viêm tụy, cắt bỏ ruột thừa, bệnh túi mật và tăng tử vong toàn bộ có thể cũng xảy ra với fenofibrat. Như vậy, các điều thận trọng liên quan đến liệu pháp fibrat cần được theo dõi.
Tính an toàn và hiệu quả của fenofibrat chưa được xác định ở trẻ em dưới 18 tuổi.
7 Thời kỳ mang thai
Không nên dùng trong thời kỳ mang thai.
8 Thời kỳ cho con bú
Không có dữ liệu. Tuy nhiên, vì an toàn không nên dùng fenofibrat cho người cho con bú.
9 Tác dụng không mong muốn (ADR)
9.1 Thường gặp
Tiêu hóa: chướng bụng, chán ăn, tiêu chảy, buồn nôn.
Gan: tăng aminotransferase (liên quan đến liều).
9.2 Ít gặp
TKTW: nhức đầu, hoa mắt.
Mạch máu: thuyên tắc mạch như mạch phổi và các tĩnh mạch sâu.
Tiêu hóa: viêm tụy.
Gan: sỏi đường mật, ứ mật.
Da: phát ban, ngứa, nổi mề đay, rụng tóc.
Cơ xương: đau cơ, viêm cơ, co cơ, yếu cơ.
Sinh dục: rối loạn chức năng cương dương.
Phản ứng nhạy cảm ánh sáng.
Thận: suy thận.
9.3 Hiếm gặp
Máu: giảm bạch cầu.
Gan: viêm gan.
Bệnh thần kinh ngoại vi.
9.4 Hướng dẫn cách xử trí ADR
Tạm ngừng dùng thuốc.
10 Liều lượng và cách dùng
10.1 Cách dùng
Điều trị fenofibrat phải phối hợp với chế độ ăn hạn chế lipid. Thường phải uống cùng với thức ăn để cải thiện sinh khả dụng, mặc dù điều này không nhất thiết với mọi dạng bào chế. Thuốc có nhiều dạng bào chế khác nhau với sinh khả dụng khác nhau. Vì vậy liều lượng là riêng biệt cho từng chế phẩm.
10.2 Liều lượng
Dạng bào chế vi hạt: Viên nang 67mg để dùng nhiều lần mỗi ngày, viên nang 200 hoặc 267 mg để dùng 1 lần/ngày.
- Liều dùng khởi đầu: Dùng nang 67 mg/lần x 3 lần/ngày hoặc nang 200 mg/lần/ngày.
- Liều có thể giảm xuống 67 mg/lần × 2 lần/ngày hoặc tăng lên 67 mg/lần × 4 lần/ngày hoặc 267 mg/lần/ngày, tùy theo đáp ứng.
Các chế phẩm có sinh khả dụng cải tiến có thể dùng với liều khoảng từ 30 mg đến 160 mg, một lần mỗi ngày.
Dạng bào chế không vi hạt: Liều khởi đầu từ 200 - 300 mg/ngày, chia làm nhiều lần, sau đó điều chỉnh tùy theo đáp ứng, tới khoảng 200 - 400 mg/ngày; 100 mg fenofibrat không vi hạt tương đương điều trị với 67 mg của dạng vi hạt chuẩn.
Trẻ em: Kinh nghiệm dùng fenofibrat ở trẻ em còn hạn chế và chỉ được dùng theo hướng dẫn của thầy thuốc chuyên khoa. Chỉ nên dùng fenofibrat cho trẻ em khi các statin hoặc thuốc gắn kết acid mật không phù hợp. Liều lượng phụ thuộc vào dạng bào chế. Với dạng fenofibrat vi hạt chuẩn, trẻ em được dùng dạng nang 67 mg. Liều dùng cho trẻ em từ 4 - 15 tuổi là một nang 67 mg cho 20 kg cân nặng mỗi ngày. Trẻ em 15 - 18 tuổi có thể dùng theo liều người lớn.
Fenofibrat không vi hạt được một số nước cho phép dùng cho trẻ em từ 10 tuổi trở lên với liều uống mỗi ngày là 5 mg/kg cân nặng. Người suy thận: Không dùng cho người suy thận nặng (eGFR < 30 ml/phút/1,73 m3). Tuy nhiên dạng 67 mg fenofibrat vi hạt chuẩn hoặc 100 mg dạng không vi hạt được phép dùng cho bệnh nhân có Clcr từ 30 - 60 ml/phút. Dạng bào chế có sinh khả dụng cải tiến được phép dùng liều hàng ngày từ 30 đến 54 mg (tương đương với khoảng 67 mg fenofibrat vi hạt chuẩn) cho bệnh nhân suy thận, nhưng chống chỉ định dùng cho người suy thận nặng.
11 Tương tác thuốc
Các thuốc ức chế HMG-CoA reductase (statin) (ví dụ Pravastatin, Simvastatin, Fluvastatin..): Sẽ làm tăng nguy cơ tổn thương cơ (như tăng creatin kinase, myoglobin niệu, tiêu cơ vân).
Cyclosporin: Làm tăng nguy cơ độc tính thận do Cyclosporin.
Các thuốc chống đông uống: Làm tăng tác dụng chống đông và nguy cơ chảy máu (do tương tác đẩy nhau ra khỏi protein huyết tương). Điều chỉnh liều của thuốc chống đông uống trong thời gian điều trị fenofibrat và 8 ngày sau khi ngừng fenofibrat.
12 Quá liều và xử trí
Thẩm tách máu không có tác dụng loại bỏ thuốc khỏi cơ thể..
Cập nhật lần cuối: 2018
Phần nghiên cứu sau được bổ sung nhằm cung cấp thêm thông tin tham khảo và cập nhật những nghiên cứu mới nhất
13 Nghiên cứu sử dụng Fenofibrate và nguy cơ tiến triển thành bệnh võng mạc tiểu đường đe dọa thị lực
Tầm quan trọng: Bệnh võng mạc tiểu đường có thể tiến triển từ bệnh võng mạc tiểu đường không tăng sinh sang bệnh võng mạc tiểu đường đe dọa thị lực. Các nghiên cứu đã điều tra việc sử dụng Fenofibrate như một biện pháp bảo vệ với các kết quả trái ngược nhau và Fenofibrate thường không được các bác sĩ nhãn khoa xem xét trong việc quản lý bệnh võng mạc tiểu đường hiện nay.
Mục tiêu: Để đánh giá mối liên quan giữa việc sử dụng Fenofibrate và sự tiến triển từ bệnh võng mạc tiểu đường không tăng sinh sang bệnh võng mạc tiểu đường đe dọa thị lực, bệnh võng mạc tiểu đường tăng sinh hoặc phù hoàng điểm do tiểu đường.
Thiết kế, bối cảnh và người tham gia: Nghiên cứu đoàn hệ đa trung tâm này đã sử dụng dữ liệu yêu cầu bồi thường y tế từ một công ty bảo hiểm lớn của Hoa Kỳ. Các đoàn hệ được tạo ra từ tất cả các bệnh nhân mắc bệnh võng mạc tiểu đường không tăng sinh từ 18 tuổi trở lên có giá trị xét nghiệm từ ngày 1 tháng 1 năm 2002 đến ngày 30 tháng 6 năm 2019. Tiêu chí loại trừ bao gồm mọi chẩn đoán trước đó về bệnh võng mạc tiểu đường tăng sinh, phù hoàng điểm do tiểu đường, bệnh dịch kính võng mạc tăng sinh hoặc phương pháp điều trị được sử dụng trong chăm sóc bệnh võng mạc tiểu đường đe dọa thị lực. Bệnh nhân cũng bị loại trừ nếu họ được chẩn đoán bệnh võng mạc tiểu đường đe dọa thị lực trong vòng 2 năm kể từ khi tham gia chương trình bảo hiểm, bất kể khi nào bệnh võng mạc tiểu đường không tăng sinh được ghi nhận lần đầu trong chương trình.
Phơi nhiễm: Sử dụng Fenofibrate.
Kết quả chính và biện pháp: Kết quả chính là chẩn đoán mới về bệnh võng mạc tiểu đường đe dọa thị lực (kết quả tổng hợp của bệnh võng mạc tiểu đường tăng sinh hoặc phù hoàng điểm do tiểu đường) hoặc phù hoàng điểm do tiểu đường và bệnh võng mạc tiểu đường tăng sinh riêng lẻ. Một mô hình cập nhật thời gian cho tất cả các đồng biến đã được sử dụng trong hồi quy nguy cơ theo tỷ lệ Cox đa biến để xác định các nguy cơ dẫn đến kết quả. Các đồng biến bổ sung bao gồm thang đo mức độ nghiêm trọng của bệnh võng mạc tiểu đường không tăng sinh, bệnh toàn thân, nhân khẩu học, chức năng thận (dựa trên mức độ lọc cầu thận ước tính), huyết sắc tố A1c, huyết sắc tố và sử dụng Insulin.
Kết quả: Tổng cộng có 5835 người dùng Fenofibrate có bệnh võng mạc tiểu đường không tăng sinh lúc ban đầu (tuổi [SD] trung bình, 65,3 [10,4] tuổi; 3564 [61,1%] nam; 3024 [51,8%] Da trắng) và 144 417 người không sử dụng Fenofibrate (tuổi trung bình [SD] , 65,7 [12,3] tuổi; 73 587 [51,0%] nam; 67 023 [46,4%] Da trắng) được đưa vào để phân tích. Trong số này, 27 325 (18,2%) tiến triển thành bệnh võng mạc tiểu đường đe dọa thị lực, 4086 (2,71%) tiến triển thành bệnh võng mạc tiểu đường tăng sinh và 22 750 (15,1%) tiến triển thành phù hoàng điểm do tiểu đường. Sau khi kiểm soát tất cả các đồng biến, kết quả mô hình Cox cho thấy Fenofibrate có liên quan đến việc giảm nguy cơ bệnh võng mạc tiểu đường đe dọa thị lực (tỷ số nguy cơ, 0,92 [KTC 95%, 0,87-0,98]; P = 0,01) và bệnh võng mạc tiểu đường tăng sinh (tỷ số nguy cơ, 0,76 [95% CI, 0,64-0,90]; P = 0,001) nhưng không phải phù hoàng điểm do tiểu đường (tỷ lệ rủi ro, 0,96 [95% CI, 0,90-1,03]; P = 0,27).
Kết luận và mức độ liên quan: Trong nghiên cứu này, việc sử dụng Fenofibrate có liên quan đến việc giảm nguy cơ bệnh võng mạc tiểu đường tăng sinh và bệnh võng mạc tiểu đường đe dọa thị lực chứ không phải riêng phù hoàng điểm do tiểu đường. Những phát hiện này hỗ trợ cơ sở cho các thử nghiệm lâm sàng bổ sung để xác định xem các mối liên quan này có thể là đại diện cho mối quan hệ nhân quả giữa việc sử dụng Fenofibrate và giảm nguy cơ bệnh võng mạc tiểu đường tăng sinh hoặc bệnh võng mạc tiểu đường đe dọa thị lực hay không.
14 Tài liệu tham khảo
1. Dược thư quốc gia Việt Nam, lần xuất bản thứ ba - Đây là phiên bản mới nhất của Dược thư Việt Nam do Bộ Y tế ban hành Quyết định số 3445/QĐ-BYT ngày 23 tháng 12 năm 2022. Trang 737-739, tải PDF TẠI ĐÂY
2. Tác giả Elana Meer, J Clay Bavinger, Yinxi Yu, Brian L VanderBeek (Ngày đăng 1 tháng 5 năm 2022). Association of Fenofibrate Use and the Risk of Progression to Vision-Threatening Diabetic Retinopathy, Pubmed. Truy cập ngày 18 tháng 8 năm 2023