Ung thư cổ tử cung: nguyên nhân, triệu chứng và điều trị
Đại học Huế - Trường ĐH Y Dược
Đồng chủ biên:
GS.TS. Nguyễn Vũ Quốc Huy,
GS.TS. Cao Ngọc Thành,
PGS.TS. Lê Minh Tâm,
PGS.TS. Trương Thành Vinh,
Cùng nhiều tác giả tham gia biên soạn.
1 ĐẠI CƯƠNG
Các tổn thương cổ tử cung (cổ tử cung) rất hay gặp, chủ yếu là các tổn thương lành tính. Vị trí của cổ tử cung cho phép quan sát trực tiếp các thay đổi sinh lý dưới tác động của các thay đổi nội tiết theo chu kỳ buồng trứng cũng như nhiều thay đổi khác về cấu trúc và bệnh lý, liên quan đến nhiễm trùng, tân sinh lành tính, tiền ung thư, ung thư và các bất thường giải phẫu bẩm sinh. Trước khi đưa ra chẩn đoán và xử trí cần được thăm khám, quan sát trực tiếp, thăm khám bằng tay, xét nghiệm tế bào cổ tử cung, xét nghiệm tác nhân nhiễm khuẩn và HPV (Human Papillomavirus), soi cổ tử cung và một số biện pháp chẩn đoán hình ảnh.
Các tổn thương lành tính này không phải là ung thư, tuy nhiên cần được phát hiện và xử trí do diễn biến có thể kéo dài, gây lo lắng, ảnh hưởng đến sinh hoạt của bệnh nhân; có thể gây viêm nhiễm đường sinh dục trên và biến chứng vô sinh - hiếm muộn.
1.1 Đại thể
cổ tử cung có thể thay đổi hình thể tùy thuộc người phụ nữ đã có con hay chưa. Ở người chưa sinh, cổ tử cung thường tròn, ở người con ra lỗ cổ tử cung có thể sẽ bè ra theo chiều ngang. cổ tử cung là phần hẹp và thấp nhất của tử cung, có nguồn gốc từ đoạn cuối ống cận trung thận, có cấu trúc mô - sợi, bao phủ bởi biểu mô lát ở cổ ngoài và biểu mô trụ ở ống cổ tử cung, chiều dài khoảng 3cm, đường kính khoảng 2,5cm, nhô vào trong âm đạo, có hình trụ của người chưa sinh, hình nón cụt của người đã sinh, teo nhỏ hình chóp nhọn ở phụ nữ mãn kinh. cổ tử cung bao gồm 2 phần: Phần dưới nằm trong âm đạo gọi là cổ ngoài chiếm khoảng 1/2 độ dài, là phần có thể thấy được khi khám bằng mỏ vịt, phần trên tiếp nối với thân tử cung bằng eo tử cung. Ống cổ tử cung thông với buồng tử cung qua eo tử cung ở phía trên, đi tù lỗ trong ra lỗ ngoài cổ tử cung mở vào khoang âm đạo.
1.2 Mô học
Phía ngoài cổ tử cung được bao phủ bởi lớp biểu mô lát tầng (các tế bào gai). Phía trong lỗ cổ tử cung được che phủ bởi lớp biểu mô tuyến (biểu mô trụ đơn). Vùng chuyển tiếp ở lỗ ngoài cổ tử cung là ranh giới giữa biểu mô lát và biểu mô trụ.
Khi mang thai cổ tử cung hé mở thấy được một phần biểu mô tuyến của ống tử cung.
Sau mãn kinh lớp tế bào biểu mô ở bề ngoài nhạt màu hơn, ranh giới tổ chức học không thấy rõ rệt vì tụt vào sâu trong ống cổ tử cung.
Biểu mô lát tầng không sừng hóa lót mặt trong thành âm đạo và túi cùng âm đạo, liên tục đến cổ ngoài, nhạy cảm với sự thay đổi nội tiết tố sinh dục nữ. 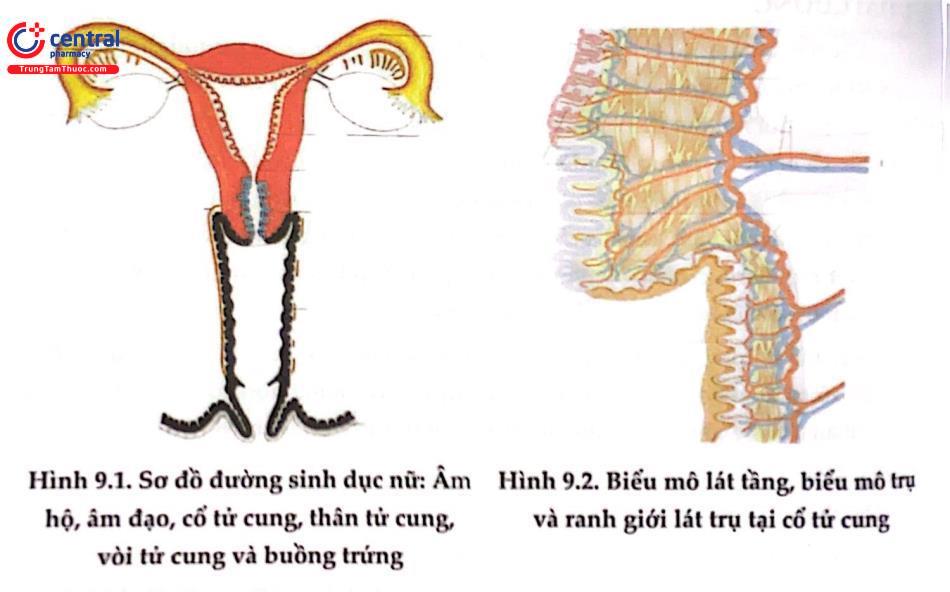
Biểu mô tuyến ống cổ tử cung có các nếp gấp tạo thành ống tuyến phát triển xuống mô liên kết bên dưới, tạo thành các phức hợp mào tuyến.
Ranh giới lát trụ (Squamocolumnar junction: SCJ): Là nơi tiếp giáp giữa biểu mô trụ và biểu mô lát. Vị trí của nó thay đổi qua các thời kỳ trong cuộc đời người phụ nữ. Trước dậy thì ranh giới này thường nằm ở lỗ ngoài cổ tử cung; ở phụ nữ đã sinh có thể nằm trên cổ ngoài; sau khi mãn kinh thường đi vào trong ống cổ tử cung. Vùng chuyển tiếp (Transformation zone - TZ): Là vùng có hiện tượng chuyển sản tại cổ tử cung. Vùng này đặc biệt quan trọng do các tế bào ở đây dễ dàng chịu tác động của các tác nhân sinh ung thư và đa số ung thư cổ tử cung xuất phát từ vùng chuyển tiếp này.
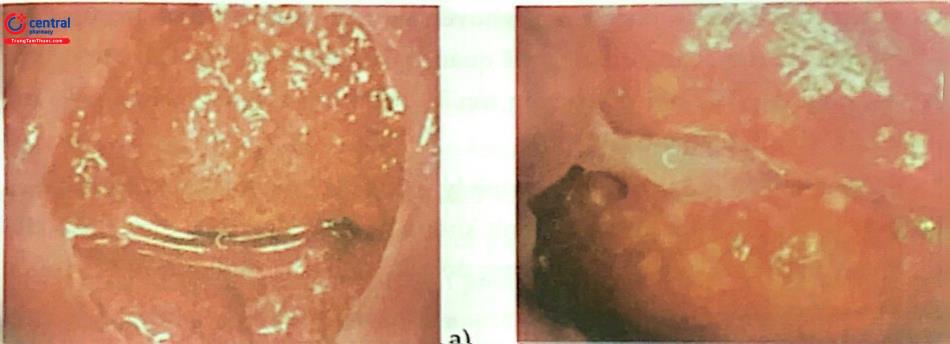
a) Pha nang noãn, chất nhầy nhiều, loãng trong
b) Pha hoàng thể: chất nhầy ít, đặc quánh
1.3 Sinh lý cổ tử cung
1.3.1 Biểu mô tuyến ở cổ tử cung
Biểu mô tuyến ở cổ tử cung gồm có hai loại tế bào:
Tế bào tiết nhầy: Nhân của tế bào bị đẩy xuống cực dưới, chất nhầy chứa bên trong tế bào.
Tế bào có nhung mao: Nhờ tác dụng của các nhung mao mà chất nhầy chế tiết ra được đẩy vào âm đạo.
Hai loại tế bào này chịu ảnh hưởng chủ yếu của estrogen, tạo ra dịch nhầy có pH khoảng 7,0-7,5, tính chất của dịch nhầy vì thế cũng thay đổi theo chu kỳ kinh:
Trong nửa đầu kỳ kinh (trước khi rụng trứng) chất nhầy ở cổ tử cung trong, nhầy và nhiều nhất vào trước ngày rụng trứng.
Trong nửa sau kỳ kinh (sau rụng trứng) dịch cổ tử cung dần đặc lại do ảnh hưởng của progesteron.
1.3.2 Hiện tượng chuyển sản
Chuyển sản là hiện tượng thay thế một loại biểu mô bằng một loại biểu mô khác. Thông thường đó là một thay đổi mang tính thích nghi, phản ứng trước một kích thích bất kỳ kiểu mãn tính, hoặc là một đáp ứng với một kích thích do nội tiết tố.
Chuyển sản biểu mô lát là sự thay thể biểu mô tuyến bằng biểu mô lát có nguồn gốc từ các tế bào dự trữ. Biểu mô chuyển sản cũng có thể biệt hóa hoàn toàn (trưởng thành) hoặc từng phần (kém trưởng thành). Tại cổ tử cung hiện tượng này diễn ra chủ yếu ở vùng tiếp giáp biểu mô lát – trụ. Đây là vùng thường diễn ra các quá trình biến đổi ác tính ở cổ tử cung.
Chuyển sản có tính hồi phục và trên lý thuyết mô mới hình thành có thể quay ngược trở lại hình thái ban đầu sau khi loại bỏ tác nhân kích thích, tuy nhiên điều này không phải luôn xảy ra. Hiện tượng chuyển sản xảy ra ở nhiều nơi trong cơ thể như ở niêm mạc dạ dày, bàng quang, phế quản... Quá trình chuyển sản được khảo sát chủ yếu nhất ở cổ tử cung, nơi có chuyển sản là quá trình chuyển đổi từ biểu mô tuyến ống cổ tử cung thành biểu mô lát.
Lộ tuyến cũng có thể là tình trạng sinh lý ở cổ tử cung, lúc này biểu mô tuyến bò ra che phủ một phần cổ tử cung, tạo nên hình ảnh không nhẵn, đỏ và có ít dịch nhầy che phủ. Lộ tuyến thường gặp ở phụ nữ trong độ tuổi sinh sản, đang dùng các thuốc tránh thai có estrogen.
1.3.3 Hiện tượng tái tạo
Quá trình lành vết thương của tổn thương loét/mất biểu mô diễn ra bằng hiện tượng tăng sinh các tế bào từ lớp đáy của biểu mô bên dưới và các tế bào dự trữ nằm ở đáy các ống tuyến. Đầu tiên vùng mất mô sẽ được bao phủ bởi các tế bào chuyển sản chưa trưởng thành, sau đó sẽ chuyển thành biểu mô lát trưởng thành hoặc biểu mô trụ.
2 ĐẠI CƯƠNG VỀ UNG THƯ CỔ TỬ CUNG
Ung thư cổ tử cung là ung thư phụ khoa đứng hàng thứ hai sau ung thư vú, thường xảy ra ở ranh giới giữa biểu mô lát tầng và biểu mô trụ của cổ tử cung.
Năm 2012, tại Việt Nam ước tính có 5.146 phụ nữ mắc ung thư cổ tử cung, tỷ lệ mắc mới ung thư cổ tử cung đã chuẩn hóa theo tuổi (ASR) là 10,6/100.000 phụ nữ, tỷ lệ này thấp hơn so với khu vực Đông Nam Á với ASR là 16,3/100.000. Tỷ lệ này đang có xu hướng gia tăng, đặc biệt tại một số tỉnh như Cần Thơ, tỷ lệ mắc thô tăng từ 15,7/100.000 vào năm 2000 lên tới 25,7/100.000 vào năm 2009. Một trong những lý do dẫn đến tình trạng này là phụ nữ chưa được sàng lọc định kỳ và chưa có hệ thống để phát hiện sớm ung thư qua các xét nghiệm thích hợp, dễ tiếp cận; và khi phát hiện tổn thương tiền ung thư thì cũng chưa được điều trị kịp thời và hiệu quả. Năm 2012, tổng gánh nặng trực tiếp của ung thư cổ tử cung khoảng 1.755 tỷ đồng, xếp thứ 4 và chiếm khoảng 0,015% tổng GDP; gánh nặng gián tiếp khoảng 418 tỷ đồng, xếp thứ 5 trong số 6 loại bệnh ung thư thường gặp nhất.
Theo nghiên cứu của Nguyễn Thị Ngọc Diệp và cộng sự năm 2019, tỷ lệ mắc mới đã hiệu chỉnh theo tuổi của ung thư cổ tử cung tại Hà Nội là 6,7/100.000 (1993-1997), thấp hơn đáng kể so Thành phố Hồ Chí Minh cùng giai đoạn là 28,8/100.000 (1995- 1998) và giai đoạn gần đây (2009-2012) là 14,1/100.000 phụ nữ. Dựa trên các số liệu thống kê dân số đô thị, dự báo xu hướng diễn tiến, nhóm tác giả đã đưa ra dự báo nếu không can thiệp, số trường hợp mắc mới sẽ gia tăng từ 6.930 (khoảng dao động 5.671-8.493) vào năm 2012 lên 8.562 (khoảng dao động 5.775-12.762) vào năm 2049, đưa tổng số trường hợp mắc mới trong giai đoạn 2013-2049 lên đến 379617 (khoảng dao động 276.879-542941).
Kết quả điều trị ung thư cổ tử cung phụ thuộc vào thời điểm chẩn đoán. Nếu chẩn đoán muộn việc điều trị gặp nhiều khó khăn và kết quả điều trị thấp.
3 NGUYÊN NHÂN VÀ YẾU TỐ NGUY CƠ
Nhiễm một hoặc nhiều type vi rút gây u nhú ở người (HPV) nguy cơ cao đã được khẳng định là nguyên nhân tiên phát của ung thư cổ tử cung. HPV là tác nhân lây truyền qua đường tình dục. Cho đến nay đã phát hiện được khoảng 150 type HPV, trong đó có hơn 30 type thường lây lan qua quan hệ tình dục.
HPV sinh dục thành hai nhóm: nhóm nguy cơ thấp (thường gặp nhất là type 6 và 11) gây nên sùi mào gà sinh dục và nhóm nguy cơ cao (có 14 type, các type thường gặp nhất là 16, 18, 31, 33 và 45) gây ra các tổn thương: CIN và/hoặc ung thư cổ tử cung, âm đạo, hậu môn, dương vật, thanh quản...
Nguy cơ tương đối hình thành ung thư cổ tử cung sau nhiễm mạn tính ít nhất một trong các type HPV sinh dục nguy cơ cao lên đến 300-500 lần, cao hơn một cách đáng kể so với nhiễm các tác nhân vi rút sinh ung thư khác như vi rút viêm gan B (100 lần), vi rút viêm gan C (20 lần).
Các yếu tố làm gia tăng nguy cơ bao gồm:
Quan hệ tình dục sớm.
Có nhiều bạn tình.
Hút thuốc lá.
Sinh nhiều: từ 5 con trở lên (nguy cơ tương đối tăng 2,0 lần).
Điều kiện kinh tế xã hội thấp.
Sử dụng thuốc tránh thai phối hợp dạng uống trên 5 năm (nguy cơ tương đối tăng 2,2 lần).
Nhiễm vi rút Herpes, HIV/AIDS, suy giảm hệ thống miễn dịch do dùng corticoid kéo dài, hóa trị liệu...
4 MÔ BỆNH HỌC
4.1 Diễn tiến tự nhiên của ung thư cổ tử cung
Vi rút HPV sau khi nhiễm vào biểu mô cổ tử cung sẽ gây ra các thay đổi ở biểu mô lát và/hoặc tuyến cổ tử cung. Phần lớn các tổn thương này tự thoái triển về bình thường sau một thời gian tương đối ngắn hoặc không tiến triển đến dạng nặng hơn. Nếu người phụ nữ nhiễm HPV type nguy cơ cao và phối hợp với các yếu tố hiệp đồng khác, tổn thương ban đầu có thể tồn tại và tiến triển trong khoảng 10-20 năm qua các giai đoạn tân sản nội biểu mô để hình thành ung thư cổ tử cung.
Có trên 90% trường hợp nhiễm HPV sẽ đào thải vi rút trong vòng 2 năm, khoảng 10% các trường hợp vẫn còn vi rút HPV sau 3 năm và có dưới 5% tiến triển thành tổn thương CIN2 hoặc nặng hơn trong 3 năm. Tổn thương xâm lấn cổ tử cung bắt đầu xuất hiện sau khoảng 13-15 năm, trong đó 20% CIN3 tiến triển thành ung thư trong 5 năm và 50% CIN3 tiến triển thành ung thư trong vòng 30 năm.
Trong ung thư cổ tử cung, ADN HPV được ghi nhận đã tích hợp vào bộ gen của tế bào vật chủ, ngược lại trong tổn thương CIN, ADN HPV chỉ hiện diện trong bào tương (dạng episome). Wall Boomers và cộng sự (1999) đã chỉ ra rằng, ADN HPV được tìm thấy ở 99,7% các trường hợp ung thư tế bào lát cổ tử cung trên tổng số 932 trường hợp ung thư cổ tử cung được khảo sát trên toàn thế giới và gần 99% các trường hợp ung thư biểu mô tuyến từ ống cổ tử cung
4.2 Tăng sản nội biểu mô cổ tử cung
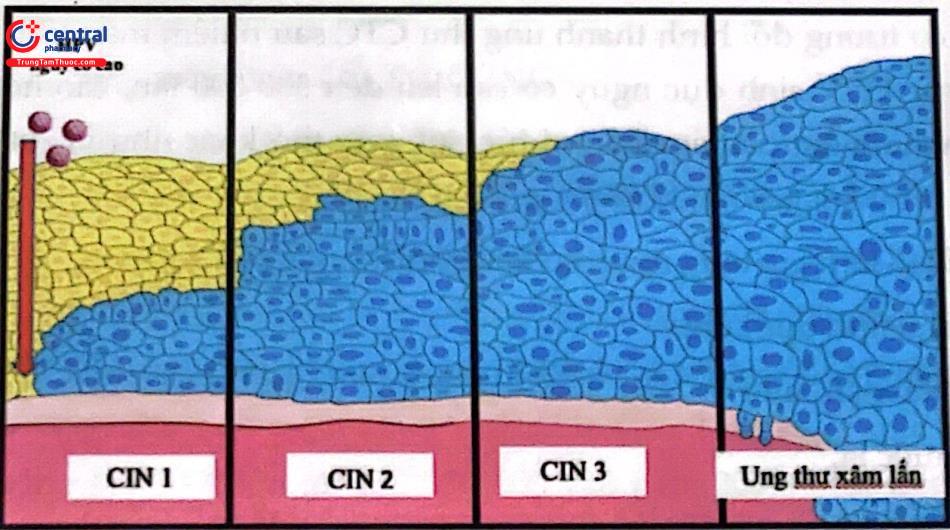
Tổn thương biểu mô lát ở cổ tử cung phát triển qua giai đoạn tân sản nội biểu mô cổ tử cung (Cervical Intraepithelial Neoplasia: CIN) trước khi hình thành ung thư xâm lấn. Tùy thuộc vào số lượng của các tế bào bất thường, tân sản nội biểu mô cổ tử cung được chia thành:
CIN1: Các tế bào biểu mô bất thường chiếm 1/3 dưới chiều dày lớp biểu mô.
CIN2: Các tế bào biểu mô bất thường chiếm 2/3 dưới chiều dày lớp biểu mô.
CIN3: Các tế bào biểu mô bất thường chiếm gần hết chiều dày lớp biểu mô, chỉ còn vài lớp tế bào bình thường. CIN3 bao gồm carcinoma in situ (CIS): toàn bộ bề dày biểu mô bao gồm các tế bào ung thư nhưng chưa phá vỡ và xâm lấn qua màng đáy, về cấu trúc mất hiện tượng phân tầng bình thường của các lớp tế bào.
4.3 Ung thư xâm lấn
Tế bào ung thư phá hủy lớp màng đáy và xâm lấn vào tổ chức đêm, trường hợp này ta gọi là ung thư xâm lấn. Có khoảng 85-90% các trường hợp là ung thư biểu mô lát và khoảng 10-15% ung thư biểu mô tuyến. Hiện nay tỷ lệ ung thư biểu mô tuyến đang có xu hướng gia tăng ở nhiều nước phát triển tỷ lệ này lên đến 20%.
4.4 Lan tràn của ung thư cổ tử cung
Lân cận:
Từ vùng chuyển tiếp ở bề mặt cổ tử cung - âm đạo lan xuống âm đạo, lan lên eo của tử cung.
Xâm lấn sâu về phía trước, đến vách bàng quang - âm đạo và bàng quang.
Xâm lấn ra phía sau phần trực tràng - âm đạo và trực tràng.
Xâm lấn ra hai bên đáy dây chằng rộng, niệu quản và vách chậu.
Theo đường bạch mạch: Ung thư lan theo đường này đến chuỗi hạch chậu ngoài, chậu trong, hiếm khi lan đến hạch bẹn; cũng có khi ung thư lan tràn bất thường, chẳng hạn bỏ qua chuỗi hạch chậu hông tới ngay nhóm hạch động mạch chủ bụng. Rất hiếm khi thấy ung thư di căn theo đường máu.
5 TRIỆU CHỨNG LÂM SÀNG VÀ CẬN LÂM SÀNG
5.1 Các thương tổn tiền lâm sàng
Ở giai đoạn sớm, các triệu chứng cơ năng thường nghèo nàn. Khi khám âm đạo - cổ tử cung bằng mỏ vịt có thể thấy cổ tử cung trông giống như bình thường hoặc có vết loét trợt, có một vùng trắng không điển hình hoặc tăng sinh mạch máu.
5.2 Các thương tổn rõ trên lâm sàng
Bệnh nhân thường đến khám với triệu chứng ra máu âm đạo bất thường giữa kỳ kinh, ra máu sau giao hợp, hoặc khí hư hội, lẫn máu, có thể phối hợp với tình trạng cơ thể suy kiệt.
Khám mỏ vịt hiện diện một khối sùi, dễ chảy máu khi chạm vào. Khi bôi Lugol vùng tổn thương không bắt màu (nghiệm pháp Schiller âm tính). Một số trường hợp muộn hơn cổ tử cung sẽ biến dạng, loét sâu hoặc cổ tử cung bị mất hẳn hình dạng. Sinh thiết được thực hiện ở cả vùng lành và vùng bệnh lý. Ngoài ra, cần phải đánh giá mức độ lan tràn và xâm lấn của ung thư vào các túi cùng âm đạo, nền dây chằng rộng, bàng quang, trực tràng và các vùng kế cận.
Giai đoạn | Triệu chứng |
Ia | Không triệu chứng |
Ib, II | Xuất huyết bất thường, huyết trắng |
III, IV | Đau lưng, phù chân do tắc mạch bạch huyết, rối loạn chức năng trực tràng (phân có máu), tiểu máu, tiểu khó |
Những phụ nữ nghi ngờ bị ung thư cổ tử cung xâm lấn cần được khám nội khoa tổng quát và khám phụ khoa.
5.3 Cận lâm sàng
5.3.1 Tế bào cổ tử cung (Pap’s smear)
Giúp phát hiện các thay đổi ở mức độ tế bào theo hướng tiền ung thư hoặc ung thư, là xét nghiệm sàng lọc ung thư cổ tử cung. Tiêu bản được nhuộm theo phương pháp Papanicolaou và xếp loại theo danh pháp Bethesda 2001 bao gồm:
Các thay đổi tế bào biểu mô lát:
ASCUS, ASC-H (bất điển hình tế bào lát có ý nghĩa không xác định).
LSIL (tổn thương nội biểu mô lát độ thấp).
HSIL (thương tổn nội biểu mô lát độ cao).
Ung thư tế bào lát.
Các thay đổi tế bào biểu mô trụ:
AGUS (bất điển hình tế bào tuyến có ý nghĩa không xác định).
AIS (ung thư biểu mô tuyến tại chỗ).
Ung thư tế bào tuyến.
5.3.2 Soi cổ tử cung
Không chuẩn bị: cần phải xác định vùng chuyển tiếp. Tổn thương dạng sùi hoặc loét, bề mặt dễ chảy máu, nhiều mạch máu tăng sinh.
Chứng nghiệm Hinselmann (chủng nghiệm acid acetic): Khi bôi acid acetic 3%, vùng tổn thương trở nên trắng đục, có thể có hình chấm đáy hoặc hình lát đá.
Chứng nghiệm Schiller: Bôi dung dịch Lugol 3%, vùng tổn thương không bắt màu nâu.
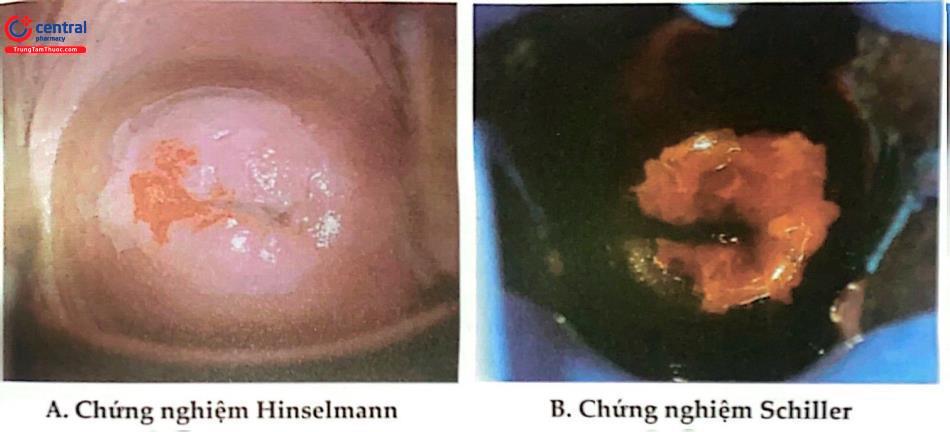
Sinh thiết
Sinh thiết cổ tử cung được lấy từ vùng chuyển tiếp và vùng nghi ngờ dưới soi cổ tử cung, cho phép khảo sát mô học một cách chính xác và đầy đủ.
Mô bệnh học được phân loại theo danh pháp CIN và ung thư của Tổ chức Y tế Thế giới.
5.3.3 Chẩn đoán hình ảnh
Để giúp đánh giá đầy đủ mức độ lan tràn và xâm lấn của ung thư, có thể chỉ định một số thăm dò sau: siêu âm, chụp cắt lớp vi tính (CT Scan), cộng hưởng từ hạt nhân (MRI).
PHÂN GIAI ĐOẠN
5.4 Phân giai đoạn theo FIGO 2018
Giai đoạn | Mô tả |
I | Ung thư chỉ giới hạn ở cổ tử cung (không tính đến lan tràn lên thân tử cung) |
IA | Ung thư xâm lấn được chẩn đoán vi thể, độ sâu xâm lấn < 5mm |
IA1 | Xâm lấn mô đệm sâu không quá 3mm |
IA2 | Xâm lấn mô đệm sâu hơn 3mm, nhưng không quá 5mm |
IB | Ung thư xâm lấn được chẩn đoán vi thể, độ sâu xâm lấn > 5mm (lớn hơn giai đoạn IA1), tổn thương giới hạn ở cổ tử cung |
IB1 | Ung thư xâm lấn mô đệm > 5mm, kích thước lớn nhất ≤ 2cm |
IB2 | Ung thư xâm lấn, kích thước lớn nhất > 2cm và ≤ 4cm |
IB3 | Ung thư xâm lấn, kích thước lớn nhất > 4cm |
II | Ung thư lan ra ngoài cổ tử cung nhưng chưa lan 1/3 dưới âm đạo hoặc đến thành chậu |
IIA | Lan tràn ung thư giới hạn ở 2/3 trên âm đạo, không xâm lấn dây chằng ngang CIC |
IIA1 | Ung thư xâm lấn, kích thước lớn nhất ≤ 4cm |
IIA2 | Ung thư xâm lấn, kích thước lớn nhất > 4cm |
IIB | Xâm lấn dây chằng ngang cổ tử cung nhưng chưa đến thành chậu |
III | Ung thư lan tràn đến 1/3 dưới âm đạo và/hoặc đến thành chậu và/hoặc gây thận ức nước hoặc thận mất chức năng và/hoặc di căn hạch chậu và/hoặc hạch cạnh động mạch chủ. |
IIIA | Ung thư lan tràn đến 1/3 dưới âm đạo, chưa đến thành chậu |
IIIB | Lan tràn đến thành chậu và/hoặc thận ứ nước, thận cầm (khi không có nguyên nhân khác) |
IIIC | Di căn đến hạch bạch huyết vùng chịu và/hoặc hạch cạnh động mạch chủ (bao gồm cả di căn vi thể), khối u bất kỳ kích thước nào |
IIIC1 | Chỉ di căn hạch bạch huyết vùng chậu |
IIIC2 | Di căn hạch bạch huyết cạnh động mạch chủ |
IV | Ung thư lan quá vùng chậu hoặc có bằng chứng mô bệnh học đã xâm lấn niêm mạc bàng quang hoặc trực tràng |
IVA | Lan tràn đến các tạng chậu lân cận |
IVB | Lan tràn đến các tạng ở xa |
5.5 Phân giai đoạn theo TNM (Tumor, Nodes, Metastases)
U nguyên phát (T) | ||
Loại T | Tiêu chuẩn | |
TX | Không tính giá được u nguyên phát | |
T0 | Không có bằng chứng của u nguyên phát | |
T1 | Ung thư cổ tử cung giới hạn ở tử cung (không tính đến lan tràn lên thân tử cung) | |
T1a | Ung thư xâm lấn chi được chẩn đoán vì thế. Xâm lấn mô đệm tối đa 5.0mm tính từ đáy của biểu mô, làm trên bề ngang không quá 7,0mm. Phân loại không tính đến xâm lấn mạch máu, tĩnh mạch hoặc bạch mạch | |
T1a1 | Xâm lấn mô đệm sâu không quá 3,0mm, bề ngang không quá 7,0mm | |
T1a2 | Xâm lấn mô đệm sâu quá 3,0mm và chưa đến 5,0mm, bề ngang không quá 7,0mm | |
T1b | Tổn thương rõ trên lâm sàng giới hạn ở cổ tử cung, hoặc tổn thương vì thế lớn hơn Tla/IA2. Bao gồm tất cả các tổn thương nhìn rõ trên đại thể, kể cả tổn thương có xâm lấn nông. | |
T1b1 | Tổn thương rõ trên lâm sàng, kích thước lớn nhất không quá 4,0cm | |
T1b2 | Tổn thương rõ trên lâm sàng, kích thước lớn nhất vượt quá 4,0cm | |
T2 | Ung thư lan tràn quả tử cung nhưng chưa đến thành chậu hoặc 1/3 dưới âm đạo | |
T2a | Khối u chưa xâm lấn dây chằng ngang cổ tử cung | |
T2a1 | Tổn thương rõ trên lâm sàng, kích thước lớn nhất không quá 4,0cm | |
T2a2 | Tổn thương rõ trên lâm sàng kích thước lớn nhất vượt quá 4,0cm | |
T2b | Khối u xâm lấn dây chằng ngang cổ tử cung | |
T3 | Khối u lan đến thành chậu bên và/hoặc đến 1/3 dưới âm đạo và hoặc gây ra thận ứ nước hoặc thận cầm | |
T3a | Khối u lan đến 1/5 dưới âm đạo nhưng chưa lan đến thành chậu | |
T3b | Khối u lan đến thành chậu bên và/hoặc gây ra thận ứ nước hoặc thận cầm T4 | |
T4 | Khối u xâm lấn đến niêm mạc bàng quang hoặc trực tràng và/hoặc lan tràn qua hố chậu | |
Hạch bạch huyết vùng (N) | ||
Loại N | Tiêu chuẩn | |
NX | Di căn hạch bạch huyết vùng | |
NO | Không khảo sát được hạch bạch huyết vùng | |
NO (i +) | Không có di căn hạch bạch huyết vùng | |
N1 | Các tế bào khối u đơn lẻ trong hạch bạch huyết vùng kích thước không lớn hơn 0.2mm | |
Di căn xa (M) | ||
Loại M | Tiêu chuẩn | |
M0 | Không có di căn xa | |
M1 | Di căn xa (bao gồm lan tràn ở phúc mạc hoặc hạch thượng đòn, hạch trung thất hoặc hạch ở xa; phổi; gan hoặc xương) | |
Phân giai đoạn tiên lượng | ||
T | M | Giai đoạn |
T1 | M0 | I |
T1a | M0 | IA |
T1a1 | M0 | IA1 |
T1a2 | M0 | IA2 |
T1b | M0 | IB |
T1b1 | M0 | IB2 |
T1b2 | M0 | II |
T2 | M0 | IIA |
T2a | M0 | IIA1 |
T2a1 | M0 | IIA2 |
T2a2 | M0 | IIB |
T2b | M0 | III |
T3 | M0 | IIIA |
T3a | M0 | IIIB |
T3b | M0 | IV |
T4 | M0 | IVA |
Mọi T | M1 | IVB |
6 CHẨN ĐOÁN PHÂN BIỆT
Lộ tuyến, loét trợt cổ tử cung: Là tổn thương thường gặp ở cổ tử cung.
Polyp cổ tử cung; Dạng polyp tuyển bị hoại tử hoặc nhiễm khuẩn.
Lạc nội mạc tử cung: Dễ nhầm nhất là vào giai đoạn chảy máu trùng với
hành kinh trên nền của tổn thương lạc nội mạc tử cung.
Giang mai cổ tử cung: Có thể gặp săng giang mai nguyên phát ở cổ tử cung.
Lao cổ tử cung: Rất hiếm gặp, có tiền sử lao sinh dục.
U đặc: Đôi khi có những u khác như u bạch huyết hay u di căn từ đường tiêu hóa, chủ yếu u đại tràng được tìm thấy ở cổ tử cung và âm đạo cạnh đó.
Ra máu âm đạo: Nếu ung thư cổ tử cung xâm lấn đi kèm với biến chứng xuất huyết nặng hay nếu ung thư xâm lấn không rõ, nên nghĩ đến các nguyên nhân gây xuất huyết bất thường khác như giảm tiểu cầu, rối loạn nội tiết, biến chứng thai kỳ và nhiễm trùng.
Khí hư: Các trường hợp viêm nặng cổ tử cung và âm đạo có thể xảy ra cùng hoặc không cùng lúc với ung thư cổ tử cung. Cần đánh giá vi khuẩn học và điều trị đầy đủ trước khi phẫu thuật hay xạ trị.
Kết quả thăm khám bất thường: U buồng trứng hay ứ dịch tai vòi có thể giả ung thư cổ tử cung giai đoạn III hoặc IV.
7 ĐIỀU TRỊ
7.1 Các biện pháp điều trị
7.1.1 Điều trị tổn thương tân sản nội biểu mô cổ tử cung
Các lựa chọn xử trí thương tổn tiền ung thư cổ tử cung (CIN) hiện nay bao gồm theo dõi, các phương pháp phá hủy và các phương pháp cắt bỏ. Các phương pháp phá hủy gồm áp lạnh, hóa hơi bằng laser hoặc đốt điện; các phương pháp cắt bỏ gồm khoét chóp, khoét chóp bằng laser, LEEP (Loop Electrosurgical Excision Procedure) hoặc cắt tử cung.
Kể từ năm 2007, Hiệp hội Soi cổ tử cung và bệnh lý cổ tử cung Hoa Kỳ (American Society for Colposcopy and Cervical Pathology - ASCCP) đã đưa ra hướng dẫn đồng thuận mới trong xử trí CIN. Theo đó, CIN I sẽ được theo dõi là chính, trong khi CIN II, III cần được điều trị ngay.
CIN I: Bệnh nhân với chẩn đoán mô học CIN I sau một kết quả tế bào học ASC-US (atypical squamous cells of undetermined significance), ASC-H (atypical squamous cells, cannot exclude HSIL) hoặc LSIL sẽ được theo dõi bằng xét nghiệm DNA HPV sau 12 tháng hoặc tế bào học mỗi 6 đến 12 tháng. Đối tượng trong độ tuổi vị thành viên sẽ được theo dõi bằng tế bào học hàng năm. Trong điều kiện nguồn lực hạn chế, để hạn chế tối đa việc “mất dấu” đối tượng có thể xem xét điều trị tổn thương CINI
CIN II, III: Có thể sử dụng cả hai nhóm phương pháp phá hủy và cắt bỏ cho phụ nữ có mô học CIN II, III và soi cổ tử cung đạt yêu cầu. Phụ nữ có CIN II, III tái phát cần cắt bỏ thương tổn để chẩn đoán mô học. Cắt tử cung không phải là điều trị chọn lựa đầu tay đối với CIN II, III. Ở phụ nữ mang thai, nếu không có bệnh lý xâm lấn và đang ở trong nửa đầu của thai kỳ, có thể theo dõi mỗi 12 tuần với soi cổ tử cung và tế bào học cho đến hết thời kỳ hậu sản.
Ung thư tuyến tại chỗ (Adenocarcinoma In Situ – AIS): Phương pháp được khuyến cáo là cắt tử cung đối với phụ nữ đã đủ con, ngược lại có thể sử dụng các phương pháp cắt bỏ và xét nghiệm mô học. Nếu bờ bệnh phẩm chưa phải là bờ lành cần tiếp tục cắt bỏ thêm. Sau điều trị cần theo dõi bệnh nhân sau 6 tháng với tế bào học, ADN HPV, soi cổ tử cung có nạo ống cổ tử cung. Cần theo dõi dài hạn đối với phụ nữ không cắt tử cung.
Trong điều kiện nguồn lực hạn chế, áp lạnh đã được chứng minh là một phương pháp an toàn, hữu hiệu và có chi phí thấp để điều trị tất cả các thương tổn CN I, II và III. Tỷ lệ lành bệnh sau áp lạnh đạt 86-95%, tương đương với LEEP.
Cần chú trọng việc tư vấn trước và sau khi thực hiện biện pháp điều trị, đặc biệt trong việc giải thích rõ các tác dụng phụ như ra khí hư có màu vàng sau đốt điện và LEEP, ra khí hư nhiều sau áp lạnh,... cũng như nhấn mạnh các dấu hiệu nguy hiểm để khách hàng hiểu rõ và hành động đúng nếu gặp phải.
Năm 2020, Hiệp hội Soi cổ tử cung và bệnh lý cổ tử cung Hoa Kỳ (American Society for Colposcopy and Cervical Pathology – ASCCP) đã đưa ra hướng dẫn xử trí mới đối với tổn thương CIN trên cơ sở đánh giá nguy cơ của tổn thương phát hiện được bằng các phương pháp sàng lọc chuẩn hóa là HPV DNA (các test được FDA Hoa Kỳ cấp phép cho sàng lọc đầu tay) và Pap’smear. Nhập các thông tin vào ứng dụng tại địa chỉ https://app.asccp.org/ hoặc ứng dụng di động “ASCCP” tải về điện thoại thông minh để tính toán nguy cơ cụ thể. Nếu nguy cơ hiện tại của tổn thương CIN > 60% cần điều trị ngay; ≥ 4% cần soi cổ tử cung, nếu đánh giá nguy cơ CIN3 sau 5 năm ≥ 0,15% cần giám sát bằng cách tái khám sau 1-3 năm. Khuyến cáo xử trí dựa trên nguy cơ giúp giảm số lượng xét nghiệm chẩn đoán (soi cổ tử cung, nạo sinh thiết cổ trong, sinh thiết), giảm mất dấu nhưng vẫn giúp xử trí đúng mức.
7.1.2 Điều trị ung thư xâm lấn
7.1.2.1 Phẫu thuật
Phẫu thuật Wertheim-Meigs:
Mở bụng, quan sát và thăm khám các cơ quan trong ổ bụng một cách hệ thống.
Lấy hạch chậu.
Cắt tử cung tận gốc với nhiều mức độ tận gốc khác nhau (Piver II/III).
Nếu có chỉ định, lấy luôn hạch cạnh động mạch chủ.
Giai đoạn I - Ilb: Chủ yếu là phẫu thuật theo phương pháp Wertheim-Meigs, cắt tử cung hoàn toàn, cắt hai phần phụ, cắt 1/3 trên âm đạo, lấy hết các tổ chức liên kết dưới hai lá dây chằng rộng, nạo hạch trong hố chậu và dọc theo động mạch chủ bụng. Đối với giai đoạn lễ, nhiều tác giả nêu lợi ích của xạ trị trước phẫu thuật nhằm giảm mức độ ác tính của tế bào ung thư, diệt những ổ lan tràn quanh tổn thương nguyên phát, ngăn chặn di căn. Xạ trị trước mổ, nguồn xạ sử dụng là césium hay radium, ngừng xạ trị khoảng 6 tuần trước phẫu thuật, xạ trị sau mổ dùng tia Cobalt chiếu vào vùng chậu nơi đã lấy hạch có tế bào ung thư.
Giai đoạn III: Xạ trị và đánh giá lại để cân nhắc chỉ định phẫu thuật.
Giai đoạn IV: Xạ trị và điều trị hỗ trợ, có thể áp dụng phẫu thuật tạm thời như dẫn lưu bàng quang, hậu môn nhân tạo.
7.1.2.2 Xạ trị
Các chỉ định xạ trị hỗ trợ sau khi cắt tử cung tận gốc
Nguy cơ cao (có di căn hạch, xâm lấn đến bờ phẫu thuật, di căn chu cung, u lớn).
Nguy cơ cao (xâm lấn vào mô đệm sâu, LVSI).
Ung thư phát hiện tình cờ (trường hợp cắt tử cung đơn thuần và phẫu thuật viên vô tình cắt ngang qua vùng ung thư).
Trong nhóm ung thư nguy cơ trung bình, xạ trị làm giảm tái phát 13%. Đối với các khối u có di căn hạch (xâm lấn vi thể) giảm tái phát đến 50%.
Chống chỉ định tương đối của xạ trị hỗ trợ
Mập phì nặng.
Tuổi trên 70.
Bệnh đường ruột (Crohn, viêm loét đại tràng).
Tình trạng giảm hiệu suất Karnofsky.
Dính nhiều do các phẫu thuật trước đây.
7.1.2.3 Xạ - hóa trị đồng thời
Thất bại trong điều trị ung thư giai đoạn tiến triển, đặc biệt những khối u có di căn hạch (đánh giá bằng MRT hoặc khối u lớn, carcinôm không biệt hóa và LVSI) cho thấy sự cần thiết cải tiến điều trị tại chỗ và toàn thân.
Một trong những điều kiện tiên quyết cho sự tối ưu hóa xạ trị đã được bàn là liều xạ trị thích hợp. Theo các nghiên cứu của Thomas (Bệnh viện Princess Margret, Canada) và các tác giả khác, liều xạ trị phải là 85 Gy ở điểm A. Sự mở rộng trường tia xạ với xạ trị cạnh động mạch chủ cải thiện tiên lượng bệnh trong các trường hợp có xâm lấn các hạch này trên vi thế. Tuy nhiên, nếu khối u ngyên phát lớn (> 4cm) hoặc nếu khối u lan rộng (giai đoạn IIb hoặc IV), không thể cải thiện tiên lượng bằng cách tăng liều. Sự kết hợp điều trị liên tiếp với hóa trị và sau đó xạ trị cũng không thể cải thiện cơ may sống sót. Mặt khác, sự kết hợp hóa và xạ trị áp dụng đồng thời làm cho đáp ứng của khối u tăng lên đáng kể và cũng cải thiện thời gian sống bệnh không tiến triển (PFS) và thời gian sống sót chung (OAS) một cách đáng kể.
Kết quả tích cực của các thử nghiệm lâm sàng ngẫu nhiên cho thấy xạ - hóa trị phối hợp với Cisplatin cho kết quả cải thiện. Duy nhất một thử nghiệm ở Canada không cho thấy tác dụng tích cực của phối hợp xạ - hóa trị (Lehman và Thomas 2001). Các tác dụng phụ về huyết học trình bày trong các nghiên cứu có thể sẽ được giảm nhẹ trong tương lai khi các sản phẩm mới thuộc công nghệ sinh học như Erythropoietin - dùng để phòng ngừa thiếu máu - và yếu tố kích thích dòng bạch cầu hạt (G-CSF) được sử dụng.
Một tổng quan Cochrane năm 2005 bao gồm 24 nghiên cứu trên 4921 bệnh nhân cho thấy xạ - hóa trị đồng thời tỏ ra có thể cải thiện thời gian sống tổng thể cũng như thời gian sống không bệnh ở nhóm bệnh nhân với tình trạng bệnh tại chỗ tiến triển, cũng như làm giảm tái phát tại chỗ và tái phát xa, gợi ý rằng hóa liệu pháp có thể thúc đẩy sự nhạy cảm với xạ trị và tăng tác dụng độc tế bào hệ thống. Tuy nhiên, trong nhóm điều trị người ta cũng ghi nhận tỷ lệ biến chứng cấp tính về huyết học và tiêu hóa cao hơn.
7.1.2.4 Hóa liệu pháp
Hóa liệu pháp trước phẫu thuật tỏ ra hữu ích trong các trường hợp khối u trên 2cm.
Liệu trình với Cisplatin 50mg/m2, Vincristine 1 mg/m2 và Bleomycine 25 mg/m2 trong ngày 1-3/3 tuần có thể làm giảm bớt kích thước khối u, tạo điều kiện cho phẫu thuật dễ dàng và kéo dài thời gian tái phát.
Hóa chất có hiệu lực nhất trong ung thư cổ tử cung là Cisplatin. Cho đến nay vẫn chưa xác định được liệu pháp hóa chất tối ưu sau phẫu thuật, nhưng kết quả từ các nghiên cứu hiện có cho thấy Cisplatin đơn thuần liều thấp (40 mg/m2 hàng tuần) hoặc Cisplatin (50-75 mg/m2 ngày thứ nhất) phối hợp với 5-FU (1000 mg/m2 trong 4 ngày tiếp theo), mỗi 3 tuần, 6-8 chu kỳ có thể cải thiện thời gian sống còn của bệnh nhân. - Tỷ lệ đáp ứng của hóa trị tiên phát (không điều trị hoặc không xạ trị trước đó) là 70-80%. Phối hợp hóa-xạ trị rất có triển vọng bởi vì Cisplatin tác dụng như chất gây nhạy cảm với xạ trị.
Các điều kiện tiên quyết của hóa liệu pháp: Bệnh nhân chấp thuận trị liệu sau được giải thích, phân loại giai đoạn trước mổ với mô tả khối u hay hạch di căn nơi mà tình trạng phục hồi có thể được đánh giá, chất chỉ điểm khối u SCC (+) và nhân viên y tế được đào tạo và có kinh nghiệm trong điều trị hóa liệu pháp.
Chống chỉ định của hóa liệu pháp có chứa Cisplatin
Suy giảm chức năng thận, gan, tủy xương.
Suy tim.
Nhiễm trùng.
Chỉ số hiệu suất thấp.
Các chỉ định được chấp nhận trong hóa liệu pháp ung thư cổ tử cung:
Xạ - hóa trị hỗ trợ sau mổ đối với ung thư cổ tử cung nguy cơ cao.
Hóa trị hỗ trợ đối với khối u to (FIGO giai đoạn I-II).
Xạ - hóa trị đối với giai đoạn tiến triển (FIGO giai đoạn III-IVa).
Đơn hoặc đa hóa trị toàn thân đối với FIGO giai đoạn IVb với di căn xa.
7.2 Điều trị phẫu thuật
7.2.1 Đánh giá trước phẫu thuật
Căn có các xét nghiệm sau: công thức máu, tốc độ lắng máu, điện giải đồ, đông máu, urê và creatinin để đánh giá chức năng thận, aminotransferase, SGOT, SGPT, phosphatase kiềm, tổng phân tích nước tiểu, chất đánh dấu khối u SCC (squamous cell cancer antigen) cho ung thư tế bào lát và CA 125 cho carcinoma tuyển (đôi khi CA 19-9) và đường huyết.
SCC bình thường < 1,5ng/ml: Bệnh nhân với SCC trước mổ > 8 ng/ml có di căn hạch 65%, trong khi SCC < 8 ng/ml thì không có di căn hạch (LinH và cộng sự 2000). Cần thủ độ thanh thải creatinin trong các trường hợp thận ứ nước và tắc nghẽn niệu quản rõ ràng hay khi kế hoạch hóa trị dự kiến có dùng Cisplatin.
Hội chẩn liên khoa: Trong tất cả các bệnh viện và trung tâm ung thư lớn nhất thiết phải có buổi hội chẩn giữa các nhà phẫu thuật phụ khoa vùng chậu, chuyên gia chẩn đoán hình ảnh, chuyên gia xạ trị để cùng thảo luận trường hợp bệnh trước khi điều trị.
7.2.2 Ung thư nội biểu mô
Ở người phụ nữ còn trẻ, còn có nguyện vọng sinh sản, có thể khoét chóp hay cắt cụt cổ tử cung và sau đó cần phải được theo dõi kỹ định kỳ 6 tháng với 3-4 lần làm tế bào học âm đạo. Ở người phụ nữ đủ con, lớn tuổi có thể cắt tử cung toàn phần rộng rãi.
7.2.3 Ung thư cổ tử cung giai đoạn la
Giai đoạn Ia1 và Ia2 bao gồm các trường hợp xâm nhiễm mô đệm sớm và ung thư vi thể. Để chẩn đoán bắt buộc phải khảo sát kỹ mẫu khoét chóp. Xâm nhiễm mô đệm được đo từ màng đáy của biểu mô gốc. Các giai đoạn theo FIGO còn mô tả thêm độ rộng của tổn thương. Độ rộng tối đa của tổn thương giai đoạn la là lan rộng ngang 7mm.
Phân loại theo FIGO không bao gồm thông tin về bờ của mẫu khoét chóp, thông tin về xâm lấn khoang mạch bạch huyết như là yếu tố tiên lượng. Chỉ 0,4% trường hợp xâm nhiễm < 3mm có di căn hạch bạch huyết. 7,3% nhóm xâm nhiễm mô đệm 3,1-5 mm cho thấy có di căn. Trong một nghiên cứu của Nhóm Ung thư Phụ khoa (GOG), 15,6% trong số 32 bệnh nhân có xâm nhiễm 3-5mm (ung thư vi thể) có di căn hạch nhưng chỉ 0,9% trong số 106 bệnh nhân không có LVSI có xâm nhiễm hạch. Như vậy, xâm nhiễm khoang mạch bạch huyết LVSI là yếu tố quyết định cho phương pháp điều trị ở giai đoạn Ial và Ia2.
Xâm nhiễm mô đệm sớm: < 1mm: Nếu xâm nhiễm mô đệm sớm được lấy trong mô lành của chóp và nếu không có yếu tố nguy cơ nào khác thì khoét chóp chẩn đoán có thể được xem là biện pháp điều trị đủ. Bệnh nhân sau đó được theo dõi kỹ bằng tế bào học và soi cổ tử cung. Nếu không có điều kiện theo dõi hoặc nếu có chỉ định cắt tử cung khác thì có thể cắt tử cung đơn giản qua đường bụng hay đường âm đạo.
Giai đoạn Ia: Xâm nhiễm < 3mm (ung thư vi thể) - không LVSI, những trường hợp bệnh nhân vẫn còn muốn có con hoặc có chống chỉ định phẫu thuật cần được theo dõi kỹ bằng tế bào học và soi cổ tử cung. Nếu bệnh nhân không còn muốn có con, nên cắt tử cung đường bụng hoặc đường âm đạo.
Giai đoạn Ia1: Xâm nhiễm < 3mm (ung thư vi thể) - có LVSI, do nguy cơ nguy cơ xâm nhiễm hạch chậu tăng khi có LVSI, người ta khuyên nên cắt tử cung và phẫu tích hạch chậu riêng biệt. Không cần thiết cắt rộng chu cung như trong cắt tử cung tận gốc cải biên (Te Linde) vì trong trường hợp ung thư vi thể không dự kiến có xâm nhiễm mô chu cung liên tục hay không liên tục. Phẫu thuật có thể được thực hiện với đường rạch ngang.
Giai đoạn Ia2: Xâm nhiễm 3-5mm có hoặc không có LVSI, điều trị bao gồm cắt tử cung đơn giản qua đường rạch ngang kèm phẫu tích hạch chậu. Một số tác giả khuyên nên cắt tử cung tận gốc cải biên (Te Linde) cho các trường hợp này. Tuy nhiên, theo các dữ liệu nghiên cứu hiện có, sự cải biên phẫu thuật này dường như không cần thiết.
7.2.4 Điều trị phẫu thuật các giai đoạn I, Ia và III
Điều trị ung thư cổ tử cung xâm lấn tiến triển khá phức tạp. Ngoài khả năng chịu đựng cuộc mổ của bệnh nhân, việc điều trị còn phụ thuộc loại mô học, thể tích khối u và giai đoạn chính xác của bệnh. Thể tích u tương quan với tiên lượng. Trong cùng một giai đoạn bệnh, thể tích khối u càng lớn thì nguy cơ điều trị thất bại tại chỗ và cách xa càng cao. Nói chung đối với giai đoạn FIGO I và II dù cách tiếp cận điều trị là phẫu thuật hoặc xạ trị thì tỷ lệ lành bệnh tương đương, tuy nhiên trong các thập niên gần đây phẫu thuật ngày càng được lựa chọn do tránh được tác dụng phụ kéo dài của xạ trên các phụ nữ phần lớn đã cận kề mãn kinh.
Chỉ định và chống chỉ định phẫu thuật
Quyết định mổ hay không mổ tùy thuộc chủ yếu kích thước khối u, kết quả phân loại giai đoạn trước phẫu thuật và tình trạng của bệnh nhân.
Chỉ định | Chống chỉ định |
Giai đoạn I FIGO Giai đoạn Ila FIGO Giai đoạn IIb FIGO (xâm nhiễm cạnh cổ tử cung hay chỉ 1/3 trong chu cung) Tuổi: < 70 Chỉ số Karnofsky > 80% CT: hạch chậu/cạnh động mạch chủ âm tính. Bệnh nhân đồng ý mổ sau khi đã được giải thích rõ | Giai đoạn IIb FIGO (xâm nhiễm 1/3 giữa và ngoài chu cung) Giai đoạn III/IV FIGO Tuổi > 70 Karnofsky: < 80% Chống chỉ định gây mê hồi sức CT: hạch cạnh động mạch chủ dương tính Đái tháo đường và các rối loạn chuyển hóa khác Nhiễm trùng nặng Béo phì nặng Thận dị dạng Dính bụng nặng do mổ trước đó |
Chỉ số hiệu suất Karnofsky
100 = Bình thường; không than phiền bệnh tật; không có bằng chứng bệnh.
90 = Có thể sinh hoạt bình thường; có dấu hiệu hay triệu chứng nhẹ của bệnh.
80 = Sinh hoạt bình thường với cố gắng; một số dấu hiệu hay triệu chứng bệnh.
70 = Tự chăm sóc được nhưng không thể sinh hoạt bình thường hoặc làm công việc linh hoạt.
60 = Đôi khi cần trợ giúp nhưng có thể tự làm phần lớn nhu cầu cá nhân.
50 = Cần trợ giúp đáng kể và chăm sóc y khoa thường xuyên.
40 = Mất khả năng; cần chăm sóc và trợ giúp đặc biệt.
30 = Mất khả năng nghiêm trọng; chỉ định nhập viện, mặc dù không chết cấp thời.
20 = Bệnh rất nặng, cần nhập viện, cần điều trị nâng đỡ tích cực
10 = Hấp hối; chết đang đến gần.
0 = Đã chết.
Cắt tử cung tận gốc phải được tùy biến cho từng cá nhân theo từng tổn thương, với lưu ý mức độ rối loạn chức năng bàng quang và ruột liên quan trực tiếp đến mức độ triệt để của phẫu tích vùng chậu.
Đường rạch da ở bụng
Đường dọc giữa dưới rốn là đường chuẩn vi cho phép tiếp cận tốt nhất tất cả các cơ quan trong ổ bụng. Các đường rạch khác như Pfannenstiel, Maylard hay Chemey được dành riêng cho những chỉ định thật đặc biệt.
Ví dụ: Phụ nữ 31 tuổi với ung thư cổ tử cung giai đoạn It sớm (xâm nhiễm 7mm trong mẫu khoét chóp, ung thư tế bào gai không sừng hóa, biệt hóa tốt, CT-Scan cho thấy hạch bình thường). Trong trường hợp này, khả năng di căn hạch quan trọng đòi hỏi phẫu tích khó khăn ở vùng chậu chung hay cạnh động mạch chủ rất ít có. Ở đây đường Pfannenstiel rộng cho phép cắt tử cung tận gốc, phẫu tích hạch điển hình, quan sát và thăm khám các cơ quan trong bụng.
Quan sát và thăm khám
Mục đích quan sát và thăm khám ổ bụng là để kiểm tra giai đoạn FIGO trước phẫu thuật. Cần quan sát tử cung và phần phụ, toàn ổ bụng bao gồm ruột non, ruột già, phúc mạc tạng và phúc mạc thành; sau đó thăm khám vùng chu cung hạch chậu và cạnh động mạch chậu. Nếu kết quả khảo sát cho thấy, tổn thương lan rộng hơn phân giai đoạn trước phẫu thuật, phải dừng cuộc mổ và bệnh nhân phải điều trị xạ phối hợp hoặc điều trị xạ-hóa.
Các tiêu chuẩn để ngừng cuộc mổ:
Di căn phúc mạc.
Xâm nhiễm 1/3 giữa và ngoài chu cung.
Hạch cạnh động mạch chủ phì đại.
Xâm nhiễm bàng quang và trực tràng.
Di căn gan, cơ hoành và lách.
Nếu phát hiện hạch di căn phì đại thì phải lấy ra để tạo điều kiện tốt cho xạ phối hợp hoặc xa-hóa trị về sau. Nếu không lấy hạch, phải dự kiến 90-100% tái phát tại vùng ngay cả sau khi điều trị xạ phối hợp hay xạ-hóa. Bóc các hạch lớn làm giảm tái phát đến 50%.
Phẫu tích hạch chậu
Kéo tử cung hướng về phía trên, rạch dọc phúc mạc bàng quang theo dây chằng tròn và nếp bàng quang - tử cung. Bàng quang được đẩy xuống và khoang cạnh bàng quang được mở bằng cách mở rộng hai đầu mũi kéo hay bằng cách dùng đầu ngón tay. Ở phần sâu của khoang cạnh bàng quang có thể thấy các tĩnh mạch lớn hơn từ đám rối Santorini; tránh không để chảy máu từ các tĩnh mạch này.

Sau đó cột cắt dây chằng tròn. Phẫu thuật viên phái quyết định cắt buồng trứng hay không. Nếu bảo tồn, buồng trứng phải được tách biệt khỏi tử cung. Nếu cắt buồng trứng, rạch phúc mạc bên ngoài phần phụ lên đến động mạch chậu chung. Sau khi nhận diện niệu quản, cắt và cột dây chằng thắt lưng chậu.
Tai vòi tử cung và buồng trứng được khấu vào tử cung. Mở phúc mạc băng ngón tay dọc theo các mạch máu chậu hướng về chỗ động mạch chủ chia đôi. Mép trong phúc mạc được cặp kéo hoặc khâu vào bên đối diện để bộc lộ niệu quản lúc này vẫn còn dính vào phúc mạc phía trong.
Các mép trong phúc mạc được kéo sang bên đối diện cùng với niệu quản nằm kề. Lúc này phẫu tích hạch bạch huyết bắt đầu từ bên ngoài giữa các mạch máu chậu ngoài và cơ thăn. Dây thần kinh sinh dục đùi cần được nhận diện ở vị trí này. Tránh bất kỳ tổn thương nào cho dây thần kinh. Giới hạn của phẫu trường bao gồm cơ thăn ở phía ngoài, chỗ chia đôi mạch chậu chung ở phía đầu, tĩnh mạch chậu ở phía trong và ống đùi ở phía chân.
Sau đó hạch bạch huyết được lấy ra từ đỉnh đến đáy bằng tay. Để tránh hình thành nang bạch huyết sau này các mạch bạch huyết cần được kẹp cắt bằng dao điện, cột hoặc kẹp với clip. Sau khi hạch dọc theo các mạch máu chậu chung đã được lấy đi, bước kế tiếp là lấy hạch giữa hai nhánh chậu và hạch bịt.
Các mạch máu chậu ngoài và chậu chung được đẩy khỏi thành chậu bằng kéo và đầu ngón tay. Các nhánh động mạch từ động mạch chậu đến cơ thăn được kẹp cắt và cột. Sau đó đi vào khoang bịt từ phía ngoài giữa mạch máu chậu ngoài và cơ thăn. Đặt dụng cụ kéo tĩnh mạch, cần nhận diện và di động dây thần kinh bịt.
Sau đó, mở khoang bịt về phía trong của các mạch chậu giữa mạch máu và niệu quản. Sau khi nhận diện dây thần kinh bịt, có thể cắt lấy toàn bộ mô mỡ bạch huyết đã được tách ra khỏi vách chậu. Bên dưới tĩnh mạch chậu các nhánh từ tĩnh mạch đến thành chậu cần được bảo tồn để tránh chảy máu. Các động mạch nhỏ được đốt điện, cột hoặc kẹp bằng clip. Trong trường hợp chảy rịn máu có thể kiểm soát chảy máu bằng cách chèn gạc ẩm, ẩm.
Cắt tử cung tận gốc
Các bước trong cắt tử cung tận gốc là:
Chuẩn bị và cắt các dây chằng caudal.
Phẫu tích, cắt, cột động mạch tử cung.
Cắt, cột dây chằng cạnh cổ tử cung.
Di động niệu quản ra khỏi phúc mạc phía trong và phẫu tích phần thấp của niệu quản cùng với di động bàng quang.
Bộc lộ kênh niệu quản.
Mở khoảng trực tràng- âm đạo, di động trực tràng, cắt, cột đầy chẳng từ Khi ng
Chuẩn bị và cắt mỗ cạnh âm đạo và 1/3 trên âm đạo (cách bờ khối u 2cm).
Dẫn lưu và đóng phúc mạc và đóng bụng.
Phẫu tích hạch chậu cho thấy sự cung cấp động mạch vùng chậu và đường đi của niệu quản đi từ ngoài vào trong bắt chéo tại chỗ chia đôi động mạch chậu chung, đôi hướng đi xuống dây chằng cạnh cổ tử cung bằng cách đi luồn bên dưới động mạch tử cung (“nước chảy dưới cầu”) và cuối cùng chạy ra phía trước để vào trong bàng quang tại tam giác bàng quang. Để chuẩn bị cho niệu quản và động mạch tử cung, tử cung được kéo ra trước hoặc ra sau hướng về bên đối diện.
Bộc lộ dây chằng cạnh cổ tử cung và xác định mạch máu tử cung bắt đầu với bộc lộ cẩn thận bằng kéo khoang cạnh bàng quang và khoang cạnh trực tràng. Ngón trỏ đặt vào khoang cạnh bàng quang, ngón giữa đặt vào khoang cạnh trực tràng cho phép xác định dây chằng cạnh cổ tử cung ở giữa các ngón tay.
Lúc này, động mạch tử cung nằm phía bụng dây chằng. Cột động mạch sát gốc với động mạch chậu trong. Động mạch tử cung phải được gọt tỉa nhẹ nhàng và phẫu tích ra khỏi tĩnh mạch tử cung bên dưới. Tổn thương tĩnh mạch tại vị trí này có thể gây chảy máu đáng kể. Sau khi phân lập động mạch được kẹp cột và mối chi cột trên mỏm cụt được để dài để giúp cho phẫu tích kênh niệu quản sau này. Các mạch máu được cột bằng chỉ Vicryl 2.0.
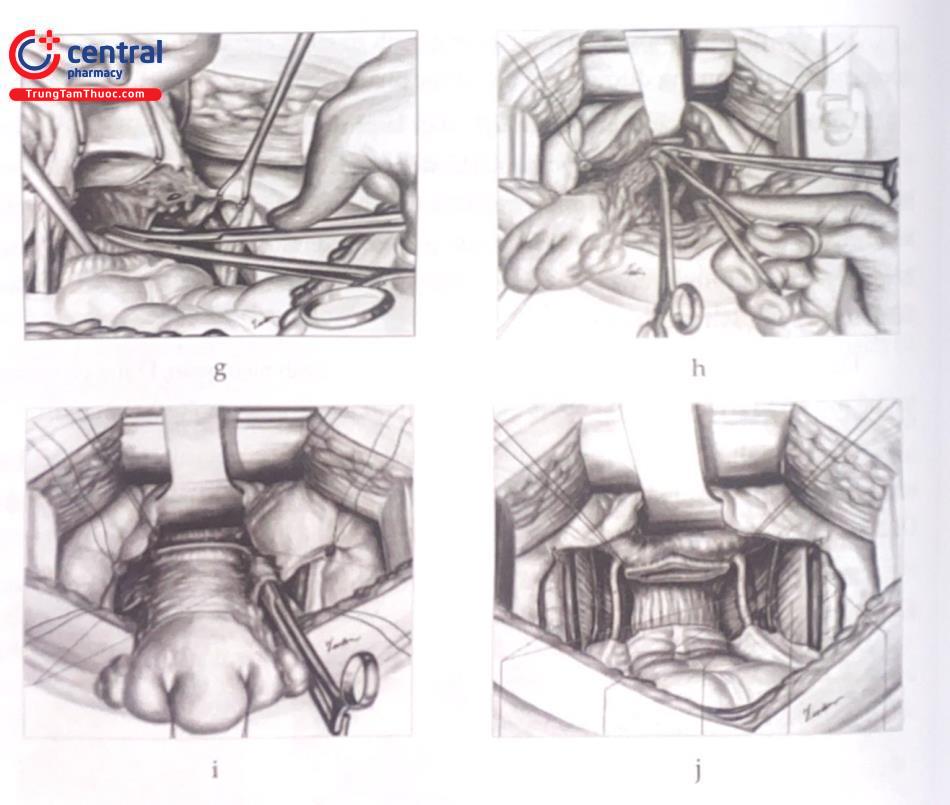
Sau đó, phần bên dưới của dây chằng cạnh tử cung chứa tĩnh mạch tử cung động mạch bàng quang dưới và âm đạo được phẫu tích kẹp cột bằng chỉ Vicryl 20.
Lúc này, niệu quản được phẫu tích khỏi lá phúc mạc trong. Để hoàn tất phẫu tích niệu quản trong dây chằng cạnh cổ tử cung, động mạch tử cung phải được nâng lên khỏi niệu quản. Sau đó kênh niệu quản có thể được chuẩn bị kỹ càng bằng cách kéo hướng đầu và sang bên với một que gạc ẩm. Kênh niệu quản được mở nóc bằng kéo mảnh dưới hướng dẫn của kẹp nâng Overholt đầu cong đã được đưa vào kênh song song với niệu quản.
Dang nhẹ hai đầu dụng cụ sẽ nâng phần nóc của kênh niệu quản. Dụng cụ trong tư thế mở tại vị trí cho phép kẹp nóc kênh niệu quản bằng overholt và tách mô.
Lúc này, di động nhẹ nhàng niệu quản ra khỏi nền của kênh niệu quản. Từ vùng này, gối niệu quản đi theo một đường cong hướng ra ngoài đến bàng quang. Di động niệu quản hướng ra ngoài cho phép kẹp cắt mô cạnh âm đạo sau này.
Di động nhẹ nhàng niệu quản ra khỏi nền của nó trong kênh niệu quản. Nóc kênh niệu quản đã được mở.

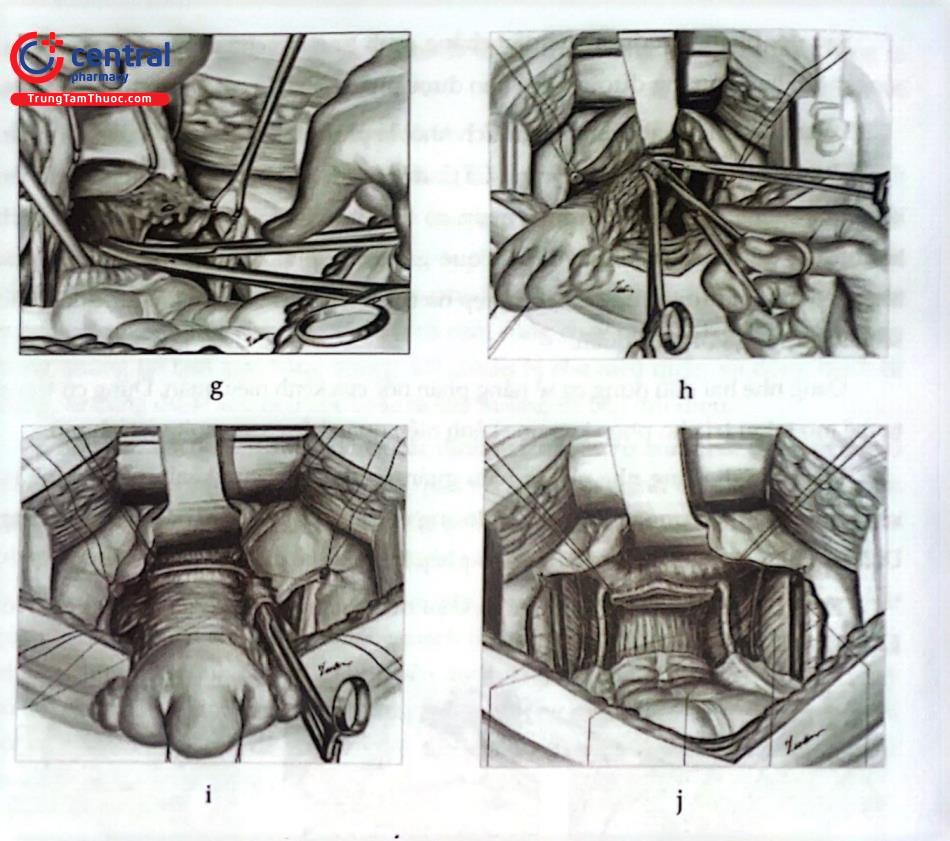
Sau khi đã thực hiện xong tất cả các bước chuẩn bị cắt tử cung tận gốc, chúng ta rạch phúc mạc túi cùng sau giữa hai dây chằng tử cung - cùng. Di động trực tràng bằng cách tách nó ra khỏi âm đạo. Kéo tù cung mạnh về hướng bàng quang trong khi trực tràng được kéo hướng đầu bằng một kẹp có gắn miếng gạc nhỏ ở đầu.
Tiếp theo kẹp cắt phần đầu của dây chẳng tử cung - cùng.
Cẩn thận không để trực tràng bị tổn thương. Phần ngoài cùng của dây chằng tử cung - cùng chứa các dây thần kinh tự động của bàng quang. Vì vậy, phần thứ hai và thứ ba của dây chằng không được kẹp quá sát xương cùng để hạn chế rối loạn chức năng bàng quang và trực tràng.
Sau khi khoang cạnh quanh bàng quang và khoang cạnh trực tràng đã được hợp nhất nhờ phẫu tích dây chằng cạnh cổ tử cung và sau khi dây chằng tử cung cùng đã được phẫu tích, có thể phẫu tích mô chu cung còn lại và mô cạnh âm đạo trong khi niệu quản di động được cẩn thận kéo ra ngoài. Lúc này kéo tử cung về hướng đối diện và mô cạnh tử cung/cạnh âm đạo được nối lại và được cắt làm 2-3 phần với kẹp chu cung chắc (kim Wertheim). Tránh chảy máu bằng cách che chắn cẩn thận bằng van bàng quang và niệu quản đã di động từ trước. Chỗ kẹp được thay thế bằng các mối chi Vicryl chắc chắn.
Kẹp Wertheim được đặt ngang qua âm đạo tránh để rơi vãi tế bào khối u vào âm đạo hoặc ổ bụng. Đường cắt bên dưới kẹp và bên trên các mối chỉ góc phải cách bờ khối u ít nhất 2-3cm. Thực hiện cắt ngang bằng kéo cong hoặc bằng dao mổ. Trước khi đóng phúc mạc và đóng bụng kiểm tra kỹ trực tràng niệu quản, bàng quang.
Nếu có nghi ngờ tổn thương bàng quang hay niệu quản có thể bơm xanh methylen vào bàng quang hay tiêm tĩnh mạch dung dịch indigocarmin để nhận diện rò rỉ.

Trước đây, phúc mạc được đóng theo Symmonds và Pratt. Phúc mạc phía bên ngoài được để hở nhằm tránh hình thành nang bạch huyết ở thành chậu. Tuy nhiên, vẫn khâu mép âm đạo trước vào phúc mạc bàng quang và mép sau vào thành trước/phúc mạc trực tràng. Theo Symmonds và Pratt cần khấu thêm đường khâu thứ hai để tách âm đạo và ổ bụng. Nhiều phẫu thuật viêm vùng chậu cho rằng điều này không cần thiết do không có bằng chứng tăng nhiễm trùng phúc mạc hay sa quai ruột vào trong âm đạo. Sau khi lấy tất cả gạc chèn, rửa ổ bụng bằng NaCl 0,9% hoặc Ringer lactate và đóng bụng theo kiểu cổ điển hay bằng thòng lọng.

Tranh cãi về cắt tử cung tận gốc
Tranh cãi chủ yếu thuộc các lĩnh vực sau:
Phẫu thuật Wertheim-Meigs phải triệt để đến mức độ nào đối với dây chằng cạnh cổ tử cung, âm đạo và dây chằng tử cung - cùng?
Phải lấy bao nhiêu hạch?
Phải làm gì nếu có di căn hạch trong vùng chậu?
Khi nào cắt và khi nào không cắt buồng trứng?
Mức độ triệt để:
PI | Cắt tử cung ngoài cân | Không có chỉ định nào khác |
PII | Lấy 1/2 trong của các dây chằng chu cung, tử cung - cùng và đến 1/3 trên âm đạo | Ung thư giai đoạn Ib, IIa |
PIII | Lấy toàn bộ các dây chằng chu cung, tử cung cùng và cắt hết 1/3 trên âm đạo | Ung thư giai đoạn Ilb |
PIV | Cắt hết mô cạnh niệu quản, động mạch trên bàng quang và 3/4 âm đạo | Tái phát phần trên trước, bảo tồn bàng quang khi có thể |
PV | Cắt một phần niệu quản và bàng quang | Ung thư tái phát đến phần xa của niệu quản và bàng quang |

Số hạch bạch huyết
Đánh giá mô bệnh học mô bạch huyết lấy từ hạch chậu cần nhận diện 20-30 hạch chậu và cần nhận diện thêm 20-30 hạch cạnh động mạch chủ nếu có nạo hạch này. Trong giai đoạn la1 không cần nạo hạch vì nguy cơ di căn hạch < 3%.
Bảo tồn buồng trứng
Bảo tồn buồng trứng trong các trường hợp phụ nữ trẻ với ung thư giai đoạn sớm có yếu tố tiên lượng tốt và không dự kiến xạ trị sau mổ. Phụ nữ trên 45-50 tuổi có u ở vị trí eo, LVSI, mô học nguy cơ cao hoặc ung thư tế bào nhỏ và biệt hóa thấp mức độ III trong mẫu khoét chóp thì nên cắt buồng trứng.
Phẫu thuật lấy hạch quanh động mạch chủ
Lấy hạch quanh động mạch chủ hay không được quyết định trong lúc mổ tuy thuộc các dấu hiệu thấy được khi mổ và tùy thuộc phân tích đánh giá giai đoạn trước mổ.
Chỉ định tuyệt đối của phẫu thuật lấy hạch quanh động mạch chủ:
Khâu lớn, giai đoạn IB2 (> 4cm), xâm lấn sâu.
Giai đoạn IIA
Trong khi mổ thấy có dấu hiệu di căn hạch chậu.
Chỉ định tương đối
Có LVSI (xâm lấn vào mạch bạch huyết) trên kết quả sinh thiết/khoét chóp trước mổ.
Hình ảnh mô học có nguy cơ cao của ung thư tế bào nhỏ.
Mức độ biệt hóa III trên kết quả sinh thiết/khoét chóp.
Các số liệu của Winter và cộng sự (1988) cho thấy không có di căn hạch cạnh động mạch chủ nếu ung thư giai đoạn Ib và cũng chỉ có 3,2% hạch dương tính nếu giai đoạn IIb. Vì vậy, những trường hợp di căn nhảy giai đoạn đến hạch cạnh động mạch chủ rất hiếm nhưng cũng có thể xảy ra.
Nếu trong lúc mổ thấy trên đại thể hạch cạnh động mạch chủ phì đại hoặc nếu trước mổ đã có dấu hiệu nghi ngờ trên CT/MRI, thị trên 45% có dương tính trên mô học.
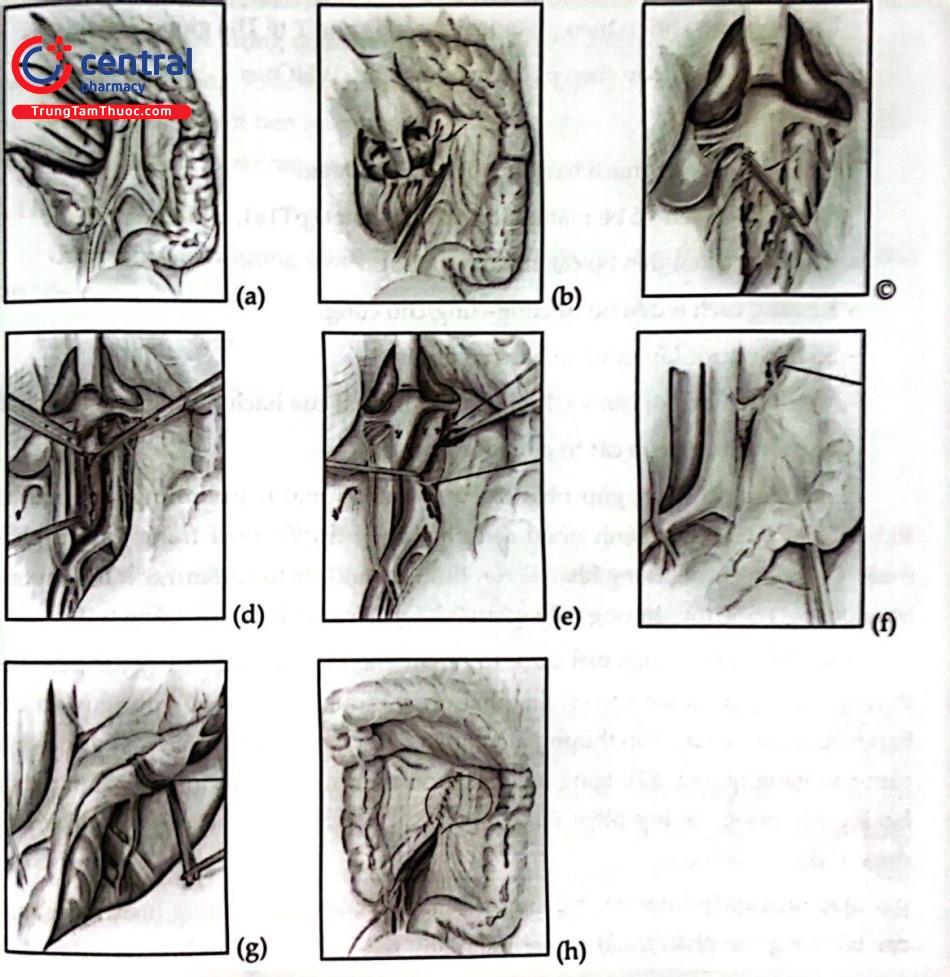
Kỹ thuật phẫu tích hạch cạnh động - tĩnh mạch chủ
Mở bụng theo đường giữa từ dước ức đến xương vệ. Sau khi lấy hạch vùng chậu, tiếp tục mở phúc mạc dọc theo động mạch chậu chung phải, ngược theo động mạch chủ đến góc Treitz. Mở một đường thứ hai vòng quanh manh tràng vào rãnh cạnh đại tràng phải lên đến gan.
Lấy hạch cạnh động mạch chủ bắt đầu với di động manh tràng và đặt ruột non vào trong một túi Nhựa ẩm.
Phẫu thuật bắt đầu từ động mạch chậu chung và tiếp tục bên phải của tĩnh mạch chủ nơi hạch và mô mỡ bạch huyết nằm trên lớp ngoại mạc của mạch máu. Phẫu tích cẩn thận bằng kềm forceps cho thấy và cho phép đốt hoặc kẹp bằng clip dễ dàng các nhánh nhỏ của các mạch máu lớn. Thông thường, có thể tìm thấy một tĩnh mạch nhỏ nằm trên chỗ chia động mạch chậu 3cm.
Sau khi tách mô bạch huyết ở phía trước, lấy các hạch ở bên phải của tĩnh mạch chủ trong khi đẩy tĩnh mạch về phía đối diện. Cần tránh không làm tổn thương các tĩnh mạch thắt lưng nhỏ ở mặt sau.
Phẫu tích hạch vùng liên tĩnh mạch - động mạch chủ. Bước kế tiếp là lấy hạch bạch huyết cạnh động mạch chủ ở phía bên trái động mạch chủ. Cần nhận diện được tĩnh mạch thận trái, gốc của tĩnh mạch buồng trứng trái và quan trọng nhất là động mạch mạc treo ruột dưới. Mạch máu này cần phải được bảo tồn trong mọi trường hợp vì nó cung cấp máu cho đại tràng. Niệu quản được nhận diện phía bên trái dù nó nằm bên trái của phẫu trường. Các mạch máu của buồng trứng trái được lấy đi bằng cách tiếp cận từ dưới kết tràng di động, từ nơi này dùng kẹp túm chặt bỏ mạch và kéo xuống.
Đặt các ống dẫn lưu mềm hút hai bên các mạch máu lớn và đóng phúc mạc phía trên các mạch máu lớn bằng mũi khâu liên tục.
Lược đồ phẫu thuật
Một bản lược đồ phẫu thuật chuẩn cắt tử cung tận gốc cần ghi lại các điểm sau:
Chẩn đoán giai đoạn theo tiêu chuẩn FIGO và tình trạng gia tăng giai đoạn so với trước mổ (nếu có). Điều trị bao gồm mức độ tận gốc (tiêu chuẩn Piver II hoặc III), có hay không cắt buồng trứng, sinh thiết lạnh, tế bào học phúc mạc... Đường rạch.
Ghi nhận những điều quan sát và sờ thấy.
Mô tả các bước phẫu thuật phẫu tích hạch chậu, cắt tử cung, phẫu tích hạch cạnh động mạch chủ.
Phần u còn lại? (RO/R1-resection). Có phần u còn lại có được đánh dấu bằng dịp để xạ trị sau này.
Kỹ thuật đóng bụng.
Các yêu cầu đối với tường trình giải phẫu bệnh
Kết quả giải phẫu bệnh phải cung cấp thông tin cần thiết cho quyết định điều trị tiếp theo, như:
Loại mô học khối u theo phân loại của Tổ chức Y tế Thế giới (WHO).
Phân loại giai đoạn theo pTNM với mô học (WHO).
Phân độ mô học.
Xâm lấn khoang mạch bạch huyết và mạch máu.
Độ sâu xâm lấn và bề mặt khối u theo milimet(pT1a1,pT1a2).
Khoảng cách u đến bờ cắt âm đạo (pT2b).
Khoảng cách u đến bờ tử cung-cung/chu cung.
Số hạch được lấy ra và số hạch có di căn.
Vị trí của hạch di căn và đường kính lớn nhất của hạch dương tính lớn nhất. Các biến chứng của cắt tử cung tận gốc
Biến chứng thường gặp nhất trong khi mổ là mất máu. Lượng máu mất từ 800-1.500ml và 1/3 các bệnh nhân cần phải được truyền máu trong và sau phẫu thuật. Các biến chứng nặng khác là tổn thương mạch máu chiếm 1,8%, tổn thương bàng quang 1,3%, tổn thương hiệu quản 0,3%, thần kinh bịt - trực tràng 0,1%.
Các tổn thương nhận biết được trong lúc mô thường được xử lý tức thời. Tổn thương niệu quản đoạn cao có thể phải được thông nối tới tận với nguy cơ chít hẹp niệu quản về sau. Tổn thương niệu quản đoạn nằm sâu tốt nhất nên được khâu cắm vào bàng quang. Khi hàng quang bị tổn thương, cần áp dụng kỹ thuật khâu hai lớp kín nước với lớp niêm mạc được khâu liên tục (chỉ 3.O) và sau đó lớp cơ được khâu vắt liên tục.
Dù niệu quản hoặc bàng quang là hậu quả của chấn thương hoặc thiếu máu cục bộ trong lúc phẫu thuật và rất hiếm xảy ra. Dò niệu quản hoặc âm đạo điển hình xảy ra ngày bảy đến ngày thứ mười sau mổ. Chẩn đoán phân biệt dò bàng quang hoặc dò niệu quản nên được xác định bằng cách bơm vào đầy bàng quang dung dịch xanh methylen và đặt một gạc khô vào âm đạo. Nếu gạc không nhuộm xanh methylen (không dò bàng quang), tiêm vào tĩnh mạch indigocarmin. Nếu góc trong âm đạo nhuộm màu sau khi tiêm thuốc thì chẩn đoán xác định có độ màu quân. Chụp hệ niệu cản quang có thể giúp xác định niệu quản nào bị tổn thương và có phối hợp với chít hẹp không. Soi bàng quang với chụp bể thận ngược chiều có thể cung cấp thêm thông tín và hiệu quản bị chít hẹp có thể được nong ra đồng thời.
Khả năng sống sót 5 năm sau cắt tử cung tận gốc.
Với điều trị phẫu thuật đơn thuần, tỷ lệ sống sót 5 năm trong ung thư cổ tử cung giai đoạn Ib đến Ilb là 70-85%. Yếu tố quyết định khả năng sống còn là di căn hạch vì đây là yếu tố tiên lượng quan trọng nhất. Bệnh nhân ung thư cổ tử cung không đi căn hạch có xác suất sống 95%, trong khi hạch bạch huyết dương tính là dấu hiệu của một bệnh toàn thân với tiên lượng không thuận lợi gia tăng. Do vậy, các bệnh nhân ung thư cổ tử cung có nguy cơ cao cần được điều trị hỗ trợ toàn thân với xạ- hóa trị.
8 TIÊN LƯỢNG
Các yếu tố tiên lượng quan trọng nhất cho kết quả lâm sàng trong ung thư cổ tử cung là:
Giai đoạn bệnh.
Kích thước khối u.
Loại mô học.
Độ biệt hóa.
Độ sâu xâm nhiễm mô đệm.
Xâm nhiễm khoang mạch bạch huyết (LVSI) và khoang mạch máu (BVSI).
Xâm nhiễm hạch bạch huyết.
Chất chỉ điểm ung thư tế bào lát.
Di căn hạch là yếu tố dự đoán độc lập quan trọng cho thời gian sống sót không bệnh và thời gian sống sót toàn bộ. Bệnh nhân giai đoạn Ib/Ila được cắt từ cung tận gốc có thời gian sống sót trung bình 90% nếu hạch chậu âm tính và chỉ 65% nếu hạch chậu dương tính. Xâm nhiễm hạch chậu hai bên không quan trọng bằng số lượng tuyệt đối hạch bị xâm nhiễm. Vì vậy, bệnh nhân với 1-3 hạch xâm nhiễm được báo cáo có thời gian sống sót 5 năm là 70%, trong khi bệnh nhân với trên 3 hạch có thời gian sống sót trung bình chỉ là 30% (Burghardt 1993).
Tỷ lệ sống sau 5 năm:
Giai đoạn 0 (ung thư trong liên bào): 100%.
Giai đoạn I: 80%.
Giai đoạn II: 50%.
Giai đoạn III: 20-30%.
Giai đoạn IV: dưới 10%.
9 DỰ PHÒNG
9.1 Dự phòng cấp 1 (dự phòng sơ cấp)
Dự phòng cấp 1 bao gồm sự thay đổi hành vi, lối sống liên quan đến việc tăng nguy cơ mắc ung thư cổ tử cung và tiêm vaccine phòng nhiễm HPV.
9.1.1 Thay đổi hành vi, lối sống
Một số hành vi, lối sống có thể làm tăng nguy cơ bị nhiễm HPV và có thể làm tăng nguy cơ ung thư cổ tử cung. Các biện pháp truyền thông, giáo dục sức khỏe nhằm giảm lối sống tình dục có nguy cơ cao, quan hệ tình dục an toàn, tránh hoặc làm giảm các yếu tố nguy cơ khác như lập gia đình sớm, có con sớm, hút thuốc lá (kể cả chủ động và thụ động). Bên cạnh đó, tăng cường chế độ ăn uống lành mạnh giàu trái cây và rau quả, duy trì cân nặng hợp lý và vận động thể lực thường xuyên có thể làm giảm nguy cơ ung thư cổ tử cung. Một lối sống lành mạnh sẽ tối ưu hóa chức năng hệ thống miễn dịch và làm giảm tác động của những yếu tố làm thúc đẩy nguy cơ ung thư trong cơ thể.
9.1.2 Tiêm vaccine phòng lây nhiễm HPV
Tiêm vaccine HPV là biện pháp dự phòng cấp 1 nhằm phòng ngừa lây nhiễm các chủng HPV nguy cơ cao, từ đó phòng ngừa ung thư cổ tử cung, âm hộ, âm đạo, các tổn thương tiền ung thư hoặc loạn sản, mụn cóc sinh dục và bệnh lý do nhiễm HPV. Hiện nay có nhiều loại vaccine HPV khác nhau (vaccine nhị giá, tứ giá, chín giá...) và tùy thuộc vào các chủng vi rút mà vaccine bảo vệ mà các vaccine có những hiệu quả bảo vệ với các bệnh khác nhau. Liệu trình tiêm vaccine HPV khác nhau tùy thuộc loại vaccine và độ tuổi của người tiêm.
Vaccine HPV không có chỉ định cho phụ nữ có thai, tuy nhiên một số bằng chứng từ nhóm các phụ nữ không biết mình mang thai tại thời điểm tiêm vaccine và tiếp tục thai kỳ cho thấy, không có ảnh hưởng có hại nào lên sự phát triển của thai và kết cục thai kỳ. Tiêm vaccine HPV không thay thế cho biện pháp sàng lọc tổn thương cổ tử cung (biện pháp dự phòng cấp 2) cũng như các cảnh báo về việc phơi nhiễm HPV và các bệnh lây truyền qua đường tình dục.
9.2 Dự phòng cấp 2 (dự phòng thứ cấp)
Dự phòng cấp 2 bao gồm sàng lọc phát hiện các tổn thương tân sản nội biểu mô cổ tử cung và xử trí phù hợp. Các phương pháp hiện được dùng trong sàng lọc các tổn thương tiền ung thư và ung thư cổ tử cung bao gồm:
Xét nghiệm tế bào cổ tử cung (cổ điển hoặc nhúng dịch).
Quan sát cổ tử cung với dung dịch acid acetic hoặc dung dịch lugol.
Xét nghiệm HPV nguy cơ cao.
Sau khi được phát hiện và chẩn đoán, có thể điều trị tổn thương tiền ung thư bằng một trong các phương pháp:
Nhóm phương pháp cắt bỏ: khoét chóp bằng dao, dao điện, laser, LEEP.
Nhóm phương pháp phá hủy: áp lạnh, đốt điện, hóa hơi bằng laser.
Để đạt được hiệu quả trên cộng đồng, các chương trình sàng lọc cần đạt được độ bao phủ tối thiểu 70% quần thể đích.
9.3 Dự phòng cấp 3 (dự phòng tam cấp)
Dự phòng cấp 3 bao gồm phát hiện các trường hợp ung thư xâm lấn ở giai đoạn sớm và điều trị triệt để tại các cơ sở có đủ điều kiện, nhằm làm giảm tỷ lệ tử vong do Ung thư cổ tử cung. Điều trị ung thư giai đoạn tiến xa và chăm sóc giảm nhẹ là các thành tố không thể thiếu trong dự phòng và kiểm soát ung thư cổ tử cung.
10 TÀI LIỆU THAM KHẢO
1. Bộ Y tế. Hướng dẫn sàng lọc, điều trị tổn thương tiền ung thư để dự phòng thứ cấp ung thư cổ tử cung. 2011.
2. Bosch FX, Burchell AN, Schiffman M, Giuliano AR, de Sanjose S, Bruni L, et al. Epidemiology and natural history of Human Papillomavirus infections and typespecific implications in cervical neoplasia. Vaccine. 2008;26(Suppl 10):K1-16.
3. Cao Ngọc Thành, Nguyễn Vũ Quốc Huy, Phụ khoa. Nhà xuất bản Y học. 2016. 4. Châu Khắc Tú, Nguyễn Vũ Quốc Huy. Ung thư cổ tử cung: từ dự phòng đến can thiệp sớm. Nhà xuất bản Đại học Huế. 2011.
5. de Sanjose S, Alemany L, Ordi J, et al. Worldwide Human Papillomavirus genotype attribution in over 2000 cases of intraepithelial and invasive lesions of the vulva. Eur J Cancer. 2013;49(16):3450-3461.
6. Diep NTN, Kate S, Huy NVQ, Thuan VT, Nga HN, LaMontagne DS, PhilipCastle, Karen C. The burden of cervical cancer in Vietnam: Synthesis of the evidence. Cancer Epidemiol. 2019,59:83-103.
7. Frumovitz M. Invasive cervical cancer: Epidemiology, risk factors, clinical manifestations, and diagnosis. UpToDate version 20.0. https://www.uptodate.com/ contents/invasive-cervical-cancer-epidemiology-risk-factors-clinical-manifestations- and-diagnosis.
8. Hướng dẫn điều trị Sản Phụ khoa. Nhà xuất bản Y học. 2016.
9. Laufer MR. Benign cervical lesions and congenital anomalies of the cervix. UpToDate version 20.0. https://www.uptodate.com/contents/benign-cervical- lesions-and-congenital-anomalies-of-the-cervix.
10. Perkins RB, Guido RS, Castle PE, Chelmow D, Einstein ME, Garcia F, et al, 2019 ASCCP Risk-Based Management Consensus Guidelines for Abnormal Cervical Cancer Screening. J Low Genit Tract Dis. 2020;24:102-131
11. Straughn Jr JM, Yashar C. Management of early-stage cervical cancer. UpToDate version 20.0. https://www.uptodate.com/contents/management-of-early- stage-cervical-cancer.
12. Straughn Jr JM, Yashar C. Management of locally advanced cervical cancer. UpToDate version 20.0. https://www.uptodate.com/contents/management- of-locally-advanced-cervical-cancer.
13. Vu HNQ Tram NVQ Tam LM, Bạch NH, Thang PVB, Vinh TQ Thanh CN, Piero C. Community-based prevalence versus hospital-based incidence of genital Human Papillomavirus infection in Central Vietnam. J Infect Dev Ctries. 2018; 12(7):568-572.

