Phân loại thuốc điều trị ung thư phổi không tế bào nhỏ và phác đồ điều trị của Bộ Y tế
1 Các phương pháp điều trị ung thư phổi không tế bào nhỏ
Ung thư phổi là nguyên nhân tử vong hàng đầu do ung thư với hơn 1,38 triệu ca tử vong toàn cầu. Ung thư phổi không tế bào nhỏ (NSCLC) chiếm 80% tổng số ca, bao gồm ung thư biểu mô tuyến (32-40%), ung thư biểu mô vảy (25-30%) và ung thư biểu mô tế bào lớn (8-16%). Việc điều trị phụ thuộc vào kích thước, mức độ lan rộng của khối u, đặc điểm sinh học của tế bào ung thư và tình trạng sức khỏe người bệnh. Các phương pháp điều trị bao gồm:
- Phẫu thuật: Cắt bỏ khối u và mô lành xung quanh. Có thể kết hợp với hóa trị hoặc xạ trị.
- Xạ trị: Dùng tia năng lượng cao để phá hủy tế bào ung thư, áp dụng khi phẫu thuật không khả thi hoặc để giảm triệu chứng di căn.
- Hóa trị: Dùng thuốc chống ung thư để tiêu diệt hoặc làm chậm sự phát triển tế bào ung thư, có thể kết hợp với phẫu thuật hoặc xạ trị.
- Liệu pháp nhắm trúng đích: Sử dụng thuốc đặc hiệu ức chế các phân tử quan trọng trong tế bào ung thư, cần xét nghiệm gen trước khi điều trị.
- Liệu pháp miễn dịch: Kích hoạt hệ miễn dịch của cơ thể để tấn công tế bào ung thư, đặc biệt khi phẫu thuật không thể thực hiện.
- Chăm sóc giảm nhẹ: Hỗ trợ giảm đau và các triệu chứng, cải thiện chất lượng cuộc sống cho bệnh nhân ung thư, kết hợp với các phương pháp điều trị chính.
===> Xem thêm bài viết: Điều trị ung thư phổi nguyên phát bằng hóa chất

2 Các thuốc hoá trị điều trị NSCLC
Các thuốc hóa trị được sử dụng trong điều trị ung thư phổi không tế bào nhỏ (NSCLC) đa dạng về cơ chế tác dụng và đặc tính dược lý, góp phần quan trọng trong kiểm soát và cải thiện tiên lượng cho bệnh nhân. Dưới đây là mô tả chi tiết về một số thuốc hóa trị phổ biến trong điều trị NSCLC:
2.1 Cisplatin
Cisplatin là thuốc hóa trị chứa nguyên tố bạch kim, được sử dụng để điều trị nhiều loại ung thư như ung thư phổi, tinh hoàn, buồng trứng, bàng quang…
Cơ chế hoạt động của thuốc được cho là liên kết chéo với các bazơ purin trên DNA, can thiệp vào cơ chế sửa chữa DNA. Điều này gây tổn thương DNA, làm gián đoạn quá trình sao chép và phiên mã DNA, dẫn đến quá trình apoptosis (chết tế bào theo chương trình) của tế bào ung thư. Thuốc chứa Cisplatin như Platinol , Platinol-AQ.
2.2 Carboplatin
Carboplatin, một loại thuốc chống ung thư thế hệ thứ hai dựa trên nguyên tố bạch kim. được thiết kế nhằm giảm độc tính so với cisplatin. Thuốc thường được dùng trong điều trị ung thư buồng trứng, phổi, và vùng đầu cổ.
Cơ chế: Tương tự cisplatin, carboplatin tạo liên kết chéo với DNA, ngăn chặn quá trình sao chép và phiên mã DNA, dẫn đến apoptosis. Carboplatin có đặc tính dược động học khác, với ít tác dụng phụ như độc thận và độc thần kinh hơn. Thuốc chứa Carboplatin như Paraplatin.
2.3 Paclitaxel
Paclitaxel là thuốc điều trị ung thư có trong vỏ cây thông đỏ Taxus brevifolia, có cấu trúc hóa học đặc biệt (một diterpen với vòng taxane và chuỗi este ở C-13).
Cơ chế: Thuốc thúc đẩy sự trùng hợp tubulin thành vi ống ổn định và ngăn chúng bị phân hủy bởi lạnh hoặc Canxi. Paclitaxel gắn đặc hiệu vào tiểu đơn vị beta của tubulin, ngay cả khi không có các yếu tố hỗ trợ như GTP hoặc protein liên kết vi ống. Sự hiện diện của thuốc gây tái cấu trúc bộ xương tế bào, tạo thành các bó vi ống lớn và bền vững, dẫn đến ức chế phân bào ở pha G2/M. Thuốc chứa Paclitaxel như Taxol.
2.4 Nab-paclitaxel
Nab-paclitaxel là dạng paclitaxel liên kết với Albumin nhằm cải thiện khả năng hòa tan và giảm phản ứng dị ứng so với dạng paclitaxel truyền thống.
Cơ chế: Tương tự paclitaxel, nab-paclitaxel ổn định vi ống và ức chế phân bào. Dạng liên kết với albumin giúp tăng cường phân phối thuốc và khả năng xâm nhập khối u thông qua các thụ thể albumin trên tế bào nội mô khối u. Thuốc chứa Nab-paclitaxel ví dụ như Abraxane.
2.5 Docetaxel
Docetaxel là thuốc hóa trị liệu thế hệ thứ hai thuộc họ taxane.
Cơ chế: Cơ chế tác dụng chính của docetaxel là liên kết với β-tubulin, làm tăng sinh và ổn định cấu hình. Điều này cản trở quá trình lắp ráp thoi phân bào, khiến tế bào bị ngừng chu kỳ ở pha G2/M. Bên cạnh đó, docetaxel còn làm giảm biểu hiện của BCL2, một gen chống apoptosis thường được biểu hiện quá mức trong tế bào ung thư, giúp tế bào ung thư dễ dàng trải qua quá trình chết theo chương trình (apoptosis) hơn. Từ đó tăng cường khả năng sống sót, thuốc chứa Docetaxel ví dụ như Taxotere.
 Xem tất cả ảnh
Xem tất cả ảnhLiên hệCòn hàng
| Công ty đăng ký | Công ty TNHH Sanofi-Aventis Việt Nam |
| Số đăng ký | VN2-129-13 |
| Dạng bào chế | Dung dịch đậm đặc |
| Quy cách đóng gói | Hộp 1 lọ x 4ml |
| Hạn sử dụng | 24 tháng |
| Mã sản phẩm | thom542 |
2.6 Gemcitabine
Gemcitabine là thuốc hóa trị dạng đồng phân nucleoside.
Cơ chế: Gemcitabine được tích hợp vào DNA trong quá trình sao chép, gây ngắt chuỗi DNA. Ngoài ra, nó còn ức chế enzyme ribonucleotide reductase, làm giảm nguồn nguyên liệu cho tổng hợp DNA, dẫn đến apoptosis. Thuốc chứa Vinorelbine ví dụ như thuốc Gemzar.
 Xem tất cả ảnh
Xem tất cả ảnhLiên hệCòn hàng
| Công ty đăng ký | Eli Lilly Asia, Inc-Thailand Branch |
| Số đăng ký | VN2-549-17 |
| Dạng bào chế | Bột đông khô pha dung dịch tiêm truyền |
| Quy cách đóng gói | Hộp 1 lọ |
| Hạn sử dụng | 36 tháng |
| Mã sản phẩm | thom415 |
2.7 Vinorelbine
Cơ chế: Vinorelbine là thuốc chống ung thư tác động lên quá trình phân bào bằng cách ức chế động lực của vi ống, dẫn đến ngừng phân chia và chết tế bào. Ở nồng độ cao, vinorelbine làm phân rã vi ống và phá hủy thoi phân bào, còn ở nồng độ thấp, nó ngăn chặn quá trình tiến triển của phân bào. Thuốc gắn vào tiểu đơn vị β-tubulin tại vị trí gắn Vinca, làm tăng sự ổn định của tubulin và giảm tốc độ biến động của vi ống, từ đó làm giảm lực căng lên kinetochore và ngăn chặn sự dịch chuyển của nhiễm sắc thể tới trung tâm thoi phân bào. Thuốc chứa Vinorelbine ví dụ như thuốc Navelbine.
2.8 Etoposide
Cơ chế: Etoposide (còn được gọi là VP-16) là chất ức chế enzyme topoisomerase II, chủ yếu tác động ở pha cuối của giai đoạn S và G2 trong chu kỳ tế bào. Topoisomerase II có vai trò cắt và nối lại cả hai mạch của chuỗi DNA để tháo xoắn trong quá trình sao chép. Etoposide can thiệp vào quá trình này bằng cách ổn định phức hợp cắt DNA của topoisomerase II, nhưng ngăn chặn bước nối lại. Sự tích tụ các đứt gãy DNA mạch kép kích hoạt các con đường gây đột biến và apoptosis.
2.9 Pemetrexed
Pemetrexed là thuốc chống folate đa mục tiêu, được dùng chủ yếu trong điều trị ung thư màng phổi và ung thư phổi không tế bào nhỏ.
Cơ chế: Pemetrexed ức chế nhiều enzyme phụ thuộc folate tham gia tổng hợp purin và pyrimidin như thymidylate synthase, dihydrofolate reductase và glycinamide ribonucleotide formyltransferase, làm giảm tổng hợp DNA và RNA, dẫn đến chết tế bào. Ví dụ như thuốc Alimta.
3 Các loại thuốc đích điều trị NSCLC
Thuốc nhắm đích có cơ chế hoạt động khác biệt so với hóa trị tiêu chuẩn, có thể mang lại hiệu quả ngay cả khi hóa trị không đáp ứng. Hiện nay, thuốc nhắm đích được ứng dụng rộng rãi trong điều trị ung thư phổi tiến triển, có thể sử dụng kết hợp với hóa trị hoặc đơn độc.
3.1 Thuốc ức chế EGFR
Cơ chế hoạt động: Thụ thể yếu tố tăng trưởng biểu bì (EGFR) là một loại protein nằm trên bề mặt tế bào, đóng vai trò quan trọng trong việc kiểm soát sự phát triển và phân chia tế bào. Ở một số trường hợp ung thư phổi không phải tế bào nhỏ (NSCLC), EGFR bị sản xuất quá mức, khiến các tế bào ung thư tăng sinh nhanh chóng. Thuốc này có thể ngăn chặn tín hiệu từ EGFR – tín hiệu vốn thúc đẩy sự phát triển của tế bào ung thư. Những thuốc này thường được sử dụng để điều trị NSCLC giai đoạn tiến triển có mang các đột biến nhất định trên gen EGFR. Ngoài ra, thuốc osimertinib cũng có thể được sử dụng như một phương pháp điều trị bổ trợ sau phẫu thuật ở một số trường hợp ung thư phổi giai đoạn sớm.
Ví dụ về thuốc ức chế EGFR:
+ Thuốc ức chế EGFR nhắm vào các tế bào có đột biến exon 19 hoặc exon 21:
- Các loại thuốc như afatinib (Gilotrif) , erlotinib (Tarceva) , dacomitinib (Vizimpro) , gefitinib (Iressa) và osimertinib ( Tagrisso ) có thể được dùng riêng.
- Lazertinib (Lazcluze) kết hợp với amivantamab (Rybrevant).
- Osimertinib phối hợp với hóa trị liệu (cisplatin hoặc carboplatin với pemetrexed).
- Erlotinib kết hợp với thuốc ức chế VEGF (ramucirumab hoặc bevacizumab).
- Amivantamab kết hợp với hóa trị liệu (carboplatin và pemetrexed).
+ Thuốc ức chế EGFR nhắm vào các tế bào có đột biến S768I, L861Q và/hoặc G719X:
- Các loại thuốc như afatinib (Gilotrif), osimertinib (Tagrisso), erlotinib (Tarceva), dacomitinib (Vizimpro) và gefitinib (Iressa) có thể được dùng riêng.
- Amivantamab kết hợp với hóa trị liệu (carboplatin và pemetrexed).
+ Thuốc ức chế EGFR nhắm vào các tế bào có đột biến exon 20:
- Amivantamab (Rybrevant) kết hợp với hóa trị liệu (carboplatin và pemetrexed).
- Amivantamab và sunvozertinib (Zegfrovy).
 Xem tất cả ảnh
Xem tất cả ảnhLiên hệCòn hàng
| Công ty đăng ký | Boehringer Ingelheim |
| Số đăng ký | VN2-602-17 |
| Dạng bào chế | Viên nén bao phim |
| Quy cách đóng gói | Hộp 4 vỉ x 7 viên |
| Mã sản phẩm | thom418 |
3.2 Thuốc ức chế VEGF
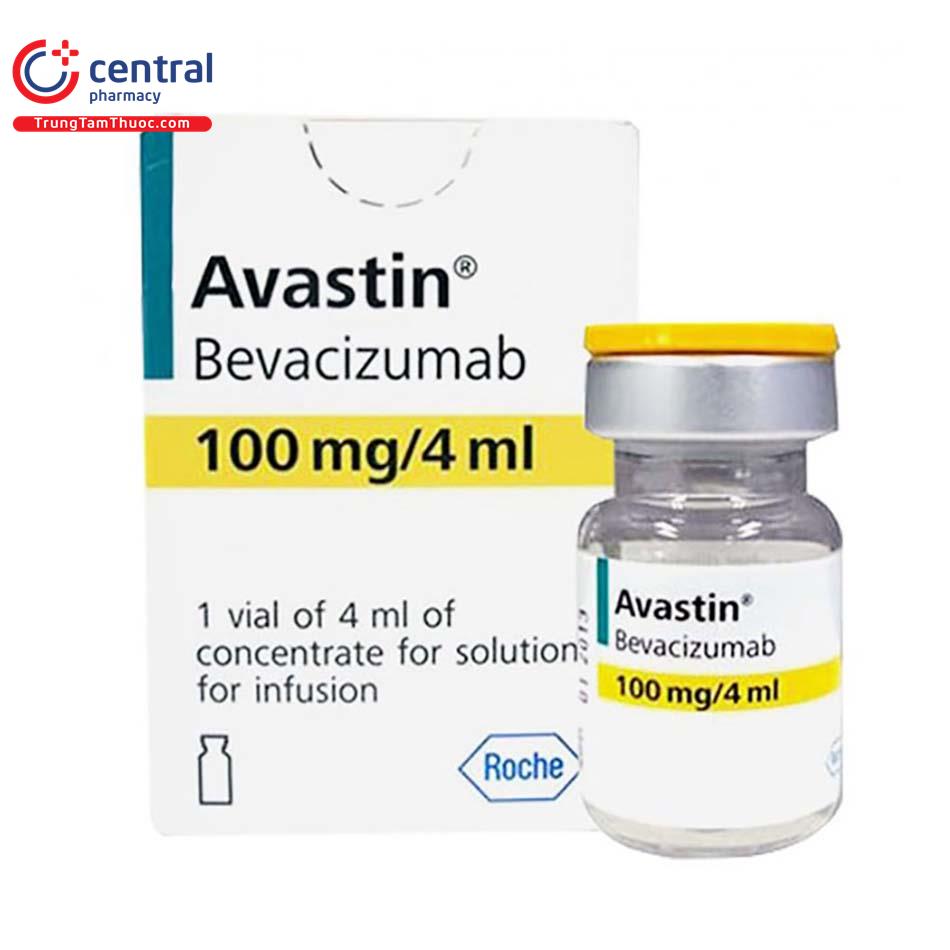
Cơ chế hoạt động: Để khối u phát triển, chúng cần tạo ra các mạch máu mới – quá trình gọi là tạo mạch. Thuốc ức chế hình thành mạch máu mới giúp ngăn chặn sự hình thành các mạch máu mới. Các thuốc ức chế này thường là kháng thể đơn dòng nhắm vào yếu tố tăng trưởng nội mô mạch máu (VEGF), một protein giúp hình thành mạch máu mới, được gọi là thuốc ức chế VEGF .
Ví dụ về thuốc ức chế VEGF: Bevacizumab (Avastin), Ramucirumab (Cyramza).
 Xem tất cả ảnh
Xem tất cả ảnh8.268.000₫Còn hàng
| Công ty đăng ký | F.Hoffmann-La Roche Ltd. |
| Số đăng ký | VN-15050-12 |
| Dạng bào chế | Dung dịch đậm đặc để pha dung dịch tiêm truyền |
| Quy cách đóng gói | Hộp 1 lọ 4ml |
| Mã sản phẩm | m5327 |
3.3 Thuốc ức chế KRAS
Cơ chế hoạt động: Một số bệnh nhân NSCLC có đột biến gen KRAS G12C, tạo ra protein KRAS bất thường thúc đẩy ung thư phát triển. Thuốc ức chế KRAS nhắm vào protein này, giúp ngăn tế bào ung thư tăng sinh. Những trường hợp có đột biến này thường kháng với các thuốc nhắm mục tiêu khác như EGFR.
Ví dụ về thuốc ức chế KRAS: Sotorasib (Lumakras) hoặc Adagrasib (Krazati)
3.4 Thuốc ức chế ALK
Cơ chế hoạt động: Khoảng 5% ung thư phổi không phải tế bào nhỏ (NSCLC) có sự sắp xếp lại gen gọi là ALK . Sự thay đổi này thường thấy ở những người không hút thuốc (hoặc hút thuốc ít), những người trẻ tuổi và mắc NSCLC loại adenocarcinoma. Sự sắp xếp lại gen ALK tạo ra một protein ALK bất thường khiến các tế bào phát triển và lan rộng.
Ví dụ về thuốc ức chế ALK: thường dùng thuốc ức chế ALK thế hệ thứ ba [lorlatinib (Lorbrena)] và thuốc ức chế ALK thế hệ thứ hai [alectinib (Alecensa), brigatinib (Alunbrig), ceritinib (Zykadia) và ensartinib (Ensacove)]. Thuốc ức chế ALK thế hệ đầu tiên: Crizotinib (Xalkori) ít dùng hơn.
3.5 Thuốc ức chế ROS1
Cơ chế hoạt động: Khoảng 1–2% trường hợp ung thư phổi không phải tế bào nhỏ (NSCLC) có sự tái sắp xếp gen ROS1 – một biến đổi di truyền thường gặp nhất ở những bệnh nhân mắc loại ung thư biểu mô tuyến, đặc biệt khi khối u không mang các đột biến ALK, KRAS hoặc EGFR. Sự thay đổi gen ROS1 có nhiều điểm tương đồng với đột biến gen ALK, và một số loại thuốc nhắm trúng đích có thể tác động lên cả hai loại biến đổi này.
Ví dụ về thuốc ức chế ROS1: Entrectinib (Rozlytrek), Crizotinib (Xalkori) và Ceritinib (Zykadia) thường là lựa chọn điều trị đầu tay, ngoài ra còn Lorlatinib (Lorbrena), Repotrectinib (Augtyro) và Taletrectinib (Ibrozi)

 Xem tất cả ảnh
Xem tất cả ảnh250.000₫Còn hàng
| Công ty đăng ký | Pfizer Inc. |
| Số đăng ký | Đang cập nhật |
| Dạng bào chế | Viên nang cứng |
| Quy cách đóng gói | Hộp 1 lọ 60 viên |
| Hạn sử dụng | 36 tháng |
| Mã sản phẩm | tv0712 |
3.6 Thuốc ức chế BRAF
Cơ chế hoạt động: Ở một số NSCLC, các tế bào có những thay đổi trong gen BRAF . Những tế bào có những thay đổi này tạo ra một protein BRAF bị biến đổi, giúp chúng phát triển. Một số loại thuốc nhắm vào protein này và các protein liên quan.
Ví dụ về thuốc ức chế BRAF:
+ Điều trị kết hợp: Sự kết hợp giữa thuốc ức chế BRAF và thuốc ức chế MEK thường được sử dụng cùng nhau như là phương pháp điều trị đầu tiên hoặc sau đó cho bệnh nhân ung thư phổi không phải tế bào nhỏ (NSCLC) tiến triển có đột biến BRAF V600E. Ví dụ bao gồm:
- Dabrafenib (Tafinlar), thuốc ức chế BRAF, với trametinib (Mekinist), thuốc ức chế MEK
- Encorafenib (Braftovi) , thuốc ức chế BRAF, với binimetinib (Mektovi) , thuốc ức chế MEK
+ Điều trị bằng thuốc đơn lẻ: Vemurafenib (Zelboraf), một thuốc ức chế BRAF khác hoặc dabrafenib có thể được dùng riêng nếu bệnh nhân không thể thực hiện phương pháp điều trị kết hợp.
3.7 Thuốc ức chế khác
Thuốc ức chế RET:
- Cơ chế hoạt động: Ở một tỷ lệ nhỏ ung thư phổi không phải tế bào nhỏ (NSCLC), các tế bào khối u có sự sắp xếp lại gen RET , khiến chúng tạo ra một dạng bất thường của protein RET. Protein bất thường này giúp các tế bào khối u phát triển, vì vậy ức chế RET giúp ức chế khối u phát triển.
- Ví dụ: Selpercatinib (Retevmo), Pralsetinib (Gavreto), Cabozantinib (Cometriq, Cabometyx).
Thuốc ức chế MET:
- Cơ chế hoạt động: Ở một số NSCLC, tế bào ung thư có những thay đổi trong gen MET , được gọi là đột biến bỏ qua exon 14 MET, khiến chúng tạo ra một dạng bất thường của protein MET. Protein bất thường này giúp tế bào ung thư phát triển và lan rộng. Ở một số NSCLC khác, tế bào có quá nhiều protein MET, giúp chúng phát triển. Thuốc ức chế MET hoạt động bằng cách tấn công protein MET.
- Ví dụ: Capmatinib (Tabrecta), tepotinib (Tepmetko), Crizotinib (Xalkori), Telisotuzumab vedotin (Emrelis).
Thuốc hướng đến HER2:
- Cơ chế hoạt động: Ở một tỷ lệ nhỏ ung thư phổi không phải tế bào nhỏ (NSCLC), các tế bào ung thư có những thay đổi nhất định trên gen HER2 (ERBB2) giúp chúng phát triển. Thuốc nhắm đích HER2 có thể được sử dụng để điều trị NSCLC di căn nếu các tế bào ung thư có một số loại thay đổi gen HER2 nhất định.
- Ví dụ: Fam-trastuzumab deruxtecan (Enhertu), Ado-trastuzumab emtansine (Kadcyla), Zenocutuzumab (Bizengri).
Thuốc ức chế TRK:
- Cơ chế hoạt động: Một số rất ít ung thư phổi không phải tế bào nhỏ (NSCLC) có những thay đổi ở một trong các gen NTRK , được gọi là hợp nhất gen NTRK. Các tế bào mang những thay đổi gen này tạo ra các protein TRK bất thường, có thể dẫn đến tăng trưởng tế bào bất thường và ung thư. Thuốc ức chế TRK nhắm mục tiêu và vô hiệu hóa các protein do gen NTRK tạo ra .
- Ví dụ: Larotrectinib (Vitrakyi) , Entrectinib (Rozlytrek) hoặc repotrectinib (Augtyro).
Liên hợp kháng thể-thuốc:
- Cơ chế hoạt động: Liên hợp kháng thể-thuốc (ADC) được tạo thành từ một kháng thể được tạo ra trong phòng thí nghiệm, nhắm vào một protein cụ thể trên tế bào ung thư, liên kết với thuốc hóa trị. Kháng thể hoạt động như một thiết bị dẫn đường khi bám vào protein và đưa thuốc hóa trị trực tiếp đến tế bào ung thư.
- Ví dụ về ADC: Fam-trastuzumab deruxtecan (Enhertu), Telisotuzumab vedotin (Emrelis), Datopotamab deruxtecan (Datroway).
4 Liệu pháp miễn dịch điều trị NSCLC
Liệu pháp miễn dịch sử dụng thuốc để kích hoạt hệ miễn dịch tấn công tế bào ung thư, đặc biệt bằng cách ngăn chặn các “điểm kiểm soát miễn dịch” – cơ chế mà tế bào ung thư lợi dụng để né tránh sự tấn công của hệ miễn dịch.
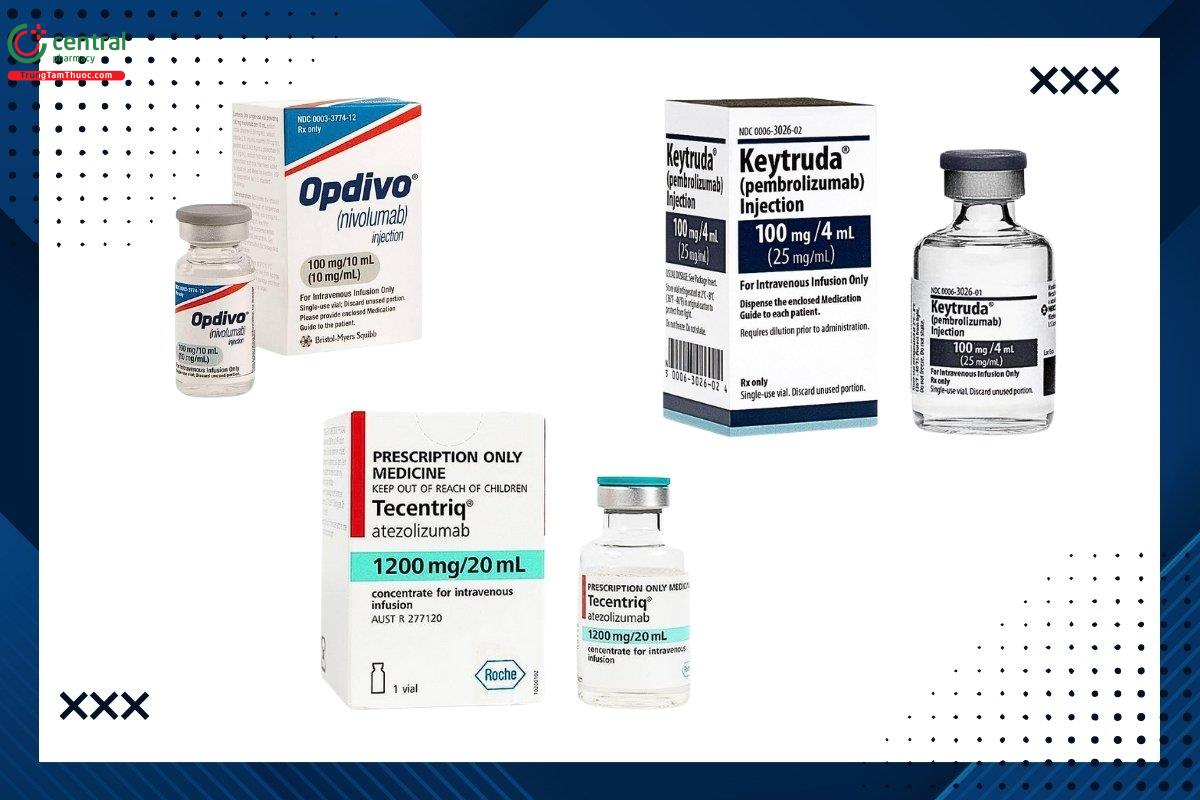
4.1 Thuốc ức chế PD-1/PD-L1
Các loại thuốc như Nivolumab (Opdivo), Pembrolizumab (Keytruda) và Cemiplimab (Libtayo) hoạt động bằng cách ngăn chặn PD-1 – một loại protein có mặt trên tế bào T, vốn giúp điều hòa hoạt động miễn dịch để không tấn công tế bào bình thường. Khi PD-1 bị ức chế, tế bào T được "giải phóng phanh", nhờ đó tăng cường khả năng phát hiện và tiêu diệt tế bào ung thư, làm khối u nhỏ lại hoặc phát triển chậm hơn.
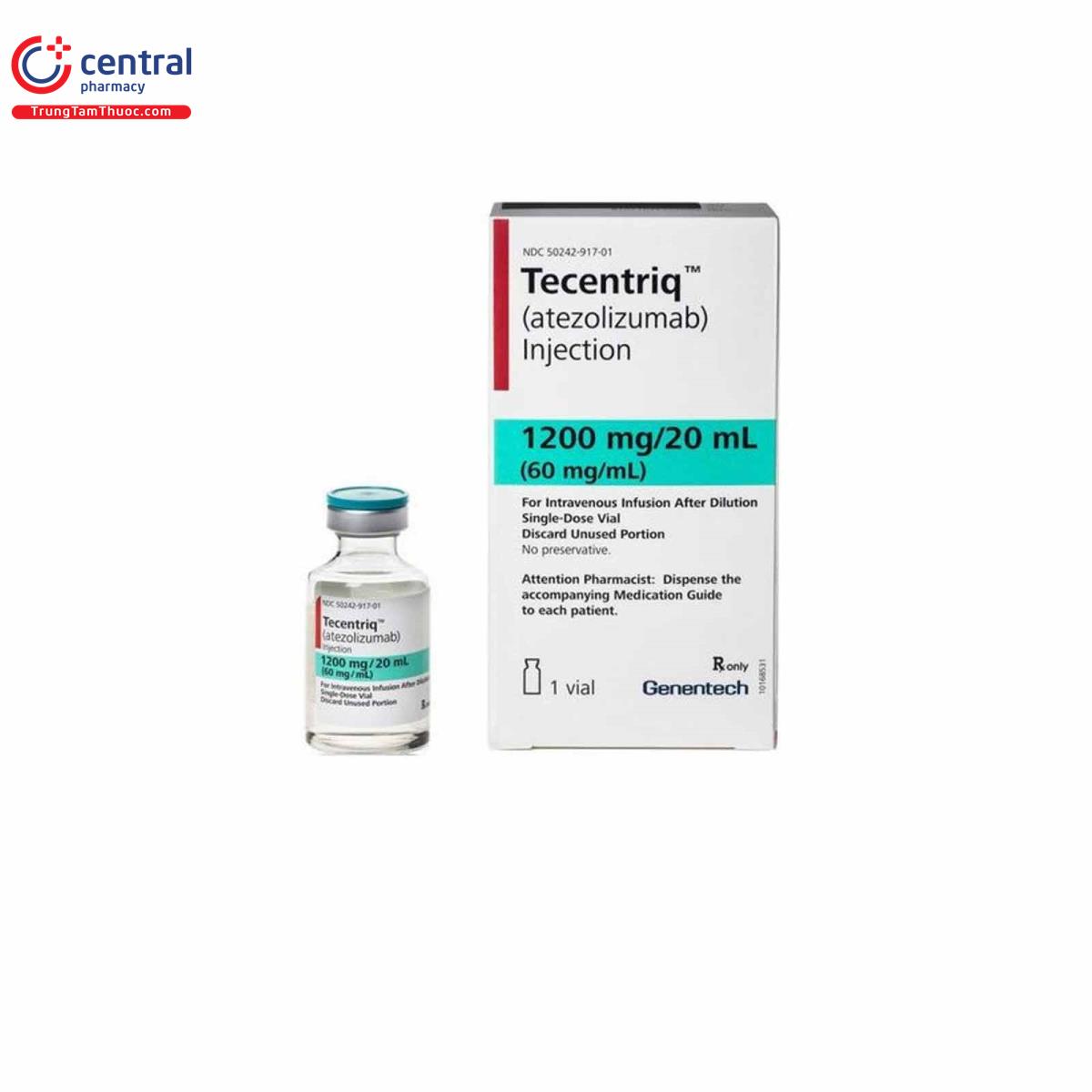
Tương tự, Atezolizumab (Tecentriq) và Durvalumab (Imfinzi) lại nhắm vào PD-L1 – một protein có liên quan đến PD-1, thường hiện diện trên bề mặt tế bào ung thư và một số tế bào miễn dịch. Việc ngăn chặn PD-L1 giúp khôi phục phản ứng miễn dịch của cơ thể chống lại ung thư, từ đó hỗ trợ kiểm soát hoặc thu nhỏ khối u.
 Xem tất cả ảnh
Xem tất cả ảnh41.000.000₫Còn hàng
| Công ty đăng ký | Roche Products Limited |
| Dạng bào chế | Dung dịch đậm đặc để pha dung dịch tiêm truyền |
| Quy cách đóng gói | Hộp 1 lọ x 20ml |
| Mã sản phẩm | at273 |
4.2 Thuốc ức chế CTLA-4
Ipilimumab (Yervoy) và Tremelimumab (Imjudo) là những thuốc tác động vào một đích miễn dịch khác – CTLA-4, một loại protein điều hòa hoạt động của tế bào T. Khi CTLA-4 bị ức chế, hệ miễn dịch được kích hoạt mạnh hơn để chống lại ung thư.
Tuy nhiên, các thuốc CTLA-4 thường không được dùng đơn lẻ. Thay vào đó, chúng được phối hợp với thuốc PD-1/PD-L1 (ví dụ: Ipilimumab kết hợp với Nivolumab, hoặc Tremelimumab kết hợp với Durvalumab) và đôi khi kết hợp thêm hóa trị. Phác đồ này thường áp dụng cho bệnh nhân ung thư phổi không phải tế bào nhỏ (NSCLC) ở giai đoạn tiến triển.
5 Phác đồ điều trị ung thư phổi không tế bào nhỏ của Bộ Y Tế
5.1 Nguyên tắc
Nguyên tắc điều trị ung thư phổi là phải cá thể hóa, tức là tùy theo từng bệnh nhân mà lựa chọn phương pháp điều trị phù hợp. Các bác sĩ sẽ xem xét nhiều yếu tố quan trọng như loại ung thư (mô bệnh học và sinh học phân tử), giai đoạn bệnh (sớm hay muộn), tình trạng sức khỏe của bệnh nhân (tuổi, thể trạng, bệnh lý kèm theo), cũng như nguyện vọng của bệnh nhân và điều kiện kinh tế xã hội. Ngoài ra, các cơ sở y tế cũng cần có đủ trang thiết bị và nguồn lực để thực hiện các phương pháp điều trị hiệu quả.
5.2 Mục tiêu điều trị
Điều trị triệt căn nhằm mục tiêu chữa khỏi: giai đoạn sớm khu trú tại chỗ tại vùng (giai đoạn I, II, IIIA).
Điều trị mang tính giảm nhẹ, tăng chất lượng cuộc sống và kéo dài thời gian sống còn áp dụng cho giai đoạn tiến triển tại chỗ-tại vùng hoặc tái phát di căn (giai đoạn IIIB, IIIC, IV).
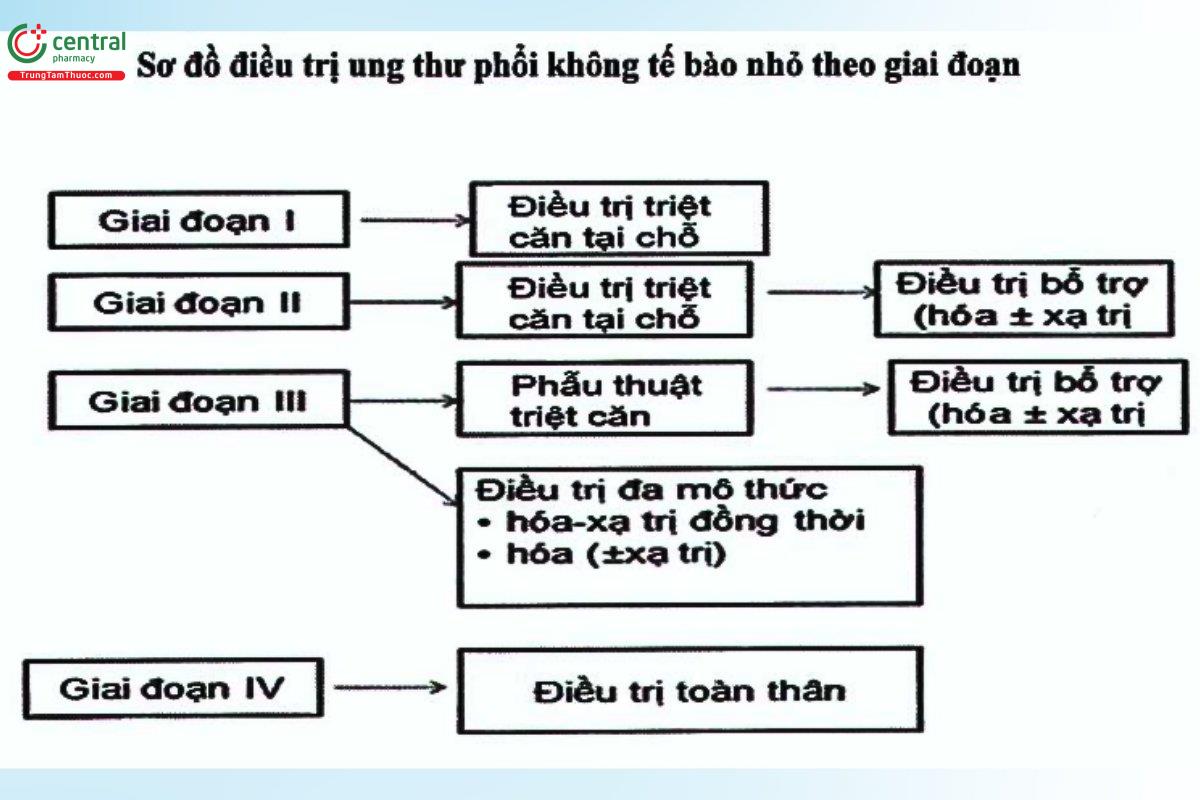
5.3 Phác đồ điều trị theo giai đoạn
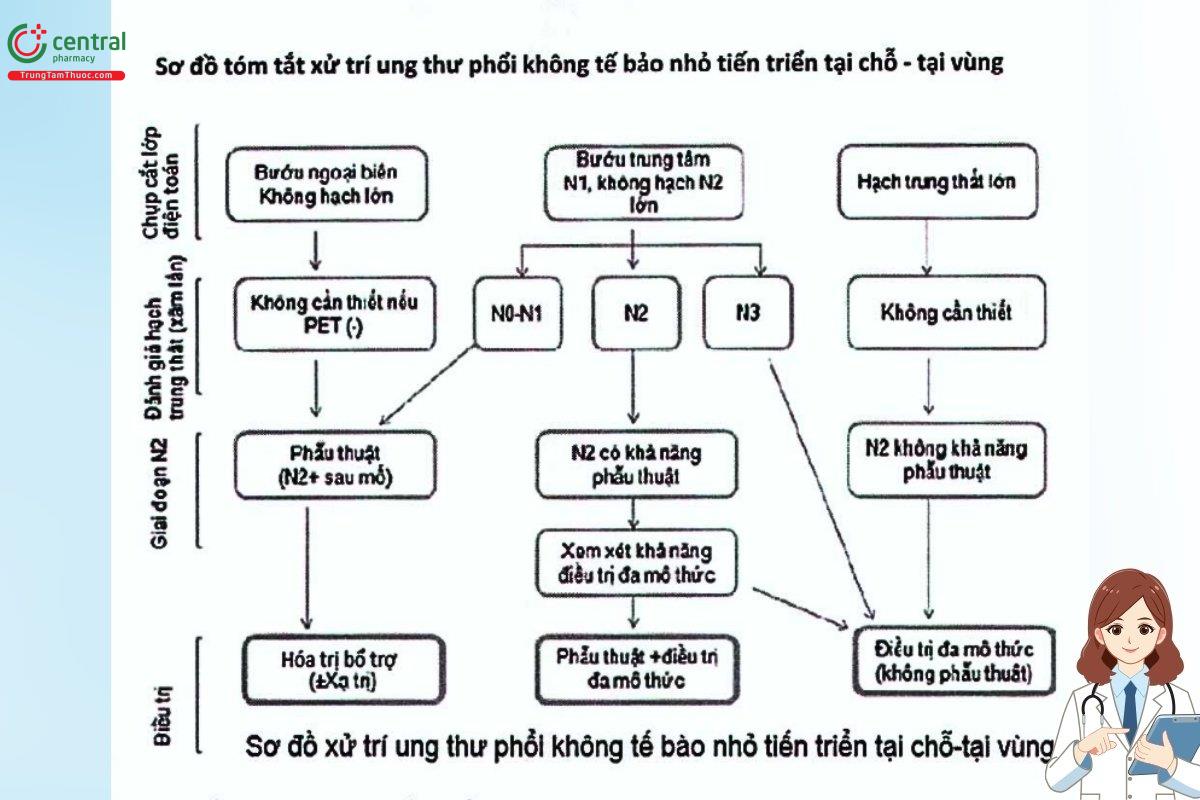
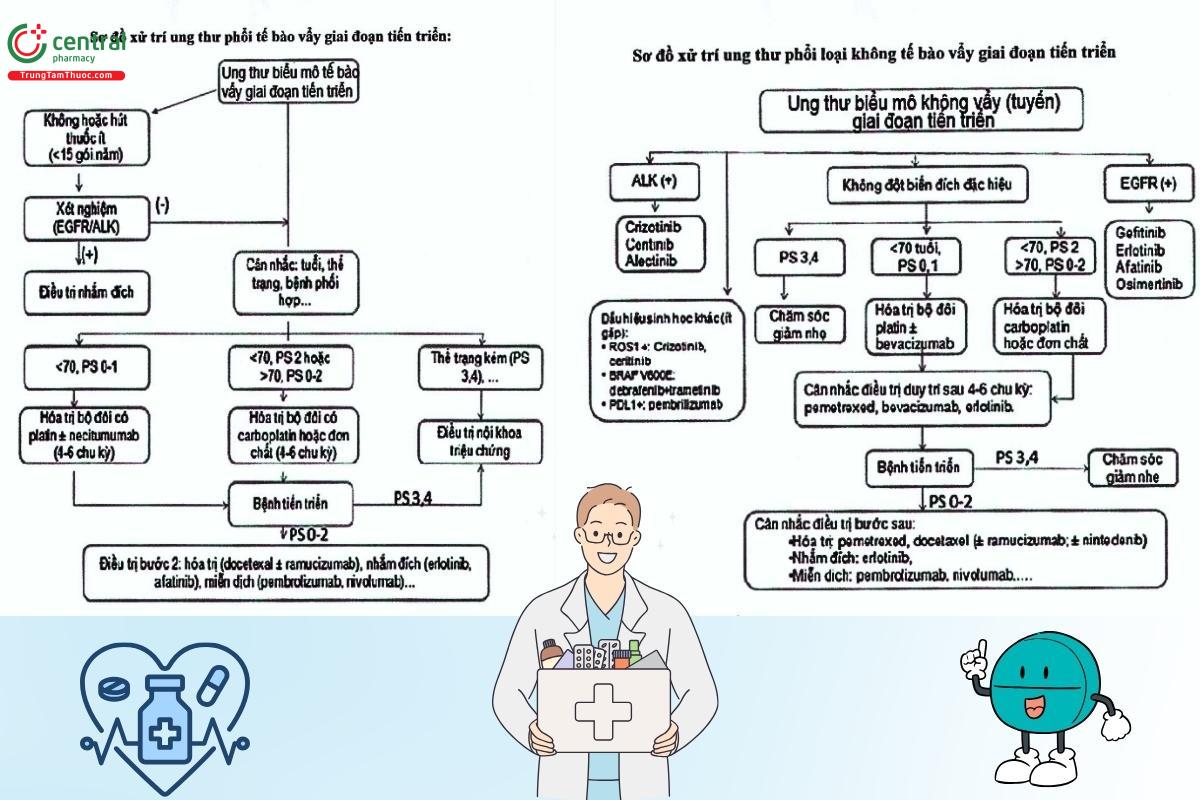
6 Một số câu hỏi thường gặp
6.1 Ung thư phổi uống thuốc đích sống được bao lâu?
Giai đoạn bệnh là yếu tố tiên lượng quan trọng nhất trong điều trị ung thư phổi. Ở giai đoạn I và II, khi khối u còn khu trú và có thể phẫu thuật được, tỷ lệ sống 5 năm của bệnh nhân dao động từ 50% đến 80%. Tuy nhiên, ở giai đoạn III, tỷ lệ này giảm xuống chỉ còn từ 20% đến 40% do ung thư đã bắt đầu lan rộng và khó điều trị hơn. Đặc biệt, ở giai đoạn IV, tỷ lệ sống 5 năm của bệnh nhân rất thấp, thường dưới 5%.
Thời gian sống của bệnh nhân ung thư phổi khi sử dụng thuốc nhắm đích phụ thuộc vào nhiều yếu tố như loại đột biến gen (EGFR, ALK, ROS1...), giai đoạn bệnh, tình trạng sức khỏe tổng thể và mức độ đáp ứng với thuốc. Ở giai đoạn sớm, nếu có đột biến gen và được điều trị bằng thuốc đích sau phẫu thuật, bệnh nhân có thể sống thêm nhiều năm, thậm chí trên 5 năm nếu kiểm soát bệnh tốt.
Một nghiên cứu lớn trên 1.663 bệnh nhân ung thư phổi không tế bào nhỏ (NSCLC) giai đoạn tiến triển được chẩn đoán từ năm 2013 đến 2019 tại Bệnh viện Liên Vân Cảng, Đại học Giang Tô. Kết quả cho thấy, bệnh nhân được điều trị bằng thuốc đích có thời gian sống trung bình lên đến 28,3 tháng, trong khi nhóm không sử dụng thuốc đích chỉ sống trung bình khoảng 15,4 tháng. Những con số này cho thấy thuốc đích giúp kéo dài thời gian sống trung bình của bệnh nhân ung thư phổi giai đoạn tiến triển gần gấp đôi so với các phương pháp điều trị không nhắm mục tiêu.
===> Xem thêm bài viết: 10 bệnh ung thư thường gặp và dấu hiệu nhận biết sớm nhất
6.2 Giá thuốc điều trị trúng đích ung thư phổi
Giá thuốc điều trị trúng đích ung thư phổi đã có sự thay đổi đáng kể trong những năm gần đây, mang lại nhiều cơ hội cho bệnh nhân trong việc tiếp cận phương pháp điều trị hiện đại này. Trước đây, chi phí cho thuốc trúng đích có thể lên đến 20-30 triệu đồng mỗi tháng, một mức giá rất cao, khiến nhiều bệnh nhân khó khăn trong việc chi trả. Tuy nhiên, hiện nay, nhờ sự phát triển của ngành dược và các chính sách bảo hiểm y tế, một số thuốc đã giảm xuống còn khoảng 2-3 triệu đồng/tháng, giúp giảm bớt gánh nặng tài chính cho bệnh nhân.
6.3 Điều trị ung thư phổi ở đâu là tốt nhất?
Một số bệnh viện uy tín bạn có thể tham khảo như:
- Bệnh viện K Trung ương: Trung tâm ung bướu hàng đầu miền Bắc với đội ngũ chuyên gia giàu kinh nghiệm.
- Bệnh viện Bạch Mai (Hà Nội): Trung tâm y tế đa khoa lớn, có khoa ung bướu chuyên sâu.
- Bệnh viện Phổi Trung ương (Hà Nội): Chuyên điều trị các bệnh về phổi, trong đó có ung thư phổi.
- Bệnh viện Ung Bướu TP.HCM: Địa chỉ điều trị ung thư hàng đầu miền Nam, áp dụng nhiều phương pháp tiên tiến.
- Bệnh viện Chợ Rẫy: Bệnh viện đa khoa lớn, có chuyên khoa ung bướu phát triển mạnh.
6.4 Thuốc điều trị ung thư phổi giai đoạn cuối
Ung thư phổi giai đoạn cuối thường di căn đến não, gây ra nhiều biến chứng nghiêm trọng và đe dọa tính mạng nếu không được điều trị kịp thời. Trước đây, các phương pháp như phẫu thuật hoặc xạ trị được ưu tiên để kiểm soát khối u não, nhưng hiện nay đã có những loại thuốc nhắm trúng đích có khả năng thẩm thấu vào não, giúp kiểm soát hiệu quả các tổn thương di căn mà không cần can thiệp phẫu thuật hoặc xạ trị. Các thuốc nhắm mục tiêu đặc hiệu dựa trên đột biến gen như EGFR (ví dụ Osimertinib) hoặc ALK (ví dụ Alectinib, Brigatinib, Lorlatinib) không chỉ làm giảm kích thước khối u phổi mà còn kiểm soát tốt khối u ở não, giúp kéo dài đáng kể thời gian sống cho bệnh nhân. Trước đây, bệnh nhân ung thư phổi giai đoạn tiến triển chỉ sống được khoảng 1 năm với hóa trị truyền thống, nhưng với sự phát triển của các thuốc nhắm trúng đích và liệu pháp miễn dịch, thời gian sống trung bình đã được kéo dài lên 3 năm hoặc hơn, đồng thời chất lượng cuộc sống cũng được cải thiện đáng kể. Tuy nhiên, các phương pháp điều trị này chưa thể chữa khỏi hoàn toàn và bệnh thường tiến triển theo thời gian do sự kháng thuốc.
6.5 Thuốc điều trị ung thư phổi của Mỹ
Vào ngày 16 tháng 5 năm 2024, Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) đã cấp phép nhanh cho tarlatamab-dlle (Imdelltra, Amgen, Inc.) để điều trị bệnh nhân ung thư phổi tế bào nhỏ giai đoạn lan rộng (ES-SCLC) có bệnh tiến triển sau hoặc trong quá trình điều trị hóa trị liệu dựa trên bạch kim.
Quyết định này dựa trên kết quả từ nghiên cứu DeLLphi-301, một thử nghiệm lâm sàng đa trung tâm, mở, đánh giá hiệu quả và độ an toàn của tarlatamab-dlle trên 99 bệnh nhân mắc ES-SCLC tái phát hoặc kháng trị. Trong nghiên cứu, bệnh nhân được loại trừ nếu có di căn não có triệu chứng, bệnh phổi kẽ, viêm phổi không nhiễm trùng hoặc suy giảm miễn dịch hoạt động.
Liều khuyến cáo của tarlatamab-dlle là 1 mg truyền tĩnh mạch trong hơn 1 giờ vào ngày 1 chu kỳ đầu, sau đó tăng lên 10 mg vào các ngày 8 và 15 của chu kỳ đó, rồi tiếp tục truyền 10 mg mỗi 2 tuần cho đến khi bệnh tiến triển hoặc xuất hiện độc tính không chấp nhận được. Thuốc hứa hẹn là một lựa chọn điều trị mới cho bệnh nhân ES-SCLC với khả năng kiểm soát bệnh trong giai đoạn tiến triển.
6.6 Thuốc điều trị ung thư phổi mới nhất
Vào ngày 23 tháng 6 năm 2025, FDA đã cấp phép nhanh cho datopotamab deruxtecan-dlnk (Datroway, Daiichi Sankyo, Inc.) để điều trị người lớn mắc ung thư phổi không phải tế bào nhỏ (NSCLC) có đột biến EGFR di căn hoặc tiến triển tại chỗ, đã từng dùng liệu pháp nhắm mục tiêu EGFR và hóa trị dựa trên bạch kim trước đó.
Hiệu quả của Datroway được đánh giá trên 114 bệnh nhân trong hai thử nghiệm lâm sàng TROPION-Lung05 và TROPION-Lung01. Kết quả cho thấy tỷ lệ đáp ứng tổng thể (ORR) đạt 45%, với thời gian đáp ứng trung vị (DOR) là 6,5 tháng, cho thấy thuốc có khả năng kiểm soát bệnh hiệu quả ở những bệnh nhân đã điều trị trước đó.
Liều dùng khuyến cáo của datopotamab deruxtecan-dlnk là 6 mg/kg (tối đa 540 mg cho bệnh nhân trên 90 kg), truyền tĩnh mạch mỗi 3 tuần cho đến khi bệnh tiến triển hoặc xuất hiện tác dụng phụ không thể chấp nhận được.
7 Kết luận
Dựa trên những thông tin về phân loại thuốc và phác đồ điều trị ung thư phổi không tế bào nhỏ (NSCLC), có thể thấy rằng việc điều trị hiện nay rất đa dạng, bao gồm phẫu thuật, xạ trị, hóa trị, liệu pháp nhắm trúng đích và liệu pháp miễn dịch. Hi vọng bài viết có thể giúp người đọc hiểu rõ hơn về phân loại và lựa chọn điều trị ung thư phổi không tế bào nhỏ, góp phần nâng cao nhận thức và hỗ trợ quyết định điều trị hiệu quả.
8 Tài liệu tham khảo
1. Bộ Y tế (Ngày đăng: Ngày 06 tháng 08 năm 2018). Hướng dẫn chẩn đoán và điều trị ung thư phổi không tế bào nhỏ. Bộ Y tế. Truy cập ngày 31 tháng 7 năm 2025.
2. Tác giả Zarogoulidis K và cộng sự (Ngày đăng: Tháng 09 năm 2013). Treatment of non-small cell lung cancer (NSCLC). Pubmed. Truy cập ngày 31 tháng 7 năm 2025.
3.Tác giả Shaloam Dasari và cộng sự (Ngày đăng: Ngày 05 tháng 10 năm 2014). Cisplatin in cancer therapy: molecular mechanisms of action. Pubmed. Truy cập ngày 31 tháng 7 năm 2025.
4. Tác giả S B Horwitz (Ngày đăng: Năm 1994). Taxol (paclitaxel): mechanisms of action. Pubmed. Truy cập ngày 31 tháng 7 năm 2025.
5. Tác giả Yardley DA (Ngày đăng: Tháng 09 năm 2013). nab-Paclitaxel mechanisms of action and delivery. Pubmed. Truy cập ngày 31 tháng 7 năm 2025.
6. Tác giả Nicole G. Farha và cộng sự (Ngày cập nhật: Ngày 08 tháng 06 năm 2024). Docetaxel. Pubmed. Truy cập ngày 31 tháng 7 năm 2025.
7. Tác giả Gizem Reyhanoglu và cộng sự (Ngày đăng: Ngày 04 tháng 07 năm 2023). Etoposide. Pubmed. Truy cập ngày 31 tháng 7 năm 2025.
8. Tác giả Capasso A và cộng sự (Ngày đăng: Tháng 7 năm 2012). Vinorelbine in cancer therapy. Pubmed. Truy cập ngày 31 tháng 7 năm 2025.
9. Tác giả Adjei AA và cộng sự (Ngày đăng: Tháng 04 năm 2004). Pharmacology and mechanism of action of pemetrexed. Pubmed. Truy cập ngày 31 tháng 7 năm 2025.
10. Chuyên gia American Cancer Society, Chemotherapy for Non-Small Cell Lung Cancer. American Cancer Society. Truy cập ngày 31 tháng 7 năm 2025.
11. Chuyên gia American Cancer Society. Targeted Drug Therapy for Non-Small Cell Lung Cancer. American Cancer Society. Truy cập ngày 31 tháng 7 năm 2025.
12. Chuyên gia American Cancer Society. Immunotherapy for Non-Small Cell Lung Cancer. American Cancer Society. Truy cập ngày 31 tháng 7 năm 2025.
13. Chuyên gia FDA. FDA grants accelerated approval to tarlatamab-dlle for extensive stage small cell lung cancer. FDA. Truy cập ngày 31 tháng 7 năm 2025.
14. Chuyên gia FDA. FDA grants accelerated approval to datopotamab deruxtecan-dlnk for EGFR-mutated non-small cell lung cancer. FDA. Truy cập ngày 31 tháng 7 năm 2025.

