Tác động huyết động của áp lực dương cuối thì thở ra sử dụng khi suy hô hấp

Curr Opin Crit Care 2023, 30:000–000
Tác động huyết động của áp lực dương cuối thì thở ra
Bản dịch của BS. Đặng Thanh Tuấn – BV Nhi Đồng 1
Xem đầy đủ bản PDF tại đây
1 Tóm tắt
1.1 Mục đích xem xét
Áp lực dương cuối thì thở ra (Positive end expiratory pressure, PEEP) là cần thiết trong định nghĩa Berlin về hội chứng nguy kịch hô hấp cấp tính và là nền tảng trong điều trị. Áp dụng PEEP làm tăng áp lực đường thở và điều chỉnh áp lực màng phổi và xuyên phổi theo cơ học hô hấp, dẫn đến thay đổi thể tích máu vào tuần hoàn phổi. Điều này lần lượt có thể ảnh hưởng đến tiền tải, hậu tải và chức năng của thất phải. Ngược lại, PEEP có thể cải thiện chức năng tâm thất trái mà không gây ra tác dụng có hại nào trên tâm thất phải.
1.2 Những phát hiện gần đây
Tổng quan này xem xét tác động của PEEP đối với chức năng tim liên quan đến tương tác tim-phổi và mô tả hậu quả của nó đối với tưới máu và chức năng của các cơ quan, bao gồm thận, ruột, gan và não. Bản thân PEEP không có lợi cũng như không có hại đối với huyết động học của cơ quan đích, nhưng tác dụng huyết động của nó thay đổi tùy theo cơ học hô hấp và mối liên quan với các biến số huyết động khác như áp lực tĩnh mạch trung tâm hoặc động mạch trung bình. Có những điểm tương đồng trong các biện pháp ngăn ngừa tác động có hại của PEEP lên phổi, tim, thận, gan và hệ thần kinh trung ương.
1.3 Tóm tắt
Nhiệm vụ cài đặt PEEP tối ưu là mục tiêu nổi bật trong nghiên cứu ARDS trong những thập kỷ qua. Bác sĩ chăm sóc đặc biệt phải duy trì mức độ cảnh giác cao đối với tác động huyết động của PEEP đối với chức năng tim và tuần hoàn của các cơ quan đích.
Những điểm chính
• Áp dụng PEEP làm thay đổi áp lực màng phổi và xuyên phổi, do đó ảnh hưởng đến tuần hoàn phổi và chức năng tim.
• PEEP quá mức có thể làm thay đổi tưới máu và chức năng của các cơ quan, bao gồm thận, ruột, gan và não.
• Sự cân bằng giữa việc huy động phế nang và tình trạng bơm phồng quá mức do PEEP gây ra chủ yếu làm trung gian cho tác động có hại của PEEP đối với chức năng và tưới máu của các cơ quan. Nó có thể dự đoán được một cách khó khăn và sau đó phải được đánh giá lại thường xuyên.
2 Giới thiệu
Hội chứng nguy kịch hô hấp cấp tính (ARDS) đã được mô tả lần đầu tiên vào năm 1967 trong một loạt trường hợp gồm 12 bệnh nhân bị thiếu oxy khởi phát mới kháng trị với oxy bổ sung, thâm nhiễm hai bên trên X quang ngực và giảm độ giãn nở của hệ hô hấp [1]. Kể từ đó, một số định nghĩa đã được đề xuất: năm 1994 với hội nghị đồng thuận Mỹ-Châu u về ARDS [2] và năm 2012 dẫn đến định nghĩa Berlin [3]. Điều này bao gồm suy hô hấp trong vòng 1 tuần kể từ khi bị tổn thương hoặc các triệu chứng hô hấp mới và/hoặc trầm trọng hơn, không được giải thích đầy đủ do rối loạn chức năng tim hoặc quá tải thể tích, hình mờ hai bên trên X quang ngực hoặc chụp cắt lớp vi tính và tình trạng thiếu oxy máu được xác định là PaO2/FiO2 ít hơn hơn 300 mmHg với ít nhất PEEP là 5cm H2O. Định nghĩa này đã được cập nhật sau đại dịch COVID 19 để bao gồm những bệnh nhân được điều trị bằng oxy qua mũi lưu lượng cao và SpO2/FiO2 dưới 315 [4].
Trong 50 năm qua, đã có những tiến bộ to lớn trong việc tìm hiểu dịch tễ học và sinh lý bệnh của ARDS [5]. Không còn nghi ngờ gì nữa, không có hội chứng chăm sóc tích cực nào khác được nghiên cứu rộng rãi như vậy, đặc biệt là liên quan đến chiến lược thông khí.
Áp lực dương cuối thì thở ra (PEEP) là bắt buộc trong định nghĩa ARDS của Berlin [3], trong khi sự hiện diện của nó để xác định ARDS gần đây đã được tranh luận rộng rãi [6]. Nhiệm vụ cài đặt PEEP tối ưu là mục tiêu nổi bật trong nghiên cứu ARDS trong những thập kỷ qua [7]. Thật vậy, việc áp dụng PEEP dẫn đến những tác động có lợi nhưng cũng có hại, chủ yếu là về huyết động và khó giải quyết sự cân bằng giữa lợi ích/nguy cơ liên quan đến mức độ của nó, áp lực đẩy được tạo ra và mức độ nghiêm trọng của tổn thương phổi. Trong hướng dẫn ESICM gần đây, các chuyên gia không thể đưa ra khuyến nghị ủng hộ hay phản đối việc áp dụng thường quy PEEP ‘cao’ so với PEEP ‘thấp’ [6].
Mặc dù tác dụng có lợi của PEEP đã được mô tả kể từ mô tả ban đầu về ARDS [8], nhưng tác dụng phụ thực sự rất nhiều, trong số đó có suy tuần hoàn là nguyên nhân chính liên quan đến tiên lượng xấu [9]. Trong một thử nghiệm ngẫu nhiên có đối chứng, các nhà điều tra ART đã báo cáo rằng chiến lược PEEP (rất) cao, cùng với các thủ thuật huy động, đã làm tăng tỷ lệ tử vong so với chiến lược PEEP thấp hơn [10]. Điều thú vị là, 1 giờ sau khi chọn ngẫu nhiên, 34,8% bệnh nhân trong nhóm PEEP cao cần bắt đầu hoặc tăng thuốc vận mạch hoặc hạ huyết áp so với 28% ở nhóm PEEP thấp [10], và sự gia tăng này dường như không liên quan tạm thời với các thủ thuật huy động. Tác dụng tiềm tàng này của PEEP đối với huyết động học đặc biệt quan trọng vì nhiều bệnh nhân được điều trị ARDS đã bị suy giảm tuần hoàn. Trong một đánh giá hệ thống và phân tích tổng hợp về tác động của PEEP đến kết quả, hơn 65% bệnh nhân mắc ARDS cần dùng thuốc vận mạch trong thời gian nằm ICU [11].
PEEP thường được đề xuất để duy trì hoặc phục hồi quá trình oxygen hóa và ngăn ngừa xẹp phế nang theo chu kỳ và tổn thương phổi do máy thở. Nếu vậy, nó có thể bảo vệ tim và huyết động. Katira và cộng sự [12] đã nhấn mạnh lại một cách thú vị rằng thể tích khí lưu thông vừa phải với PEEP bằng 0 (áp lực đẩy cao) gây ra tổn thương phổi cấp tính ở động vật so với cùng thể tích khí lưu thông nhưng áp dụng PEEP (áp lực đẩy thấp). Điều đáng chú ý trong nghiên cứu của họ là suy tim phải được quan sát dần dần ở nhóm trước trong khi không thấy ở nhóm sau [12].
Đánh giá này trước tiên sẽ xem xét tác động của PEEP đối với chức năng tim liên quan đến tương tác tim-phổi và thứ hai sẽ mô tả hậu quả của nó đối với tưới máu và chức năng của các cơ quan, bao gồm thận, ruột, gan và não.
3 Tác động của áp lực dương cuối thì thở ra lên chức năng tim
3.1 Những cân nhắc về giải phẫu và sinh lý
Hệ thống mạch máu tim phổi trong lồng ngực chứa khoảng 17% thể tích mạch máu, 9% nằm trong tuần hoàn phổi chịu trách nhiệm tạo ra tiền tải thất trái và thể tích nhát bóp (stroke volume, SV) [13]. Khi đó, mọi hiện tượng ảnh hưởng đến lượng máu vào tuần hoàn phổi đều trực tiếp làm thay đổi SV và huyết động.
Các khoang tim (trong trường hợp không có tràn dịch màng ngoài tim) và một số mạch máu lớn như tĩnh mạch chủ trên hoặc động mạch phổi chịu áp lực màng phổi (pleural pressure, Ppl) trực tiếp trong khi mao mạch phổi chịu áp lực xuyên phổi (transpulmonary pressure, TPP), đó là áp lực làm căng phổi. Màng ngoài tim là một lớp bao bọc không thể mở rộng xung quanh tim, có nghĩa là mọi thay đổi về thể tích của một tâm thất sẽ ảnh hưởng đến thể tích của tâm thất kia thông qua vách liên thất, một hiện tượng gọi là sự phụ thuộc lẫn nhau của hai tâm thất [14].
Thông khí theo chu kỳ và áp dụng PEEP làm tăng áp lực đường thở (Paw) và sau đó thay đổi Ppl và TPP, theo cơ học hô hấp, dẫn đến thay đổi thể tích máu vào tuần hoàn phổi [15]. Điều này chủ yếu được thực hiện qua trung gian bởi những thay đổi về tiền tải, hậu tải và chức năng thất phải. Ngược lại, thông qua hoạt động của nó trên tâm thất trái, PEEP có thể cải thiện chức năng tâm thất trái và SV ở một số loại bệnh nhân, miễn là không có tác dụng có hại nào xảy ra ở bên phải.
3.2 Ảnh hưởng của áp lực dương cuối thì thở ra lên tâm thất phải
Theo sinh lý học Guyton, hồi lưu tĩnh mạch hệ thống (systemic venous return, Qvr) có thể được viết như sau: Qrv = (Pms-Pra)/Rvr trong đó Pms là áp lực đổ đầy hệ thống trung bình, Pra là áp lực nhĩ phải và Rvr sức cản hồi lưu tĩnh mạch. Trong hầu hết các trường hợp, áp dụng PEEP làm giảm hồi lưu tĩnh mạch hệ thống nhưng không phải lúc nào cũng làm giảm tiền tải thất phải, đặc biệt ở những bệnh nhân thở máy vì ARDS. Tóm lại, nó phụ thuộc vào cơ học hô hấp và thể tích. Tăng PEEP làm giảm tiền tải thất phải có nghĩa là tâm thất phải tác động lên phần dốc của đường cong Frank-Starling (phần phụ thuộc tiền tải). Trong tình huống này, Ppl thường bị ảnh hưởng nhiều hơn TPP bởi PEEP và thường xuyên xuất hiện tình trạng giảm thể tích [16]. Qvr giảm do Pra tăng đơn giản do sự truyền đén của Ppl hoặc do Rvr tăng do hiện tượng 'thích nghi' thông qua các thụ thể áp lực trên ngực [17] hoặc do xẹp tĩnh mạch chủ trên [18]. Lai và cộng sự [19&] gần đây đã báo cáo ở 66 bệnh nhân được thở máy với PEEP cao (66% trong số họ mắc ARDS) rằng việc giảm PEEP (12 đến 7 cmH2O) chỉ gây ra sự gia tăng cung lượng tim khi bệnh nhân đáp ứng với dịch (khi đó tâm thất phải hoạt động trên phần dốc của đường cong Frank-Starling).
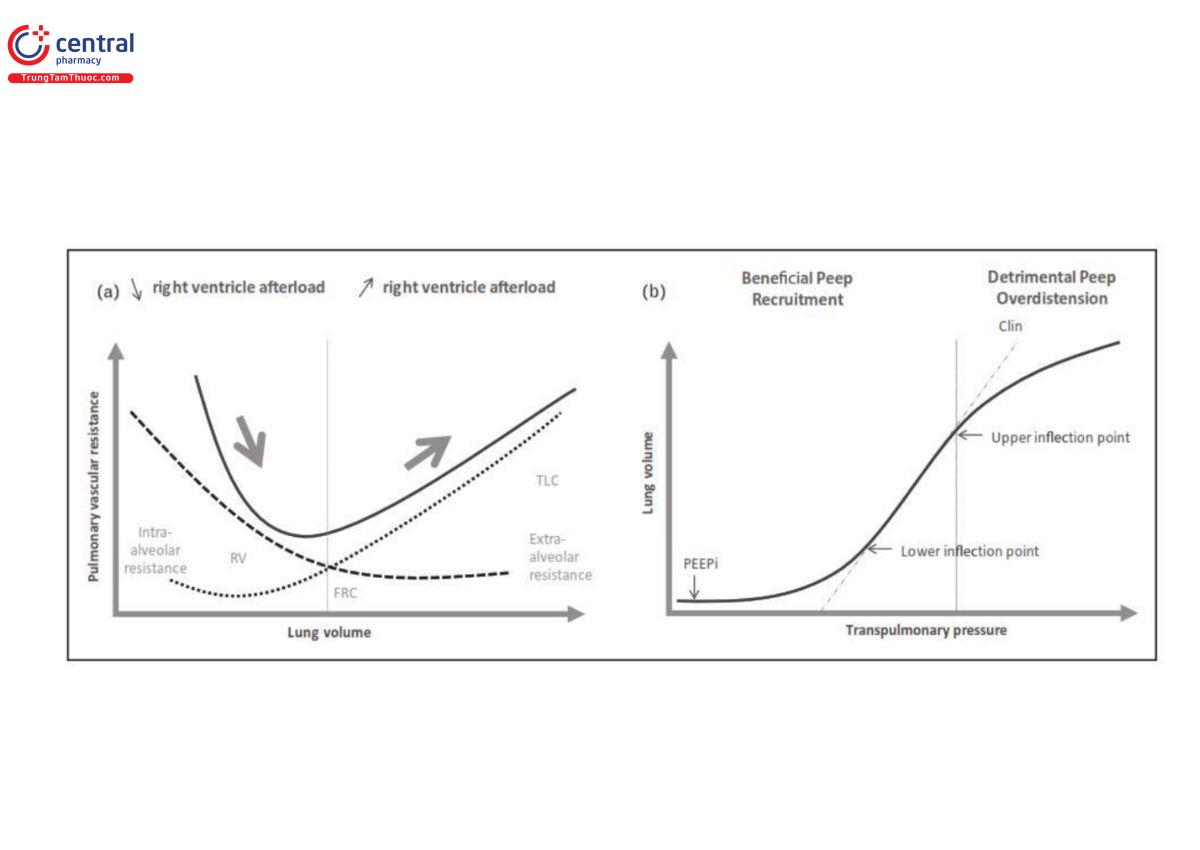
Tuy nhiên, việc tăng PEEP cũng có thể làm giảm Qvr do tăng tiền tải thất phải. Trong trường hợp này, Pra tăng do PEEP gây ra sự gia tăng hậu tải thất phải dẫn đến tắc nghẽn tống máu thất phải [20] dẫn đến giãn tim phải. Khi độ giãn nở của phổi bị suy giảm nghiêm trọng [21] và tình trạng siêu căng phồng phổi xảy ra [22], áp lực đường thở ít được truyền đến áp lực màng phổi và TPP bị ảnh hưởng nhiều hơn khi tăng PEEP, một tình huống thường được quan sát thấy hơn ở những bệnh nhân thở máy vì ARDS. Những bệnh nhân như vậy đặc biệt nhạy cảm với tác dụng này vì ARDS cũng là một bệnh về tuần hoàn phổi [23] và có liên quan đến tăng áp phổi [24]. Khi PEEP tăng, những thay đổi có lợi dự kiến là việc huy động các vùng không được thông khí với sự phân bổ khí ở vùng phụ thuộc của phổi (chủ yếu là các phần sau ở tư thế nằm ngửa). Tuy nhiên, khi khí được phân bổ nhiều hơn ở các khu vực không phụ thuộc (chủ yếu là phần trước ở tư thế nằm ngửa), tình trạng siêu bơm phồng xảy ra ở khu vực này với sự chèn ép của mao mạch phổi bởi TPP và cuối cùng là tăng hậu tải thất phải kèm theo rối loạn huyết động. Valta và cộng sự [25] đã báo cáo rằng ở mức PEEP 12 cmH2O, tỷ lệ huy động phổi chỉ chiếm 25% diện tích delta trong dung tích cặn chức năng (FRC) do PEEP gây ra. Chúng tôi tìm thấy kết quả tương tự [26]. Sử dụng ống thông động mạch phổi, Jardin và cộng sự [27] đã báo cáo trong ARDS về tác dụng phụ của PEEP đối với hậu tải và chức năng của thất phải khi cuối thì thở ra trong thử nghiệm PEEP từ 0 đến 15 cmH2O. Họ nhận thấy sự gia tăng dần dần hậu tải thất phải cùng với sự giảm dần SV tâm thất phải [27]. Gần đây hơn, chúng tôi đã báo cáo kết quả tương tự khi sử dụng siêu âm tim trong chăm sóc tích cực [28]. Tóm lại, đây là sự cân bằng giữa huy động và siêu bơm phồng, m và Dương được thảo luận bởi Rouby và Brochard [29], quyết định ảnh hưởng của PEEP lên chức năng tâm thất phải. PEEP có thể dẫn đến việc huy động phế nang và khi m (huy động) chiếm ưu thế, việc tăng PEEP thậm chí có thể làm giảm hậu tải thất phải và cải thiện chức năng và huyết động của thất phải. Trong tình huống này, PEEP cũng thường xuyên làm giảm tình trạng co mạch phổi do thiếu oxy. Hình 1 tóm tắt các tình huống khác nhau trong đó PEEP có thể giảm tải hoặc làm quá tải tâm thất phải. Nó phụ thuộc vào mức PEEP, mức độ nghiêm trọng của “phổi trẻ em” và khả năng phục hồi của nó (FRC giảm và bình thường như thế nào) và áp lực xuyên phổi do PEEP tạo ra.
3.3 Ảnh hưởng của áp lực dương cuối thì thở ra lên tâm thất trái
Một mặt, người ta mong đợi PEEP cải thiện chức năng thất trái và SV bằng cách giảm hậu tải thất trái. Bằng cách tăng ITP, PEEP làm tăng áp lực xung quanh tất cả cấu trúc trong lồng ngực, nhiều hơn áp lực trong khoang bụng, so với áp lực khí quyển, tạo ra một chênh lệch áp lực giữa tâm thất trái (left ventricle, LV) và động mạch chủ và phần còn lại của hệ tuần hoàn. làm việc ở áp lực khí quyển. Do đó, ITP tăng làm giảm áp lực xuyên thành thất trái và lực cần thiết để đẩy máu vào tuần hoàn [30,31]. Ở phía bên kia, chức năng tâm trương thất trái có thể được thay đổi bằng cách tăng PEEP [32]. Điều này xảy ra khi tâm thất phải (right ventricle, RV) bị PEEP quá tải như đã thảo luận ở trên. Trong trường hợp này, sự gia tăng kích thước và áp lực thất phải sẽ làm dịch chuyển vách liên thất về phía tâm thất trái, làm giảm khả năng đổ đầy của nó [33].
4 Hậu quả lên tưới máu và chức năng của cơ quan
Trong những thập kỷ qua, các nghiên cứu chuyên sâu đã nhấn mạnh sự phức tạp của sự tương tác chéo giữa các cơ quan giữa phổi, thận và tim [34,35]. Theo nghĩa này, PEEP tham gia vào sự tương tác chéo này thông qua các tác động về huyết động, viêm và thần kinh nội tiết của nó.
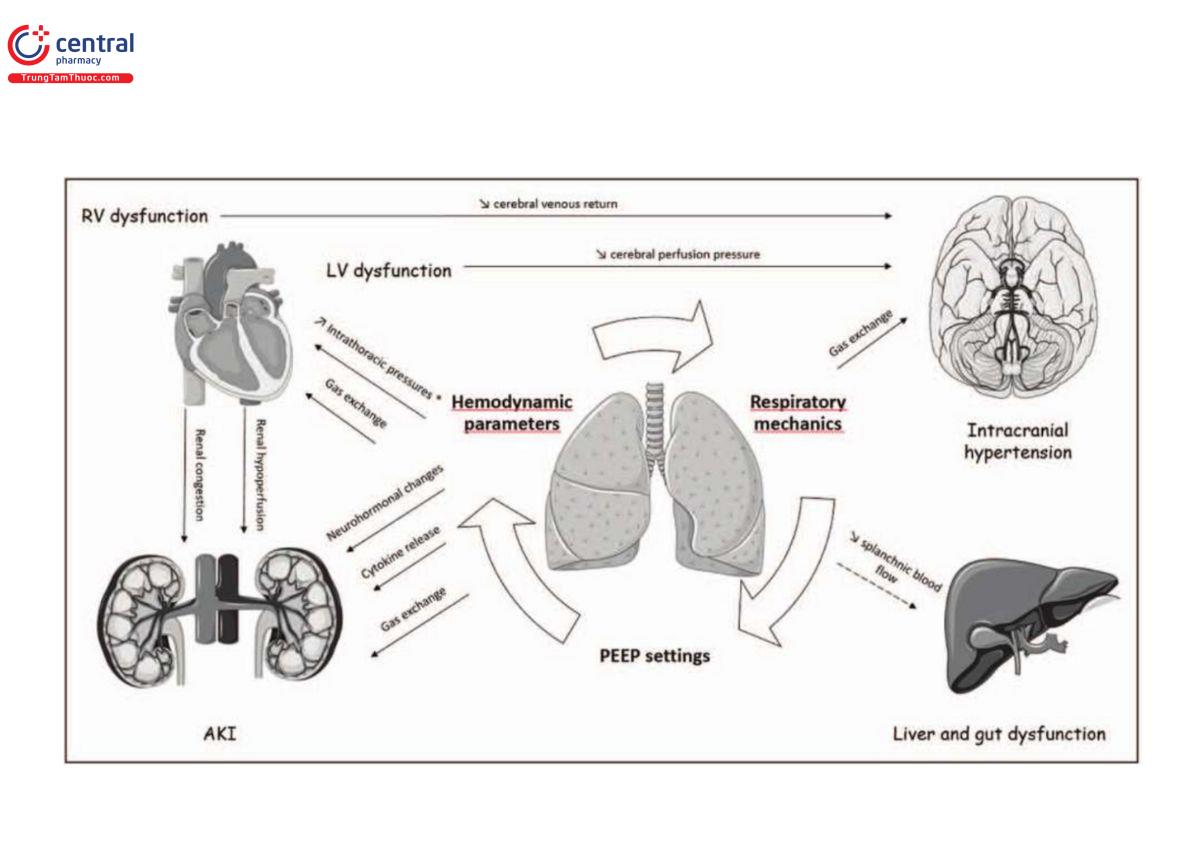
Trong các phần sau, chúng tôi sẽ mô tả tác động của PEEP đối với tuần hoàn thận, ruột, gan và não, nhấn mạnh tác động lâm sàng của cài đặt PEEP trong bối cảnh suy đa cơ quan (Hình 2). Như đã thảo luận ở trên, tác động của PEEP phụ thuộc vào tác động tương ứng của nó lên phổi và do đó, chức năng tim và tắc nghẽn cơ quan là một phần trong định nghĩa về suy thất phải [36]. Tuy nhiên, tác động của PEEP ít nhất là không thể đoán trước và cần được theo dõi thường xuyên.
4.1 Tác động của áp lực dương cuối thì thở ra đến huyết động thận và nguy cơ tổn thương thận cấp
Chấn thương thận cấp tính (acute kidney injury, AKI) ảnh hưởng đến hơn một nửa số bệnh nhân ICU và ảnh hưởng sâu sắc đến tiên lượng [37]. Một mặt, bệnh nhân AKI có nguy cơ phải thở máy xâm lấn cao gấp đôi [35–38], nhưng mặt khác, bệnh nhân thở máy cũng phải đối mặt với nguy cơ chấn thương thận tăng gấp ba lần [39,40].
Bản thân suy hô hấp cấp tính có liên quan đến việc tăng nguy cơ phát triển AKI [41,42], ngoài ra, việc áp dụng thở máy từ lâu đã bị nghi ngờ có liên quan đến việc làm suy giảm chức năng thận [30,43], khiến các tác giả đặt ra thuật ngữ này: tổn thương thận do thở máy [25]. Các cơ chế mà thông khí cơ học góp phần gây ra AKI là đa yếu tố và liên quan đến việc giải phóng các chất trung gian gây viêm do chấn thương sinh học [42,44–48], giảm lưu lượng máu thận thứ phát do tăng CO2 máu [49– 52], huyết động và thần kinh. - các quá trình nội tiết tố [35] liên quan đến tăng áp lực trong lồng ngực và độc tính thận của thuốc dùng đồng thời (ví dụ oxit nitric dạng hít [53,54]). Từ quan điểm cơ học và như được mô tả ở trên, việc áp dụng PEEP có thể làm tăng Pra. Vì Pra, còn được gọi là áp lực tĩnh mạch trung tâm (CVP), đóng vai trò là áp lực dòng máu thận chảy ra, CVP tăng dẫn đến tăng áp lực tĩnh mạch thận, còn gọi là tắc nghẽn thận. Tăng huyết áp tĩnh mạch thận tác động lên việc tăng áp lực ly tâm, tăng áp lực thủy tĩnh trong cầu thận và giảm áp lực lọc ròng, cuối cùng dẫn đến xẹp mao mạch cầu thận [55]. Tắc nghẽn tĩnh mạch, thay vì suy giảm cung lượng tim, được coi là nguyên nhân chính gây tổn thương thận trong suy tim mất bù [56], trong khi nguyên nhân chính ở bệnh nhân bị sốc có lẽ là áp lực tưới máu trung bình (huyết áp động mạch trung bình trừ CVP) [57]. Tương tự, CVP luôn có liên quan đến việc tăng nguy cơ AKI ở bệnh nhân ICU [58]. Cụ thể hơn, ở những bệnh nhân được thở máy, một nghiên cứu gần đây đã tìm thấy tác động bất lợi tổng hợp của mức CVP và PEEP đối với việc làm suy giảm chức năng thận [59]. Ngoài ra, rối loạn chức năng thất phải do PEEP gây ra có thể dẫn đến tăng áp lực ổ bụng, điều này cũng có thể làm thay đổi chức năng thận [60,61]. Giảm tiền tải thất trái và cung lượng tim do tác dụng phụ của tình trạng căng quá mức phế nang có thể gây nguy hiểm cho lưu lượng máu qua thận [34], mặc dù cơ chế này có thể góp phần ít hơn vào rối loạn chức năng thận do PEEP gây ra [56].
Sự thay đổi nội tiết tố thần kinh do PEEP gây ra cũng có thể gây ứ nước. Hệ thống thần kinh giao cảm, hệ thống renin-angiotensin-aldosterone và hormone chống bài niệu được kích thích sau khi áp dụng PEEP [62]. Điều thú vị là, ở những người nhận ghép thận, việc hủy thần kinh giao cảm ở thận dường như không làm giảm tác dụng của PEEP, cho thấy tác dụng này phụ thuộc vào áp lực tưới máu hơn là do hormone gây ra [63].
Ngoài tắc nghẽn thận, thông khí cơ học gây tổn thương với thể tích khí lưu thông cao và PEEP thấp đã được chứng minh là gây ra tình trạng viêm toàn thân trong bối cảnh ARDS, với việc giải phóng IL-1B, IL-6, IL-8 TNF-alpha, MCP -1 và VEGF, dẫn đến apoptosis tế bào biểu mô [64,65]. Ngược lại, thông khí bảo vệ phổi bằng PEEP dựa trên đường cong áp lực-thể tích có liên quan đến nồng độ thấp hơn của các dấu hiệu viêm trong huyết tương và rửa phế quản phế nang [66,67], mặc dù những phát hiện này chưa được lặp lại trong thử nghiệm ALVEOLI [68]. Điều thú vị là, dữ liệu tiền lâm sàng và liều lượng từ huyết thanh của bệnh nhân cho thấy rằng hệ thống phối tử Fas-Fas, có liên quan đến việc điều hòa sự chết của tế bào và dung nạp miễn dịch, có liên quan đến quá trình chết theo chương trình của tế bào biểu mô ống thận, nêu bật tiềm năng điều trị trong việc phong tỏa con đường này trong ARDS - gây ra rối loạn chức năng thận và đa cơ quan [65].
Tóm lại, tác dụng của PEEP đối với huyết động học và chức năng thận không đơn giản. sự tương tác giữa tác dụng của PEEP đối với cơ học phổi, chức năng tim, CVP và tình trạng dịch có nhiều khả năng ảnh hưởng đến nguy cơ AKI khi thở máy [59,69]. Liệu một chiến lược thông khí nhất định có khả năng bảo vệ thận mà không hy sinh sự hỗ trợ của hệ hô hấp hay không cần được nghiên cứu thêm.
4.2 Tác động của áp lực dương cuối thì thở ra lên tuần hoàn đường tiêu hóa và gan
Tương tự như AKI, tác động có hại của mức PEEP không đủ đối với cơ học phổi có thể chuyển thành tăng áp lực tĩnh mạch ảnh hưởng đến huyết động học của đường tiêu hóa và gan. Vì tưới máu nội tạng đặc biệt nhạy cảm và việc giảm tưới máu nhỏ có thể làm tổn hại chức năng rào cản của nó, nên việc giảm lưu lượng máu mạc treo và cửa đã bị nghi ngờ là nguyên nhân thúc đẩy tiến triển đến rối loạn chức năng đa cơ quan ở bệnh nhân mắc ARDS [70,71].
Trong một mô hình khác ngoài ARDS, ví dụ như suy tim tiến triển mất bù, Nikolaou và cộng sự [72] cho rằng tắc nghẽn gây ra tắc nghẽn ống mật và sau đó làm tăng phosphatase kiềm, trong khi thiếu máu cục bộ ở gan gây ra hoại tử tế bào trung tâm tiểu thùy và sau đó làm tăng trans-aminase. Rối loạn chức năng gan sớm, được phản ánh bằng nồng độ bilirubin huyết thanh tăng trong giai đoạn đầu của ARDS, được thấy ở khoảng 15–20% bệnh nhân và có liên quan chặt chẽ với tỷ lệ tử vong trong 90 ngày [73,74]. Mặc dù tương tác giữa phổi và gan đã được nghiên cứu rộng rãi, chủ yếu liên quan đến việc điều chỉnh tình trạng viêm và cơ chế sửa chữa [75], hiện vẫn thiếu dữ liệu chắc chắn về tác động của các thông số máy thở đối với sự phát triển của bệnh suy gan và tiêu hóa. Các mô hình thí nghiệm từ những năm 1980 đến 1990 cho thấy mối quan hệ nghịch đảo giữa mức PEEP và lưu lượng máu nội tạng, chủ yếu là do giảm cung lượng tim, trong khi mức tiêu thụ oxy của nội tạng thường được duy trì bằng cách tăng lượng oxy trích xuất để bù [76,77]. Mặt khác, tỷ lệ apoptosis tế bào biểu mô tăng lên cũng được ghi nhận ở nhung mao ruột non ở động vật phải thở máy gây tổn thương với thể tích khí lưu thông cao (15–17 ml/kg) và PEEP thấp (0–3 cmH2O) [ 65].
Ở người, một số nghiên cứu nhỏ không cho thấy bất kỳ sự thay đổi nào trong tưới máu niêm mạc dạ dày [78] hoặc lưu lượng máu nội tạng khi truyền liên tục thuốc nhuộm màu xanh lá cây indocyanine [79] để đáp ứng với việc tăng PEEP, nhưng do thiếu dữ liệu gần đây về quản lý thông khí hiện tại của ARDS, rất khó để đưa ra kết luận về ý nghĩa lâm sàng của những phát hiện này và vai trò của PEEP trong suy gan và đường tiêu hóa ở bệnh nhân ARDS vẫn chưa được xác định.
Điểm Hệ thống phân loại quá tải tĩnh mạch bằng siêu âm (Venous Excess Ultrasound Grading System, VExUS), một quy trình siêu âm bốn bước đánh giá tĩnh mạch chủ dưới, tĩnh mạch thận, cũng như tĩnh mạch gan và tĩnh mạch cửa bằng Doppler, đã được đề xuất như một phương tiện để đo tắc nghẽn tĩnh mạch [80]. Nó tương quan với Pra [81]
và có thể dự đoán tổn thương thận cấp tính sau phẫu thuật bắc cầu tim phổi [82]; tuy nhiên, ý nghĩa lâm sàng của nó trong bối cảnh thông khí, sung huyết tĩnh mạch do PEEP và tổn thương gan vẫn còn được đánh giá.
Ngoài bối cảnh ARDS, việc áp dụng các mức PEEP khác nhau trong quá trình ghép gan dường như không ảnh hưởng đến huyết động và chức năng gan, mặc dù CVP tăng [83–85].
5 Tác động của áp lực dương cuối thì thở ra đến tuần hoàn não
Thông khí cơ học là phương pháp chính trong việc quản lý bệnh nhân bị suy thần kinh. Hơn nữa, tổn thương phổi cấp tính là biến chứng ngoài sọ phổ biến nhất ở bệnh nhân chấn thương não cấp tính, ảnh hưởng tới 35% bệnh nhân [86]. Mặc dù tác động của PaCO2 đối với áp lực nội sọ (ICP) đã được ghi nhận và tính toán rõ ràng, nhưng tác động của cài đặt máy thở và PEEP đối với huyết động học não ít được đánh giá cao [87].
PEEP có thể ảnh hưởng đến ICP thông qua các cơ chế riêng biệt. Đầu tiên, những thay đổi về PaCO2 liên quan đến việc huy động/căng phổi quá mức có thể điều chỉnh dòng máu vào động mạch. Sau đó, áp lực trong lồng ngực và tĩnh mạch cảnh tăng lên sẽ cản trở sự hồi lưu của tĩnh mạch não. Dòng máu vào lớn hơn hoặc dòng máu ra ít hơn cuối cùng sẽ dẫn đến tăng ICP khi khả năng dịch chuyển dịch não tủy bị vượt quá. Cuối cùng, trong trường hợp mức PEEP làm giảm cung lượng tim, áp lực tưới máu não thấp hơn cơ chế tự điều hòa của não sẽ làm giảm ICP. Trong trường hợp cơ chế tự điều hòa não bị suy yếu, tồn tại mối quan hệ tuyến tính giữa áp lực động mạch trung bình và áp lực tưới máu não và bất kỳ tác động nào của PEEP lên cung lượng tim sẽ chuyển thành những thay đổi về áp lực tưới máu não, có khả năng ảnh hưởng đến tưới máu não.
Không có gì đáng ngạc nhiên, việc áp dụng mức PEEP vừa phải ở những bệnh nhân trải qua phẫu thuật ngoài sọ (não không bị tổn thương) dường như không ảnh hưởng đến ICP [88,89]. Ngược lại, việc tăng mức PEEP sẽ dẫn đến tăng ICP ở những bệnh nhân được chăm sóc đặc biệt trong phẫu thuật thần kinh, không phải lúc nào cũng có ý nghĩa lâm sàng và không dẫn đến giảm áp lực tưới máu não một cách có hệ thống [90–94]. Trong một nghiên cứu đơn tâm gần đây, PEEP tăng ICP ở 58% và oxygen hóa mô não (PbtO2) ở 21% bệnh nhân, nhưng những thay đổi này phần lớn là không thể đoán trước và không tìm thấy mối tương quan giữa DPEEP và DPbtO2 hoặc DICP [95].
Thay vì độ giãn nở ban đầu của hệ hô hấp, việc huy động phế nang và những thay đổi về độ giãn nở hô hấp sau khi áp dụng PEEP có liên quan đến những thay đổi trong ICP, nhấn mạnh tầm quan trọng của việc chuẩn độ PEEP tối ưu và tích hợp cơ học hô hấp trong dự đoán tác dụng huyết động của PEEP lên các cơ quan ở xa [91,95-97]. Một số tác giả đã đề xuất PICGap, đại diện cho khoảng trống (gap) giữa áp lực nội sọ cơ bản và CVP, như một yếu tố dự báo tiềm năng về khả năng đáp ứng của ICP đối với các điều chỉnh PEEP [98]. Điều này gợi lại ý tưởng rằng bản thân PEEP không có lợi cũng như không có hại đối với huyết động học của cơ quan đích, nhưng tác dụng của nó phụ thuộc vào cơ học hô hấp và mối liên quan với các biến số huyết động khác như CVP [59].
Dựa trên những cân nhắc này, không nên khuyến khích áp dụng chiến lược thông khí bảo vệ phổi ở bệnh nhân tổn thương não mắc ARDS và nên xác định mức PEEP tối ưu bằng cách sử dụng các thông số hô hấp và huyết động thông thường cũng như theo dõi ICP [93,99,100]. Do đó, chiến lược thông khí có tính đến các hậu quả về não của PEEP (và các thông số hô hấp khác) có vị trí nổi bật nhất ở những bệnh nhân phẫu thuật thần kinh có tiền sử hoặc có nguy cơ tăng áp lực nội sọ. Mặt khác, hậu quả về não của PEEP trong bối cảnh ARDS không có suy thần kinh sẽ ít có ý nghĩa lâm sàng hơn.
Tác động huyết động của áp lực dương cuối thì thở ra trong các thử nghiệm có kiểm soát ngẫu nhiên. Bằng chứng đáng tin cậy nhất về tác động của PEEP đối với cung lượng tim và chức năng của các cơ quan nội tạng dự kiến sẽ đến từ các thử nghiệm ngẫu nhiên có đối chứng, trong suốt lịch sử của ARDS, đã cố gắng xác định cài đặt PEEP tốt nhất [7]. Điều này được tóm tắt trong Bảng 1.
Việc giải thích những kết quả này trở nên khó khăn do các biện pháp can thiệp đồng thời về thể tích khí lưu thông, chiến lược máy thở và thủ thuật huy động, cũng như loại trừ các bệnh nhân bị chấn thương não cấp tính/tăng ICP hoặc bệnh gan mãn tính. Hơn nữa, tác động lên chức năng não, ruột và gan hiếm khi được báo cáo. Tuy nhiên, mức PEEP cao hơn kết hợp với các thủ thuật huy động phổi dường như có liên quan đến tác động có hại đến tim mạch [2,3], trong khi việc chuẩn độ PEEP dựa trên cơ học hô hấp dường như có liên quan đến việc tăng cung lượng tim và ổn định huyết động [101 –103].
6 Kết luận
Cài đặt PEEP lý tưởng phải hướng tới sự cân bằng giữa khả năng mở lại phổi bị xẹp và nguy cơ căng quá mức ở các phế nang đã mở. Trong phần tường thuật này, chúng tôi mô tả các tác động sinh lý bệnh của PEEP đối với chức năng tim và tuần hoàn của các cơ quan nội tạng, nhấn mạnh tính hai mặt của tác động huyết động của PEEP tùy thuộc vào cả cơ học hô hấp và mối liên quan với các biến số huyết động khác như CVP hoặc huyết áp động mạch trung bình. Có những điểm tương đồng trong các biện pháp ngăn ngừa tác động có hại của PEEP lên phổi, tim, thận, gan và não. Việc chuẩn độ PEEP có nên dựa trên độ giãn nở của hệ hô hấp [102,104], oxygen hóa [68,105], đường cong áp lực-thể tích [106,107] hay áp lực xuyên phổi [108–110] vẫn còn được tranh luận gay gắt [6]. Theo quan điểm của chúng tôi, giao thức cài đặt PEEP cũng nên tính đến các tác động đến huyết động của PEEP. Theo dõi cung lượng tim, chức năng tâm thất phải và áp lực trong lồng ngực là nền tảng trong điều trị ARDS và là bước đầu tiên trong việc ngăn ngừa những cạm bẫy của PEEP đối với huyết động của cơ quan đích [6]. Các bác sĩ chăm sóc đặc biệt nên duy trì mức độ cảnh giác cao đối với các tác động lên huyết động của PEEP.
Bảng 1. Tác động của áp lực dương cuối thì thở ra lên tuần hoàn của tim, thận, ruột, gan và hệ thần kinh trung ương ở các thử nghiệm ngẫu nhiên có đối chứng chính với các cài đặt PEEP khác nhau
| Thử nghiệm | Cài đặt PEEP | Ảnh hưởng đến huyết áp/cung lượng tim | Ảnh hưởng đến chức năng thận | Tác dụng lên chức năng ruột và gan | Tác dụng lên hệ thần kinh trung ương |
| Amato, NEJM. 1998 [112] | 9,3 ± 0,5 so với 13,2 ± 0,4 cmH2O (với chiến lược thông khí bảo vệ) | NA | RRT: 5 (21%) so với 7 (24%) bệnh nhân, P > 0,10 | Một trường hợp tử vong do xuất huyết tiêu hóa lan tỏa ở nhóm thở máy bảo vệ | NA |
| Mạng ARDS, NEJM. 2000 [67] | 8,6 ± 3,6 so với 9,4 ± 3,6 cmH2O (với thể tích khí lưu thông thấp hơn) | Ngày không suy tuần hoàn: 19 ± 10 so với 17 ± 11 ngày, P = 0,004 | Số ngày không suy thận 20 ± 11 so với 18 ± 11 ngày, P = 0,005 | NA | NA |
| Ranieri, JAMA. 2000 [113] | 6,5 ± 1,7 so với 14,8 ± 2,7 cmH2O | Suy tim mạch: 8 (36%) so với 3 (14%) | AKI: 19 (86%) so với 4 (18%), P = 0,04 | 5 (23%) so với 1 (5%) rối loạn chức năng gan | Suy nhược thần kinh: 4 (18%) so với 0 (0%) |
| Brower, NEJM. 2004 (ALVEOLI) [68] | 8,3 ± 3,2 so với 13,2 ± 3,5 cmH2O | Không có sự khác biệt đáng kể về số ngày không bị suy tuần hoàn, gan, thận | NA | ||
| Villar, CCM. 2006 [102] | 9,0 ± 2,7 so với 14,1 ± 2,8 cmH2O (PEEP trên điểm uốn dưới của đường cong thể tích áp lực của hệ hô hấp) | Suy tim mạch: 28 (62%) so với 9 (18%), P < 0,001. Chỉ số tim 4,7 ± 1,4 so với 5,8 ± 1,5 l/phút/m2, P <0,05 | 18 (40%) so với 21 (42%) | Suy gan 8 (17,8%) so với 4 (8%) Suy tiêu hóa 8 (17,8%) so với 8 (16%) | 8 (18%) so với 5 (10%) |
| Manzano, CCM. 2008 [114] | 0,12 ± 0,7 so với 5,78 ± 1,0 cmH2O | NA | RRT: 3 (5%) so với 1 (2%) | NA | NA |
| Mercat, JAMA. 2008 (EXPRESS) [103] | 7,1 ± 1,8 so với 14,6 ± 3,2 cmH2O | Số ngày suy tim mạch: 21(4-26) so với 23 (10--26), P = 0,09 | Số ngày không bị suy thận: 27,5 (8,0-28,0) so với 28,0 (11,0-28,0) ngày, P = 0,23 | NA | NA |
| Talmor, NEJM. 2008 [109] | 10 ± 4 so với 17 ± 6 cmH2O (được hướng dẫn bởi áp lực thực quản) | Ngày không sốc: 17 (0-21) so với 14 (0-21), P = 0,47 | NA | NA | NA |
| Meade, JAMA. 2008 (LOVS) [106] | 10,1 ± 3,0 so với 15,6 ± 3,9 cmH2O | Số ngày dùng thuốc vận mạch: 5 (2-9) so với 4 (2--8) ngày | RRT: 85 (19%) so với 71 (17%) | NA | NA |
| Pintado, ERJ. 2013 [104] | 10 ± 3 so với 12 ± 2 cmH2O (theo hướng dẫn của độ giãn nở) | Ngày huyết động không suy ở ngày 28: 16 (0-23,75) so với 22 (0-25) ngày, P = 0,04 | Số ngày không còn suy thận sau 28 ngày: 28 (0--28) so với 28 (0--28), P = 0,39 | Số ngày không bị suy gan ở 28 ngày 28 (0--28) so với 28 (0--28) P 1⁄4 0,08 | NA |
| Kacmarek, CCM. 2016 [105] | 11,6 ± 2,5 so với 15,8 ± 3,8 cmH2O | Suy tim là nguyên nhân chính gây tử vong 1 (3%) so với 1 (4%). Suy đa tạng là nguyên nhân chính gây tử vong 10 (33%) so với 4 (16%) | NA | NA | NA |
| Cavalcanti, JAMA. 2017 (ART) [10] | 12,0 ± 0,6 so với 16,2 ± 0,7 cmH2O(+ thủ thuật huy động phổi) | Hạ huyết áp 144 (28%) so với 174 (35%), P = 0,03 | NA | NA | NA |
| Hodgson, AJRCCM. 2019 (PHARLAP) [101] | 11,7 ± 3,0 so với 16,1 ± 3,6 cmH2O (với thao tác huy động bậc thang) | Hạ huyết áp nặng 12 (21%) so với 20 (35%), P = 0,12 | NA | NA | NA |
| Beitler, JAMA. 2019 [111] | 16 ± 4 so với 17 ± 6 cmH2O (được hướng dẫn bởi áp lực thực quản) | NA | RRT: 21 (21%) so với 32 (33%), P = 0,056 | NA | NA |

