Tiếp cận mới chẩn đoán điều trị suy tim phân suất tống máu giảm 2025

Nguồn tham khảo: “Heart failure with reduced ejection fraction”, The Lancet 2025
Người dịch: PGS.TS.BS Trần Kim Sơn - Chủ tịch Liên Chi hội tăng huyết áp ĐBSCL
ThS.BS Nguyễn Thiên Thạch - Liên Chi hội Tăng huyết áp ĐBSCL
Suy tim là một hội chứng lâm sàng phức tạp, ảnh hưởng đến khoảng 70 triệu người trên toàn cầu. Tỷ lệ hiện mắc vào khoảng 2% ở châu Âu và Bắc Mỹ, và xấp xỉ 1% ở châu Á và Nam Mỹ. Chẩn đoán chính xác dựa trên sự hiện diện của các triệu chứng và dấu hiệu điển hình, nồng độ peptide lợi niệu tăng, cùng với bằng chứng về các bất thường cấu trúc hoặc chức năng tim thông qua các kỹ thuật chẩn đoán hình ảnh tim mạch. Khoảng một nửa số trường hợp suy tim là do giảm chức năng tâm thu thất trái - được phân loại là suy tim với phân suất tống máu giảm (HFrEF). Các liệu pháp điều trị theo khuyến cáo hiện nay đã cải thiện rõ rệt tỷ lệ sống còn và chất lượng cuộc sống của bệnh nhân HFrEF.
Chiến lược điều trị hiện đại nhấn mạnh việc khởi trị sớm và tăng liều nhanh của bốn nhóm thuốc nền tảng gồm: thuốc ức chế hệ renin–angiotensin hoặc thuốc ức chế thụ thể angiotensin–neprilysin (ARNI), thuốc chẹn β, thuốc kháng thụ thể mineralocorticoid (MRA), thuốc ức chế đồng vận chuyển natri–glucose type 2 (SGLT2i), đi kèm với thuốc lợi tiểu để giảm triệu chứng ứ dịch. Mặc dù đã có nhiều tiến bộ trong điều trị, suy tim vẫn là nguyên nhân hàng đầu gây bệnh tật và tử vong tim mạch, một phần do việc không triển khai đầy đủ và tuân thủ điều trị kém.
Các định hướng tương lai nhằm cải thiện kết cục bao gồm tích hợp các phương pháp y học cá thể hóa, phân tích đa chiều, và thiết kế thử nghiệm lâm sàng đổi mới để giải quyết nguy cơ tồn dư và xác định các mục tiêu điều trị mới. Bài Seminar này cung cấp cái nhìn tổng quan về chẩn đoán và điều trị dược lý hiện tại ở bệnh nhân HFrEF, nhấn mạnh những tiến bộ đã đạt được và những thách thức còn tồn tại.
1 Giới thiệu
Suy tim là một hội chứng lâm sàng phức tạp, ảnh hưởng đến khoảng 60–70 triệu người trên toàn thế giới. Tỷ lệ hiện mắc chiếm khoảng 2–3% trong dân số chung. Thay vì là một chẩn đoán bệnh lý đơn thuần, suy tim được đặc trưng bởi một phổ rộng các triệu chứng và dấu hiệu điển hình. Những biểu hiện này bắt nguồn từ các bất thường cấu trúc và/hoặc chức năng của tim, dẫn đến tăng áp lực đổ đầy tim và/hoặc cung lượng tim không đầy đủ khi nghỉ ngơi hoặc khi gắng sức.
Suy tim chiếm khoảng 2% tổng chi phí chăm sóc sức khỏe, trong đó nhập viện chiếm phần lớn chi phí.
2 Phân loại
Hiện nay, suy tim được phân loại dựa trên sự hiện diện hoặc không có rối loạn chức năng tâm thu, được đánh giá bằng phân suất tống máu thất trái (LVEF). Suy tim được chia thành: Suy tim với phân suất tống máu giảm (HFrEF): khi LVEF < 40%, Suy tim với phân suất tống máu giảm nhẹ (HFmrEF): khi LVEF từ 41% đến 49%, Suy tim với phân suất tống máu bảo tồn (HFpEF): khi LVEF ≥ 50%. Một số định nghĩa cũng bao gồm suy tim với phân suất tống máu cải thiện (HFimpEF), được mô tả ở những bệnh nhân có LVEF ban đầu < 40% nhưng cải thiện > 10% và đạt ≥ 40% trong quá trình theo dõi. Suy tim cũng được phân loại theo mức độ nặng. Hệ thống phân loại triệu chứng được sử dụng rộng rãi nhất là New York Heart Association (NYHA), phân từ: Độ I: không triệu chứng khi hoạt động thông thường, Độ IV: triệu chứng xuất hiện cả khi nghỉ ngơi. Hướng dẫn của Hoa Kỳ mô tả thêm tiến trình phát triển bệnh từ: Giai đoạn A: có nguy cơ, đến Giai đoạn D: suy tim giai đoạn cuối. Tuy nhiên, các hệ thống phân loại này chủ yếu dựa vào triệu chứng và chưa phản ánh sự khác biệt về bất thường cấu trúc tim.
3 Dịch tễ học
HFrEF chiếm từ 48% đến 66% tổng số bệnh nhân suy tim. Trong nghiên cứu đoàn hệ tại Olmsted (Mỹ): tỷ lệ mắc HFrEF là 1,5 ca trên 1000 người-năm ở nam giới, 0,8 ca trên 1000 người-năm ở nữ giới. Theo thời gian, tỷ lệ mắc HFrEF đã giảm đáng kể sau điều chỉnh theo tuổi và giới, với mức giảm 45% từ năm 2000 đến 2010. Tương tự, trong Nghiên cứu Tim Framingham và Cardiovascular Health Study: tỷ lệ mắc chuẩn hóa theo tuổi ở những người > 60 tuổi giảm khoảng 20%, từ 6,6 (KTC 95%: 5,9–7,3) ca/1000 người-năm trong thập niên 1990 xuống 6,2 (5,4–6,9) ca/1000 người-năm trong thập niên 2000. Tỷ lệ hiện mắc của HFrEF cũng thay đổi tùy thuộc vào đặc điểm quần thể được nghiên cứu và bối cảnh địa lý.
Tại Hoa Kỳ, dữ liệu từ cơ sở dữ liệu Get With The Guidelines–Heart Failure (GWTG-HF) cho thấy HFrEF chiếm 53% tổng số bệnh nhân suy tim (trong đó 39% là HFrEF và 14% là HFmrEF).
Tại châu Âu, dữ liệu từ cơ sở dữ liệu theo dõi dài hạn của Hội Tim mạch châu Âu (ESC Heart Failure Long-Term Registry) cho thấy 60% bệnh nhân suy tim được phân loại là HFrEF và 24% là HFmrEF.
Tại Vương quốc Anh, HFrEF chiếm khoảng một nửa số ca nhập viện vì suy tim, với mức giảm dần 16% được ghi nhận từ năm 2018 đến 2022. Hiện có rất ít dữ liệu cập nhật về dịch tễ học của HFrEF ở các quốc gia thu nhập thấp và trung bình. Tại châu Á, tỷ lệ hiện mắc HFrEF dao động từ 0,7% đến 1,0%, trong khi tại Nam Mỹ, tỷ lệ hiện mắc suy tim nói chung vào khoảng 1,0%.
4 Nguyên nhân và bệnh đi kèm
HFrEF xuất hiện do sự tương tác phức tạp của nhiều nguyên nhân và bệnh lý đi kèm, trong đó tăng huyết áp là yếu tố nguy cơ quy thuộc cho dân số (population-attributable risk factor) phổ biến nhất đối với suy tim. Trong Nghiên cứu Framingham, tăng huyết áp xuất hiện ở tới 70% bệnh nhân suy tim, trong khi tại Nghiên cứu Olmsted County, tình trạng này ảnh hưởng đến khoảng 74% bệnh nhân HFrEF. Trong cơ sở dữ liệu OPTIMISE-HF, tăng huyết áp là nguyên nhân hàng đầu của biểu hiện lâm sàng ở khoảng một phần ba trường hợp. Bệnh tim thiếu máu cục bộ cũng là nguyên nhân phổ biến gây HFrEF. Tại các quốc gia phương Tây, bệnh này là nguyên nhân chính ở khoảng 50% bệnh nhân HFrEF và 42% bệnh nhân HFmrEF. Tại Vương quốc Anh, tỷ lệ mắc bệnh tim thiếu máu cục bộ ở bệnh nhân nhập viện vì HFrEF vào khoảng 40%. Tuy nhiên, ở châu Phi, tỷ lệ này thấp hơn đáng kể, chiếm dưới 20% bệnh nhân HFrEF. Các nguyên nhân thường gặp khác tại các nước phát triển bao gồm: bệnh cơ tim di truyền, các bệnh lý thâm nhiễm như amyloidosis và sarcoidosis, độc tính trên tim do điều trị ung thư, bệnh van tim, các bệnh viêm hệ thống mạn tính.
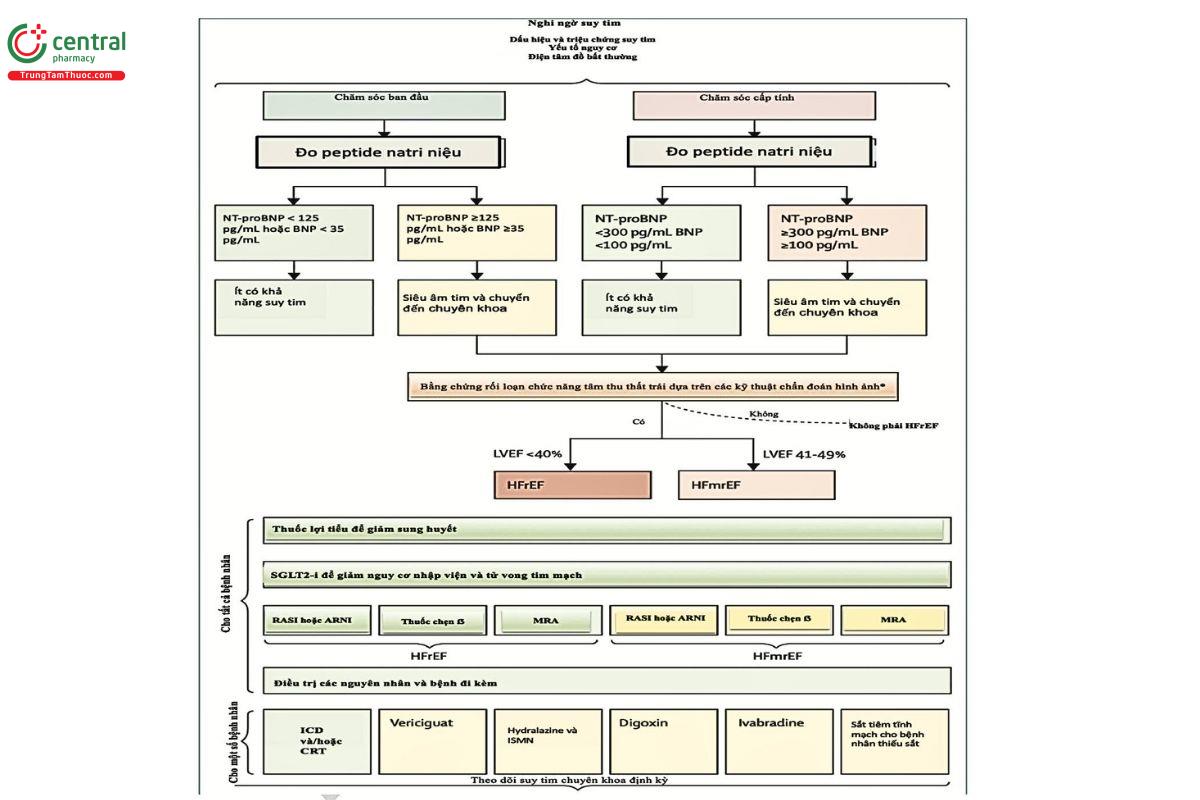
Màu xanh = Khuyến cáo mức I. Màu cam = Khuyến cáo mức II. ARNI = ức chế thụ thể angiotensin neprilysin. BNP = peptide lợi não (brain natriuretic peptide).HFrEF = suy tim với phân suất tổng máu giảm. HFmrEF = suy tim với phân suất tống máu nhẹ giảm. ICD = máy khửrung tim cấy ghép. ISMN = isosorbide mononitrate. LVEF = phân suất tổng máu thất trái (left ventricular ejection fraction). MRA = thuốc đối kháng thụ thể mineralocorticoid.NT-proBNP N-terminal pro-BNP (peptide lợi não). RASi = thuốc ức chế hệ renin-angiotensin.SGLT2-i = thuốc ức chế đồng vận chuyển natri-glucose 2. Echocardiography hoặc chụp cộng hưởng từ tim (cardiac magnetic resonance imaging).
5 Dấu hiệu và triệu chứng
Biểu hiện lâm sàng của HFrEF rất đa dạng. Đặc trưng chính là các triệu chứng và dấu hiệu của quá tải dịch và/hoặc tăng áp lực trong buồng tim. Các triệu chứng thường gặp bao gồm: khó thở khi nghỉ hoặc gắng sức; khó thở khi nằm (orthopnoea); khó thở kịch phát về đêm; và khó thở khi cúi người (bendopnoea). Các triệu chứng khác như giảm khả năng gắng sức, mệt mỏi, đầy bụng sớm, tiểu đêm, và yếu cơ phản ánh tình trạng giảm cung lượng tim và giảm tưới máu hệ thống. Dấu hiệu lâm sàng của suy tim thường do ứ dịch và tăng áp lực đổ đầy, bao gồm ran phổi, phù ngoại biên, tĩnh mạch cổ nổi, cổ trướng, và mỏm tim lệch sang bên. Rối loạn chức năng tâm thu thất trái không triệu chứng - giai đoạn tiền lâm sàng của HFrEF - rất phổ biến, đặc biệt ở bệnh nhân có các yếu tố nguy cơ như tăng huyết áp, bệnh cơ tim, hoặc bệnh tim thiếu máu cục bộ. Đối với người thân của bệnh nhân mắc bệnh cơ tim di truyền, tầm soát rối loạn chức năng tâm thu thất trái không triệu chứng có thể mang lại lợi ích cho chẩn đoán và điều trị sớm.
6 Chẩn đoán
Chẩn đoán suy tim đòi hỏi một quy trình hệ thống theo từng bước (hình 1). Một số bệnh nhân HFrEF có thể đến bệnh viện do đợt mất bù cấp. Tuy nhiên, nhiều bệnh nhân có khởi phát triệu chứng và dấu hiệu suy tim dần dần và thường xuất hiện đầu tiên tại tuyến chăm sóc ban đầu. Ở những bệnh nhân có triệu chứng và/hoặc dấu hiệu gợi ý suy tim, các thăm dò ban đầu nên bao gồm: điện tâm đồ 12 chuyển đạo (ECG), định lượng peptide lợi niệu trong huyết tương - BNP hoặc NT-proBNP, X-quang ngực nhằm phát hiện dấu hiệu sung huyết, yếu tố làm nặng hoặc chẩn đoán thay thế. Peptide lợi niệu đặc biệt có giá trị nhờ độ tin cậy cao khi kết quả âm tính. Ngưỡng ≤125 pg/mL có thể loại trừ hiệu quả chẩn đoán suy tim. Tuy nhiên, tại Vương quốc Anh, ngưỡng cao hơn là 400 pg/mL được khuyến cáo vì hiệu quả chi phí tốt hơn.
7 Xác nhận chẩn đoán
Việc xác nhận suy tim đòi hỏi bằng chứng về bất thường cấu trúc và/hoặc chức năng tim, thường được đánh giá bằng siêu âm tim qua thành ngực. Siêu âm tim cung cấp đánh giá toàn diện về: kích thước buồng tim, chức năng tâm thu và tâm trương, độ dày thành tim, rối loạn vận động vùng, bệnh van tim, đánh giá gián tiếp áp lực động mạch phổi và tình trạng thể tích trong lòng mạch.
Do phân suất tống máu thất trái (LVEF) bằng kỹ thuật 2D hoặc 3D vẫn là trung tâm của phân loại suy tim. Kỹ thuật 2D có mức dao động nội – liên quan sát viên khoảng ±5%, trong khi kỹ thuật 3D thường chính xác hơn, nhưng yêu cầu chất lượng hình ảnh cao hơn. Kỹ thuật siêu âm tim tiên tiến: siêu âm Doppler mô (tissue Doppler imaging), phân tích biến dạng cơ tim bằng speckle-tracking (strain), giúp phát hiện sớm rối loạn chức năng tâm thu dưới lâm sàng bằng cách đánh giá biến dạng cơ tim - thường nhạy hơn LVEF.
Khi đánh giá siêu âm tim không kết luận được hoặc bị hạn chế về mặt kỹ thuật, có thể sử dụng các phương thức chẩn đoán hình ảnh nâng cao như cộng hưởng từ tim. Cộng hưởng từ tim (CMR) cho phép mô tả chi tiết mô cơ tim, đồng thời cung cấp đánh giá chính xác hơn về phân suất tống máu thất trái (LVEF).
CMR cũng có thể được dùng để phát hiện viêm cơ tim, các bệnh lý thâm nhiễm, xơ hóa cơ tim, và đánh giá mức độ còn khả năng sống của cơ tim. Do đó, CMR đặc biệt hữu ích trong việc khảo sát nguyên nhân nền của HFrEF. CMR cũng giúp phát hiện huyết khối thất trái tiềm ẩn cần điều trị chống đông. Chụp CT tim và xạ hình SPECT cũng có thể cung cấp thông tin về giải phẫu động mạch vành, thể tích thất, chức năng tim, và tình trạng thiếu máu cơ tim.
Các thăm dò xâm lấn thường quy, như chụp mạch vành, không bắt buộc để chẩn đoán suy tim, nhưng có thể được chỉ định nhằm đánh giá nguyên nhân của rối loạn chức năng tim. Chụp mạch vành có thể được cân nhắc ở những bệnh nhân: đau thắt ngực dai dẳng dù đã điều trị tối ưu, rối loạn nhịp thất tái phát, hoặc có xác suất tiền-test trung bình đến cao của bệnh động mạch vành.
Sinh thiết nội tâm mạc - cơ tim nên được xem xét ở các bệnh nhân có suy tim tiến triển nhanh nhằm xác định các bệnh lý viêm hoặc thâm nhiễm cần điều trị đặc hiệu.
Các thăm dò khác, bao gồm: nghiệm pháp gắng sức tim phổi (CPET), nghiệm pháp đi bộ 6 phút, Holter điện tâm đồ 24 giờ, và thông tim phải, có thể cung cấp thêm thông tin chẩn đoán ở các trường hợp được chọn lọc, nhưng không được yêu cầu thường quy để chẩn đoán suy tim.
Tất cả bệnh nhân cũng cần được làm các xét nghiệm máu cơ bản, bao gồm: công thức máu, chức năng thận, chức năng gan, xét nghiệm chức năng tuyến giáp, và HbA1c.
8 Lộ trình chăm sóc cho bệnh nhân nghi ngờ suy tim
Bệnh nhân nghi ngờ suy tim cần được tiếp cận chẩn đoán nhanh chóng và chính xác. Điều này đòi hỏi triển khai các quy trình chuyển tuyến rõ ràng và hiệu quả. Tất cả các hướng dẫn quốc tế đều khuyến nghị rằng chăm sóc suy tim phải được thực hiện theo mô hình đa chuyên khoa, vì điều này cải thiện kết cục điều trị. Các dịch vụ chăm sóc suy tim đa chuyên khoa nên bao gồm cả chăm sóc ban đầu nhằm đảm bảo quản lý tối ưu cho bệnh nhân, bất kể họ bắt đầu hành trình chăm sóc sức khỏe ở đâu. Cách triển khai cụ thể sẽ khác nhau tùy theo hệ thống y tế. Tại Vương quốc Anh, tất cả người lớn đến khám tại cơ sở chăm sóc ban đầu với nghi ngờ suy tim nên được đo NT-proBNP và, nếu tăng, được chuyển tuyến để được bác sĩ chuyên khoa đánh giá tại cơ sở tuyến hai hoặc tuyến ba bằng siêu âm tim qua thành ngực.
Những người có NT-proBNP từ 400 đến 2000 pg/mL cần được khám bởi chuyên gia suy tim trong vòng 6 tuần. Những người có NT-proBNP > 2000 pg/mL cần được khám trong vòng 2 tuần. Chiến lược này có ưu điểm được thiết kế đơn giản để dễ triển khai rộng rãi. Tuy nhiên, nó có thể đánh giá quá mức suy tim ở khoảng một phần ba bệnh nhân, đặc biệt là người cao tuổi.
Một lộ trình chăm sóc tích hợp giữa tuyến cơ sở và tuyến chuyên khoa cũng rất quan trọng nhằm nâng cao hiệu quả chăm sóc và giảm các ca nhập viện ngoài kế hoạch. Trong thời gian chờ cuộc hẹn chuyên khoa sau khi đã được chỉ định chuyển tuyến, bác sĩ tuyến cơ sở có thể xem xét: đánh giá các bệnh đồng mắc và điều trị quá tải dịch bằng thuốc lợi tiểu quai.
Bệnh nhân nhập viện vì chẩn đoán mới nghi ngờ suy tim cấp: Đối với bệnh nhân nhập viện với chẩn đoán mới nghi ngờ suy tim cấp, nên đo NT-proBNP một lần để loại trừ suy tim. Những bệnh nhân có NT-proBNP tăng cần được thực hiện siêu âm tim, tốt nhất trong vòng 48 giờ, nhằm xác định kiểu hình suy tim. Bệnh nhân được xác nhận suy tim nên được chuyển sớm và liên tục đến nhóm chăm sóc suy tim đa chuyên khoa.
Sau khi chẩn đoán Bệnh nhân HFrEF cần được bắt đầu điều trị chuẩn theo khuyến cáo (GDMT) và tăng liều nhanh nhất có thể. Sau đó, bệnh nhân cần được tái khám mỗi 6 tháng.
9 Chăm sóc sau xuất viện
Bệnh nhân sau khi ra viện cần được cung cấp thông tin chi tiết và đầy đủ về: chẩn đoán, điều trị đã được khởi trị, kế hoạch điều chỉnh và tăng liều thuốc, theo dõi tác dụng phụ, và thời gian tái khám. Tái khám với bác sĩ chuyên khoa suy tim hoặc điều dưỡng suy tim cộng đồng nên diễn ra trong 2–6 tuần sau xuất viện, tùy theo tình trạng lâm sàng. Các quản lý tiếp theo - bao gồm tăng liều GDMT, theo dõi điều trị và tái khám định kỳ - cần được phối hợp giữa đội ngũ suy tim và bác sĩ chăm sóc ban đầu.
10 Điều trị
Bệnh nhân HFrEF có triệu chứng cần được khởi trị nhanh và tăng liều sớm GDMT trước khi xem xét các can thiệp thiết bị (device-based therapies). Mục tiêu bao gồm: làm giảm dấu hiệu sung huyết, giảm tỷ lệ bệnh tật và tử vong, cải thiện chất lượng cuộc sống.
Quản lý suy tim cần phối hợp hai hướng tiếp cận bổ sung: Điều trị tổng quát hội chứng suy tim và Điều trị nhắm trúng nguyên nhân nền
Ở bệnh nhân HFrEF, điều trị tổng quát chủ yếu bao gồm thuốc (bảng 1 và 2), và các can thiệp bằng thiết bị chỉ dành cho một số đối tượng được chọn.
Bảng 1: Các thuốc điều trị suy tim
| Thuốc | Liều khởi trị | Liều mục tiêu | Tác dụng phụ / CCD |
| Thuốc ức chế đồng vận chuyển natri–glucose 2 (SGLT2 inhibitors) | |||
| Empagliflozin | 10 mg một lần/ngày | 10 mg một lần/ngày | Nhiễm toan ceton do đái tháo đường; nhiễm trùng đường tiểu; đái tháo đường type 1 |
| Dapagliflozin | 10 mg một lần/ngày | 10 mg một lần/ngày | |
| Thuốc đối kháng thụ thể mineralocorticoid (MRA) | |||
| Spironolactone | 12,5–25 mg một lần/ngày | 100 mg một lần/ngày | Tăng Kali máu; suy giảm chức năng thận; vú to ở nam giới |
| Eplerenone | 25 mg một lần/ngày | 50 mg một lần/ngày | Tăng kali máu; suy giảm chức năng thận; táo bón; phát ban |
| Finerenone | 10 mg hoặc 20 mg một lần/ngày | 40 mg một lần/ngày | Tăng kali máu; suy giảm chức năng thận; ngứa |
| Thuốc ức chế men chuyển / ức chế thụ thể angiotensin, ± ức chế neprilysin (RAAS inhibitors) | |||
| Captopril | 6,25 mg ba lần/ngày | 50 mg ba lần/ngày | Tăng kali máu; suy giảm chức năng thận; hạ huyết áp; hẹp động mạch thận; phù mạch; ho; vị kim loại; giảm bạch cầu trung tính/mất bạch cầu hạt; phát ban |
| Enalapril | 2–5 mg hai lần/ngày | 10–20 mg hai lần/ngày | Tăng kali máu; suy giảm chức năng thận; hạ huyết áp; hẹp động mạch thận; phù mạch; ho |
| Lisinopril | 2,5–5 mg một lần/ngày | 20–35 mg một lần/ngày | Tăng kali máu; suy giảm chức năng thận; hạ huyết áp; hẹp động mạch thận; phù mạch; ho |
| Ramipril | 2,5 mg một lần/ngày | 5 mg hai lần/ngày | Tăng kali máu; suy giảm chức năng thận; hạ huyết áp; hẹp động mạch thận; phù mạch; ho; rối loạn tiêu hóa; khô miệng (hiếm) |
| Trandolapril | 0,5 mg một lần/ngày | 4 mg một lần/ngày | Tăng kali máu; suy giảm chức năng thận; hạ huyết áp; hẹp động mạch thận; phù mạch; ho; khó chịu tiêu hóa; tiêu chảy; da khô |
| Candesartan | 4 mg một lần/ngày | 32 mg một lần/ngày | Tăng kali máu; suy giảm chức năng thận; hạ huyết áp; hẹp động mạch thận; phù mạch; chóng mặt |
| Losartan | 25 mg một lần/ngày | 150 mg một lần/ngày | Tăng kali máu; suy giảm chức năng thận; hạ huyết áp; hẹp động mạch thận; phù mạch; phát ban; khó tiêu; hạ đường huyết |
| Valsartan | 20 mg hai lần/ngày | 160 mg hai lần/ngày | Tăng kali máu; suy giảm chức năng thận; hạ huyết áp; hẹp động mạch thận; phù mạch; mất ngủ; đau khớp |
| Sacubitril–Valsartan | Sacubitril 24 mg hai lần/ngày; Valsartan 26 mg hai lần/ngày | Sacubitril 97 mg hai lần/ngày; Valsartan 103 mg hai lần/ngày | Tăng kali máu; suy giảm chức năng thận; hạ huyết áp; hẹp động mạch thận; phù mạch |
| Thuốc chẹn beta (β-blockers) | |||
| Bisoprolol | 1,25 mg một lần/ngày | 10 mg một lần/ngày | Hen phế quản nặng; nhịp chậm; hạ huyết áp; khô mắt; buồn nôn; hiện tượng Raynaud; khí sắc trầm; rối loạn cương |
| Carvedilol | 3,125 mg hai lần/ngày | 25 mg hai lần/ngày | Hen phế quản nặng; nhịp chậm; hạ huyết áp; khô mắt; khí sắc thấp; rối loạn cương; phát ban; mất ngủ |
| Metoprolol succinate (CR/XL) | 12,5–25 mg một lần/ngày | 200 mg một lần/ngày | Hen phế quản nặng; nhịp chậm; hạ huyết áp; khí sắc thấp; rối loạn cương; hiện tượng Raynaud; rối loạn giấc ngủ; suy giảm thị lực |
| Nebivolol | 1–2,5 mg một lần/ngày | 10 mg một lần/ngày | Hen phế quản nặng; nhịp chậm; hạ huyết áp; khô mắt; khí sắc thấp; rối loạn cương; rối loạn giấc ngủ; suy giảm thị lực |
| Các thuốc khác | |||
| Ivabradine | 5 mg hai lần/ngày | 7,5 mg hai lần/ngày | Nhồi máu cơ tim cấp; hội chứng QT bẩm sinh; nhịp chậm; block nhĩ thất; chóng mặt; đau đầu; tăng huyết áp; nhìn mờ |
| Vericiguat | 2,5 mg một lần/ngày | 10 mg một lần/ngày | Hạ huyết áp; thiếu máu; chóng mặt; triệu chứng tiêu hóa; đau đầu |
| Digoxin | 62,5–250 µg một lần/ngày | – | Nguy cơ ngộ độc digitalis tăng nếu tăng kali máu; hạ kali máu; hạ Magie máu; thiếu oxy; bệnh thận mạn |
| Hydralazine–Isosorbide dinitrate | Hydralazine 37,5 mg ba lần/ngày; Isosorbide dinitrate 20 mg ba lần/ngày | Hydralazine 75 mg ba lần/ngày; Isosorbide dinitrate 40 mg ba lần/ngày | Nặng lên đau thắt ngực; chóng mặt; bốc hỏa; rối loạn tiêu hóa; đau đầu; hạ huyết áp; đau khớp; hội chứng giống lupus; hồi hộp |
Bảng 2: Điều trị lợi tiểu cho suy tim
| Thuốc | Liều khởi trị | Liều tối đa | Thời gian bán thải | Tác dụng phụ / CCD |
| Thuốc lợi tiểu quai (Loop diuretics) | ||||
| Furosemide | 20–40 mg | 400–600 mg | 1–3 giờ | Giảm kali máu; giảm natri máu; giảm thể tích tuần hoàn; nặng lên chức năng thận |
| Bumetanide | 0,5–1 mg | 10–15 mg | 1–1,5 giờ | Giảm kali máu; giảm natri máu; giảm thể tích; nặng lên chức năng thận |
| Torasemide | 10 mg | 200-300 mg | 3–6 giờ | Giảm kali máu; giảm natri máu; giảm thể tích; nặng lên chức năng thận |
| Thuốc lợi tiểu thiazide | ||||
| Hydrochlorothiazide | 12,5–25 mg | 200 mg | 6–15 giờ | Giảm kali máu; giảm chlore máu; tăng đường huyết; tăng acid uric máu; buồn nôn; hạ huyết áp tư thế; lupus ban đỏ hệ thống; nặng lên chức năng thận |
| Bendroflumethiazide | 2,5 mg | 10 mg | 3–4 giờ | Giảm kali máu; giảm chlore máu; tăng đường huyết; tăng acid uric máu; buồn nôn; hạ huyết áp tư thế; lupus ban đỏ hệ thống; nặng lên chức năng thận |
| Indapamide | 2,5 mg | 5 mg | 14–24 giờ | Giảm kali máu; giảm chlore máu; tăng đường huyết; tăng acid uric máu; buồn nôn; hạ huyết áp tư thế; porphyria cấp; nặng lên chức năng thận |
| Metolazone | 2,5 mg | 20 mg | 6–20 giờ | Giảm kali máu; giảm chlore máu; tăng đường huyết; tăng acid uric máu; buồn nôn; hạ huyết áp tư thế; porphyria cấp; nặng lên chức năng thận |
| Chlorthalidone | 25 mg | 100 mg | 45–60 giờ | Giảm kali máu; giảm chlore máu; tăng đường huyết; tăng acid uric máu; buồn nôn; hạ huyết áp tư thế; nặng lên chức năng thận |
| Đối kháng thụ thể mineralocorticoid và thuốc giữ kali | ||||
| Spironolactone | 25 mg | 100 mg | Khoảng 90 phút | Tăng kali máu; nặng lên chức năng thận; vú to ở nam |
| Eplerenone | 25 mg | 50 mg | 3–6 giờ | Tăng kali máu; nặng lên chức năng thận; táo bón; phát ban |
| Amiloride | 5 mg | 20 mg | 6–9 giờ | Tăng kali máu; nặng lên chức năng thận; bệnh Addison; rụng tóc; thiếu máu; rối loạn tiêu hóa; đau |
| Triamterene | 150 mg | 250 mg | 2 giờ | Tiêu chảy; tăng kali máu; buồn nôn; khô miệng; nặng lên chức năng thận |
| Thuốc ức chế đồng vận chuyển natri–glucose 2 (SGLT2 inhibitors) | ||||
| Dapagliflozin | 10 mg | 10 mg | 13 giờ | Nhiễm toan ceton do đái tháo đường; nhiễm trùng đường tiểu; đái tháo đường type 1 |
| Empagliflozin | 10 mg | 10 mg | 12 giờ | Nhiễm toan ceton do đái tháo đường; nhiễm trùng đường tiểu; đái tháo đường type 1 |
| Các thuốc khác | ||||
| Acetazolamide | 250–375 mg | 500 mg | 2–5 giờ | Toan chuyển hóa; sỏi thận; dị cảm; rối loạn điện giải |
| Tolvaptan | 15 mg | 120 mg | 12 giờ | Giảm cảm giác thèm ăn; suy nhược; táo bón; mất nước; tiêu chảy; chóng mặt; rối loạn tiêu hóa; đau đầu; rối loạn gan; tăng đường huyết; tăng natri máu; tăng acid uric máu; mất ngủ; co thắt cơ; khát nhiều; phản ứng da |
11 Thuốc lợi tiểu trong suy tim
Lợi tiểu giúp giảm sung huyết bằng cách tạo cân bằng âm natri và nước. Mặc dù có ít thử nghiệm ngẫu nhiên đánh giá việc sử dụng lợi tiểu ở bệnh nhân HFrEF, hiệu quả của chúng đã được khẳng định rõ ràng. Đáng lưu ý, tất cả các thử nghiệm lớn về các liệu pháp điều trị thay đổi tiến triển bệnh (disease-modifying therapies) cho HFrEF đều được tiến hành trên nền tảng tỷ lệ sử dụng lợi tiểu quai rất cao, với 80–100% bệnh nhân được dùng lợi tiểu. Các thuốc lợi tiểu được sử dụng phổ biến nhất là lợi tiểu quai (ví dụ: Furosemide, torsemide và bumetanide), tác động lên quai Henle để thúc đẩy bài tiết natri. Bệnh nhân suy tim thường xuất hiện tình trạng kháng lợi tiểu, đòi hỏi bổ sung thêm các lợi tiểu khác để đạt được mức bài tiết natri và giảm sung huyết đầy đủ. Cách tiếp cận này, được gọi là phong tỏa tuần tự nephron (sequential nephron blockade), thường bao gồm phối hợp lợi tiểu quai với các thuốc tác động lên các đoạn nephron khác nhau. Các tác nhân này có thể bao gồm chất ức chế đồng vận chuyển natri–glucose type 2 (SGLT2-i) hoặc Acetazolamide tác động lên ống lượn gần; thiazide hoặc đối kháng thụ thể mineralocorticoid (MRA) tác động lên ống lượn xa; hoặc đối kháng thụ thể Vasopressin như tolvaptan, tác động lên ống góp để ức chế tác dụng của ADH.
Tuy nhiên, điều trị lợi tiểu có thể góp phần làm nặng chức năng thận và gây rối loạn điện giải, và các tác dụng phụ này trở nên trầm trọng hơn khi áp dụng phong tỏa tuần tự nephron. Tình trạng xấu đi chức năng thận - được định nghĩa là tăng creatinine huyết thanh trên 0,3 mg/dL (26,0 mmol/L) hoặc giảm >20% eGFR - là phổ biến. Tuy vậy, suy giảm chức năng thận này thường chỉ thoáng qua và chủ yếu do thay đổi huyết động hơn là tổn thương ống thận trực tiếp.
Trong thực hành lâm sàng, đặc biệt ở bệnh nhân HFrEF, khuyến cáo sử dụng liều lợi tiểu thấp nhất có hiệu quả để đạt được giảm sung huyết, nhằm hạn chế tối đa các tác dụng bất lợi.
12 Điều trị nội khoa cải thiện tiên lượng (disease-modiĩying therapy) dành cho tất cả bệnh nhân HfrEF
Trước kia, điều trị suy tim chủ yếu gồm chế độ ăn ít muối, digoxin và thuốc lợi tiểu. Bằng chứng đầu tiên về các thuốc có khả năng thay đổi tiến triển bệnh (disease-modifying drugs) xuất phát từ thử nghiệm Cooperative North Scandinavian Enalapril Survival Study (CONSENSƯS). Enalapril, một thuốc ức chế men chuyển angiotensin (ACE-i), giúp giảm khoảng 40% tủ’ vong do mọi nguyên nhân so với giả dược sau 6 tháng ở 253 bệnh nhân suy tim NYHA IV. Sau thử nghiệm CONSENSUS, các thử nghiệm lâm sàng khác tiếp tục chứng minh hiệu quả của các ACE- i khác ưong việc giảm tử vong ở bệnh nhân HFrEF (bảng 2). Mặc dù phần lớn các thử nghiệm HFrEF sử dụng enalapril, Ramipril cũng được kê đơn khá phổ biến, với liều mục tiêu 5 mg hai lần mỗi ngày, như trong thử nghiệm Acute Infarction Ramipril Efficacy ở bệnh nhân HFrEF sau nhồi máu cơ tim. Ở bệnh nhân không dung nạp ACE-i do ho hoặc phù mạch, thuốc chẹn thụ thể angiotensin (ARBs) là một lựa chọn hợp lý, mặc dù hiện nay việc sử dụng ARB đã trở nên hạn chế hơn do hiệu quả vượt trội của sacubitril-valsartan. Phối họp ACE-i và ARB không được khuyến cáo, vì không mang lại thêm lợi ích về biến cố tim mạch và làm tăng nguy cơ tác dụng bất lợi ở bệnh nhân suy tim. Chiến lược tăng cường phong tỏa hệ RAS thông qua ARB được nâng lên một bước nữa với sự phát triển của thuốc ức chế thụ thể angiotensin kết họp ức chế neprilysin (ARNI) Sacubitril-valsartan (kết hợp giữa ARB valsartan và chất ức chế neprilysin sacubitril) giúp ngăn cản sự phân hủy các hormone peptide lợi niệu có tác dụng điều hòa ngược có lợi. Trong thử nghiệm PARADIGM-HF (Prospective Comparison of ARNI with ACEi to Determine Impact on Global Mortality and Morbidity in Heart Failure), sacubitril-valsartan làm giảm 20% tử vong tim mạch hoặc nhập viện vì suy tim so với enalapril.
Với lợi ích tiên lượng rõ rệt này, tất cả các hướng dẫn quốc tế đều khuyến cáo khởi trị và tăng liều tối ưu thuốc ức chế RAS hoặc ARNI ở mọi bệnh nhân HFrEF còn triệu chứng dù đã điều trị bằng ACEi, nhằm giảm nguy cơ tử vong và nhập viện do suy tim. Cách tiếp cận theo từng bước này dựa trên thiết kế của thử nghiệm PARADIGM-HF, trong đó bệnh nhân HFrEF được ngẫu nhiên hoá chỉ sau khi dung nạp được enalapril trong giai đoạn run-in. Tuy nhiên, sacubitril- valsartan cũng có thể sử dụng cho bệnh nhân chưa từng dùng ACEi, dựa trên các nghiên cứu nhỏ hơn ủng hộ việc dùng thuốc ở nhóm này.
Phong tỏa hệ thần kinh giao cảm bằng thuốc chẹn 0-adrenoreceptor (beta-blockers), vốn ban đầu dùng trong điều trị đau thắt ngực, từng bị chống chỉ định ở bệnh nhân suy tim do lo ngại tác dụng inotropic âm. Tuy nhiên, từ cuối những năm 1990, nhiều thử nghiệm lâm sàng đã chứng minh hiệu quả của beta-blockers ở bệnh nhân suy tim triệu chứng mức độ trung bình. Trong thử nghiệm CIBIS-II, điều trị bằng Bisoprolol với liều mục tiêu 10 mg/ngày giúp giảm 44% tử vong và giảm nguy cơ tử vong đột ngột so với giả dược. Tương tự, trong thử nghiệm MERIT-HF, Metoprolol giúp giảm 44% tử vong do mọi nguyên nhân trong 1 năm so với giả dược.
Aldosterone đóng vai trò quan trọng trong sinh lý bệnh của suy tim. Thử nghiệm Randomized Aldactone Evaluation Study chứng minh Spironolactone - một thuốc đối kháng thụ thể mineralocorticoid (MRA) không chọn lọc - giảm 30% tử vong mọi nguyên nhân so với giả dược ở bệnh nhân HFrEF. Tương tự, eplerenone làm giảm nguy cơ tử vong mọi nguyên nhân so với giả dược trong các thử nghiệm EPHESUS52 và EMPHASIS-HF. Mặc dù hai thuốc có hiệu quả tương đương ở bệnh nhân HFrEF, eplerenone có thể được ưu tiên dùng để giảm nguy cơ tác dụng phụ liên quan hormone sinh dục của spironolactone như chứng vú to ở nam.
SGLT2-i được khuyến cáo là một phần của điều trị nội khoa tối ưu cho bệnh nhân HFrEF. Điều trị bằng SGLT2-i giúp cải thiện tiên lượng, giảm nhập viện và cải thiện chất lượng cuộc sống so với giả dược.
Điều trị suy tim hướng đến cải thiện tiên lượng, nâng cao chất lượng cuộc sống và giảm nhập viện. Ở bệnh nhân nhập viện vì suy tim, chiến lược tăng liều nhanh và tối ưu hóa điều trị nội khoa có liên quan với giảm nguy cơ tử vong mọi nguyên nhân hoặc tái nhập viện vì suy tim. Bất kể thứ tự khởi trị GDMT, tất cả bệnh nhân HfrEF nên được khởi trị sớm với bốn trụ cột điều trị (four pillars of therapy), và các thuốc này cần được tăng liều đến mức dung nạp tối đa càng sớm càng tốt.
13 Điều trị nội khoa dành cho các bệnh nhân HFrEF được lựa chọn
Ở những bệnh nhân HFrEF vẫn còn triệu chứng dù đã được điều trị đầy đủ với bốn trụ cột điều trị cơ bản, có thể cân nhắc thêm các lựa chọn điều trị nội khoa khác.
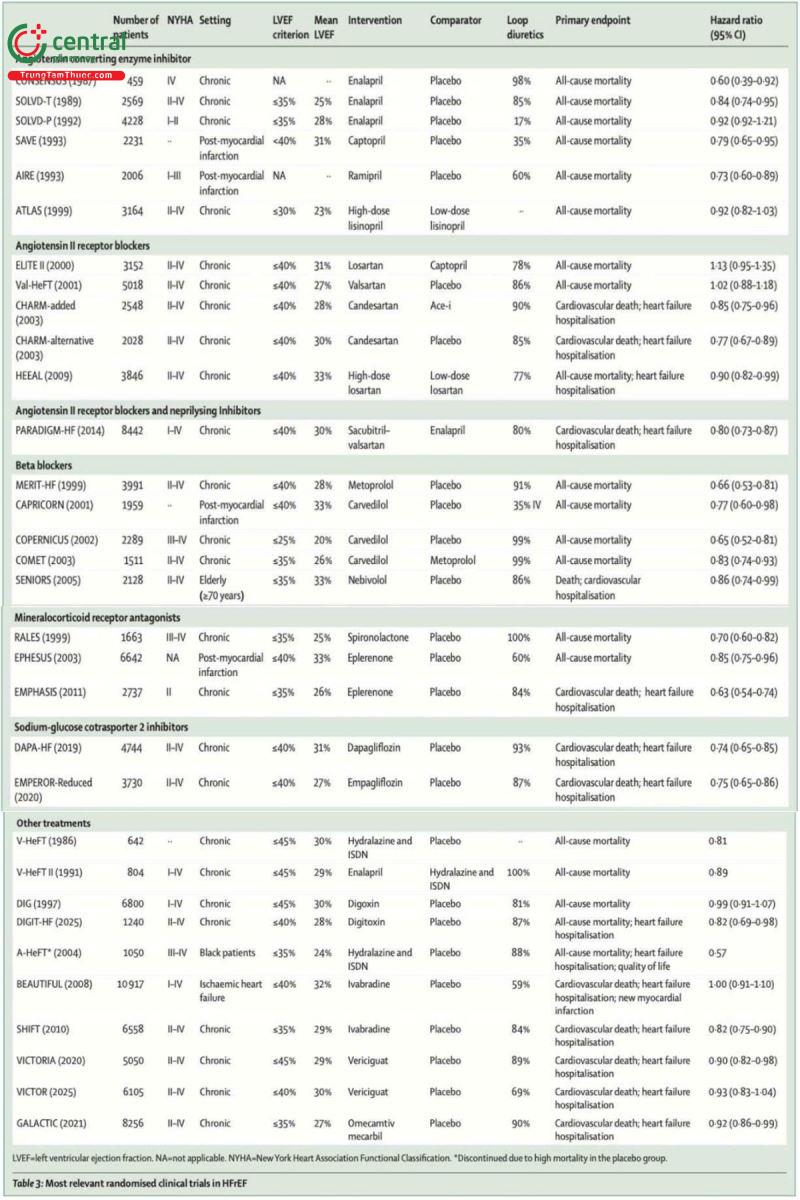
Ivabradine, một thuốc ức chế chọn lọc nút xoang giúp giảm nhịp tim ở bệnh nhân có nhịp xoang, có thể được cân nhắc ở bệnh nhân HFrEF vẫn còn triệu chứng dù đã dùng liều tối đa dung nạp của thuốc chẹn beta, và có nhịp tim lúc nghỉ >70 lần/phút. Mặc dù Ivabradine cho thấy lợi ích ở một số bệnh nhân HFrEF, hiệu quả của thuốc thay đổi tùy theo đặc điểm quần thể bệnh nhân và thiết kế các thử nghiệm (bảng 3).
Vericiguat, một thuốc kích thích guanylate cyclase hòa tan, cũng có thể được cân nhắc cho bệnh nhân HFrEF còn triệu chứng dù đã điều trị GDMT. Thử nghiệm VICTORIA cho thấy vericiguat làm giảm nhập viện vì suy tim so với giả dược. Tuy nhiên, thử nghiệm VICTOR - tiến hành trên các bệnh nhân ngoại trú HFrEF ổn định - không đạt tiêu chí chính gộp của tử vong tim mạch hoặc nhập viện vì suy tim, nhưng lại cho thấy giảm tử vong tim mạch và tử vong mọi nguyên nhân. Do đó, vericiguat có thể sử dụng cho một nhóm bệnh nhân được lựa chọn kỹ, còn triệu chứng dù đã tối ưu GDMT.
Ở bệnh nhân da Đen tự nhận, mắc HFrEF có triệu chứng dù đã điều trị GDMT hoặc không dung nạp ACE-i/ARB, có thể cân nhắc phối hợp hydralazine và isosorbide dinitrate để giảm tử vong và nhập viện vì suy tim. Tuy nhiên, phác đồ này nhìn chung chỉ dành cho bệnh nhân không thể dùng ACE-i hoặc ARNI do suy thận, hoặc các bệnh nhân da Đen.
Digoxin từng là trụ cột điều trị suy tim trong lịch sử. Tuy nhiên, qua thời gian, việc sử dụng digoxin giảm dần do thiếu bằng chứng về lợi ích rõ rệt đối với tiên lượng ở bệnh nhân HFrEF. Trong thử nghiệm DIG (Digitalis Investigators Group), digoxin giúp giảm nhập viện vì suy tim ở bệnh nhân HFrEF có nhịp xoang, nhưng không cải thiện tỷ lệ tử vong. Do khoảng điều trị hẹp và nguy cơ độc tính, đặc biệt ở bệnh nhân nhịp xoang, việc sử dụng digoxin cần thận trọng.
Tuy nhiên, thử nghiệm DIGIT-HF gần đây với digitoxin cho thấy giảm 18% biến cố gộp gồm tử vong mọi nguyên nhân và nhập viện vì suy tim ở bệnh nhân HFrEF có cả nhịp xoang và rung nhĩ, vốn đã được điều trị tốt bằng GDMT hiện đại. Không ghi nhận tăng tử vong. Kết quả DIGIT- HF có thể mở đường cho sự “hồi sinh” của nhóm digitalis ở HFrEF còn triệu chứng dù đã điều trị tối ưu. Mặc dù cùng nhóm glycoside trợ tim, digitoxin có thời gian bán hủy dài hơn, được thải trừ qua gan, và không tích tụ trong suy thận. Dự kiến sẽ có thêm bằng chứng về hiệu quả của digoxin với kết quả thử nghiệm DECISION sắp tới.
Omecamtiv mecarbil, một chất hoạt hóa myosin tim chọn lọc, dù chưa được phê duyệt chính thức cho HFrEF, đã cho thấy giảm tiêu chí chính gồm tử vong tim mạch hoặc biến cố suy tim trong thử nghiệm GALACTIC-HF; tuy nhiên, không ghi nhận giảm tử vong tim mạch hoặc tử vong mọi nguyên nhân. Thử nghiệm COMET-HF (NCT06736574) hiện đang tiến hành để xác nhận.
Việc bàn luận chi tiết hơn về điều trị nội khoa hoặc can thiệp cho các tình trạng tim mạch quan trọng xảy ra đồng thời với HFrEF - như rung nhĩ hoặc bệnh van tim - vượt ra ngoài phạm vi bài tổng quan này. Tuy nhiên, triệt đốt rung nhĩ và sửa van qua da mang lại lợi ích ở các bệnh nhân HFrEF có triệu chứng được lựa chọn.
Liệu pháp thiết bị (device therapy) cũng đóng vai trò quan trọng. Máy khử rung tự động (ICD) được chỉ định ở bệnh nhân bệnh tim thiếu máu cục bộ có LVEF <35% dù đã điều trị GDMT, nhằm dự phòng tử vong đột ngột, và có thể cân nhắc ở bệnh nhân không do thiếu máu cục bộ nếu LVEF <35%.4 Ở bệnh nhân HFrEF có triệu chứng và có rối loạn dẫn truyền trên ECG (QRS >130 ms) hoặc cần tạo nhịp thất phải lâu dài, liệu pháp tái đồng bộ tim (CRT), có hoặc không kèm ICD, cũng được chỉ định.
14 Điều trị HfmrEF
Điều trị tối ưu cho HFmrEF vẫn chưa rõ ràng do bằng chứng hiện có còn hạn chế. Không có thử nghiệm ngẫu nhiên lớn nào đặc biệt thiết kế cho HFmrEF, phần lớn dữ liệu đến từ các phân tích dưới nhóm của các thử nghiệm HFpEF - vốn nhiều nghiên cứu có kết quả trung tính. Do đó, điều trị HFmrEF thường dựa trên bằng chứng của HFrEF hoặc HFpEF. Hầu hết các thử nghiệm HFpEF sử dụng ngưỡng LVEF >40% hoặc >45%, bao gồm cả bệnh nhân HFmrEF. Ngày nay, HFmrEF được xem là giống với HFrEF về dịch tễ học và đáp ứng với điều trị nội khoa. Mặc dù không có thử nghiệm riêng cho ACE-i trong HFmrEF, phân tích thứ cấp từ chương trình CHARM và PARAGON-HF cho thấy RAS-i và ARNI có thể hiệu quả, đặc biệt ở nhóm có LVEF gần giới hạn thấp của phổ HFmrEF.
Beta-blockers cũng có thể được cân nhắc ở bệnh nhân HFmrEF. Nhiều phân tích gộp đã gợi ý rằng lợi ích của beta-blocker quan sát được ở HFrEF có thể mở rộng sang HFmrEF.71-76 Do đó, beta-blockers được khuyến cáo để giảm nguy cơ từ vong hoặc nhập viện vì suy tim ở cả HFrEF và HFmrEF.
Ngoài ra, các phân tích gộp từ hai chương trình Deliver và DAPA-HF, cũng như chương trình EMPEROR, cho thấy hiệu quả của thuốc ức chế SGLT2 (SGLT2-i) là nhất quán trên toàn bộ phổ phân suất tống máu (LVEF).
Bằng chứng cho thấy việc sử dụng MRA mang lại lợi ích ở bệnh nhân HfìnrEF. Mặc dù thử nghiệm TOPCAT (Treatment of Preserved Cardiac Function Heart Failure with an Aldosterone Antagonist) không chứng minh được giảm tiêu chí chính bao gồm tử vong tim mạch, ngừng tim hồi phục hoặc nhập viện vì suy tim khi so sánh spironolactone với giả dược ở bệnh nhân suy tim với LVEF >45%, phân tích hậu định (post-hoc) cho thấy hiệu quả cao hơn của spironolactone ở nhóm bệnh nhân có LVEF thấp hơn trong phổ này (p = 0,046). Thử nghiệm FINEARTS-HF gần đây cho thấy fmerenone cải thiện nguy cơ tử vong tim mạch hoặc tổng số biến cố suy tim ở bệnh nhân HFpEF và HFmrEF. Phân tích định trước xác nhận hiệu quả điều trị ổn định trên toàn phổ LVEF(HR 0,84; KTC 95%: 0,68-1,03 cho LVEF <50%; p tương tác = 0,70).
Do đó, ở bệnh nhân HFmrEF, các hướng dẫn quốc tế khuyến nghị: Thuốc lợi tiểu để giảm triệu chứng và dấu hiệu sung huyết, SGLT2-i để giảm nguy cơ nhập viện vì suy tim, Có thể cân nhắc sử dụng RAS-i/ARNI, chẹn p, và MRA, tương tự như điều trị HFrEF.
Với các đặc điểm lâm sàng tương đồng và đáp ứng điều trị gần giống, HFmrEF có thể được gộp vào nhóm HFrEF trong tương lai, với ngưỡng LVEF cao hơn để xác định suy chức năng tâm thu. Điều này có thể dẫn đến phân loại lại các kiểu hình suy tim, với HFrEF đại diện cho suy tim với giảm EF và một nhóm mới HFnEF (Heart Failure with normal EF)với ngưỡng LVEF khoảng 50%, giúp phân định chiến lược điều trị tốt hơn.
15 Điều trị đặc hiệu các bệnh đồng mắc, căn nguyên HFrEF và tác dụng phụ của GDMT
15.1 Thiếu sắt
Thiếu Sắt được định nghĩa là íerritin <100 ng/mL hoặc íerritin 100-299 ng/mL kèm độ bão hòa transíerrin <20%, là bệnh đồng mắc phổ biến ở bệnh nhân HFrEF.
Ảnh hưởng khoảng 40% bệnh nhân suy tim mạn. Tăng nguy cơ tử vong, nhập viện, giảm chất lượng sống và khả năng gắng sức, không phụ thuộc có thiếu máu hay không
Các thử nghiệm ngẫu nhiên và phân tích gộp cho thấy: sắt tĩnh mạch (ferric carboxymaltose hoặc ferric derisomaltose) giảm tiêu chí chính gộp tử vong tim mạch hoặc nhập viện suy tim tái phát (RR 0,75; KTC 95%: 0,61-0,93; p <0,01) Hiệu quả chính nằm ở giảm nhập viện vì suy tim, Không giảm tử vong tim mạch hay tử vong mọi nguyên nhân trong 1 năm.
Hiện nay, sắt tĩnh mạch dùng để cải thiện triệu chứng ở bệnh nhân HFrEF và HFmrEF còn triệu chứng dù đã tối ưu GDMT.
15.2 Bệnh thận mạn (CKD)
CKD (eGFR <60 mL/ph/1,73 m2) ảnh hưởng khoảng 30% bệnh nhân HFrEF và làm tiên lượng xấu hơn. Suy thận là trở ngại trong tối ưu GDMT do thuốc kháng thần kinh-hormone có thể làm giảm eGFR. Giảm eGFR nhẹ (<30% so với nền) sau khi dùng ACEi/ARB/ARNI thường được xem là chấp nhận được và có thể là giả giảm chức năng thận (pseudo-worsening). Không nên ngừng GDMT trừ khi suy thận tiến triển thực sự.
Lợi ích của GDMT thường vượt trội rủi ro ở bệnh nhân HFrEF có CKD.
15.3 Tãng kali máu
Tăng kali là tác dụng phụ thường gặp của RASi và MRA, có thể hạn chế khởi trị hoặc chỉnh liều. Cần điều chỉnh GDMT để đưa kali về bình thường. Nếu tăng kali dai dẳng (đã loại trừ nguyên nhân ngoại sinh), có thể dùng chất gắn kali: Patữomer, Sodium zirconium cyclosilicate (SZC) nhằm giảm kali và cho phép tiếp tục/up-titration GDMT.
Hạ kali máu
Hạ kali cũng nguy hiểm không kém tăng kali. Thường do lợi tiểu quai và thiazide —> tăng thải kali Liên quan tăng nguy cơ: loạn nhịp thất, đột tử, giảm hiệu quả digoxin. Có thể đối kháng tác dụng giữ kali của RASi và MRA. Thử nghiệm POTCAST (bệnh nhân có ICD, ~2/3 suy tim) cho thấy: Các nghiên cứu cho thấy rằng duy trì nồng độ kali mục tiêu từ 4,5-5 mmol/L giúp giảm đáng kể nguy cơ: nhịp nhanh thất bền bỉ hoặc sốc điện thích hợp từ ICD, Nhập viện không theo kế hoạch do rối loạn nhịp hoặc suy tim, Tử vong do mọi nguyên nhân, so với chăm sóc tiêu chuẩn. Kết quả này nhấn mạnh tầm quan trọng của việc duy trì nồng độ kali huyết thanh đầy đủ, đặc biệt ở những bệnh nhân đang điều trị bằng thuốc lợi tiểu.
Hạ huyết áp, thường gặp ở bệnh nhân HFrEF, là một trong những rào cản chính đối với việc triển khai đầy đủ GDMT và có thể dẫn đến ngừng điều trị.99 Nhiều liệu pháp điều trị suy tim làm giảm huyết áp như một tác dụng chính. Nếu bệnh nhân không có triệu chứng, có thể tiếp tục GDMT, trừ khi huyết áp tâm thu giảm nặng (tức <80 mmHg).
Hạ huyết áp có triệu chứng hoặc hạ huyết áp tư thế có thể được xử trí bảo tồn thông qua tư vấn và giáo dục bệnh nhân, không nhất thiết phải giảm liều hoặc ngừng GDMT. Việc quản lý bệnh nhân HFrEF có hạ huyết áp nên dựa vào đánh giá lâm sàng của bác sĩ.
15.4 Nhịp chậm
Nhịp chậm cũng là một tác dụng phụ có thể gặp, chủ yếu do thuốc chẹn beta. Giảm liều thuốc chẹn p có thể cần thiết ở bệnh nhân có nhịp tim <50 bpm hoặc có triệu chứng do nhịp chậm.
Bệnh nhân suy tim cần được đánh giá kỹ lưỡng để tìm các dấu hiệu hoặc triệu chứng gợi ý bệnh động mạch vành. Việc đánh giá bao gồm khai thác bệnh sử cá nhân và gia đình, khám lâm sàng, ECG và các xét nghiệm hình ảnh phù hợp. Việc xác định thiếu máu cơ tim ở bệnh nhân suy tim có thể khó khăn do khả năng gắng sức thấp và tăng áp lực cuối tâm trương thất trái, làm giảm độ nhạy của một số nghiệm pháp gắng sức. Trong những trường hợp này, chụp động mạch vành hoặc chụp CT mạch vành có thể được xem xét nhằm đánh giá giải phẫu mạch vành và xác định hoặc loại trừ bệnh động mạch vành tắc nghẽn.
Ớ những bệnh nhân HFrEF do bệnh tim thiếu máu cục bộ, tái thông mạch vành - dù bằng can thiệp qua da hay phẫu thuật - không vượt trội hơn điều trị nội khoa trong việc giảm nguy cơ tử vong hoặc nhập viện.101 >102 Do đó, các can thiệp xâm lấn không nên được ưu tiên so với điều trị nội khoa, và điều trị nội khoa nên được xem như liệu pháp hàng đầu ở bệnh nhân HFrEF ổn định
.jpg)
HFrEF = suy tim với phân suất tống máu giảm.
16 Tỷ lệ tử vong của HFrEF và HFmrEF
Suy tim có tỷ lệ tử vong cao: khoảng 9% bệnh nhân tử vong trong thời gian nằm viện, 30% tử vong trong vòng 1 năm kể từ khi nhập viện, và lên đến 50% tử vong trong vòng 5 năm. Các liệu pháp điều trị nội khoa và thiết bị dựa trên bằng chứng đã giúp giảm đáng kể tỷ lệ mắc bệnh và tử vong ở bệnh nhân HFrEF. GDMT hiện đại có thể tăng tuổi thọ của bệnh nhân lên gấp ba lần, với mức tăng ròng 8 năm sống thêm so với điều trị thông thường. Những tiến bộ này góp phần làm giảm đáng kể tỷ lệ tử vong trong 1 năm ở châu Âu ở bệnh nhân HFrEF, từ 20% năm 2000 xuống còn 11% năm 2022 (mức thay đổi phần trăm hằng năm -2,6%; KTC 95% -3,9 đến -1,1; p<0,001).
Ở bệnh nhân HFrEF mạn tính, tỷ lệ tử vong 1 năm khoảng 9%. Tuy nhiên, bệnh nhân HFrEF vẫn có nguy cơ cao xảy ra biến cố bất lợi, đặc biệt sau khi nhập viện do đợt cấp suy tim. Tại Vương quốc Anh, tỷ lệ tử vong trong 1 năm sau nhập viện ở bệnh nhân HFrEF đã giảm từ khoảng 35% (2018-19)xuống 29% (2021-22) (HR 0,87; KTC 95% 0,85-0,89; p<0,001).
17 Các chỉ số chất lượng chăm sóc và vai trò của chuyên khoa suy tim
Nhiều chỉ số chất lượng chăm sóc đã được thiết lập để đánh giá hiệu quả quản lý bệnh nhân suy tim. NICE (Vương quốc Anh) và ESC xác định năm lĩnh vực cốt lõi trong chăm sóc suy tim, gồm: Chất lượng cấu trúc hệ thống chăm sóc, Đánh giá bệnh nhân, Điều trị dược lý ban đầu, Tối ưu hóa điều trị, Chất lượng cuộc sống
Những chỉ số này hữu ích trong việc theo dõi chất lượng chăm sóc dành cho bệnh nhân HFrEF. Việc chăm sóc suy tim cần được triển khai theo mô hình đa chuyên khoa, cả trong bệnh viện và ngoài cộng đồng. Các đội chuyên trách suy tim bao gồm bác sĩ chuyên khoa suy tim, điều dưỡng chuyên ngành suy tim và dược sĩ lâm sàng. Chăm sóc bởi chuyên gia suy tim giúp: cải thiện việc triển khai điều trị nội khoa, giảm nhu cầu dùng thuốc lợi tiểu khi xuất viện ở bệnh nhân suy tim trên toàn phổ LVEF.
Do đó, bệnh nhân được chăm sóc bởi chuyến gia suy tim có kết cục lâu dài tốt hơn. Thêm vào đó, theo dõi tại phòng khám do điều dưỡng dẫn dắt liên quan độc lập với giảm nguy cơ tử vong ở bệnh nhân suy tim.
18 Triển vọng tương lai
Mặc dù đã đạt được nhiều tiến bộ trong điều trị bệnh nhân suy tim, đặc biệt là HFrEF (hình 2), một tỷ lệ đáng kể bệnh nhân vẫn có nguy cơ cao gặp các biến cố tim mạch bất lợi. Nguy cơ này cao hơn so với nhiều bệnh lý tim mạch khác hoặc so với người không mắc suy tim (phụ lục trang l). Bất chấp nhiều nỗ lực, việc triển khai GDMT trong thực hành lâm sàng vẫn chưa tối ưu. Việc xác định các rào cản đối với việc triển khai GDMT, giảm sự trì hoãn lâm sàng, và cải thiện tuân thủ cũng như khả năng tiếp cận chăm sóc có thể mang lại lợi ích tiên lượng đáng kể cho bệnh nhân HFrEF. Bằng chứng hiện nay cho cách tiếp cận điều trị tổng quát đối với bệnh nhân HFrEF chủ yếu đến từ các thử nghiệm lâm sàng ngẫu nhiên quy mô lớn, vốn phức tạp và tốn kém. Cách tiếp cận này đã góp phần làm giảm đáng kể tỷ lệ tử vong theo thời gian (hình 2). Tuy nhiên, các thiết kế thử nghiệm truyền thống dựa trên các tiêu chí tử vong hoặc nhập viện có thể không còn đủ để chứng minh thêm sự giảm rõ rệt về các biến cố suy tim kinh điển. Do đó, các thiết kế thử nghiệm mới, như umbrella trials, basket trials và plattồrm trials, mang lại hướng tiếp cận đầy hứa hẹn nhằm nghiên cứu nhóm bệnh nhân suy tim gần với thực tế hơn và phát hiện thêm các phương pháp điều trị hiệu quả. Những thiết kế này cho phép đánh giá nhiều can thiệp đồng thời trong cùng quần thể bệnh nhân suy tim, đồng thời phân tầng bệnh nhân dựa trên các dấu ấn sinh học hoặc đặc điểm lâm sàng cụ thể. Nhờ vậy, có thể xác định phương pháp điều trị mới hiệu quả hơn và ít tốn kém hơn. Trong kỷ nguyên y học chính xác, việc quản lý suy tim cần được cá thể hóa dựa trên đặc điểm cụ thể của từng bệnh nhân, thông qua các đội chuyên trách suy tim. Việc định kiểu sâu hơn (deep phenotyping), gồm phân tích nguyên nhân bằng di truyền học và các phương pháp multiomics, có thể giúp xác định nhóm bệnh nhân hưởng lợi từ các liệu pháp đích. Tái định vị thuốc (drug repurposing), chẳng hạn như các thuốc kháng viêm, kháng thể đơn dòng hoặc các phân tử nhỏ tác động lên các đường chuyển hóa tim mạch, cũng mở ra những hướng điều trị mới. Bên cạnh đó, lĩnh vực miễn dịch học tim mạch (cardioimmunology) - nghiên cứu sự tương tác giữa hệ miễn dịch và bệnh lý tim mạch - đang nổi lên như một triển vọng hứa hẹn trong việc tìm kiếm các mục tiêu điều trị mới. Việc tích hợp multiomics với điểm nguy cơ đa gen (polygenic risk scores) cũng có thể mở rộng hướng nghiên cứu trong HFrEF. Liệu pháp gen mang lại cơ hội phát triển các phương pháp điều trị mới nhằm giảm tỷ lệ mắc bệnh và tử vong trong suy tim. Trí tuệ nhân tạo (AI) là lĩnh vực đang phát triển nhanh chóng và có tiềm năng đóng vai trò then chốt trong y học. Các công cụ AI có thể hỗ trợ chẩn đoán HFrEF thông qua phân tích nâng cao hình ảnh, dấu ấn sinh học và dữ liệu lâm sàng, đồng thời cải thiện chẩn đoán sớm, tinh chỉnh phân tầng bệnh nhân, và hồ trợ cá thể hóa điều trị
19 Kết luận
Suy tim vẫn là một trong những nguyên nhân hàng đầu gây bệnh tật và tử vong trên toàn thế giới. Các liệu pháp GDMT hiện nay đã cải thiện đáng kể tuổi thọ và chất lượng cuộc sống của bệnh nhân. Điều trị tối ưu cần bao gồm khởi trị và tăng liều nhanh bốn nhóm thuốc nền tảng (RAS-i hoặc ARNI, thuốc chẹn p, MRA và SGLT2-Ĩ) kết hợp với thuốc lợi tiểu nhằm kiểm soát ứ dịch. Trong tương lai, cách tiếp cận cá thể hóa trong chẩn đoán và điều trị sẽ tiếp tục thúc đẩy các tiến bộ mới, cải thiện cả chất lượng và thời gian sống cùa bệnh nhân HFrEF trên toàn cầu.