Quản lý xuất huyết tiêu hóa trên theo hướng dẫn của ACG 2021
Bản dịch: QUẢN LÝ XUẤT HUYẾT TIÊU HÓA TRÊN THEO ACG 2021 - Được dịch bởi NT HN
Đề xuất đánh giá nguy cơ tại khoa cấp cứu để xác định những bệnh nhân nguy cơ rất thấp (ví dụ: điểm Glasgow-Blatchford 0-1) có thể được cho xuất viện và theo dõi ngoại trú. Đối với bệnh nhân nhập viện vì xuất huyết tiêu hóa trên, chúng tôi đề xuất truyền hồng cầu khi ngưỡng hemoglobin là 7 g/dL. Khuyến cáo truyền erythromycin trước khi nội soi, và nên thực hiện nội soi trong vòng 24 giờ sau khi nhập viện. Điều trị nội soi được khuyến cáo đối với các ổ loét đang chảy máu thành tia hoặc rỉ máu, cũng như các mạch máu lộ không chảy máu. Sau khi cầm máu qua nội soi, khuyến cáo sử dụng thuốc PPI liều cao, truyền liên tục hoặc ngắt quãng trong 3 ngày, sau đó dùng thuốc PPI đường uống 2 lần trong 2 tuần đầu sau nội soi. Nên nội soi lại nếu chảy máu tái phát, và nếu điều trị nội soi thất bại, khuyến cáo thuyên tắc mạch qua catheter.
1 DANH SÁCH CÁC KHUYẾN CÁO TRONG HƯỚNG DẪN
Phân tầng nguy cơ
1. Chúng tôi đề xuất rằng những bệnh nhân đến khoa cấp cứu với xuất huyết tiêu hóa trên (UGIB) được phân loại nguy cơ rất thấp – được định nghĩa là có điểm đánh giá nguy cơ với tỷ lệ âm tính giả ≤ 1% đối với kết cục cần can thiệp tại bệnh viện hoặc tử vong (ví dụ: điểm Glasgow-Blatchford 0-1) – có thể được cho xuất viện và theo dõi ngoại trú thay vì nhập viện (chất lượng bằng chứng rất thấp).
Truyền hồng cầu
2. Chúng tôi đề xuất chiến lược truyền hồng cầu hạn chế, với ngưỡng truyền khi hemoglobin là 7 g/dL ở bệnh nhân xuất huyết tiêu hóa trên (chất lượng bằng chứng thấp).
Điều trị nội khoa trước nội soi
3. Chúng tôi đề xuất truyền erythromycin trước khi nội soi ở bệnh nhân UGIB (chất lượng bằng chứng rất thấp).
4. Chúng tôi chưa thể đưa ra khuyến cáo ủng hộ hay phản đối việc sử dụng PPI trước nội soi ở bệnh nhân UGIB.
Nội soi trong xuất huyết tiêu hóa trên
5. Chúng tôi đề xuất rằng những bệnh nhân nhập viện hoặc đang được theo dõi tại bệnh viện vì UGIB nên được nội soi trong vòng 24 giờ kể từ khi nhập viện (chất lượng bằng chứng rất thấp).
6. Chúng tôi khuyến cáo điều trị nội soi ở bệnh nhân UGIB do loét có chảy máu thành tia, chảy máu rỉ rả, hoặc có mạch máu lộ không chảy máu (khuyến cáo mạnh, chất lượng bằng chứng trung bình).7. Chúng tôi chưa đưa ra khuyến cáo ủng hộ hay phản đối điều trị nội
soi ở bệnh nhân UGIB do loét có cục máu đông bám dính.
8. Chúng tôi khuyến cáo điều trị cầm máu nội soi bằng đốt điện, đầu dò nhiệt, hoặc tiêm Ethanol cho bệnh nhân UGIB do loét (khuyến cáo mạnh, chất lượng bằng chứng trung bình).
9. Chúng tôi đề xuất điều trị cầm máu nội soi bằng clips, argon, hoặc đốt điện đơn cực cho bệnh nhân UGIB do loét (chất lượng bằng chứng từ rất thấp đến thấp).
10. Chúng tôi khuyến cáo không sử dụng epinephrine đơn độc cho bệnh nhân UGIB do loét, mà nên phối hợp với một phương pháp cầm máu khác (khuyến cáo mạnh, chất lượng bằng chứng từ rất thấp đến trung bình).
11. Chúng tôi đề xuất điều trị cầm máu nội soi bằng bột cầm máu TC-325 cho bệnh nhân có loét đang chảy máu (chất lượng bằng chứng rất thấp).
12. Chúng tôi đề xuất sử dụng clip over-the-scope như một phương pháp cầm máu cho bệnh nhân bị chảy máu do loét tái phát sau khi đã cầm máu nội soi thành công trước đó (chất lượng bằng chứng thấp).
Điều trị ức chế tiết acid sau cầm máu nội soi trong loét chảy máu
13. Chúng tôi khuyến cáo sử dụng PPI liều cao, truyền liên tục hoặc ngắt quãng trong 3 ngày sau khi đã cầm máu nội soi thành công cho loét chảy máu (khuyến cáo mạnh, chất lượng bằng chứng từ trung bình đến cao).
14. Chúng tôi đề xuất rằng những bệnh nhân nguy cơ cao bị UGIB do loét, sau khi đã cầm máu nội soi và điều trị PPI liều cao ngắn hạn tại bệnh viện, nên tiếp tục dùng PPI đường uống ngày 2 lần cho đến 2 tuần sau lần nội soi ban đầu (chất lượng bằng chứng thấp).
Chảy máu ổ loét tái phát sau khi đã cầm máu nội soi thành công
15. Chúng tôi đề xuất rằng những bệnh nhân bị chảy máu tái phát sau điều trị nội soi cho loét chảy máu nên được nội soi lại và tiếp tục điều trị nội soi, thay vì phẫu thuật hoặc thuyên tắc động mạch qua catheter.
Thất bại của điều trị cầm máu nội soi đối với loét chảy máu
16. Chúng tôi đề xuất rằng những bệnh nhân loét chảy máu không đáp ứng với điều trị nội soi nên được điều trị tiếp theo bằng thuyên tắc động mạch qua catheter (chất lượng bằng chứng rất thấp).
2 TỔNG QUAN
| Các yếu tố nguy cơ | Điểm |
|---|---|
| BUN (mg/dL) | |
| 18.2 đến < 22.4 | 2 |
| 22.4 đến < 28 | 3 |
| 28 đến < 70 | 4 |
| ≥ 70 | 6 |
| Hemoglobin (g/dL) | |
| 12 đến < 13 (nam); 10 đến < 12 (nữ) | 1 |
| 10 đến < 12 (nam) | 3 |
| < 10 | 6 |
| Huyết áp tâm thu (mmHg) | |
| 100 - 109 | 1 |
| 90 - 99 | 2 |
| < 90 | 3 |
| Nhịp tim (lần/phút) | |
| ≥ 100 | 1 |
Bệnh lý gan và suy tim không nằm trong thang điểm gốc của Glasgow-Blatchford. Một nghiên cứu gần đây định nghĩa bệnh lý gan đã biết, hoặc bằng chứng lâm sàng và cận lâm sàng bệnh gan mạn tính hoặc cấp tính, hoặc lâm sàng và bằng chứng siêu âm tim của suy tim. | |
2.1 Phân tầng nguy cơ
2.1.1 Chúng tôi đề xuất rằng những bệnh nhân đến khoa cấp cứu với xuất huyết tiêu hóa trên (UGIB) được phân loại nguy cơ rất thấp – được định nghĩa là có điểm đánh giá nguy cơ với tỷ lệ âm tính giả ≤ 1% đối với kết cục cần can thiệp tại bệnh viện hoặc tử vong (ví dụ: điểm Glasgow-Blatchford 0-1) – có thể được cho xuất viện và theo dõi ngoại trú thay vì nhập viện (chất lượng bằng chứng rất thấp).
2.1.1.1 Tóm tắt bằng chứng
Mục tiêu của việc xác định nhóm bệnh nhân nguy cơ rất thấp là cho phép một số bệnh nhân có thể được xuất viện an toàn từ khoa cấp cứu và theo dõi ngoại trú, qua đó giảm chi phí với rất ít hoặc hầu như không có nguy cơ xảy ra các kết cục xấu cần can thiệp hoặc lẽ ra có thể phòng tránh nếu được điều trị nội trú. Do đó, lợi ích chính của khuyến cáo này mang tính kinh tế nhờ giảm số ca nhập viện.
Các kết cục gộp thường được sử dụng trong các nghiên cứu về thang điểm đánh giá nguy cơ. Chúng tôi chủ yếu dựa vào các kết cục gộp như được định nghĩa trong các nghiên cứu đã được xem xét, vì chúng được xem là phù hợp hơn so với các kết cục đơn lẻ như tái xuất huyết hoặc tử vong khi xác định bệnh nhân nguy cơ rất thấp. Kết cục gộp trong 4 nghiên cứu riêng lẻ mà chúng tôi đánh giá bao gồm các can thiệp tại bệnh viện cho vấn đề xuất huyết (truyền máu và các biện pháp cầm máu) và tử vong, trong khi tổng quan hệ thống các nghiên cứu khác còn bao gồm thêm tình trạng tái xuất huyết dẫn đến tái nhập viện trong kết cục gộp.
Đạt được độ nhạy cao - nhằm giảm thiểu các trường hợp âm tính giả - là yếu tố then chốt khi đưa ra quyết định về quản lý ngoại trú. Âm tính giả xảy ra khi những bệnh nhân thực sự cần can thiệp hoặc có nguy cơ tử vong lại bị phân loại sai bằng công cụ đánh giá nguy cơ là không cần can thiệp hoặc không có nguy cơ tử vong. Điều này có thể dẫn đến việc cho xuất viện những bệnh nhân đáng lẽ cần can thiệp hoặc có thể tử vong. Mục tiêu lý tưởng là không có trường hợp âm tính giả (độ nhạy 100%), nhưng bác sĩ và bệnh nhân có thể cân nhắc mức độ chắc chắn cần thiết để cảm thấy an tâm khi quyết định cho xuất viện từ khoa cấp cứu.
Bệnh nhân có điểm Glasgow-Blatchford bằng 0 có ước tính độ nhạy từ 99%-100%, với giới hạn dưới của khoảng tin cậy 95% là 98%, mặc dù độ đặc hiệu thấp với các ước tính chỉ từ 8% đến 22%. Bệnh nhân có GBS = 0-1 có ước tính độ nhạy khoảng 99%, với cận dưới của CI 95% là 96%-98%; độ đặc hiệu cao hơn, với các ước tính điểm dao động từ 27% đến 40%. Hai nghiên cứu đa trung tâm quy mô lớn cho thấy GBS = 0-1 gặp ở khoảng 19%-24% bệnh nhân đến khám vì xuất huyết tiêu hóa trên. Một mô hình gần đây của Shung và cộng sự có thể được thiết lập để đạt được độ nhạy 99% (tương đương GBS = 0-1) hoặc 100% (tương đương GBS = 0), với độ đặc hiệu cao hơn GBS.
Hình bên dưới minh họa cách tính độ nhạy và độ đặc hiệu cho một quần thể giả định gồm 250 bệnh nhân UGIB, sử dụng ngưỡng GBS = 1 để xác định nhóm nguy cơ rất thấp. Độ nhạy 99% có nghĩa là trong mỗi 100 bệnh nhân thực sự cần can thiệp tại bệnh viện hoặc tử vong, sẽ có 1 trường hợp âm tính giả - tức là 1 bệnh nhân có GBS 0-1 bị phân loại sai là không cần can thiệp hoặc không có nguy cơ tử vong. Như đã đề cập, khi độ nhạy cao thì độ đặc hiệu thường thấp. Hình bên dưới cho thấy trong số 150 bệnh nhân không cần can thiệp hoặc không tử vong, chỉ có 50 người được phân loại đúng là nguy cơ rất thấp theo GBS = 0-1 (độ đặc hiệu 33%, tỷ lệ dương tính giả 67%). Do đó, phần lớn bệnh nhân không cần can thiệp hoặc không tử vong - và có thể không hưởng lợi từ nhập viện - lại không được phân loại là nguy cơ rất thấp. Việc cải thiện độ đặc hiệu trong khi vẫn duy trì độ nhạy cao là mục tiêu quan trọng trong phát triển mô hình đánh giá nguy cơ mới.
Ban hướng dẫn đã cân nhắc liệu mức độ nhạy thấp hơn 100% có chấp nhận được hay không và kết luận rằng mục tiêu đạt độ nhạy 99% là hợp lý, vì độ đặc hiệu cao hơn đi kèm với mức giảm nhẹ về độ nhạy sẽ cho phép nhiều bệnh nhân được xuất viện hơn. Hai công cụ phân tầng nguy cơ dường như đạt độ nhạy khoảng 99% là GBS = 0-1 và mô hình của Shung. Tuy nhiên, ban hướng dẫn chỉ đề cập đến GBS trong khuyến cáo vì GBS đã được nghiên cứu rộng rãi trong nhiều bối cảnh khác nhau, trong khi mô hình của Shung hiện mới chỉ được đánh giá trong một bối cảnh.
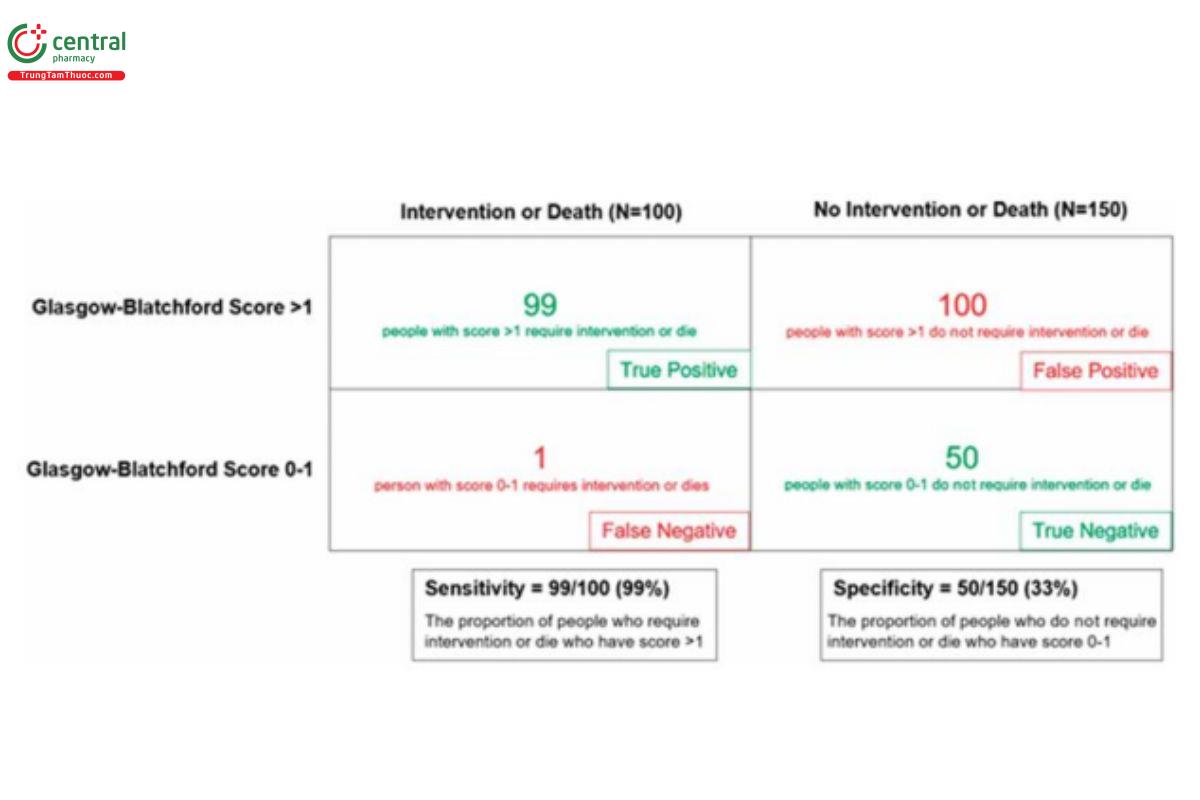
Bảng 2x2 để xác định độ nhạy và độ đặc hiệu cho quần thể giả định gồm 250 bệnh nhân đến khám vì xuất huyết tiêu hóa trên, sử dụng ngưỡng điểm Glasgow-Blatchford là 1. Hàng trên bao gồm những bệnh nhân có điểm 0-1 (được xem là nguy cơ rất thấp). Cột bên trái thể hiện 100 bệnh nhân sẽ cần can thiệp tại bệnh viện hoặc tủ vong, trong đó độ nhạy được tính theo công thức: số dương tính thật chia cho tổng số bệnh nhân cần can thiệp hoặc tử vong (99/100 = 99%). Cột bên phải thể hiện 150 bệnh nhân không cần can thiệp tại bệnh viện hoặc không tử vong, trong đó độ đặc hiệu được tính theo công thức: số âm tính thật chia cho tổng số bệnh nhân không cần can thiệp hoặc không tử vong (50/150 = 33%).
Điều quan trọng là ngưỡng được đề xuất với tỷ lệ âm tính giả 1% (tương ứng với độ nhạy 99%) cho kết cục cần can thiệp tại bệnh viện hoặc tử vong đóng vai trò như một định hướng để đánh giá các mô hình tiên lượng sẽ được phát triển trong tương lai. Nguyện vọng bệnh nhân và bác sĩ liên quan đến mức độ chắc chắn về nguy cơ và mong muốn điều trị ngoại trú so với nội trú nên đóng vai trò quan trọng trong việc quyết định các ngưỡng này. Các quyết định cần được cá thể hóa dựa trên tuổi bệnh nhân, bệnh kèm, độ tin cậy, khả năng tiếp cận cơ sở y tế sau khi xuất viện.
Mặc dù các nghiên cứu quan sát cho thấy điểm GBS và mô hình có thể xác định bệnh nhân nguy cơ rất thấp với độ nhạy cao, nhưng bằng chứng còn hạn chế để chứng minh rằng việc cho những bệnh nhân này xuất viện từ khoa cấp cứu và quản lý ngoại trú thực sự an toàn, với rất ít hoặc không có nguy cơ, so với việc nhập viện. Chỉ có 1 nghiên cứu đáp ứng tiêu chí của PICO này được xác định. Trước khi áp dụng quy tắc rằng bệnh nhân có GBS = 0 sẽ không nhập viện trừ khi có lý do khác, không có trường hợp nào trong số 105 bệnh nhân có GBS = 0 cần can thiệp tại bệnh viện (truyền máu, nội soi hoặc phẫu thuật) hoặc tử vong trong vòng 30 ngày. Sau khi áp dụng quy tắc này, cũng không có trường hợp nào trong 84 bệnh nhân có GBS = 0 không nhập viện cần can thiệp tại bệnh viện hoặc tử vong trong thời gian theo dõi. Ngoài ra, một loạt ca hồi cứu ghi nhận rằng sau khi triển khai một quy trình trong đó những bệnh nhân xuất huyết tiêu hóa trên cấp có GBS = 0-1 sẽ được cho xuất viện từ khoa cấp cứu và theo dõi ngoại trú nếu không có lý do khác để nhập viện, thì không có bệnh nhân nào trong số 103 người có GBS = 0-1 được xuất viện cần can thiệp tại bệnh viện hoặc tử vong trong vòng 30 ngày.
2.1.1.2 Kết luận
Việc sử dụng công cụ đánh giá nguy cơ xác định những bệnh nhân có nguy cơ ≤ 1% cần truyền máu, can thiệp cầm máu hoặc tử vong - những người có thể được cho xuất viện và điều trị ngoại trú - sẽ giúp giảm số ca nhập viện và chi phí. Điểm Glasgow-Blatchford 0-1 đáp ứng được tiêu chí này và cho phép nhiều bệnh nhân được xuất viện hơn so với ngường GBS = 0, vốn là ngưỡng được đề xuất trong hướng dẫn ACG năm 2012.
2.1.2 Truyền khối hồng cầu
Chúng tôi đề xuất chiến lược truyền hồng cầu hạn chế, với ngưỡng truyền khi hemoglobin là 7 g/dL ở bệnh nhân xuất huyết tiêu hóa trên (chất lượng bằng chứng thấp).
2.1.2.1 Tóm tắt bằng chứng
Đối với dân số chung bị thiếu máu (không chỉ riêng UGIB), các hướng dẫn hiện hành tại Hoa Kỳ đưa ra khuyến cáo mạnh về ngưỡng truyền hồng cầu hạn chế là 7 g/dL ở những bệnh nhân nhập viện có huyết động ổn định, bao gồm cả bệnh nhân hồi sức tích cực, và ngưỡng 8 g/dL ở những bệnh nhân đang trải qua phẫu thuật chỉnh hình hoặc tim mạch, cũng như những người có bệnh tim mạch từ trước. Khuyến cáo này cho rằng ngưỡng 7 g/dL có khả năng tương đương với 8 g/dL, nhưng chưa có đủ bằng chứng từ các thử nghiệm ngẫu nhiên ở tất cả các nhóm bệnh nhân; đặc biệt, bằng chứng được đánh giá là chưa đủ để đưa ra khuyến cáo ở bệnh nhân có hội chứng vành cấp. Các khuyến cáo này dựa trên một tổng quan hệ thống cho thấy các chiến lược truyền máu hạn chế giúp giảm 43% số bệnh nhân cần truyền hồng cầu, mà không có bằng chứng cho thấy ảnh hưởng đến các kết cục lâm sàng quan trọng.
Có hai thử nghiệm ngẫu nhiên có đối chứng đáp ứng tiêu chí để đánh giá chiến lược truyền máu hạn chế so với tự do trong xuất huyết tiêu hóa trên. Villaneuva và cộng sự đã thực hiện một nghiên cứu so sánh ngẫu nhiên giữa ngưỡng truyền 7 g/dL và 9 g/dL trên 899 bệnh nhân, với kết cục chính là tử vong sau 45 ngày. Những bệnh nhân có chảy máu ồ ạt mất máu cấp và những người có bệnh mạch máu ngoại biên có triệu chứng, đột quỵ hoặc cơn thiếu máu não thoáng qua trong vòng 90 ngày trước đó đã bị loại trừ. Việc truyền máu ít xảy ra hơn ở nhóm chiến lược hạn chế (49% so với 86%, p < 0.001). Nhóm hạn chế có tỷ lệ tử vong thấp hơn (5% so với 9%, p = 0.02), ít chảy máu tái phát hơn (10% so với 16%, p = 0.01) và ít phản ứng truyền máu (3% so với 9%, p = 0.001) cũng như biến chứng tim mạch (11% so với 16%, p = 0.04) hơn.
Jairath và cộng sự đã thực hiện một thử nghiệm ngẫu nhiên theo cụm, trong đó các cơ sở tham gia được phân ngẫu nhiên vào các nhánh nghiên cứu. Ba bệnh viện được phân vào ngưỡng truyền máu 8 g/dL và ba bệnh viện vào ngưỡng 10 g/dL, với tiêu chí loại trừ duy nhất là xuất huyết mất máu ồ ạt. Sự phân bố không đồng đều giữa hai nhóm nghiên cứu (43% và 57%); đồng thời cũng ghi nhận khả năng có sai lệch chọn mẫu. Sự khác biệt về tỷ lệ bệnh nhân được truyền máu giữa nhóm hạn chế và nhóm tự do nhỏ hơn dự kiến (33% so với 46%, p = 0.23), có thể ít nhất một phần do mức độ tuân thủ chính sách truyền máu thấp hơn ở nhóm tự do. Không có sự khác biệt có ý nghĩa thống kê giữa chiến lược hạn chế và tự do về tử vong trong vòng 28 ngày (5% so với 7%), chảy máu tái phát (5% so với 9%), phản ứng truyền máu (1% so với 2%), hoặc các biến cố huyết khối/thiếu máu cục bộ (4% so với 7%).
Dựa trên các bằng chứng, hướng dẫn đề xuất chiến lược truyền máu hạn chế. Ngưỡng truyền máu được chọn là hemoglobin 7 g/dL (tức là truyền khi Hb giảm dưới 7 g/dL), vì thử nghiệm ngẫu nhiên cho thấy lợi ích của chiến lược hạn chế trong UGIB đã sử dụng ngưỡng này. Ngoài ra, một phân tích gộp các RCT ở bệnh nhân có chỉ định truyền máu bất kỳ cho thấy không có sự khác biệt có ý nghĩa về ảnh hưởng lên tử vong giữa chiến lược truyền hạn chế và tự do khi so sánh nhóm sử dụng ngưỡng hạn chế 8-9 g/dL với nhóm sử dụng ngưỡng 7 g/dL. Do các RCT này loại trừ bệnh nhân UGIB mất máu ồ ạt và thực tế rằng nồng độ hemoglobin ở bệnh nhân tụt huyết áp sẽ giảm thêm sau hồi sức dịch ngay cả khi không còn chảy máu, hướng dẫn thống nhất rằng việc truyền máu cho bệnh nhân tụt huyết áp trước khi Hb giảm đến 7 g/dL là hợp lý.
Do thiếu bằng chứng từ các thử nghiệm ngẫu nhiên ở bệnh nhân UGIB có bệnh tim mạch từ trước, và theo khuyến cáo hiện hành sử dụng ngưỡng 8 g/dL ở nhóm này, hướng dẫn cho rằng ngưỡng này là hợp lý đối với bệnh nhân UGIB có bệnh nền tim mạch. Cần phân biệt nhóm này với bệnh nhân có hội chứng vành cấp. Ở nhóm sau, bằng chứng rất hạn chế; tuy nhiên, phân tích gộp từ 2 nghiên cứu nhỏ ở bệnh nhân thiếu máu kèm hội chứng vành cấp (N = 141) hoặc bệnh mạch vành ổn định được can thiệp tim mạch (N = 14) cho thấy có thể có xu hướng tăng tử vong với chiến lược truyền máu hạn chế (ngưỡng 8 g/dL hoặc Hct 24%). Do đó, có thể cân nhắc ngưỡng cao hơn 8 g/dL ở bệnh nhân UGIB kèm hội chứng vành cấp, dù bằng chứng còn rất hạn chế.
2.1.2.2 Kết luận
Chiến lược truyền hồng cầu hạn chế - truyền khi hemoglobin giảm dưới 7 g/dL - có vẻ giúp giảm chảy máu tái phát và tử vong; kết luận này không thay đổi so với hướng dẫn ACG năm 2012. Ở bệnh nhân tụt huyết áp, có thể truyền ở mức hemoglobin cao hơn do sự cân bằng lại sau hồi sức dịch, và ngưỡng 8 g/dL là hợp lý ở bệnh nhân có bệnh tim mạch trước đó.
2.2 Điều trị nội khoa trước nội soi
2.2.1 Chúng tôi đề xuất truyền erythromycin trước khi nội soi ở bệnh nhân UGIB (chất lượng bằng chứng rất thấp)
2.2.1.1 Tóm tắt bằng chứng
Cơ sở lý luận của việc sử dụng thuốc tăng nhu động như erythromycin là giúp đẩy máu và cục máu đông xuống đoạn xa của Đường tiêu hóa trên, từ đó cải thiện khả năng quan sát khi nội soi và nâng cao giá trị chẩn đoán. Việc tăng khả năng chẩn đoán lý tưởng sẽ cải thiện các kết cục lâm sàng quan trọng như chảy máu tái phát, nhờ tăng tỷ lệ bệnh nhân được xử trí phù hợp (ví dụ: điều trị nội soi và điều trị nội khoa) dựa trên các phát hiện nội soi. Hướng dẫn cũng xác định trước các lợi ích tiềm năng khác có ý nghĩa: giảm nhu cầu nội soi lại (nếu chẩn đoán chính xác hơn ngay từ lần nội soi đầu) và giảm thời gian nằm viện (do chẩn đoán sớm các trường hợp nguy cơ thấp để xuất viện sớm hơn, đồng thời giảm số lần nội soi lặp lại - yếu tố có thể kéo dài thời gian nằm viện).
Quá trình tìm kiếm của chúng tôi xác định được một tổng quan hệ thống gồm 8 thử nghiệm ngẫu nhiên có đối chứng và thêm 1 RCT được công bố sau đó, bao gồm 29 bệnh nhân được phân vào nhóm erythromycin hoặc rửa dạ dày. Chỉ có 1 trong số 9 RCT này báo cáo kết quả về tiêu chí quan trọng là chảy máu tái phát: 1/14 ở nhóm erythromycin so với 2/15 ở nhóm rửa dạ dày; chênh lệch -6%. Kết quả về tử vong được báo cáo trong 3 RCT; phân tích gộp của chúng tôi cho thấy với erythromycin so với giả dược/không điều trị, RR = 0.81. Phân tích gộp 8 RCT cho thấy erythromycin giúp giảm nhu cầu nội soi lại và giảm số ngày nằm viện. Số đơn vị máu truyền có xu hướng thấp hơn khi dùng erythromycin, tuy nhiên sự không đồng nhất đáng kể giữa các nghiên cứu.
Mặc dù chưa có bằng chứng cho thấy erythromycin giúp giảm chảy máu tái phát và tử vong, thuốc này vẫn mang lại những lợi ích đáng kể như giảm nhu cầu nội soi lặp lại và rút ngắn thời gian nằm viện. Lợi ích kinh tế từ việc giảm số thủ thuật và thời gian nằm viện, cùng với mong muốn của bệnh nhân tránh các thủ thuật và ngày nằm viện, chi phí tương đối thấp và dễ sử dụng, đã khiến ban hướng dẫn đưa ra khuyến cáo có điều kiện về việc sử dụng erythromycin trước nội soi. Các bằng chứng hiện có không cho thấy lợi ích chỉ giới hạn ở một nhóm bệnh nhân cụ thể nào trong UGIB cấp. Bằng chứng về thuốc tăng nhu động khác như Metoclopramide còn rất hạn chế, chủ yếu từ các tóm tắt nghiên cứu cũ, và không ủng hộ cho việc sử dụng thuốc này.
Liều khuyến cáo là truyền tĩnh mạch 250 mg, vì đây là liều được sử dụng phổ biến nhất trong các RCT. Thuốc được truyền trong 5-30 phút (thường là 20-30 phút), sau đó tiến hành nội soi trong vòng 20-90 phút. Erythromycin đường tĩnh mạch có thể kéo dài khoảng QT, với mức độ ảnh hưởng liên quan đến tốc độ truyền và liều dùng, và rất hiếm khi gây rối loạn nhịp thất như xoắn đỉnh. Tuy nhiên, tổng quan các báo cáo ca bệnh cho thấy biến cố này chủ yếu xảy ra khi dùng liều cao hơn và/hoặc lặp lại nhiều lần. Dù vậy, một số nghiên cứu đã loại trừ các bệnh nhân có yếu tố nguy cơ làm tăng khả năng xoắn đỉnh, bao gồm kéo dài QT trên điện tâm đồ, bệnh tim, rối loạn điện giải, rối loạn chức năng gan, dùng thuốc chống loạn nhịp, và các thuốc kéo dài QT là cơ chất của CYP3A4 (ví dụ: terfenadine, astemizole).
2.2.1.2 Kết luận
Truyền tĩnh mạch 250 mg erythromycin trong vòng 20-90 phút trước nội soi có thể giúp giảm nhu cầu nội soi lặp lại và rút ngắn thời gian nằm viện, mặc dù chưa có bằng chứng cho thấy cải thiện kết cục lâm sàng như chảy máu tái phát. Hướng dẫn ACG năm 2012 đã nêu rằng việc truyền thuốc này “nên được cân nhắc”.
2.2.2 Chúng tôi chưa thể đưa ra khuyến cáo ủng hộ hay phản đối việc sử dụng PPI trước nội soi ở bệnh nhân UGIB
2.2.2.1 Tóm tắt bằng chứng
Tổng quan hệ thống xác định được 3 thử nghiệm ngẫu nhiên có đối chứng với giả dược đánh giá việc sử dụng PPI trước nội soi. Tuy nhiên, trong 2 nghiên cứu này, tất cả bệnh nhân vẫn tiếp tục điều trị theo nhóm ban đầu (giả dược hoặc PPI) sau khi nội soi. Do thực hành lâm sàng hiện nay yêu cầu sử dụng PPI ở bệnh nhân loét, nên 2 nghiên cứu này không phù hợp với thực hành hiện tại. Thiết kế này cũng có vấn đề về phương pháp luận, vì nếu bệnh nhân trong nhóm giả dược cần PPI nhưng vẫn tiếp tục dùng giả dược sau nội soi, trong khi nhóm PPI tiếp tục được dùng PPI, thì sẽ tạo ra sai lệch có lợi cho nhóm PPI. Do đó, hai nghiên cứu này không cho phép đánh giá các kết cục sau nội soi như chảy máu tái phát và tử vong, nên hướng dẫn chỉ dựa vào nghiên cứu của Lau và cộng sự để đánh giá các kết cục này. Cả 3 nghiên cứu được sử dụng để đánh giá các kết cục trước thời điểm nội soi, chẳng hạn như nhu cầu điều trị nội soi.
Lau và cộng sự không tìm thấy bằng chứng cho thấy lợi ích của PPI (Omeprazole đường tĩnh mạch, bolus 80 mg sau đó truyền 8 mg/giờ) so với giả dược trong việc giảm chảy máu tái phát hoặc tử vong. Tương tự, phân tích gộp của chúng tôi từ 2 nghiên cứu khác bị loại trừ cũng không cho thấy lợi ích về chảy máu tái phát hoặc tử vong, mặc dù có xu hướng thiên lệch có lợi cho PPI. Tuy nhiên, phân tích gộp của cả 3 nghiên cứu cho thấy việc sử dụng PPI so với giả dược giúp giảm nhu cầu điều trị cầm máu nội soi trong lần nội soi ban đầu.
Do đó, các bằng chứng hạn chế và chất lượng thấp cho thấy không có lợi ích rõ ràng của việc dùng PPI trước nội soi đối với tình trạng chảy máu tiếp diễn hoặc tử vong, mặc dù các khoảng tin cậy cho những kết cục này còn rộng. Trong bối cảnh thiếu bằng chứng về lợi ích lâm sàng, hội đồng chuyên gia không thể đưa ra khuyến cáo chống lại việc sử dụng PPI trước nội soi. Tuy nhiên, hội đồng cũng không khuyến cáo chống lại việc dùng PPI trước nội soi, do bằng chứng còn thiếu chính xác và có thêm các dữ liệu gián tiếp khác. Dữ liệu từ thử nghiệm ngẫu nhiên cho thấy liệu pháp PPI liều cao sau nội soi giúp giảm chảy máu tái phát sau can thiệp nội soi ở bệnh nhân có loét với dấu hiệu nguy cơ cao, cũng như ở những bệnh nhân có cục máu đông bám dính nhưng không được điều trị nội soi. Điều này gợi ý rằng PPI trước nội soi có thể mang lại một số lợi ích cho một nhóm nhỏ bệnh nhân xuất huyết tiêu hóa trên. Ngoài ra, ở những bệnh nhân không được nội soi hoặc điều trị cầm máu nội soi, hoặc bị trì hoãn, hội đồng cho rằng có thể cân nhắc dùng PPI trước nội soi dựa trên bằng chứng rất gián tiếp từ một phân tích gộp các thử nghiệm ngẫu nhiên. Phân tích này cho thấy giảm nguy cơ chảy máu tái phát, nhưng không giảm tử vong, khi so sánh PPI với giả dược hoặc thuốc đối kháng thụ thể H2.
Việc dùng PPI trước nội soi có thể giúp giảm nhẹ nhu cầu can thiệp nội soi. Những bác sĩ và bệnh nhân coi trọng việc giảm nhu cầu can thiệp này có thể lựa chọn sử dụng PPI trước nội soi. Các yếu tố kinh tế cũng khác nhau tùy từng hệ thống y tế: chi phí tăng thêm khi dùng PPI cho tất cả bệnh nhân xuất huyết tiêu hóa trên so với khoản tiết kiệm nhờ tránh được nội soi ở một số ít bệnh nhân có thể ảnh hưởng đến quyết định.
2.2.2.2 Kết luận
Các bằng chứng hiện có cho thấy không có lợi ích của việc dùng PPI trước nội soi đối với các kết cục lâm sàng, do đó không thể đưa ra khuyến cáo sử dụng. Tuy nhiên, do có giảm nhẹ nhu cầu can thiệp nội soi, cùng với khả năng chưa được chứng minh rằng PPI có thể mang lại lợi ích cho một nhóm nhỏ bệnh nhân và/hoặc những trường hợp không thể thực hiện nội soi hoặc bị trì hoãn, chúng tôi không khuyến cáo chống lại việc sử dụng. Các hướng dẫn khác đưa ra quan điểm rất khác nhau, từ khuyến cáo sử dụng đến khuyến cáo không sử dụng PPI trước nội soi. Trong các hướng dẫn trước đây, chúng tôi cho rằng PPI trước nội soi có thể được cân nhắc để giảm nhu cầu can thiệp nội soi nhưng không cải thiện kết cục lâm sàng. Các hướng dẫn nên đưa ra một hành động khuyến cáo cụ thể. Do đó, những cách diễn đạt như “có thể cân nhắc” vốn không nghiêng về khuyến cáo hay không sử dụng (ví dụ như dùng PPI), hiện không còn được sử dụng.
Nội soi trong xuất huyết tiêu hóa trên
2.2.3 Chúng tôi đề xuất rằng những bệnh nhân nhập viện hoặc đang được theo dõi tại bệnh viện vì UGIB nên được nội soi trong vòng 24 giờ kể từ khi nhập viện (chất lượng bằng chứng rất thấp)
2.2.3.1 Tóm tắt bằng chứng
Việc chẩn đoán sớm không đủ để là lý do cho nội soi sớm; cần có bằng chứng cho thấy lợi ích về mặt lâm sàng, kinh tế hoặc các kết cục hướng đến bệnh nhân. Những lợi ích tiềm năng của nội soi sớm bao gồm đánh giá tiên lượng chính xác hơn để định hướng xử trí (ví dụ: thời điểm cho ăn lại và xuất viện) và triển khai sớm điều trị nội soi hoặc nội khoa dựa trên kết quả nội soi. Những nguy cơ tiềm tàng có thể bao gồm tử vong hoặc biến chứng nếu nội soi được thực hiện trước khi hồi sức thích hợp và kiểm soát các bệnh đi kèm đang hoạt động, cũng như kết cục kém hơn khi nội soi ngoài giờ hành chính. Khuyến cáo này chỉ áp dụng cho bệnh nhân đã nhập viện hoặc đang được theo dõi tại bệnh viện. Những bệnh nhân được xác định là nguy cơ rất thấp và được xuất viện từ khoa cấp cứu với kế hoạch theo dõi ngoại trú không được xem xét. Các nghiên cứu quan sát được đưa vào do thiếu RCT trực tiếp trả lời câu hỏi nghiên cứu. Vì có thể tồn tại những khác biệt cơ bản về các đặc điểm quan trọng ảnh hưởng đến kết cục giữa nhóm được nội soi sớm và không được nội soi sớm trong các nghiên cứu không ngẫu nhiên, nên chỉ những nghiên cứu quan sát có điều chỉnh thống kê đầy đủ trong đánh giá kết cục mới được đưa vào phân tích.
Quần thể chung bệnh nhân xuất huyết tiêu hóa trên. Không có thử nghiệm ngẫu nhiên có đối chứng nào đánh giá nội soi trong vòng 24 giờ so với sau 24 giờ. Tuy nhiên, có một RCT so sánh nội soi thực hiện ≤ 12 giờ so với > 12 giờ sau khi bệnh nhân đến khám ở các bệnh nhân xuất huyết tiêu hóa trên. Tác giả chỉ báo cáo kết quả ở những bệnh nhân có chảy máu do loét được xác nhận qua nội soi, và nhận thấy không giảm tình trạng chảy máu tái phát hoặc tử vong. Bằng chứng chất lượng rất thấp từ các nghiên cứu quan sát cho thấy những bệnh nhân nhập viện vì xuất huyết tiêu hóa trên và được nội soi trong vòng 1 ngày sau nhập viện có thời gian nằm viện ngắn hơn so với những người không được nội soi sớm. Hai trong số các nghiên cứu quan sát này còn ghi nhận nguy cơ phải phẫu thuật thấp hơn, và một nghiên cứu khác báo cáo giảm tỷ lệ tử vong khi nội soi trong vòng 1 ngày sau nhập viện. Tuy nhiên, vẫn chưa chắc chắn liệu nội soi được ghi nhận là “trong vòng 1 ngày sau nhập viện” trong các nghiên cứu sử dụng dữ liệu cơ sở có thực sự diễn ra trong vòng 24 giờ hay không; một số trường hợp có thể được thực hiện vào ngày tiếp theo, tức là sau hơn 24 giờ kể từ khi nhập viện.
Đặc điểm lâm sàng nguy cơ thấp. Hai thử nghiệm ngẫu nhiên có đối chứng nhỏ trên những bệnh nhân có đặc điểm lâm sàng nguy cơ thấp (huyết động ổn định, không có bệnh nặng đi kèm) cho thấy nội soi trong vòng 2-6 giờ sau đánh giá ban đầu giúp phát hiện các tổn thương nguy cơ thấp trên nội soi (ví dụ: loét đáy sạch, Mallory-Weiss). Những phát hiện này cho phép xuất viện và theo dõi ngoại trú ở ít nhất 40% bệnh nhân. Việc giảm nhu cầu điều trị nội trú chỉ được ghi nhận ở một trong hai nghiên cứu, do ở nghiên cứu còn lại, các bác sĩ điều trị không tuân theo khuyến cáo của bác sĩ nội soi về việc cho xuất viện và theo dõi ngoại trú ở khoảng 80% bệnh nhân có tổn thương nguy cơ thấp. Không ghi nhận sự khác biệt về chảy máu tái phát hoặc tử vong giữa các nhóm. Do không có RCT nào so sánh nội soi trong vòng 24 giờ với sau 24 giờ, các tác giả cũng xem xét một nghiên cứu thuần tập lớn gồm 5.415 bệnh nhân huyết động ổn định, không có bệnh nặng đi kèm có loét chảy máu được xác nhận qua nội soi. Kết quả cho thấy nội soi trong vòng 24 giờ kể từ khi nhập viện có xu hướng giảm tử vong trong thời gian nằm viện nhưng không làm giảm tử vong sau 30 ngày.
Đặc điểm lâm sàng nguy cơ cao. Các hướng dẫn trước đây đã gợi ý cân nhắc nội soi trong vòng 12 giờ ở những bệnh nhân có đặc điểm nguy cơ cao như huyết động không ổn định hoặc xơ gan, mặc dù bằng chứng hỗ trợ là rất hạn chế. Các nghiên cứu liên quan được xác định bao gồm 2 nghiên cứu, nhưng kết quả không nhất quán. Một nghiên cứu thuần tập đại Đan Mạch trên các bệnh nhân có loét chảy máu được xác nhận qua nội soi cho thấy tăng tỷ lệ tử vong ở những bệnh nhân nguy cơ cao khi nội soi được thực hiện quá sớm hoặc quá muộn. Cụ thể, tỷ lệ tử vong trong viện thấp hơn khi nội soi được thực hiện 6-24 giờ sau nhập viện ở bệnh nhân huyết động không ổn định và 12-36 giờ sau nhập viện ở bệnh nhân huyết động ổn định nhưng có bệnh nền kèm theo so với khi nội soi được thực hiện ngoài các khoảng thời gian này. Nghiên cứu này đặt ra khả năng nội soi quá sớm có thể gây hại nếu chưa tiến hành hồi sức huyết động đầy đủ và xử trí các bệnh nền đang diễn tiến trước khi nội soi. Ngược lại, một nghiên đơn trung tâm tại Hàn Quốc cho thấy tỷ lệ tử vong sau 28 ngày giảm khi nội soi được thực hiện trong vòng 6 giờ so với 6-48 giờ sau khi bệnh nhân đến khám.
Một thử nghiệm RCT ban đầu được báo cáo dưới dạng tóm tắt năm 2015 với kết quả tạm thời và sau đó được công bố đầy đủ vào năm 2020 đã so sánh nội soi khẩn trong vòng 6 giờ sau khi hội chẩn chuyên khoa tiêu hóa với nhóm đối chứng được chỉ định nội soi trong vòng 6-24 giờ sau hội chẩn ở 516 bệnh nhân được dự đoán nguy cơ cao dựa trên điểm GBS ≥ 12. Kết quả cho thấy không giảm chảy máu tái phát cũng như không giảm tử vong khi nội soi sớm. Tương tự, không ghi nhận lợi ích về thời gian nằm viện hay nhu cầu truyền máu, mặc dù can thiệp cầm máu nội soi được thực hiện nhiều hơn 11.6% ở nhóm nội soi khẩn. Do có khoảng cách thời gian từ lúc bệnh nhân đến viện đến khi được phân nhóm ngẫu nhiên, nghiên cứu thực tế đã so sánh nội soi tại thời điểm trung bình 10 giờ so với 25 giờ sau khi đến viện, với 55% bệnh nhân nhóm đối chứng được nội soi sau hơn 24 giờ. Những dữ liệu này gợi ý rằng khoảng thời gian chờ nội soi thậm chí trên 24 giờ có thể vẫn chấp nhận được trong một số trường hợp.
Nghiên cứu này loại trừ các bệnh nhân sốc tụt huyết áp không ổn định sau hồi sức ban đầu, nhóm chỉ chiếm khoảng 5% bệnh nhân nguy cơ cao. Dựa trên kinh nghiệm lâm sàng, hội đồng chuyên gia cho rằng những bệnh nhân này cần can thiệp khẩn, bằng nội soi hoặc can thiệp mạch.
2.2.3.2 Kết luận
Hội đồng khuyến nghị rằng các bệnh nhân nhập viện hoặc đang được theo dõi tại bệnh viện vì xuất huyết tiêu hóa trên rõ ràng, dù được dự đoán nguy cơ thấp hay cao về chảy máu tái phát và tử vong, nên được nội soi tiêu hóa trong vòng 24 giờ kể từ khi đến khám. Quyết định này dựa trên bằng chứng về lợi ích kinh tế (giảm thời gian nằm viện) cũng như lợi ích lâm sàng có thể có về giảm tỷ lệ tử vong và nhu cầu phẫu thuật trong các nghiên cứu quan sát. Chúng tôi lựa chọn tính thời gian từ lúc bệnh nhân đến khám thay vì từ lúc nhập viện, do sự khác biệt lớn về thời gian từ khi đến khám đến khi nhập viện giữa các cơ sở y tế. Mặc dù các nghiên cứu quan sát ủng hộ mốc “trong vòng 1 ngày” sử dụng thời điểm nhập viện, hội đồng lo ngại rằng ở những nơi kéo dài giữa thời gian khám và nhập viện, việc tính từ lúc nhập viện có thể gây trì hoãn nội soi quá mức chấp nhận được. Trong các dữ liệu từ một nghiên cứu quan sát lớn cho thấy khả năng gây hại khi nội soi quá sớm ở bệnh nhân huyết động không ổn định hoặc có bệnh nền đáng kể, cùng với một thử nghiệm ngẫu nhiên lớn cho thấy không có lợi ích của nội soi rất sớm ở bệnh nhân nguy cơ cao, hội đồng thống nhất rằng cần hồi sức đầy đủ và xử trí các bệnh nền đang diễn tiến trước khi tiến hành nội soi. Do đó, hội đồng không đưa vào khuyến nghị từ hướng dẫn năm 2012 rằng nội soi trong vòng 12 giờ “có thể được cân nhắc” ở bệnh nhân có đặc điểm nguy cơ cao. Hội đồng cũng lưu ý rằng cách tiếp cận này có vẻ khác với xử trí sốc mất máu do chấn thương, vốn có thể bao gồm can thiệp cầm máu nhanh, hạn chế truyền dịch tinh thể và mục tiêu huyết áp thấp. Tuy nhiên, chưa rõ liệu các chiến lược này có mang lại lợi ích cho một số bệnh nhân sốc do xuất huyết tiêu hóa trên hay không. Dữ liệu ở bệnh nhân huyết động ổn định, không có bệnh nền kèm theo cho thấy nên thực hiện nội soi càng sớm càng tốt trong giờ làm việc thông thường, vì có thể cho phép xuất viện sớm ở một tỷ lệ đáng kể bệnh nhân có tổn thương nguy cơ thấp trên nội soi, từ đó giảm thời gian nằm viện và chi phí.
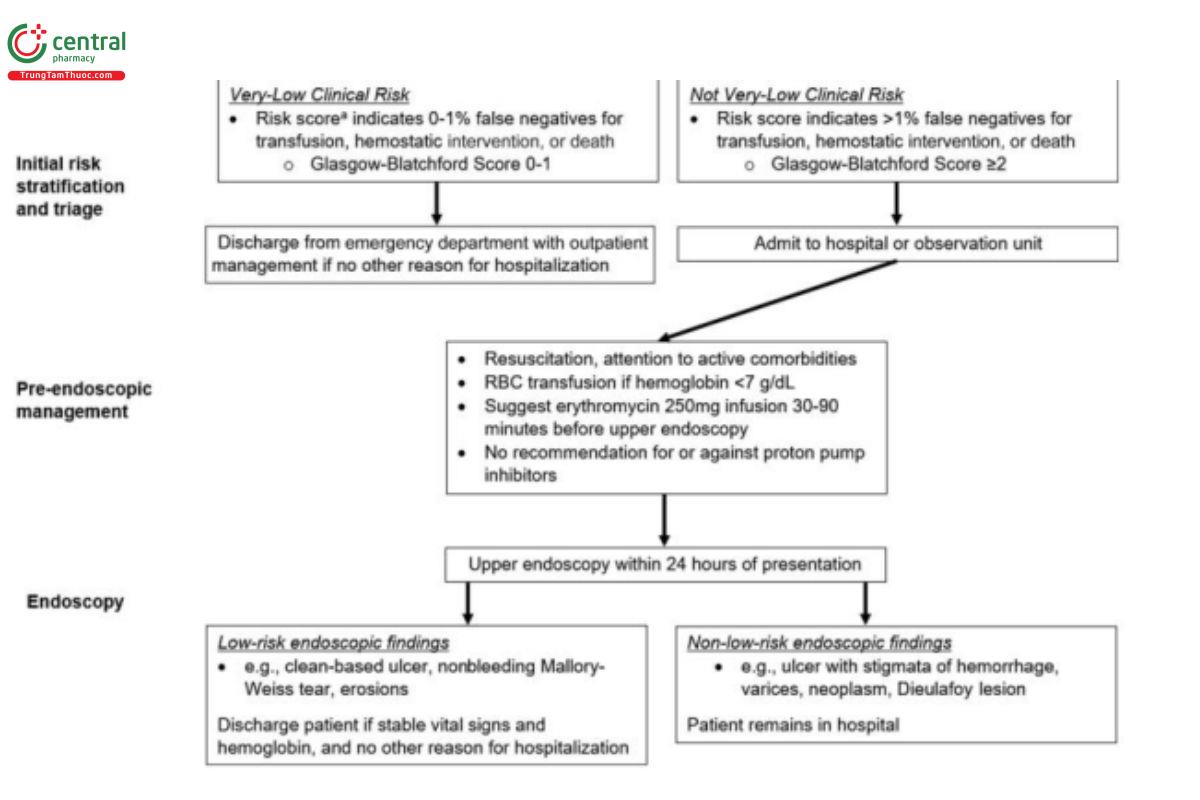
Xử trí ban đầu đối với bệnh nhân đến khám với xuất huyết tiêu hóa trên rõ ràng. Có thể sử dụng các công cụ đánh giá nguy cơ trong tương lai nếu thang điểm đó phân biệt được nguy cơ cần truyền máu, can thiệp cầm máu hoặc tử vong với độ nhạy 99-100% (tỷ lệ âm tính giả 0%-1%).
2.2.4 Chúng tôi khuyến cáo điều trị nội soi ở bệnh nhân UGIB do loét có chảy máu thành tia, chảy máu rỉ rả, hoặc có mạch máu lộ không chảy máu (khuyến cáo mạnh, chất lượng bằng chứng trung bình
2.2.4.1 Tóm tắt bằng chứng
Một phân tích gộp năm 2009 gồm 19 thử nghiệm ngẫu nhiên có đối chứng cho thấy lợi ích rõ rệt của điều trị nội soi so với điều trị không nội soi trong việc giảm chảy máu tái phát ở bệnh nhân đang bị chảy máu và bệnh nhân có lộ mạch máu không chảy máu. Tuy nhiên, chưa ghi nhận lợi ích về giảm tử vong. Không có thêm thử nghiệm ngẫu nhiên phù hợp nào được công bố sau đó.
Hầu hết các thử nghiệm ngẫu nhiên có đối chứng và phân tích gộp được trích dẫn đều gộp chảy máu phun thành tia và rỉ máu vào một nhóm chung gọi là “chảy máu hoạt động”. Trong thực tế, chảy máu phun thành tia ít gặp hơn nhiều so với rỉ máu. Ngoài ra, nguy cơ chảy máu tái phát có vẻ cao hơn ở bệnh nhân chảy máu phun thành tia so với rỉ máu. Tuy nhiên, ngay cả ở bệnh nhân rỉ máu mà không được điều trị nội soi, tỷ lệ chảy máu tái phát vẫn đủ cao để ủng hộ việc điều trị nội soi. Một tổng hợp từ 8 thử nghiệm tiến cứu trên các bệnh nhân rỉ máu không được can thiệp nội soi cho thấy tỷ lệ chảy máu tái phát gộp là 39%. Cần lưu ý định nghĩa “rỉ máu” có thể khác nhau đáng kể giữa các bác sĩ nội soi. Một số thử nghiệm yêu cầu chảy máu liên tục trong 5 phút quan sát mới được xem là rỉ máu hoạt động, nhằm tránh phân loại nhầm các trường hợp chảy máu nhẹ, thoáng qua là rỉ máu hoạt động.
2.2.4.2 Kết luận
Như đã nêu trong hướng dẫn ACG năm 2012, điều trị nội soi mang lại lợi ích lâm sàng quan trọng ở những bệnh nhân xuất huyết tiêu hóa trên do loét có các dấu hiệu nguy cơ cao, bao gồm chảy máu đang hoạt động và lộ mạch máu không chảy máu.
(Mục 7-12 liên quan đến nội soi)
2.2.5 Chúng tôi khuyến cáo sử dụng PPI liều cao, truyền liên tục hoặc ngắt quãng trong 3 ngày sau khi đã cầm máu nội soi thành công cho loét chảy máu (khuyến cáo mạnh, chất lượng bằng chứng từ trung bình đến cao)
2.2.5.1 Tóm tắt bằng chứng
Giả thuyết dẫn đến việc sử dụng PPI liều cao ở bệnh nhân loét chảy máu là giảm acid trong dạ dày giúp thúc đẩy hình thành và ổn định cục máu đông. Tuy nhiên, vẫn chưa rõ mức pH dạ dày mục tiêu nên đạt gần 7 hay chỉ cần ức chế sự tiêu hủy cục máu đông do pepsin ở pH > 4-5 là đã đủ.
Chúng tôi xác định được 7 thử nghiệm ngẫu nhiên có đối chứng với 8 so sánh ngẫu nhiên giữa PPI liều cao (định nghĩa là ≥ 80 mg/ngày trong ít nhất 3 ngày) với giả dược (6 RCT) hoặc không điều trị (2 so sánh trong 1 RCT) sau khi đã cầm máu nội soi thành công. Trong đó, 4 so sánh sử dụng PPI đường tĩnh mạch liên tục với bolus 80 mg, sau đó truyền 8 mg/giờ trong 72 giờ ; 4 so sánh sử dụng PPI ngắt quãng gồm 40 mg uống 2 lần/ngày, 20 mg uống mỗi 6 giờ, hoặc bolus 80 mg, sau đó 40 mg tĩnh mạch mỗi 12 giờ. Có 7 so sánh từ châu Á và 1 từ Iran. Bằng chứng chất lượng cao cho thấy PPI làm giảm chảy máu tái phát, tử vong và nhu cầu phẫu thuật rõ rệt so với giả dược/không điều trị. Phân tích theo phân nhóm không ghi nhận sự khác biệt hiệu quả giữa truyền PPI liên tục và PPI ngắt quãng.
Chúng tôi xác định được 9 thử nghiệm ngẫu nhiên có đối chứng so sánh PPI liều cao với thuốc đối kháng thụ thể H2 sau khi đã cầm máu nội soi thành công. Trong đó, 4 RCT sử dụng PPI tĩnh mạch với liều bolus 80 mg, sau đó truyền 8 mg/giờ ; 1 RCT sử dụng liều bolus 40 mg, sau đó truyền 6,7 mg/giờ ; 4 RCT sử dụng PPI tĩnh mạch ngắt quãng bao gồm 40 mg mỗi 6 giờ hoặc mỗi 12 giờ, hoặc bolus 80 mg, sau đó 40 mg mỗi 8 giờ hoặc 2 lần/ngày. Có 6 RCT được thực hiện tại Hoa Kỳ hoặc châu Âu. Bằng chứng chất lượng trung bình cho thấy PPI giúp giảm chảy máu tái phát so với thuốc đối vận thụ thể H2. Tuy nhiên, không ghi nhận sự giảm có ý nghĩa về tử vong hoặc nhu cầu phẫu thuật khi dùng PPI. Tương tự như các phân tích trước, không có bằng chứng cho thấy sự khác biệt hiệu quả giữa PPI truyền liên tục và PPI ngắt quãng.
Chúng tôi xác định được 12 thử nghiệm ngẫu nhiên có đối chứng so sánh phác đồ bolus 80 mg, sau đó truyền liên tục 8 mg/giờ trong 3 ngày với các phác đồ PPI cường độ thấp hơn sau khi đã cầm máu nội soi thành công. Các phác đồ so sánh bao gồm : 40 mg/ngày trong 4 RCT ; 40 mg x 2 lần/ngày trong 3 RCT ; 80 mg x 2 lần/ngày trong 1 RCT ; bolus 80 mg, sau đó 40-80 mg mỗi 6-12 giờ trong 3 RCT ; bolus 40 mg, sau đó truyền 4 mg/giờ trong 1 RCT. Kết quả phân tích gộp cho thấy đối với chảy máu tái phát, phác đồ bolus + truyền liên tục so với phác đồ ít tích cực hơn có xu hướng làm tăng nhẹ nguy cơ chảy máu tái phát. Tuy nhiên, giới hạn dưới của khoảng tin cậy 95% vẫn phù hợp với khả năng giảm nguy cơ tương đối đến 14% hoặc giảm nguy cơ tuyệt đối 2% với phác đồ bolus + truyền liên tục. Phân tích theo nhóm cho thấy không có sự khác biệt có ý nghĩa liên quan đến liều dùng, tần suất hoặc đường dùng của PPI.
Hội đồng đã đưa ra khuyến cáo mạnh về việc sử dụng PPI liều cao, truyền liên tục hoặc ngắt quãng trong 3 ngày sau khi cầm máu nội soi thành công, dựa trên bằng chứng chất lượng cao cho thấy giảm đáng kể nguy cơ chảy máu tái phát và tử vong so với giả dược/không điều trị, và bằng chứng chất lượng trung bình cho thấy giảm chảy máu tái phát so với thuốc đối kháng thụ thể H2. Mức độ lợi ích trong các RCT này gần như tương đương giữa phác đồ bolus liều cao, sau đó truyền liên tục (bolus 80 mg, truyền 8 mg/giờ), và phác đồ PPI liều cao ngắt quãng với tổng liều trung bình 80-160 mg/ngày (một số có bolus khởi đầu 80 mg).
Hội đồng sau đó đã xem xét liều dùng và đường dùng của các phác đồ PPI liều cao. Bằng chứng chất lượng cao ủng hộ phác đồ bolus 80 mg, sau đó truyền liên tục 8 mg/giờ ở những bệnh nhân sử dụng PPI tĩnh mạch liều cao truyền liên tục. Ngược lại, các dữ liệu hiện có chưa cho phép xác định chắc chắn liều tối ưu của PPI liều cao dùng ngắt quãng. Dựa trên các RCT, có thể sử dụng liều ngắt quãng 40 mg, 2-4 lần/ngày, dùng đường uống hoặc tĩnh mạch. Tổng liều cao hơn có thể phù hợp hơn với các quần thể phương Tây, do PPI được ghi nhận có tác dụng dược lực học và lâm sàng kém hơn so với ở các quần thể châu Á. Một liều bolus khởi đầu 80 mg (đường uống hoặc tĩnh mạch) có thể thích hợp nhằm đạt hiệu quả tăng pH dạ dày nhanh hơn trong ngày điều trị đầu tiên. Liều ngắt quãng có thể dùng đường uống nếu bệnh nhân tỉnh táo, không buồn nôn, không nôn và không khó nuốt. Đường uống dường như tạo ra hiệu quả dược lực học tương đương với liều tĩnh mạch tương đương, mặc dù sự tăng pH dạ dày ban đầu khi dùng đường uống có thể chậm hơn khoảng 15-60 phút so với đường tĩnh mạch. Việc lựa chọn giữa truyền liên tục hay dùng ngắt quãng có thể phụ thuộc vào các yếu tố như tính thuận tiện trong sử dụng và chi phí.
2.2.5.2 Kết luận
Liệu pháp PPI liều cao, được định nghĩa là ≥ 80 mg/ngày trong ≥ 3 ngày, truyền liên tục hoặc ngắt quãng sau khi cầm máu nội soi giúp giảm chảy máu tái phát và tử vong. Phác đồ truyền liên tục nên là bolus 80 mg, sau đó truyền 8 mg/giờ. Ngược lại, liều tối ưu của PPI dùng ngắt quãng (đường uống hoặc tĩnh mạch) vẫn chưa chắc chắn, tuy nhiên chúng tôi đề xuất bolus 80 mg, sau đó 40 mg, 2-4 lần/ngày. Khuyến cáo hiện tại mở rộng so với hướng dẫn năm 2012 của ACG, không chỉ giới hạn ở PPI truyền liên tục mà còn bao gồm PPI liều cao dùng ngắt quãng đường uống hoặc tĩnh mạch.
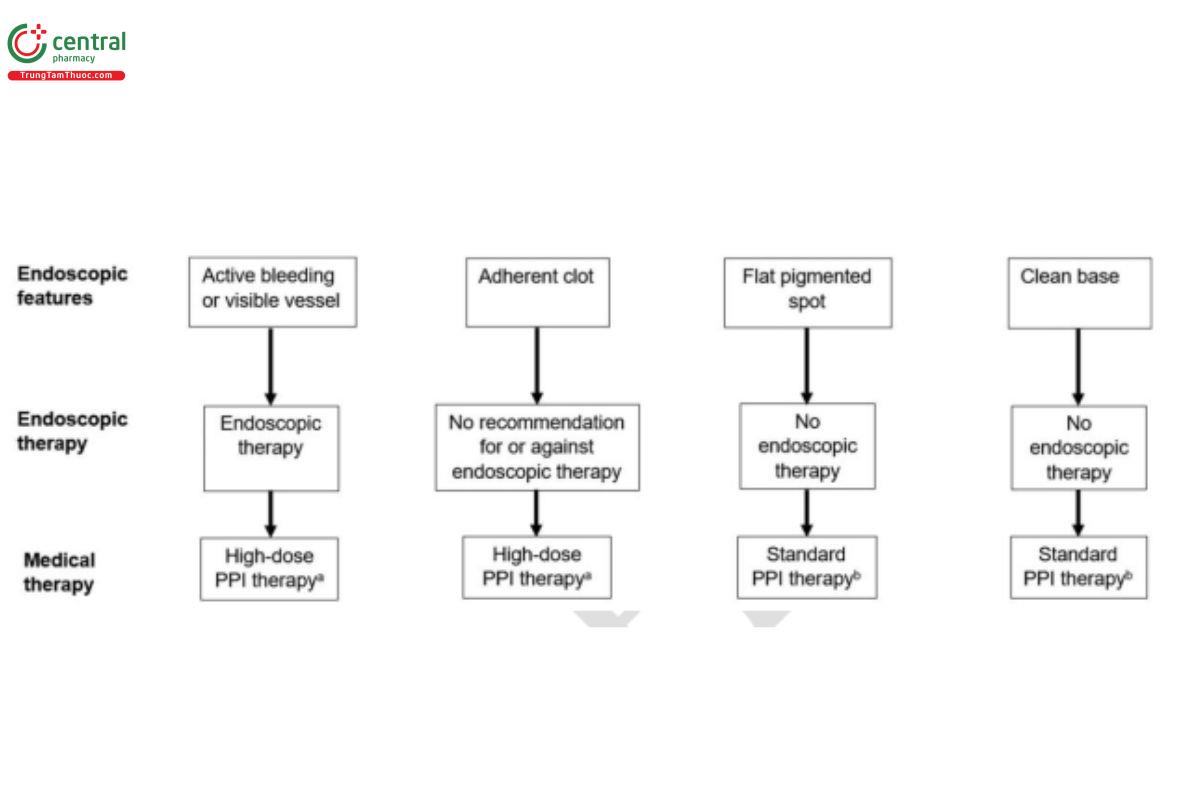
Điều trị nội soi và nội khoa cho loét chảy máu dựa trên đặc điểm nội soi của ổ loét. Đối với phác đồ truyền liên tục, khuyến cáo bolus 80 mg, sau đó truyền 8 mg/giờ trong 3 ngày. Đối với phác đồ ngắt quãng, gợi ý dùng 40 mg, 2-4 lần/ngày trong 3 ngày, ưu tiên đường uống nếu khả thi và có thể dùng bolus khởi đầu 80 mg. Liệu pháp PPI chuẩn (ví dụ : PPI uống 1 lần/ngày) đã được khuyến cáo trong các hướng dẫn trước đây của ACG, nhưng không được đánh giá trong tài liệu hiện tại.
2.2.6 Chúng tôi đề xuất rằng những bệnh nhân nguy cơ cao bị UGIB do loét, sau khi đã cầm máu nội soi và điều trị PPI liều cao ngắn hạn tại bệnh viện, nên tiếp tục dùng PPI đường uống ngày 2 lần cho đến 2 tuần sau lần nội soi ban đầu (chất lượng bằng chứng thấp)
2.2.6.1 Tóm tắt bằng chứng
Hội đồng đã xem xét liều PPI ở các bệnh nhân nguy cơ cao đã được điều trị nội soi và dùng PPI liều cao ngắn hạn. Chỉ có một thử nghiệm ngẫu nhiên có đối chứng được xác định, bao gồm các bệnh nhân có điểm Rockall ≥ 6, đã được cầm máu nội soi thành công đối với loét có chảy máu hoạt động, lộ mạch máu không chảy máu hoặc cục máu đông bám dính, và đã dùng PPI bolus rồi truyền liên tục trong 3 ngày. Các bệnh nhân được phân ngẫu nhiên dùng Esomeprazole 40 mg uống 2 lần/ngày so với 1 lần/ngày trong 11 ngày, sau đó tất cả đều tiếp tục esomeprazole 40 mg/ngày thêm 2 tuần. Kết quả cho thấy giảm chảy máu tái phát ở cả mốc 14 ngày và phân tích chính tại 28 ngày. Việc dùng PPI uống 2 lần/ngày trong khoảng 2 tuần được hội đồng đánh giá là an toàn, dung nạp tốt, dễ tiếp cận và chi phí tương đối thấp. Những yếu tố này, cùng với bằng chứng hiệu quả còn hạn chế nhưng có lợi trong giảm chảy máu tái phát, đã dẫn đến khuyến cáo có điều kiện sử dụng PPI 2 lần/ngày đến 2 tuần sau nội soi ban đầu ở nhóm bệnh nhân này. Sau 2 tuần, theo phác đồ của nghiên cứu RCT trên, bệnh nhân được chuyển sang PPI 1 lần/ngày trong 2 tuần tiếp theo. Tuy nhiên, bằng chứng hiện có chưa đủ để xác định liệu việc kéo dài thời gian dùng PPI 2 lần/ngày hoặc kéo dài tổng thời gian điều trị PPI có mang lại thêm lợi ích hay không.
2.2.6.2 Kết luận
Ở bệnh nhân nguy cơ cao đã được điều trị nội soi và dùng PPI liều cao trong 3 ngày, việc dùng PPI 2 lần/ngày từ ngày 4 đến ngày 14 sau nội soi giúp giảm chảy máu tái phát so với dùng 1 lần/ngày. Đây là khuyến cáo mới dựa trên các bằng chứng xuất hiện sau khi công bố hướng dẫn năm 2012 của ACG.
3 TÀI LIỆU THAM KHẢO
Laine L, Barkun AN, Saltzman JR, Martel M, Leontiadis GI. ACG Clinical Guideline: Upper Gastrointestinal and Ulcer Bleeding. Am J Gastroenterol. 2021 May 1;116(5):899-917. doi: 10.14309/ajg.0000000000001245.

