Phân tích sinh lý và hiệu suất lâm sàng của tỷ lệ thông khí trong hội chứng nguy kịch hô hấp cấp tính

Trungtamthuoc.com - Tỷ lệ thông khí là một chỉ số tại giường đơn giản có thể được tính toán bằng cách sử dụng các biến số hô hấp được đo thường xuyên và là thước đo tình trạng thông khí bị suy yếu.
Bản dịch của Bác sĩ Đặng Thanh Tuấn - Bệnh viện Nhi Đồng 1
Tải PDF bản dịch TẠI ĐÂY
1 Tóm tắt
Cơ sở lý luận: Tỷ lệ khoảng chết của phổi (VD/VT) là yếu tố dự báo độc lập về tỷ lệ tử vong trong hội chứng nguy kịch hô hấp cấp tính (ARDS). Tuy nhiên, nó hiếm khi được sử dụng trong thực tế. Tỷ lệ thông khí là một chỉ số tại giường đơn giản có thể được tính toán bằng cách sử dụng các biến số hô hấp được đo thường xuyên và là thước đo tình trạng thông khí bị suy yếu. Tỷ lệ thông khí được định nghĩa là [thông khí phút (ml/phút) X PaCO2 (mm Hg)]/(trọng lượng cơ thể dự đoán X 100 X 37,5).
Mục tiêu: Xác định mối liên quan giữa tỷ lệ thông khí với VD/VT trong ARDS.
Phương pháp: Đầu tiên, trong một nghiên cứu quan sát tiến cứu, đơn trung tâm về ARDS, chúng tôi đã thử nghiệm mối liên quan giữa VD/VT với tỷ lệ thông khí. Với tỷ lệ tử vong tại bệnh viện là kết quả chính và số ngày không thở máy là kết quả phụ, chúng tôi đã thử nghiệm vai trò của tỷ lệ thông khí như một yếu tố dự đoán kết quả. Những phát hiện từ nghiên cứu này đã được xác nhận thêm trong các phân tích thứ cấp của hai thử nghiệm ngẫu nhiên có đối chứng trên Mạng NHLBI ARDS.
Phép đo và kết quả chính: Tỷ lệ thông khí có tương quan dương với VD/VT. Các nhóm thông khí chia theo thứ tự tỷ lệ thông khí có VD/VT cao hơn đáng kể. Tỷ lệ thông khí có liên quan độc lập với việc tăng nguy cơ tử vong sau khi điều chỉnh PaO2/FiO2 và áp lực dương cuối thì thở ra (tỷ lệ chênh lệch, 1,51; P = 0,024) và sau khi điều chỉnh Đánh giá sinh lý cấp tính và Đánh giá sức khỏe mãn tính II điểm (tỷ lệ chênh lệch, OR 1,59; P = 0,04). Những phát hiện này đã được nhân rộng hơn nữa trong các phân tích thứ cấp của hai thử nghiệm ngẫu nhiên có đối chứng NHLBI riêng biệt.
Kết luận: Tỷ lệ thông khí tương quan tốt với VD/VT trong ARDS và giá trị cao hơn ở mức cơ bản có liên quan đến việc tăng nguy cơ xảy ra kết quả bất lợi. Những kết quả này đầy hứa hẹn cho việc sử dụng tỷ lệ thông khí như một chỉ số đơn giản tại giường về tình trạng thông khí bị suy giảm trong ARDS.
Sơ lược bình luận Kiến thức khoa học về chủ đề Nhiều nghiên cứu đã phát hiện ra rằng thông khí bị suy giảm, được đo bằng khoảng chết của phổi, là một yếu tố dự báo quan trọng về kết cục của hội chứng nguy kịch hô hấp cấp tính (ARDS). Tuy nhiên, do sự phức tạp trong việc đo lường nên khoảng chết hiếm khi được sử dụng trong môi trường chăm sóc tích cực. Do đó, PaO2/FiO2 vẫn là biến số sinh lý đo được duy nhất được sử dụng để xác định mức độ nghiêm trọng của ARDS. Nghiên cứu này bổ sung thêm gì vào lĩnh vực này Nghiên cứu mô tả một chỉ số mới về tình trạng suy giảm thông khí được gọi là tỷ lệ thông khí (ventilatory ratio - VR). VR có thể được tính toán dễ dàng bằng cách sử dụng PaCO2 đo được và thông khí phút. Trong hai nhóm ARDS, VR được phát hiện có mối liên quan đáng kể với tỷ lệ khoảng chết ở phổi. Khi đo ở mức cơ bản, VR được phát hiện có liên quan độc lập với việc tăng nguy cơ tử vong trong các đoàn hệ thử nghiệm ngẫu nhiên và có đối chứng về ARDS. VR cung cấp giải pháp đơn giản và thực tế để theo dõi tình trạng suy giảm thông khí ở bệnh nhân thở máy và có thể được sử dụng để phân loại bệnh nhân mắc ARDS. |
Trao đổi khí bao gồm hai chức năng thiết yếu là oxygen hóa và thông khí. Phương pháp thứ nhất, được định lượng bằng tỷ lệ PaO2/FiO2, là phương pháp chính để chẩn đoán và phân loại bệnh nhân trong hội chứng nguy kịch hô hấp cấp tính (ARDS). Loại thứ hai được theo dõi tốt nhất bằng cách đo tỷ lệ khoảng chết của phổi (VD/VT). Bằng chứng đáng chú ý ủng hộ tỷ lệ khoảng chết ở phổi như một yếu tố dự báo độc lập về tỷ lệ tử vong trong ARDS (1, 2). Tuy nhiên, nó hiếm khi được đo lường hoặc sử dụng trong thực hành lâm sàng. Chủ yếu, điều này là do thiếu chỉ số đầu giường đơn giản để theo dõi khoảng chết và chi phí bổ sung liên quan đến việc đo lường nó trong môi trường chăm sóc tích cực (3). Do đó, sự cố thông khí, mặc dù tầm quan trọng của nó, hoàn toàn bị loại trừ như một biến phân tầng trong ARDS.
Để giải quyết vấn đề này, chúng tôi đã mô tả tỷ lệ thông khí (VR), một chỉ số đơn giản tại giường về hiệu quả thông khí bị suy giảm (4). VR được mô tả là:
VR = (VEmeasured x PaCO2measured) / (VEpredicted x PaCO2ideal) (1)
ở đây VEmeasured là thông khí phút đo được (ml/phút), PaCO2measured là áp lực động mạch đo được của carbon dioxide (mm Hg), VEpredicted là thông khí phút dự đoán được tính bằng trọng lượng cơ thể dự đoán X 100 (ml/phút) (5), và PaCO2ideal là áp lực động mạch dự kiến của carbon dioxide trong phổi bình thường nếu được thông khí với thông khí phút dự đoán. PaCO2ideal được đặt ở mức 37,5 mm Hg (5 kPa) cho tất cả bệnh nhân (4).
VR là một tỷ lệ không có đơn vị và giá trị xấp xỉ 1 sẽ biểu thị phổi thông khí bình thường. Phân tích sinh lý cho thấy VR bị ảnh hưởng bởi cả tỷ lệ khoảng chết của phổi và VCO2 (ml/phút) (Phương trình bổ sung 2-7). Giá trị VR tăng cao sẽ biểu thị khoảng chết ở phổi tăng lên, tăng VCO2 hoặc cả hai. Trước đây, chúng tôi đã báo cáo rằng VR là một yếu tố dự báo độc lập về tỷ lệ tử vong trong hai quần thể thử nghiệm ngẫu nhiên có đối chứng ARDS riêng biệt, nhưng tỷ lệ khoảng chết ở phổi không được đo lường trong một trong hai nghiên cứu đó (6, 7). Do đó, mối quan hệ của VR với tỷ lệ khoảng chết ở phổi trong ARDS vẫn chưa được biết. Về mặt giả thuyết, mối liên quan đáng kể giữa hai biến số sẽ gợi ý rằng VR có thể được sử dụng như một dấu hiệu thực tế tại giường cho tình trạng thông khí bị suy giảm.
Có hai mục tiêu chính cho nghiên cứu này. Đầu tiên, chúng tôi đã thử nghiệm mối quan hệ của VR với khoảng chết phổi đo được trong ARDS. Thứ hai, trong cùng một quần thể, chúng tôi đã kiểm tra xem liệu VR có dự đoán kết quả độc lập với các yếu tố tiên lượng đã biết khác trong một đoàn hệ quan sát lớn hay không. Cuối cùng, trong hai thử nghiệm lâm sàng ngẫu nhiên riêng biệt được NHLBI hỗ trợ, chúng tôi đã tìm cách tái tạo những phát hiện của tập dữ liệu chính.
2 Phương pháp
2.1 Dân số nghiên cứu để phân tích sơ cấp
Dữ liệu được trích xuất từ cơ sở dữ liệu đảm bảo chất lượng ARDS đang được tích lũy triển vọng tại Bệnh viện Đa khoa Zuckerberg San Francisco. Cơ sở dữ liệu được bắt đầu vào tháng 9 năm 2000 sau khi xuất bản nghiên cứu mang tính bước ngoặt của Mạng thử nghiệm lâm sàng NHLBI ARDS (8) và quyết định triển khai các phác đồ máy thở tiêu chuẩn cho bệnh nhân mắc ARDS. Thông khí kiểm soát hỗ trợ thể tích là chế độ máy thở chính được sử dụng khi thực hiện các giao thức này.
Bệnh viện Đa khoa Zuckerberg San Francisco là bệnh viện quận và trung tâm chấn thương cấp 1 liên kết với Đại học California, San Francisco và có nhiều ICU chăm sóc các bệnh nhân nội khoa, phẫu thuật và chấn thương. Bệnh nhân được chẩn đoán mắc ARDS bằng cách sử dụng tiêu chí của Hội nghị đồng thuận Mỹ-Châu Âu về ARDS (xem quy trình chi tiết trong phần bổ sung trực tuyến) (9). Hội đồng đánh giá tổ chức địa phương đã cấp quyền từ bỏ sự đồng ý để xem xét dữ liệu được xác định rõ ràng cho mục đích nghiên cứu.
2.2 Đo đạc
Khí máu động mạch được rút ra đồng thời ghi lại lượng CO2 thở ra trung bình (PECO2) được đo bằng phương pháp đo thể tích capnography (máy theo dõi NICO, Philips/Respironics) và các biến số thông khí khác, như được mô tả trong các nghiên cứu trước đây của chúng tôi (10). Tỷ lệ khoảng chết của phổi được đo bằng phương trình Enghoff-Bohr (VD/VT = [PaCO2 - PECO2]/PaCO2). Chỉ các phép đo đầu tiên của mỗi bệnh nhân mới được sử dụng để phân tích trong nghiên cứu này vì các phép đo khoảng chết lặp đi lặp lại được ghi lại không nhất quán. Chi tiết về quy trình nghiên cứu được nêu trong phần bổ sung trực tuyến.
Ngoài ra, tại thời điểm đo PECO2, loại bỏ CO2 (VCO2) cũng được đo. VCO2 được đo bằng phương pháp capnography theo thể tích là thể tích CO2 thở ra mỗi phút. Ở trạng thái ổn định, giá trị này được coi là đại diện cho khối lượng CO2 được sản xuất mỗi phút. Cả khí máu động mạch và phép đo capnography theo thể tích đều thu được sau một thời gian ổn định trên cài đặt máy thở được chỉ định và sau một thời gian nghỉ ngơi khi bệnh nhân không được điều dưỡng và/hoặc can thiệp vật lý trị liệu.
Trọng lượng cơ thể dự đoán được tính toán bằng công thức mạng NHLBI ARDS (xem phần bổ sung trực tuyến). Giá trị thông khí phút (VE) và PaCO2 tại thời điểm đo PECO2 được sử dụng để tính toán VR bằng Công thức 1. Các biến số hô hấp được ghi đồng thời được sử dụng để tính toán PaO2/FiO2, áp lực đẩy (áp lực bình nguyên - áp lực dương cuối thì thở ra [PEEP]) và chỉ số oxygen hóa [OI = (FiO2 X áp lực đường thở trung bình X 100)/PaO2]. Ngoài VD/VT và VR, chỉ số thứ ba về tình trạng thiếu thông khí được nhóm đồng thuận Berlin sử dụng được gọi là thông khí phút hiệu chỉnh (VEcorr = VE X PaCO2/40) cũng được tính toán (11).
2.3 Phân tích xác minh
Để xác minh những phát hiện trong tập dữ liệu trên, chúng tôi đã thực hiện phân tích thứ cấp của hai thử nghiệm ARDS Mạng NHLBI đa trung tâm. Đầu tiên, để kiểm tra mối tương quan của VD/VT với VR, chúng tôi đã phân tích một nghiên cứu nhỏ về thử nghiệm lâm sàng về albuterol khí dung đối với ARDS (ALTA) (12). Trong nghiên cứu con đó, VD/VT nối tiếp và VCO2 được đo trong 6 ngày ở 126 bệnh nhân. Để sao chép các phép đo trong tập dữ liệu chính, chỉ những bệnh nhân đã thực hiện các phép đo này trong vòng 12 giờ kể từ khi tuyển dụng vào thử nghiệm mới được đưa vào phân tích. Giống như tập dữ liệu chính, các phép đo khí máu động mạch và các biến số thông khí được sử dụng để tính toán VR. Ngoài ra, phép đo VCO2 đã được sử dụng để kiểm tra mối tương quan của nó với VR.
Trong thử nghiệm ngẫu nhiên có đối chứng thứ hai (FACTT), chúng tôi đã kiểm tra khả năng tiên lượng của VR để dự đoán kết quả trong ARDS. Thử nghiệm FACTT đã thu nhận 1.000 bệnh nhân mắc ARDS từ năm 2000 đến năm 2005. Bệnh nhân được chọn ngẫu nhiên để nhận liệu pháp truyền dịch tự do hoặc bảo tồn. Không có phép đo khoảng chết nào được thực hiện trong thử nghiệm này. Các phép đo được gắn nhãn “cài đặt máy thở cơ bản” trong bộ dữ liệu FACTT đã được sử dụng để tính toán VR vì những dữ liệu này là đầy đủ nhất cho VE và PaCO2 và chúng gần nhất với tập dữ liệu chính theo thời gian. Thông tin chi tiết về cả hai thử nghiệm này có thể được tìm thấy trong các báo cáo ban đầu được công bố (13, 14).
Cuối cùng, để kiểm tra tiện ích tiên lượng của VR trong ARDS, chúng tôi đã tiến hành phân tích hậu kỳ sao cho các bộ dữ liệu chính và FACTT được phân tầng bằng cách sử dụng một ngưỡng cắt đơn giản cho VR. Các nhóm được phân tầng thành “VR thấp” nếu VR nhỏ hơn 2 và “VR cao” nếu VR lớn hơn hoặc bằng 2. Giá trị bằng 2 đã được chọn cho mục đích thực tế và gần đúng với giá trị trung bình trong nghiên cứu này và các nghiên cứu trước đây của chúng tôi (7). Ngoài ra, giá trị của 2 cũng gần đúng với ngưỡng chính xác nhất cho VR (1,96) thu được từ mô hình hồi quy logistic đơn biến sử dụng chỉ số Youden (phân tích không được hiển thị) trong tập dữ liệu chính. Sự khác biệt về kết quả lâm sàng được so sánh giữa nhóm VR cao và thấp. Tất cả bệnh nhân đều được đưa vào phân tích phân tầng chính; tuy nhiên, đối với các phân tích thứ cấp trong các phân nhóm mức độ nghiêm trọng của ARDS, bệnh nhân ARDS nhẹ đã bị loại trừ vì hai lý do. Đầu tiên, trong tập dữ liệu chính, tỷ lệ VR cao ở ARDS nhẹ là thấp (n = 18). Thứ hai, các phân tích trước đây của một phần của bộ dữ liệu này cho thấy rằng không có sự khác biệt đáng kể về VD/VT giữa những người sống sót và những người không sống sót với ARDS nhẹ (10).
2.4 Phân tích thống kê
Dữ liệu tham số được trình bày dưới dạng trung bình ± SD và dữ liệu không tham số được trình bày dưới dạng trung vị (phạm vi liên vùng) tùy thuộc vào phân phối của các biến. Để so sánh giữa các nhóm, bài kiểm tra t của Student's được sử dụng cho dữ liệu tham số và bài kiểm tra Mann-Whitney được sử dụng để so sánh dữ liệu không tham số. ANOVA một chiều được sử dụng để so sánh các phương tiện giữa nhiều nhóm. Dữ liệu phân loại được so sánh bằng cách sử dụng thử nghiệm chi bình phương. Đối với dữ liệu thứ tự, phép thử chi bình phương cho các xu hướng được sử dụng để kiểm tra mối liên hệ của biến phụ thuộc giữa các nhóm thứ tự.
Trước đây trong phân tích silico về mối quan hệ giữa VR và VD/VT cho thấy mối quan hệ đường cong giữa các biến (6). Để kiểm tra mối tương quan giữa các biến này, một phép biến đổi tuyến tính của VD/VT đã được thực hiện bằng cách sử dụng công thức sau: 1/[1 - (VD/VT)] (xem Phương trình bổ sung 7) (6). Một hệ số tương quan Pearson đã sửa đổi đã được tính toán để kiểm tra mối quan hệ tuyến tính giữa 1/[1 - (VD/VT)] và VR (15). Việc sửa đổi là cần thiết để hiệu chỉnh sự khớp nối toán học giữa hai biến, cho trước PaCO2 đã được sử dụng để tính toán cả hai. Hệ số tương quan Spearman được sử dụng để kiểm tra mối liên quan giữa sản sinh CO2 (VCO2) và VR. Để kiểm tra sự khác biệt về VD/VT với các giá trị VR tăng lên, chúng tôi chia quần thể thành các phần tư VR và vẽ biểu đồ phân bố VD/VT trong mỗi phần tư.
Để phân tích tiên lượng, chúng tôi sử dụng tỷ lệ tử vong tại bệnh viện và số ngày không thở máy làm thước đo kết quả chính. Đối với tập dữ liệu chính, tỷ lệ tử vong được xác định là tử vong tại bệnh viện, trong khi trong thử nghiệm FACTT, tỷ lệ tử vong được xác định là tỷ lệ tử vong tại bệnh viện trong 60 ngày. Trong FACTT, bệnh nhân xuất viện trước Ngày 60 được cho là còn sống khi kết thúc nghiên cứu (14). Những ngày không có máy thở được định nghĩa là những ngày không có hỗ trợ thở máy xâm lấn cho đến Ngày 28. Tử vong trước thời điểm này được coi là số ngày không có máy thở.
Ngoài điểm Đánh giá sinh lý cấp tính và Đánh giá sức khỏe mãn tính (APACHE), chỉ các biến số hô hấp liên quan đến tỷ lệ tử vong gia tăng trong các nghiên cứu trước đây mới được chọn làm biến dự đoán cho mô hình hồi quy logistic (16 - 18). Tỷ lệ chênh lệch (OR) được tính trên mỗi đơn vị thay đổi của các biến, ngoại trừ VD/VT, trong đó OR được tính trên mỗi mức tăng 0,05 (Công thức 1). Đối với phân tích đa biến, VR và VE-corr là các biến dự đoán chính và được dùng làm mô hình cơ sở. Sự kết hợp giữa quy trình từng bước lùi và loại bỏ các biến có tính tuyến tính cao đã được sử dụng để chọn các biến để điều chỉnh cho mô hình cơ sở (xem phần bổ sung trực tuyến). Tất cả các phân tích được thực hiện bằng phần mềm RStudio phiên bản 1.0.143 (Dự án R dành cho tính toán thống kê).
Bảng 1. Đặc điểm dân số cơ bản với sự phân tầng theo tỷ lệ tử vong tại ICU
| Dân số (n = 520) | Người sống sót (n = 317) | Người không sống sót (n = 203) | Giá trị P | |
| Giới tính, n (%) | ||||
| Nữ giới | 135 (26) | 87 (27) | 48 (24) | 0,755* |
| Nam giới | 376 (72) | 225 (71) | 152 (75) | |
| Chuyển giới | 8 (2) | 5 (2) | 3 (1) | |
| Dân tộc, n (%) | ||||
| Da trắng | 204 (39) | 126 (40) | 78 (38) | 0,845* |
| Gốc Tây Ban Nha | 116 (22) | 73 (23) | 43 (21) | |
| Da đen | 97 (19) | 61 (19) | 36 (18) | |
| Châu Á | 94 (18) | 52 (16) | 42 (21) | |
| Khác | 9 (2) | 5 (2) | 4 (2) | |
| Tuổi, năm | 52 ± 16 | 49 ± 16 | 56 ± 16 | <0,001 |
| Trọng lượng, kg | 82 ± 24 | 84 (25) | 79 (23) | 0,042 |
| Chiều cao (cm) | 169 ± 10 | 170 ± 10 | 169 ± 10 | 0,203 |
| BMI, kg/m2 | 29 ± 8 | 29 ± 8 | 28 ± 8 | 0,165 |
| Điểm APACHE II | 23 (18–31) | 21 (16,25–26,75) | 29 (23–35) | <0,001† |
| Yếu tố rủi ro ARDS, n (%) | ||||
| Viêm phổi | 142 (27) | 95 (30) | 47 (23) | 0,007* |
| Nhiễm trùng huyết | 110 (21) | 62 (20) | 48 (24) | |
| Chấn thương | 108 (21) | 77 (24) | 31 (15) | |
| Hít sặc | 98 (19) | 52 (16) | 46 (23) | |
| Khác | 62 (12) | 31 (10) | 31 (15) | |
| Loại ARDS, n (%) | ||||
| Nhẹ | 79 (15) | 63 (20) | 16 (8) | <0,001* |
| Vừa phải | 243 (47) | 164 (52) | 79 (39) | |
| Nghiêm trọng | 198 (38) | 90 (28) | 108 (53) | |
| Huyết áp tâm thu, mm Hg | 83 ± 27 | 84 ± 24 | 81 ± 31 | 0,177 |
| Bicarbonat, mEq/L | 21 ± 6 | 22 ± 6 | 20 ± 7 | <0,001 |
| Creatinin, mg/dl | 1,6 ± 1,6 | 1,6 ± 1,7 | 1,8 ± 1,5 | 0,163 |
| Bilirubin, mg/dl | 1,8 ± 1,9 | 1,2 ± 1,5 | 2,7 ± 4,2 | <0,001 |
| Số lượng bạch cầu, tế bào/L | 14 ± 11 | 14 ± 10 | 13 ± 11 | 0,341 |
| Tiểu cầu | 180 ± 124 | 202 ± 125 | 146 ± 113 | <0,001 |
| pH | 7,26 ± 0,14 | 7,29 ± 0,13 | 7,22 ± 0,14 | <0,001 |
| Lượng nước tiểu, L/24 giờ | 2,2 ± 1,9 | 2,4 ± 1,7 | 1,9 ± 2,2 | 0,006 |
| Kết quả | ||||
| Tỷ lệ tử vong tại BV | 203 (39%) | |||
| Ngày không máy thở | 5 (0–21) | 19 (10,25–23) | 0 (0–0) | <0,001* |
Định nghĩa chữ viết tắt: APACHE = Đánh giá sinh lý cấp tính và Đánh giá sức khỏe mãn tính; ARDS = hội chứng nguy kịch hô hấp cấp tính; BMI = chỉ số khối cơ thể.
Giá trị P được xác định bằng bài kiểm tra t Student’s trừ khi có quy định khác.
* Kiểm định chi bình phương.
† Phép thử Mann-Whitney.
3 Kết quả
Từ tập dữ liệu chính, trong số 1.017 bệnh nhân được sàng lọc, 685 bệnh nhân được quản lý bằng giao thức mạng ARDS và được xem xét cho nghiên cứu. Trong số này, 520 bệnh nhân nghiên cứu có khoảng chết, VCO2 và chiều cao đo được vào ngày chẩn đoán ARDS và được đưa vào phân tích. Mẫu này đại diện cho 76% bệnh nhân được đo khoảng chết trong khoảng thời gian từ tháng 3 năm 2010 đến tháng 4 năm 2016 (xem Hình E1 trong phần bổ sung trực tuyến). Không có sự khác biệt đáng chú ý về nhân khẩu học, đặc điểm lâm sàng hoặc tỷ lệ tử vong giữa dân số được nghiên cứu và dữ liệu còn thiếu (xem Bảng E1). Các phép đo VD/VT được thực hiện trong vòng 12 giờ kể từ khi bắt đầu quy trình. Chín mươi bảy phần trăm số đo được thực hiện vào ngày bắt đầu ARDS. Thêm 2% phép đo được thực hiện trong vòng 48 giờ kể từ khi khởi phát ARDS và phần còn lại trong vòng 96 giờ. Bảng 1 tóm tắt nhân khẩu học và các đặc điểm cơ bản của dân số được phân tầng theo tình trạng sức khỏe khi xuất viện.
Điểm APACHE II trung bình của tập dữ liệu chính là 23 (18-31). Tổng cộng có 203 (39%) bệnh nhân tử vong trước khi xuất viện. PaO2/FiO2 trung bình là 133 ± 60 mm Hg và thể tích khí lưu thông trung bình là 6,4 ± 1,5 ml/kg. VD/VT trung bình là 0,57 ± 0,17 và VR trung bình là 1,9 ± 0,6. Bảng E2 tóm tắt sự phân bố của các biến số hô hấp tại thời điểm đo capnography theo thể tích với sự phân tầng theo tỷ lệ tử vong trong bệnh viện.
3.1 VR tương quan với khoảng chết nhưng không tương quan với sản xuất CO2 (VCO2)
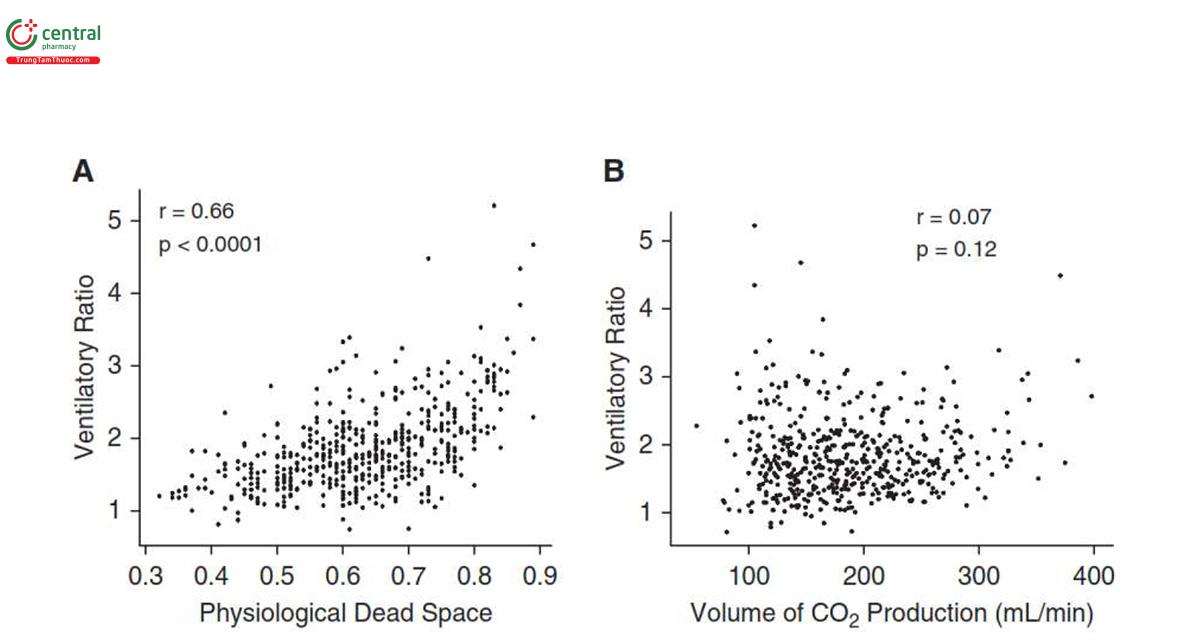
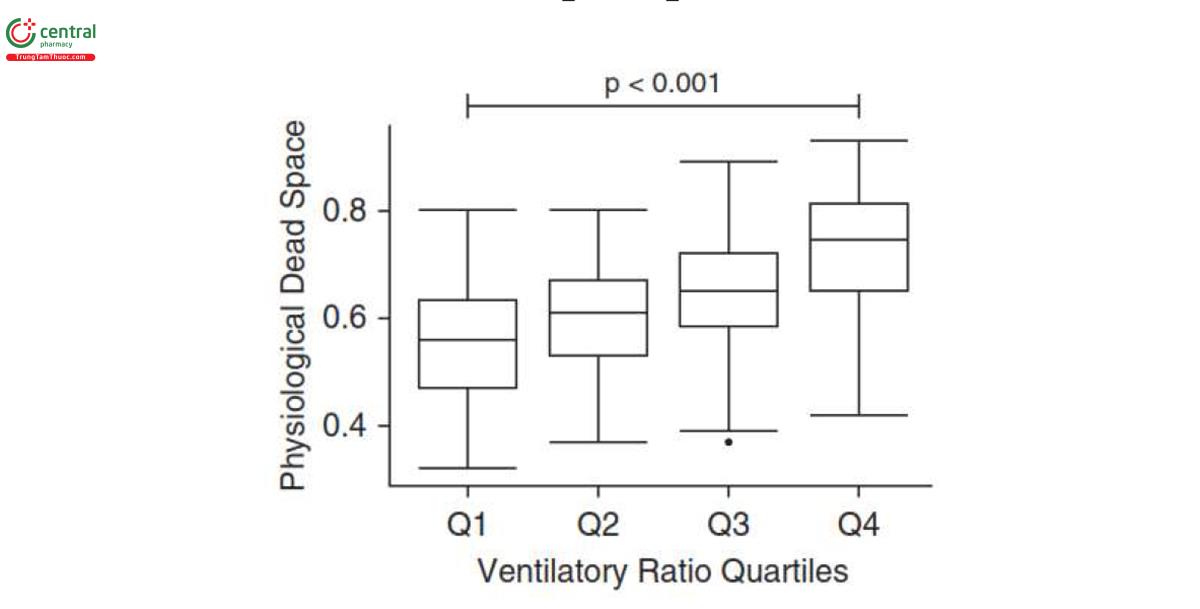
Có mối tương quan tuyến tính dương vừa phải giữa VR và 1/[1 - (VD/VT)] (r đã sửa đổi = 0,66; P < 0,0001) (Hình 1A). Độ dốc tách rời, được hiệu chỉnh cho biến ghép đôi về mặt toán học (PaCO2) rất có ý nghĩa cho thấy mối quan hệ thực sự giữa hai biến số (P < 0,0001). Không có mối tương quan nào được quan sát giữa VR và VCO2 (r = 0,07; P = 0,12) (Hình 1B). Khi chia thành các tứ phân vị thứ tự của VR, VD/VT cao hơn đáng kể ở mỗi tứ phân vị VR tuần tự (P < 0,001) (Hình 2).
3.2 VR là yếu tố dự báo tỷ lệ tử vong tại bệnh viện trong phân tích đa biến
VR cao hơn ở những người không sống sót so với những người sống sót (2,02 ± 0,8 so với 1,75 ± 0,5; P < 0,001) (xem Bảng E2). Trong phân tích hồi quy logistic đơn biến, VR tăng có liên quan đến tỷ lệ tử vong tại bệnh viện tăng (OR, 2,07; khoảng tin cậy [CI], 1,53-2,83). PaO2/FiO2, OI, áp lực đẩy, PEEP, VD/VT và VE-corr cũng liên quan đến việc tăng nguy cơ tử vong trong phân tích đơn biến (xem Bảng E3). Trong phân tích đa biến, VR có liên quan độc lập với tỷ lệ tử vong tăng lên sau khi điều chỉnh tỷ lệ PaO2/FiO2 và áp lực đẩy (OR, 1,51; 95% CI, 1,09-2,12), OI và áp lực đẩy (OR, 1,44) ; 95% CI, 1,01-2,07) và sau khi điều chỉnh điểm APACHE II (OR, 1,59; 95% CI, 1,15-2,32) (Bảng 2). Ngược lại, VE-corr không còn liên quan đến việc tăng nguy cơ tử vong sau khi điều chỉnh tỷ lệ PaO2/FiO2 và áp lực đẩy (xem Bảng E3). Tương tự như vậy, VE-corr không liên quan đến việc tăng nguy cơ tử vong sau khi điều chỉnh điểm OI hoặc APACHE II (dữ liệu không được hiển thị). Điều thú vị là, trong phân tích đa biến, cả PaCO2 (OR, 1,01; 95% CI, 0,98-1,03) hay thông khí phút (OR, 1,04; 95% CI, 0,98-1,12) đều không liên quan đến việc tăng nguy cơ tử vong sau khi điều chỉnh PaO2/FiO2.
3.3 VR tăng theo mức độ nghiêm trọng của bệnh trong ARDS
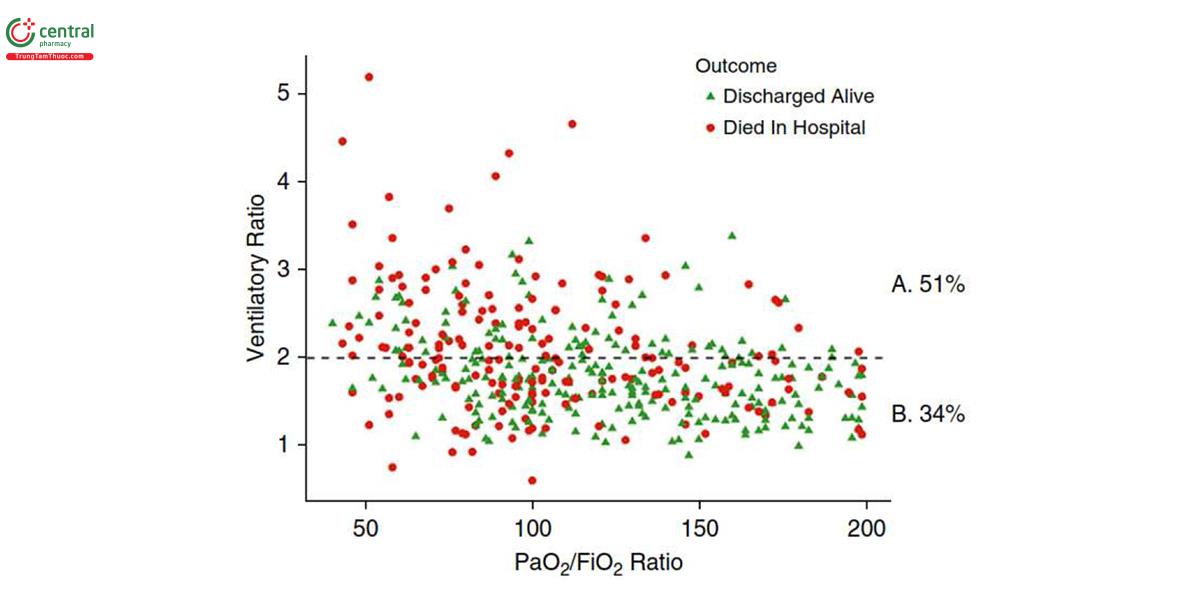
Giá trị trung bình của VR cao hơn đáng kể ở các nhóm ARDS nặng hơn: nhẹ 1,5 ± 0,5, trung bình 1,8 ± 0,5 và nặng 2,1 ± 0,7 (ANOVA, P < 0,001) (xem Hình E2). Tình trạng thiếu oxy máu trầm trọng hơn (PaO2/FiO2) có liên quan đến tình trạng suy giảm thông khí trầm trọng hơn được đo bằng VR (Hình 3). Có mối tương quan nghịch yếu nhưng đáng kể giữa VR và PaO2/FiO2 (Pearson, r = -0,37; CI, -0,29 đến -0,44).
3.4 Nghiên cứu xác minh Xác thực kết quả của nghiên cứu chính
Dữ liệu cần thiết từ thử nghiệm NHLBI ALTA đã có sẵn cho 94 bệnh nhân lúc ban đầu. Như trong tập dữ liệu chính, đã quan sát thấy mối tương quan dương vừa phải giữa VR và 1/[1 - (VD/VT)] (r = 0,64; P < 0,0001). Không có mối tương quan nào được quan sát giữa VR và VCO2 (r = 0,14; P = 0,19) (xem Hình E3). VD/VT cao hơn đáng kể trong các tứ phân vị liên tiếp của VR (P < 0,0001) (xem Hình E4).
Bảng 2. Tỷ lệ chênh lệch cho tỷ lệ tử vong tại ICU sử dụng hồi quy logistic đa biến với tỷ lệ thông khí làm mô hình cơ sở trong bộ dữ liệu chính
| Tỷ số chênh | Khoảng tin cậy 95% | Giá trị P | |
| Phân tích đơn biến | |||
| Tỷ lệ thông khí (mô hình cơ sở) | 2.07 | 1,53–2,85 | <0,001 |
| Phân tích đa biến | |||
| Mô hình cơ sở + tỷ lệ PF | 1,60 | 1,16–2,24 | 0,005 |
| Mô hình cơ sở + tỷ lệ PF + PEEP | 1,48 | 1,06–2,08 | 0,024 |
| Mô hình cơ sở + tỷ lệ PF + DP | 1,51 | 1,09–2,12 | 0,015 |
| Mô hình cơ sở + OI | 1,42 | 1,01–2,03 | 0,045 |
| Mẫu cơ bản + OI + PEEP | 1,42 | 1,00–2,02 | 0,049 |
| Mô hình cơ sở + OI + DP | 1,44 | 1,01–2,07 | 0,047 |
| Mô hình cơ sở + điểm APACHE II | 1,59 | 1,15–2,32 | 0,004 |
Định nghĩa chữ viết tắt: APACHE = Đánh giá sinh lý cấp tính và Đánh giá sức khỏe mãn tính; DP = áp lực đẩy; OI = chỉ số oxygen hóa; PEEP = áp lực dương cuối thì thở ra; Tỷ lệ P/F = tỷ lệ PaO2/FiO2.
Tỷ lệ chênh lệch là trên mỗi đơn vị thay đổi của tỷ lệ thông khí.
Đối với đoàn hệ xác minh thứ hai, dữ liệu đầy đủ đã có sẵn cho 946 bệnh nhân trong thử nghiệm FACTT. VR có liên quan độc lập với việc tăng nguy cơ tử vong trong cả phân tích không điều chỉnh và trong các mô hình được điều chỉnh để kết hợp PaO2/FiO2, OI, PEEP và áp lực đẩy (xem Bảng E5). VR cũng liên quan đến việc tăng tỷ lệ tử vong sau khi điều chỉnh điểm APACHE III. Điều thú vị là, trong quần thể này, trong mô hình được mô tả, tỷ lệ PaO2/FiO2 không còn liên quan độc lập với tỷ lệ tử vong tăng lên (dữ liệu không được hiển thị).
Trong cả ALTA và FACTT, VR cao hơn đáng kể ở các dạng ARDS nghiêm trọng hơn (P = 0,001) và tỷ lệ tử vong cao hơn đáng kể ở các tứ phân vị thứ tự của VR (P < 0,001). Giống như tập dữ liệu chính, trong FACTT, có mối tương quan nghịch khiêm tốn giữa VR và tỷ lệ PaO2/FiO2 (r = -0,32; P < 0,001).
3.5 Phân loại kết quả theo VR: VR cao so với VR thấp
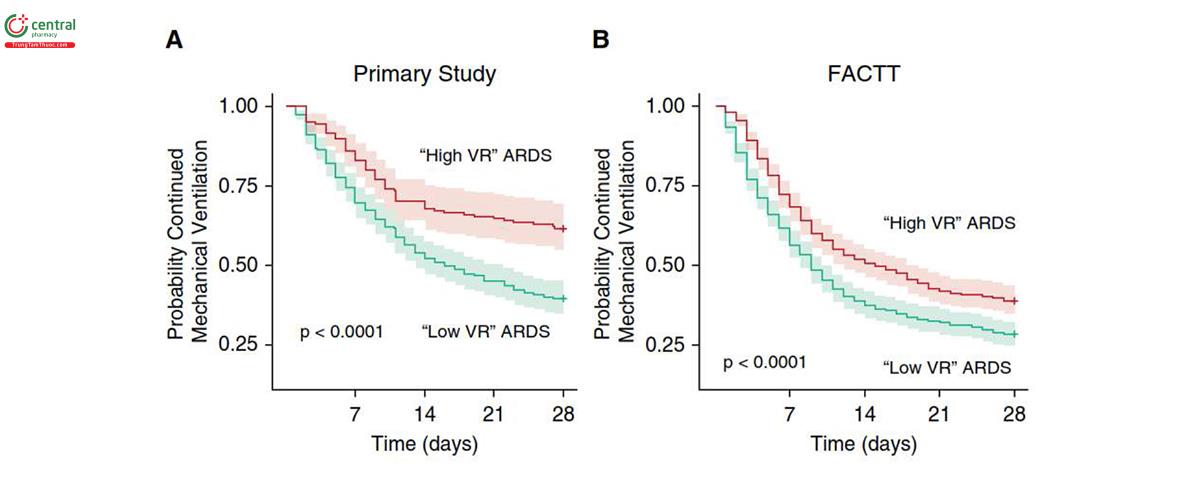
Sử dụng chiến lược phân tầng đơn giản này, chúng tôi nhận thấy tỷ lệ tử vong ở nhóm VR cao cao hơn so với nhóm VR thấp (46% so với 33%; P = 0,003). Sự khác biệt về tỷ lệ tử vong này rõ rệt hơn ở những bệnh nhân mắc ARDS vừa và nặng (51% so với 34%; P <0,001) (Bảng 3) và trong ARDS nặng (61% so với 46%) (Bảng 3). Nguy cơ thở máy kéo dài cũng cao hơn đáng kể ở ARDS có VR cao (Hình 4A).
Bảng 3. ARDS vừa và nặng chia thành các nhóm nhị phân theo VR: Dữ liệu từ Bộ dữ liệu chính
| Nhóm ARDS | N (Tổng) | ARDS có VR thấp (<2) [n (%)] | ARDS có VR cao (≥2) [n (%)] | Giá trị P | ||
| N | Tử vong tại BV | N | Tử vong tại BV | |||
| Tất cả bệnh nhân | 520 | 255 | 83 (33) | 255 | 117 (46) | 0,003 |
| ARDS vừa + nặng | 433 | 217 (50) | 74 (34) | 216 (50) | 110 (51) | <0,001 |
| ARDS vừa phải | 238 | 136 (57) | 37 (27) | 102 (43) | 41 (40) | <0,001 |
| ARDS nặng | 195 | 81 (42) | 37 (46) | 114 (58) | 69 (61) | <0,001 |
Định nghĩa: ARDS = hội chứng nguy kịch hô hấp cấp tính; N = số lượng quan sát; VR = tỷ lệ thông khí. Giá trị P đại diện cho phép thử chi bình phương.
“ARDS có VR thấp” dùng để chỉ những bệnh nhân có VR <2. “ARDS có VR cao” dùng để chỉ VR ≥2.
Bảng 4. ARDS vừa và nặng chia thành các nhóm nhị phân theo VR: Dữ liệu từ Bộ dữ liệu FACTT
| Nhóm ARDS | N (Tổng) | ARDS có VR thấp (<2) [n (%)] | ARDS có VR cao (≥2) [n (%)] | Giá trị P | ||
| N | Tử vong tại BV | N | Tử vong tại BV | |||
| Tất cả bệnh nhân | 946 | 477 | 107 (22) | 469 | 140 (30) | 0,011 |
| ARDS vừa + nặng | 731 | 326 (45) | 70 (21) | 405 (55) | 123 (30) | 0,007 |
| ARDS vừa phải | 491 | 276 (56) | 60 (22) | 225 (44) | 52 (24) | 0,521 |
| ARDS nặng | 240 | 76 (32) | 20 (26) | 164 (68) | 61 (37) | 0,097 |
Định nghĩa chữ viết tắt: ARDS = hội chứng nguy kịch hô hấp cấp tính; FACTT = Thử nghiệm điều trị bằng dịch truyền và ống thông; N = số lượng quan sát; VR = tỷ lệ thông khí.
Giá trị P đại diện cho phép thử chi bình phương.
“ARDS có VR thấp” dùng để chỉ những bệnh nhân có VR <2. “ARDS có VR cao” dùng để chỉ VR ≥2.
Những phát hiện này cũng được lặp lại trong bộ dữ liệu FACTT, mặc dù tỷ lệ tử vong chung thấp hơn và thời gian thở máy thấp hơn. Tỷ lệ tử vong cao hơn ở ARDS có VR cao so với VR thấp (30% so với 22%; P = 0,007) (Bảng 4). Tương tự, nguy cơ thở máy kéo dài cũng cao hơn đáng kể ở những bệnh nhân có VR cao trong bộ dữ liệu FACTT (Hình 4B).
4 Thảo luận
Các kết quả chính của nghiên cứu này có thể được tóm tắt như sau. VR tương quan dương với khoảng chết ở phổi ở bệnh nhân mắc ARDS. Giá trị VR cao hơn có liên quan đến khoảng chết ở phổi cao hơn. Trong phân tích đa biến, VR có liên quan độc lập với việc tăng nguy cơ tử vong tại bệnh viện sau khi điều chỉnh sự kết hợp của các dấu hiệu hỗ trợ cơ học và tình trạng thiếu oxy máu (Bảng 2; xem Bảng E5). VR cũng vẫn liên quan đến việc tăng nguy cơ tử vong sau khi điều chỉnh điểm APACHE (Bảng 2; xem Bảng E5). Hơn nữa, chúng tôi đã chứng minh tiện ích tiên lượng của VR ở mức cơ bản trong một nhóm thử nghiệm ngẫu nhiên có đối chứng và quan sát. Những phát hiện của nghiên cứu này xác nhận giả thuyết rằng VR có thể được sử dụng như một chỉ số đơn giản tại giường về tình trạng suy giảm thông khí và về cơ bản, nó là một dấu hiệu sinh lý tiên lượng hữu ích trong ARDS.
Mười sáu năm đã trôi qua kể từ khi nghiên cứu của Nuckton và đồng nghiệp (1) cho thấy tỷ lệ khoảng chết ở phổi là một yếu tố dự báo độc lập về tỷ lệ tử vong trong ARDS. Một số nghiên cứu kể từ thời điểm đó đã củng cố những phát hiện này (12, 19, 20). Tuy nhiên, việc đo khoảng chết ở phổi và suy giảm thông khí phần lớn vẫn chưa được sử dụng trong thực hành lâm sàng hoặc như một biến số nghiên cứu. Cách tiếp cận hiện tại của chúng tôi để phân tầng trong ARDS đã bỏ qua sự bất thường sinh lý chính này. Trong nghiên cứu được trình bày, phân tích dữ liệu FACTT cho thấy PaO2/FiO2 không còn là yếu tố dự báo độc lập về tỷ lệ tử vong khi được điều chỉnh theo VR. Những phát hiện này làm tăng thêm mối lo ngại được nêu ra bởi những người khác (21, 22), rằng PaO2/FiO2 có những hạn chế khi là biến phân tầng chính trong ARDS.
Khi mức độ nghiêm trọng của ARDS tăng lên, các đơn vị phế nang có thông khí/tưới máu không đồng nhất dẫn đến thiếu oxy và tăng CO2, phần nào giải thích mối tương quan nghịch giữa VR và PaO2/FiO2. Tuy nhiên, hầu hết, thông khí và oxygen hóa là các quá trình khác biệt về mặt sinh lý và do đó mối tương quan quan sát được giữa hai biến số là yếu (Hình 3), chỉ ra rằng thông tin tiên lượng và sinh lý bệnh do VR cung cấp không thể được trích xuất chỉ từ tỷ lệ PaO2/FiO2 và ngược lại.
Ưu điểm của VR là nó có thể được tính toán dễ dàng bằng cách sử dụng các biến số thông thường tại đầu giường. Giá trị của nó phản ánh khả năng bài tiết carbon dioxide đầy đủ của phổi. Như được nhấn mạnh trong Công thức bổ sung 7, VR được xác định bởi cả VD/VT và quá trình sản xuất CO2 (VCO2). VR không phải là số đo trực tiếp của VD/VT và không thể dùng để ước tính giá trị của nó. Tuy nhiên, mối quan hệ giữa hai biến thể hiện trong nghiên cứu này chỉ ra rằng VR, giống như VD/VT, có thể là một chỉ số hữu ích tại giường để theo dõi tình trạng suy giảm thông khí ở những bệnh nhân nguy kịch. Những phát hiện này trong ARDS tương tự với những phát hiện trước đây của chúng tôi ở những bệnh nhân suy hô hấp thiếu oxy cấp tính (23). Mặc dù hệ số tương quan thấp hơn trong nghiên cứu hiện tại (r = 0,66 và r = 0,64 so với r = 0,71), cỡ mẫu được tăng cường đáng kể trong nghiên cứu được trình bày làm tăng thêm sức mạnh và tính tổng quát của mối quan hệ được quan sát của các biến.
Ngược lại, sự thiếu tương quan giữa VR và VCO2 chỉ ra rằng so với VD/VT, VCO2 là yếu tố quyết định ít ảnh hưởng hơn đến VR. Sản xuất carbon dioxide là một yếu tố quan trọng trong cân bằng nội môi CO2 ở những bệnh nhân bị bệnh nặng và tác động đến bất kỳ biện pháp suy giảm thông khí nào, có thể là VR hoặc VD/VT. Các yếu tố ảnh hưởng đến tốc độ trao đổi chất cơ bản, chẳng hạn như ăn uống và nhiễm trùng huyết, có thể làm thay đổi VCO2 (24). Ngoài ra, các can thiệp điều dưỡng, vật lý trị liệu và đặt lại máy thở cũng được biết là có ảnh hưởng đến VCO2, mặc dù chỉ thoáng qua (25).
Trong điều kiện hoạt động bình thường, để đáp ứng với sự gia tăng VCO2, phổi có thể tăng cường đào thải CO2 bằng cách tăng thông khí phút. Trong ARDS, có hai yếu tố hạn chế những phản ứng này. Đầu tiên, khả năng tăng thông khí phút có thể bị suy giảm hoặc bị hạn chế một cách cố ý để đạt được thông khí bảo vệ phổi. Thứ hai, khả năng loại bỏ CO2 bị suy giảm do sự không phù hợp giữa thông khí và tưới máu. Ảnh hưởng chính xác của VCO2 về nhu cầu thông khí ở bệnh nhân nguy kịch vẫn chưa được biết. Ravenscraft và đồng nghiệp (26) phát hiện ra rằng khoảng chết là yếu tố chính quyết định thông khí phút quá mức ở bệnh nhân ICU thở máy. Cụ thể, các tác giả nhận thấy rằng trong ARDS giai đoạn đầu, sự đóng góp của VCO2 đến mức thông khí phút vượt mức là tối thiểu. Những phát hiện này tương tự với dữ liệu được trình bày trong nghiên cứu này.
Bất kể, VCO2 chắc chắn sẽ giải thích cho một số khác biệt quan sát được giữa VR và VD/VT. Cho rằng VR được điều chỉnh theo chiều cao của từng cá nhân, một số phương sai tự nhiên trong VCO2 quan sát được trên các quần thể được đưa vào tỷ lệ. Tuy nhiên, những cá nhân có cùng một phần khoảng chết có thể có VR khác nhau tùy thuộc vào VCO2. Khó có khả năng là ảnh hưởng của VCO2 đồng nhất cho cả VR và VD/VT do đó dẫn đến một số phương sai quan sát được giữa hai biến.
Nguồn phương sai tiềm ẩn thứ hai giữa VR và VD/VT là VR giả định mối quan hệ tuyến tính giữa VE và PaCO2. Tuy nhiên, mối quan hệ sinh lý của thể tích khí lưu thông với PaCO2 được biết là không có triệu chứng. Hơn nữa, đối với cùng một thông khí phút, tỷ lệ thể tích khí lưu thông và nhịp thở ảnh hưởng đến VD/VT là khác nhau. Ví dụ, giả sử phần giải phẫu của khoảng chết là không đổi, việc giảm thể tích khí lưu thông và tăng nhịp thở để duy trì thông khí phút như nhau, sẽ làm tăng VD/VT, nhưng VR tạm thời sẽ không thay đổi. Bất kỳ sự gia tăng nào như vậy về VD/VT theo thời gian sẽ dẫn đến giảm khả năng loại bỏ CO2 và tăng PaCO2, lượng khí này sẽ được VR thu giữ. Hạn chế này của VR nhấn mạnh tầm quan trọng của việc đạt được khoảng thời gian ổn định trên cài đặt thông khí được quy định trước khi tính toán VR để giải thích tối ưu giá trị của nó.
Các nguồn khác biệt khác giữa VR và VD/VT có thể là do ảnh hưởng của hệ thống tim mạch lên VD/VT theo phương trình Enghoff-Bohr. Cả hai trạng thái shunt và cung lượng tim thấp đều là những yếu tố quyết định VD/VT. Sự gần đúng giữa PCO2 động mạch và PCO2 phế nang (xem Công thức bổ sung 6) là một giả định phổ biến đối với cả Enghoff-Bohr VD/VT và VR. Do đó, tỷ lệ shunt tăng dẫn đến tăng hỗn hợp tĩnh mạch dẫn đến PaCO2 tăng cao. Điều này dẫn đến sự gia tăng VD/VT mà không phải là yếu tố trực tiếp làm suy giảm thông khí (3). Hiện tượng này cũng sẽ được quan sát thấy trong VR. Tuy nhiên, điều không thể xảy ra là việc tăng VR sẽ tỷ lệ thuận với VD/VT, dẫn đến một số phương sai giữa hai biến.
Cung lượng tim thấp cũng có thể ảnh hưởng đến VD/VT (27). Giảm lưu lượng máu phổi ở trạng thái cung lượng tim thấp dẫn đến giảm cung cấp CO2 phế nang và giảm đào thải CO2. Điều này lần lượt dẫn đến PỆ CO2 thấp hơn và do đó VD/VT tăng lên, một lần nữa đây là đặc điểm của tưới máu hơn là thông khí. Tuy nhiên, không giống như shunt, VR khó có khả năng ảnh hưởng đến trạng thái tim thấp đến quá trình trao đổi khí. Sự đóng góp của tưới máu lên VD/VT có nhiều khả năng biểu hiện hơn trong các trường hợp khi VD/VT cao (> 0,75) và phần nào có thể giải thích tại sao mối tương quan với VR không mạnh bằng trong phạm vi này (Hình 1A). Điều thú vị là, ở trạng thái cung lượng tim thấp, có thể hình dung rằng VR có thể là thước đo chính xác hơn về tình trạng suy giảm thông khí so với v; tuy nhiên, lý thuyết này cần được đánh giá trong tương lai.
Bất chấp các nguồn phương sai được nêu ra, dữ liệu được trình bày chỉ ra rằng VR và tỷ lệ khoảng chết ở phổi là các biến số có liên quan chặt chẽ với nhau. Do đó, không có gì đáng ngạc nhiên khi VR, giống như khoảng chết trong phổi, là một yếu tố dự đoán kết quả trong ARDS. Những phát hiện trong nghiên cứu này phù hợp với nghiên cứu trước đây của chúng tôi, nghiên cứu này cũng cho thấy VR có liên quan đến việc tăng nguy cơ tử vong trong các thử nghiệm Mạng lưới NHLBI ARDS (7). Hơn nữa, những phát hiện này hiện cũng có thể khái quát hóa cho các nhóm quan sát ARDS.
Các tác giả của định nghĩa ARDS ở Berlin đã thử tầm quan trọng của nghiên cứu về tình trạng suy giảm thông khí. Họ đã sử dụng VE-corr làm dấu hiệu cho thấy tình trạng suy giảm thông khí trong ARDS và không tìm thấy giá trị tiên lượng nào (11, 28). Trong nghiên cứu hiện tại, và như các nhà điều tra Berlin đã ám chỉ, thông khí phút đã điều chỉnh không còn là yếu tố dự đoán kết quả một khi đã điều chỉnh PaO2/FiO2. Những phát hiện này cho thấy VR hoạt động tốt hơn thông khí phút đã điều chỉnh. Các mô hình khác cũng đã được mô tả để ước tính khoảng chết ở phổi (29). So với VR, sự phức tạp vốn có của các mô hình đa biến này khiến chúng không hấp dẫn khi sử dụng trên lâm sàng và phủ nhận bất kỳ giá trị nào có được từ mối tương quan mạnh hơn với tỷ lệ khoảng chết phổi đo được. Sự khan hiếm trong việc áp dụng các mô hình này và đo khoảng chết của phổi trong thực hành lâm sàng nhấn mạnh tầm quan trọng của tính thực dụng và tính đơn giản của VR, mặc dù có những hạn chế cố hữu đã biết.
Khi tiến hành nghiên cứu về các hội chứng không đồng nhất, chẳng hạn như ARDS, việc làm giàu tiên lượng không cần giới hạn ở các phép đo sinh học. Các phương pháp sinh lý thực tế do VR cung cấp có thể hữu ích (30). Các nghiên cứu gần đây cho thấy phân tầng theo mức độ nghiêm trọng của tình trạng thiếu oxy máu là một chiến lược hữu ích trong nghiên cứu ARDS (31, 32). Tương tự, dữ liệu từ nghiên cứu này chỉ ra rằng việc kết hợp VR trong sàng lọc các thử nghiệm lâm sàng có thể tạo điều kiện thuận lợi cho việc cải thiện tiên lượng và cho phép một cách tiếp cận có ý nghĩa hơn về mặt sinh lý đối với việc lựa chọn bệnh nhân (Bảng 2 Và Hình 3).
Hơn nữa, trái ngược với PaO2/FiO2 (21), thông khí suy giảm, được đo bằng phân số khoảng chết của phổi, được biết đến là một biến số đáng tin cậy hơn và duy trì giá trị tiên lượng theo thời gian (20, 33). Ngoài khả năng tiên lượng, việc đo tỷ lệ khoảng chết của phổi cũng được chứng minh là một biến số hữu ích khi tối ưu hóa PEEP, dự đoán thất bại của rút ống nội khí quản và theo dõi đáp ứng với tư thế nằm sấp (34 - 38). Giả sử rằng các chiến lược thông khí không thay đổi, VR có thể là một biến số tiên lượng ổn định hơn PaO2/FiO2 và các giá trị delta của nó trong từng cá nhân có thể được sử dụng như một công cụ để theo dõi tình trạng suy giảm thông khí sau các biện pháp can thiệp. Cần có các nghiên cứu sâu hơn để kiểm tra tiện ích tiên lượng của VR qua các thời điểm khác nhau, ở các chế độ thông khí khác nhau và các biện pháp can thiệp trị liệu sau đây để kiểm tra các giả thuyết này. Sự đơn giản của việc tính toán VR có thể làm tăng tính khả thi của các nghiên cứu kiểm tra vai trò của tình trạng thông khí bị suy giảm trong bối cảnh lâm sàng.
Để chứng minh giá trị của VR như một biến phân tầng, chúng tôi đã tạo một sơ đồ đơn giản chia nhỏ định nghĩa Berlin thành ARDS với VR thấp, trong đó VR nhỏ hơn 2 và ARDS với VR cao, trong đó VR lớn hơn hoặc bằng 2 (Bảng 3 và Hình 4). Trong tập dữ liệu chính, sử dụng cách phân tầng đơn giản này, tỷ lệ tử vong cao hơn ở nhóm VR cao trong tổng dân số và ở ARDS mức độ trung bình và nặng. Trong FACTT, tỷ lệ tử vong ở nhóm VR cao cũng cao hơn đáng kể. Tuy nhiên, trong các nhóm mức độ nghiêm trọng của ARDS, có xu hướng tỷ lệ tử vong cao hơn nhưng điều này không có ý nghĩa thống kê.
Một phần, những phát hiện này có thể được giải thích là do tỷ lệ tử vong chung trong FACTT thấp hơn so với tập dữ liệu chính. Những phát hiện này phù hợp với xu hướng đã được thiết lập hướng tới kết quả lâm sàng tốt hơn trong các thử nghiệm ngẫu nhiên có đối chứng so với các nghiên cứu quan sát vì các tiêu chí thu nhận trước đây nghiêm ngặt hơn (39). Một hạn chế khác trong bộ dữ liệu FACTT có thể giải thích những phát hiện này là các phép đo PCO2 động mạch được sử dụng để tính VR có thể không đồng thời với các bản ghi thông khí phút ở tất cả các bệnh nhân. Hướng dẫn thử nghiệm ban đầu nêu rõ: “Nếu không có khí máu trong thời gian tham chiếu, hãy sử dụng các giá trị gần nhất với thời gian tham chiếu trong cùng một ngày theo lịch”.
Nghiên cứu này có những hạn chế khác. Mặc dù dữ liệu được tích lũy theo triển vọng nhưng tất cả các tập dữ liệu đều được thẩm vấn hồi cứu. Ngoài ra, chỉ có một điểm thời gian duy nhất được sử dụng để tính toán VR, hạn chế việc giải thích giá trị của nó đối với tiên lượng cơ bản. Hơn nữa, hiệu chỉnh được sử dụng cho khớp nối toán học khi kiểm tra mối tương quan giữa VR và phần khoảng chết của phổi là một hạn chế lớn trong việc ngoại suy những dữ liệu này thành giá trị delta ở các cá nhân.
Một hạn chế khác của nghiên cứu là mặc dù các phép đo khoảng chết và VR trong nghiên cứu này được thực hiện với các bệnh nhân ở chế độ thông khí bắt buộc, nhưng không thể xác định liệu nỗ lực hô hấp tự phát bổ sung có được thực hiện tại thời điểm đo này hay không. Nhịp thở tự nhiên có thể đã dẫn đến những thay đổi động học trong cả VR và khoảng chết của phổi, điều này có thể dẫn đến sự khác biệt lớn hơn giữa hai biến số (40). Dữ liệu về việc sử dụng thuốc gây tê và mức độ an thần cũng không có sẵn và có thể ảnh hưởng đến suy giảm thông khí. VR cũng vẫn chưa được kiểm tra ở những bệnh nhân được thở máy ở chế độ hỗ trợ áp lực. Các nghiên cứu tiền cứu là cần thiết để giải quyết những hạn chế này.
Tóm lại, VR là một phương pháp đơn giản và có căn cứ về mặt sinh lý để đánh giá tình trạng suy giảm thông khí ở đầu giường. VR tương quan với khoảng chết ở phổi và giá trị cao hơn có liên quan đến việc tăng nguy cơ tử vong. VR hứa hẹn là một phương pháp đơn giản để phân loại bệnh nhân ARDS thành các nhóm nhỏ có ý nghĩa lâm sàng và có thể là một công cụ hữu ích để cải thiện tiên lượng trong các thử nghiệm lâm sàng trong tương lai.

