Hướng dẫn phân biệt u buồng trứng lành tính và ung thư buồng trứng
Nguồn: Giáo trình Sản phụ khoa - Tập 2: Phụ khoa.
Đại học Huế - Trường ĐH Y Dược
Đồng chủ biên:
GS.TS. Nguyễn Vũ Quốc Huy,
GS.TS. Cao Ngọc Thành,
PGS.TS. Lê Minh Tâm,
PGS.TS. Trương Thành Vinh,
Cùng nhiều tác giả tham gia biên soạn.
1 PHẦN A. KHỐI U BUỒNG TRỨNG LÀNH TÍNH
U nang buồng trứng (Ovarian cyst) là khối u buồng trứng có vỏ mỏng bên trong có chứa dịch đơn thuần hay phối hợp với các thành phần khác. Bệnh thường gặp ở mọi lứa tuổi, nhiều nhất từ 30-45 tuổi. Chẩn đoán tương đối dễ nhưng triệu chứng và tiến triển phức tạp nên việc điều trị và tiên lượng còn gặp nhiều khó khăn.
1.1 PHÂN LOẠI KHỐI U BUỒNG TRỨNG LÀNH TÍNH
1.1.1 Nang cơ năng (Functional ovarian cysts)
Đây là loại nang thường gặp, không do tổn thương giải phẫu, hình thành do bất thường về hoạt động chức năng buồng trứng. Đường kính thường nhỏ hơn 6cm, có loại lớn nhanh nhưng biến mất nhanh, chỉ tồn tại sau vài chu kỳ kinh nguyệt. Có ba loại nang cơ năng:
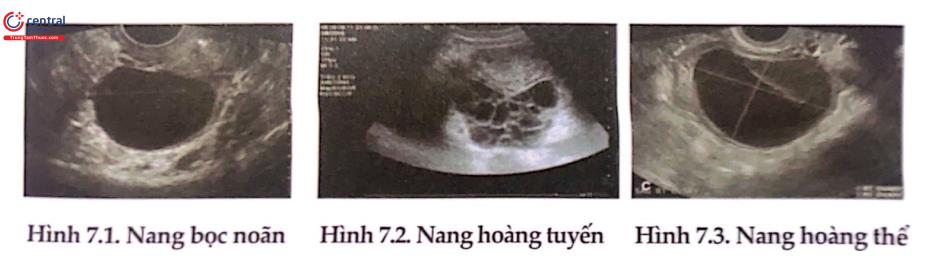
1.1.1.1 Nang bọc noãn (Follicular cysts)
Được sinh ra từ nang De Graaf (nang trội) không vỡ như sinh lý, tiếp tục tiết estrogen, kích thước thường nhỏ, chứa dịch màu vàng, giàu estrogen. Thường tự biến mất trong vòng 6 tuần.
1.1.1.2 Nang hoàng thể (Corpus luteum cysts)
Đây là loại u nang không phổ biến. Xuất phát từ hoàng thể, nang chế tiết nhiều estrogen và progesterone. Có hai loại nang hoàng thể đã được ghi nhận. Nang hoàng thể phì đại nhẹ, có thể vẫn tiếp tục sản xuất Progesterone dài ngày hơn so với thông thường. Kỳ kinh nguyệt bị trì hoàn từ vài ngày đến vài tuần, thông thường là trong vòng hai tuần so với chu kỳ đã lỡ, gọi là nang hoàng thể tồn lưu. Nang hoàng thể to nhanh do xuất huyết trong nang vào giai đoạn hoàng thể của chu kỳ kinh nguyệt được gọi là nang hoàng thể xuất huyết, có thể diễn tiến tới vỡ muộn trong giai đoạn hoàng thể.
1.1.1.3 Nang hoàng tuyến (Theca Lutein Cysts)
Đây là loại nang hiếm gặp nhất và liên quan đến thai kỳ. Có nhiều nang phi đại cùng lúc. Thường xuất hiện ở cả hai bên, thường gặp ở bệnh nhân đa thai, bệnh lý tế bào nuôi hoặc kích thích buồng trứng trong hỗ trợ sinh sản, do tăng hCG. Khi khỏi bệnh nguyên bào nuôi, nang hoàng tuyến sẽ biến mất.
1.1.2 Khối u buồng trứng tân sinh lành tính (Benign neoplastic ovarian cysts)
Các cấu trúc tân sinh được phân loại dựa trên nguồn gốc mô học bao gồm: u biểu mô (epithelial tumors), u tế bào mầm (germ cell tumors), u mô đệm – thừng sinh dục (sex cord-stromal tumors) và các u khác.
1.1.2.1 Các khối u biểu mô lành tính
Đây là loại thường gặp nhất của cấu trúc tân sinh buồng trứng, chiếm 50-60% các khối u buồng trứng. Các u thường gặp bao gồm:
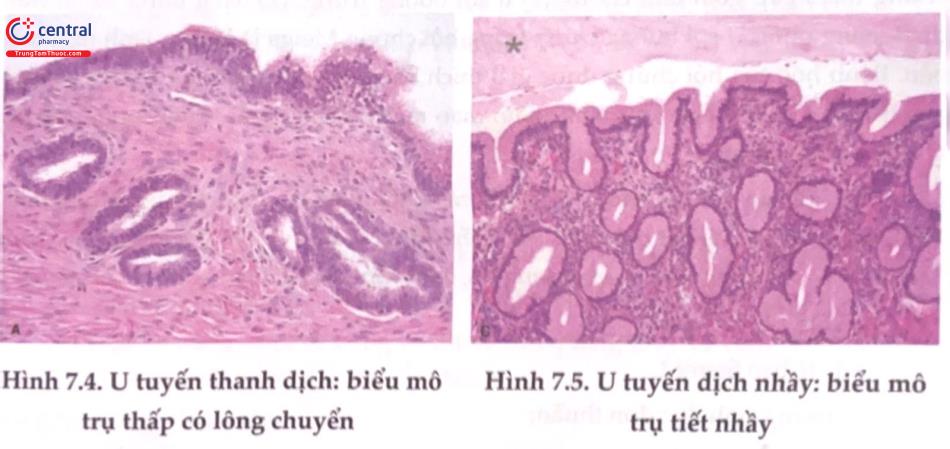
U tuyến thanh dịch (Serous cystadenoma): Thường xảy ra trong độ tuổi sinh sản, u có bề mặt trơn láng, vỏ mỏng, đơn thùy hoặc đa thùy, bên trong chứa dịch trong hoặc vàng chanh.
U tuyến dịch nhầy (Mucinous cystadenoma): Là loại u to nhất có khi nặng 40-50kg, có khi lấp đầy khoang chậu và chèn ép vào khoang bụng hay dính các tạng xung quanh, u nang có nhiều thùy. Dịch trong nang đặc hay dịch nhầy, màu vàng nhạt hay nâu.
Ngoài ra, u biểu mô lành tính còn bao gồm: u dạng nội mạc tử cung (endometrioid), u tế bào sáng (clear cell), u Brenner.
1.1.2.2 Các khối u tế bào mầm lành tính
U quái: U quái phát sinh từ một tế bào mầm duy nhất và do đó có thể chứa bất kỳ hợp phần nào trong ba lớp mầm: Ngoại bì, trung bì hoặc nội bì. Khoảng 95% các u quái là trưởng thành. U quái trưởng thành lành tính có dạng nang bì, chứa các mô trưởng thành mà thành phần thường gặp nhất là các cấu trúc ngoại bì gồm da, nang tóc, răng tuyến bã.
.jpg)
1.1.2.3 Các khối u mô đệm – thùng sinh dục lành tính
Khối u xuất phát từ mô đệm sinh dục thường là các u xuất phát từ mô đệm hay từ thừng sinh dục, có thể đơn thuần hay kết hợp.
U mô đệm đơn thuần:
U sợi (fibroma) và hội chứng Demons - Meigs: Hội chứng Meigs là một hội chứng hiếm gặp gồm tam chứng (1) u sợi buồng trứng, (2) báng bụng và (3) tràn dịch màng phổi. U sợi buồng trứng trong hội chứng Meigs là khối u lành tính một bên. Bệnh học của hội chứng được giải thích bằng các yếu tố tăng trưởng nội mạc mạch máu (VEGF) làm tăng tính thấm mao mạch. Bệnh thoái triển sau khi cắt bỏ khối u buồng trứng.
U tế bào vỏ (thecoma): Hầu hết các khối u tế bào vỏ xuất hiện ở tuổi mãn kinh. U tế bào vỏ chế tiết estrogen. Rất hiếm khi u tế bào vỏ chế tiết androgen. Trên đại thể, u là một u đặc. Tổn thương dạng sợi, màu vàng điển hình do hormones steroid.
U tế bào Leydig.
U tế bào Steroid.
U thừng sinh dục đơn thuần:
U tế bào hạt (granulosa cell tumor): U có đặc trưng vi thể của tế bào hạt và chế tiết estrogen. U tế bào hạt là loại u thừng giới bào thường gặp. U thường xảy ra ở một bên, kích thước trung bình 15cm. U có dạng nang, mật độ mềm hoặc chắc.
Nhìn mặt cắt của khối u giống với u tuyến nhầy, nhưng chứa đầy dịch máu; 95% type mô học trưởng thành, xảy ra vào những năm đầu sau mãn kinh (adult granulosa tumour); 5% type mô học trẻ xảy ra giữa dậy thì và những năm đầu thời kỳ sinh sản (juvenile granulosa tumour).
U tế bào Sertoli: hiếm gặp, thường xảy ra ở người dưới 30 tuổi và chế tiết trong hơn 95% trường hợp. U Sertoli đơn thuần thường có xu hướng chế tiết estrogen.
U hỗn hợp mô đệm và thừng sinh dục: U tế bào Sertoli – Leydig: hiếm gặp, chế tiết androgen, vì vậy biểu hiện rậm lông, phì đại âm vật, gây dậy thì sớm. các khảo sát như Testosterone, androstenedione và tiền chất 17-hydroxyprogesterone có thể có giá trị.
1.2 CHẨN ĐOÁN
1.2.1 Triệu chứng cơ năng
U nang nhỏ: Triệu chứng thường nghèo nàn, khối u tiến triển chậm, bệnh nhân vẫn hoạt động bình thường, được phát hiện khi khám sức khỏe, khám phụ khoa hay siêu âm.
Trường hợp u lớn: Cảm giác nặng bụng dưới, có dấu hiệu chèn ép các tạng xung quanh gây tiểu rắt, bí tiểu, bí đại tiện.
1.2.2 Triệu chứng thực thể
U to, thấy bụng dưới to lên như mang thai, sờ thấy khối u di động, có khi đau. Khám âm đạo tử cung nhỏ, cạnh tử cung có khối tròn đều, di động dễ dàng ranh giới biệt lập với tử cung.
Trường hợp u dính hay u trong dây chằng rộng thì di động hạn chế, có khi kẹt trong tiểu khung. Chú ý, khi khám không nên đè mạnh hay đẩy lên có thể gây vỡ nang.
1.2.3 Cận lâm sàng
Xét nghiệm hCG âm tính.
Siêu âm thấy khối u ranh giới rõ.
Soi ổ bụng chẩn đoán chỉ làm khi khối u nhỏ, nghi ngờ thai lạc chỗ.
Chụp bụng không chuẩn bị nếu là u nang bì sẽ thấy cản quang.
Chụp tử cung - vòi tử cung có thuốc cản quang thấy tử cung lệch một bên, vòi tử cung bên khối u kéo dài ôm lấy khối u.
1.2.4 Chẩn đoán phân biệt
Có thai: tắt kinh, tử cung to, mềm, hCG (+).
Ứ dịch vòi tử cung: có tiền sử viêm nhiễm, thường viêm 2 bên.
Thai ngoài tử cung thể huyết tụ thành nang: chậm kinh, rong huyết, có khối cạnh tử cung đau.
U xơ tử cung (UXTC) có cuống: siêu âm có thể gợi ý, nội soi chẩn đoán trong trường hợp khó xác định.
Báng: gõ đục toàn bụng khám khối u không rõ.
Lách to: có tiền sử sốt rét hay các bệnh về máu, khối u ở cao.
Thận đa nang, u mạc treo: khối u cao, chạm cực dưới khó khăn.
Bàng quang đầy nước tiểu: cần thông tiểu trước khi khám.
Một số trường hợp khó, cần khám kỹ, kết hợp lâm sàng, cận lâm sàng để xác định thêm.
1.3 BIẾN CHỨNG
1.2.4.1 Xoắn u nang
Khối u buồng trứng có thể gây ra biến chứng xoắn phần phụ. Đây là biến chứng hay gặp nhất và chiếm khoảng 3% các trường hợp cấp cứu phụ khoa, thường xảy ra trong độ tuổi sinh sản. Có 2 dạng xoắn
Xoắn cấp tính: Xảy ra đột ngột, đau bụng dữ dội, có thể ngất, mạch, huyết áp ổn định, có thể kèm buồn nôn hoặc nôn. Khám ấn vào khối u rất đau, di động hạn chế.
Xoắn bán cấp: Đau âm ỉ, giảm khi thay đổi tư thế, sau đó thỉnh thoảng lại tái phát. Các khối u có đường kính trung bình (từ 8-15cm), cuống dài, dễ di động có tỷ lệ xoắn lớn hơn. Xoắn thường xảy ra ở phần phụ bên phải, có thể do khả năng di chuyển của buồng trứng trái bị hạn chế bởi đại tràng sigma.
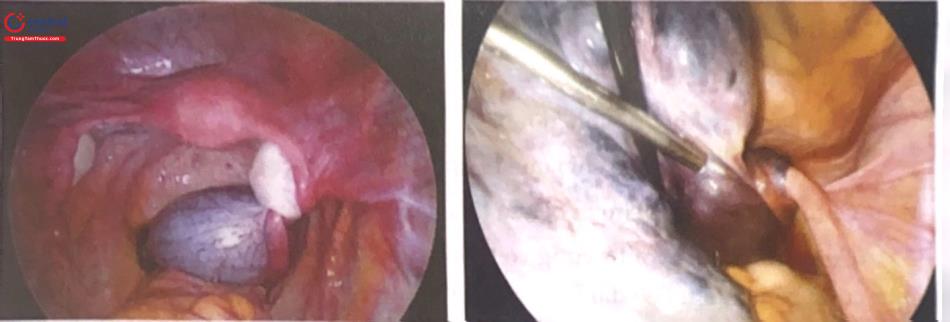
Nếu can thiệp điều trị kịp thời, khả năng bảo tồn buồng trứng sẽ tăng lên. Tuy nhiên, vẫn cần phải cắt bỏ phần phụ trong trường hợp tổn thương hoại tử, chảy máu nhiều hoặc nghi ngờ ác tính. Phẫu thuật cắt buồng trứng – vòi tử cung với những trường hợp xoắn buồng trứng ở độ tuổi mãn kinh. Mức độ xoắn có thể được đánh giá qua nội soi hoặc mổ hở. Trước đây, thường cắt phần phụ trước khi tháo để tránh nguy cơ giải phóng huyết khối. Tuy nhiên, hiện tại các bằng chứng không ủng hộ quan điểm này. McGovern và cộng sự (1999) đã hồi cứu gần 1000 trường hợp xoắn u nang buồng trứng và báo cáo tỷ lệ tắc mạch phổi chỉ là 0,2%.
Xử trí trong thai kỳ không có sự khác biệt. Tuy nhiên, trong trường hợp phải cắt bỏ nang hoàng thể, khuyến cáo nên điều trị hỗ trợ progesterone cho đến tuần thứ 10 của thai kỳ.
Các chế phẩm progesterone phù hợp là:
(1) Progesterone vi hạt (Prometrium) viên nhộng 200mg đặt âm đạo 2-3 lần/ngày.
(2) Progesterone 8% (Crinone) dạng gel bôi âm đạo 90mg 1-2 lần/ngày.
(3) Progesterone viên đặt âm đạo (Endometrin) 100mg 2-3 lần/ngày.
(4) Progesterone vi hạt đường uống (Prometrium) 200mg uống 2-3 lần/ngày.
(5) Dầu progesterone (compound in a specialty pharmacy) 50-100mg/ngày tiêm bắp.
(6) 17-hydroxyprogesterone caproate 150mg tiêm bắp mỗi tuần.
1.3.1 Chảy máu trong nang
Là hậu quả của xoắn. Cơ chế như buộc ga-rô lỏng, máu ứ không trở về được gây vỡ mạch, nang to dần lên.
1.3.2 Vỡ u nang
Do xoắn nang không được điều trị kịp thời, do sang chấn, do đè ép khi khám. Hậu quả là chảy máu ổ bụng cấp tính.
1.3.3 Viêm dính và chèn ép
U nang dính với các tạng xung quanh gây ra viêm phúc mạc khu trú, có thể chèn ép các tạng lân cận gây bán tắc ruột, đại, tiểu tiện khó.
1.3.4 Ung thư hóa
Ung thư có thể xảy ra ở cả 3 loại u nang thực thể, nhưng u nang thanh dịch thường gặp nhất. Bệnh nhân gầy, u to nhanh, nhiều thùy xâm lấn các tạng xung quanh.
1.3.5 U nang và thai kỳ
U nang buồng trứng trong thai kỳ có thể tăng nguy cơ sẩy thai, sinh non, u tiền đạo, ngôi bất thường, xoắn u nang sau sinh.
1.4 ĐIỀU TRỊ
1.4.1 U nang cơ năng
Cần theo dõi định kỳ, chỉ phẫu thuật khi biến chứng.
1.4.2 U nang thực thể
Phẫu thuật là chủ yếu. Trường hợp u lành tính, u ở 2 buồng trứng, bệnh nhân trẻ nên bóc u nang để lại phần lành. Khi mổ cần bóc cả khối, để lại phần mô buồng trứng lành. Nếu u mắc kẹt hay quá to, khi hút bớt dịch nên chèn gạc tốt để hạn chế dịch chảy vào ổ bụng.
Cần thận trọng với các khối u dính vì có thể gây tổn thương các tạng xung quanh.
Với u nang buồng trứng xoắn, tiến hành tháo xoắn và đánh giá tình trạng buồng trứng. Hầu hết các trường hợp đều có thể bảo tồn buồng trứng sau khi đã bóc khối u nang mà không phải cắt bỏ buồng trứng.
Các khối u đều phải gửi làm giải phẫu bệnh để xác định lành hay ác tính.
Khi mổ nếu tổn thương nghi ngờ ác tính, có thể sinh thiết tức thì và nếu là u ác tính phải cắt tử cung hoàn toàn, cắt bỏ phần phụ bên còn lại, cắt một phần mạc nối lớn và tiếp tục điều trị hóa chất.
2 PHẦN B. UNG THƯ BUỒNG TRỨNG
Ung thư buồng trứng (UTBT) là loại ung thư thường gặp, đứng hàng thứ 3 trong các ung thư phụ khoa, sau ung thư vú và ung thư cổ tử cung, có tỷ lệ tử vong cao và tiên lượng xấu. Khoảng 70% UTBT được chẩn đoán ở giai đoạn tiến triển (giai đoạn III - IV), lúc này tỷ lệ sống sau 5 năm là 20-25%, nếu bệnh được phát hiện ở giai đoạn sớm thì tỷ lệ này là 90%.
2.1 CƠ CHẾ BỆNH SINH
Hiện nay, có một số giả thuyết về cơ chế bệnh sinh UTBT được giới thiệu, tuy nhiên chưa có giả thuyết nào được chấp nhận rộng rãi.
2.1.1 Thuyết rụng trứng liên tục
Theo quan điểm cổ điển, tất cả các loại UTBT đều có nguồn gốc từ lớp biểu mô. Hiện tượng phóng noãn gây tổn thương vật lý lớp này, ngay lập tức các thương tổn được sửa chữa. Trong suốt cuộc đời người phụ nữ, sự rụng trứng xảy ra liên tục nên quá trình tổn thương và tái tạo lớp biểu mô lặp đi lặp lại, các cytokine viêm được tạo ra cùng với các tác nhân oxy hóa gây phá hủy và tổn thương DNA tế bào. Các tế bào này rất dễ bị biến đổi và dễ xâm lấn vào trong lớp đệm vùng vỏ. Cuối cùng sẽ bị mắc kẹt và tạo nên một khối các tế bào biểu mô trong mô đệm được gọi là những nang vùi vùng vỏ (Cortical Inclusion Cysts: CICs). Trong khi đó, các nội tiết tố trong buồng trứng kích thích tế bào biểu mô tăng sinh, biến đổi thành tế bào ung thư. Giả thuyết này phù hợp về mặt dịch tễ học, trong đó số chu kỳ rụng trứng có liên quan đến nguy cơ UTBT.
2.1.2 Thuyết vòi tử cung
Trước đây, hầu hết các nghiên cứu cho rằng UTBT có nguồn gốc từ chính buồng trứng. Tuy nhiên, một số nghiên cứu khác lại cho rằng vòi tử cung có thể là vị trí của các tổn thương tiền ung thư và lan dẫn đến buồng trứng lân cận.
Loạn sản biểu mô vòi tử cung chiếm tỷ lệ cao (50%) ở những phụ nữ có đột biến gen BRCA1/2 đã phẫu thuật cắt bỏ vòi tử cung - buồng trứng dự phòng. Sự biến đổi mô học này có bản chất giống như ung thư biểu mô buồng trứng tuyến thanh dịch độ biệt hóa cao, được gọi là ung thư trong biểu mô vòi tử cung thanh dịch (Serous Tubal Intraepithelial Carcinoma: STIC). Đột biến gen TP53 cũng được tìm thấy trong STIC. Xét nghiệm hóa mô miễn dịch vòi tử cung bình thường nhận thấy những biểu hiện TP53 trong các tế bào tiết giống hệt như đột biến TP53 trong UTBT tuyến thanh dịch. Tuy nhiên, khoảng 50% đột biến TP53 có nguy cơ trở thành ung thư.
Sự biểu hiện TP53 phản ánh sự xuất hiện của tổn thương DNA trong các tế bào biểu mô ống do tiếp xúc với các cytokine và chất oxy hóa. Khoảng 70-90% các ung thư trong biểu mô vòi tử cung (TIC) được tìm thấy ở tua vòi. Tua vòi nằm rất gần buồng trứng nên dễ chịu tác động của các tác nhân gây stress lên buồng trứng. Ngoài ra, phần này có rất nhiều mạch máu, thuận lợi di căn đến buồng trứng qua đường máu.
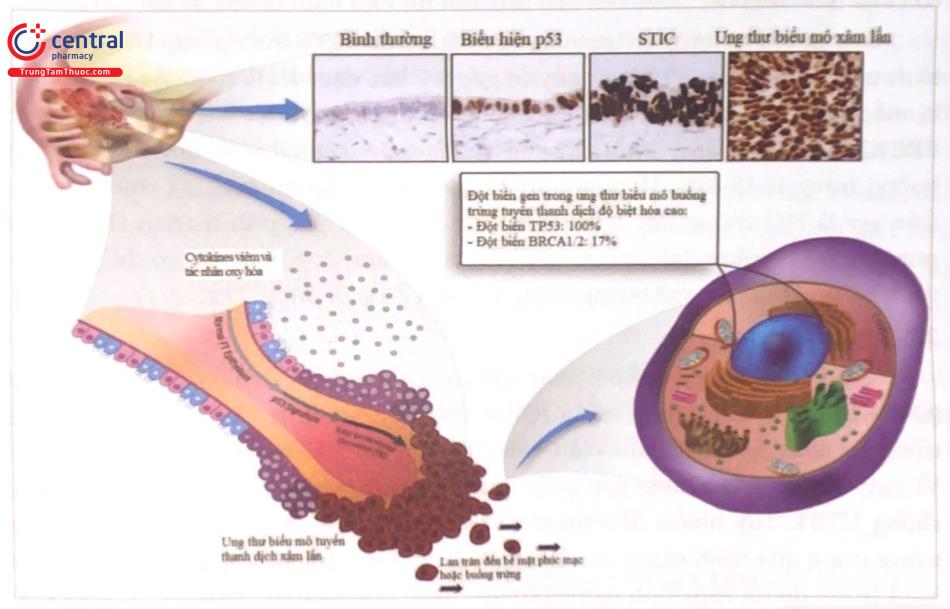
2.1.3 Thuyết hai con đường (Two – Pathways Theory)
Thuyết hai con đường được Kurman và Shih giới thiệu vào năm 2004, phân chia UTBT thành hai loại dựa vào các triệu chứng lâm sàng, kết quả mô bệnh học và đặc điểm di truyền.
Loại I bao gồm ung thư tuyến thanh dịch độ biệt hóa thấp (LGSOC), ung thư tuyến dịch nhầy, ung thư dạng nội mạc, ung thư tế bào sáng và u Brenner ác tính. Các tổn thương tiền ung thư có nguồn gốc từ buồng trứng. Đặc điểm tiến triển chậm, thường chỉ ảnh hưởng đến buồng trứng và ổn định về mặt di truyền. Các thay đổi di truyền phổ biến nhất là các đột biến KRAS và BRAF.
Loại II bao gồm ung thư tuyến thanh dịch độ biệt hóa cao (HGSOC), ung thư không rõ loại và loại ung thư biểu mô – liên kết. Các tổn thương tiền ung thư bắt nguồn từ bên ngoài buồng trứng, có thể là vòi tử cung. Đặc điểm phát triển mạnh hơn, không ổn định về mặt di truyền và thường được chẩn đoán ở giai đoạn tiến triển. Biểu hiện đột biến gen TP53 (50-80%), HER2/neu (10-20%), AKT (12-18%), BRCA1/2.
2.2 CÁC YẾU TỐ NGUY CƠ
Cho đến nay, nguyên nhân của UTBT vẫn chưa được biết rõ, tuy vậy những yếu tố về di truyền, sinh sản, môi trường được xác định có liên quan đến nguy cơ UTBT.
2.2.1 Yếu tố di truyền
Đây là yếu tố nguy cơ quan trọng nhất, có đến 25% trường hợp UTBT có yếu tố di truyền. Họ hàng F1 tăng nguy cơ gấp 3-7 lần, đặc biệt là có nhiều người thân bị mắc bệnh và khởi phát ở độ tuổi sớm. Những người đột biến gen BRCA1 và BRCA2 có 50-80% nguy cơ bị ung thư vú và nguy cơ phát triển ung thư biểu mô buồng trứng là 15-45%. Hơn nữa, trong gia đình có người mắc hội chứng Lynch (còn gọi là Hội chứng ung thư đại trực tràng không polyp di truyền: Hereditary non-polyposis colorectal cancer, HNPCC) cũng làm tăng nguy cơ, có thể chiếm ít nhất 2% ung thư biểu mô buồng trứng và nguy cơ suốt đời là 20%.
2.2.2 Yếu tố sinh sản
Các khối u không chế tiết nhầy có liên quan chặt chẽ đến chu kỳ kinh nguyệt (OR = 1,5) và chu kỳ rụng trứng (OR = 2,8). Phụ nữ chưa có chu kỳ rụng trứng trong 8,7 năm, nguy cơ giảm 4 lần. Điều này ủng hộ giả thuyết rụng trứng liên tục. Vì vậy, bất kỳ yếu tố nào góp phần giảm rụng trứng có thể có tác dụng bảo vệ chống UTBT. Tuy nhiên, Moorman và cộng sự lại cho rằng, trái với ngưng rụng trứng trong quá trình mang thai hoặc sử dụng thuốc tránh thai đường uống, giảm rụng trứng do rối loạn kinh nguyệt có liên quan đến tăng nguy cơ UTBT. Mãn kinh muộn là một yếu tố nguy cơ với mức nguy cơ tăng từ 1,5-2,5 lần sau 50 tuổi.
Vô sinh là một yếu tố nguy cơ. Ảnh hưởng của điều trị vô sinh đến tăng nguy cơ UTBT là chưa có bằng chứng xác thực. Một số nghiên cứu cho rằng tỷ số rủi ro tăng lên ở những phụ nữ vô sinh điều trị bằng Clomiphene Citrate (mức độ bằng chứng chắc chắn rất thấp). Nguy cơ UTBT tăng nhẹ ở những phụ nữ có từ 1-3 chu kỳ thụ tinh trong ống nghiệm đã được báo cáo, nhưng không có ý nghĩa lâm sàng (p = 0,18). Vì vậy, thuốc điều trị vô sinh có thể làm tăng nhẹ nguy cơ UTBT so với quần thể chung hoặc phụ nữ hiếm muộn không điều trị (mức độ bằng chứng thấp).
Phẫu thuật cắt vòi tử cung và cắt tử cung giúp giảm đáng kể nguy cơ UTBT. Theo đó, giảm 20% nguy cơ ung thư biểu mô tuyến thanh dịch độ biệt hóa cao, giảm 19% ung thư tuyến thanh dịch xâm lấn, giảm 32% ung thư tuyến dịch nhầy xâm lấn, giảm 42% ung thư tế bào sáng và giảm 52% ung thư dạng nội mạc.
Sử dụng thuốc tránh thai kết hợp đường uống kéo dài giảm đến 50% nguy cơ UTBT, thời gian bảo vệ trên 30 năm từ lần sử dụng cuối. Thuốc tránh thai progestin đơn thuần cũng có thể giảm nguy cơ UTBT.
2.2.3 Yếu tố chủng tộc và môi trường
Tuổi và chủng tộc: nguy cơ gia tăng từ 40-79 tuổi với tỷ lệ tương ứng từ 15,7 đến 54/100.000. Độ tuổi trung bình được chẩn đoán là 63 tuổi, trong đó trên 55 tuổi chiếm 69,4%. UTBT hay gặp hơn ở quần thể người da trắng hơn người da vàng hay da den.
Thức ăn và yếu tố hình thể: Ăn mỡ, đặc biệt mỡ động vật làm tăng nguy cơ. Tiêu thụ rau quả và chất xơ đặc biệt B carotene làm giảm nguy cơ. Dinh dưỡng, cân nặng và chiều cao là ba thông số liên quan chặt chẽ. Sự phối hợp vừa thức ăn nhiều năng lượng dưới dạng mỡ và đạm động vật, quá cân và tăng chiều cao là yếu tố nguy cơ có thể giải thích được một vài khác biệt về địa lý của tỷ lệ mới mắc UTBT.
Bột talc (Talcum, Talc): Các nghiên cứu về ảnh hưởng của bột talc trên UTBT vẫn còn mâu thuẫn. Bột talc được chứng minh có liên quan đến nguy cơ UTBT lần đầu tiên vào năm 1960 do có đặc tính sinh học tương tự với Amiăng (Asbestos), là chất gây ung thư được biết trước đó. Một nghiên cứu đa phân tích gồm 11.933 phụ nữ chứng minh nguy cơ UTBT tăng 33% khi tiếp xúc với chất này. Tuy nhiên, nghiên cứu của Katie O'Brien đăng trên Tạp chí Hiệp hội Y khoa Hoa Kỳ (Journal of the American Medical Association: JAMA) gồm 250.000 phụ nữ trong giai đoạn 1982 – 2017 cho thấy không có mối liên quan giữa UTBT và sử dụng bột talc.
2.3 TRIỆU CHỨNG VÀ CHẨN ĐOÁN
2.3.1 Triệu chứng
Trước đây, UTBT được xem như là “kẻ giết người thầm lặng”, vì khoảng 2/3 trường hợp được chẩn đoán ở giai đoạn muộn, lúc đó các triệu chứng thường xuất hiện rõ và tiến triển. Tuy nhiên, một số nghiên cứu cho thấy các triệu chứng đường tiêu hóa, tiết niệu và rối loạn kinh nguyệt có thể gợi ý chẩn đoán sớm UTBT.
Các dấu hiệu cảnh báo sớm của UTBT bao gồm: bụng lớn dần, đầy hơi, đau bụng khó tiêu, táo bón, đau lưng sút cân (không giải thích được), mệt mỏi, tiểu không tự chủ, tiểu nhiều lần. Một số dấu hiệu hiếm gặp bao gồm ra máu tử cung bất thường, bụng báng (cổ trướng), dấu hiệu “Sister Mary Joseph” là một nốt ở rốn, phản ánh tình trạng lan tràn từ ung thư trong ổ bụng.
Các nhà nghiên cứu từ Đại học Washington đã thiết lập “chỉ số triệu chứng” hữu ích trong chẩn đoán sớm UTBT. Chỉ số triệu chứng dự đoán nguy cơ UTBT cao nhất (dương tính) nếu có bất kỳ triệu chứng nào dưới đây (1) xuất hiện ≤ 1 năm và (2) xảy ra hơn 12 lần/tháng:
Đau vùng chậu hoặc đau bụng.
Bụng lớn dần hoặc đầy hơi.
Khó ăn hoặc cảm giác no nhanh.
Độ nhạy và độ đặc hiệu chung của chỉ số này lần lượt là 70% và 86%. Độ nhạy ở giai đoạn sớm là 56,7%, ở giai đoạn tiến triển là 79,5%, độ đặc hiệu ở phụ nữ trên 50 tuổi là 90%, ở phụ nữ dưới 50 tuổi là 86,7%. Từ góc độ lâm sàng, chỉ số triệu chứng rất hữu ích trong phân tầng nguy cơ UTBT, đây là bước đầu tiên trong trình đánh giá, bao gồm xét nghiệm CA125 và siêu âm cho những đối tượng có chỉ số triệu chứng dương tính.
Khối u có khả năng ác tính khi khám thấy kích thước khối u phát triển nhanh, mật độ khối u chắc, di động hạn chế và phát triển cả hai bên buồng trứng.
Khám âm đạo: nếu u nhỏ rất khó nhận biết sự bất thường. Khi khối u lớn (đường kính từ 5cm trở lên) ở những phụ nữ 40-60 tuổi, có thể cảm nhận u lổn nhổn, nhiều thùy, nhiều nhú, có thể có dịch ổ bụng di động hạn chế, thường phát triển cả hai buồng trứng.
Về sự lan tràn ung thư buồng trứng có ba cách:
Lan tràn trực tiếp từ khối u tới chậu hông và màng bụng.
Tế bào khối u di căn đến hạch chậu hông và hạch vị qua đường bạch mạch.
Qua đường bạch huyết dọc theo buồng trứng tới hạch cạnh động mạch chủ, thận, mạc nối lớn, gan, phổi. Tắc ruột và sự xâm nhập niệu quản là biến chứng phổ biến. Trong giai đoạn muộn có thể có cổ trướng và kết quả là suy mòn, gọi là vẻ mặt buồng trứng.
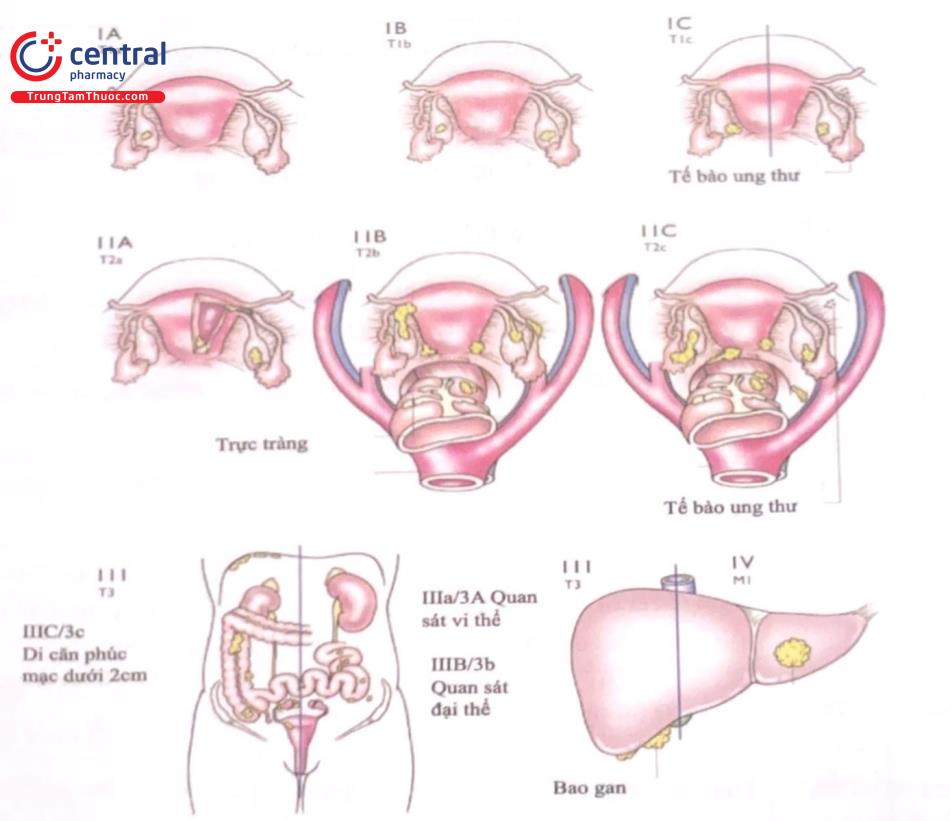
2.3.2 Phân giai đoạn của ung thư buồng trứng
Chẩn đoán giai đoạn dựa vào kích thước, vị trí và mức độ xâm lấn của khối u trong khoang phúc mạc theo Liên đoàn Sản Phụ khoa Quốc tế (FIGO) năm 2014.
TNM | FIGO | Mô tả |
Tx |
| U nguyên phát không đánh giá được. |
T0 |
| ;Không có bằng chứng của khối u nguyên phát. |
T1 | I | U khu trú tại buồng trứng. |
T1a | IA | U một bên, vỏ bọc còn nguyên vẹn; không có tế bào ác tính ở dịch ổ bụng hoặc dịch rửa màng bụng. |
T1b | IB | U một hoặc hai bên, vỏ bọc còn nguyên vẹn; không có u trên bề mặt buồng trứng; không có tế bào ác tính ở dịch ổ bụng hoặc dịch rửa màng bụng. |
T1c | IC | U một hoặc hai bên kèm bất kỳ điều nào sau đây |
T1c1 | IC1 | U vỡ trong phẫu thuật. |
T1c2 | IC2 | Vỏ vỡ trước phẫu thuật hoặc u nằm trên bề mặt buồng trứng. |
T1c3 | IC3 | Tế bào ác tính trong dịch ổ bụng hoặc dịch rửa màng bụng. |
T2 | II | U một hoặc cả hai bên xâm lấn đến cơ quan khác trong tiểu khung, |
T2a | IIa | Lan rộng, xâm lấn đến tử cung và/hoặc vòi tử cung |
T2b | IIb | Xâm lấn đến các cơ quan khác trong tiểu khung. |
T3 | III | U một hoặc cả hai bên, với tế bào học hay giải phẫu bệnh xác nhận có đi căn màng bụng và/hoặc di căn hạch lympho ngoài phúc mạc. |
T3a | IIIa | Di căn hạch sau phúc mạc hoặc di căn vi thể phúc mạc ngoài tiểu khung (trên giới hạn tiểu khung). |
T3b | IIIb | Di căn đại thể phúc mạc ngoài tiểu khung, đường kính < 2cm, kèm hoặc không kèm di căn hạch sau phúc mạc. |
T3c | IIIc | Di căn đại thể phúc mạc ngoài tiểu khung, đường kính > 2cm, kèm hoặc không kèm di căn hạch sau phúc mạc (loại trừ sự lan tràn của khối u đến bao gan hoặc vỏ lách mà không xâm lấn nhu mô các tạng này) |
M1 | IV | Di căn xa (di căn ngoài phúc mạc) ngoại trừ di căn phúc mạc |
M1a | IVA | Tràn dịch màng phổi với tế bào học dương tính |
M1b | IVB | Di căn nhu mô và di căn đến các tạng ngoài ổ bụng (bao gồm cả hạch bẹn và hạch ngoài khoang bụng) |
2.3.3 Phân loại mô bệnh học khối u buồng trứng theo Tổ chức Y tế Thế giới 2014
Phân loại | Lành tính | Ác tính |
Biểu mô
| U tuyến thanh dịch | Ung thư biểu mô tuyến thanh dịch
|
U tuyến dịch nhày | Ung thư biểu mô tuyến dịch nhầy | |
U dạng nội mạc tử cung | Ung thư biểu mô dạng nội mạc | |
U Brenner lành tính | U Brenner ác tính | |
U tế bào sáng | Ung thư tế bào sáng | |
U tế bào gai | Ung thư biểu mô kém biệt hóa | |
U giáp biên thanh dịch | ||
U giáp biên nhầy | ||
Carcinoma không rõ loại | ||
| Tế bào mầm
| U quái trưởng thành | U nghich mầm |
U quái giáp | U xoang nội bị | |
| Ung thư biểu mô phổi | |
U quái không trưởng thành | ||
Đệm – sinh dục | U hạt – vỏ bào lành tính | U hạt – vỏ bào ác tính |
U xơ buồng trứng | U tế bào Sertoli và Leydig ác tính | |
U tế bào Sertoli và Leydig |
|
2.3.4 Cận lâm sàng
2.3.4.1 Các chất chỉ điểm huyết thanh
CA125 huyết thanh
Kháng nguyên ung thư 125 (viết tắt là CA125) được Robert Bast và cộng sự đã phát hiện vào đầu thập niên 1980 trên cơ sở nồng độ CA125 tăng ≥ 35 UI/mL ở khoảng 82% bệnh nhân ung thư biểu mô buồng trứng được phẫu thuật và chỉ 1% dân số bình thường. CA125 được FDA khuyến cáo trong thực hành lâm sàng.
Nồng độ CA125 tăng trong nhiều bệnh lý lành tính hoặc ác tính khác nhau như lạc nội mạc tử cung, khối u buồng trứng, viêm vùng chậu, u xơ tử cung, ung thư nội mạc tử cung. Ngoài ra, CA125 còn biểu hiện ở bề mặt tế bào viêm nên nồng độ cao cũng có thể gặp trong các bệnh viêm khớp dạng thấp, xơ cứng bì, Lupus ban đỏ hệ thống và hội chứng Sjogren. Các yếu tố chủng tộc, sắc tộc, độ tuổi, cắt tử cung tiền sử hút thuốc lá, béo phì có thể ảnh hưởng đến nồng độ CA125 huyết thanh.
Hiện nay, trị số 35 UI/mL thường được dùng là giá trị ngưỡng phân biệt (cut- off point) bình thường với bất thường. Tại điểm cắt này, độ nhạy và độ đặc hiệu của CA125 trong chẩn đoán phân biệt khối u buồng trúng lành tính và ác tính lần lượt là 78,0-78,7% và 77,9-95,0%. Tuy nhiên, đối với những người đã mãn kinh hoặc đã cắt tử cung kèm hai buồng trứng thì nên chọn giá trị ngưỡng thấp hơn, từ 20-26 UI/mL.
Nồng độ CA125 trước phẫu thuật có mối liên quan đáng kể với giai đoạn ung thư và độ mô học. Khoảng 80% ung thư biểu mô buồng trứng có nồng độ CA125 trên 35 UI/mL và tăng lên 50-60% ở giai đoạn I, 80-90% ở giai đoạn II và trên 90% ở giai đoạn III – IV. Tần suất tăng nồng độ cao nhất ở ung thư biểu mô buồng trứng tuyến thanh dịch, tiếp theo là ung thư dạng nội mạc và ung thư tế bào sáng. Đối với các u buồng trứng ngoài biểu mô (u tế bào mầm và u đệm – sinh dục) không biểu hiện glycoprotein này hoặc chỉ biểu thị mức độ thấp.
Ngoài ra, CA125 còn có vai trò theo dõi sự tái phát của ung thư biểu mô buồng trứng sau điều trị. Khi nồng độ CA125 giảm biểu hiện bệnh thoái triển, thông thường sau phẫu thuật nồng độ CA125 trở lại bình thường sau 3 tháng.
Tóm lại, CA125 vẫn là dấu ấn sinh học quan trọng nhất, được ứng dụng rộng rãi nhất trong ung thư biểu mô buồng trứng.
HE4 huyết thanh
Protein mào tính người 4 (Human Epididymal protein 4, viết tắt là HE4) do Kirchoff phát hiện vào năm 1991. HEA rất có giá trị trong chẩn đoán UTBT, được FDA phê duyệt trong thực hành lâm sàng vào năm 2011.
Điểm cắt để tiên lượng UTBT là 70 pmol/l đối với phụ nữ độ tuổi sinh sản và 140 pmol/l đối với phụ nữ sau mãn kinh. Khi CA125 kết hợp với HE4 thì tỷ lệ phát hiện bệnh ác tính cao hơn. Do đó, dấu ấn sinh học này được kết hợp với CA125 trong thuật toán có tên là thuật toán ROMA, đã được FDA công nhận như một công cụ trong chẩn đoán UTBT.
HE4 huyết thanh có thể tăng trong các bệnh lý ác tính khác như ung thư nội mạc tử cung, vòi tử cung, ung thư âm hộ và ung thư phổi. Hơn nữa, có nhiều yếu tố ảnh hưởng đến nồng độ HE4 như độ tuổi (nồng độ HE4 tăng cao phụ nữ trên 40 tuổi), hút thuốc lá (mức HE4 tăng khoảng 30% ở người hút thuốc so với người không hút thuốc) và chức năng thận. Mối liên quan giữa HE4 và chu kỳ kinh nguyệt hoặc điều trị thuốc nội tiết còn nhiều tranh luận. Một số nghiên cứu cho thấy, nồng độ HE4 trong giai đoạn rụng trúng cao hơn giai đoạn nang noãn và hoàng thể, trong khi đó, một số nghiên cứu khác khẳng định giá trị HE4 không phụ thuộc vào chu kỳ kinh nguyệt hoặc điều trị nội tiết tố.
Các chất chỉ điểm khác
Một số chất chỉ điểm khác như beta hCG, Lactate Dehydrogenase (LDH), alpha Fetoprotein (AFP), inhibin có thể hỗ trợ cho chẩn đoán UTBT.
Loại mô học | Beta-hCG | AFP | LDH | CA125 |
U nghịch mầm | + | - | + | - |
U xoang nội bì | - | + | - | - |
Ung thư nguyên bào nuôi | + | - | - | - |
U quái không trưởng thành | - | + | + | + |
Ung thư biểu mô phôi | + | + | - | - |
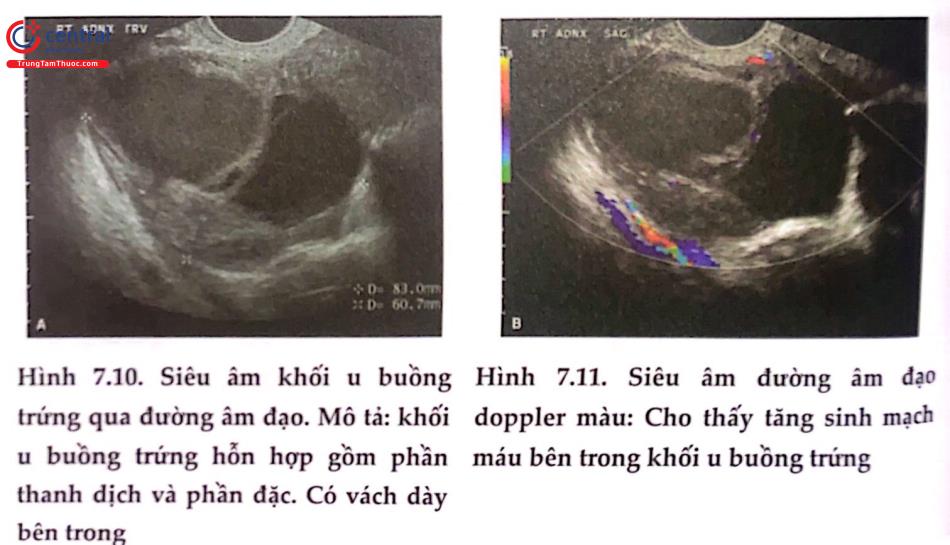
2.3.4.2 Siêu âm
Siêu âm đường âm đạo được xem là phương tiện đầu tay để đánh giá khối u phần phụ, sử dụng sóng âm tần số cao, cung cấp hình ảnh độ phân giải cao, cho phép đánh giá chi tiết cấu trúc u và giúp đánh giá khả năng lành tính của khối u như số lượng và kích thước u, thành phần khối u (dạng nang hay đặc hay hỗn hợp), tính chất phản âm bên trong nang, cấu trúc vách chồi, dịch ổ bụng hay không và các đặc điểm của cơ quan khác ở vùng bụng. Các đặc điểm gợi ý khối u ác tính gồm: nang nhiều thủy, có thành phần đặc, hiện diện cả 2 bên buồng trứng dịch báng ổ bụng, di căn ổ phúc mạc. Ngoài ra, siêu âm Doppler màu giúp khảo sát đặc điểm tưới máu của khối u vùng chậu. Siêu âm qua đường bụng hữu ích khi khối u có kích thước lớn vượt khỏi giới hạn vùng chậu hoặc trong trường hợp bệnh nhân có tiền sử phẫu thuật làm các cấu trúc vùng chậu thay đổi vị trí.
Năm 2000, nhóm Nghiên cứu Khối u buồng trứng Quốc tế (The International Ovarian Tumor Analysis: IOTA) đã phát triển và công bố đồng thuận về các thuật ngữ, định nghĩa, cách đo đạc và mô tả đặc điểm khối u buồng trứng trên siêu âm nhằm thống nhất giữa các bác sĩ siêu âm. Quy luật đơn giản của IOTA được xây dựng vào năm 2008 dựa vào 10 đặc điểm mô tả trên siêu âm để phân nhóm lành tính (B – rules) và ác tính (M – rules) trong tiên đoán khối u buồng trứng, với độ nhạy 93% và độ đặc hiệu 90%.
Quy luật tiên đoán ác tính | Quy luật tiên đoán lành tính (B – rules) |
M1: U đặc không đều M2: Có dịch ổ bụng M3; Có ít nhất 4 cấu trúc chồi nhú M4: U đa thùy đặc, không đều, đường kính lớn nhất ≥ 100mm M5: Tưới máu nhiều (4 điểm) | B1: Nang đơn thùy B2: Phần đặc đường kính lớn nhất <7mm B3: Có bóng lưng B4: U đa thùy trơn láng, đường kính lớn nhất < 100mm B5: Không có tưới máu (1 điểm) |
2.3.4.3 Các xét nghiệm khác
Chụp cộng hưởng từ: Được chỉ định khi muốn đánh giá (1) mức độ tổn thương lan tràn ở vùng chậu và (2) khảo sát cấu trúc tổn thương và mối liên quan với cơ quan vùng chậu.
Dịch báng ổ bụng (cổ trướng) là dịch vàng chanh và thường có tiên lượng xấu. Khoảng 32% bệnh nhân UTBT có cổ trướng sẽ tử vong trong năm đầu. Dịch cổ trướng thường do các tế bào ung thư lan tràn trong ổ bụng kích thích phúc mạc tiết dịch và cổ trướng lại màng tế bào ung thư lan đi khắp các phủ tạng. Nếu dịch bảng đỏ máu thì tiên lượng càng xấu, 70% bệnh nhân tử vong trong năm đầu.
Xét nghiệm tế bào nước cổ trướng: 96% ung thư giai đoạn muộn có tế bào ung thư dịch bảng (+). Tuy nhiên, trường hợp ung thư giai đoạn sớm, tế bào không bong vào trong ổ bụng do đó có khoảng 34% âm tính giả. Đây là phương pháp tốt để chẩn đoán và theo dõi sự tiến triển của bệnh.
2.3.5 Phân tầng nguy cơ ác tính khối u buồng trứng trước phẫu thuật
2.3.5.1 Thuật toán nguy cơ ác tính buồng trứng (ROMA)
Năm 2009, Richard G. Moore và cộng sự đã xây dựng thuật toán nguy cơ ác tính buồng trứng (viết tắt là ROMA) để đánh giá nguy cơ ác tính của khối u buồng trứng trước phẫu thuật. Thuật toán này bao gồm nồng độ HE4, CA125 huyết thanh và tình trạng mãn kinh.
Cách tính chỉ số: Giá trị ROMA (%) = exp(PI)/[1 + exp(PI)] * 100
Trong đó, PI (Predictive Index) là chỉ số dự đoán được tính như sau:
Phụ nữ trước mãn kinh: PI= –12,0 + 2,38*Ln(HE4) + 0,0626*Ln(CA125)
Phụ nữ sau mãn kinh: PI= –8,09 + 1,04*Ln(HEA) + 0,732*Ln(CA125)
Trong đó, exp(PI) = el và Ln() là logarit tự nhiên (hay logarit cơ số e).
ROMA đánh giá bệnh nhân thành 2 nhóm: Nguy cơ cao và nguy cơ thấp UTBT. Bệnh nhân có nguy cơ cao UTBT khi điểm cắt của ROMA:
Kít nhà sản xuất | Phụ nữ trước mãn kinh | Phụ nữ sau mãn kinh |
Cobas 6000 | ≥ 11,4% | ≥ 29,9% |
Architect i1000 | ≥ 7,4% | ≥ 25,3% |
2.3.5.2 Chỉ số nguy cơ ác tính
Jacobs và cộng sự đã đề xuất một thuật toán, là chỉ số nguy cơ ác tính (RMI) bằng cách kết hợp các giá trị của CA125, siêu âm và tình trạng mãn kinh. Thuật toán này đã được sử dụng trên lâm sàng trong một thời gian dài ở ba phiên bản khác nhau (RMI I, II và III). Điểm RMI ≥ 200 chứng tỏ có mối liên quan chặt chẽ với nguy cơ cao ác tính (độ nhạy 85,4% và độ đặc hiệu 96,9%).
Năm 2009, Yamamoto và cộng sự đã phát triển thành RMI IV bằng cách thêm vào kích thước khối u.
Như vậy, công thức của RMI IV là: RMI IV = U x M x S x CA125 Trong đó:
U (Ultrasound score): Khảo sát đặc điểm hình thái khối u trên siêu âm. Các đặc điểm gợi ý khối u ác tính gồm: nang nhiều thùy, có thành phần đặc, hiện diện cả 2 bên buồng trứng, dịch báng ổ bụng, di căn ở phúc mạc. U = 1 nếu có tối đa 1 đặc điểm, U = 4 nếu có từ 2 đặc điểm trở lên.
M (Menopausal status): M = 1 nếu trước mãn kinh, M = 4 nếu sau mãn kinh.
S = 1 nếu kích thước lớn nhất khối u nhỏ hơn 7cm, S = 2 nếu ≥7cm.
CA125: nồng độ CA125 huyết thanh (Ul/ml).
Điểm số RMI IV ≥ 450 là nghi ngờ ác tính.
2.4 ĐIỀU TRỊ
Điều trị khối u ác tính buồng trứng thường khó khăn, do bệnh thường phát hiện muộn, tính chất giải phẫu bệnh phức tạp, tiến triển và tiên lượng khó dự báo. Điều trị cần kết hợp nhiều mô thức điều trị và chăm sóc toàn diện, trong đó chủ yếu là phẫu thuật và hóa trị. Khoảng 80% bệnh nhân đáp ứng với điều trị ban đầu, do đó tỷ lệ sống sót ngắn hạn tương đối cao. Tuy nhiên, hầu hết bệnh nhân bị tái phát trong vòng 16-18 tháng kháng hóa trị và thời gian sống thêm 5 năm giảm đáng kể. Hiện nay, bên cạnh những tiến bộ về phẫu thuật thì sự phát triển của hóa trị và liệu pháp miễn dịch bước đầu được nghiên cứu đã mở ra nhiều hy vọng sống cho bệnh nhân UTBT.
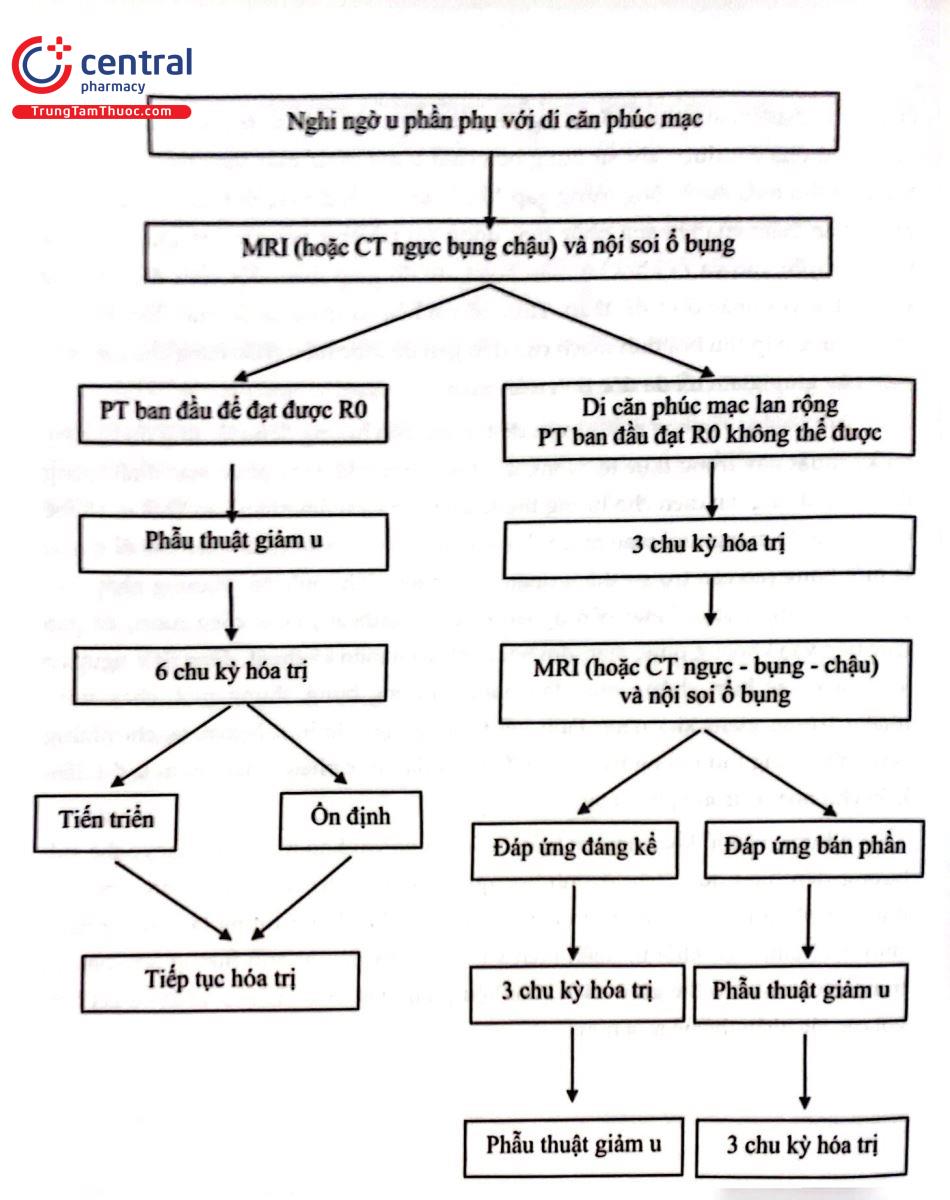
2.4.1 Phẫu thuật
Là biện pháp đầu tiên và quan trọng nhằm mục đích (1) đánh giá toàn bộ khối u, (2) lấy tổ chức làm giải phẫu bệnh hoặc (3) giúp điều trị hóa liệu pháp bổ sung. Nếu trường hợp không cắt được toàn bộ khối u thì lấy mẫu sinh thiết, sau đó hóa trị hỗ trợ và phẫu thuật lại (nếu có chỉ định).
Chẩn đoán khả năng phẫu thuật cắt bỏ u:
Dựa vào nồng độ CA125: Dưới 500 UI/ml: 84% cắt bỏ tối ưu. Trên 500 UI/ml: 14% cắt bỏ tối ưu.
Các tiêu chí dự báo không có khả năng cắt bỏ hoàn toàn
Xâm lấn mạc treo tràng, xâm lấn rộng mạc nối lớn kèm xâm lấn lách.
Tổn thương hơn 2cm ở vòm hoành hay nhu mô gan.
Có hạch cạnh động mạch chủ trên thận.
Báng lớn.
Nội soi ổ bụng:
Nội soi là phương tiện tốt nhất và không thể thiếu trong đánh giá khả năng cắt bỏ ban đầu, đồng thời cho phép chẩn đoán mô học và xét nghiệm tế bào học dịch báng.
Sử dụng thang điểm Fagotti để đánh giá sự lan tràn của di căn ổ bụng và dự đoán khả năng phẫu thuật giảm khối. Mỗi mục được tính từ 0-2 điểm => điểm từ 0-14. Phẫu thuật cắt bỏ không đạt mức hoàn toàn ở 100% bệnh nhân có chỉ số 28.
Tiêu chí | 0 điểm | 2 điểm |
Ung thư biểu mô màng bụng | Tổn thương ung thư xâm lấn 1 vùng giới hạn (dọc theo rãnh đại tràng bên hoặc phúc mạc vùng chậu) và có thể tách khỏi phúc mạc | Tổn thương phúc mạc không bóc tách được với các tổn thương |
Xâm lần cơ hoành | Không thâm nhiễm ung thư bề mặt cơ hoành | Lan truyền rộng thâm nhiễm ung thư hoặc các nốt tụ lại bề mặt cơ hoành |
Thâm nhiễm mạc treo ruột | Không có nốt lớn thâm nhiễm và không thâm nhiễm vào cuống của mạc treo ruột (nhu động ruột không bị giới hạn) | Các khối u thâm nhiễm lớn hoặc sự xâm lấn cuống mạc treo ruột và hạn chế nhu động ruột |
Thâm nhiễm mạc nối lớn | Không có lan tràn u dọc theo mạch nối đến bờ cong lớn của dạ dày | Lan tràn u dọc theo mạch nối đến bờ cong lớn của dạ dày |
Thâm nhiễm ruột | Không thấy tổn thương ung thư biểu mô dạng hạt kê trên đoạn ruột | Có tổn thương ung thư biểu mô tế bào như hạt kê trên đoạn ruột cùng. |
Thâm nhiễm dạ dày | Không quan sát thấy ung thư thâm nhiễm thành dạ dày | Có ung thư thâm nhiễm thành dạ dày |
Di căn gan | Không có tổn thương bề mặt | Bất kỳ tổn thương bề mặt nào |
2.4.2 Hóa liệu pháp
Hóa trị được xem là “tiêu chuẩn chăm sóc” trong hầu hết UTBT, phối hợp với phẫu thuật nhằm hy vọng trị khỏi bệnh gọi là hóa trị hỗ trợ phẫu thuật, gồm hóa trị tân hỗ trợ (hóa trị trước mô) và hóa trị bổ túc sau mổ. Hơn nữa, hóa trị nhằm giảm nhẹ các triệu chứng của ung thư giai đoạn muộn gọi là hóa trị giảm nhẹ để tăng chất lượng sống của bệnh nhân, dù có thể không tăng thời gian sống. Hóa liệu pháp bao gồm phác đồ hóa trị toàn thân (intravenous: IV) hoặc hóa trị trong phúc mạc (intraperitoneal: IP).
2.4.2.1 Hóa trị toàn thân (intravenous chemotherapy)
Đối với ung thư loại biểu mô: Hiện nay, phác đồ chuẩn bao gồm 6 chu kỳ truyền tĩnh mạch của Paclitaxel và Carboplatin mỗi 21 ngày (chu kỳ 3 tuần). Về tác dụng phụ: bên cạnh các tác dụng phụ chung của hóa chất (rụng tóc, ói mửa, phá hủy tế bào máu, tổn thương gan, thận), thì thuốc Paclitaxel còn có tác dụng phụ quan trọng như phản vệ, đau nhức (thận, cơ, xương khớp), tê tay chân (có thể kéo dài sau khi kết thúc hóa trị), thuốc Carboplatin có thể gây độc thận nặng. Các phác đồ khác: tùy theo sức khỏe, diễn tiến bệnh, khả năng tài chính, thầy thuốc sẽ có các phác đồ thay thế phác đồ chuẩn: Phác đồ DC: Docetaxel (thay cho Paclitaxel) - Cisplatin, phác đồ Paclitaxel mỗi tuần (thay vì mỗi 3 tuần như phác đồ chuẩn), phác đồ Lipodox - Carboplatin, phác đồ Cyclophosphamide – Cisplatin.
Đối với ung thư loại không biểu mô (ung thư tế bào mầm, đệm – sinh dục): Phác đồ chuẩn (BEP) gồm Bleomycine (B), Etoposide (E), Cisplatin (P), Cách cho thuốc đường tĩnh mạch, chu kỳ 3 tuần, số chu kì: 3-4, thời gian cho thuốc mỗi chu kỳ: 5 ngày với (E) & (P), mỗi tuần với (B). Về tác dụng phụ: ngoài các tác dụng phụ chung của hóa chất, thì tác dụng phụ riêng của Bleomycine là xơ phổi, Etoposide là vô sinh. Các phác đồ khác: EP, VAC, VBP, TC...
2.4.2.2 Hóa trị trong phúc mạc (intraperitoneal chemotherapy)
UTBT lây lan qua sự bong ra của các tế bào ác tính vào dịch ổ bụng xâm lấn dọc theo ổ bụng và phúc mạc vùng chậu, hậu quả là chủ yếu di căn phúc mạc. Trên cơ sở đó, hóa trị trong phúc mạc đã được một số nhóm tác giả nghiên cứu và chứng minh có cải thiện về tổng thể và khả năng sống không bệnh.
Chỉ định và chống chỉ định:
Hóa trị trong phúc mạc đạt được hiệu quả tối ưu trong các trường hợp ung thư biểu mô buồng trứng giai đoạn III đã được phẫu thuật cắt bỏ tối đa, kích thước u < 1cm. Một số trường hợp giai đoạn sớm cũng được cân nhắc.
Có nhiều nghiên cứu cho rằng không nên dùng hóa trị trong phúc mạc trong ung thư biểu mô buồng trứng giai đoạn IV hoặc các khối u chưa được phẫu thuật cắt bỏ tối đa (khối u có đường kính lớn hơn 1cm).
Một số chống chỉ định của hóa trị trong phúc mạc:
Không có khả năng chịu đựng phẫu thuật giảm khối u (cytoreductive surgery).
Viêm phúc mạc hoặc nhiễm trùng huyết (sepsis) tiến triển.
Dính ổ bụng diện rộng, cản trở phân phối hóa chất một cách đầy đủ.
Ô nhiễm phúc mạc rõ ràng (Obvious peritoneal contamination).
Chức năng thận không đảm bảo để đào thải Cisplatin.
Không có khả năng trải qua lịch trình quản lý hóa trị trong phúc mạc.
Ưu điểm của phác đồ này là hóa chất được đưa thẳng vào khoang phúc mạc, nên nồng độ thuốc trong khoang phúc mạc cao hơn, thời gian bán hủy dài hơn so với truyền tĩnh mạch đơn thuần, thuốc tiếp xúc trực tiếp với khối u, các mô xung quanh và các cơ quan lân cận. Một số nghiên cứu chứng minh nồng độ đỉnh của Cisplatin, Paclitaxel, Carboplatin và Docetaxel trong khoang phúc mạc cao gấp 2,5-8 lần trong huyết tương, thậm chí 4 ngày sau hóa trị, điều này cho phép tăng nồng độ thuốc để đạt hiệu quả tối ưu. Đối với các tổn thương 2-3mm hoặc nhỏ hơn thì hóa chất tác dụng trực tiếp đến khối u tốt hơn so với phác đồ toàn thân; do đó sử dụng phác đồ hóa trị trong phúc mạc đối với các khối u vi thể tỏ ra ưu thế hơn.
Đối với Ciplastin, loại thuốc được nghiên cứu rộng rãi nhất từ trước đến nay, nhận thấy hiệu quả đạt được khi sử dụng hóa chất trong phúc mạc tăng tiếp xúc với tế bào ung thư biểu mô buồng trứng gấp 10-20 lần so với đường tĩnh mạch. Hơn nữa, màng bán thẩm của khoang phúc mạc đóng vai trò như một rào cản giúp hạn chế thuốc truyền vào và ra khỏi hệ tuần hoàn, do đó giúp giảm độc tính, điều này là không thể với phác đồ toàn thân. Thực tế với hóa trị trong phúc mạc, hầu hết các thuốc được hấp thu bởi tĩnh mạch cửa đến gan để thực hiện chức năng chuyển hóa, điều này giúp giảm tối đa độc tính toàn thân.
Tuy nhiên, vẫn còn một số vấn đề tồn tại, ảnh hưởng đến việc ứng dụng rộng rãi kỹ thuật này trong thực tế. Nồng độ thuốc trong khoang phúc mạc định lượng được lại không đại diện cho lượng thuốc đã thực sự thâm nhập vào khối u, có thể một phần do mạng lưới mao mạch dày đặc, xơ hóa và bám dính quanh khối u như là một hàng rào cản trợ sự thâm nhập của thuốc. Bên cạnh đó, phương pháp này phải sử dụng một catheter bên ngoài (external catheter) hoặc cổng (port) để gắn trực tiếp vào khoang phúc mạc, đòi hỏi có chuyên môn kỹ thuật, đồng thời nguy cơ xuất hiện các biến chứng như đau bụng, chướng bụng, thủng ruột, chảy máu, nhiễm trùng, giảm khả năng lành vết thương, gây dính.... Ngoài ra, chỉ những bệnh nhân ung thư buồng trứng giai đoạn III đã được phẫu thuật tối ưu là đủ điều kiện cho hóa trị trong phúc mạc.
Những yếu tố khác như tái tuần hoàn thuốc sau hấp thu phúc mạc có thể ảnh hưởng đến hiệu quả. Yếu tố sinh học quan trọng quyết định sự thành công của phương pháp này vẫn chưa được hiểu biết đầy đủ. Trong tương lai, những bằng chứng về sinh học khối u, miễn dịch và vì môi trường bị ảnh hưởng bởi điều trị trong phúc mạc có thể giúp triển khai liệu pháp này một cách tốt nhất và kết hợp với các tác nhân thế hệ mới hơn.
2.4.3 Liệu pháp miễn dịch
Tối ưu hóa các phác đồ điều trị góp phần làm tăng cơ hội sống cho nhiều bệnh nhân ung thư phụ khoa, đặc biệt là ung thư giai đoạn tiến triển/tái phát hoặc kháng trị, trong đó có UTBT. Trong 10 năm trở lại đây, liệu pháp miễn dịch đã trở thành “vũ khí” chính trong cuộc chiến chống ung thư. Năm 2018, Giải thưởng Nobel Y Sinh học đã được trao cho hai nhà khoa học James Allison (Mỹ) và Tasuku Ho (Nhật Bản) nhờ công trình nghiên cứu liệu pháp điều trị ung thư bằng cách ư thế điều hòa hệ miễn dịch âm tính. Các nhà khoa học đã tìm ra cách "khóa" các protein ức chế hệ miễn dịch đó là CLTA-4 (Cytotoxic T-Lymphocyte-Associated protein 4) và PD-1 (Programmed death-1), nhờ đó kích hoạt tế bào lympho T tiêu diệt khối u. Điều đó đã mở ra một “kỷ nguyên mới” trong điều trị ung thư. Tại Việt Nam, liệu pháp tế bào miễn dịch đã được áp dụng điều trị cho 5 loại ung thư phổi, gan, dạ dày, đại tràng và vú. Đối với UTBT, đã có những kết quả ban đầu của các thử nghiệm lâm sàng về liệu pháp ức chế chốt kiểm miễn dịch dưới dạng đơn thuần hoặc kết hợp với một số liệu pháp khác, hứa hẹn nhiều triển vọng trong ứng dụng thực tiễn lâm sàng.
Hiện có 813 thử nghiệm lâm sàng đang được tiến hành, trong đó có 72 nghiên cứu tập trung vào các chất ức chế chốt kiểm, với 27 nghiên cứu dựa vào kháng thể kháng PD-1 và 36 nghiên cứu dựa vào kháng thể kháng PD-L1. Thử nghiệm trên chuột cho thấy ức chế PD-1/PD-L1 gây ra sự thoái triển của khối u, củng cố mối liên quan của con đường điều hòa này trong quá trình sinh ung thư. Tuy nhiên, liệu pháp ICI đơn thuần cho kết quả còn khiêm tốn, có thể do nhiều con đường kháng miễn dịch trong UTBT.
Các thuốc ức chế PD-1/PD-L1 được sử dụng trong UTBT bao gồm:
(1) Ức chế PD-1: Pembrolizumab, Nivolumab.
(2) Ức chế PD-L1: Avelumab, Atezolizumab, Durvalumab.
Tóm lại, từ những kết quả ban đầu của các thử nghiệm lâm sàng và tỷ lệ thành công còn khiêm tốn đối với liệu pháp ICI đơn thuần hoặc kết hợp trong UTBT cho thấy vẫn còn nhiều điều cần khám phá thêm trong lĩnh vực này.
2.5 TIÊN LƯỢNG
Tỷ lệ tử vong đã không thay đổi trong 30 năm qua, thậm chí dự đoán đến năm 2040, tỷ lệ này sẽ gia tăng đáng kể. Người ta ước tính rằng, đến năm 2035, tỷ lệ mắc bệnh sẽ tăng lên 371.000 một năm (55%) và số người chết sẽ tăng 67% lên 254.000 người. Hơn nữa, triệu chứng UTBT rất nghèo nàn nên khoảng 70% trường hợp được chẩn đoán ở giai đoạn tiến triển (giai đoạn III – IV), diễn biến bệnh phức tạp. Điều này khiến việc điều trị trở nên khó khăn, tốn kém, ảnh hưởng đến chất lượng sống và tiên lượng sống của người bệnh. Vì vậy, phát hiện sớm ung thư buồng trứng có ý nghĩa hết sức to lớn.
Giai đoạn ung thư | Tỷ lệ sống sót 5 năm |
Giai đoạn I | 85-95% |
Giai đoạn II | 70-78% |
Giai đoạn III | 40-60% |
Giai đoạn IV | 15-20% |
Tiên lượng kém hơn khi khối u có độ mô học cao hơn hoặc khi phẫu thuật không thể loại bỏ tất cả mô xâm nhiễm được nhìn thấy; trong những trường hợp như vậy, tiên lượng tốt nhất khi mô ung thư xâm lấn có thể được giảm xuống < 1cm hoặc lý tưởng là mô tồn tại chỉ còn thấy trên vi thể (phẫu thuật giảm u). Với giai đoạn III và IV, tỷ lệ tái phát khoảng 70%.
Việc tư vấn cho bệnh nhân có tính chất đặc biệt quan trọng. Công tác chăm sóc sức khỏe phải làm tốt ở tuyến cơ sở. Tổ chức khám phụ khoa định kỳ để phát hiện sớm các khối u buồng trứng ở mọi lứa tuổi. Những khối u buồng trứng dù nhỏ cũng cần được quản lý, theo dõi chặt chẽ. Nên chuyển tuyến có đủ điều kiện để xác định chẩn đoán và xử lý kịp thời các trường hợp nghi ngờ ác tính.
3 TÀI LIỆU THAM KHẢO
1. American College of Obstetricians and Gynecologists' Committee. Evaluation and Management of Adnexal Masses. Obstet Gynecol. 2016;128(5):210-226.
2. Barbara LH, John OS. Benign Adnexal Mass, Epithelial Ovarian Cancer. Williams Gynecology 4th Edition.Mc Graw Hill. 2020:246-782.
3. Bộ Y tế. U buồng trứng. Hướng dẫn quốc gia về chăm sóc sức khỏe sinh sản. Nhà xuất bản Thanh Hóa, 2017:191-192.
4. Bray F, Ferlay J, Soerjomataram I, Siegel RL, Torre LA, Jemal A. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2018;68(6):394-424.
5. Isherwood A, Bamford J, Dupuy AV. Ovarian cancer in select EU countries: incidence, treatable populations and sales by key drug class. Rev Epidemiol Sante Publique. 2018;66:5286.
6. Kurman R, Carcangiu M, Herrington C, Young R. WHO Classification of Tumours of Female ReSroductive Organs. Lyon: IARC. 2014.
7. Momenimovahed Z, Ghoncheh M, Pakzad R, Hasanpour H, Salehiniya H. Incidence and mortality of uterine cancer and relationship with human development index in the world. Cukurova Med J. 2017;42(2):233–240.
8. Robert C, Alice C, Alice RG, Nancy AH, Patrice MW, Charles RB, Frank WL. Ovarian and Andexal Disease. Beckmann and Ling's Obstetrics and Gynecology 8th Edition. Wolters Kluwer. 2018;50(6):1004-1032.

