Kỹ thuật Sinh thiết da đầu trong quản lý các rồi loạn về tóc

Tác giả: Mariya Miteva
Dịch: Bs. Trương Tấn Minh Vũ
Xem và tải PDF, Tại đây
1 Giá trị của sinh thiết da đầu
Sinh thiết da đầu là một kỹ thuật hữu ích trong quản lý các rối loạn về tóc và da đầu, quyết định trong chẩn đoán rụng tóc có sẹo và hữu ích trong việc phân biệt các loại rụng tóc không sẹo dựa trên số lượng và tỷ lệ nang tóc trong mặt cắt ngang [1].
Sinh thiết da đầu không hữu ích trong chẩn đoán các rối loạn thân tóc mà nên sử dụng trichoscopy và soi dưới kính hiển vi điện tử để chẩn đoán [2] .
Các ứng dụng chính của sinh thiết da đầu bao gồm:
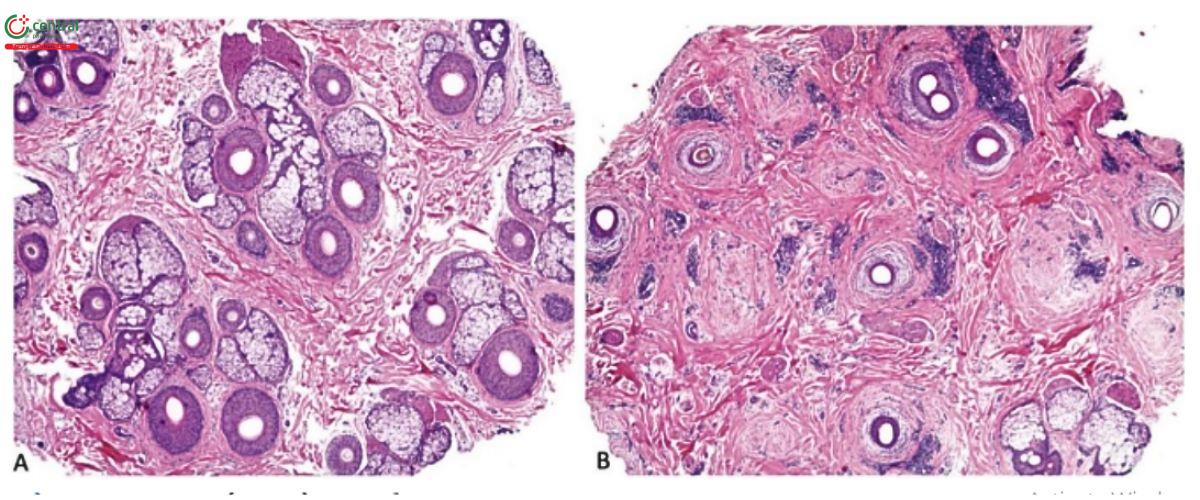
- Phân biệt rụng tóc có sẹo và rụng tóc không có sẹo dựa trên tổng quan về cấu trúc nang tóc bao gồm sự thay thế các đơn vị nang tóc và từng nang bởi sẹo nang tóc /các vùng xơ hóa (mất nang tóc) cũng như sự biến mất của tuyến bã nhờn (ngoại trừ rụng tóc do lực kéo) ) (Hình 7.1)
- Đánh giá mức độ hoạt động của bệnh trong rụng tóc có sẹo dựa trên sự hiện diện và mật độ của thâm nhiễm viêm và sự chiếm ưu thế của nang tóc so với các vùng xơ hóa
- Cung cấp thông tin chi tiết giúp định hướng việc quản lý (như mật độ thâm nhiễm viêm trong rụng tóc có sẹo, loại thâm nhiễm viêm, sự hiện diện của tình trạng viêm và mức độ xơ hóa quanh nang tóc trong rụng tóc androgen, mức độ giảm tỷ lệ tóc terminal : tóc vellus (một tỷ lệ tóc terminal : tóc vellus là 2,5:1 có thể gợi ý một cách tiếp cận quản lý khác trong rụng tóc androgen so với tỷ lệ 0,7:1)
- Kiểm tra lại sự hiện diện của lichen phẳng nang tóc không rõ ràng ở những bệnh nhân không có triệu chứng trước khi tiến hành thủ thuật cấy tóc [3]
- Xác minh các giả thuyết nghiên cứu bằng cách cung cấp giá trị về hình thái.
2 Thực hiện sinh thiết da đầu
Sinh thiết da đầu được thực hiện tại phòng khám ngoại trú. Thông thường một sinh thiết da đầu được thực hiện mặc dù dữ liệu có sẵn cho thấy chẩn đoán chính xác đạt được ở 98% các trường hợp được sinh thiết ba lần so với 79% với một lần sinh thiết theo chiều ngang [4]. Một nghiên cứu chứng minh rằng ở 106 bệnh nhân được chẩn đoán lâm sàng bị rụng tóc androgen kiểu nam, 100% mẫu sinh thiết ngang gợi ý chẩn đoán này nhưng chỉ có 67% được chẩn đoán [5]. Một lời giải thích phù hợp cho mối tương quan lâm sàng-bệnh lý dưới mức tối ưu có thể là do vị trí sinh thiết được chọn không chính xác [6], đặc biệt trong trường hợp rụng tóc có sẹo, các sai sót trong quá trình xử lý mẫu sinh thiết da đầu [7] hoặc đơn giản là lỗi tiêu chuẩn trong trường hợp rụng tóc lan tỏa không sẹo, là do sinh thiết bấm lỗ 4 mm chỉ phát hiện được khoảng 32–50 nang tóc trong khi toàn bộ da đầu có 100.000–150.000 nang tóc. Sinh thiết nên được thực hiện theo góc của sợi tóc đang nhô lên và phải chứa lớp mỡ dưới da.
Dưới đây là một số khuyến nghị về cách tối ưu hóa việc thu thập mẫu sinh thiết da đầu:
- Trong rụng tóc lan tỏa không sẹo, nên thực hiện sinh thiết bấm lỗ 4 mm từ đỉnh da đầu hoặc phần giữa da đầu vì đây được coi là vị trí tối ưu để đánh giá sự thu nhỏ nang tóc, đặc biệt là trong trường hợp rụng tóc kiểu nữ sớm [8]. Không nên lấy sinh thiết ở đường rẽ ngôi để tránh để lại sẹo dễ thấy.
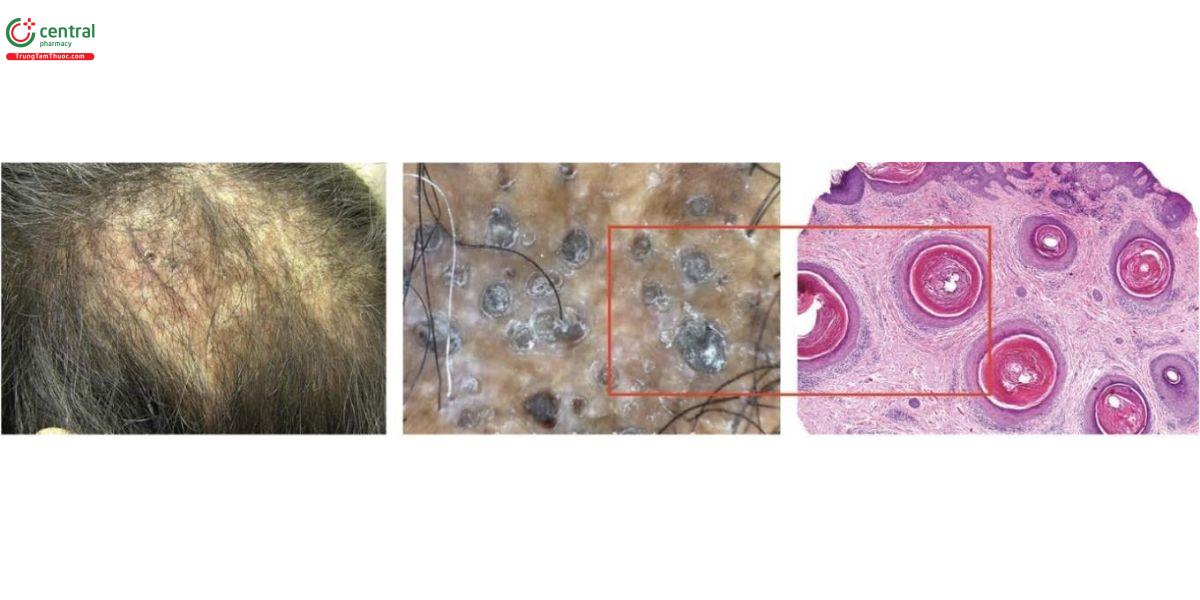
- Trong rụng tóc có sẹo, mẫu bệnh phẩm tối ưu được lấy bằng cách sử dụng máy soi da cầm tay hoặc máy soi da video để hướng dẫn vị trí sinh thiết (sinh thiết da đầu dưới hướng dẫn dermoscopy/trichoscopy) (Hình 7.2) [9].
- Trong rụng tóc xơ hóa vùng trán (FFA), sinh thiết bấm lỗ 3 mm thường là đủ để chẩn đoán, đặc biệt nếu sử dụng kỹ thuật hướng dẫn bằng dermoscopy; sinh thiết bấm lỗ 2 mm dưới hướng dẫn của trichoscopy là đủ cho lông mày.
- Ở những bệnh nhân có biểu hiện lâm sàng và trichoscopy không rõ ràng, số lượng và tỷ lệ nang tóc không quan trọng đối với chẩn đoán, như bệnh mô liên kết có thể xảy ra với bệnh trứng cá đỏ trên da đầu, hai mẫu sinh thiết là cần thiết và cắt theo chiều dọc được ưu tiên.
- Trong các tình trạng viêm da đầu có vảy như viêm da tiết bã, bệnh vảy nến, lichen simplex mãn tính và viêm nang tóc, cắt theo chiều dọc được ưu tiên.
- Trong bất kỳ tình trạng rối loạn tóc không rõ ràng nào, có biểu hiện rụng tóc và có thể có nguyên nhân viêm/tự miễn dịch – nên lấy hai mẫu sinh thiết, một cho các mặt cắt ngang và một cho các mặt cắt dọc.
3 Thực hiện sinh thiết theo mặt cắt ngang
Việc giải thích mô bệnh học của các dấu hiện nang tóc trong sinh thiết da đầu là khó khăn do sự phức tạp về mặt giải phẫu của cấu trúc nang tóc bình thường ở các giai đoạn khác nhau của chu kỳ tóc [1]. Mặt cắt ngang được Headington giới thiệu lần đầu tiên vào năm 1984, công trình của ông đã trở thành hướng dẫn then chốt cho các bác sĩ da liễu đọc sinh thiết tóc và da đầu [1]. Các phương pháp khác bao gồm kỹ thuật HoVert và Tyler [10, 11].
Mặt cắt ngang tốt hơn mặt cắt dọc trong nghiên cứu về đường kính của nang tóc và chu kỳ tóc [1, 5, 12]. Chúng cho phép hình dung tất cả các nang tóc có trong sinh thiết đục lỗ 4 mm và để thực hiện đếm số lượng tóc [13].
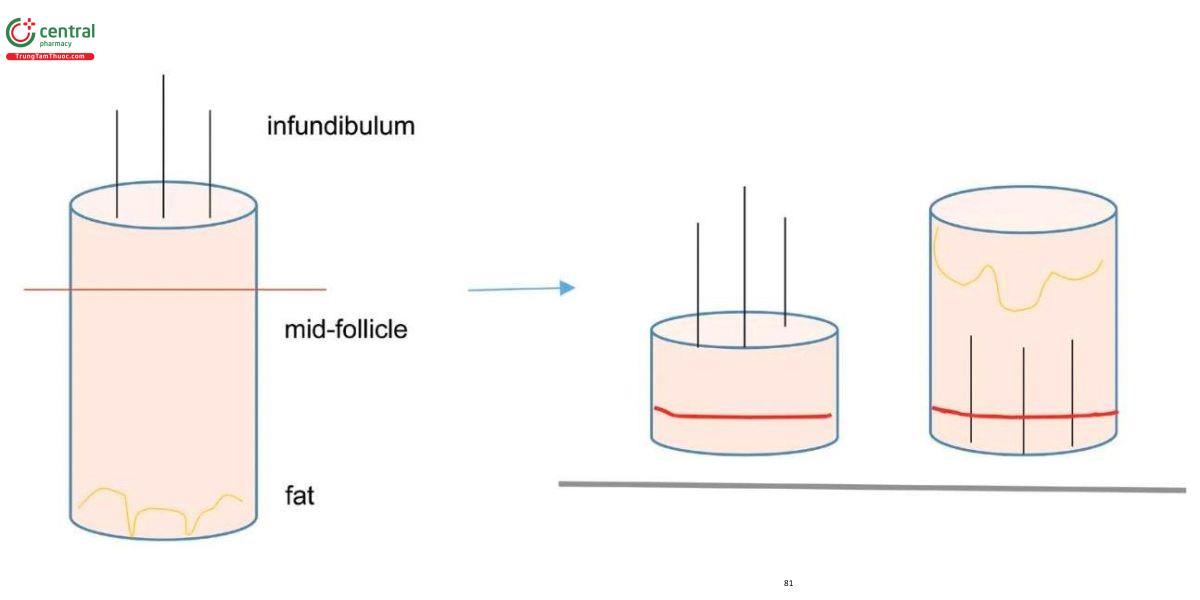
Theo kỹ thuật của Headington, mẫu sinh thiết đục lỗ được cắt đôi chính xác song song với bề mặt da thành hai nửa được đặt trong cùng một khay với bề mặt cắt ở dưới và được cắt cùng nhau (Hình 7.3). Việc cắt đôi thực hiện ở mức eo nang tóc (1–1,5 mm dưới điểm nối biểu bì-bì). Từ một nửa từ vết cắt xuống lớp mỡ dưới da và từ một nửa từ vết cắt đến mức phễu nang tóc và lớp biểu bì (Hình 7.4). Bằng cách này, các nang tóc được đánh giá theo chiều dài ở mức củ nang tóc, trên củ nang tóc, eo nang tóc và phễu nang tóc. Nếu mẫu sinh thiết được cắt đôi chính xác, thường có tới 20 lát cắt là đủ để đánh giá nang tóc dọc theo toàn bộ chiều dài của nó [14], tuy nhiên đôi khi có tới 60 lát cắt được cắt để đạt đến mức phễu nang tóc. Sinh thiết đục lỗ 4 mm có chu vi 12,6 mm2 trong khi sinh thiết 3 mm có chu vi 7 mm2 [15], có nghĩa là 5,6 mm2 bị bỏ qua đánh giá nếu thu mẫu sinh thiết nhỏ hơn.
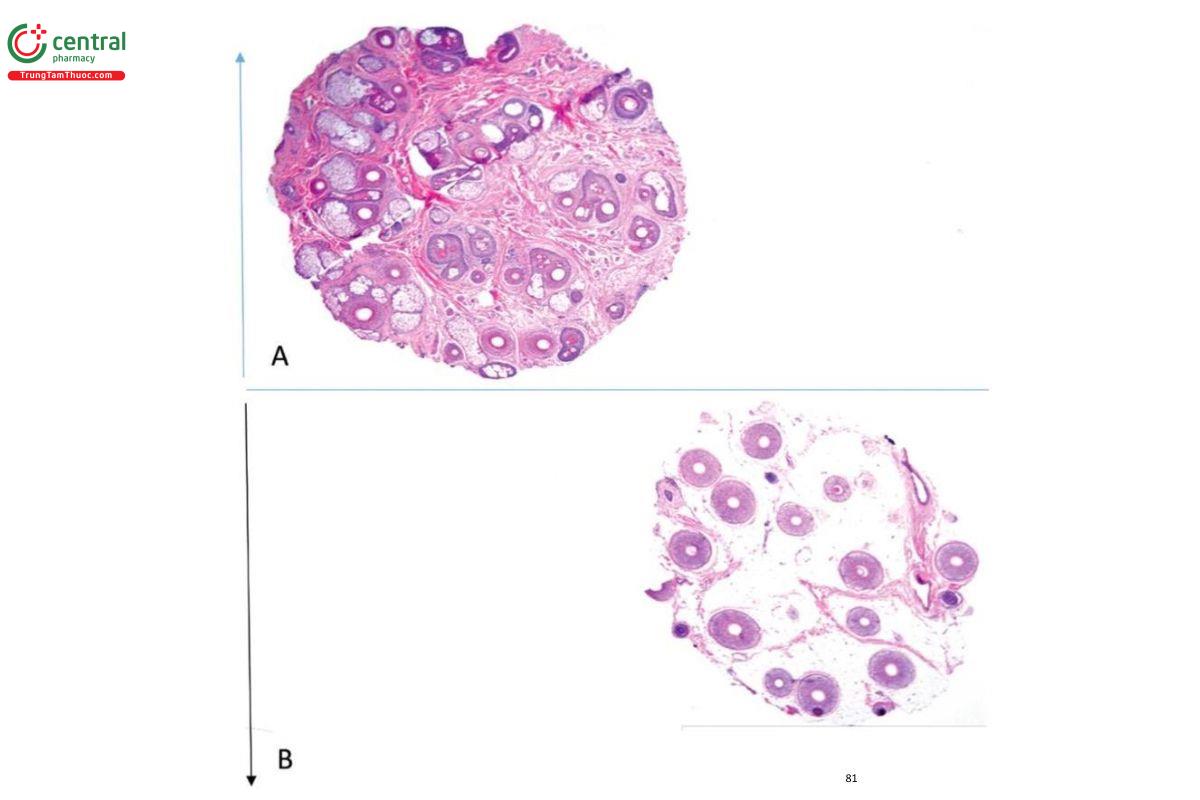
Cấu trúc nang tóc bình thường chứa từ 10–14 đơn vị nang tóc (cấu trúc hình lục giác được bao bọc bởi mạng lưới Collagen lỏng lẻo và bao gồm 3–4 nang tóc terminal và 1 nang tóc vellus với các tuyến bã nhờn kèm theo và cơ dựng tóc). Các đơn vị nang tóc có sự phân bố có trật tự ở mức trung bì giữa (eo nang tóc) và phân bố tuyến tính ở mức trung bì cao (phễu nang tóc).
Nhiều tài liệu hướng dẫn hiện có về chi tiết cụ thể của giải phẫu nang tóc theo các mặt cắt ngang [5, 15, 18] bao gồm hình thái của các loại nang tóc (anagen, catagen, telogen) và kích thước (vellus, trung gian và terminal).
Các thông số nang tóc bình thường được thiết lập tốt nhất trong sinh thiết da đầu 4 mm từ người da trắng [19]:
- Đơn vị nang tóc – 12–14.
- Mật độ nang tóc – 38–40 nang tóc (2–3,1 nang/mm2)
- Tóc terminal anagen – 31
- Tóc terminal catagen/telogen – 2
- Tóc vellus/thu nhỏ (anagen + telogen): –5
- Dải sợi: –2
- Nang tóc terminal: nang tóc vellus: ≥4:1
- Số lượng tóc telogen: ≤15%
Mẫu sinh thiết từ bệnh nhân người Mỹ gốc Phi cho thấy mật độ nang tóc thấp hơn, ở mức 22 nang tóc /mẫu sinh thiết da đầu đục lỗ 4 mm và tỷ lệ terminal:vellus (6:1) [20], và người châu Á thậm chí c n cho thấy mật độ nang tóc thấp hơn là 14– 16 nang tóc /mẫu sinh thiết đục lỗ 4 mm (1,2 nang/mm2) [21].
4 Kỹ thuật bổ sung trong đánh giá sinh thiết da đầu
Không có bằng chứng nào cho thấy một bảng các mẫu nhuộm đặc biệt hoặc nhuộm hóa mô miễn dịch có thể hữu ích khi sử dụng thường quy trong bệnh học tóc [22]. Không có mẫu nhuộm nào có thể phân biệt hiệu quả giữa rụng tóc không sẹo và rụng tóc có sẹo. Một trong những mẫu nhuộm phổ biến nhất được các nhà nghiên cứu bệnh học dùng trong sinh thiết tóc là Verhoeff-Van Gieson (VVG), còn được gọi là nhuộm Elastin Van Gieson (EVG). Một nghiên cứu về mô đàn hồi trong mẫu sẹo được cắt bỏ cho thấy rằng các sợi đàn hồi không được phát hiện trong sẹo có thời gian dưới 3 tháng, sau đó chúng sẽ tăng lên [23]. Do đó, do sẹo hình thành theo thời gian nên mô đàn hồi trong giai đoạn đầu của rụng tóc có sẹo có thể không thể phân biệt được với mô đàn hồi trong rụng tóc không có sẹo [24, 25]. EVG được cho là hữu ích trong rụng tóc để làm nổi bật các vùng xơ hóa (sẹo nang tóc) trên nền lớp bì hyalin hóa trong rụng tóc có sẹo giai đoạn cuối [24].
Các kiểu sợi đàn hồi ở da đầu bình thường, rụng tóc không có sẹo và rụng tóc có sẹo [25] được tóm tắt trong Bảng 7.1
BẢNG 7.1 Các dạng sợi đàn hồi ở da đầu bình thường, rụng tóc không sẹo và rụng tóc có sẹo
| Rối loạn tóc | Kiểu sợi đàn hồi |
| Da đầu bình thường Rụng tóc không sẹo Rụng tóc có sẹo | Các sợi mảnh ở lớp bì nhú và các sợi dày hơn ở lớp bì lưới Không có thay đổi trong sợi đàn hồi • Giai đoạn sớm: chưa có sẹo • Giai đoạn trễ: • Sẹo hình nêm nông không có viêm đáng kể (lichen planopilaris) • Sẹo lan rộng với bạch cầu trung tính không thường xuyên (viêm nang tóc decalvan) • Sẹo toàn bộ lớp bì với mất mô đàn hồi (lupus ban đỏ dạng đĩa) • Lớp bì hyalin hóa với các vùng xơrộng và các sợi đàn hồi dày cuộn lại (rụng tóc có sẹo trung tâm ly tâm). |
Chúng tôi cũng sử dụng kính hiển vi phân cực để phân biệt các dải sợi hyalin hóa lâu dài trong rụng tóc androgen kéo dài với rụng tóc bẩm sinh tập trung từ các dải sợi trong rụng tóc có sẹo nguyên phát dựa trên thực tế là collagen của con người có khả năng cho ánh sáng truyền qua trong một mặt phẳng cụ thể (lưỡng chiết) [26].
Các tình huống chẩn đoán phân biệt phổ biến (manh mối và mẹo):
1. Rụng tóc androgen (AGA) so với AGA có lichen planopilaris (rụng tóc xơ hóa theo phân bố kiểu hình, FAPD)
Theo kinh nghiệm của tôi, một vấn đề phổ biến trong thực hành bệnh học tóc hàng ngày là thâm nhiễm tế bào lympho nhẹ kèm theo xơ hóa nhẹ ở mức phễu nang tóc thường bị chẩn đoán quá mức là lichen phẳng nang tóc. Theo Whiting, 70% mẫu sinh thiết từ rụng tóc kiểu hình ở nam giới (MPHL) cho thấy một số loại viêm và xơ hóa, với 36% cho thấy tình trạng viêm/xơ hóa đáng kể so với 9% ở nhóm chứng khỏe mạnh. Những trường hợp này được gọi là MPHL “phức tạp” và MPHL “đơn giản” đối với những trường hợp không thể hiện đặc điểm này (Hình 7.5) [19]. Trong AGA, thâm nhiễm viêm và xơ hoá thường bao quanh các nang tóc riêng lẻ và xơ hóa không xếp thành lớp và dày mà khá lỏng lẻo và nhẹ, và vỏ rễ ngoài còn nguyên vẹn. Các mặt cắt ngang hữu ích để xác định xem từng nang tóc có bị ảnh hưởng hay không và đánh giá đúng cấu trúc nang tóc với các vùng tập trung của nang tóc mất đi.
2. Rụng tóc từng vùng (AA) và trichotillomania (TTM)
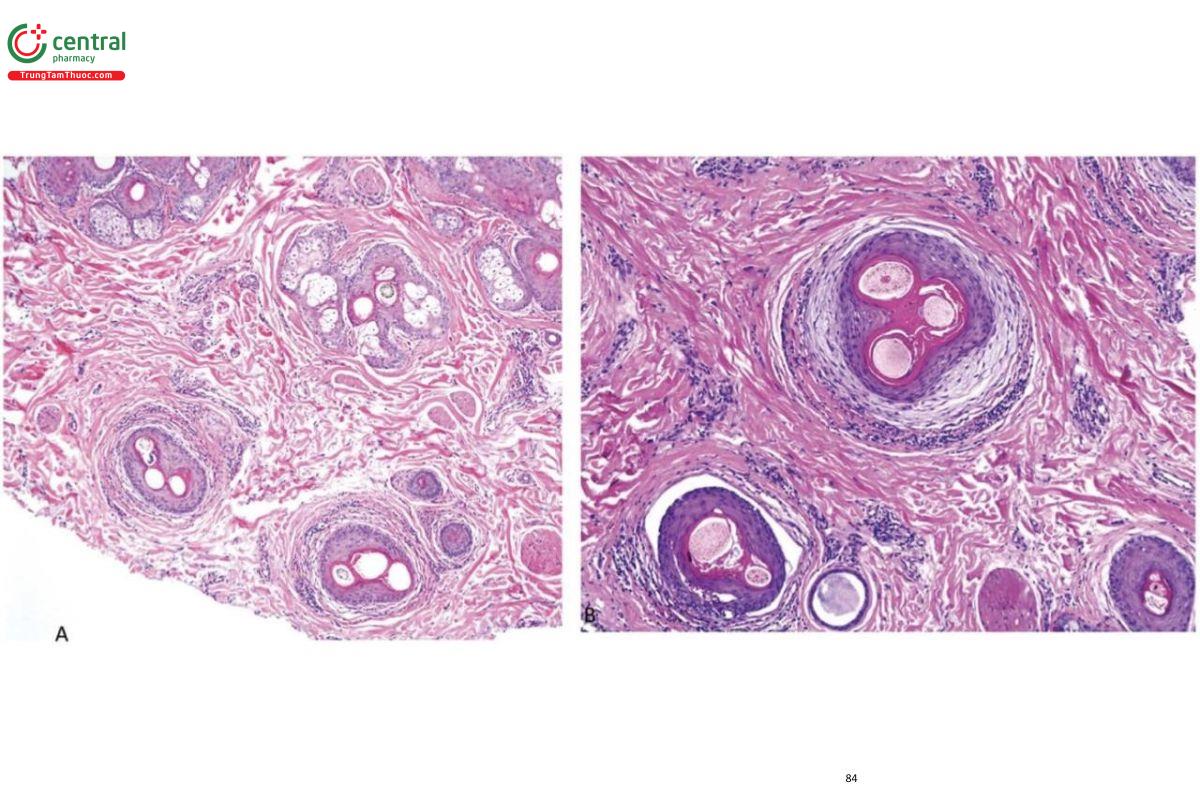
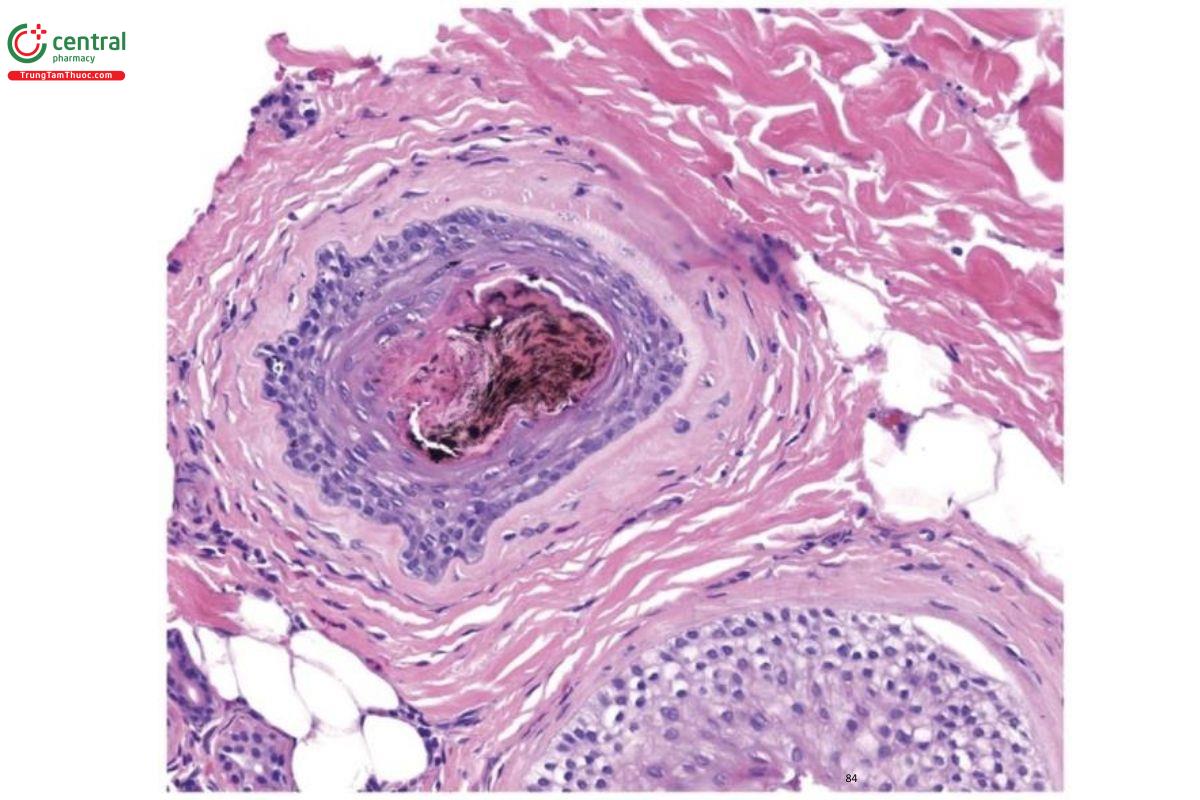
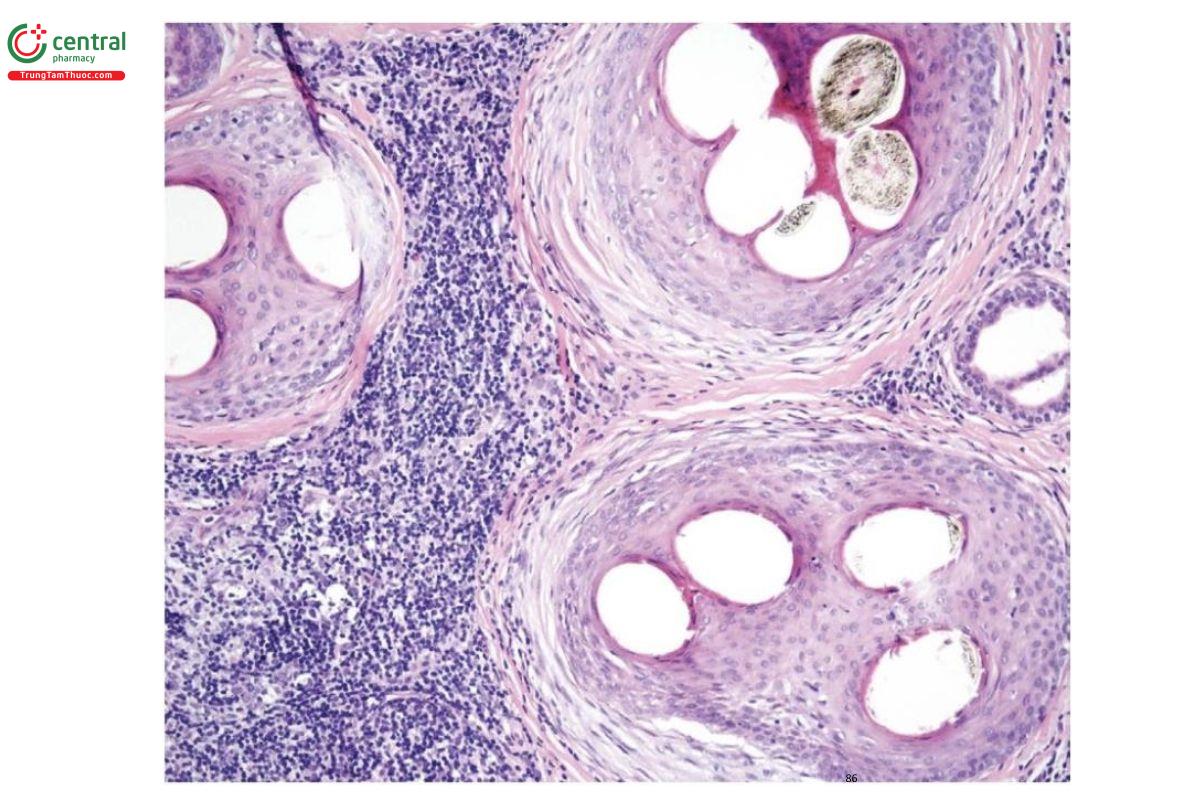
Nhiều khi khó để phân biệt hai tình trạng này về mặt lâm sàng và mô học, đặc biệt khi biểu hiện lâm sàng bao gồm các mảng đơn lẻ hoặc khi cả hai tình trạng cùng tồn tại. Việc phát hiện các trụ có sắc tố trên bệnh lý có thể được sử dụng như một đầu mối để chẩn đoán chính xác. Các trụ có sắc tố xuất hiện dưới dạng các khối melanin thô vô định hình trong cấu trúc nang tóc. Chúng được báo cáo là có nguồn gốc từ các mảnh vụn, chất nền ngoài vị trí bình thường hoặc biểu mô vỏ [27]. Trong TTM, chúng có thể được thấy dưới dạng các khối melanin hình bầu dục, xoắn hoặc tuyến tính bất thường (dấu kéo và nút) ở tất cả các mức của ống nang tóc nhưng không nằm trong các dải sợi hoặc trong các nang tóc vellus. Các nang tóc bị ảnh hưởng thường có biểu hiện apoptosis ở vỏ rễ ngoài (Hình 7.6) [28].
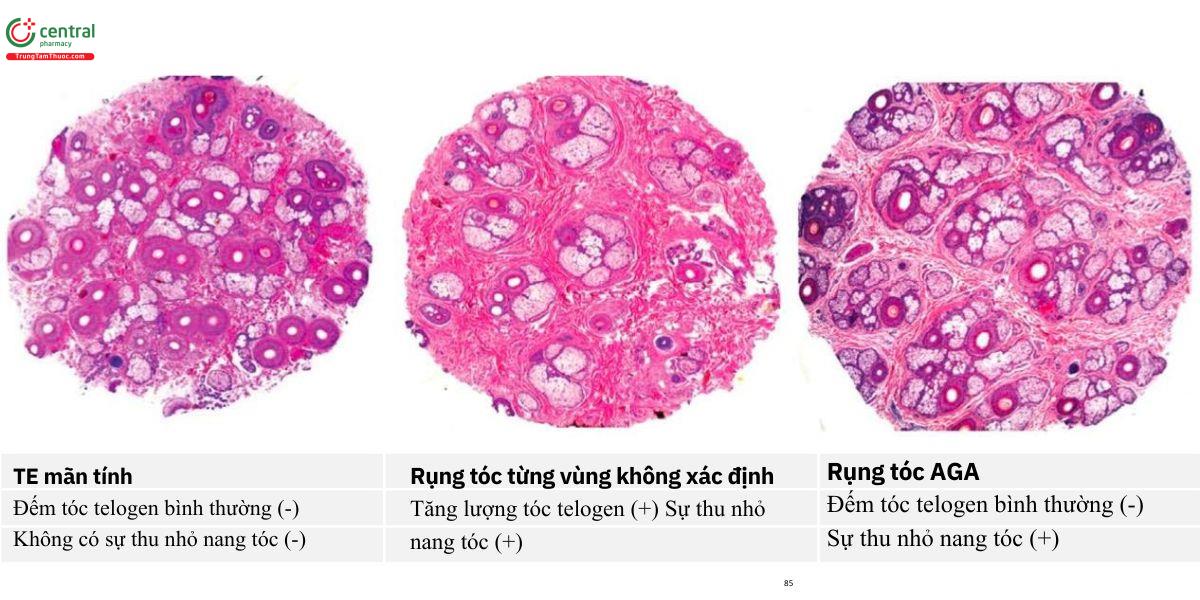
3. Rụng tóc AGA vs rụng tóc telogen (TE) vs rụng tóc từng vùng không xác định (AAI) Đây là một tình huống phổ biến trong thực hành lâm sàng và bệnh học tóc. Điều quan trọng là liên hệ giữa chẩn đoán lâm sàng và mô học trong các trường hợp rụng tóc lan tỏa không sẹo ở phụ nữ vì các đặc điểm trùng lặp và không có tiêu chí rõ ràng để chẩn đoán AAI trên TE. Tuy nhiên, sự xuất hiện đột ngột của hiện tượng rụng tóc lan tỏa mà không có yếu tố kích thích trước đó, liên quan thử nghiệm kéo tóc dương tính rõ, tóc mỏng lan tỏa và các đặc điểm mô học của sự thu nhỏ nang tóc ở rìa tóc (khoảng 3:1) với tăng số lượng tóc telogen (khoảng 30%), lỗ phễu nang tóc giãn (kiểu phô mai Thụy Sĩ) và sự tăng số lượng nang tóc vellus telogen và đơn vị phôi telogen phù hợp với chẩn đoán AAI (Hình 7.7) [29]. Chỉ có thể sử dụng các mặt cắt ngang để chẩn đoán.
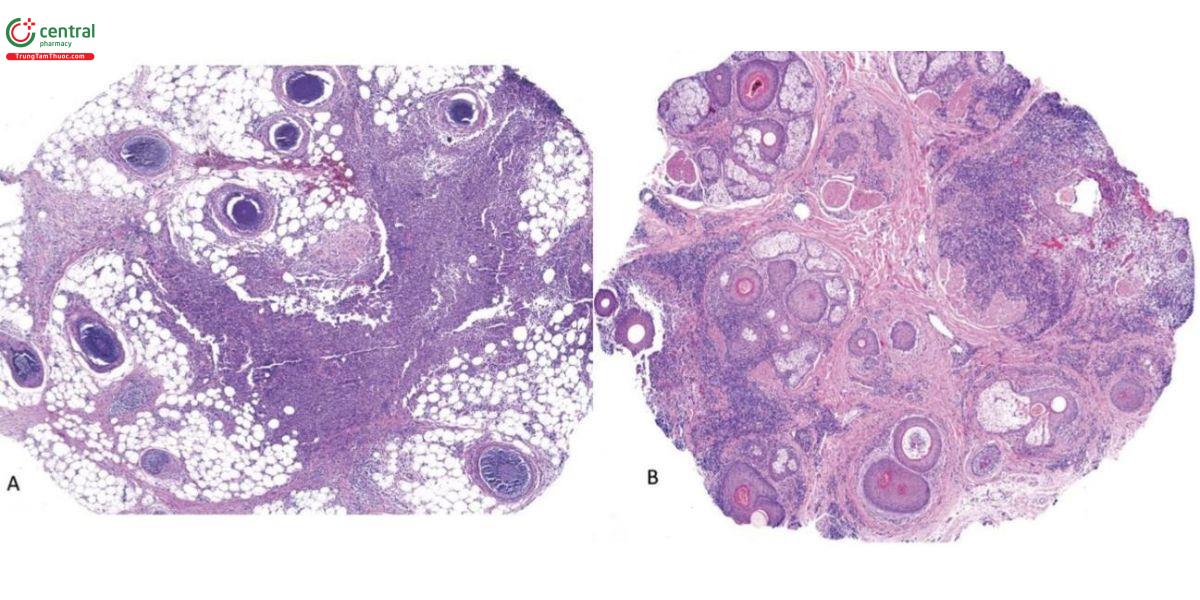
4. Viêm nấm da đầu (TC) và viêm mô tế bào nứt nẻ da đầu (DCS)
Mẫu sinh thiết từ DCS sớm cho thấy thâm nhiễm tế bào hỗn hợp dày đặc và lan tỏa chiếm phần dưới của lớp bì và lớp dưới da. Phần thâm nhiễm cũng chứa các tế bào khổng lồ, phù nề, giãn mạch và sự thoát mạch của hồng cầu. Phần lớn các nang tóc đều ở giai đoạn telogen và tuyến bã nhờn vẫn có thể được bảo tồn ở giai đoạn đó (Hình 7.8). Chẩn đoán phân biệt bao gồm nấm da đầu kerion trong đó tình trạng viêm kéo dài từ bề mặt đến dưới lớp bì [30]. Nhiều mặt cắt liên tiếp là cần thiết để chẩn đoán. Đáng chú ý, trong một nghiên cứu về kerion trong 35% trường hợp, nhuộm bạc methenamine (GMS) PAS và Grocott âm tính với nấm [31] và do đó KOH cũng như nuôi cấy hữu ích hơn PAS trong việc phát hiện nấm.
5. Viêm nang tóc decalvans (FD) và lichen phẳng nang tóc (LPP) Có một nhóm nhỏ bệnh nhân bị rụng tóc có sẹo biểu hiện các đặc điểm kép của cả FD và LPP cả về mặt lâm sàng và mô học. Những bệnh nhân này biểu hiện các đặc điểm lâm sàng và trichoscopy của LPP với các đặc điểm đồng thời không thể chỉ quy cho kiểu hình LPP và gợi ý FD. Chúng bao gồm (a) nhiều sợi tóc (2–5 sợi tóc), (b) nuôi cấy vi khuẩn dương tính với Staphylococcus ở hơn một nửa số bệnh nhân và (c) các đặc điểm mô học bao gồm cấu trúc nang tóc đa hợp (hơn hai nang hợp nhất), teo biểu mô nang, thành phần tế bào plasma nổi bật trong thâm nhiễm (cả lichen hoá và vùng kẽ) và u hạt (Hình 7.9) [32].
5 Tài liệu tham khảo
1. Headington JT. Transverse microscopic anatomy of the human scalp. A basis for a morphometric approach to disorders of the hair follicle. Arch Dermatol. Apr 1984;120(4):449–456.
2. Miteva M, Tosti A. Dermatoscopy of hair shaft disorders. J Am Acad Dermatol. Mar 2013;68(3):473– 481.
3. Baquerizo Nole KL, Nusbaum B, Pinto GM, Miteva M. Lichen planopilaris in the androgenetic alopecia area: A pitfall for hair transplantation. Skin Appendage Disord. Mar 2015;1(1):49–53.
4. Sinclair R, Jolley, D, Mallari, R, Magee, J. The reliability of horizontally sectioned scalp biopsies in the diagnosis of chronic diffuse telogen hair loss in women. J Am Acad Dermatol. 2004;51:189–199.
5. Whiting DA. Diagnostic and predictive value of horizontal sections of scalp biopsy specimens in male pattern androgenetic alopecia. J Am Acad Dermatol. May 1993;28(5 Pt 1):755–763.
6. Harries MJ, Trueb RM, Tosti A, et al. How not to get scar(r)ed: Pointers to the correct diagnosis in patients with suspected primary cicatricial alopecia. Br J Dermatol. Mar 2009;160(3):482–501.
7. Miteva M, Lanuti E, Tosti A. Ex vivo dermatoscopy of scalp specimens and slides. Journal of the European Academy of Dermatology and Venereology: JEADV. Sep 2014;28(9):1214–1218.
8. Whiting, DA. Scalp biopsy as a diagnostic and prognostic tool in androgenetic alopecia. Dermatol Ther. 1998;3:24–33.
9. Miteva M, Tosti A. Dermoscopy guided scalp biopsy in cicatricial alopecia. Journal of the European Academy of Dermatology and Venereology: JEADV. Oct 2013;27(10):1299–1303.
10. Nguyen JV, Hudacek K, Whitten JA, et al. The HoVert technique: A novel method for the sectioning of alopecia biopsies. J Cutan Pathol. May 2011;38(5):401–406.
11. Elston D. The ‘Tyler technique’ for alopecia biopsies. J Cutan Pathol. Feb 2012;39(2):306.
12. Solomon AR. The transversely sectioned scalp biopsy specimen: The technique and an algorithm for its use in the diagnosis of alopecia. Adv Dermatol. 1994;9:127–157; discussion 158.
13. Sperling LC. Scarring alopecia and the dermatopathologist. J Cutan Pathol. Aug 2001;28(7):333–342.
14. Frishberg DP, Sperling LC, Guthrie VM. Transverse scalp sections: A proposed method for laboratory processing. J Am Acad Dermatol. Aug 1996;35(2 Pt 1):220–222.
15. Sperling LC. An Atlas of Hair Pathology with Clinical Correlations. New York: Parthenon Publishing; 2003.
16. Miteva M. A comprehensive approach to hair pathology of horizontal sections. Am J Dermatopathol. Jul 2013;35(5):529–540.
17. Stefanato CM. Histopathology of alopecia: A clinicopathological approach to diagnosis. Histopathology. Jan 2010;56(1):24–38.
18. Miteva M. Hair pathology: The basics. In: Miteva M, ed. Alopecia. 1st ed. United States: Elsevier; 2018:23 – 41.
19. DA W. Scalp biopsy as a diagnostic and prognostic tool in androgenetic alopecia. Dermatol Ther. 1998;8(24):33.
20. Sperling LC. Hair density in African Americans. Arch Dermatol. Jun 1999;135(6):656–658.
21. Lee HJ, Ha SJ, Lee JH, et al. Hair counts from scalp biopsy specimens in Asians. J Am Acad Dermatol. Feb 2002;46(2):218–221.
22. LaSenna C, Miteva M. Special stains and immunohistochemical stains in hair pathology. Am J Dermatopathol. May 2016;38(5):327–337.
23. Roten SV, Bhat S, Bhawan J. Elastic fibers in scar tissue. J Cutan Pathol. Feb 1996;23(1):37–42.
24. Elston DM, McCollough ML, Warschaw KE, et al. Elastic tissue in scars and alopecia. J Cutan Pathol. 2000;27:147–152.
25. Kazlouskaya V, Malhotra S, Lambe J, et al. The utility of elastic Verhoeff-Van Gieson staining in dermatopathology. J Cutan Pathol. Feb 2013;40(2):211–225.
26. Miteva M, Tosti A. Polarized microscopy as a helpful tool to distinguish chronic nonscarring alopecia from scarring alopecia. Arch Dermatol. Jan 2012;148(1):91–94.
27. Sperling LC, ed. An Atlas of Hair Pathology with Clinical Correlations. New York: Parthenon Publishing Group; 2003; No. 1.
28. Miteva M, Romanelli P, Tosti A. Pigmented casts. Am J Dermatopathol. Jan 2014;36(1):58–63.
29. Miteva M, Misciali C, Fanti PA, Tosti A. Histopathologic features of alopecia areata incognito: A review of 46 cases. J Cutan Pathol. Jun 2012;39(6):596–602.
30. Isa-Isa R, Arenas R, Isa M. Inflammatory tinea capitis: kerion, dermatophytic granuloma, and mycetoma. Clin Dermatol. Mar 04 2010;28(2):133–136.
31. Arenas R, Toussaint S, Isa-Isa R. Kerion and dermatophytic granuloma. Mycological and histopathological findings in 19 children with inflammatory tinea capitis of the scalp. Int J Dermatol. 2006;45:215–219.
32. Egger A, Stojadinovic O, Miteva M. Folliculitis decalvans and lichen planopilaris phenotypic spectrum- A series of 7 new cases with focus on histopathology. Am J Dermatopathol. Mar 2020;42(3):173–177.

