Hướng dẫn thực hành lâm sàng về Bệnh loét dạ dày tá tràng JSGE 2020

Trungtamthuoc.com - Năm 2020 Hiệp hội tiêu hóa Nhật Bản (JSGE) đã sửa đổi hướng dẫn thực hành lâm sàng dựa trên bằng chứng lần 3 về bệnh loét dạ dày – tá tràng.
Người dịch: BS Văn Viết Thắng
Hướng dẫn thực hành lâm sàng dựa trên bằng chứng về bệnh loét dạ dày tá tràng (xem bản gốc tại đây)
1 Tóm lược
Hiệp hội tiêu hóa Nhật Bản đã sửa đổi hướng dẫn lâm sàng lần 3 về bệnh loét dạ dày – tá tràng năm 2020 và tạo một phiên bản tiếng Anh. Hướng dẫn được sửa đổi gồm 9 nội dung: Dịch tễ học, xuất huyết dạ dày và tá tràng do loét, liệu pháp không diệt trừ, loét do thuốc, không nhiễm H. Pylori, và loét do NSAID, loét trên dạ dày còn lại, điều trị bằng phẫu thuật và điều trị bảo tồn cho thủng và hẹp. phương pháp điều trị khác nhau dựa trên biến chứng của loét. Ở bệnh nhân loét do NSAID, các thuốc NSAID được ngưng và sử dụng thuốc chống loét. Nếu NSAID không thể ngưng sử dụng, loét sẽ được điều trị bằng thuốc ức chế bơm Proton. Vonoprazon và kháng sinh được khuyến cáo là lựa chọn hàng đầu cho diệt trừ HP, và PPIs hoặc Vonoprazan kết hợp kháng sinh được khuyến cáo là điều trị hàng thứ 2. Bệnh nhân không sử dụng NSAIDs và có HP âm tính thì nghĩ đến loét dạ dày tá tràng tự phát. Chiến lược để dự phòng loét dạ dày tá tràng do NSAID và Aspirin liều thấp được trình bày trong hướng dẫn này. Cách thức điều trị khác nhau phụ thuộc vào việc đồng thời sử dụng NSAIDs hoặc Aspirin liều thấp với tiền sử loét hoặc xuất huyết tiêu hóa trước đây. Ở bệnh nhân có tiền sử loét có sử dụng NSAIDs, PPIs có hoặc không Celecoxib được khuyến cáo và sử dụng. Vonoprazon được đề nghị để dự phòng loét tái phát. Ở bệnh nhân có tiền sử loét có uống Aspirin liều thấp, PPIs hoặc Vonoprazon được khuyến cáo và điều trị bằng kháng Histamine H2 được đề nghị đề dự phòng loét tái phát.
2 Giới thiệu
Năm 2009, hiệp hội tiêu hóa Nhật Bản đã cho ra đời hướng dẫn thực hành lâm sàng dựa trên bằng chứng về bệnh loét dạ dày tá tràng. Hướng dẫn này được sửa đổi vào năm 2015 và lần nữa vào năm 2020. Trong số 90 câu hỏi trong hướng dẫn trước đó, có những câu hỏi có kết luận rõ ràng, và có những câu hỏi phải phụ thuộc vào kết quả của những nghiên cứu trong tương lai, chúng được giải đáp và sửa đổi trong hướng dẫn này. Vì thế, hướng dẫn sửa đổi này bao gồm 9 nội dung (28 câu hỏi lâm sàng và 1 câu hỏi giải đáp trong nghiên cứu gần đây), bao gồm, cũng là lần đầu tiên về dịch tễ học và ổ loét dạ dày – tá tràng còn tổn tại. Cả dịch tễ học và phương pháp điều trị bảo tồn cho thủng và hẹp trong các câu hỏi nền tảng. Dự phòng xuất huyết do loét dạ dày – tá tràng ở bệnh nhân uống thuốc kháng tiểu cầu và điều trị loét tá tràng do thiếu máu cục bộ đã được them vào câu hỏi lâm sàng và câu hỏi cần trả lời trong tương lai.
Tìm kiếm tài liệu trên thư viện Medline và Cochrane đã được thực hiện về tài liệu liên quan đến các câu hỏi lâm sàng đăng tải từ năm 1983 đến tháng 10 năm 2018, và cơ sở dữ liệu Igaku Chuo Zasshi được tìm kiếm về dữ liệu đăng tải từ 1983 đến tháng 10 năm 2018. Hướng dẫn này được phát triển sử dụng hệ thống thẩm định, phát triển và đánh giá khuyến cáo (GRADE). Chất lượng bằng chứng được chia thành các mức A (cao), B (trung bình), C (thấp) và D (rất thấp). Độ mạnh khuyến cáo được chia thành khuyến cáo mạnh hoặc khuyến cáo yếu. Các đội đánh giá có hệ thống bao gồm các nghiên cứu phân tích tổng hợp và đưa ra quyết định về độ mạnh của bằng chứng từ A đến D. Sự đồng thuận được định nghĩa khi có ít nhất 70% đồng ý.
Ở Nhật Bản, tỷ lệ mắc bệnh nhồi máu não và nhồi máu cơ tim đang tăng và nhiều bệnh nhân đang sử dụng thuốc kháng kết tập tiểu cầu bao gồm cả liệu pháp kháng kết tập tiểu cầu kép. Trong thực hành lâm sàng về nội soi, trọng tâm đã chuyển đổi từ nguy cơ xuất huyết tiêu hóa sang thuyên tắc – huyết khối có liên quan đến tác dụng phụ của liệu pháp kháng kết tập tiểu cầu. Ngoài ra, trong 50 trở lại đây, thuốc kháng đông đường uống như thuốc kháng vitamin K (Warfarin), tuy nhiên, 4 loại thuốc kháng đông không tác dụng thụ thể vitamin K (DOACs) hiện được sử dụng. Phần hướng dẫn được sửa đổi ở bệnh xuất huyết tiêu hóa do loét dạ dày và tá tràng nhấn mạnh phương pháp để ngưng kháng kết tập tiểu cầu bao gồm cả DOACs và dự phòng xuất huyết tiêu hóa do loét ở bệnh nhân uống thuốc kháng đông và kháng kết tập tiểu cầu gồm cả liệu pháp kháng kết tập tiểu cầu kép
Vonoprazan (VPZ) cung cấp ức chế tiết acid dạ dày kéo dài và mạnh, và tính hiệu quả của nó. Vì thế, nó được mong đợi sẽ vượt trội hơn thuốc ức chế bơm Proton (PPIs). Những báo cáo hiện tại chỉ ra rằng liệu pháp bộ ba bao gồm Vonoprazan có hiệu quả trong phác đồ “first line” và “second line” diệt trừ HP. Một vài nghiên cứu chỉ ra VPZ có hiệu quả chữa trị loét dạ dày – tá tràng và dự phòng tái phát ở bệnh nhân loét dạ dày có liên quan đến việc sử dụng NSAIDs và Aspirin liều thấp. Phiên bản sửa đổi lần này cũng nhấn mạnh kết quả lâm sàng của VPZ.
3 Xuất huyết tiêu hóa do loét dạ dày – tá tràng
Liệu pháp cầm máu ở bệnh nhân không nội soi
Câu hỏi lâm sàng 1: Điều trị bệnh nhân XHTH do loét dạ dày – tá tràng như thế nào ở nhóm BN có sử dụng kháng đông và/ hoặc kháng kết tập tiểu cầu?
- Khuyến cáo Aspirin được tiếp tục sử dụng ở nhóm bệnh nhân ở nhóm nguy cơ cao có biến cố huyết khối/ tắc mạch.
- Khuyến cáo: mạnh, 100% đồng thuận, mức độ chứng cứ: B
- Đề xuất chuyển thuốc kháng kết tập tiểu cầu sang Aspirin ở Bn trong tình trạng có nguy cơ cao có biến cố huyết khối/tắc mạch.
- Khuyến cáo: yếu. 100% đồng thuận. Mức chứng cứ: D
- Đề xuất ngưng kháng kết tập tiểu cầu, ngoại trừ ở bệnh nhân có nguy cơ cao có biến cố huyết khối/ tắc mạch.
- Khuyến cáo: yếu. 100% đồng thuận. Mức chứng cứ: D
- Đề nghị ngưng Wafarin, nếu có thể, ở bệnh nhân cầm máu qua nội soi. Nếu Wafarin được ngưng sử dụng, chúng tôi đề nghị Heparin hoặc tiếp tục Wafarin càng sớm khi việc cầm máu được thiết lập.
- Khuyến cáo: mạnh. 100% đồng thuận. Mức độ bằng chứng: C
- Đề xuất tiếp tục DOACs sớm (trong vòng 1 – 2 ngày) sau khi xác nhận cầm máu qua nội soi.
- Khuyến cáo: yếu. 100% đồng thuận. Mức chứng cứ: D
- Ở bệnh nhân sử dụng kháng kết tập tiểu cầu kép và Wafarin, đề xuất đổi kháng kết tập tiểu cầu kép sang Aspirin và Cilostazol. Tiếp tục Wafarin dưới ngưỡng PT-INR phù hợp hoặc chuyển Wafarin sang Heparin.
- Khuyến cáo yếu, 100% đồng thuận , Mức chứng cứ D
- Ở bệnh nhân sử dụng kháng kết tập tiểu cầu kép, khuyến cáo tiếp tục sử dụng 1 mình Aspirin.
Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ D
Bình luận: Nguy cơ tái xuất huyết vì tiếp tục sử dụng kháng đông và/hoặc kháng kết tập tiểu cầu và nguy cơ huyết khối/tắc mạch liên quan đến việc ngưng sử dụng chúng phải được cân nhắc. Một nghiên cứu ngẫu nhiên có đối chứng đã báo cáo tỷ lệ tử vong thấp hơn có ý nghĩa ở nhóm bệnh nhân tiếp tục sử dụng thuốc kháng đông, kháng kết tập tiểu cầu so với nhóm không sử dụng. Tuy nhiên, bằng chứng lâm sàng hiện tại đang thiếu để ủng hộ quản lí nhóm bệnh nhân này, những người đang uống thuốc kháng kết tập tiểu cầu, kháng đông và DOACs có xuất huyết tiêu hóa. Chúng tôi đã xem xét những khuyến cáo trên dựa trên ý kiến chuyên gia của hướng dẫn nội soi tiêu hóa Nhật Bản, Hiệp hội nội soi Châu Á – Thái Bình Dương và Châu Âu. Cần thiết có sự hợp tác chặt chẽ giữa các chuyên gia tiêu hóa và chuyên gia tim mạch ở bệnh nhân có nguy cơ cao huyết khối/ tắc mạch bị XHTH do loét dạ dày – tá tràng không ổn định.
Câu hỏi lâm sàng 2: Hiệu quả của can thiệp động mạch dưới DSA ở bệnh nhân XHTH do loét dạ dày – tá tràng diễn tiến tái xuất huyết sau khi điều trị nội soi như thế nào?
- Ở bệnh nhân diễn tiến tái xuất huyết sau khi điều trị nội soi, can thiệp động mạch dưới DSA được đề xuất vì tính an toàn và hiệu quả.
Khuyến cáo yếu, 100% đồng thuận, Mức chứng cứ: C
Bình luận: Tính hiệu quả của can thiệp làm thuyên tắc động mạch qua catheter dưới DSA được chứng minh với 2 nghiên cứu phân tích tổng hợp [9,10]. Chúng tôi đã báo cáo rằng khi so sánh với phẫu thuật, can thiệp động mạch có tỷ lệ tái xuất huyết cao hơn nhưng không khác biệt có ý nghĩa về tử vong, cần can thiệp thêm, hoặc tỷ lệ biến chứng giữa 2 loại điều trị. Can thiệp động mạch có thể là lựa chọn khả thi để điều trị tái xuất huyết; tuy nhiên, một số lượng giới hạn bệnh viện có thể thực hiện can thiệp.
Câu hỏi lâm sàng 3: Loại thuốc và thuốc kháng acid nào được sử dụng sau khi điều trị nội soi XHTH do loét dạ dày – tá tràng?
- Thuốc ức chế bơm proton sau khi điều trị nội soi được khuyến cáo để cải thiện kết cục điều trị.
Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ A
Bình luận: so sánh với giả dược, liệu pháp PPI tĩnh mạch sau điều trị nội soi đã được chứng minh giảm tỷ lệ tái xuất huyết, thể tích máu cần truyền, thời gian điều trị, và tỷ lệ chuyển sang phẫu thuật ở hai nghiên cứu phân tích tổng hợp [11,12] và vài nghiên cứu ngẫu nhiên có đối chứng. Hiệu quả của liệu pháp PPI liều cao không cao hơn không sử dụng PPI liều cao về giảm tái xuất huyết, can thiệp phẫu thuật, hoặc tử vong sau cầm máu nội soi.
Không có sự khác biệt có ý nghĩa giữa liệu pháp PPI đường uống và đường tiêm trên tử vong, tái xuất huyết, cần truyền máu, thời gian nằm viện hoặc phẫu thuật.
So sánh với thuốc kháng Histamin H2 đường tĩnh mạch, liệu pháp PPI giảm tỷ lệ tái xuất huyết do loét, can thiệp phẫu thuật, còn thời gian nằm viện tổng thể không khác biệt về tử vong [15]. Xem xét lợi ích của bệnh nhân, chúng tôi đề nghị liệu pháp PPI sau điều trị nội soi ở bệnh nhân XHTH do loét dạ dày – tá tràng.
Câu hỏi lâm sàng 4: Thuốc nào được khuyến cáo để dự phòng XHTH do loét dạ dày tá tràng ở người sử dụng thuốc kháng kết tập tiểu cầu?
- Ở bệnh nhân sử dụng thuốc kháng kết tập tiểu cầu kép, chúng tôi đề nghị kết hợp sử dụng PPIs để phòng ngừa xuất huyết tiêu hóa trên.
Khuyến cáo mạnh, 100% đồng thuận , Mức chứng cứ A
- Nếu uống Wafarin, chúng tôi đề xuất sử dụng PPIs để phòng ngừa XHTH trên ở bệnh nhân uống kháng kết tập tiểu cầu hoặc NSAIDs kết hợp.
Khuyến cáo yếu, 100% đồng thuận, Mức chứng cứ: C
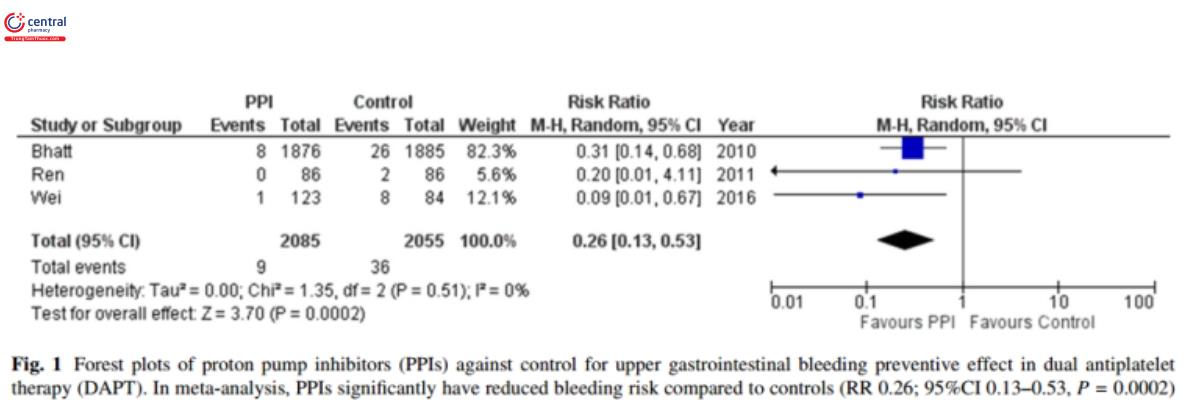
Bình luận: Nhiều phân tích tổng hợp của các nghiên cứu ngẫu nhiên có đối chứng nhằm xác định liệu sự kết hợp PPIs có hữu ích để dự phòng XHTH trên ở bệnh nhân sử dụng kháng kết tập tiểu cầu kép là Aspirin và Clopidogel. Ngoài ra còn có thử nghiệm ngẫu nhiên lớn COGENT [16], một phân tích tổng hợp được tiến hành liên quan đến 3 nghiên cứu (trong đó có 2 nghiên cứu ngẫu nhiên có đối chứng) [17,18] so sánh sử dụng PPI. PPIs ngăn ngừa một cách có ý nghĩa XHTH trên (risk ratio [RR] 0.26; khoảng tin cậy 95% [CI] 0.13 – 1.26, P = 0.0002) (hình 1). Không có sự khác biệt có ý nghĩa ở các biến cố tim mạch chính khi sử dụng hoặc không sử dụng PPI (RR 1.01, 95%CI 0.80-1.26, P=0.96). Năm 2017, cập nhật hướng vào nhóm bệnh nhân sử dụng kháng kết tập tiểu cầu kép ở bệnh động mạch vành của Hội Tim mạch Châu Âu, PPIs kết hợp với DAPT được khuyến cáo (khuyến cáo mở mức I) [19]. Chỉ các nghiên cứu quan sát được thực hiện ở bệnh nhân XHTH trên sử dụng Wafarin dự phòng bằng PPI. Rat et al. [20], trong một nghiên cứu đoàn hệ hồi cứu lớn, đã nhận thấy rằng PPI giảm một cách có ý nghĩa nguy cơ nhập viện vì XHTH trên ở bệnh nhân uống Wafarin đồng thời với kháng kết tập tiểu cầu hoặc NSAIDs (giảm 45% (tỉ số Hazard 0.55; khoảng tin cậy 95% 0.39 – 0.77), P = 0.0004).
4 Liệu pháp diệt trừ Helicobater Pylori
4.1 Phác đồ ưu tiên hàng đầu
Câu hỏi lâm sàng 5: Phác đồ nào được lựa chọn hàng đầu để diệt trừ HP?
- Phác đồ diệt HP sử dụng Vonoprazan (VPZ) với Amixicilin và Clarithromycin có tỷ lệ diệt từ cao hơn khi so sánh với PPIs, VPZ được khuyến cáo ưu tiên hàng đầu.
- Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ A
- Kháng sinh được khuyến cáo hàng đầu bao gồm: Amoxicilin, clarithromycin, hoặc Metronidazole. Ở Nhật bản, phối hợp Amoxiciline và Metronidazole được khuyến cáo bởi vì tỷ lệ lưu hành cao của kháng clarithromycin (nó cũng không được bảo hiểm nhật chi trả).
- Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ A
- Khi ức chế bơm Proton được sử dụng, phác đồ nối tiếp và đồng thời 4 thuốc được đề xuất vì tỷ lệ diệt HP cao ưu tiên hàng đầu khi so sánh với phác đồ 3 thuốc.
Khuyến cáo yếu, 100% đồng thuận, Mức chứng cứ A
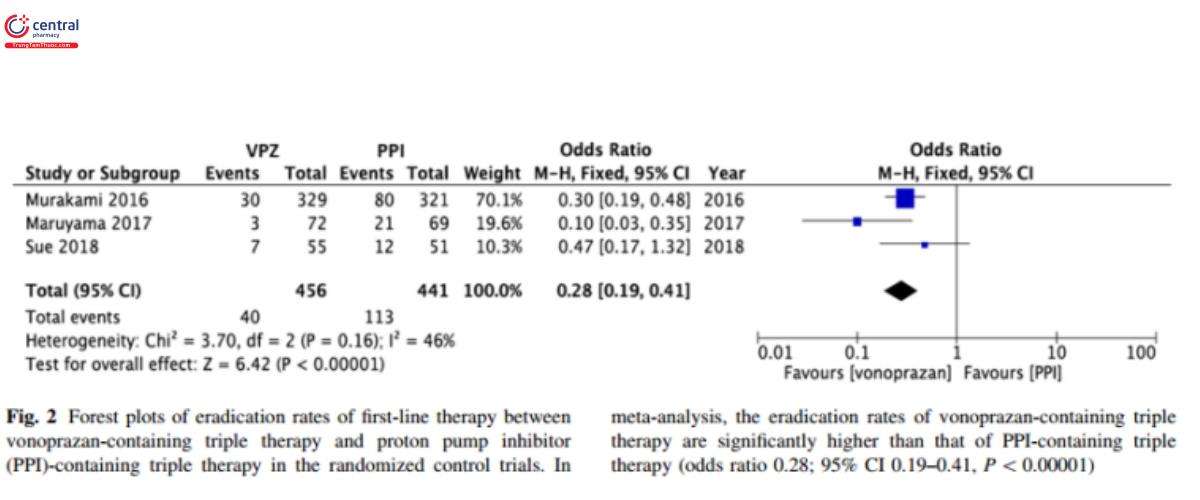
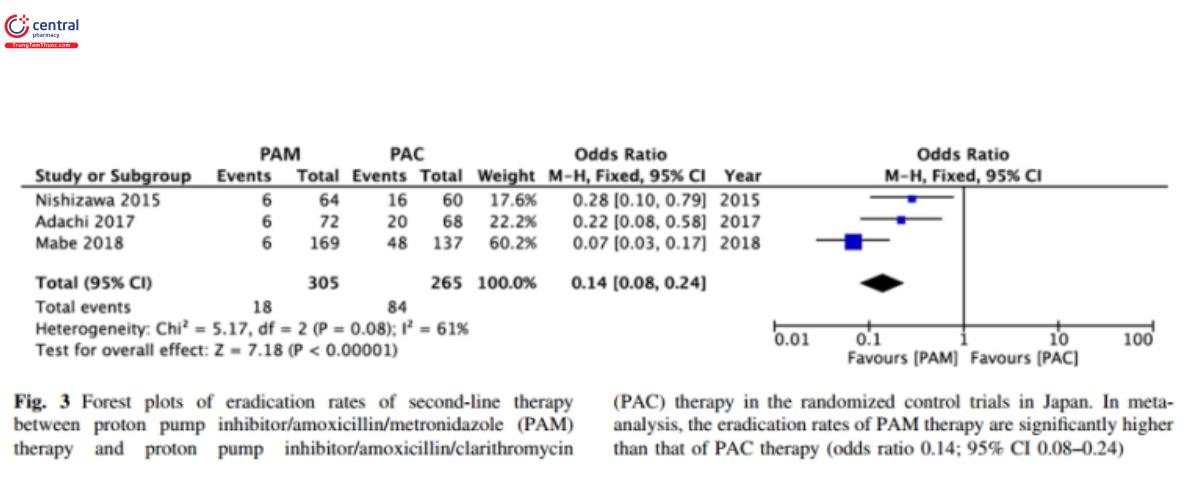
Bình luận: Trong hệ thống bảo hiểm Nhật bản, phác đồ 3 thuốc với PPI hoặc VPZ, Amoxiciline và Clarithromycin được sử dụng như phác đồ đầu tay. Khi mà mức độ và thời gian ức chế acid có liên quan đến tỷ lệ chữa HP [22], một nghiên cứu phân tích tổng hợp so sánh hiệu quả của phác đồ có VPZ với phác đồ có PPI (hình 2) [23]. Ở khu vực có tỷ lệ kháng Clarythromycin cao (>15%), phác đồ đầu tay sử dụng Clarithromycin không được sử dụng, phác đồ 4 thuốc có Bismuth (PPI/Bismuth/Tetracycline/Metronidazole) hoặc phác đồ 4 thuốc đồng thời (PPI/Amoxiciline/Clarithromycin/Nitroimidazole hoặc Metronidazole) được khuyến cáo. Ngoài ra ở những khu vực có tỷ lệ kháng Metronidazole thấp và Clarithromycin cao, PPI/Amoxiciline/Metronidazole có tỷ lệ diệt HP cao hơn PPI/Amoxiciline/Clarithromycin (hình 3) [25].
4.2 Phác đồ diệt trừ Helicobacter Pylori hàng thứ 2
Câu hỏi lâm sàng 6: Phác đồ nào được lựa chọn cho liệu pháp diệt trừ HP hàng thứ hai?
- Phác đồ 3 thuốc gồm PPI/VPZ, Amoxiciline, và Metronidazole được khuyến cáo.
Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ A
Bình luận: hai phân tích tổng hợp [26,27] chỉ ra tetracycline/quinolone trên liệu pháp năm hoặc bốn thuốc hiệu quả hơn các liệu pháp khác. Một nghiên cứu ngẫu nhiên có đối chứng tiết lộ rằng Levofloxacin trong phác đồ nối tiếp có hiệu quả hơn Levofloxacin trong phác đồ 3 thuốc [28]. Những thuốc này chưa từng được chấp thuận cho liệu pháp diệt trừ HP ở Nhật Bản. Ngoài ra, tử lệ nhiễm HP có đề kháng nguyên pháp với levofloxacin cao ở Nhật. Tỷ lệ diệt trừ của liệu pháp 3 thuốc với PPI,VPZ, Amoxiciline và Metronidazole vẫn cao.
4.3 Liệu pháp diệt trừ HP hàng thứ ba
Câu hỏi lâm sàng 7: Phác đồ nào được lựa chọn cho liệu pháp diệt trừ HP hàng thứ ba?
- Phác đồ 3 thuốc gồm PPI, Sitafloxacin, và Metronidazole hoặc PPI, Sitafloxacin và Amoxiciline được đề xuất.
Khuyến cáo yếu, 100% đồng thuận, Mức chứng cứ B
Bình luận: Ba nghiên cứu ngẫu nhiên có đối chứng của liệu pháp hàng thứ ba chỉ ra tỷ lệ diệt trừ là 70-90.9% [32-34]. Tỷ lệ diệt trừ của thuốc đồ 3 thuốc với PPI, sitafloxacin, Metronidazole là 70-88.9%, với PPI,Sitafloxacin, Amoxiciline là 72.4-90.9%[33, 34]. Bởi vì tỷ lệ diệt trừ này không đủ cao, những phác đồ này không được khuyến cáo, chúng tôi chỉ đề xuất.
4.4 Loét tái phát sau diệt trừ Helicobater Pylori
Câu hỏi lâm sàng 8: Có cần thiết duy trì điều trị khi loét dạ dày – tá tràng tái phát sau diệt trừ thành công H.Pylori?
- Khi nguyên nhân của loét tái phát không rõ, duy trì điều trị kéo dài với PPIs hoặc thuốc kháng Histamin H2 được đề xuất.
Khuyến cáo yếu, 100% đồng thuận, Mức chứng cứ D
Bình luận: hiện tại chưa có nhiều nghiên cứu ngẫu nhiên có đối chứng hoặc phân tích tổng hợp được đăng tải. Nguyên nhân của tái phát loét sau diệt trừ thành công H.Pylori bao gồm sử dụng Aspirin liều thấp, NSAIDs, tái nhiễm HP, và hútthuốc lá. Để phòng ngừa loét dạ dày – tá tràng tái phát, việc cần thiết phải loại trừ các yếu tố trên. Loét dạ dày – tá tràng tự phát khi không có nguyên nhân nào sau diệt trừ thành công HP. Vì thế, duy trì điều trị kéo dài với PPIs hoặc ức chế histamin H2 được đề xuất, khi nguyên nhân của loét tái phát không rõ.
5 Liệu pháp không diệt trừ
Phác đồ khởi đầu
5.1 Loét dạ dày
Câu hỏi lâm sàng 9: Loại thuốc đầu tay nào để khởi đầu điều trị loét dạ dày không diệt trừ HP (HP âm tính)?
- Cả PPIs hoặc thuốc kháng acid cạnh tranh Kali được khuyến cáo.
Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ A
- Nếu cả PPIs và thuốc kháng acid canh tranh Kali không được kê đơn, thuốc kháng Histamin H2 được khuyến cáo
Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ B.
- Nếu cả PPIs và thuốc kháng acid canh tranh Kali không được kê đơn, Pirenzepine, Sucralfate, và Misoprostol được đề xuất.
Khuyến cáo yếu, 100% đồng ý, Mức chứng cứ B
- Nếu tất cả thuốc kể trên không thể kê đơn, thuốc bảo vệ niêm mạc dạ dày (ngoại trừ Sucralfate và Misoprostol) được đề xuất.
Khuyến cáo yếu, 100% đồng thuận, Mức chứng cứ B
Bình luận: chúng tôi khuyến cáo PPIs hoặc thuốc kháng acid canh tranh kali bởi vì tỷ lệ chữa lành loét của chúng cao hơn có ý nghĩa so với thuốc kháng histamin H2 [35-38]. Thuốc kháng acid canh tranh kali nhận được sự phổ biến trong những năm gần đây vì hiệu quả chữa lành loét dạ dày cao hơn khi so sánh với Lansoprazole [39]. Khi PPIs và thuốc kháng acid cạnh tranh Kali không thể kê đơn, thuốc kháng Histamin H2 được khuyến cáo. Không có báo cáo về sự khác biệt có ý nghĩa giữa các loại thuốc kháng Histamin H2. Hơn thế nữa, Pirenzepine, Sucralfate, và Misoprostol được đề xuất vì tỷ lệ chữa lành của chúng bằng với những thuốc kháng Histamin H2
5.2 Loét tá tràng
Câu hỏi lâm sàng 10 Loại thuốc đầu tay nào để khởi đầu điều trị loét tá tràng không diệt trừ HP (HP âm tính)?
- Cả PPIs hoặc thuốc kháng acid cạnh tranh Kali được khuyến cáo.
Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ A
- Nếu cả PPIs và thuốc kháng acid canh tranh kali không được kê đơn, thuốc kháng Histamin H2 được khuyến cáo
Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ B.
- Nếu cả PPIs và thuốc kháng acid canh tranh kali không thể kê đơn, Pirenzepine, Sucralfate, và Misoprostol được đề xuất.
Khuyến cáo yếu, 100% đồng ý, Mức chứng cứ B
Bình luận: chúng tôi khuyến cáo PPIs hoặc thuốc kháng acid canh tranh kali vì tỷ lệ chữa lành loét của PPIs cao hơn có ý nghĩa so với thuốc kháng histamin H2. ]. Thuốc kháng acid canh tranh kali nhận được sự phổ biến trong những năm gần đây vì hiệu quả chữa lành loét dạ dày cao hơn khi so sánh với lansoprazole [39]. Khi PPIs và thuốc kháng acid cạnh tranh kali không thể kê đơn, thuốc kháng histamin H2 được khuyến cáo.
6 Loét do thuốc
6.1 Loét do NSAID không chọn lọc
6.1.1 Điều trị
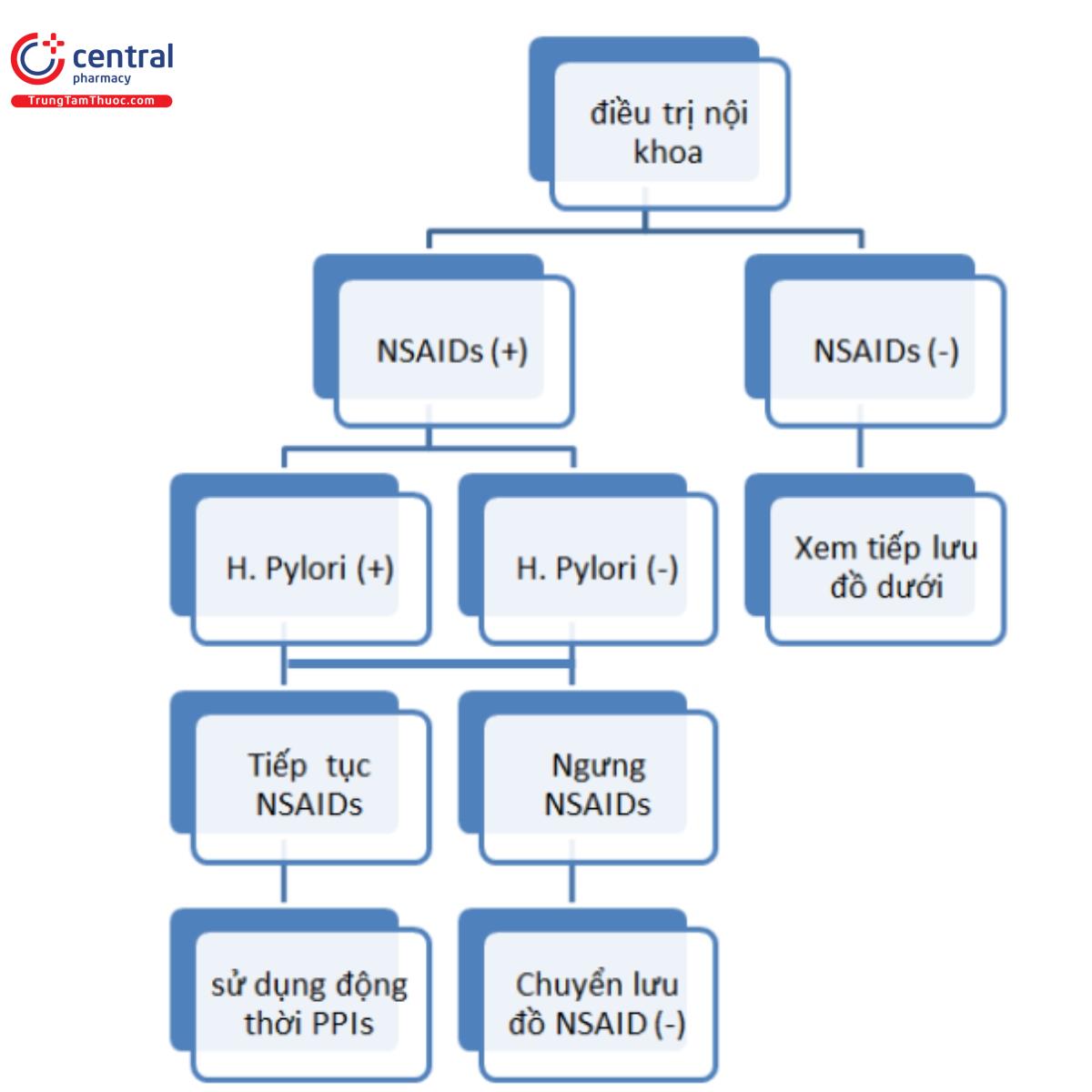
Câu hỏi lâm sàng 11: phải điều trị loét dạ dày – tá tràng do NSAID như thế nào?
- NSAIDs phải được ngưng sử dụng, và sử dụng thuốc chống loét.
Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ A
- Nếu NSAIDs không thể ngừng sử dụng, sử dụng PPIs được khuyến cáo là liệu pháp đầu tay.
Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ A
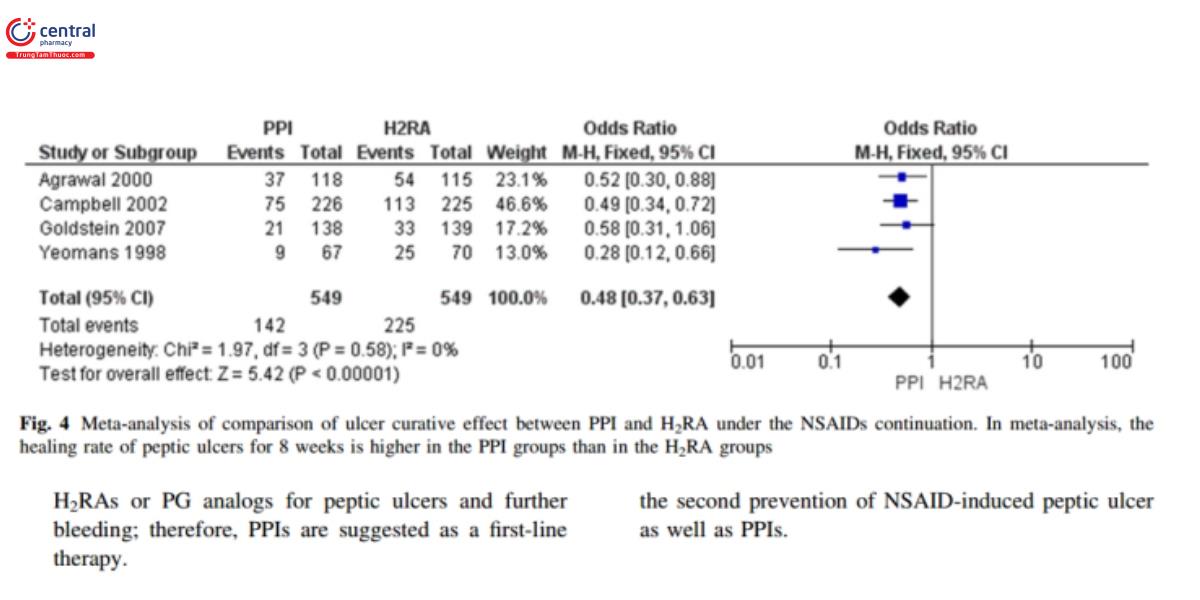
Bình luận: loét dạ dày và tá tràng do NSAID có tỷ lệ chữa lành cao khi NSAID được ngưng[41]. Các nghiên cứu so sánh PPIs với kháng Histamin H2 và PPIs với chất tương tự Prostaglandin [43], tỷ lệ chữa lành loét dạ dày và tá tràng cao hơn ở nhóm sử dụng PPI. Nghiên cứu phân tích tổng hợp nguyên bản trong hướng dẫn này chỉ ra tỷ lệ chữa lành loét sau 8 tuần ở nhóm bệnh nhân sử dụng PPI cao hơn nhóm dùng thuốc kháng Histamin H2, vì thế PPIs được khuyến cáo là lựa chọn đầu tay. (hình 4)
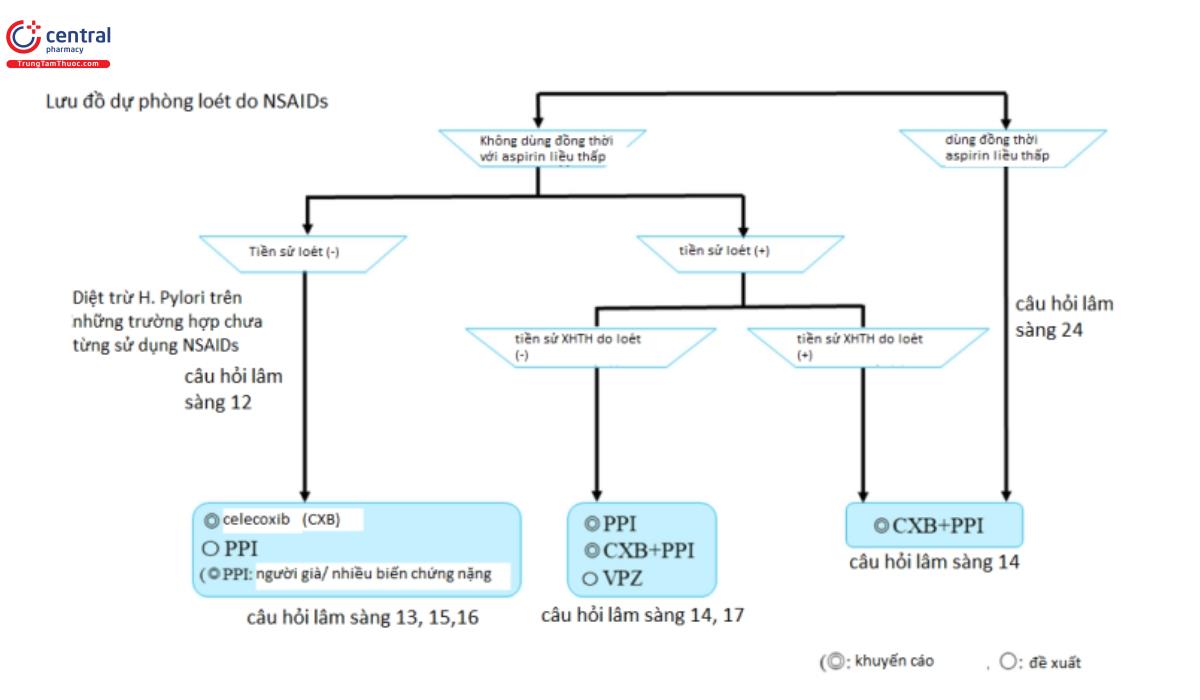
6.1.2 Phòng ngừa
Câu hỏi lâm sàng 12: nếu bệnh nhân đang uống NSAIDs có H.Pylori dương tính, có nên diệt trừ HP?
- Diệt trừ HP được khuyến cao để dự phòng loét ở bệnh nhân uống NSAIDs
Khuyến cáo mạnh, 100% đồng ý, Mức chứng cứ A
Bình luận: trong vài nghiên cứu so sánh giữa PPIs và diệt trừ HP, PPIs vượt trội hơn diệt trừ HP trong ngăn ngừa tái xuất huyết ở bệnh nhân uống NSAIDs [44].
Nhiều nghiên cứu chỉ ra rằng diệt trừ HP sẽ giảm tỷ lệ loét ở bệnh nhân uống NSAIDs; tuy nhiên, tác dụng của liệu pháp diệt HP để dự phòng loét dạ dày tá tràng không được như mong đợi trong suốt liệu pháp NSAIDs. Trong một báo cáo phân tích tổng hợp năm 2012, hiệu quả của liệu pháp diệt trừ HP để ngăn ngừa loét được quan sát, đặc biệt ở bệnh nhân chưa sử dụng NSAIDs và ở dân số châu Á [46].
Câu hỏi lâm sàng 13: Liệu pháp dự phòng loét do NSAIDS có cần thiết ở bệnh nhân không có tiền sử loét?
- Dự phòng loét dạ dày – tá tràng do NSAIDs bằng cách sử dụng PPIs là cần thiết và được đề xuất thậm chí ở bệnh nhân không có tiền sử loét.
Khuyến cáo yếu, 100% đồng thuận, Mức chứng cứ : A
(PPIs không được bảo hiểm Nhật bản chi trả cho dự phòng nguyên phát loét dạ dày – tá tràng ở bệnh nhân uống NSAIDs.
Bình luận: ở bệnh nhân sử dụng NSAIDs trên 3 tháng, hiệu quả của chất tương tự Prostaglandin, PPIs, hoặc liều cao kháng histamin h2 sử dụng để dự phòng nguyên phát đã từng được báo cáo. Scally B et al, [50] chỉ ra rằng PPIs có sự bảo vệ lớn hơn kháng Histamin h2 hoặc chất tương tự Prostaglandin trong loét dạ dày – tá tràng và xuất huyết thêm; vì thế, PPIs được đề xuất là lựa chọn đầu tay.
Câu hỏi lâm sàng 14: Dự phòng tái phát như thế nào ở bệnh nhân có tiền sử loét hoặc xuất huyết dạ dày – tá tràng mà đang sử dụng NSAIDs?
- PPIs được khuyến cáo, và VPZ được đề xuất để ngăn ngừa loét do NSAIDs ở bệnh nhân có tiền sử loét.
Khuyến cáo yếu, 100% đồng thuận, Mức chứng cứ B
- Sử dụng đồng thời NSAID chọn lọc với PPI được khuyến cáo để dự phòng tái xuất huyết ở bệnh nhân loét dạ dày – tá tràng do NSAIDs có tiền sử XHTH trên.
Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ B
Bình luận: mặc dù hiệu quả của chất tương tự prostaglandin [51] cho dự phòng thứ phát được quan sát ở nhóm bệnh nhân nguy cơ cao với tiền sử loét dạ dày – tá tràng, bệnh nhân không thế tiếp tục quan sát vì tiêu chảy xảy ra phổ biến.
Nhiều nghiên cứu nhận thấy rằng PPI vượt trội hơn giả dược ở giảm nguy cơ tái loét ở bệnh nhân có tiền sử loét đang sử dụng NSAIDs kéo dài [52, 53].
Câu hỏi lâm sàng 15: Nên dự phòng loét dạ dày tá tràng như thế nào cho bệnh nhân sử dụng liều cao NSAIDs hoặc kết hợp NSAIDs với kháng kết tập tiểu cầu hoặc Glucocorticoid hoặc Bisphosphonates, người mà đã lớn tuổi hoặc có nhiều biến chứng nặng?
- Ở bệnh nhân sử dụng kết hợp NSAIDs và Glucocorticoids hoặc thuốc kháng kết tập tiểu cầu, sử dụng thuốc ức chế COX2 được khuyến cáo để dự phòng loét dạ dày – tá tràng.
Khuyến cáo mạnh, 100% đồng ý, Mức chứng cứ B
- Ở bệnh nhân già hoặc có nhiều biến chứng nặng, sử dụng PPIs được khuyến cáo để dự phòng loét do NSAIDs.
Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ A
Bình luận: sự sử dụng đồng thời NSAIDS không chọn lọc hoặc Aspirin liều thấp, nhưng không ức chế chọn lọc cox2, với corticosteroids hoặc thuốc kháng đông, tăng nguy cơ XHTH trên, nhận thẩy rằng thuốc ức chế chọn lọc COX-2 không tăng nguy cơ XHTH trên [55]. Hiệu quả của PPI để dự phòng biến chứng đã từng được minh chứng trong nghiên cứu trước đây [56].
6.2 Loét do thuốc NSAID chọn lọc
Câu hỏi lâm sàng 16: Thuốc ức chế chọn lọc COX-X có hữu ích trong dự phòng loét do NSAID?
- Thuốc ức chế chọn lọc COX – 2 được khuyến cáo cho dự phòng loét dạ dày – tá tràng do NSAIDs.
Khuyến cáo mạnh, 100% đồng ý, Mức chứng cứ A
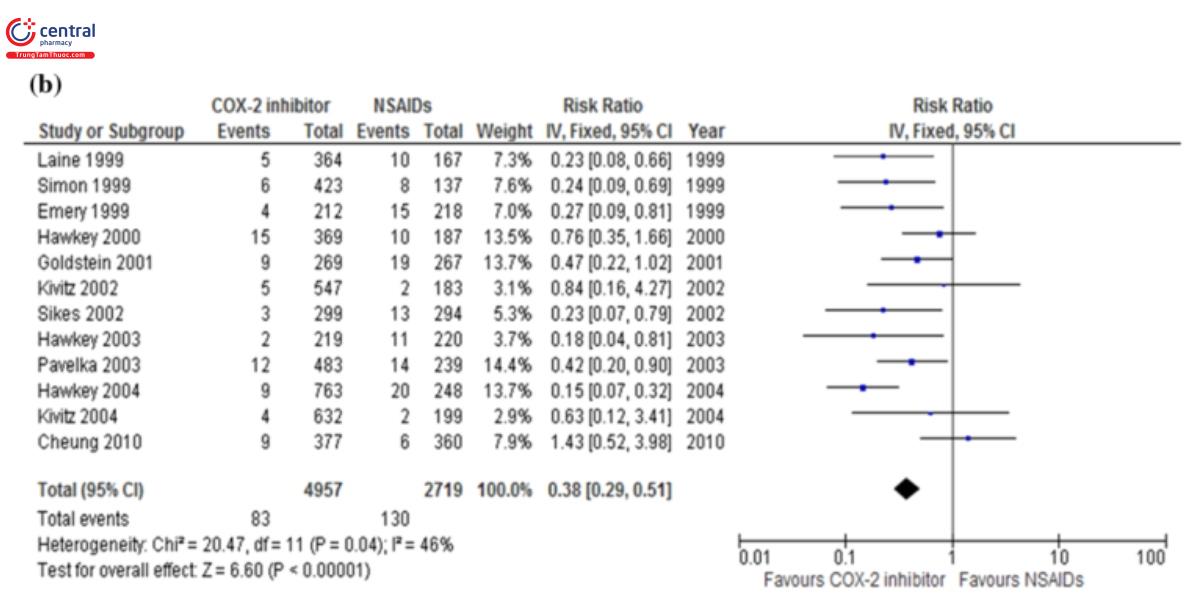
Bình luận: tỷ lệ loét dạ dày – tá tràng ở các quốc gia phía tây thấp hơn có ý nghĩa ở nhóm bệnh nhân uống ức chế cox – 2 chọn lọc hơn bệnh nhân uống NSAIDs không chọn lọc [57 – 59]. Chúng tôi đã tiến hành một phân tích tổng hợp và nhận thấy rằng tỷ lệ lưu hành của loét dạ dày (RR 0.21; CI 0.18 – 0.25, P < 0.00001) (hình 6a) và loét tá tràng (RR 0.38; 95%CI 0.29 – 0.51, P < 0.00001) (hình 6b) thấp hơn ở bệnh nhân sử dụng thuốc ức chế chọn lọc COX-2 hơn bệnh nhân sử dụng NSAIDs không chọn lọc. Sử dụng thuốc ức chế chọn lọc COX- 2 có tỷ lệ thấp hơn phát triên các biến chứng nghiêm trọng của loét.
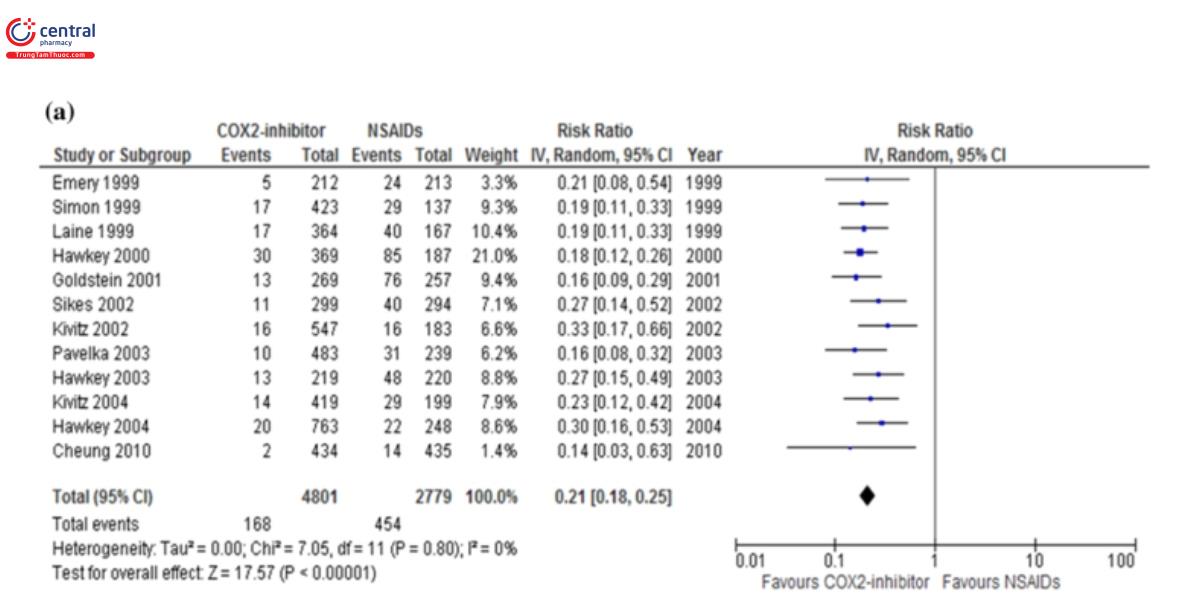
Một nghiên cứu ngẫu nhiên có đối chứng ở các đối tượng là những người tình nguyện khỏe mạnh ở Nhật bản cho chúng ta thấy tỷ lệ mắc loét dạ dày – tá tràng là 1.4%, 27.6% và 2.7% tương ứng ở nhóm sử dụng celecoxib, Loxoprofen và giả dược (P<0.0001) [60]. Chúng tôi tiến hành một phân tích tổng hợp và nhận thấy tỷ lệ mắc bệnh thấp hơn ở bệnh nhân sử dụng thuốc ức chế COX-2 hơn nhóm sử dụng NSAIDs (RR 0.13; 95%CI 0.04- 0.44, P= 0.0010), tương tự với nhóm bệnh nhân ở các nước phương tây. Kết quả trên cho thấy rằng thuốc ức chế chọn lọc COX-2 hữu ích để dự phòng loét do NSAID và các biến chứng nghiêm trọng của nó.
Câu hỏi lâm sàng 17: Có cần dự phòng loét dạ dày – tá tràng ở bệnh nhân sử dụng thuốc ức chế chọn lọc COX-2?
- Dự phòng với các thuốc chống loét được khuyến cáo cho bệnh nhân sử dụng thuốc ức chế chọn lọc COX-2 có tiền sử loét hoặc xuất huyết.
Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ B
- Không dự phòng với các thuốc chống loét được khuyến cáo cho bệnh nhân sử dụng thuốc ức chế chọn lọc COX-2 KHÔNG có tiền sử loét hoặc xuất huyết.
Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ B
Bình luận: Một nghiên cứu phân tích tổng hợp chỉ ra tỷ lệ mặc bệnh của loét do thuốc tiến triển tương tự ở bệnh nhân sử dụng thuốc ức chế chọn lọc COX-2 và giả dược, gợi ý thuốc ức chế chọn lọc COX-2 không làm tăng nguy cơ loét do thuốc [60-62].
6.3 Loét do Aspirin liều thấp
6.3.1 Điều trị
Câu hỏi lâm sàng 18: Loét dạ dày – tá tràng liên quan Aspirin liều thấp nên được điều trị như thế nào?
- Đồng thời sử dụng PPIs và tiếp tục Aspirin liều thấp được khuyến cáo cho loét do Aspirin liều thấp.
Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ A
Bình luận: Ở bệnh nhân có tiền sử xuất huyết tiêu hóa trên có liên quan đến Aspirin liều thấp, việc sử dụng đồng thời PPIs với tiếp tục Aspirin liều thấp sau khi cầm máu qua nội soi có tỷ lệ tái xuất huyết bằng nhau khi so sánh với nhóm sử dụng đồng thời giả dược và PPIs. Hơn thế nữa, tiếp tục Aspirin liều thấp giảm tỷ lệ tử vong tổng thể liên quan đến biến cố tim mạch [8]. Trong một nghiên cứu tương tư, sử dụng đồng thời PPIs và tiếp tục Aspirin liều thấp không làm tăng tỷ lệ tái xuất huyết [8]. Tỷ lệ lành tương tự giữa nhóm sử dụng đơn độc PPI và nhóm kết hợp PPI với Aspirin liều thấp.
6.3.2 Dự phòng
Câu hỏi lâm sàng 19: Loại thuốc nào nên dùng đồng thời để có hiệu quả giảm tỷ lệ mắc bệnh và tỷ lệ lưu hành của loét liên quan Aspirin liều thấp?
- PPIs hoặc thuốc kháng Histamin H2 được khuyến cáo để giảm tỷ lệ mắc bệnh và tỷ lệ lưu hành loét liên quan spirin liều thấp.
Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ A
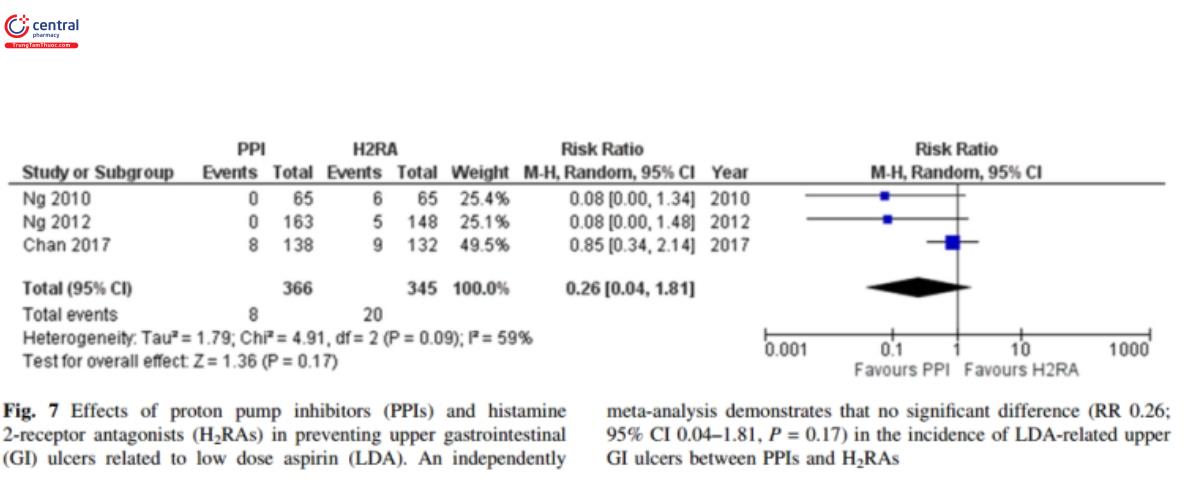
Bình luận: Nghiên cứu phân tích tổng hợp chỉ ra rằng điều trị bằng Aspirin liều thấp với đồng thời sử dụng thuốc kháng Histamin h2 hoặc PPIs làm giảm nguy cơ loét liên quan Aspirin liều thấp [65,66]. PPIs vượt trội hơn thuốc kháng histamin h2 trong dự phòng loét tiêu hóa trên có liên quan Aspirin liều thấp [67]. Tuy nhiên 1 nghiên cứu ngẫu nhiên có đối chứng thực hiện bởi Chan và cộng sự [68] chỉ ra rằng không có khác biệt có ý nghĩa giữa Rabeprazol với Famotidine trong tỷ lệ tái phát loét có liên quan Aspirin liều thấp. chúng tôi đã sử dụng dữ liệu từ 2 nghiên cứu ngẫu nhiên có đối chứng [69, 70] của Mo và cộng sự [67] và một nghiên cứu ngẫu nhiên [68] để thực hiện một nghiên cứu phân tích tổng hợp độc lập. Chúng tôi đã tìm thấy không có sự khác biệt có ý nghĩa của PPIs và thuốc ức chế Histamin h2 (hình 7) (RR 0.26; 95% CI 0.04–1.81, P = 0.17)
Câu hỏi lâm sàng 20: Loại thuốc nào nên dùng đồng thời để có hiệu quả giảm tỷ lệ mắc bệnh và tỷ lệ lưu hành của XHTH trên liên quan Aspirin liều thấp?
- PPIs và VPZ được khuyến cáo để giảm tỷ lệ mắc bệnh và tỷ lệ lưu hành của XHTH trên liên quan Aspirin liều thấp.
Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ A
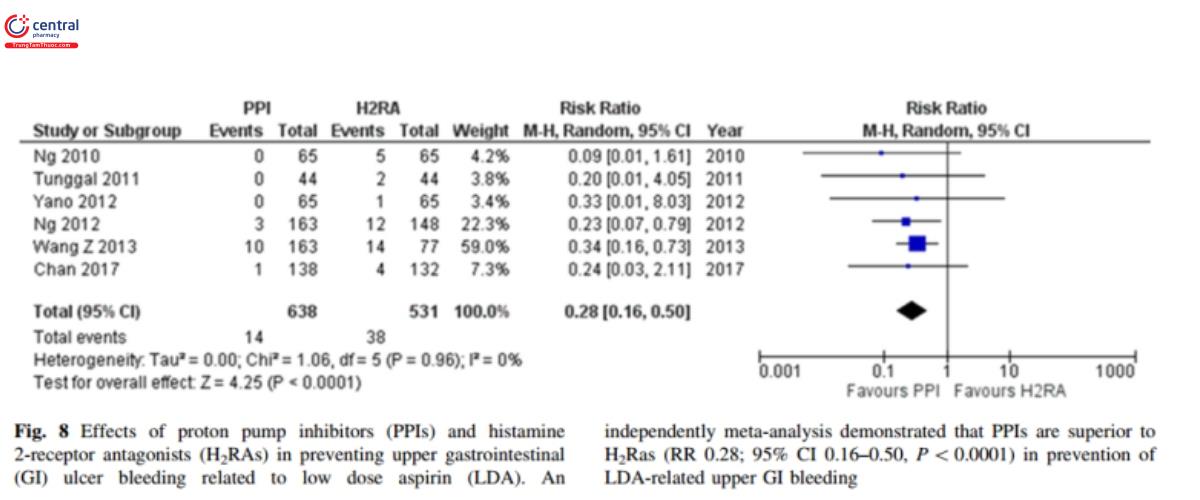
Bình luận: Nghiên cứu phân tích tổng hợp chỉ ra rằng điều trị bằng Aspirin liều thấp với đồng thời sử dụng thuốc kháng Histamin H2 hoặc PPIs làm giảm nguy cơ XHTH trên liên quan Aspirin liều thấp [65,71]. PPIs vượt trội hơn thuốc kháng histamin h2 trong dự phòng xuất huyết tiêu hóa trên có liên quan Aspirin liều thấp [66,67]. Chúng tôi đã sử dụng dữ liệu từ 3 nghiên cứu ngẫu nhiên có đối chứng [68, 70] của Mo và cộng sự [67] và 3 nghiên cứu ngẫu nhiên có đối chứng [72-74] để thực hiện một nghiên cứu phân tích tổng hợp độc lập so sánh PPIs và thuốc kháng Histamin H2. Chúng tôi đã tìm thấy PPIs vượt trội so với thuốc ức chế Histamin H2 trong dự phòng XHTH trên có liên quan Aspirin liều thấp (hình 8).
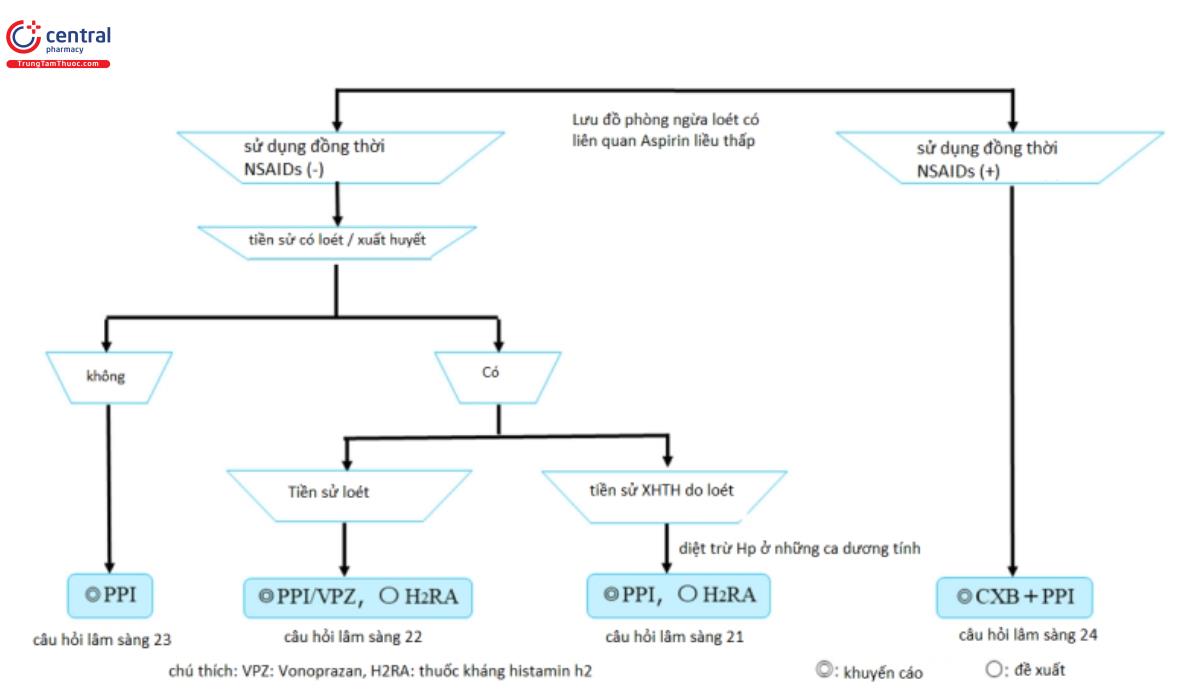
Câu hỏi lâm sàng 21: Loại thuốc nào nên dùng đồng thời để có hiệu quả giảm tỷ lệ mắc bệnh và tỷ lệ lưu hành của tái XHTH trên liên quan Aspirin liều thấp?
- PPIs thêm vào đó là diệt trừ HP được khuyến cáo để giảm tỷ lệ mắc bệnh và tỷ lệ lưu hành của tái XHTH trên liên quan Aspirin liều thấp
Khuyến cáo: mạnh, 100% đồng thuận, Mức chứng cứ B
- Thuốc ức chế Histamin H2 và diệt trừ HP được đề xuất để giảm tỷ lệ mắc bệnh và tỷ lệ lưu hành của tái XHTH trên liên quan Aspirin liều thấp
Khuyến cáo: Yếu, 100% đồng thuận, Mức chứng cứ C
Bình luận: Diệt trừ HP bằng với điều trị với Omeprazol ở bệnh nhân uống Aspirin liều thấp trong xác xuất tái xuất huyết tiêu hóa [75]. Ở bệnh nhân có biến chứng của loét liên quan đến sử dụng Aspirin liều thấp trong thời gian dài, điều trị với lansoprazol thêm vào đó là diệt trừ HP làm giảm một cách có ý nghĩa tỷ lệ tái phát XHTH do loét khi so sánh với giả dược + diệt trừ HP [76]. Ở bệnh nhân có loét dạ dày – tá tràng liên quan Aspirin liều thấp, liệu pháp Famotidine liều cao vượt trội hơn Pantoprazol trong dự phòng tái phát XHTH do loét mà vẫn tiếp tục uống Aspirin liều thấp [69]. Điều trị Aspirin liều thấp đồng thời với sử dụng Rabeprazole không khác biệt về tỷ lệ tái phát XHTH trên do loét khi so sánh với nhóm bệnh nhân sử dụng Famotidine có tiền sử XHTH do loét dạ dày – tá tràng có liên quan Aspirin liều thấp.
Câu hỏi lâm sàng 22: Loét dạ dày – tá tràng liên quan Aspirin liều thấp được dự phòng như thế nào ở bệnh nhân có liền sử loét dạ dày – tá tràng?
- PPI hoặc VPZ được khuyến cáo để giảm tỷ lệ tái phát loét dạ dày – tá tràng liên quan Aspirin liều thấp.
Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ A
- Thuốc kháng histamin H2 được đề xuất để giảm tỷ lệ tái phát loét dạ dày – tá tràng liên quan Aspirin liều thấp.
Khuyến cáo yếu, 100% đồng thuận, Mức chứng cứ C
Câu hỏi lâm sàng 23: Bệnh nhân không có tiền sử loét dạ dày – tá tràng, có cần thiết phải dự phòng loét do Aspirin liều thấp?
- PPIs được khuyến cáo cho dự phòng nguyên phát của loét dạ dày – tá tràng liên quan spirin liều thấp không có tiền sử loét.
Khuyến cáo mạnh, 82% đồng thuận, Mức chứng cứ A
Câu hỏi lâm sàng 24: Có phải thuốc ức chế chọn lọc cox-2 giảm tỷ lệ loét dạ dày – tá tràng khi so sánh với NSAIDs không chọn lọc khi bệnh nhân có sử dụng Aspirin liều thấp?
- Thuốc ức chế chọn lọc COX-2 giảm nguy cơ loét dạ dày – tá tràng và xuất huyết ở bệnh nhân sử dụng Aspirin liều thấp khi so sánh với NSAIDs không chọn lọc.
Khuyến cáo mạnh, 100% đồng thuận,Mức chứng cứ A
- Sử dụng đồng thời celecoxib với PPIs được khuyến cáo để dự phòng tổn thương dạ dày ở bệnh nhân có nguy cơ loét trung bình hoặc thấp mà cần sử dụng Aspirin liều thấp hoặc NSAIDs.
Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ A
Câu hỏi lâm sàng 25: Có khuyến cáo PPI để dự phòng tái phát loét dạ dày – tá tràng khi điều trị NSAIDs ở bệnh nhân đang uống Aspirin liều thấp?
- Celecoxib sử dụng đồng thời với PPIs được khuyến cáo để dự phòng tái phát loét sau khi điều trị NSAIDs ở bệnh nhân uống Aspirin liều thấp.
Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ A
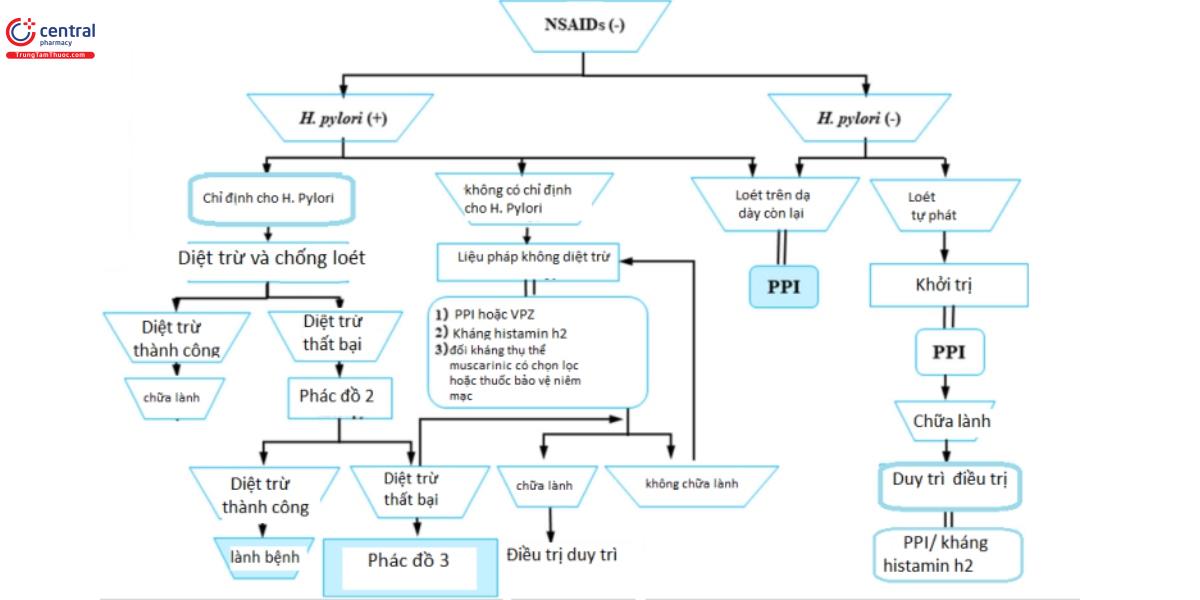
7 Loét dạ dày tá tràng không do NSAIDs, HP âm tính
Câu hỏi lâm sàng 26: Phải điều trị Loét dạ dày tá tràng không do NSAIDs, HP âm tính như thế nào?
- PPIs được đề xuất để khởi trị loét dạ dày - tá tràng tự phát không do NSAIDs và HP âm tính với PPIs hoặc kháng histamin h2 đề ngăn ngừa tái phát.
Khuyến cáo yếu, 100% đồng thuận, Mức chứng cứ C
Bình luận: Tình trạng tăng tiết acid và tăng tiết gastrin được quan sát thấy ở bệnh nhân loét tự phát [94], chúng tôi đề xuất PPIs khi khởi trị. Tuy nhiên, Kanno và cộng sự [95] báo cáo tỷ lệ chữa lành sau 12 tuần với PPIs đạt 77.4% với loét tự phát so với 95% với loét do HP. Vì thế, PPIs có thế không đủ để điều trị loét tự phát. Wong và cộng sự [96] báo cáo rằng tỷ lệ loét tái phát tích lũy trong nhóm loét tự phát trong 7 năm không điều trị dự phòng là 42.3%, cao hơn nhóm loét do HP (11.2%). Hơn nữa, trong nghiên cứu ngẫu nhiên có đối đối được thực hiện bởi họ, họ đã so sánh hiệu quả của PPI và thuốc kháng histamin h2 trong dự phòng tái phát loét vô căn và đã báo cáo rằng tỷ lệ XHTH trên tích lũy trong 24 tháng là 0.88% khi sử dụng PPI (Lansoprazol 30mg 1 viên mỗi ngày) và 2.63% khi sử dụng kháng Histamin H2 (Famotidine 40mg 1 viên mỗi ngày). Tác dụng này không khác biệt có ý nghĩa giữa 2 nhóm (P= 0.336) [97]. Vì thế, chúng tôi đề xuất cả PPIs và kháng Histamin H2 là ứng cử viên để dự phòng tái phát.
8 Loét trên bệnh nhân cắt dạ dày
Câu hỏi lâm sàng 27: Điều trị ổ loét dạ dày sau khi cắt dạ dày như thế nào?
- Điều trị PPI được khuyến cáo cho loét trên dạ dày còn lại.
Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ C
Bình luận: Điều trị hàng đầu cho loét trên dạ dày còn lại là điều trị bằng thuốc. Trong một thử nghiệm mở so sánh Omeprazol, Cimetidine, Sucralfate, Bismuth và Misoprostol cho loét trên dạ dày còn lại, Omeprazol là tốt nhất để chữa lành vết loét về tỷ lệ và thời gian [98]. Tỷ lệ lành vết loét sau 2 tuần lần lượt là 66.7; 43.3; 22.2; 22.3 và 16.7%.
9 Phẫu trị
Câu hỏi lâm sàng 28: Có cần diệt trừ HP sau khi phẫu thuật loét dạ dày - tá tràng?
- Diệt trừ HP được khuyến cáo sau thủ thuật vá lỗ thủng ở bệnh nhân loét dạ dày - tá tràng có HP dương tính.
Khuyến cáo mạnh, 100% đồng thuận, Mức chứng cứ A
Bình luận: Về điều trị hậu phẫu, các báo báo về diệt trừ HP được tìm thấy, nhưng không có cho PPI hoặc kháng histamin h2. Vài báo cáo đồng ý với khuyến cáo diệt trừ HP để dự phòng tái phát loét sau phẫu thuật bảo tồn dạ dày [103-107]. El-Nakeeb và cộng sự [107] chỉ ra diệt trừ HP sớm sau phẫu thuật vá cho thủng ổ loét tá tràng được khuyến cáo để làm tăng tốc quá trình lành vết loét 8 tuần sau phẫu thuật.
Dự phòng tái loét bằng diệt trừ HP sau cắt dạ dày chưa phù hợp giữa các báo cáo. Hơn nữa, các phân tích cần được chứng minh tác động của sự phục hồi tiết acid sau diệt trừ HP.
10 Câu hỏi cần nghiên cứu trong tương lai số 1
Điều trị loét tá tràng do thiếu máu như thế nào?
- Đề xuất PPIs hoặc misoprotol được xem là điều trị bảo tồn. Các tình trạng cơ bản như huyết khối và hẹp động mạch phải được đánh giá, xem xét. Can thiệp động mạch dưới tia x hoạc phẫu thuật có lẽ được cân nhắc nếu tình trạng bệnh nhân nặng lên sau điều trị bảo tồn.
Bình luận: Mười bốn trường hợp được báo về loét tá tràng do thiếu máu được xác định. Các triệu chứng bao gồm: đau bụng cấp, tiêu phân nên, nôn ra máu, đau bụng mạn và sụt cân. Dấu hiệu nội soi kinh điển cho vùng thiếu máu gồm vết loét theo chiều dọc, và thay đổi phù nề, sung huyết ở niêm mạc chung quanh hơn ổ loét thường. Nguyên nhân của thiếu máu cấp gồm thuyên tắc do cầm máu khi có XHTH hoặc liệu pháp tắc mạch ở bệnh nhân ung thư tế bào gan, huyết khối thuyên tắc hệ thống [108,109], và các trường hợp không rõ nguyên nhân. Triệu chứng mạn được báo cáo ở bệnh nhân có nguy cơ bệnh xơ vữa động mạch và hẹp nặng động mạch chủ hoặc động mạch mạc treo tràng trên. Nhịn ăn và ức chế tiết acid đã từng được sử dụng là phương pháp điều trị bảo tồn. Tuy nhiên, không có tác dụng giảm tiết acid trên lâm sàng ở phần hành tá tràng, nơi có sự đổ vào của dịch mật và dịch tụy, phần còn lại không rõ. Từ khía cạnh bảo vệ niêm mạc, misoprotol được đề xuất. Trong trường hợp loét do thiếu máu khởi phát cấp tính, quan sát cẩn thận được đặt ra, xem xét khả năng huyết khối toàn thân.
11 Lưu đồ điều trị
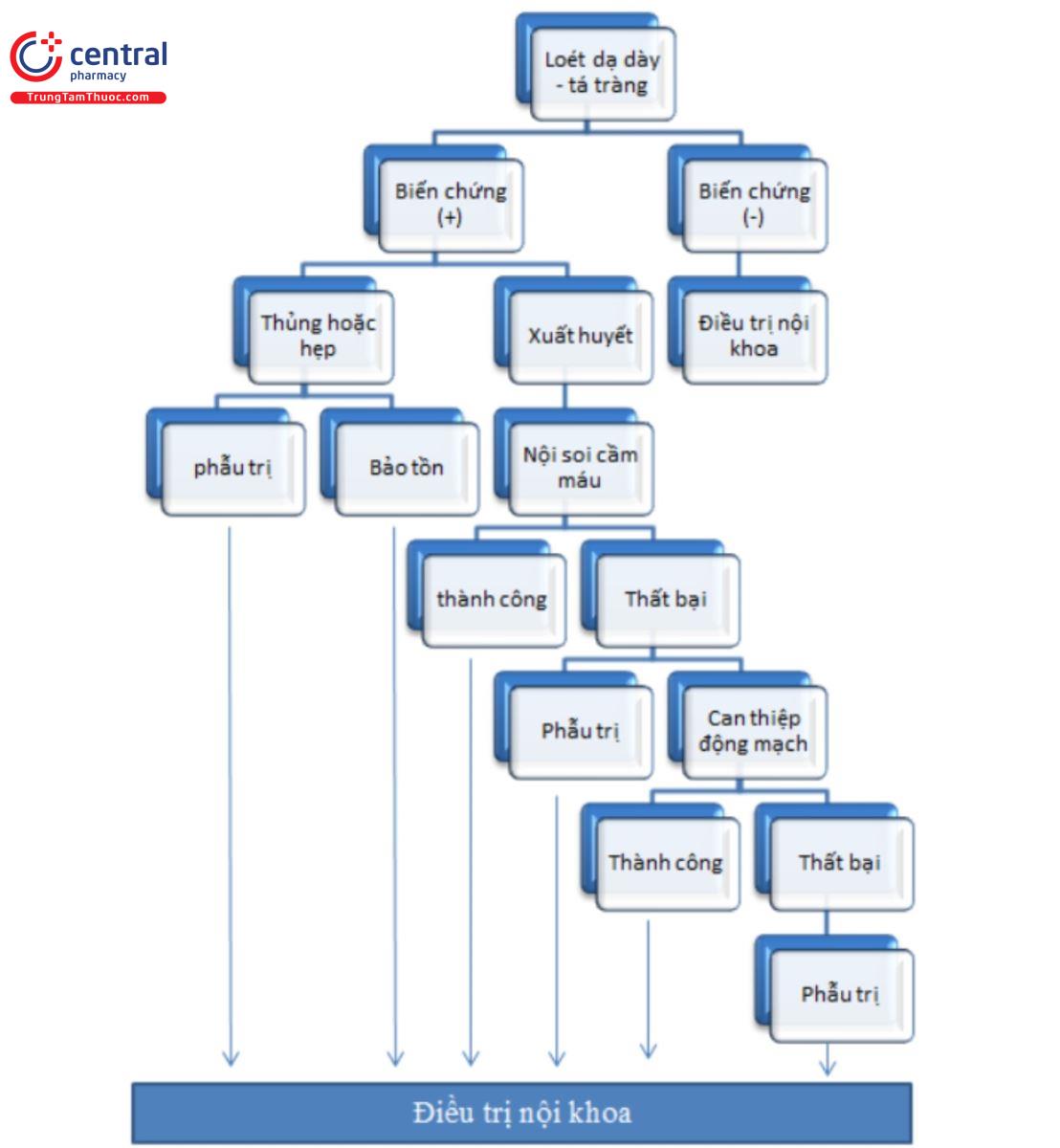
12 Nguồn tài liệu
1. Yoshida M, Kinoshita Y, Watanabe M, et al. JSGE clinical practice guideline 2014: standards, methods, and process of developing guidelines. J Gastroenterol. 2015;50:4–10.
2. Fujimoto K, Fujishiro M, Kato M, et al. Guidelines for gastroenterological endoscopy in patients undergoing antithrombotic treatment. Dig Endosc. 2014;26:1–14.
3. Kato M, Uedo N, Hokimoto S, et al. Guidelines for gastroenterological endoscopy in patients undergoing antithrombotic treatment: 2017 appendix on anticoagulants including direct oral anticoagulants. Dig Endosc. 2018;30:433–40.
4. Murakami K, Sakurai Y, Shiino M, et al. Vonoprazan, a novel potassium competitive acid blocker, as a component of first-line and second-line triple therapy for Helicobacter pylori eradication: a phase III, randomised, double-blind study. Gut. 2016;65:1439–46.
5. Miwa H, Uedo N, Watari J, et al. Randomised clinical trial: efficacy and safety of vonoprazan vs. Lansoprazole in patients with gastric or duodenal ulcers-results from two phase 3, noninferiority randomised controlled trials. Aliment Pharmacol Ther. 2017;45:240–52.
6. Mizokami Y, Oda K, Funao N, et al. Vonoprazan prevents ulcer recurrence during long-term NSAID therapy: randomised, lansoprazole-controlled non inferiority and single-blind extension study. Gut. 2018;67:1042–51.
7. Kawai T, Oda K, Funao N, et al. Vonoprazan prevents low-dose Aspirin associated ulcer recurrence: randomised phase 3 study. Gut. 2018;67:1033–41.
8. Sung JJ, Lau JY, Ching JY, et al. Continuation of low-dose Aspirin therapy in peptic ulcer bleeding: a randomized trial. Ann Intern Med. 2010;152:1–9.
9. Tarasconi A, Baiocchi GL, Pattonieri V, et al. Transcatheter arterial embolization versus surgery for refractory non-variceal upper gastrointestinal bleeding: a meta-analysis. World J Emerg Surg. 2019;14:3.
10. Kyaw M, Tse Y, Ang D, et al. Embolization versus surgery for peptic ulcer bleeding after failed endoscopic hemostasis: a metaanalysis. Endos Int Open. 2014;2:E6-14.
11. Selby NM, Kubba AK, Hawkey CJ. Acid suppression in peptic ulcer haemorrhage: a ‘meta-analysis.’ Aliment Pharmacol Ther. 2000;14:1119–26.
12. Leontiadis GI, Sharma VK, Howden CW. Systematic review and meta analysis: proton-pump inhibitor treatment for ulcer bleeding reduces transfusion requirements and hospital stay-results from the Cochrane Collaboration. Aliment Pharmacol Ther. 2005;22:169–74.
13. George S, George G, Androniki P, et al. High-dose vs. low-dose Proton pump inhibitors post endoscopic hemostasis in patients with bleeding peptic ulcer: a meta-analysis and meta-regression analysis. Turk J Gastroenterol. 2018;29:22-31.
14. Jian Z, Li H, Race NS, et al. Is the era of intravenous Proton pump inhibitors coming to an end in patients with bleeding peptic ulcers? Meta-analysis of the published literature. Br J Clin Pharmacol. 2016;82:880–9.
15. Wang J, Yang K, Ma B, et al. Intravenous Pantoprazole as an adjuvant therapy following successful endoscopic treatment for peptic ulcer bleeding. Can J Gastroenterol. 2009;23:287–99.
16. Bhatt DL, Cryer BL, Contant CF, COGENT Investigators, et al. Clopidogrel with or without omeprazole in coronary artery disease. N Engl J Med. 2010;363:1909–17.
17. Ren YH, Zhao M, Chen YD, et al. Omeprazole affects clopidogrel efficacy but not ischemic events in patients with acute coronary syndrome undergoing elective percutaneous coronary intervention. Chin Med J. 2011;124:856–61.
18. Wei P, Zhang YG, Ling L, et al. Effects of the short-term application of pantoprazole combined with Aspirin and clopidogrel in the treatment of acute STEMI. Exp Ther Med. 2016;12:2861–4.
19. Valgimigli M, Bueno H, Byrne RA, ESC Scientific Document Group; ESC Committee for Practice Guidelines (CPG); ESC National Cardiac Societies, et al. 2017 ESC focused update on dual antiplatelet therapy in coronary artery disease developed in collaboration with EACTS: The Task Force for dual antiplatelet therapy in coronary artery disease of the European Society of Cardiology (ESC) and of the European Association for CardioThoracic Surgery (EACTS). Eur Heart J. 2018;39:213–60.
20. Ray WA, Chung CP, Murray KT, et al. Association of Proton pump inhibitors with reduced risk of warfarin-related serious upper gastrointestinal bleeding. Gastroenterology. 2016;151:1105–12.
21. Kato M, Ota H, Okuda M, et al. Guidelines for the management of Helicobacter pylori infection in Japan: 2016 Revised Edition. Helicobacter. 2019;24:e12597.
22. Sugimoto M, Furuta T, Shirai N, et al. Evidence that the degree and duration of acid suppression are related to Helicobacter pylori eradication by triple therapy. Helicobacter. 2007;12:317–23.
23. Sugimoto M, Yamaoka Y. Role of vonoprazan in Helicobacter pylori eradication therapy in Japan. Front Pharmacol. 2018;9:1560.
24. Malfertheiner P, Megraud F, O’Morain CA, et al. Management of Helicobacter pylori infection-the Maastricht V/Florence Consensus Report. Gut. 2017;66:6–30.
25. Murata M, Sugimoto M, Mizuno H, et al. Clarithromycin versus Metronidazole in first-line Helicobacter pylori triple eradication therapy based on resistance to antimicrobial agents: meta-analysis. J Clin Med. 2020;9:543.
26. Mansour-Ghanaei F, Joukar F, Naghipour MR, et al. Seven-day quintuple regimen as a rescue therapy for Helicobacter pylori eradication. World J Gastroenterol. 2015;21:661–6.
27. Hsu PI, Tsai FW, Kao SS, et al. Ten-day quadruple therapy comprising Proton pump inhibitor, bismuth, Tetracycline, and levofloxacin is more effective than standard levofloxacin triple therapy in the second-line treatment of Helicobacter pylori infection: a randomized controlled trial. Am J Gastroenterol. 2017;112:1374–81.
28. Liou JM, Bair MJ, Chen CC, et al. Levofloxacin sequential therapy vs levofloxacin triple therapy in the second-line treatment of Helicobacter pylori: a randomized trial. Am J Gastroenterol. 2016;111:381–7.
29. Tsujimae M, Yamashita H, Hashimura H, et al. A comparative study of a new class of gastric acid suppressant agent named vonoparazan versus esomeprazole for the eradication of Helicobacter pylori. Digestion. 2016;94:240–6.
30. Sakurai K, Suda H, Ido Y, et al. Comparative study: Vonoprazan and Proton pump inhibitors in Helicobacter pylori eradication therapy. World J Gastroenterol. 2017;23:668–75.
31. Sue S, Kuwashima H, Iwata Y, et al. The superiority of vonoprazan-based first-line triple therapy with clarithromycin: a prospective multi-center cohort study on Helicobacter pylori eradication. Intern Med. 2017;56:1277–85.
32. Murakami K, Furuta T, Ando T, et al. Multi-center randomized controlled study to establish the standard third-line regimen for Helicobacter pylori eradication in Japan. J Gastroenterol. 2013;48:1128–35.
33. Furuta T, Sugimoto M, Kodaira C, et al. Sitafloxacin-based third-line rescue regimens for Helicobacter pylori infection in Japan. J Gastroenterol Hepatol. 2014;29:487–93.
34. Mori H, Suzuki H, Matsuzaki J, et al. Efficacy of 10-day sitafloxacin containing third-line therapies for Helicobacter pylori strains containing the gyrA mutation. Helicobacter. 2015;21:286–94.
35. Di Mario F, Battaglia G, Leandro G, et al. Short-term treatment of gastric ulcer: a meta-analytical evaluation of blind trials. Dig Dis Sci. 1996;41:1108–31.
36. Eriksson S, Langstrom G, Rikner L, et al. Omeprazole and H2- receptor antagonists in the acute treatment of duodenal ulcer, gastric ulcer and reflux oesophagitis: a meta-analysis. Eur J Gastroenterol Hepatol. 1995;7:467–75.
37. Salas M, Ward A, Caro J. Are Proton pump inhibitors the first choice for acute treatment of gastric ulcers? A meta-analysis of randomized clinical trials. BMC Gastroenterol. 2002;2:17.
38. Tunis SR, Sheinhait IA, Schmid CH, et al. Lansoprazole compared with histamine 2-receptor antagonists in healing gastric ulcers: a meta-analysis. Clin Ther. 1997;19:743–57.
39. Echizen H. The first-in-class potassium-competitive acid blocker, vonoprazan fumarate: pharmacokinetic and pharmacodynamic considerations. Clin Pharmacokinet. 2015;55:409–18 ([Epub ahead of print]).
40. Poynard T, Lemaire M, Agostini H. Meta-analysis of randomized clinical trials comparing lansoprazole with ranitidine or famotidine in the treatment of acute duodenal ulcer. Eur J Gastroenterol Hepatol. 1995;7:661–5.
41. Tildesley G, Ehsanullah RS, Wood JR. Ranitidine in the treatment of gastric and duodenal ulcers associated with non-steroidal anti-inflammatory drugs. Br J Rheumatol. 1993;32:474–8.
42. Agrawal NM, Campbell DR, Safdi MA, NSAID-Associated Gastric Ulcer Study Group, et al. Superiority of lansoprazole vs ranitidine in healing nonsteroidal anti-inflammatory drug-associated gastric ulcers: results of a double blind, randomized, multicenter study. Arch Intern Med. 2000;160:1455–61.
43. Hawkey CJ, Karrasch JA, Szczepan˜ski L, Omeprazole vs. Misoprostol for NSAID-induced Ulcer Management (OMNIUM) Group, et al. Omeprazole compared with misoprostol for ulcers associated with nonsteroidal antiinflammatory drugs. N Engl J Med. 1998;338:727–34.
44. Chan FK, To KF, Wu JC, et al. Eradication of Helicobacter pylori and risk of peptic ulcers in patients starting long-term treatment with non-steroidal anti inflammatory drugs: a randomised trial. Lancet. 2002;359:9–13.
45. Vergara M, Catalan M, Gisbert JP, et al. Meta-analysis: role of Helicobacter pylori eradication in the prevention of peptic ulcer in NSAID users. Aliment Pharmacol Ther. 2005;21:1411–8.
46. Tang CL, Ye F, Liu W, et al. Eradication of Helicobacter pylori infection reduces the incidence of peptic ulcer disease in patients using nonsteroidal anti inflammatory drugs: a meta-analysis. Helicobacter. 2012;17:286–96.
47. Koch M. Non-steroidal anti-inflammatory drug gastropathy: clinical results with misoprostol. Ital J Gastroenterol Hepatol. 1999;31(Suppl 1):S54-62.
48. Bianchi Porro G, Lazzaroni M, Petrillo M, et al. Prevention of gastroduodenal damage with omeprazole in patients receiving continuous NSAIDs treatment: a double blind placebo controlled study. Ital J Gastroenterol Hepatol. 1998;30:43-7.
49. Taha AS, Hudson N, Hawkey CJ, et al. Famotidine for the prevention of gastric and duodenal ulcers caused by nonsteroidal antiinflammatory drugs. N Engl J Med. 1996;334:1435–9.
50. Scally B, Emberson JR, Spata E, et al. Effects of gastroprotectant drugs for the prevention and treatment of peptic ulcer disease and its complications: a meta-analysis of randomised trials. Lancet Gastroenterol Hepatol. 2018;3:231–41.
51. Koch M, Deiz A, Tarquini M, et al. Prevention of non-steroidal anti inflammatory drug-induced gastrointestinal mucosal injury: risk factors for serious complications. Digest Liver Dis. 2000;32:138–51.
52. Sugano K, Kontani T, Katsuo S, et al. Lansoprazole for secondary prevention of gastric or duodenal ulcers associated with long-term non-steroidal anti inflammatory drug (NSAID) therapy: results of a prospective, multicenter, double-blind, randomized, double-dummy, active-controlled trial. J Gastroenterol. 2012;47:540–52.
53. Sugano K, Kinoshita Y, Miwa H, Esomeprazole NSAID Preventive Study Group, et al. Randomised clinical trial: esomeprazole for the prevention of nonsteroidal anti-inflammatory drug-related peptic ulcers in Japanese patients. Aliment Pharmacol Ther. 2012;36:115–25.
54. Chan FK, Wong VW, Suen BY, et al. Combination of a cyclooxygenase-2 inhibitor and a proton-pump inhibitor for prevention of recurrent ulcer bleeding in patients at very high risk: a double-blind, randomised trial. Lancet. 2007;369:1621–6.
55. Masclee GM, Valkhoff VE, Coloma PM, et al. Risk of upper gastrointestinal bleeding from different drug combinations. Gastroenterology. 2014;147:784–92.
56. Vonkeman HE, Fernandes RW, van der Palen J, et al. Protonpump inhibitors are associated with a reduced risk for bleeding and perforated gastroduodenal ulcers attributable to non-steroidal anti-inflammatory drugs: a nested case-control study. Arthritis Res Ther. 2007;9:R52.
57. Emery P, Zeidler H, Kvien TK, et al. Celecoxib versus Diclofenac in long term management of rheumatoid arthritis: randomized double-blind comparison. Lancet. 1999;354:2106–11.
58. Laine L, Harper S, Simon T, et al. A randomized trial comparing the effect of rofecoxib, a cyclooxygenase 2-specific inhibitor, with that of Ibuprofen on the gastroduodenal mucosa of patients with osteoarthritis: Rofecoxib Osteoarthritis Endoscopy Study Group. Gastroenterology. 1999;117:776–83.
59. Pavelka K, Recker DP, Verburg KM. Valdecoxib is as effective as diclofenac in the management of rheumatoid arthritis with a lower incidence of gastroduodenal ulcers: results of a 26-week trial. Rheumatology. 2003;42:1207–15.
60. Sakamoto C, Kawai T, Nakamura S, et al. Comparison of gastroduodenal ulcer incidence in healthy Japanese subjects taking celecoxib or loxoprofen evaluated by endoscopy: a placebocontrolled, double-blind 2-week study. Aliment Pharmacol Ther. 2013;37:346–54.
61. Goldstein JL, Kivitz AJ, Verburg KM, et al. A comparison of the upper gastrointestinal mucosal effects of valdecoxib, naproxen and placebo in healthy elderly subjects. Aliment Pharmacol Ther. 2003;18:125–32.
62. Feng GS, Ma JL, Wong BC, et al. Celecoxib-related gastroduodenal ulcer and cardiovascular events in a randomized trial for gastric cancer prevention. World J Gastroenterol. 2008;14:4535–9.
63. Yuan JQ, Tsoi KK, Yang M, et al. Systematic review with network meta-analysis: comparative effectiveness and safety of strategies for preventing NSAID-associated gastrointestinal toxicity. Aliment Pharmacol Ther. 2016;43:1262–75.
64. Liu CP, Chen WC, Lai KH, et al. Esomeprazole alone compared with esomeprazole plus Aspirin for the treatment of aspirin-related peptic ulcers. Am J Gastroenterol. 2012;107:1022–9.
65. Tricco AC, Alateeq A, Tashkandi M, et al. Histamine H2 receptor antagonists for decreasing gastrointestinal harms in adults using acetylsalicylic acid: systematic review and metaanalysis. Open Med. 2012;6:e109–17.
66. Mo C, Sun G, Lu ML, et al. Proton pump inhibitors in prevention of low-dose aspirin-associated upper gastrointestinal injuries. World J Gastroenterol. 2015;21:5382–92.
67. Mo C, Sun G, Wang Y, et al. PPI versus histamine H2 receptor antagonists for prevention of upper gastrointestinal injury associated with low-dose Aspirin: Systematic review and metaanalysis. PLoS ONE. 2015;10:e0131558.
68. Chan FK, Kyaw M, Tanigawa T, et al. Similar efficacy of proton-pump inhibitors vs H2-receptor antagonists in reducing risk of upper gastrointestinal bleeding or ulcers in high-risk users of low-dose Aspirin. Gastroenterology. 2017;152:105–10.
69. Ng FH, Wong SY, Lam KF, et al. Famotidine is inferior to pantoprazole in preventing recurrence of aspirin-related peptic ulcers or erosions. Gastroenterology. 2010;138:82–8.
70. Ng FH, Tunggal P, Chu WM, et al. Esomeprazole compared with famotidine in the prevention of upper gastrointestinal bleeding in patients with acute coronary syndrome or myocardial infarction. Am J Gastroenterol. 2012;107:389–96.
71. Lanas A, Wu P, Medin J, et al. Low doses of acetylsaiicyiic acid increase risk of gastrointestinal bleeding in a meta-analysis. Clin Gastroenterol Hepatol. 2011;9:762–8.
72. Yano H, Tsukahara K, Morita S, et al. Influence of omeprazole and famotidine on the antiplatelet effects of clopidogrel in addition to Aspirin in patients with acute coronary syndromes: a prospective, randomized, multicenter study. Circ J. 2012;76:2673–80.
73. Wang Z, Yang X, Cai J, et al. Influence of different Proton pump inhibitors on platelet function in acute myocardial infarction patients receiving clopidogrel treatment after percutaneous coronary intervention. Biomed Res. 2013;24:453–7.
74. Tunggal P, Ng FH, Lam KF, et al. Effect of esomeprazole versus famotidine on platelet inhibition by clopidogrel: a double-blind, randomized trial. Am Heart J. 2011;162:870–4.
75. Chan FK, Chung SC, Suen BY, et al. Preventing recurrent upper gastrointestinal bleeding in patients with Helicobacter pylori infection who are taking low-dose Aspirin or naproxen. N Engl J Med. 2001;344:967–73.
76. Lai KC, Lam SK, Chu KM, et al. Lansoprazole for the prevention of recurrence of ulcer complications from long-term low-dose Aspirin use. N Engl J Med. 2002;346:2033–8.
77. Sugano K, Matsumoto Y, Itabashi T, et al. Lansoprazole for secondary prevention of gastric or duodenal ulcers associated with long-term low-dose Aspirin therapy: results of a prospective, multicenter, double-blind, randomized, double-dummy, active-controlled trial. J Gastroenterol. 2011;46:724–5.
78. Sanuki T, Fujita T, Kutsumi H, Case Study Group, et al. Rabeprazole reduces the recurrence risk of peptic ulcers associated with low-dose Aspirin in patients with cardiovascular or cerebrovascular disease: a prospective randomized active-controlled trial. J Gastroenterol. 2012;47:1186–97.
79. Iwakiri R, Higuchi K, Kato M, et al. Randomised clinical trial: prevention of recurrence of peptic ulcers by rabeprazole in patients taking low-dose Aspirin. Aliment Pharmacol Ther. 2014;40:780–95.
80. Sugano K, Choi MG, Lin JT, on behalf of the LAVENDER Study Group, et al. Multinational, double-blind, randomised, placebo-controlled, prospective study of esomeprazole in the prevention of recurrent peptic ulcer in low-dose acetylsalicylic acid users: the LAVENDER study. Gut. 2014;63:1061–8.
81. Taha AS, McCloskey C, Prasad R, et al. Famotidine for the prevention of peptic ulcers and oesophagitis in patients taking low-dose Aspirin (FAMOUS): a phase III, randomised, doubleblind, placebo-controlled trial. Lancet. 2009;374:119–25.
82. Takeuchi T, Ota K, Harada S, et al. Comparison of teprenone and famotidine against gastroduodenal mucosal damage in patients taking low-dose Aspirin. J Gastroenterol Hepatol. 2014;29(Suppl. 4):11–5.
83. Scheiman JM, Devereaux PJ, Herlitz J, et al. Prevention of peptic ulcers with esomeprazole in patients at risk of ulcer development treated with low-dose acetylsalicylic acid: a randomised, controlled trial (OBERON). Heart. 2011;97:797–802.
84. Laine L, Maller ES, Yu C, et al. Ulcer formation with low-dose enteric coated Aspirin and the effect of COX-2 selective inhibition: a double-blind trial. Gastroenterology. 2004;127:395–402.
85. Strand V. Are COX-2 inhibitors preferable to non-selective nonsteroidal anti-inflammatory drugs in patients with risk of cardiovascular events taking low-dose Aspirin. Lancet. 2007;370:2138–51.
86. Goldstein J, Lowry SC, Lanza FL, et al. The impact of low-dose Aspirin on endoscopic gastric and duodenal ulcer rates in users of a non-selective non-steroidal anti-inflammatory drug or a cyclo-oxygenase-2-selective inhibitor. Aliment Pharmacol Ther. 2006;23:1489–98.
87. Goldstein JL, Cryer B, Amer F, et al. Celecoxib plus Aspirin versus naproxen and lansoprazole plus Aspirin: a randomized, double-blind, endoscopic trial. Clin Gastroenterol Hepatol. 2007;5:1167–74.
88. Chan FKL, Ching JYL, Tse YK, et al. Gastrointestinal safety of celecoxib versus naproxen in patients with cardiothrombotic diseases and arthritis after upper gastrointestinal bleeding (CONCERN): an industry-independent, double-blind, doubledummy, randomised trial. Lancet. 2017;389:2375–82.
89. Nissen SE, Yeomans ND, Solomon DH, et al. Cardiovascular safety of celecoxib, naproxen, or ibuprofen for arthritis. N Engl J Med. 2016;375:2519–29.
90. Mcgettigan P, Henry D. Cardiovascular risk and inhibition of cyclooxygenase: a systematic review of the observational studies of selective and nonselective inhibitors of cyclooxygenase 2. JAMA. 2006;296:1633–44
91. Lanza FL, Chan FKL, Quigley EMM. Guidelines for prevention of NSAID-related ulcer complications. Am J Gastroenterol. 2009;104:728–38.
92. Goldstein JL, Huang B, Amer F, et al. Ulcer recurrence in highrisk patients receiving nonsteroidal anti-inflammatory drugs plus low-dose Aspirin: results of a post Hoc subanalysis. Clin Ther. 2004;26:1637–43.
93. Goldstein JL, Hochberg MC, Fort JG, et al. Clinical trial: the incidence of NSAID-associated endoscopic gastric ulcers in patients treated with PN 400 (naproxen plus esomeprazole magnesium) vs. enteric-coated naproxen alone. Aliment Pharmacol Ther. 2010;32:401–13.
94. Mcoll KEL, LE- Nujumi AM, Chittajallu RS, et al. A study of the pathogenesis of Helicobacter pylori negative chronic duodenal ulceration. Gut. 1993;34:762–8.
95. Kanno T, Iijima K, Abe Y, et al. Helicobacter pylori-negative and non-steroidal anti-inflammatory drugs-negative idiopathic peptic ulcers show refractoriness and high recurrence incidence: multicenter follow-up study of peptic ulcers in Japan. Dig Endosc. 2016;28:556–63.
96. Wong GL, Wong VW, Chan Y, et al. High incidence of mortality and recurrent bleeding in patients with Helicobacter pylori-negative idiopathic bleeding ulcers. Gastroenterology. 2009;137:525–31.
97. Wong GLH, Lau LHS, Ching JYL, et al. Prevention of recurrent idiopathic gastroduodenal ulcer bleeding: a double-blind, randomised trial. Gut. 2020;69:652–7.
98. Janke A, Stasiewicz J, Namiot Z, et al. Treatment of gastric stump ulcer: an open study with five drugs. Hepatogastroenterology. 2000;47:1195–8.
99. Leivonene MK, Haglund CH, Nordling SFA. Helicobacter pylori infection after partial gastrectomy for peptic ulcer and its role in relapsing disease. Eur J Gastroenterol Hepatol. 1997;9:371–4.
100. Lee YT, Sung JJ, Choi CL, et al. Ulcer recurrence after gastric surgery: is Helicobacter pylori the culprit? Am J Gastroenterol. 1998;93:928–31.
101. Huang WH, Wang HH, Wu WW, et al. Helicobacter pylori infection in patients with ulcer recurrence after partial gastrectomy. Hepatogastroenterology. 2004;51:1551–3.
102. Schilling D, Adamek HE, Wilke J, et al. Prevalence and clinical importance of Helicobacter pylori infection in patients after partial gastric resection for peptic ulcer disease. Z Gastroenterol. 1999;37:127–32.
103. Rodrı ´guez-Sanjua´n JC, Ferna´ndez-Santiago R, Garcı ´a RA, et al. Perforated peptic ulcer treated by simple closure and Helicobacter pylori eradication. World J Surg. 2005;29:849–52.
104. Ng EK, Lam YH, Sung JJ, et al. Eradication of Helicobacter pylori prevents recurrence of ulcer after simple closure of duodenal ulcer perforation: randomized controlled trial. Ann Surg. 2000;231:153–8.
105. Kate V, Ananthakrishnan N, Badrinath S. Effect of Helicobacter pylori eradication on the ulcer recurrence rate after simple closure of perforated duodenal ulcer: retrospective and prospective randomized controlled studies. Br J Surg. 2001;88:1054–8.
106. Tomtitchong P, Siribumrungwong B, Vilaichone RK, et al. Systematic review and meta-analysis: Helicobacter pylori eradication therapy after simple closure of perforated duodenal ulcer. Helicobacter. 2012;17:148–52.
107. El-Nakeeb A, Fikry A, Abd El-Hamed TM, et al. Effect of Helicobacter pylori eradication on ulcer recurrence after simple closure of perforated duodenal ulcer. Int J Surg. 2009;7:126–9.
108. Force T, MacDonald D, Eade OE, et al. Ischemic gastritis and duodenitis. Dig Dis Sci. 1980;25:307–10.
109. Julka RN, Aduli F, Lamps LW, et al. Ischemic duodenal ulcer, an unusual presentation of sickle cell disease. J Natl Med Assoc. 2008;100:339–41.

