Hướng dẫn KDIGO 2026 về quản lý thiếu máu trong bệnh thận mạn (CKD)

Bài gốc KDIGO 2026 Clinical Practice Guideline for the Management of Anemia in Chronic Kidney Disease (CKD)
Sau 14 năm kể từ hướng dẫn 2012, KDIGO đã chính thức công bố bản cập nhật 2026 với những thay đổi mang tính bước ngoặt trong chẩn đoán và điều trị thiếu máu trên bệnh nhân CKD. Trong bài viết dưới đây chúng tôi sẽ tóm tắt những điểm mới nhất và những thay đổi quan trọng nhất trong thực hành lâm sàng.
1 Định nghĩa về thiếu máu và gánh nặng
Thiếu máu là một biến chứng phổ biến ở những người mắc bệnh thận mạn tính (CKD) và có liên quan đến các kết quả lâm sàng bất lợi.
Theo WHO, chẩn đoán thiếu máu khi Hb <13g/dl [130g/l] ở nam; Hb <12g/dl [120g/l] ở nữ.
Tình trạng thiếu máu rất phổ biến và tăng dần theo giai đoạn của bệnh thận mạn (CKD). Hậu quả liên quan đến thiếu máu trong CKD:
- Tỷ lệ tử vong cao hơn
- Tăng nguy cơ suy thận/ tiến triển bệnh thận mạn tính
- Tăng nguy cơ bệnh tim mạch vành biến cố tim mạch nghiêm trọng
- Phì đại thất trái nhiều hơn
- Tăng nguy cơ suy tim
- Chất lượng cuộc sống thấp hơn
- Giảm khối lượng và sức mạnh cơ ở người nhận thận được đo bằng lượng creatinin bài tiết qua nước tiểu trong 24 giờ thấp hơn, khối lượng cơ xương đo bằng BIA, sức mạnh cầm nắm và điểm số bài kiểm tra FTSTS kém hơn
- Năng suất lao động thấp hơn
- Suy giảm nhận thức nhiều hơn
- Tăng nguy cơ sa sút trí tuệ
- Nhu cầu truyền máu cao hơn
- Nhập viện nhiều hơn (do mọi nguyên nhân, tim mạch và xuất huyết)
- Chi phí y tế cao hơn
2 Sinh lý bệnh
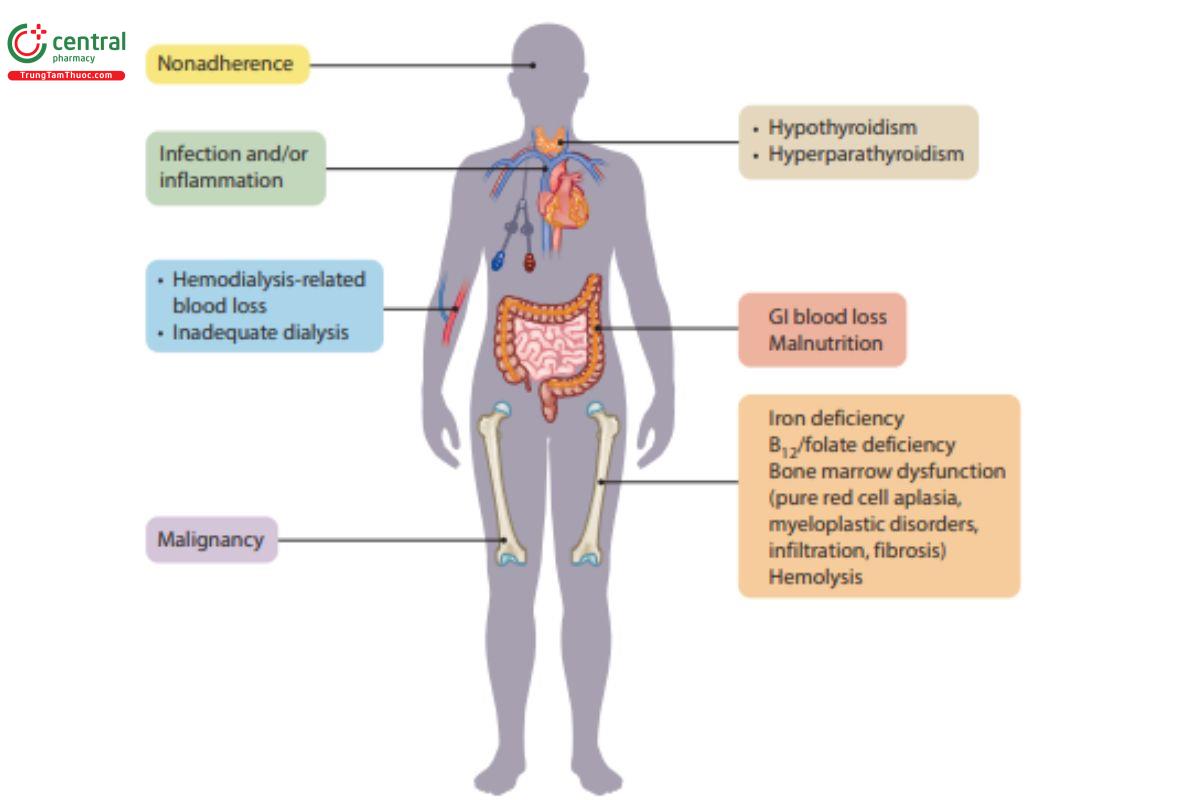
2.1 Nguyên nhân
Giảm sản xuất và cản trở quá trình tạo máu
- Thiếu hụt EPO tương đối
- Viêm hệ thống làm ức chế tạo máu
- Tủy xương đề kháng EPO
Thiếu hụt nguyên liệu
- Thiếu sắt
- Thiếu hụt dinh dưỡng khác (folate, Vitamin B12)
Tăng phá hủy
- Mất máu mạn (như mất máu Đường tiêu hóa, lọc máu)
- Thời gian sống của hồng cầu ngắn
2.2 Vai trò của Hepcidin
- Trong viêm mạn tính là tăng Hepcidin.
- Khi Hepcidin làm ức chế việc hấp thu sắt, đồng thời khóa chặt Sắt ở trong kho dự trữ.
- Hậu quả dẫn đến thiếu nguyên liệu để sản sinh hồng cầu mặc dù sắt ở trong kho dự trữ đầy.

3 Chẩn đoán thiếu sắt ở CKD
3.1 Thiếu sắt hệ thống
TSAT < 20% và:
- Ferritin < 100 ng/ml (Chưa lọc máu/PD)
- Ferritin < 200 ng/ml (Lọc máu G5HD)
3.2 Sinh hồng cầu hạn chế do sắt
TSAT < 20% và Ferritin > 100-200 ng/ml
4 Điều trị thiếu sắt ở bệnh nhân bệnh thận mạn
Thử nghiệm PIVOTAL so sánh giữa bù sắt đường tĩnh mạch liều cao so với liều thấp ở CKDG% cho thấy việc dùng sắt liều cao có thể cải thiện các biến cố tim mạch và làm giảm tỷ lệ tử vong. Điều này là cơ sở cho việc chẩn đoán và điều trị thiếu sắt cho bệnh nhân CKD.
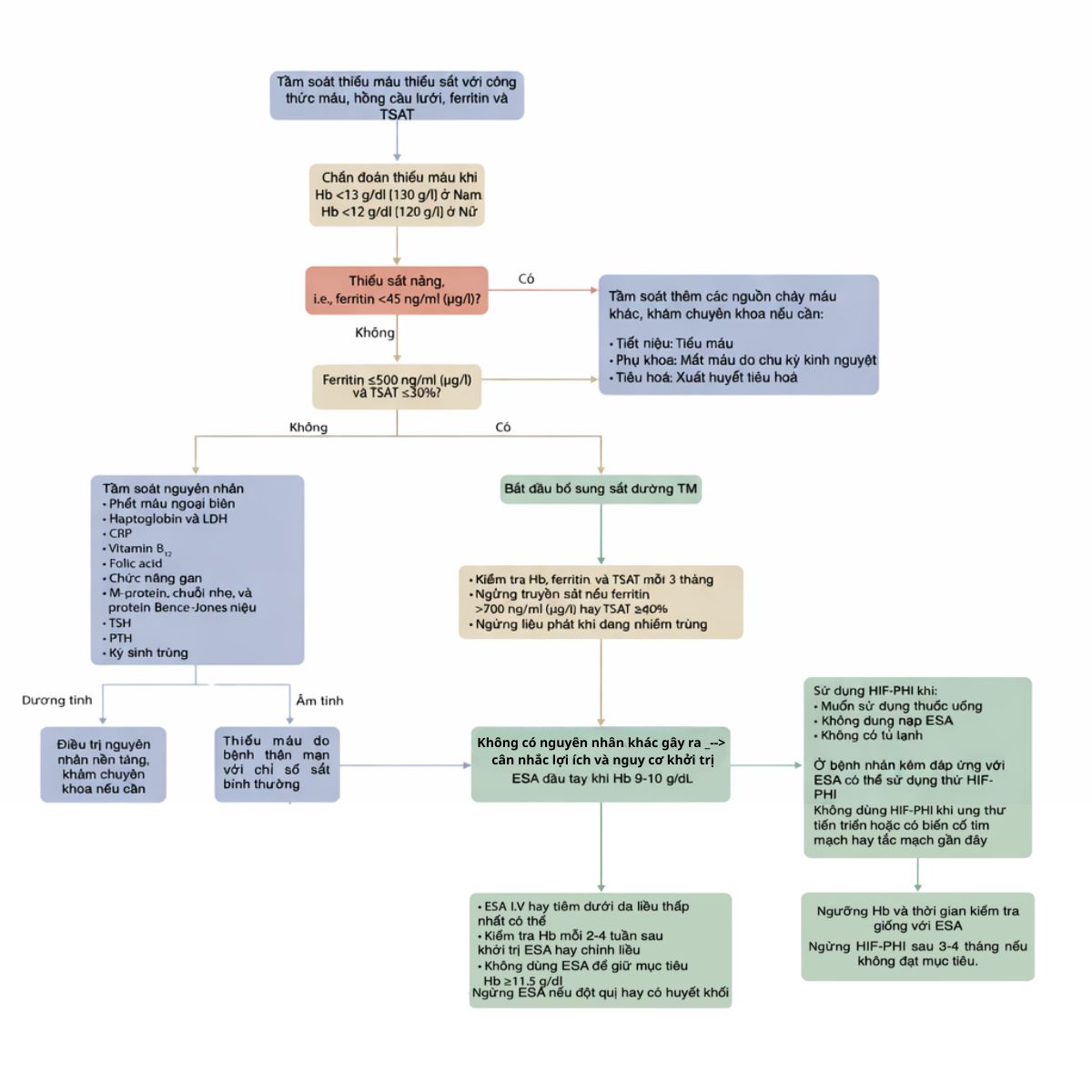
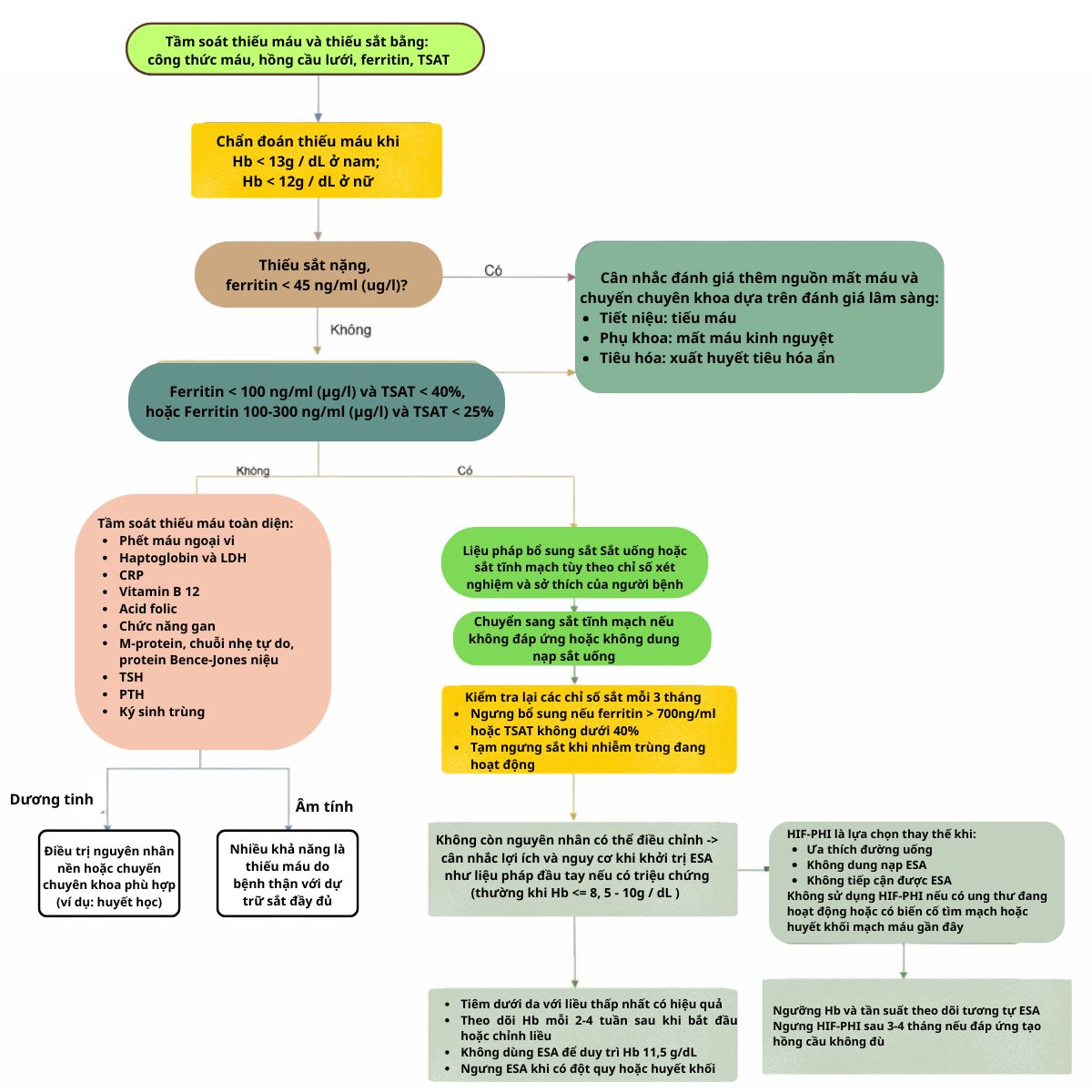
Tầm soát ban đầu
Cần tầm soát thiếu máu và thiếu sắt ở bệnh nhân bệnh thận mạn khi có triệu chứng thiếu máu và theo dõi định kỳ.
Theo dõi định kỳ cho:
- CKD G3: 1 lần/năm
- CKD G3: 2 lần/năm
- CKD G5 đang hay chưa lọc máu: mỗi 3 tháng
Bộ xét nghiệm tầm soát ban đầu bao gồm: Công thức máu, hồng cầu lưới, Ferritin và TSAT.
Nếu bộ xét nghiệm ban đầu không tìm ra nguyên nhân cần phải làm bộ xét nghiệm chuyên sâu.
4.1 Sử dụng sắt điều trị thiếu sắt, thiếu máu ở bệnh nhân bệnh thận mạn
4.1.1 Ngưỡng khởi trị và mục tiêu điều trị sắt
- Duy trì dự trữ sắt đầy đủ để hỗ trợ quá trình sinh hồng cầu.
- Tăng lượng Hemoglobin, giảm nhu cầu sử dụng thuốc kích thích tạo hồng cầu và truyền máu.
- Hạn chế nguy cơ thừa sắt (tránh nhiễm trùng và căng thẳng oxy hóa).
Bệnh thận mạn giai đoạn 5 có lọc máu chu kỳ (Dựa trên thử nghiệm lâm sàng PIVOTAL: chiến lược bổ sung sắt đường tĩnh mạch chủ động)
- Bắt đầu điều trị khi: Ferritin ≤ 500 ng/mL VÀ Độ bão hòa Transferrin ≤ 30%
- Ngừng điều trị khi: Ferritin > 700 mL HOẶC Độ bão hòa Transferrin ≥ 40%
Bệnh thận mạn không lọc máu
Bắt đầu điều trị khi:
- Ferritin < 100 ng/mL và Độ bão hòa Transferrin < 40%
- hoặc Ferritin từ 100 – 300 ng/mL và Độ bão hòa Transferrin < 25%
Ngừng điều trị khi: Ferritin > 700 ng/mL hoặc Độ bão hòa Transferrin ≥ 40%
4.1.2 Cá Thể Hóa Đường Dùng, Chế Phẩm Sắt Và Chiến Lược Điều Trị
Bệnh thận mạn giai đoạn 5 có lọc máu chu kỳ
- Ưu tiên sắt đường tĩnh mạch: Hiệu quả cao hơn so với đường uống (đã được chứng minh qua thử nghiệm lâm sàng PIVOTAL) và tiện lợi khi kết hợp tại trung tâm lọc máu.
- Theo dõi: Kiểm tra Hemoglobin, Ferritin và Độ bão hòa Transferrin mỗi 1 đến 3 tháng.
Bệnh thận mạn không lọc máu
- Linh hoạt đường uống hoặc tĩnh mạch: Cá thể hóa dựa trên mức độ thiếu máu và thiếu sắt, khả năng dung nạp, chi phí và điều kiện tiếp cận.
- Chiến lược chuyển đổi: Đổi sang đường không có đáp ứng tĩnh mạch nếu dùng đường uống từ 1 đến 3 tháng không có đáp ứng
- Theo dõi: Kiểm tra các chỉ số định kỳ ít nhất mỗi 3 tháng.
Lưu ý khi lựa chọn chế phẩm sắt
- Tiêu chí lựa chọn: Phụ thuộc vào chi phí, mức độ sẵn có, khả năng dung nạp và phác đồ liều lượng của người bệnh.
- Cảnh báo an toàn: Một số chế phẩm sắt đường tĩnh mạch (như ferric carboxymaltose) có thể gây hạ phosphat trong máu, do đó cần phải theo dõi sát chỉ số phosphat máu.
4.1.3 Cải Thiện Tính An Toàn Của Liệu Pháp Điều Trị Bằng Sắt
Nguy cơ nhiễm trùng
- Dù sắt có thể thúc đẩy vi khuẩn phát triển, hiện chưa có thử nghiệm RCT nào chứng minh rõ ràng nguy cơ này. nhịp
- Khuyến cáo: Cần tạm ngừng sử dụng liệu pháp sắt khi ngu thân. bệnh đang có tình trạng nhiễm trùng toàn thân.
Phản ứng quá mẫn với sắt đường tĩnh mạch
- Tác dụng phụ này hiếm gặp nhưng có thể tiến triển nặng và không yêu cầu phải thử liều trước khi tiêm truyền.
- Bắt buộc thực hiện truyền sắt tại các cơ sở y tế có đủ khả năng và trang thiết bị cấp cứu sốc phản vệ.
- Hướng xử trí phản ứng nhẹ: Tạm ngừng truyền, sau đó giảm tốc độ truyền, có thể cân nhắc dùng thêm thuốc kháng histamin hoặc corticosteroid.
- Hướng xử trí phản ứng phản vệ nặng: Bắt buộc ngừng sử dụng chế phẩm này vĩnh viễn.
Tình trạng quá tải sắt
- Chỉ định ngừng điều trị ngay khi nồng độ Ferritin > 700 ng/mL hoặc Độ bão hòa Transferrin ≥ 40%.
- Cần tiếp tục theo dõi và thu thập thêm bằng chứng về các độc tính của việc dư thừa sắt trong dài hạn.
4.1.4 Khuyến Cáo Dành Cho Nghiên Cứu Trong Tương Lai
Cần thêm các nghiên cứu để đánh giá:
- Ngưỡng mục tiêu và Liều lượng: Phác đồ sắt cho người bệnh thận mạn (có hoặc không lọc máu chu kỳ) với mục tiêu Ferritin và Độ bão hòa Transferrin ở mức trung gian hoặc cao hơn thử nghiệm lâm sàng PIVOTAL.
- Đối tượng đặc thù: Phác đồ tối ưu cho người bệnh thận mạn dùng thuốc ức chế men prolyl hydroxylase, người thiếu sắt nhưng không thiếu máu, và phụ nữ có thai.
- Chế phẩm và Cách dùng: So sánh sắt đường uống thế hệ mới với các loại đường uống truyền thống và mạch; đối chiếu hiệu quả uống sắt cách ngày so với uống mỗi ngày.
- Quá tải sắt: Tỷ lệ quá tải sắt, các dấu ấn sinh học và kỹ thuật hình ảnh mới, cùng các ngưỡng nồng độ liên quan đến độc tính.
4.2 Sử dụng thuốc kích thích tạo hồng cầu (ESAs), thuốc ức chế enzym Prolyl hydroxylase của yếu tố cảm ứng thiếu oxy (HIF-PHIs) và các thuốc khác trong điều trị thiếu máu ở người bệnh thận mạn
Ở những người bị thiếu máu và bệnh thận mạn tính, cần giải quyết tất cả các nguyên nhân gây thiếu máu có thể điều trị được, bao gồm cả thiếu sắt, trước khi bắt đầu điều trị bằng ESA hoặc HIF-PHI.
Cá Thể Hóa Ngưỡng Hemoglobin Để Khởi Trị Bằng ESAs
Nguyên tắc chung
- Thuốc kích thích tạo hồng cầu giúp cải thiện triệu chứng và giảm nguy cơ cần truyền hồng cầu.
- Thuốc không làm giảm nguy cơ mắc các biến mạch bất lợi.
- Đặt mục tiêu Hb quá cao có thể làm tăng nguy cơ đột quỵ và tắc đường vào mạch máu.
Bệnh thận mạn giai đoạn 5 có lọc máu định kỳ
- Có thể cân nhắc khởi trị khi nồng độ hemoglobin ≤ 9-10g/dL.
- Cá thể hóa dựa trên: nguy cơ biến cố tim mạch, tiền sử đột quỵ, tình trạng tắc đường vào mạch máu, và nguyện vọng tránh truyền máu của người bệnh.
Bệnh thận mạn không lọc máu
- Ngưỡng khởi trị cho hầu hết người bệnh thường là 8,5-10 g/dl.
- Cá thể hóa dựa trên: triệu chứng thiếu máu, nguy cơ tim mạch, bệnh lý thuyên tắc huyết khối, và tình trạng ung thư đang hoạt động.
4.2.1 Cá Thể Hóa Mục Tiêu Hemoglobin ở Người Đang Dùng ESAs
Ở người lớn
- Mục tiêu thường dao động 10-11,5 g/dl.
- Khuyến cáo duy trì nồng độ Hb không quá 11,5 g/dl
- Cần tránh mục tiêu cao hơn do làm tăng nguy cơ THA và các biến cố mạch máu
Ở trẻ em
- Mục tiêu Hb cần được cá thể hóa cho cho từng trường hợp.
- Các yếu tố cần cân nhắc bao gồm: sự phát triển thể chất và tâm lý, nguy cơ biến cố tim mạch thấp hơn so với người lớn, và tầm quan trọng của việc tránh mẫn cảm miễn dịch để tạo thuận lợi cho việc ghép thận.
Đường dùng
- Đối với người bệnh lọc máu định kỳ: đường tiêm tĩnh mạch hoặc TDD.
- Đối với người bệnh thận mạn chưa lọc máu: Ưu tiên sử dụng đường TDD.
4.2.2 Cải Thiện Tính An Toàn Của Điều Trị Bằng ESAs
Nguyên tắc an toàn và điều chỉnh liều
- Cần tăng nồng độ Hb một cách từ từ, điều chỉnh liều để tránh mức tăng quá 1 g/dl/2 tuần.
- Nếu mức tăng quá nhanh, cần giảm liều thuốc từ 25% đến 50%.
- Khi hemoglobin vượt quá 11,5 g/dl, ưu tiên giảm đột ngột. thuốc thay vì tạm ngưng sử dụng
Cân nhắc tạm ngưng thuốc khi nhập viện
- Đột quỵ cấp tính.
- Huyết khối đường vào mạch máu hoặc các biến cố thuyên tắc huyết khối khác.
- Ở người bệnh có ung thư đang hoạt động, việc dùng thuốc có thể làm tăng nguy cơ tiến triển ung thư và tử vong; cần cân nhắc kỹ lưỡng dựa trên sở thích và mục tiêu điều trị.
Kháng thuốc ESAS
- Định nghĩa: Không đạt được mục tiêu Hb dù đã tăng liều thuốc đáng kể, hoặc tiếp tục cần liều rất cao để duy trì mục tiêu.
- Xử trí: Cần tìm và điều trị các nguyên nhân tiềm ẩn như thiếu sắt, tình trạng viêm mạn tính, lọc máu không đạt hiệu quả tối ưu, và mất máu ẩn.
4.2.3 Vai Trò Của Thuốc HIF-PHIS
Cơ chế tác dụng
- Đây là các thuốc dùng đường uống.
- Kích thích cơ thể sản xuất Erythropoietin nội sinh thông qua ổn định các yếu tố phiên mã.
So sánh với thuốc kích thích tạo hồng cầu
- Hiệu quả đạt được nồng độ Hb tương đương nhau.
- Còn thiếu dữ liệu dài hạn về tính an toàn khi sử dụng
- Một số nghiên cứu gợi ý nhóm thuốc này có thể có nguy cơ gây ra biến cố tim mạch và mạch máu cao hơn ở bệnh nhân chưa lọc máu.
Khi nào nên cân nhắc sử dụng
- Người bệnh bị giảm đáp ứng hoặc không thể dung nạp thuốc kích thích tạo hồng cầu.
- Người bệnh gặp rào cản hoặc không thuận tiện với việc sử dụng thuốc tiêm.
Lưu ý chống chỉ định và phối hợp
- Không sử dụng khi người bệnh đang có bệnh ung thư tiến triển hoặc có biến cố huyết khối tim mạch / mạch máu gần đây.
- Không sử dụng phối hợp đồng thời với thuốc ESAs do thiếu dữ liệu về an toàn và hiệu quả.
4.2.4 Khuyến Cáo Dành Cho Các Nghiên Cứu Trong Tương Lai
Cần có thêm các nghiên cứu chuyên sâu để:
Tối ưu hóa việc sử dụng thuốc kích thích tạo hồng ở các nhóm:
- Người bệnh đang lọc màng bụng duy trì.
- Người nhận ghép thận.
- Trẻ em ở mọi mức độ nghiêm trọng ca của bệnh thận mạn.
So sánh rủi ro và lợi ích dài hạn
- Đánh giá giữa liệu pháp dùng thuốc HIF-PHIs so với thuốc ESAS.
- Đánh giá trên đối tượng người lớn và trẻ em mắc bệnh thận mạn có lọc máu hoặc chưa lọc máu.
4.3 Truyền hồng cầu trong điều trị thiếu máu ở bệnh nhân bệnh thận mạn
4.3.1 Truyền Khối Hồng Cầu Để Điều Trị Thiếu Máu Trong Bệnh Thận Mạn
- Việc bổ sung sắt và thuốc kích thích tạo hồng cầu giúp làm giảm đáng kể nhu cầu truyền máu.
- Tuy nhiên, truyền máu vẫn đóng vai trò thiết yếu để quản lý tình trạng thiếu máu nặng hoặc thiếu máu kháng trị ở dân số người bệnh này.
- Trọng tâm cần nắm rõ là các chỉ định khi nào thực sự cần sử dụng liệu pháp truyền khối hồng cầu.
- Cần áp dụng các chiến lược nhằm giảm thiểu tối đa các biến chứng, đặc biệt là tình trạng mẫn cảm miễn dịch đồng loài.
4.3.2 Cơ Sở Cho Chiến Lược Truyền Máu Hạn Chế
Lý do áp dụng chiến lược hạn chế
- Các biến chứng đã được ghi nhận của truyền khối hồng cầu bao gồm: quá tải tuần hoàn, tổn thương phổi cấp tính, mẫn cảm miễn dịch đồng loài và phản ứng tan máu.
- Đặc biệt ở người bệnh thận mạn, mẫn cảm miễn dịch đồng loài sau truyền máu có thể làm giảm khả năng tìm được người hiến phù hợp cho việc ghép thận trong tương lai.
Cân nhắc lợi ích và rủi ro
- Cần đặt các rủi ro của việc truyền máu lên bàn cân cùng với những nguy cơ nghiêm trọng của tình trạng thiếu máu nặng không được điều trị.
- Thiếu máu nặng không điều trị có thể dẫn đến thiếu máu cục bộ cơ tim, suy tim mất bù hoặc thậm chí tử vong.
4.3.3 Chỉ Định Truyền Khối Hồng Cầu
Thiếu máu cấp đe dọa tính mạng
- Chỉ định truyền khi cần điều chỉnh nhanh nồng độ Hb để ổn định lâm sàng (ví dụ: xuất huyết cấp tính hoặc bệnh động mạch vành không ổn định)
- Giai đoạn trước phẫu thuật
- Cân nhắc điều chỉnh nồng độ hemoglobin cho người bị thiếu máu nặng chuẩn bị bước vào cuộc phẫu thuật dự kiến sẽ có lượng máu mất đi đáng kể.
- Thiếu máu mạn tính
- Cân nhắc truyền máu khi liệu pháp dùng thuốc ESAs hoặc HIF-PHIs không mang lại hiệu quả (như bệnh lý Hb, suy tủy, hoặc kháng thuốc).
- Cân nhắc truyền máu khi các liệu pháp dùng thuốc trên có thể gây hại (như người bệnh có tiền sử đột quỵ hoặc đang mắc ung thư).
4.3.4 Ngưỡng Hemoglobin Để Chỉ Định Truyền Máu
- Các dấu hiệu và triệu chứng lâm sàng liên quan đến quyết định chính để truyền máu, thay vì dựa vào ngưỡng Hb cố định
- Có thể truyền máu khi nồng độ hemoglobin < 7g/dl đối với bệnh nhân nội viện ổn định về huyết động và không có triệu chứng
- Có thể cân nhắc truyền máu ở ngưỡng Hb < 7, 5g / d cho người bệnh chuẩn bị phẫu thuật tim
- Có thể cân nhắc truyền máu ở ngưỡng Hb <8 g/dl cho người chuẩn bị phẫu thuật chỉnh hình hoặc có bệnh lý tim mạch trên lâm sàng.
4.3.5 Giảm Thiểu Nhu Cầu Truyền Khối Hồng Cầu
- Áp dụng phác đồ chuẩn hóa để phát hiện và điều chỉnh thiếu sắt kịp thời.
- Tuân thủ nghiêm ngặt hướng dẫn lâm sàng khi sử dụng sắt đường tĩnh mạch và thuốc ESAs.
- Giáo dục người bệnh về các lựa chọn điều trị thiếu máu hiện có.
- Cung cấp công cụ hỗ trợ người bệnh đưa ra quyết định truyền máu phù hợp với mục tiêu cá nhân.
4.3.6 Khuyến cáo dành cho nghiên cứu trong tương lai
- Nghiên cứu hiện trạng: Tiến hành các nghiên cứu quan sát về thực trạng truyền khối hồng cầu, bao gồm chỉ định và tỷ lệ ghép thận sau đó.
- An toàn miễn dịch: Nghiên cứu sâu hơn về nguy cơ mẫn cảm miễn dịch đồng loài sau khi truyền máu ở bệnh nhân thận mạn.
- Quản lý lâm sàng: Đánh giá, đối chiếu thực hành lâm sàng giữa các khu vực để tìm phương pháp quản lý thiếu máu tối ưu, hạn chế truyền máu.
- Xử lý và bảo quản: Đánh giá các phương pháp xử lý, bảo quản khối hồng cầu tối ưu và tác động của chúng đến kết quả lâm sàng và ghép thận.
5 Kết luận
Các cập nhật mới của KDIGO 2026 quản lý thiếu máu trong bệnh thận mạn:
- Cập nhật toàn diện hướng dẫn năm 2012 dựa trên bằng chứng mới.
- Chuẩn hóa chẩn đoán và cá thể hóa điều trị thiếu máu ở bệnh thận mạn
- Làm rõ chiến lược sử dụng sắt, ESAS, HIF-PHIs.
- Nhấn mạnh cân bằng lợi ích - nguy cơ, đặc biệt với mục tiêu Hb.
- Xác định các khoảng trống bằng chứng và định hướng nghiên cứu tương lai.
Thông điệp chính: Điều trị thiếu máu ở bệnh thận mạn phải dựa trên bằng chứng, cá thể hóa và hướng đến an toàn lâu dài cho người bệnh.

