Hướng dẫn chẩn đoán và điều trị bệnh gan nhiễm mỡ không do rượu (NAFLD) - AACE và AASLD 2022

Trungtamthuoc.com - Bệnh gan nhiễm mỡ không do rượu là nguyên nhân phổ biến nhất của bệnh gan mạn tính, ảnh hưởng đến 25% dân số toàn cầu. Mặc dù tỷ lệ mắc bệnh ngày càng tăng, tuy nhiên chỉ có ít bệnh nhân được nhận thức về bệnh. Bài viết dưới đây sẽ cung cấp kiến thức về cách dự đoán và điều chỉnh NAFLD.
Lần đầu tiên, Hội Nội tiết lâm sàng Hoa Kỳ (AACE) được phân phối hợp hợp với Hội Hoa Kỳ đưa ra khuyến nghị hướng dẫn Dự đoán và điều trị bệnh gan nhiễm mỡ không rượu (NAFLD) dành cho bác sĩ đa khoa và bác bác sĩ nội tiết tại Quốc hội ngày 05/12/2022.
Bệnh gan nhiễm mỡ không do rượu là nguyên nhân phổ biến nhất của bệnh gan mạn tính, ảnh hưởng đến 25% dân số toàn cầu. Mặc dù tỷ lệ bệnh ngày càng gia tăng, tuy nhiên có < 5% số bệnh nhân NAFLD đã nhận được biểu thức về bệnh so với 38% ở bệnh nhân viêm gan virus. Tìm kiếm tỷ lệ 12-14% bệnh nhân NAFLD ở dạng NASH, có thể diễn ra thành quá trình xơ hóa gan tiến triển, xơ gan hoặc ung thư gan. Ở những người béo phì và/hoặc mở đường (ĐTĐ) loại 2, nguy cơ mắc NASH tăng 2-3 lần. NASH là một trong những nguyên nhân hàng đầu gây ung thư gan, đồng thời là nguyên nhân phức hợp khối hàng thứ hai ở Hoa Kỳ sau viêm gan C. Chẩn đoán NAFLD dựa trên kết quả xét nghiệm sinh hóa gan, dự đoán hình hình ảnh, và không liên quan đến việc sử dụng rượu quá mức hoặc các nguyên nhân gây bệnh khác. Chẩn đoán NASH xác định bằng thiết bị sinh học; tuy nhiên, các xét nghiệm huyết thanh và hình ảnh đặc biệt có thể dùng để xác định nguy cơ xơ hóa gan có ý nghĩa. NAFLD thường đi kèm với các bệnh tim mạch chuyển hóa như: (1) béo phì, (2) để phản insulin, (3) Bệnh tim mạch 2, (4) tăng huyết áp và (5) rối loạn lipid máu nguy hại mạch máu, những bệnh này đều làm tăng nguy cơ máu cơ tim hoặc tắc nghẽn và là những nguyên nhân gây tử vong phổ biến. Điều trị NAFLD chủ yếu là giảm cân nặng bằng chế độ ăn calo thấp; hạn chế chất béo bão hòa, tinh bột, đường; chế độ ăn cải tiến (ví dụ, chế độ ăn Địa Trung Hải và thực phẩm thô qua ít biến); file edit. Có thể nhận được những lợi ích về tim mạch chuyển hóa và mỡ ở gan khi giảm > 5% lượng cơ thể. Giảm cân nhiều hơn ( ≥10% chất lượng) sẽ tăng cường các lợi ích và có thể đảo ngược tình trạng viêm gan nhiễm mỡ hoặc xơ hóa gan. Hiện tại chưa có thuốc nào được Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) chấp thuận để điều trị NAFLD; tuy nhiên, một số thuốc điều trị béo và béo phì có thể có lợi. Phẫu thuật giảm cân cũng có tác dụng giảm cân và giảm mỡ gan ở những bệnh nhân béo phì nặng.
Mức độ khuyến khích: A: rất mạnh; B: mạnh; C: không mạnh; D: ý kiến của chuyên gia
BEL: mức độ bằng chứng tốt nhất: Bằng chứng tốt nghiệp.
1 CHẨN ĐOÁN NAFLD
1.1. Đối tượng nào mắc bệnh NALFD nên xem xét là có “nguy cơ cao” về xơ hóa gan có ý nghĩa lâm sàng (giai đoạn F2-F4) và có nguy cơ xơ gan?
• Nên xem xét các bệnh nhân béo phì và/hoặc có các yếu tố của hội chứng chuyển hóa, tiền bệnh tiểu đường hoặc bệnh tiểu đường loại 2, và những người có gan nhiễm mỡ trên bất cứ xét nghiệm hình ảnh học nào và/hoặc tăng aminotransferase Mạch kéo dài ( ≥ 6 tháng) thuộc nhóm "nguy cơ cao" và cần tầm Kiểm soát NAFLD và xơ hóa gan tiến phát triển. ( Mức B; cường độ bằng chứng trung bình/cao; BEL 2 )
• Đánh giá sự hiện diện và mức độ nguy hiểm của NASH ở những bệnh nhân tiến hành chiến thuật giảm cân (phẫu thuật giảm cân), và cân bằng sinh thiết gan vào lúc thẳng thần kinh giảm cân. Ở bệnh nhân có phân tầng nguy cơ xơ hóa trước kỹ thuật thuộc tính trung bình hoặc cao, nên tiến hành sinh thiết gan. ( Mức B; mức độ mạnh bằng chứng chỉ trung bình; BEL 2 )
Nguyên nhân của bệnh gan nhiễm mỡ thứ phát và xét nghiệm đánh giá nguyên nhân thứ phát của bệnh gan |
| Nguyên nhân |
• Uống rượu quá mức • Viêm gan C (kiểu gen 3) • Loạn dưỡng mỡ • Sụt cân cấp tính (p thuật giảm cân hoặc đói) • Suy dinh dưỡng • Nuôi dưỡng đường tĩnh • Thiếu máu beta-lipoprotein • Chứng chỉ Reye • Liên quan thai kỳ
• Thuốc (ví dụ: corticosteroid, mipomersen, lomitapide, Amiodarone, Methotrexate, Tamoxifen, valproate, các loại thuốc kháng retrovirus) • Các nguyên nhân hiếm gặp: viêm gan tự miễn, thiếu A1AT, hội chứng Wilson và nguyên nhân khác |
| kinh nghiệm |
• Viêm gan C
• Các xét nghiệm bổ sung cần xem xét
|
Từ viết tắt: AMA = kháng thể kháng ty thể (kháng thể kháng ty thế); ANA = kháng thể kháng nhân (kháng thể kháng nhân); A1AT = alpha-1 antitrypsin; ASMA = kháng thể kháng cơ trơn (kháng thể kháng cơ trơn); HCV = virus viêm gan C (virus viêm gan C); HELLP = Tan huyết, Tăng men gan và Giảm tiểu cầu (Hội chứng tan máu, tăng men gan và giảm tiểu cầu); ARN = axit ribonucleic. a Ở những người có nguy cơ cao mắc bệnh NAFLD (ví dụ: Bệnh tiểu đường loại 2, béo phì, hội chứng chuyển hóa), dự đoán gan nhiễm mỡ không bắt buộc phải có bụng siêu âm bất thường, và thích hợp khi tiến hành phân tầng nguy cơ sau khi loại trừ các nhân vật khác của bệnh gan. b Không thực hiện anti-HBc cho tất cả mọi người vì tỷ lệ dương tính cao và chưa rõ giá trị lâm sàng |
1.2. Những xét nghiệm máu nào có thể được sử dụng để dự đoán NAFLD với tình trạng xơ hóa có ý nghĩa lâm sàng (giai đoạn F2-F4) ở người lớn?
• Nên sử dụng công thức dự kiến để đánh giá nguy cơ xơ hóa ở bệnh nhân NAFLD. FIB-4 là test không được nhập ưu tiên để đánh đầu giá trị. ( Mức B; mức độ mạnh bằng chứng chỉ trung bình; BEL 2 )
• Cân nhắc đo LSM (đo độ cứng gan: đo độ cứng của gan) hoặc xét nghiệm ELF (Tăng cường kiểm tra xơ hóa gan: xét nghiệm xơ hóa gan nâng cao) khi có thể đối lập với các bệnh nhân thuộc nhóm “nguy cơ cao” (đã đề cập ở trên) có điểm FIB-4 cao hoặc trung bình. ( Mức B; độ mạnh bằng chứng trung bình; BEL 2 )
1.3. Những kỹ thuật thần tốc dự đoán hình ảnh nào có thể được sử dụng để dự đoán NAFLD với tình trạng xơ hóa gan có ý nghĩa lâm sàng (giai đoạn F2-F4) ở bệnh nhân lớn?
• Để phân giai đoạn nguy cơ xơ hóa, nên ưu tiên sử dụng VCTE (đo độ đàn hồi gan thoáng qua) được xem là tốt nhất để xác định tiến trình phát triển của bệnh và các kết nối cục bộ liên quan đến gan. Có thể cân nhắc các kỹ thuật dự đoán hình ảnh thay thế như: siêu âm đo độ đàn hồi bằng biến dạng sóng biến dạng (shear wave elastography) (ít được công nhận hơn) và/hoặc đo độ đàn hồi bằng cộng tác động từ ( chính xác nhất nhưng chi phí cao và khả năng sử dụng thấp; tốt nhất khi được chỉ định bởi bác sĩ chuyên khoa gan mật cho một số trường hợp hợp). ( Mức B; mức độ mạnh bằng chứng chỉ trung bình; BEL 2 )
1.4. Có phải tất cả bệnh nhân bệnh nên tầm soát xơ hóa gan có ý nghĩa lâm sàng (giai đoạn F2-F4) kèm theo NAFLD không?
• Ở bệnh nhân bệnh tiểu đường loại 2, nên cân nhắc tầm kiểm soát quá trình hóa gan có ý nghĩa lâm sàng (giai đoạn F2 – F4) bằng xét nghiệm FIB-4 ngay cả khi họ có nam giới gan bình thường. ( Mức B; cường độ bằng chứng trung bình/cao; BEL 2 )
• Ở bệnh nhân bệnh đái tháo đường type 1 có thể xem xét sẵn sàng lọc NAFLD với tình trạng xơ hóa có ý nghĩa lâm sàng (giai đoạn F2-F4) bằng cách sử dụng FIB-4, chỉ khi có các yếu tố nguy cơ cơ như: Béo phì, các đặc tính của hội chứng chuyển hóa, tăng aminotransferase máu (>30 U/L), hoặc gan nhiễm mỡ trên hình ảnh học. ( Mức độ C; mức độ mạnh bằng chứng minh trung bình/yếu; BEL 2; giảm mức độ khuyến khích dựa trên sự không thống nhất của các nghiên cứu và mức độ sai số từ trung bình đến cao )
• Phân tầng thấp nguy cơ bổ sung cho bệnh nhân bệnh tiểu đường loại 2, hoặc bệnh tiểu đường loại 1 có: nguy cơ tim mạch chuyển hóa và/hoặc tăng aminotransferase huyết (>30 U/L) bằng cách sử dụng xét nghiệm FIB-4, đo đàn hồi phục và/hoặc kiểm tra ELF. ( Mức B; bằng chứng cao/trung bình; BEL 2 )
1.5. Khi bệnh nhân lớn nào nên được chuyển đến bác sĩ chuyên khoa tiêu hóa/gan mật để điều trị?
• Bệnh nhân có ALT hoặc AST kéo dài và/hoặc có gan nhiễm mỡ trên hình ảnh học và nguy cơ trung bình (FIB-4: 1,3 - 2,67; LSM: 8 – 12 kPa; hoặc test ELF: 7.7 - 9.8) hoặc nguy cơ cao (FIB-4: >2,67; LSM: >12 kPa; hoặc test ELF: >9.8) dựa trên kết quả xét nghiệm máu và/hoặc hình ảnh học (đã được mô tả ở đây) trên) thì nên chuyển đến bác sĩ chuyên khoa tiêu hóa hoặc bác sĩ chuyên khoa gan mật để đánh giá giá sâu hơn (chẳng hạn như sinh thiết gan). ( Mức B; mức độ mạnh bằng chứng chỉ trung bình; BEL 2 )
• Chuyến chuyến bệnh nhân đến bác sĩ chuyên khoa tiêu hóa/gan mật nếu có bằng chứng lâm sàng của bệnh gan tiến phát triển (báng, bệnh não não, thư giãn mạch thực quản, hoặc bằng chứng suy chức năng tế bào gan) để đánh giá sâu hơn. ( Mức B; cường độ bằng chứng trung bình/cao; BEL 2 )
2 Điều TRỊ NAFLD Ở NGƯỜI LỚN
2.1. Làm thế nào để quản lý nguy cơ chuyển hóa mạch cơ sở và các chứng chỉ bên ngoài trong bối cảnh NAFLD?
• Bệnh nhân NAFLD với: béo phì, hội chứng chuyển hóa, tiền đái tháo đường, bệnh tim mạch, rối loạn lipid máu, tăng huyết áp, và bệnh tim mạch phải được quản lý dựa trên các dịch vụ chăm sóc hiện tại. ( Cấp độ A; bằng chứng chỉ cao/trung bình; BEL 1 )
2.2. Những sản phẩm khuyến mãi thay đổi lối sống (can thiệp về chế độ ăn và tập thể dục) ở bệnh nhân mắc NAFLD hoặc NASH?
• Ở những bệnh nhân nhiều mỡ thừa và NAFLD, nên thay đổi đường sống với mục tiếu ít giảm nhất 5% (tốt hơn là ≥10%) cân nặng, vì giảm nhiều cân hơn giúp cải thiện mô học gan và lợi về chuyển mạch thời gian. ( Mức độ B; độ mạnh bằng chứng minh trung bình/cao; BEL 1; giảm độ khuyến khích do kích thước nghiên cứu nhỏ, các can be rất không đồng nhất, thời gian thử nghiệm ngắn, ít mẫu nghiên cứu về sinh thiết gan )
• Khuyến cáo phải thay đổi chế độ ăn ở bệnh nhân NAFLD, bao gồm giảm thành phần dinh dưỡng đa lượng để gây thiếu sức mạnh (bằng cách hạn chế chất béo bão hòa, tinh bột và thức ăn chứa nhiều đường) và ứng dụng sử dụng chế độ ăn lành mạnh hơn (ví dụ chế độ ăn Địa Trung Hải). ( Mức A; mức độ mạnh bằng chứng chỉ trung bình; BEL 1 )
• Bệnh nhân NAFLD cần hoạt động chất để cải thiện thành phần cơ thể (thành phần cơ thể: tỷ lệ phần trăm chất béo, xương và cơ trong cơ thể) và vấn đề tim mạch chuyển hóa. Khuyến khích bệnh nhân nên tham gia vào các kế hoạch đào tạo (nếu có) và cần phù hợp với lối sống và sở thích của từng bệnh nhân. ( Mức A; mức độ mạnh bằng chứng chỉ trung bình; BEL 1 )
2.3. Những loại thuốc nào đã được chứng minh là có tác dụng điều trị bệnh gan và bệnh lý tim mạch chuyển hóa ở bệnh nhân NAFLD hoặc NASH?
• Khuyến cáo sử dụng pioglitazone và thuốc đồng vận động GLP-1 (GLP-1 RA) ở bệnh nhân đồng bệnh đái tháo đường type 2 và NASH (đã được dự đoán bằng sinh thiết). ( Mức A; bằng chứng chỉ cao; BEL 1 )
• Ở bệnh nhân có khả năng mắc bệnh NASH dựa trên các xét nghiệm không xâm lấn và tăng aminotransferase, phải cân nhắc điều trị bệnh đái tháo đường bằng pioglitazone và/hoặc GLP 1-RA. ( Mức A; bằng chứng chỉ cao; BEL 1 )
• Ở bệnh nhân đồng bệnh bệnh đái tháo đường type 2 và NAFLD, phải cân nhắc sử dụng GLP-1 RA, pioglitazone, hoặc thuốc ức chế SGLT-2 để đạt được lợi ích về tim mạch chuyển hóa; tuy nhiên, không có bằng chứng cho thấy lợi ích của thuốc ức chế SGLT-2 trong điều trị viêm gan nhiễm mỡ. ( Mức A; bằng chứng chỉ cao; BEL 1 )
• Thiếu bằng chứng cho thấy hiệu quả nên không quảng cáo các loại thuốc như: metformin, Acarbose, thuốc ức chế DPP-4 và Insulin trong điều trị viêm gan nhiễm mỡ tế tế bào gan), nhưng có thể sử dụng khi cần thiết để điều trị tăng đường huyết ở bệnh nhân đồng bệnh đái tháo đường 2 và NAFLD hoặc NASH. ( Mức độ B; độ mạnh bằng chứng cao; BEL 1; giảm độ khuyến khích sử dụng kết quả thay thế trong nghiên cứu )
• Đối với bệnh nhân NASH không kèm theo bệnh đái tháo đường týp 2, có thể cân nhắc sử dụng vitamin E để điều trị; Nhưng nếu bệnh nhân mắc bệnh kèm theo bệnh loại 2 hoặc xơ hóa gan tiến triển thì hiện tại vẫn chưa đủ bằng chứng để khuyến cáo sử dụng. ( Mức B; mức độ mạnh bằng chứng cao; BEL 1; giảm khuyến khích do nguy cơ/lợi ích )
• Hiện tại không khuyến khích sử dụng các loại thuốc khác ở bệnh nhân NASH vì thiếu bằng chứng về những lợi ích lâm sàng. ( Mức A; bằng chứng chỉ cao; BEL 1 )
| Thuốc điều trị bệnh và tác dụng hiệu quả của nó trong điều trị NAFLD | ||
| Thuốc | Size at gan | Hoạt động của bệnh (viêm gan nhiễm mỡ / NAS) |
| metformin | Không thể thay đổi | Trung tính |
| Pioglitazone | Giảm | Cải thiện sự cải thiện |
| insulin | Giảm | Chưa rõ tác động |
| GLP1-RA (Semaglutide và Liraglutide) | Giảm | Cải thiện sự cải thiện |
| Ức chế SGLT2 (dapagliflozin, Empagliflozin và canagliflozin) | Giảm | Chưa rõ tác động |
| Ức chế độ DPP-4 (Sitagliptin và Vildagliptin) | Không thay đổi (Trong RCT | Chưa rõ tác động |
Chú thích: DPP-4= dipeptidyl peptidase IV; NAS = Điểm hoạt động của NAFLD; RCTs = thử nghiệm ngẫu nhiên có bằng chứng. a: Tác động làm tăng xơ hóa gan của các loại thuốc điều trị bệnh cải thiện viêm gan nhiễm mỡ nhìn chung là rất nhỏ, mặc dù có một số nghiên cứu riêng lẻ và các phân tích tổng hợp về RCT có sẵn báo cáo giảm độ xơ cứng hóa học với pioglitazone | ||
2.4. Thuốc điều trị béo phì nào đã được chứng minh là có lợi trong điều trị bệnh gan và tình trạng mạch chuyển hóa ở bệnh nhân mắc bệnh NAFLD hoặc NASH?
• Nên sử dụng các loại thuốc điều trị béo phì ở những bệnh nhân béo phì kèm NAFLD hoặc NASH nếu thay đổi đường sống đơn thuần không đạt mục tiêu giảm ít nhất 5% (tốt hơn là ≥10%) cân nặng, vì giảm nhiều Cân bằng hơn giúp cải thiện mô gan và lợi ích về thời gian chuyển hóa. ( Mức độ B; mức độ mạnh bằng chứng minh trung bình; BEL 1; giảm độ khuyến khích do kích thước nghiên cứu nhỏ và thời gian thử nghiệm ngắn )
• Để quản lý tình trạng cân nặng kéo dài ở những bệnh nhân có BMI ≥27 kg/m2 kèm theo NAFLD hoặc NASH, nên ưu tiên sử dụng semaglutide 2,4 mg/tuần (có bằng chứng tốt) hoặc liraglutide 3 mg/ngày. ( Mức độ B; mức độ mạnh bằng chứng minh cao/trung bình; BEL 1; giảm độ khuyến cáo có sự khác biệt về dạng bào chế và dư lượng của semaglutide và liraglutide được sử dụng trong các thử nghiệm về NASH )
• Phải xem xét điều trị béo phì bằng thuốc (ưu tiên semaglutide 2,4 mg/tuần (có bằng chứng tốt) hoặc liraglutide 3 mg/ngày) như là điều trị hỗ trợ cho việc thay đổi lối sống ở những bệnh nhân béo thuốc kèm theo NAFLD hoặc NASH để cải thiện sức khỏe về tim mạch chuyển hóa, và điều trị hoặc phòng bệnh: Bệnh tim mạch và các biểu hiện nặng khác của bệnh béo phì. ( Cấp độ A; bằng chứng chỉ cao/trung bình; BEL 1 )
2.5. Phẫu thuật giảm cân ảnh hưởng gì đến bệnh gan và bệnh tim mạch chuyển hóa ở bệnh nhân mắc NAFLD hoặc NASH?
• Nên xem chiến thuật giảm cân là một lựa chọn để điều trị NAFLD (Mức B; tăng cường bằng chứng trung bình/yếu; BEL 2) và cải thiện sức khỏe về tim mạch chuyển hóa (Mức A; tăng cường bằng chứng cao /trung bình; BEL 2; quà khuyến khích tăng dựa trên các lợi ích về tim mạch chuyển hóa và tử vong do mọi nguyên nhân ở tất cả những bệnh nhân có hoặc không có NAFLD) dành cho những bệnh nhân NAFLD có BMI ≥35 kg/m2 (232,5 kg/m2 đối với người châu Á), đặc biệt khi mắc bệnh tiểu đường loại 2. Điều này cũng nên xem xét là một lựa chọn ở những bệnh nhân có BMI ≥ 30 đến 34,9 kg/m2 ( ≥27,5 đến 32,4 kg/m2 đối với người châu Á). ( Mức B; cường độ bằng chứng trung bình/yếu; BEL 2 )
• Đối với các bệnh nhân NASH và xơ gan còn bù, cần thận trọng khi chỉ định kỹ thuật giảm cân, nên chỉ định tùy từng bệnh nhân và thực hiện tại các trung tâm có kinh nghiệm. ( Mức B; cường độ bằng chứng trung bình/yếu; BEL 2 )
• Đối với những bệnh nhân bị xơ gan mất bù, không khuyến khích khoa học giảm cân bằng chứng hữu hạn và có khả năng gây nguy hại. ( Mức B; cường độ bằng chứng trung bình/yếu; BEL 2 )
• Không khuyến khích các liệu pháp về mặt chuyển hóa và điều trị giảm cân qua nội soi và các thiết bị hỗ trợ cung qua đường miệng (thiết bị uống) ở bệnh nhân NAFLD không có đủ bằng chứng. ( Mức độ C; mức độ mạnh bằng chứng minh trung bình/yếu; BEL 2; giảm độ khuyến khích chất lượng của các nghiên cứu và kích thước mẫu nhỏ )
3 CHẨN ĐOÁN VÀ QUẢN LÝ TRẺ MẮC NAFLD
3.1. Đối tượng nào sẽ được sàng lọc NAFLD và các bệnh đi kèm?
• Trẻ em ở mọi lớp tuổi và thanh thiếu niên có béo phì hoặc bệnh tiểu đường loại 2, nhưng không mắc bệnh tiểu đường loại 1 thì nên sẵn sàng lọc NAFLD bằng phương pháp xét nghiệm ALT huyết thanh. ( Mức B; Độ mạnh bằng chứng chỉ trung bình/cao; BEL 2 ).
• Sẵn sàng lọc NAFLD cho bệnh nhân nữ tuổi thành niên mắc chứng bệnh nguy hiểm bằng huyết thanh ALT. ( Mức B; Độ mạnh bằng chứng chỉ trung bình/cao; BEL 2 )
• Sẵn sàng lọc tiến trình bệnh lý hoặc bệnh tiểu đường loại 2 cho trẻ em và thanh thiếu niên mắc bệnh NAFLD sử dụng pháp dung nạp Glucose nếu cường độ đường huyết lúc đói ≥100 mg/mL hoặc nếu HbA1c nằm trong tiến trình bệnh học ( ≥ 5,7% đến 6,4%). ( Mức B; Độ mạnh bằng chứng chỉ trung bình; BEL 2 )
3.2. Những xét nghiệm nào có thể được sử dụng để dự đoán NAFLD ở trẻ em?
• Khuyến khích nên sử dụng aminotransferase huyết thanh để kiểm tra những trẻ có nguy cơ cao mắc bệnh NAFLD. ( Mức B; Độ mạnh bằng chứng chỉ trung bình; BEL 2 )
• Có thể dự đoán NAFLD ở trẻ em bằng hình ảnh học (siêu âm hoặc MRI-tỉ số mỡ mật độ proton :MRI-proton Density Fat Fat) hoặc sinh thiết bị kết hợp với các loại trừ các nguyên nhân gây gan nhiễm mỡ không phải NAFLD khác như chứng minh Wilson, bệnh lý thể và thuốc. ( Mức B; Độ mạnh bằng chứng chỉ trung bình; BEL 2 )
• Không nên sử dụng các công thức dự đoán xơ cứng hóa và các dấu hiệu sinh học đặc biệt hiện có để dự đoán quá trình phát triển của người lớn cho trẻ em vì chúng không chính xác hoặc cần xác nhận thêm. ( Mức B; Độ mạnh bằng chứng chỉ trung bình; BEL 2 )
3.3. Thay đổi đường sống, điều trị thuốc hoặc thuốc chữa bệnh nhi mắc NAFLD như thế nào? Vai trò của pháp luật sử dụng thuốc điều trị các rối loạn nội tiết ở bệnh nhi mắc bệnh NAFLD là gì?
• Khuyến khích bệnh nhi mắc bệnh NAFLD nên thay đổi lối sống, cung cấp việc làm thay đổi chế độ ăn để gây thiếu hồng lực và giảm tiêu thụ đường thúc đẩy tối ưu hóa chỉ số BMI. ( Level B; Độ mạnh bằng chứng minh trung bình; BEL 1; giảm mức độ khuyến khích do số lượng giới hạn của thử nghiệm ngẫu nhiên có chứng minh và mô hình kích thước nhỏ )
• Có thể xem xét dùng thuốc đồng vận thụ thể GLP-1 để điều trị cho bệnh nhi béo phì và bệnh tiểu đường loại 2 (Mức D; ý kiến của chuyên gia; BEL 4), thuốc này cũng có thể mang lại lợi ích cho Bệnh nhi mắc NAFLD (mặc dù FDA không chấp thuận chỉ định điều này). ( Cấp D; Ý kiến của Chuyên gia; BEL 4 )
Xem sơ đồ quản lý bệnh nhân NAFLD bên dưới
1. Sơ đồ quản lý NAFLD - Tổng quan
2. Dự phòng xơ gan ở bệnh nhân NAFLD
3. Quản lý cân nặng ở bệnh nhân NAFLD
4. Quản lý bệnh nhân NAFLD
5. Quản lý tăng huyết áp ở bệnh nhân NAFLD
6. Quản lý rối loạn lipid máu nguy cơ xơ cứng mạch ở bệnh nhân NAFLD
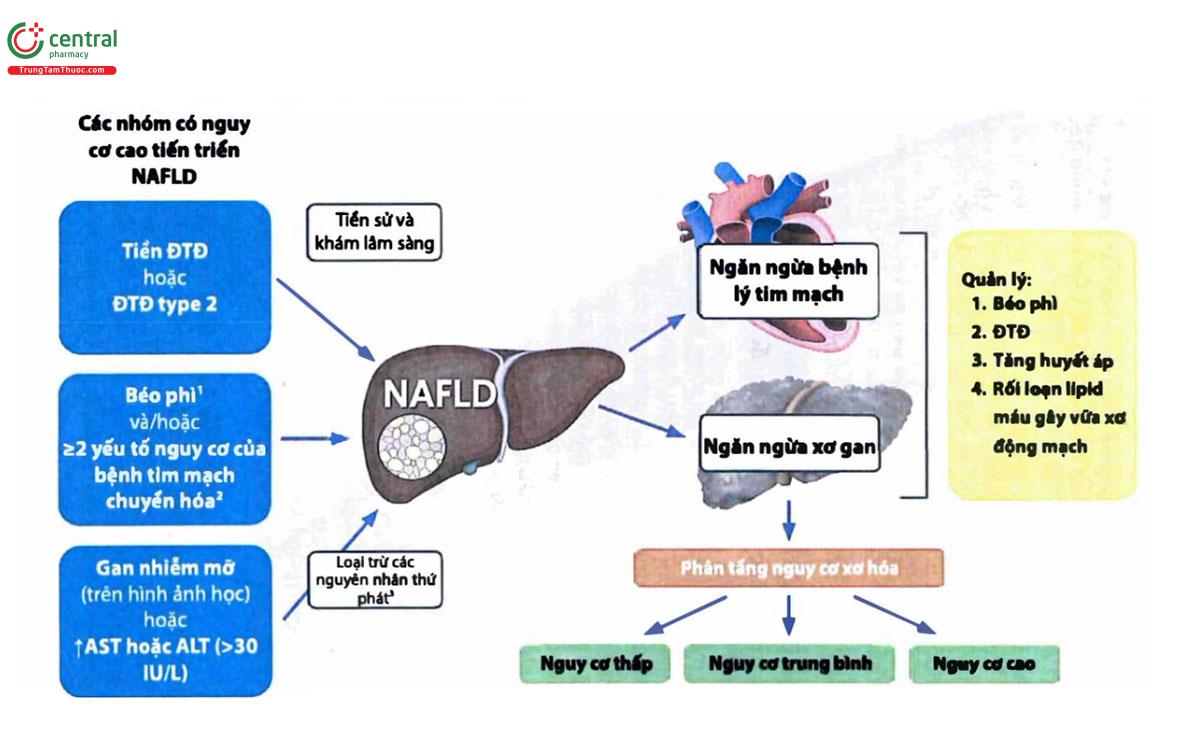
(1) Bệnh mạn tính có tính giảm béo (Adiposity-based Chronic disease: ABCD) là một thuật ngữ mang tính dự đoán được sản xuất bởi AACE cải thiện béo phì theo cách tập trung vào chứng minh biến thể bất ngờ khối mô mỡ, phân bố, chức năng mô mỡ và bệnh cơ chế có thể cải thiện bằng cách giảm cân.
(2) Các yếu tố nguy cơ tim mạch chuyển hóa của hội chứng chuyển hóa là chu vi vòng bụng >100 cm ở nam, >90 cm ở nữ; triglycerid ≥ 150 mg/dL, HDL-C< 40 mg/dL ở nam, <50 mg/dL ở nữ; HA ≥ 130/285 mmHg; Cơn đói glucose ≥100 mg/dL (NCEP ATP III)
(3) Các nguyên nhân thứ phát của gan nhiễm mỡ hoặc tăng transaminase (AST hoặc ALT): Dùng rượu quá nhiều ( ≥196 g/ tuần ở nữ hoặc ≥294 g/ tuần ở nam), viêm gan B, viêm gan C (genotype 3), bệnh Wilson, thiếu alpha 1 antitrypsin, rối loạn mỡ, chế độ ăn kiêng, nuôi dưỡng tĩnh mạch, thiếu beta lipoprotein máu, bệnh huyết sắc tố, thâm thương u, thuốc và một số nguyên nhân khác .
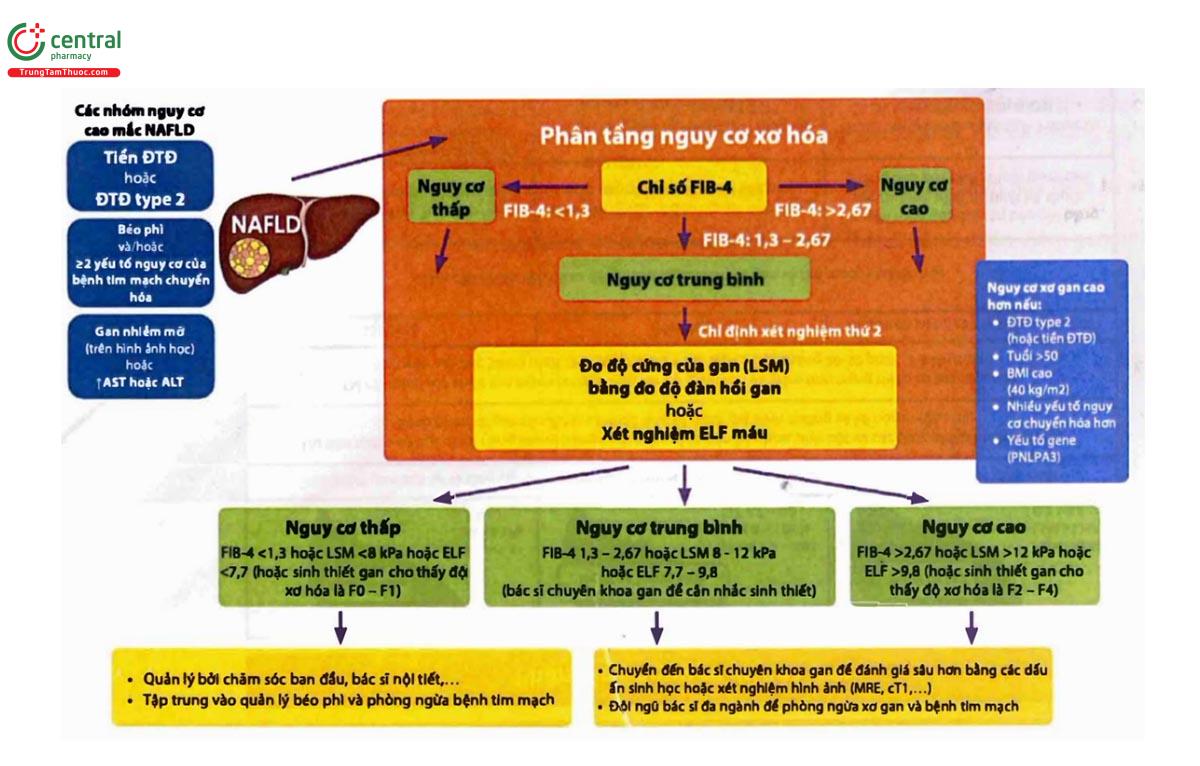
Chú thích: CT1 = gan multiscan, ELF = Xét nghiệm xơ hóa gan nâng cao, kPa = kilopascals, LSM = Đo độ cứng của gan, MRE = đo độ đàn hồi bằng cộng tác động.
QUẢN LÝ CÂN NẶNG Ở BỆNH NHÂN NAFLD
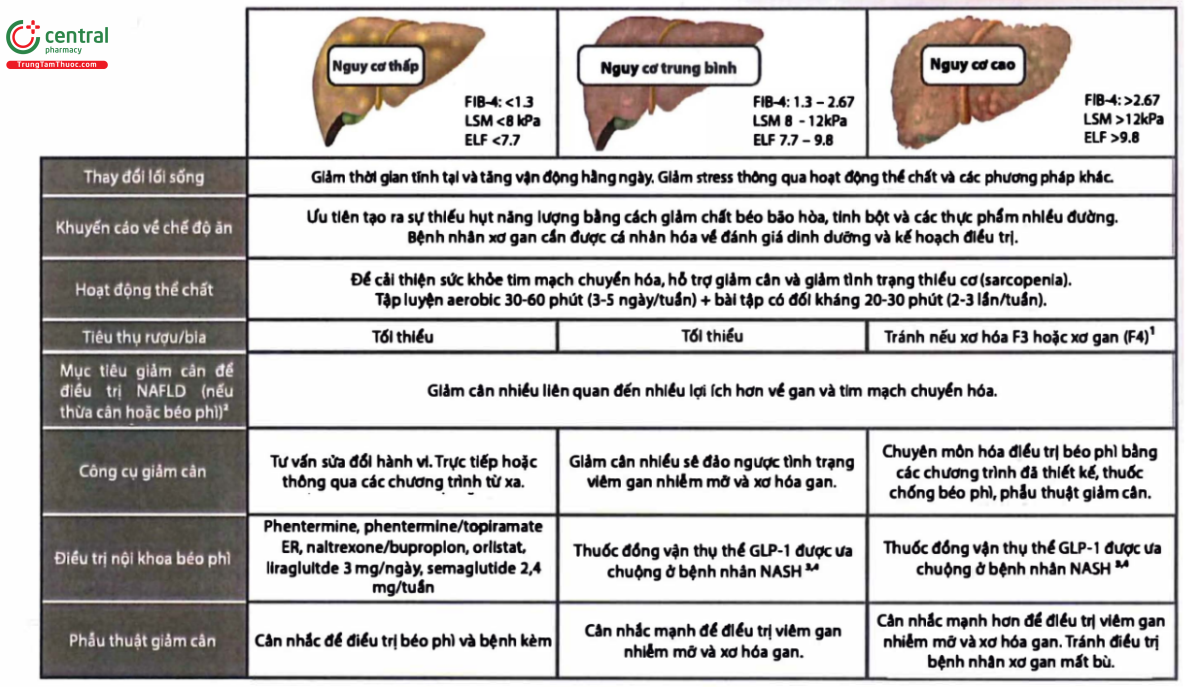
Chú thích:
(1) Theo dõi chặt chẽ ung thư tế bào tế bào gan ở bệnh nhân được dự đoán sợi dựa trên sinh thiết hoặc có khả năng sản xuất gan dựa trên LSM >13,6 kPa từ Fibroscan, ELF ≥9,8 hoặc >5,0 kPa trên MRE. Kích thước tầm Yên tĩnh tĩnh mạch nếu LMS >20 kPa hoặc tiểu cầu <150.000/mm³
(2) Nên xem những mục tiêu này như một hướng dẫn mở rộng. Ngoài mức độ giảm cân, NAFLD/NASH có thể được cải thiện thông qua thay đổi thành phần dinh dưỡng đa lượng, luyện tập thể lực và những yếu tố khác. Tất cả những nghiên cứu chất lượng cao hiện có được giới hạn thời gian tối đa là 12 tháng.
(3) Không có bằng chứng chất lượng cao về thuốc điều trị bệnh nhân xơ gan do NASH. Nên cá nhân hóa điều trị và sử dụng thận trọng bởi các chuyên gia về gan.
(4) Trong các thuốc đồng vận thụ thể GLP-1, semaglutide có bằng chứng lợi ích tốt nhất ở bệnh nhân viêm gan nhiễm mỡ và xơ hóa gan.
QUẢN LÝ ĐTĐ Ở BỆNH NHÂN NAFLD
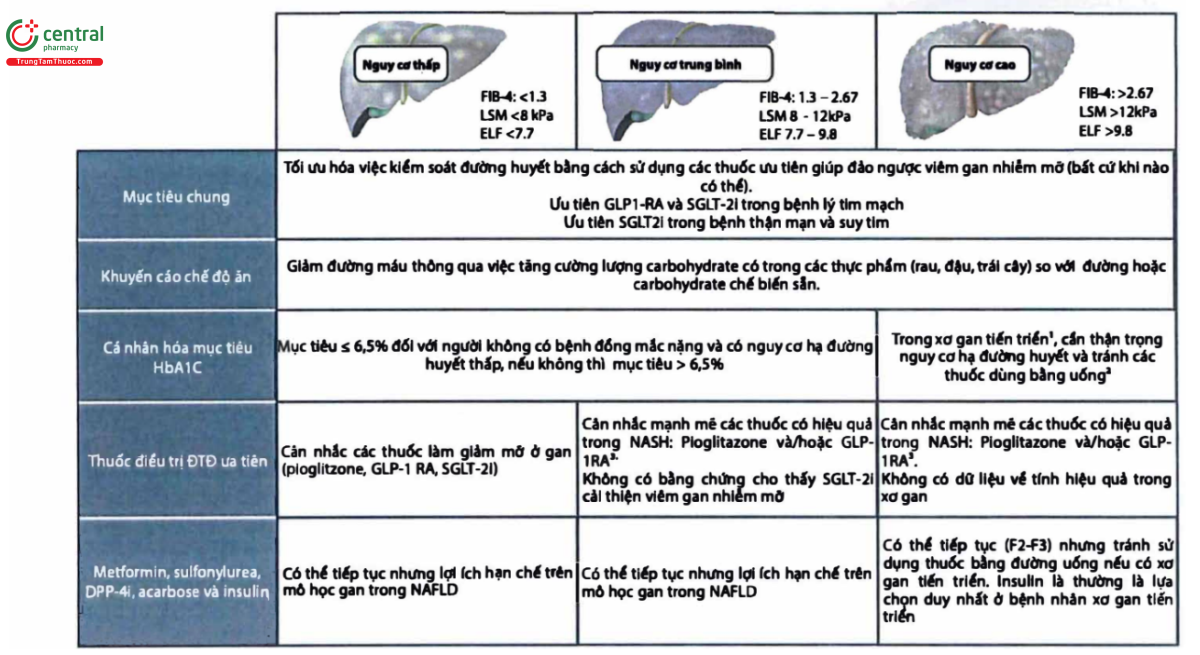
Chú thích:
(1) Xơ gan tiến triển được định nghĩa là những bệnh nhân được chẩn đoán xơ gan dựa trên sinh thiết, phân loại Child B hoặc C với bằng chứng lâm sàng về các biến chứng đi kèm (giãn tĩnh mạch thực quản, tăng áp lực tĩnh mạch cửa, cổ trướng, ...)
(2) Dữ liệu hạn chế về sử dụng các thuốc ĐTĐ qua đường uống và GLP1-RA ở bệnh nhân xơ gan. Cần tránh dùng metformin, GLP1-RA có vẻ an toàn, và nên ưu tiên sử dụng insulin. Tránh các thuốc đường uống trong xơ gan tiến triển.
(3) Trong các thuốc thuộc nhóm GLP-1RA, semaglutide có bằng chứng tốt nhất về lợi ích ở những bệnh nhân viêm gan nhiễm mỡ và xơ hóa
QUẢN LÝ HUYẾT ÁP Ở BỆNH NHÂN NAFLD
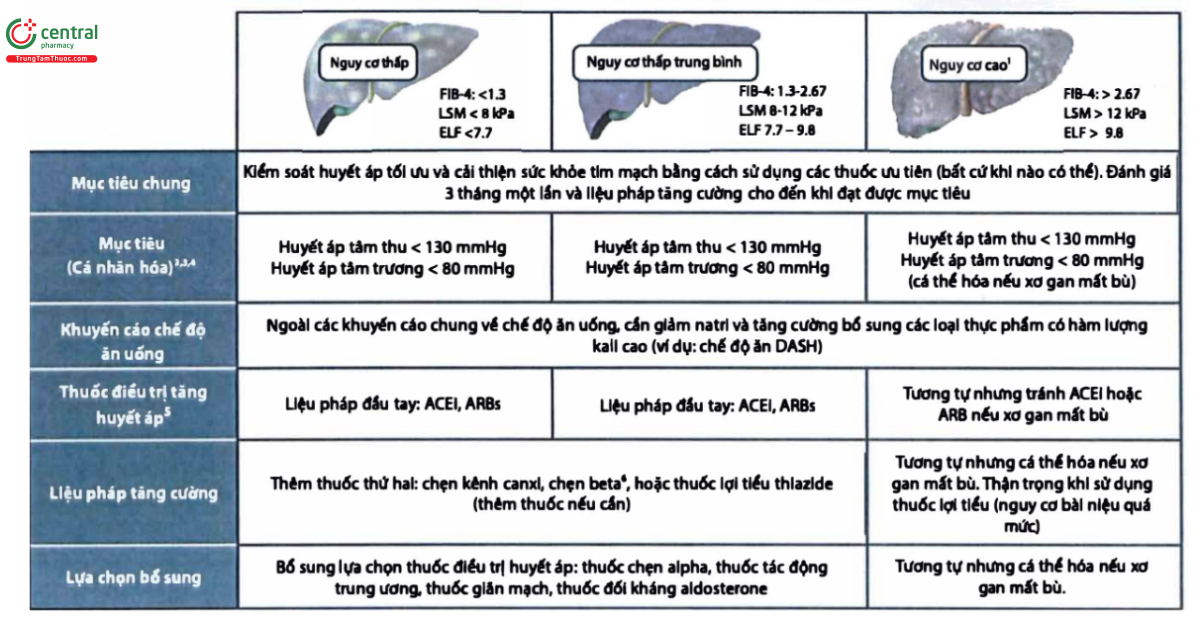
Chú thích:
(1) Xơ gan tiến triển được định nghĩa là xơ gan dựa trên sinh thiết, Child B hoặc C với các biến chứng trên lâm sàng đi kèm (giãn tĩnh mạch thực quản, tăng áp lực tĩnh mạch cửa, báng, ...)
(2) AACE khuyến cáo kiểm soát huyết áp nên cá nhân hóa, nhưng mục tiêu <130/80 mmHg là phù hợp với hầu hết bệnh nhân
(3) Cân nhắc mục tiêu huyết áp ít nghiêm ngặc hơn ở bệnh nhân với các bệnh kèm phức tạp hoặc những người có tác dụng phụ của thuốc
(4) Cân nhắc mục tiêu nghiêm ngặt hơn (ví dụ: <120/80 mmHg, nếu có thể đạt được) mà không có tác dụng phụ do thuốc
(5) Nếu huyết áp ban đầu >150/100 mmHg, bắt đầu với liệu pháp kép (ACEi hoặc ARB, + chẹn kênh Canxi, chẹn beta hoặc lợi tiểu thiazide)
(6) Ưu tiên thuốc chẹn beta ít ảnh hưởng cân nặng: Carvedilol, nebivolol
QUẢN LÝ RỐI LOẠN LIPID MÁU GÂY VỮA XƠ ĐỘNG MẠCH Ở BỆNH NHÂN NAFLD
Mức nguy cơ lipid giống nhau ở bệnh nhân NAFLD hoặc NASH
| Mục tiêu chung | Cần sớm điều trị tích cực cho tình trạng rối loạn lipid máu để giảm thiểu nguy cơ tim mạch. Tích cực điều trị cho đến khi lipid máu đạt mục tiêu. | ||
| Khuyến cáo chế độ ăn | Tăng tiêu thụ chất xơ (>25 g/ngày), ưu tiên rau, trái cây, ngũ cốc, các loại hạt, giảm chất béo bão hòa và đường bổ sung (ví dụ: chế độ ăn Địa Trung Hải). | ||
| Mức nguy cơ lipid | Nguy cơ tim mạch cao1 ĐTĐ hoặc bệnh thận mạn giai đoạn 23 không kèm theo các yếu tố nguy cơ khác | Nguy cơ tim mạch rất cao1 Bệnh tim mạch do vữa xơ có biểu hiện lâm sàng hoặc nguy cơ tim mạch 10 năm >20%. ĐTĐ kèm 21 yếu tố nguy cơ bệnh thận mạn 23, HeFH | Nguy cơ tim mạch cực kỳ cao1 Bệnh lý tim mạch tiến triển; Bệnh lý tim mạch + ĐTĐ hoặc bệnh thận mạn 23 hoặc HeFH Tiền sử gia đình mắc bệnh lý tim mạch lúc trẻ (nam <55 tuổi, nữ <65 tuổi |
| Mục tiêu LDL-C (mg/dl) | <100 | <70 | <55 |
| Mục tiêu Non-HDL-C (mg/dl) | <130 | <100 | <80 |
| Mục tiêu triglycerides (mg/dl) | <150 | <150 | <150 |
| Mục tiêu Apo B (mg/dl) | <90 | <80 | <80 |
| Liệu pháp đầu tay: Statin | Sử dụng statin cường độ trung bình đến cao2 nếu không có chống chỉ định. Statin an toàn ở bệnh nhân NAFLD hoặc NASH nhưng không được sử dụng trong xơ gan mất bù (Child C) | ||
| Nếu LDL-C không đạt mục tiêu3: tăng cường độ Statin | Sử dụng liều cao hơn hoặc statin có hoạt lực cao | ||
| Nếu LDL-C không đạt mục tiêu (hoặc không dung nạp statin)4: thêm thuốc thứ 2, sau đó thêm thuốc thứ 3 | Ezetimibe, thuốc ức chế PCSK9, acid bempedolc, colesevelam, inclisiran. | ||
| Nếu TG >500 mg/dL | Fibrates, acid béo Omega 3, Icosapent ethyl (nếu có đái tháo đường cần tối ưu hóa kiểm soát đường huyết và cân nhắc cho ploglitazone)5 | ||
| Nếu TG 135-499 mg/dL khi đã dùng liều statin tối đa | Nhấn mạnh chế độ ăn (như trên) | Thêm icosapent ethyl6 | Thêm icosapent ethyl6 |
Chú thích: HeFH: tăng cholesterol máu dị hợp tử có tính gia đình
(1) Yếu tố nguy cơ chính: tuổi >40, ĐTĐ, tăng huyết áp, tiền sử gia đình mắc bệnh lý tim mạch lúc trẻ, HDL-C thấp, LDL-C tăng, hút thuốc lá, bệnh thận mạn giai đoạn 3-4
(2) Liệu pháp statin cường độ cao: rosuvastatin 20-40 mg/ngày; artovastatin 40-80 mg/ngày
(3) Nếu không đạt mức lipid mục tiêu, kết hợp các thuốc hạ lipid máu khác (ezetimibe, ức chế PCSK9, bempedoic acid, colesevelam, hoặc inclisiran) với statin liều tối đa có thể dung nạp.
(4) Sử dụng các xét nghiệm chuyên biệt và theo dõi bệnh nhân để đánh giá mức độ đạt mục tiêu và khả năng dung nạp của liệu pháp statin
(5) Niacin có thể làm giảm triglyceride nhưng không làm giảm bệnh lý tim mạch và làm nặng thêm tình trạng đề kháng insulin. Nó có thể thúc đẩy tình trạng tăng đường huyết ở bệnh nhân có nguy cơ cao ĐTĐ.
(6) Khuyến cáo Icosapent ethyl 4 g/ngày như một thuốc bổ trợ cho liệu pháp statin với liều tối đa có thể dung nạp để làm giảm nguy cơ bệnh lý tim mạch ở nhóm bệnh nhân có nguy cơ cao.
4 PHỤ LỤC ĐÁNH GIÁ TÌNH TRẠNG XƠ HÓA GAN THƯỜNG DÙNG TRÊN LÂM SÀNG
Đánh giá sớm tình trạng xơ hoá của gan có vai trò rất quan trọng, là sự phối hợp của nhiều phương pháp, bao gồm lâm sàng và các test đánh giá được tóm tắt dưới đây:
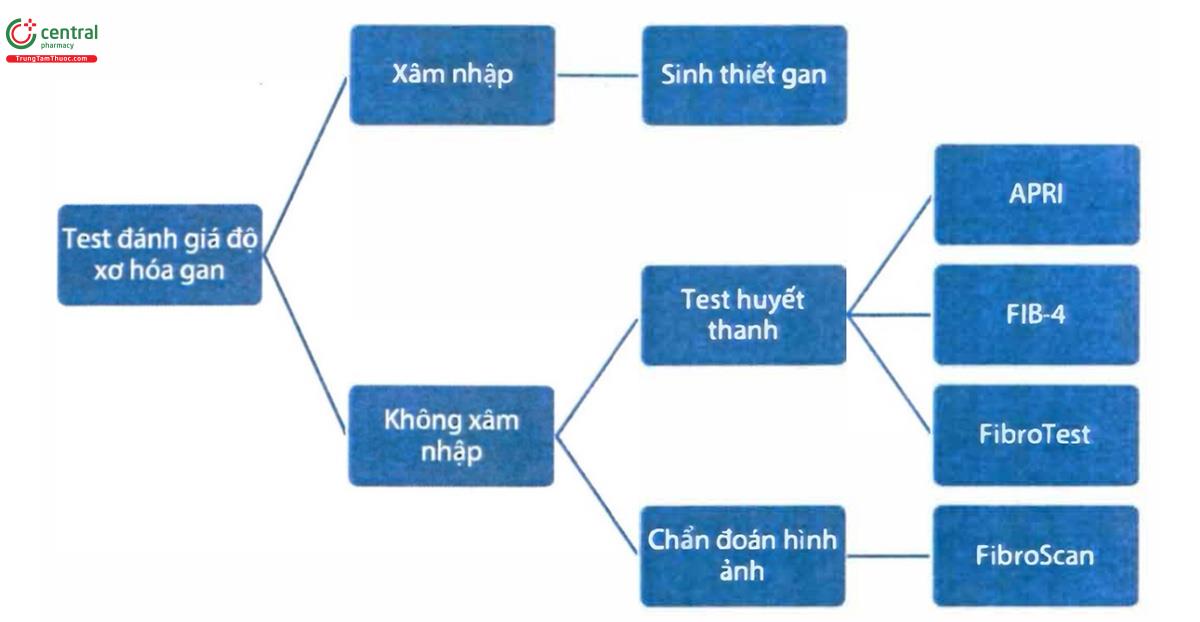
* Sinh thiết gan là tiêu chuẩn vàng để đánh giá giai đoạn bệnh gan và độ xơ hoá của gan.
Tuy nhiên, sinh thiết gan chưa được sử dụng rộng rãi do các nhược điểm sau:
- Xét nghiệm xâm nhập
- Giá thành cao
- Gây khó chịu cho bệnh nhân
- Nguy cơ biến chứng cao
- Có thể sai sót trong lấy mẫu
- Cần phải có bác sĩ chuyên khoa đọc kết quả
Bảng 1: Hệ thống điểm METAVIR trên sinh thiết gan
| Giai đoạn | F0 | F1 | F2 | F3 | F4 |
| Định nghĩa | Không xơ hoá | Xơ hoá khoảng cửa không có dải xơ | Xơ hóa khoảng cửa có vài dải xơ | Nhiều dải xơ nhưng chưa xơ gan | Xơ gan thật sự |
*Các test không xâm nhập (NITs - Non-invasive tests)
Bảng 2: Các test không xâm nhập đánh giá độ xơ hoá gan
| Xét nghiệm | Các thông số cần thiết | Các giai đoạn đánh giá | Yêu cầu | Giá cả |
| APRI | AST, Tiểu cầu | ≥F2, F4 (xơ gan) | Các xét nghiệm huyết học và hoá sinh cơ bản | + |
| FIB-4 | Tuổi, AST, ALT, Tiểu cầu | ≥F3 | Các xét nghiệm huyết học và hoá sinh cơ bản | + |
| FibroTest | GGT, Haptoglobulin, Bilirubin, A1 apolipoprotein, a2-macroglobulin | ≥F2, F4 (xơ gan) | Các xét nghiệm chuyên môn hoá đòi hỏi phòng thí nghiệm chuyên biệt. Đây là xét nghiệm có tính thương mại. | ++ |
| FibroScan | Đo độ đàn hồi thoáng qua | ≥F2, F4 (xơ gan) | Thiết bị chuyên dụng | +++ |
Công thức tính APRI và FIB-4
APRI = (AST/ULN x 100)/Tiểu cầu (109/L)
FIB-4 = [Tuổi (năm) x AST(IU/L)]/[Tiểu cầu (109/L) x ALT(IU/L)1/2]
Trong đó ULN là giới hạn trên giá trị bình thường của AST
Gần đây, các kĩ thuật mới đo độ xơ hoá gan được phát triển dựa trên nguyên lý của siêu âm. Với các xét nghiệm này, độ đàn hồi thoáng qua (transient elastography) được đo bởi FibroScan (Echosens, Paris). Đây là xét nghiệm không xâm nhập, tốn chưa đầy 10 phút, có thể áp dụng cho bệnh nhân ngoại trú và dễ thực hiện. Tuy nhiên, những yếu tố làm hạn chế sử dụng kĩ thuật này đó là: giá thành thiết bị cao, nhu cầu bảo trì thường xuyên và người sử dụng cần được huấn luyện cũng như thiếu các điểm cắt (cut-off) đặc hiệu cho từng giai đoạn chuyên biệt của xơ gan. Ngoài ra còn có các kĩ thuật khác như ARFI (kĩ thuật ghi hình bằng xung lực xạ âm) và kĩ thuật đo độ đàn hồi bằng sóng biến dạng (shear-wave elastography). Các kĩ thuật này sử dụng nguyên lý tương tự kĩ thuật đo độ đàn hồi thoán ua nhưng kĩ thuật phức tạp hơn FibroScan.
APRI (aspartate aminotransferase [AST]-to-platelet ratio index) là test không xâm nhập được ưu tiên để đánh giá sự hiện diện của xơ gan (chỉ số APRI>2 ở người lớn) trong điều kiện nguồn lực hạn chế. Kĩ thuật đo độ đàn hồi thoáng qua (ví dụ FibroScan) hoặc FibroTest có thể được ưu tiên nếu sẵn có và chi phí không phải là vấn đề uan trọn. (Khu ến cáo hạn chế, chất lượn bàn chứn thấp).
5 TÀI LIỆU THAM KHẢO
Guideline for the Diagnosis and Management of Nonalcoholic Fatty Liver Disease in Primary Care and Endocrinology Clinical Settings, 2022
6 BỆNH GAN MỠ KHÔNG DO RƯỢU AASLD 2018 (NAFLD - Non-Alcoholic Fatty Liver Disease)
6.1 TỔNG QUAN
Định nghĩa bệnh gan mỡ không do rượu (NAFLD) cần có:
• Bằng chứng nhiễm mỡ ở gan, dựa trên chẩn đoán hình ảnh hoặc mô học.
• Không có các nguyên nhân gây gan nhiễm mỡ thứ phát (bảng 1) như: uống nhiều rượu, dùng những thuốc gây mỡ hoá trong thời dài hoặc bệnh lí di truyền đơn gen.
Đa phần, NAFLD liên quan với các yếu tố nguy cơ (bảng 2) như béo phì, đái tháo đường, rối loạn lipid máu, các rối loạn chuyển hóa khác.
Về mô học NAFLD chia làm 2 loại gan nhiễm mỡ không do rượu (NAFL) và viêm gan mỡ không do rượu (NASH).
| NAFL | NASH | |
| Gan nhiễm mỡ (1) | + | + |
| Tổn thương tế bào gan dạng thoái hóa nước | - | + |
| Xơ hóa gan | - | +/- |
Chú thích: (1) Gan nhiễm mỡ được định nghĩa là tích luỹ chất béo trong gan vượt quá 5% trọng lượng của gan hoặc quan sát dưới kính hiển vi thấy nhiều hơn 5% số tế bào gan chứa các hạt mỡ. Trong gan nhiễm mỡ, lượng chất béo có thể chiếm đến 50% trọng lượng của gan, trong đó hơn một nửa là các Triglyceride.
Bảng 1: Nguyên nhân gây gan nhiễm mỡ thứ phát
| Nhiễm mỡ dạng túi lớn (chất béo ứ đọng trong tế bào gan tạo thành những hạt mỡ lớn làm đấy lệch nhân | Lạm dụng rượu |
| Viêm gan C (genotype 3) | |
| Bệnh Wilson | |
| Loạn dưỡng mỡ | |
| Đói kéo dài | |
| Dinh dưỡng ngoài ruột | |
| Bệnh Abetalipoproteinemia | |
| Thuốc (Amiodarone, Methotrexate, Tamoxifen, Corticosteroids) | |
| Nhiễm mỡ dạng túi nhỏ (chất béo ứ đọng trong tế bào gan tạo thành những hạt mỡ nhỏ nằm xung quanh nhân) | Hội chứng Reye |
| Thuốc (Valproate, kháng Retrovirus) | |
| Gan nhiễm mỡ cấp thai kỳ | |
| Hội chứng HELLP | |
| Bất thường bẩm sinh về chuyển hoá (thiếu LCAT, bệnh tích trữ Cholesterol ester, bệnh Wolman) |
Bảng 2: Các yếu tố nguy cơ liên quan đến NAFLD
Các yếu tố đã được công nhận
| Các yếu tố vừa được đề xuất
|
• Sinh bệnh học của NAFLD vẫn chưa được hiểu biết một cách đầy đủ. Giả thuyết được chấp nhận rộng rãi nhất hiện nay xem để kháng Insulin là cơ chế chính. Vì thế, có tác giả cho rằng NAFLD chính là biểu hiện tại gan của hội chứng chuyển hóa. Sự để kháng Insulin dẫn đến tích luỹ mỡ ở gan, làm gan nhạy cảm hơn với các tác nhân như viêm, peroxide hóa lipid, những stress oxi hóa do thiếu Sắt, leptin và chất chống oxi hóa... Ngoài ra, theo nghiên cứu của B. Orlik và cộng sự, các hormone và cytokin do tế bào mỡ tiết ra đóng vai trò trung gian giữa béo phì, để kháng Insulin và NAFLD.
• Về phương diện chẩn đoán, hầu hết bệnh nhân NAFLD không có triệu chứng đặc hiệu. Các biểu hiện có thể là mệt mỏi, khó chịu ở vùng hạ sườn phải hay gan lớn.
- Trong các xét nghiệm thường qui, men gan tăng ở khoảng 90% bệnh nhân NAFLD nhưng Phosphatase kiếm và Bilirubin thường trong giới hạn cho phép. Tuy nhiên, men gan bình thường không loại trừ NAFLD. Theo H.Rodriguez- Hernandez, có thể nhận biết sớm NAFLD dựa vào đường máu, mỡ máu tăng hoặc tỷ AST/ALT >1.
- Siêu âm: có thể cho hình ảnh tăng âm hơn do tế bào gan nhiễm mỡ, nhưng hoàn toàn không đặc hiệu, vì vậy, đây là phương tiện góp phần sàng lọc bệnh chứ không phải là tiêu chuẩn chẩn đoán.
- CT-scan và MRI: có giá trị trong xác định tình trạng nhiễm mỡ nhưng lại không khảo sát được hiện tượng viêm hay xơ hóa. Sinh thiết gan: là tiêu chuẩn chẩn đoán xác định NAFLD. Tuy nhiên, đây là xét nghiệm xâm nhập và không phải cơ sở nào cũng làm được nên trong thực tế lâm sàng có thể dùng các dấu hiệu lâm sàng cũng như một số xét nghiệm cận lâm sàng gợi ý như đã đề cập ở trên để chẩn đoán sàng lọc NAFLD.
6.2 HƯỚNG DẪN CHẨN ĐOÁN VÀ ĐIỀU TRỊ NAFLD THEO AASLD 2018
NAFLD và lượng rượu tiêu thụ
1.NAFLD xảy ra ở các bệnh nhân không có tiền sử sử dụng rượu đáng kể (>21 drinks/tuần đối với nam và >14 drinks/tuần đối với nữ). (1 drink ~ 14 g Ethanol)
2. Bệnh nhân có kết quả gan nhiễm mỡ rõ ràng trên chẩn đoán hình ảnh nếu có triệu chứng cơ năng, thực thể của bệnh lý gan hoặc xét nghiệm sinh hóa bất thường, nên nghĩ đến bệnh gan nhiễm mỡ không do rượu và cần được đánh giá kĩ lưỡng hơn.
Sàng lọc NAFLD tại phòng khám sức khỏe ban đầu
3. Bệnh nhân có kết quả gan nhiễm mỡ rõ ràng trên chẩn đoán hình ảnh nhưng không có bất kì triệu chứng của bệnh gan đồng thời có xét nghiệm sinh hóa bình thường, thì cũng nên đánh giá các yếu tố nguy cơ chuyển hóa như béo phì, rối loạn dung nạp Glucose, rối loạn Triglycerid, và các nguyên nhân gây nhiễm mỡ gan khác như sử dụng rượu quá mức hoặc do thuốc.
4. Tại thời điểm hiện tại, sàng lọc thường quy NAFLD ở bệnh nhân nguy cơ cao như béo phì và đái tháo đường vẫn không được khuyến cáo vì các xét nghiệm chẩn đoán và lựa chọn điều tri còn chưa rõ ràng, cùng với việc thiếu bằng chứng về lợi ích lâu dài, chi phí và hiệu quả của sàng lọc.
5. Bệnh nhân đái tháo đường type 2 có nguy cơ cao bị NAFLD và NASH. Thang điểm NFS hoặc xơ hóa-4 (FIB-4) hoặc siêu âm đàn hồi VCTE (vibration controlled transient elastography) có thể được sử dụng để xác định nguy cơ xơ hóa tiến triển (xơ hóa bắc cầu hoặc xơ gan).
Sàng lọc các thành viên trong gia đình
6. Không khuyến cáo sàng lọc có tính hệ thống cho các thành viên trong gia đình bệnh nhân bị NAFLD.
Đánh giá ban đầu ở bệnh nhân nghi ngờ NAFLD
7. Khi đánh giá một bệnh nhân nghi ngờ NAFLD, cần loại trừ các nguyên nhân gây gan nhiễm mỡ khác và các bệnh gan mạn tính phối hợp thường gặp. 8. Ở bệnh nhân có Ferritin huyết thanh tăng cao, kéo dài và tăng độ bão hòa sắt, nhất là trong trường hợp có đột biến đồng hợp từ hoặc dị hợp tử C282Y HFE, chỉ định sinh thiết gan nên được xem xét
9. Nếu tự kháng thể có hiệu giá huyết thanh cao cùng với các đặc điểm khác gợi ý bệnh gan tự miễn (Aminotransferases rất cao >5 lần, Globulin cao, hoặc tỉ protein toàn phần/albumin cao) cần phải nhanh chóng làm rõ chẩn đoán bệnh gan tự miễn.
10. Trong đánh giá ban đầu bệnh nhân nghi ngờ NAFLD, nên xem xét kĩ lưỡng sự hiện diện của các bệnh đi kèm thường gặp như béo phì, rối loạn lipid máu, tình trạng đề kháng Insulin, đái tháo đường, suy giáp, hội chứng buồng trứng đa nang và ngưng thở khi ngủ.
Các test không xâm lấn tình trạng viêm gan nhiễm mỡ và xơ hóa gan tiến triển trong NAFLD
11. Vì hội chứng chuyển hóa là một dự báo cho viêm gan nhiễm mỡ ở bệnh nhân NAFLD nên sự hiện diện của nó có thể được sử dụng để chỉ định sinh thiết gan cho bệnh nhân.
12. Thang điểm xơ hóa NAFLD (NAFLD Fibrosis Score) hoặc chỉ số FIB-4 là những công cụ lâm sàng hữu ích dùng để xác định bệnh nhân NAFLD có khả năng cao có cầu xơ (F3) và/hoặc xơ gan (F4).
13.VCTE hoặc MRE là những công cụ hữu ích để xác nhận tình trạng xơ hóa gan tiến triển ở bệnh nhân NAFLD.
Khi nào tiến hành sinh thiết gan ở bệnh nhân NAFLD
14. Sinh thiết gan nên được xem xét ở những bệnh nhân NAFLD có nguy cơ cao với viêm gan nhiễm mỡ và xơ hóa tiến triển.
15. Sự hiện diện của hội chứng chuyển hóa, thang điểm xơ hóa NAFLD, chỉ số FIB-4, độ cứng gan trên VCTE hoặc MRE có thể được sử dụng để xác định nguy cơ bị viêm gan nhiễm mỡ và xơ hóa tiến triển trên bệnh nhân.
16. Sinh thiết gan cần được xem xét ở những bệnh nhân nghi ngờ NAFLD mà không thể loại trừ các nguyên nhân gây nhiễm mỡ gan khác cũng như các bệnh gan mạn tính phối hợp.
Mô bệnh học của NAFLD ở người lớn
17. Kết quả đọc mô bệnh học được xem là có gía trị trên lâm sàng khi phân biệt NAFL (gan nhiễm mỡ), hay NASH (gan nhiễm mỡ, viêm thùy gan, khoảng cửa và thoái hóa gan dạng bóng nước) và đánh giá mức độ nặng (nhẹ, trung bình hoặc nặng) Các thang điểm như NAS và/hoặc SAF có thể được sử dụng.
18. Sự hiện diện hay vắng mặt của xơ hóa phải được mô tả. Nếu có, nên mô tả rõ hơn về vị trí, số lượng và sự tái cấu trúc nhu mô gan.
6.3 ĐIỀU TRỊ NAFLD
Những đối tượng nào nên được điều trị?
19. Điều trị NAFLD bao gồm điều trị bệnh gan cũng như các rối loạn chuyển hóa liên quan như béo phì, tăng lipid máu, đề kháng Insulin và đái tháo đường type 2. Bệnh nhân bị NAFLD mà không có NASH và xơ hóa đều có tiên lượng tốt. Điều trị bằng thuốc nhằm chủ yếu cải thiện mô bệnh học gan nói chung nên được giới hạn ở những người bị NASH và xơ hóa được chứng minh bằng sinh thiết.
Thay đổi lối sống
20. Nhìn chung, giảm cân bằng cách giảm cung cấp năng lượng đơn thuần hoặc kết hợp với tăng hoạt động thể lực giúp làm giảm quá trình nhiễm mỡ gan. Kết hợp chế độ ăn giảm calo (mỗi ngày giảm 500-1000 kcal) với hoạt động thể lực trung bình giúp giảm cân hiệu quả, ổn định.
21. Giảm ít nhất 3-5% trọng lượng cơ thể là cần thiết để cải thiện tình trạng nhiễm mỡ và giảm cân nhiều hơn (lên đến 10%) là cần thiết để cải thiện phần lớn các đặc điểm mô bệnh học của NASH, bao gồm cả xơ gan.
22. Hoạt động thể lực đơn thuần ở người lớn bị NAFLD có thể ngăn ngừa hoặc giảm được tình trạng gan nhiễm mỡ nhưng khả năng cải thiện các khía cạnh khác về mô học gan vẫn còn chưa rõ.
Các thuốc tăng nhạy cảm insulin
Metformin
23. Metformin không có hiệu quả đáng kể trên mô học gan và không được khuyến cáo điều trị đặc hiệu cho người lớn bị viêm gan mỡ không do rượu (NASH).
Thiazolidinediones
24. Pioglitazone cải thiện mô học gan ở bệnh nhân có hoặc không có đái tháo đường type 2 được chẩn đoán NASH trên sinh thiết, do đó nên được sử dụng cho những đối tượng này. Nguy cơ và lợi ích nên nên được thảo luận với từng bệnh nhân. (liều Pioglitazone trong nghiên cứu ở bệnh nhân không đái đường là 30 mg/ngày)
25. Cho đến khi có các bằng chứng mới về tính an toàn và hiệu quả, Pioglitazone không nên được sử dụng cho bệnh nhân NAFLD mà không có NASH trên sinh thiết.
Thuốc đồng vận GLP1
26. Là quá sớm để xem GLP1 là thuốc điều trị đặc hiệu bệnh gan trên bệnh nhân NAFLD hoặc NASH
Trong nghiên cứu LEAN (ngẫu nhiên đa trung tâm, mù đôi, so sánh với giả dược pha 2) được công bố gần đây (2016) trên 52 bệnh nhân bị NASH đã được chứng minh bằng sinh thiết, Liraglutide tiêm dưới da mỗi ngày một lần trong 48 tuần có liên quan đến cải thiện viêm gan nhiễm mỡ cao hơn và ít tiến triển xơ hóa hơn, tuy nhiên, Liraglutide có liên quan đến giảm cân nhiều hơn, cũng có tác dụng phụ tiêu hóa nhiều hơn
Vitamin E
27. Vitamin E (a-tocopherol) liều 800 IU/ngày có tác dụng cải thiện mô học gan ở những bệnh nhân NASH (được chẩn đoán xác định bằng sinh thiết) không kèm đái tháo đường, do đó nên được xem xét là phương pháp điều trị cho nhóm bệnh nhân này. Lợi ích và nguy cơ nên được thảo luận với bệnh nhân trước khi điều trị.
28. Cho đến khi có bằng chứng mới về tính hiệu quả, Vitamin E không được khuyến cáo điều trị cho bệnh nhân NASH có đái tháo đường, NAFLD không có sinh thiết gan, xơ gan do NASH hoặc xơ gan không rõ nguyên nhân.
Phẫu thuật giảm cân
29. Phẫu thuật giảm cân cắt bỏ ruột trước (foregut bariatric surgery) có thể được xem xét ở những người béo phì mắc NAFLD hoặc NASH và thỏa các tiêu chuẩn khác của phẫu thuật.
30. Là quá sớm để xem phẫu thuật giảm cân cắt bỏ ruột trước là phương pháp đặc hiệu để điều trị NASH.
31. Sự an toàn và hiệu quả của phẫu thuật giảm cân cũng như loại phẫu thuật nào nên được ưu tiên chỉ định ở người béo phì có xơ gan do NAFLD và thỏa các tiêu chuẩn khác của phẫu thuật giảm cân chưa được chứng minh. Ở những bệnh nhân NASH còn bù hoặc xơ gan không rõ nguyên nhân, phẫu thuật giảm cân có thể được xem xét trên từng trường hợp cụ thể, nên được thực hiện bởi phẫu thuật viên giàu kinh nghiệm.
Ursodeoxycholic Acid, Omega-3
32. Ursodeoxycholic acid (UDCA) không được khuyến cáo trong điều trị NAFLD và NASH.
33. Acid béo Omega-3 không nên được sử dụng như là thuốc điều trị đặc hiệu NAFLD hay NASH nhưng chúng có thể được cân nhắc để điều trị tăng Triglyceride máu ở bệnh nhân NAFLD.
Vấn để sử dụng rượu
34. Bệnh nhân bị NAFLD không nên uống nhiều rượu. (24 drink/ ngày hoặc >14 drink/ tuần ở nam, ≥3 drink/ngày hoặc 7 drink/ngày ở nữ)
35. Hiện không đủ dữ liệu để khuyến cáo sử dụng lượng rượu ít hơn (<1 drink/ngày) ở bệnh nhân NAFLD.
Điều trị bệnh lí tim mạch và rối loạn lipid máu
36. Bệnh nhân NAFLD có nguy cơ cao mắc bệnh lí tim mạch, do đó nên tầm soát và điều chỉnh các yếu tố nguy cơ tim mạch ở tất cả bệnh nhân NAFLD.
37. Bệnh nhân bị NAFLD hoặc NASH không phải là đối tượng nguy cơ cao của tổn thương gan do Statin, do đó Statin có thể được sử dụng để điều trị rối loạn lipid máu ở bệnh nhân NAFLD hoặc NASH. Tuy nhiên, ở những bệnh nhân xơ gan do NASH, chỉ dùng Statin khi xơ gan còn bù.
Các thuốc khác
38. Cho tới khi có bằng chứng về hiệu quả, tính an toàn, Obeticholic acid không được khuyến cáo để điều trị NASH.
NASH, béo phì, ghép gan
39. Bệnh nhân xơ gan do NASH có tỉ lệ cao mắc bệnh lí tim mạch (biểu hiện lâm sàng có thể rõ hoặc không), do đó phải đánh giá kĩ lưỡng trong suốt quá trình ghép gan.
Một số khuyến cáo khác trên thực hành lâm sàng:
40. Bệnh nhân xơ gan do NASH nên được đánh giá tình trạng giãn tĩnh mạch dạ dày - thực quản dựa theo khuyến cáo AASLD/ACG
41. Bệnh nhân xơ gan nghi do NASH nên được theo dõi nguy cơ mắc HCC (ung thư biểu mô tế bào gan) dựa theo khuyến cáo AASLD/ACG.
42. Bằng chứng hiện tại không ủng hộ tầm soát và theo dõi HCC ở bệnh nhân không có xơ gan do NASH.
43. Bằng chứng hiện tại không ủng hộ việc thực hiện sinh thiết gan thường xuyên ở bệnh nhân NAFL hay NASH, nhưng có thể xem xét tùy từng tình huống cụ thé.
NAFLD ở trẻ em
44. Trẻ em bị gan nhiễm mỡ khi còn rất nhỏ hoặc khi không thừa cân nên được kiểm tra những nguyên nhân di truyền đơn gen của các bệnh gan mạn như những khiếm khuyết oxy hóa acid béo, bệnh dự trữ Lysosom và những rối loạn thế Peroxisome, thêm vào đó là những nguyên nhân đã đề cập đến ở phần NAFLD người lớn.
45. Tự kháng thể thường xuất hiện với hiệu giá thấp trong huyết thanh ở những trẻ em mắc NAFLD. Nếu có hiệu giá cao hơn, đặc biệt khi có sự gia tăng của aminotransferases,globulin trong huyết thanh, ti protein toàn phần/albumin nên cân nhắc sinh thiết gan để xác định bệnh viêm gan tự miễn và các bệnh lí tự miễn liên quan.
46. Vì có rất ít bằng chứng nên không thể đưa ra khuyến cáo chính thức về việc sàng lọc NAFLD ở những trẻ em thừa cân và béo phì.
Khi nào cần sinh thiết gan ở bệnh nhi NAFLD:
47. Sinh thiết gan ở những trẻ em có nghi ngờ NAFLD nên được thực hiện khi chẩn đoán chưa rõ ràng, khi có nhiều chẩn đoán có khả năng hay trước khi bắt đầu các liệu pháp điều trị có khả năng gây độc cho gan.
48. Thực hiện sinh thiết gan trước khi sử dụng thuốc điều trị NASH.
49. Các nhà giải phẫu bệnh nên dựa vào mẫu mô bệnh học đặc hiệu thường gặp ở trẻ em để đối chiếu nhằm tránh chẩn đoán sai NAFLD ở trẻ em.
Điều trị NAFLD ở trẻ em:
50. Lựa chọn hàng đầu là tích cực thay đổi lối sống. Điều này giúp cải thiện men gan và tình trạng mô học của gan ở trẻ bị NAFLD.
51. Metformin 500 mg với liều hai lần mỗi ngày không cho thấy hiệu quả ở trẻ em bị NAFLD, do đó không nên được chỉ định. Tác dụng của Metformin liều cao chưa được biết đến.
52. Vitamin E 800 IU/ngày (RRR a-tocopherol) giúp cải thiện về mặt mô học ở những trẻ bị NASH đã được khẳng định bằng sinh thiết. Độ an toàn của sử dụng vitamin E liều cao thời gian dài ở trẻ em vẫn chưa rõ. Do đó vitamin E có thể được sử dụng ở trẻ em, nhưng nguy cơ và lợi ích nên được xem xét.
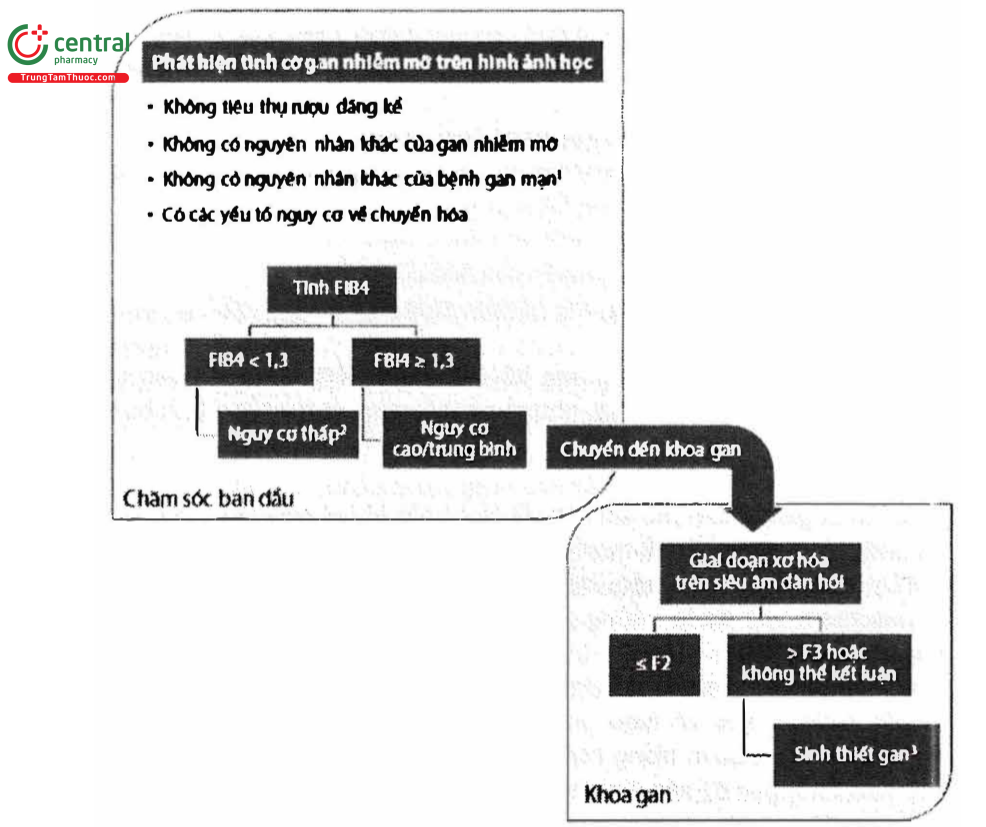
Chú thích:
1 Nên thực hiện xét nghiệm huyết thanh HBV và HCV ở cơ sở chăm sóc ban đầu, các bước tiếp theo được khoa gan điều chỉnh cho phù hợp với từng bệnh nhân. Lưu ý rằng NAFLD có thể đồng mắc với các bệnh gan mãn tính khác.
2 Chưa có khuyến cáo theo dõi bệnh nhân NAFLD tối ưu dựa trên bằng chứng. EASL khuyến cáo theo dõi những bệnh nhân có nguy cơ thấp mắc NAFLD mà không có tình trạng xấu đi của các yếu tố nguy cơ chuyển hóa sau mỗi 2 đến 3 năm.
3 Nên xem xét sinh thiết ở những bệnh nhân tăng số lượng bệnh chuyển hóa (những người có nguy cơ cao viêm gan nhiễm mỡ).
Bảng 3: ĐIỂM GIỐNG VÀ KHÁC NHAU GIỮA CÁC HƯỚNG DẪN CỦA CHÂU ÂU, CHÂU Á VÀ HOA KỲ
| AASLD (2018) | EASL (2016) | Asia-Pacific (2017) | |
| Định nghĩa mức tiêu thụ rượu đáng kể | - Nam: 21 ly tiêu chuẩn/tuần hoặc 294 g/tuần - Nữ: 14 ly tiêu chuẩn/tuần hoặc 196 g/tuần | - Nam: 30 g/ngày - Nữ: 20 g/ngày | - Nam: 2 ly tiêu chuẩn / ngày hoặc 140 g/tuần - Nữ: 1 ly tiêu chuẩn/ngày hoặc 70 g/tuần |
| Sàng lọc NAFLD | Không khuyến cáo sàng lọc trong cộng đồng | ||
- Khuyến cáo không nên sàng lọc ngay cả ở những nhóm dân số có nguy cơ cao vì thiếu phương pháp điều trị bằng thuốc hiệu quả, phân tích hiệu quả chi phí và lợi ích lâu dài không rõ ràng đối với việc sàng lọc - "Chỉ số nghi ngờ cao" cho NAFLD được khuyến cáo cho bệnh nhân ĐTĐ type 2. | - Khuyến cáo sàng lọc ở bệnh nhân - Khuyến cáo sàng lọc ở bệnh nhân có men gan bất thường kéo dài (A1) | - Xem xét sàng lọc ở bệnh nhân béo phì hoặc ĐTĐ type 2 (B2) | |
| Đánh giá xơ hóa | - Chỉ số xơ hóa NAFLD (NFS), FIB-4, và siêu âm đàn hồi - Không khuyến cáo trình tự các xét nghiệm ưu tiên đánh giá xơ hóa | - Chỉ số xơ hóa NAFLD (NFS) và FIB- 4 để phân tầng nhóm nguy cơ thấp so với nhóm trung bình/cao đối với xơ hóa gan có ý nghĩa. - Chuyến tuyến tới khoa gan cho những bệnh nhân có nguy cơ trung bình/cao để làm xét nghiệm thêm bằng kỹ thuật đo độ đàn hồi và xác định những người cần sinh thiết gan | - Không khuyến cáo trình tự các xét nghiệm ưu tiên đánh giá xơ hóa |
Sinh thiết gan vẫn là tiêu chuẩn vàng để phân biệt NAFL với NASH và giai đoạn xơ hóa gan. Tiến hành sinh thiết gan nếu: (1) nghi ngờ bệnh NAFLD có xơ hóa tiến triển (2) hoặc lo lắng về căn nguyên bệnh gan mãn tính đang cùng tồn tại hoặc cạnh tranh (B2). | |||
| Can thiệp lối sống | Mục tiêu giảm cân từ 7% đến 10% trọng lượng cơ thể (B1). Giảm 500-1000 calo mỗi ngày và tập thể dục cường độ vừa phải, hơn là xây dựng một chương trình giảm cân (C2). | ||
| Không có khuyến cáo cụ thể nào liên quan đến chế độ dinh dưỡng đa lượng (macronutrient diets) hoặc chế độ luyện tập | Chế độ ăn địa trung hải, tránh thức ăn chế biến sẵn và thêm đường Fructose (B1) | Không có khuyến cáo cụ thể nào liên quan đến chế độ dinh dưỡng đa lượng (macronutrient diets) hoặc chế độ luyện tập | |
| Điều trị bằng thuốc | Hiện không có loại thuốc nào được chấp thuận để điều trị NAFLD hoặc NASH. Tuy nhiên, nhiều thuốc đang thử nghiệm giai đoạn 3. Bệnh nhân có chỉ định statins trong các bệnh lí tim mạch thì có thể sử dụng an toàn ở bệnh nhân NASH và xơ gan còn bù (B1) | ||
- Vitamin E 800 IU mỗi ngày có thể được xem xét ở bệnh nhân không mắc ĐTĐ có NASH (được chứng minh bằng sinh thiết mà không có xơ gan) - Pioglitazone 30 mg mỗi ngày có thể được xem xét ở bệnh nhân NASH (được chứng minh bằng sinh thiết) có hoặc không có ĐTĐ type 2 | - Cần điều trị bằng thuốc cho nhóm bệnh nhân NASH có xơ hóa (giai đoạn F2 trở lên) hoặc NASH có nguy cơ cao tiến triển bệnh (ĐTĐ type 2, hội chuyến chứng hóa, tăng ALT) ( B1 ) - Không có khuyến mãi nào hỗ trợ mạnh về việc sử dụng pioglitazone hoặc vitamin E ( B2 ) | - Pioglitazone chỉ khuyến khích sử dụng trong thời gian ngắn ở bệnh nhân NASH ma tiền chiết rút đường hoặc chiết rút đường ( B2 ) - Không có quảng cáo nào hỗ trợ việc sử dụng vitamin E do không đủ bằng chứng ( A2 ) | |
Ly tiêu chuẩn (đồ uống tiêu chuẩn): ~ 14 g Ethanol LỚP, mức thưởng, được liệt kê trong khung đơn. | |||
7 KẾT LUẬN
NAFLD là bệnh lí ngày càng phổ biến. Cơ chế bệnh sinh chưa rõ ràng, tuy nhiên dựa trên những hiểu biết mới về bệnh sinh học và kết quả của một số thử nghiệm lâm sàng sẵn có, nhiều biện pháp điều trị đã được áp dụng cho bệnh nhân và bước đầu đã mang lại một định nghĩa số kết quả tối đa, nhưng cho đến nay vẫn chưa có một bản phác thảo thực sự nào có kết quả hiệu quả về lâu dài. Trong thực tế, việc điều trị cần phối hợp nhiều yếu tố trong đó việc điều chỉnh các bệnh lý nền và thay đổi lối sống đóng vai trò khá quan trọng. Vì thế cần có nhiều nghiên cứu sâu hơn nữa về NAFLD.
8 TÀI LIỆU THAM KHẢO CHÍNH
1. Chẩn đoán và quản lý bệnh gan nhiễm mỡ không do rượu: Hướng dẫn thực hành của Hiệp hội nghiên cứu bệnh gan Hoa Kỳ 2018
2. Bệnh gan nhiễm mỡ không do rượu và những cập nhật hướng dẫn gần đây Yumi Ando, MD,* và Janice H. Jou, MD, MHS, Nhận được ngày 6 tháng 5 năm 2020; được chấp nhận vào ngày 20 tháng 9 năm 2020.

