Đại cương về nội tiết sinh sản, cơ chế hoạt động của hormone sinh dục

Đại học Huế - Trường ĐH Y Dược
Đồng chủ biên
GS.TS. Nguyễn Vũ Quốc Huy
GS.TS. Cao Ngọc Thành
PGS.TS. Lê Minh Tâm
PGS.TS. Trương Thành Vinh
Cùng nhiều tác giả tham gia biên soạn.
1 ĐẠI CƯƠNG
Nội tiết phụ khoa là một ngành học về nội tiết tố và các yếu tố thần kinh nội tiết được tạo ra bởi các mô cơ quan sinh sản. Các mô cơ quan này bao gồm vùng dưới đồi, thùy trước tuyến yên, buồng trứng, nội mạc tử cung và bánh nhau.
Nội tiết tố kinh điển được xem là một sản phẩm tế bào được chế tiết vào tuần hoàn ngoại biên và đến tác động vào cơ quan đích ở xa. Đây được gọi là sự chế tiết nội tiết. Ngoài ra, còn có dạng tác động tế bào – tế bào rất quan trọng trong sinh lý sinh sản.
Tác động cận tiết thường thấy ở buồng trứng liên quan đến sự trao đổi các tín hiệu hóa học giữa các tế bào lân cận.
Tự tiết xảy ra khi một tế bào giải phóng các chất ra ngoài để tác động lên chính nó.
Khi tế bào sản xuất các chất để tác động lên chính nó trước khi tiết ra ngoài thì gọi là tác động nội tại.
2 TRỤC DƯỚI ĐỒI – TUYẾN YÊN – BUỒNG TRỨNG
2.1 Vùng dưới đồi
2.1.1 Giải phẫu học
Vùng dưới đồi (vùng dưới đồi) là một cấu trúc thần kinh nhỏ, nằm ở sàn não, trên giao thoa thị và dưới não thất ba. Về mặt giải phẫu nó được chia làm 3 vùng: vùng quanh não thất, vùng giữa và vùng bên. Do không có sự liên kết thần kinh trực tiếp với tuyến yên, nên để tác động lên tuyến yên, vùng dưới đồi cần có một phương tiện liên kết. Máu cung cấp cho thùy trước tuyến yên xuất phát từ các mao mạch có rất nhiều ở trung tâm hạ đồi. Các mạch máu trên tuyến yến tạo thành mạng mao mạch dày đặc rồi chảy vào hệ thống cửa đi xuống, vào thùy trước tuyến yên. Những can thiệp làm ảnh hưởng đến tuần hoàn cửa sẽ làm bất hoạt và teo tuyến sinh dục cùng với sự giảm hoạt động tuyến giáp và tuyến thượng thận. Dòng chảy của máu trong tuần hoàn cửa là từ não đến tuyến yên, nhưng người ta nhận thấy có sự chảy ngược trở lại, nhờ đó các hormon tuyến yên có thể tác động trực tiếp lên vùng dưới đồi tạo thành cơ chế điều hòa ngược vùng dưới đồi chủ yếu chế tiết các yếu tố giải phóng tuyến yên:
Gonadotropin - releasing hormone (GnRH) kiểm soát việc chế tiết Luteinizing hormone (LH) và Follicle stimulating hormone (FSH).
Corticotropin - releasing hormone (CRF) kiểm soát việc giải phóng adrenocorticotropic hormone (ACTH).
Grouth hormone - releasing hormone (GH-RH) điều hòa sự giải phóng Growth hormone (GH).
Thyrotropin - releasing hormone (TRH) điều hòa sự chế tiết thyroid - stimulating hormone (TSH).

2.1.2 Hoạt động nội tiết vùng dưới đồi
Gonadotropin-releasing hormone (GnRH):
GnRH là một peptit nhỏ gồm mười amino acids (decapeptide) theo thứ tự:

Các tế bào sản xuất GnRH xuất phát từ vùng khứu giác. Trong thời kỳ hình thành phôi, các tế bào này di chuyển theo các thần kinh sọ nối mũi và não trước với vị trí ban đầu của chúng, có đến 1.000-3.000 tế bào sản xuất GnRH tìm thấy trong nhân vùng dưới đồi.
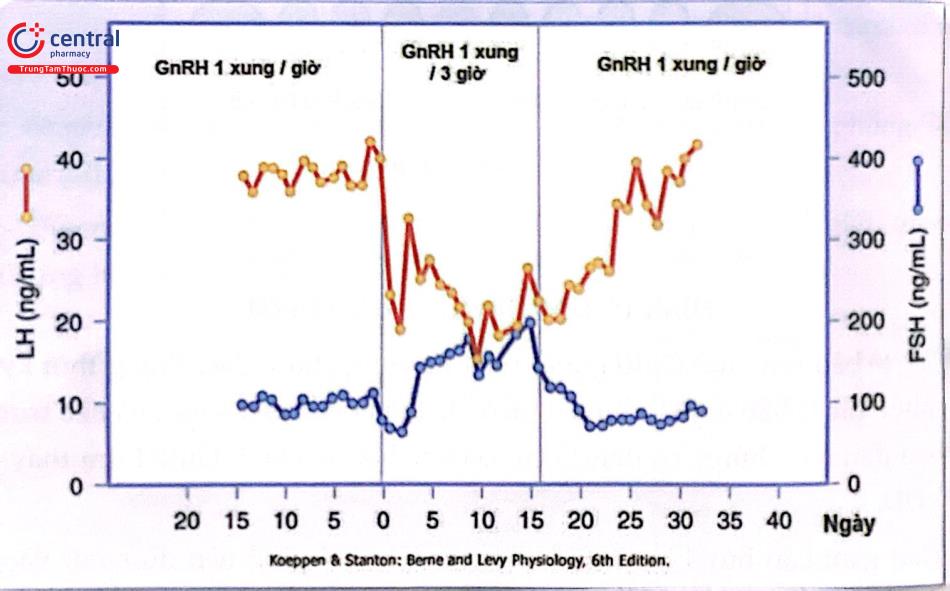
Thời gian bán hủy của GnRH rất ngắn, chỉ 2-4 phút nên dù có đi vào tuần hoàn ngoại biên nhưng tác động về mặt sinh lý của GnRH cũng chỉ giới hạn ở hệ thống cửa. Người ta đã chứng minh được rằng sự chế tiết gonadotropin bình thường cần có sự chế tiết GnRH theo dạng xung trong phạm vi tần số và cường độ nhất định. Phạm vi này khá hẹp. Khi tiêm GnRH 1mg/phút trong 6 phút tạo ra trong tuần hoàn của nồng độ tương đương nồng độ đỉnh ở tuần hoàn của ở người. Tăng tần số 2-5 nhịp/giờ sẽ ngăn chặn tiết gonadotropin, kết quả tương tự khi tăng liều GnRH. Việc tẩm nhuận liên tục với GnRH của tế bào gonadotrope của tuyến yên sẽ dẫn đến hiện tượng điều hòa giảm, do không chỉ giảm thụ thể của GnRH ở bề mặt tế bào mà còn làm trợ hóa và không gắn kết của các thụ thể.

Ở pha nang noãn sự chế tiết dạng xung dày hơn nhưng cường độ thấp hơn so với pha hoàng thể. Cần lưu ý rằng, các giá trị này không hằng định,
2.2 Tuyến yên
2.2.1 Giải phẫu
Tuyến yên là một cấu trúc gồm 3 thùy: Thùy trước, thùy giữa và thủy sau, nằm trong hố tuyến yên. Thùy trước tuyến yên tự nó không có hệ thống cấp máu trực tiếp. Nguồn cấp máu chủ yếu là nguồn mạch của vùng dưới đồi - tuyến yên.
Thùy sau tuyến yên chỉ gồm các mô thần kinh, là sự kéo dài trực tiếp của vùng dưới đồi. Nó nằm sát với thùy trước tuyến yên nhưng khác biệt về mặt phôi thai học, xuất phát từ chỗ lõm của mô ngoại bì thần kinh ở não thất ba. Những sợi trục của thùy sau tuyến yên xuất phát từ các neurone có thân tế bào nằm ở hai vùng riêng biệt ở vùng dưới đồi, nhân trên thị và nhân cạnh não thất.
2.2.2 Hoạt động nội tiết
2.2.2.1 Thùy trước tuyến yên
Thùy trước tuyến yên chịu trách nhiệm chế tiết các yếu tố giải phóng hormone chính: FSH, LH, TSH và ACTH cũng như GH và prolactin. Mỗi hormone được giải phóng bởi các loại tế bào tuyến yên đặc hiệu.

Gonadotropin
FSH và LH được chế tiết bởi các tế bào gonadotropin thủy trước tuyến yên và chịu trách nhiệm cho sự phát triển nang noãn. Về mặt cấu trúc FSH và LH khá tương tự nhau, chúng đều là các glycoprotein với tiểu đơn vị a giống nhau và chỉ khác nhau ở tiểu đơn vị B có tính đặc hiệu thụ thể.
Follicular stimulating hormone (FSH, follitropin): Hormone kích thích nang noãn ở người là một glycoprotein trọng lượng xấp xỉ 30.000 daltons. Tiểu đơn vị a của FSH chứa 92 amino acids và tương tự với tiểu đơn vị a của LH, hCG và TSH. Tiểu đơn vị B của TSH là duy nhất và tạo nên tính đặc hiệu về mặt chức năng và về tính miễn dịch của nó.
FSH kích thích sự phát triển nang noãn trong buồng trứng. Cả FSH và LH được chế tiết dạng xung. Đợt xung của FSH ít rõ hơn so với của LH. Sự giải phóng FSH và LH từ tuyến yên chịu sự kiểm soát điều hòa ngược âm tính bởi tuyến sinh dục. Nồng độ FSH lưu hành trong tuần hoàn thay đổi trong chu kỳ kinh nguyệt đáp ứng lại nồng độ estradiol và progesterone.
Luteinizing hormone (LH, lutropin): Hormone hoàng thể ở người là một glycoprotein có trọng lượng phân tử xấp xỉ 30.000 daltons. Tiểu đơn vị a của LH chúa 92 amino acids tương tự như tiểu đơn vị a của FSH, hCG và TSH. Tiểu đơn vị B của LH chứa 112 aminoacid và khá khác biệt so với FSH và TSH.
LH được chế tiết bởi các tế bào hướng sinh dục ở tuyến yên đáp ứng lại hormone giải phóng hướng sinh dục (GnRH) từ vùng dưới đồi. Ngay trước khi có đỉnh LH giữa chu kỳ, steroid buồng trứng, đặc biệt là estradiol, gây điều hòa ngược dương tỉnh lên sự giải phóng LH.
Việc xác định nồng độ LH cần thiết cho việc dự đoán phóng noãn và để chẩn đoán các rối loạn chức năng tuyến yên - buồng trứng. Tăng nồng độ LH dẫn đến phóng noãn và là thời điểm quan trọng trong điều trị vô sinh - thời điểm giao hợp, bơm tinh trùng hay chọc hút noãn làm thụ tinh trong ống nghiệm.
Prolactin
Prolactin là một polypeptid gồm 198 Amino acid do các tế bào lactotroph thùy trước tuyến yên tiết ra, có tác dụng kích thích sự sinh sữa ở vú. Sự sản xuất prolactin chịu sự kiểm soát ức chế do sự chế tiết dopamine ở vùng dưới đồi. Về mặt lâm sàng nghi ngờ tình trạng bất thường khi nồng độ prolactin tăng kết hợp với vô kinh và tiết sữa.
Mặc dù prolactin chịu sự ức chế thường xuyên, nhưng nhiều yếu tố kích thích có thể giải phóng nó như kích thích ở vú, thuốc, stress, hoạt động thể lực, một số thức ăn.
Thyroid stimulating hormone, adrenocorticotropic hormone, growth hormone
Các hormon khác được sản xuất ở thùy trước tuyến yên gồm TSH, ACTH và GH. TSH được các tế bào thyrotrop tuyến yên chế tiết đáp ứng với TRH. Cũng như GnRH, TRH được tổng hợp ban đầu ở nhân cùng của vùng dưới đồi và rồi chế tiết vào tuần hoàn cửa đi đến tuyến yên. Bên cạnh việc kích thích giải phóng TSH, TRH còn kích thích giải phóng prolactin. TSH kích thích tuyến giáp chế tiết T3 và T4 và chúng lại có tác động điều hòa ngược âm tính lên sự chế tiết TSH tuyến yên. Các bất thường chế tiết của tuyến giáp (cường giáp hay nhược giáp) thường kết hợp với rối loạn phóng noãn do thay đổi hoạt động trục dưới đồi – tuyến yên – buồng trứng.
ACTH được chế tiết do đáp ứng với CRH, kích thích giải phóng glucocorticoid tuyến thượng thận. Không giống các hormon khác của thùy trước tuyến yên, sự chế tiết ACTH thay đổi theo nhịp ngày đêm, đạt đỉnh vào sáng sớm và thấp nhất vào cuối đêm. Cũng như những hormone tuyến yên khác, sự chế tiết ACTH được điều hòa bằng cơ chế điều hòa ngược âm tính của sản phẩm đích cortisol.
2.2.2.2 Thùy sau tuyến yên
Các tế bào thần kinh chế tiết của vùng dưới đồi
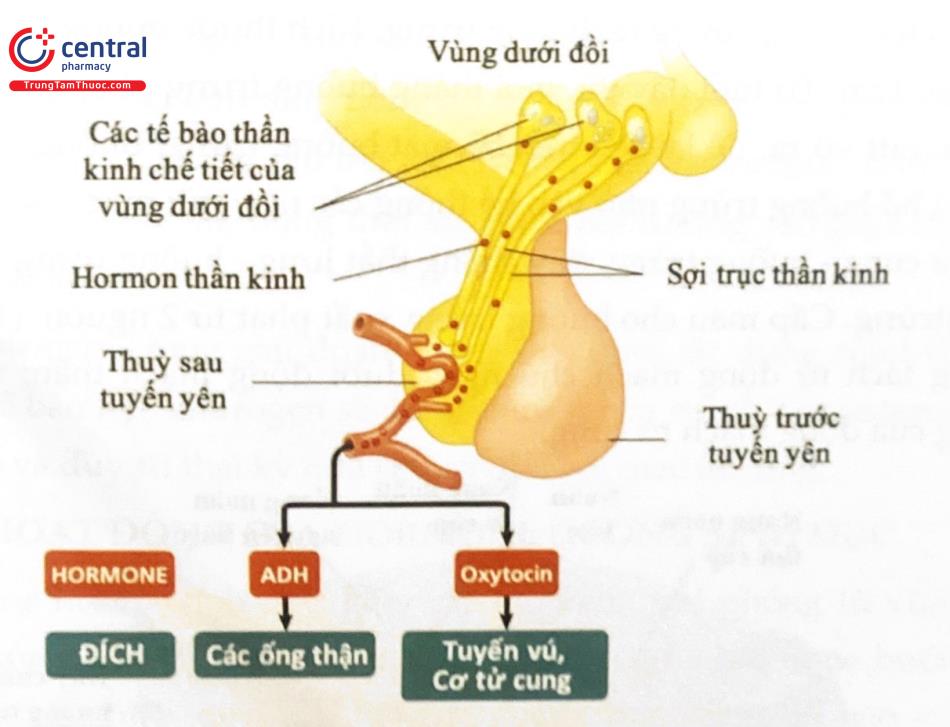
Oxytocin là một peptid gồm 9 amino acid được chế tiết ở nhân cạnh não thất của vùng dưới đồi. Ở người hormone này kích thích hai loại co cơ đặc hiệu. Thứ nhất là có cơ tử cung, xảy ra trong chuyển dạ. Thứ hai là co cơ biểu mô ống dẫn sữa xảy ra trong phản xạ xuống sữa. Sự giải phóng oxytocin được kích thích bởi động tác mút, sự kích thích núm vú được truyền theo thần kinh ngực vào tủy sống rồi đến vùng dưới đồi, ở đó oxytocin được chế tiết từng đợt
Arginine vasopressin (AVP)
AVP còn được biết là hormon chống bài niệu hay ADH, là sản phẩm chế tiết chính thứ hai của thùy sau tuyến yên. Nó được tổng hợp bởi các neurone có thân tế bào nằm ở nhân trên thị. Chức năng chính của nó là điều hòa thể tích máu tuần hoàn, huyết áp và áp lực thẩm thấu. Các thụ thể đặc hiệu có khắp nơi trong cơ thể có thể kích thích giải phóng AVP. Các thụ thể thẩm thấu (osmoreceptor) của vùng dưới đồi nhận cảm sự thay đổi của áp lực thẩm thấu máu trung bình ở 285 mOsm/kg. Các thụ thể khí áp (baroreceptor) cảm nhận sự thay đổi huyết áp gây ra do thay đổi thể tích máu và nằm ở thành nhĩ trái, xoang cảnh và cung động mạch chủ.
2.3 Buồng trứng
2.3.1 Giải phẫu học
Buồng trứng là một cơ quan sinh sản vừa có tác dụng ngoại tiết (phóng noãn) vừa có tác dụng nội tiết (tiết hormone sinh dục). Buồng trứng có hình hạt, dẹt, có hai mặt ngoài và trong, hai đầu trên và dưới, nằm áp vào thành bên chậu hông phía sau dây chằng rộng trong hố buồng trứng. Kích thước buồng trứng dài 3.5cm, rộng 2cm, dày 1cm. Từ tuổi dậy thì, mỗi tháng buồng trứng phóng thích một noãn từ nang De Graff vỡ ra, để lại sẹo trên bề mặt buồng trứng. Buồng trứng được cố định tại vị trí hố buồng trứng nhờ vào hệ thống các neo giữ: mạc treo buồng trứng dây chằng tử cung - buồng trứng, dây chằng thắt lưng - buồng trứng và dây chằng vòi - buồng trứng. Cấp máu cho buồng trứng xuất phát từ 2 nguồn: (1) động mạch buồng trứng tách từ động mạch chủ ngay dưới động mạch thận; và (2) nhánh buồng trứng của động mạch tử cung.

2.3.2 Hoạt động nội tiết
Mỗi chu kỳ, hàng trăm nang noãn nguyên thủy được chiêu mộ để phát triển. Cuối chu kỳ trước, khi hoàng thể bị thoái hóa, nồng độ các hormone sinh dục giảm đi làm cho tuyến yên thoát ức chế, tăng sản xuất nồng độ gonadotropin. Vào nửa đầu chu kỳ sau, trong pha nang noãn, các nang này sẽ phát triển, tăng dần kích thuộc và chức năng chế tiết hormone. Các tế bào vỏ và tế bào hạt của nang noãn tăng dần số lượng. Tế bào hạt tạo nên khoang chứa dịch bên trong nang, chịu trách nhiệm chủ yếu cho dinh dưỡng và sự phát triển của noãn. Tác động của LH và FSH lên thụ thể trên tế bào vỏ và hạt nang noãn tạo nên các hormone sinh dục.
Androgen: Trong giai đoạn nang noãn, LH tác động lên thụ thể của nó trên tế bào vỏ buồng trứng, kích thích sản xuất androgen, chủ yếu là androstenedione và Testosterone từ cholesterol.
Estrogen: Androgen từ tế bào vỏ được hấp thu vào dịch nang. Dưới tác dụng của FSH lên tế bào hạt giúp chuyển hóa androgen thành estrogen (E2). Estradiol được hấp thu vào máu làm tăng nồng độ E2 huyết tương. Sự gia tăng này sẽ cùng với FSH để duy trì số lượng thụ thể FSH trên tế bào hạt và thúc đẩy sự hình thành thụ thể LH trên tế bào hạt, đồng thời tạo phản hồi dương vào giữa chu kỳ dẫn tới sự xuất hiện đỉnh LH.
Progesterone: Trong giai đoạn hoàng thể, dưới tác dụng của LH lên thụ thể của nó trên tế bào hạt, androgen sẽ được chuyển hóa thành Progesterone, tác động lên sự làm tổ và duy trì thai kỳ qua sự biến đổi nội mạc tử cung.
3 CƠ CHẾ HOẠT ĐỘNG CỦA HORMON HƯỚNG SINH DỤC
Hormon hướng sinh dục, gồm các hormon giải phóng từ vùng dưới đồi, thùy trước tuyến yên và bánh nhau. Tính đặc hiệu của hormon hướng sinh dục tùy thuộc vào sự hiện diện thụ thể của chúng trên màng tế bào của mô đích. Hormon hướng sinh dục không đi vào trong tế bào để gây hiện tượng sinh lý mà nó chỉ kết hợp với thụ thể trên bề mặt tế bào.
Các thụ thể protein bề mặt có thể hoặc là đóng vai trò chủ động, sau khi gắn kết sẽ hoạt động như một kênh ion, hoặc hoạt động như một enzyme. Các phân tử thông tin nội bào chính là AMP vòng, Inositol 1,4,5-triphosphate (IP3), 1,2-diacylglycerol (1,2-DG), ion Canxi và GMP vòng
3.1 Cơ chế AMP vòng
AMP vòng là một thông tin nội bào cho FSH, LH, hCG, TSH và ACTH. Hormon hướng sinh dục với thụ thể màng tế bào của nó hoạt hóa men adenylate cyclase ở trong thành tế bào dẫn đến sự chuyển adenosine-5-triphosphate (ATP) trong tế bào thành cAMP, Tính đặc hiệu và độ nhạy với kích thích có thể thay đổi do những thay đổi về cấu trúc hoặc mật độ các thụ thể tại vị trí gắn kết ở thành tế bào, Cùng với những thay đổi hoạt động sinh lý do thay đổi tế bào mô đích, những thay đổi cấu trúc phân tử hormon hướng sinh dục có thể ảnh hưởng đến gắn kết tế bào và hoạt động sinh lý.
Cơ chế nhạy cảm tế bào với nồng độ hormon hướng sinh dục tuần hoàn thấp là do chúng có số thụ thể cực lớn nhưng thường chỉ sử dụng một tỷ lệ rất nhỏ (khoảng 1%). cAMP được giải phóng gắn kết đặc hiệu vào các protein thụ thể trong bào tương và phức hợp cAMP-thụ thể này hoạt hóa một protein kinase. Protein kinase hiện diện ở trạng thái bất hoạt dạng tetramer (cấu trúc bộ 4) chứa 2 tiểu đơn vị điều hòa và 2 tiểu đơn vị xúc tác. Khi cAMP gắn vào các tiểu đơn vị điều hòa làm giải phóng các tiểu đơn vị xúc tác. Tiểu đơn vị xúc tác tác động lên phản ứng phosphoryl hóa serin và threonine như các enzyme, mitochondrial, microsomal và chromatin protein. Sau đó cAMP bị thoái hóa do men phosphodiesterase thành trạng thái bất hoạt 5’-AMP. Đáng lưu ý nhất là DNA chứa các yếu tố đáp ứng được phosphoryl hóa do các tiểu đơn vị xúc tác, làm hoạt hóa sự giải mã gene. Vì LH có thể kích thích sự sản xuất hormone sinh dục mà không có sự thay đổi của cAMP rõ ràng (nồng độ thấp), nên rất có thể có một con đường tác động độc lập.
Hệ thống cAMP có khả năng khuếch đại các tín hiệu nội tiết mờ nhạt lưu hành trong máu. Mỗi phân tử cyclase tạo ra nhiều cAMP; protein kinase hoạt hóa một lượng lớn các phân tử. Đây là điểm quan trọng của tính nhạy cảm hệ nội tiết, là lý do tại sao chỉ một tỷ lệ nhỏ các thụ thể màng tế bào được dùng để điều hòa đáp ứng.
Prostaglandin kích thích hoạt động adenylate cyclase và tích lũy cAMP. Bất kể ảnh hưởng của adenylate cyclase như thế nào, prostaglandin được tổng hợp sau hoạt động của cAMP. Điều này có nghĩa là các hormon hướng sinh dục kích thích cAMP trước, rồi các cAMP hoạt hóa sự tổng hợp prostaglandin, cuối cùng prostaglandin nội bào được chuyển đến thành tế bào để hỗ trợ cho đáp ứng với hormon hướng sinh dục. Ngoài tác động qua trung gian cAMP, prostaglandin có thể làm thay đổi nồng độ canxi nội bào.
Prostaglandin và cGMP (cyclic guanosine 3’5’-monophosphate) tham gia vào cơ chế điều hòa ngược âm tính nội bào. Nói cách khác, chức năng tế bào được xác định nhờ vào sự tương tác giữa prostaglandin, cAMP và cGMP.
Có sự khác nhau giữa các hormon hướng sinh dục. Oxytocin, growth hormone, prolactin và human placental lactogen (hPL) không dùng cơ chế adenylate cyclase. Các thụ thể của prolactin, GH và một số cytokine thuộc về một nhóm thụ thể domain xuyên màng duy nhất.
GnRH có cơ chế hoạt động phụ thuộc canxium và dùng IP3 và 1,2-DG như hệ thống thông tin thứ hai để kích thích hoạt động protein kinase. Những đáp ứng này yêu cầu có protein kết hợp với sự giải phóng có chu kỳ ion canxi lưu trữ nội bào và mỏ các kênh màng tế bào cho canxi ngoại bào xâm nhập.
3.2 Hệ thống thông tin Canxi
Nồng độ ion canxi nội bào là một yếu tố điều hòa nồng độ cAMP và cGMP. Sự hoạt hóa các thụ thể bề mặt hoặc mở các kênh trên màng tế bào làm cho ion Canxi đi vào tế bào hoặc giải phóng canxi từ nơi lưu trữ. Nguồn canxi này là một yếu tố điều hòa nội bào quan trọng với đáp ứng của hormone.
Hệ thống thông tin canxi được gắn với liên kết hormone - thụ thể bằng một enzyme đặc hiệu – phospholipase C, xúc tác sự thủy phân polyphosphatidylinositol, một Phospholipid đặc hiệu trên màng tế bào. Enzyme này được hoạt hóa khi hormone gắn vào thụ thể của nó dẫn đến sự phát sinh hai thông tin nội bào, inositol triphosphate (IP3) và diacylglycerol (DAG), làm khởi phát hoạt động hai phần của hệ thống canxi. Phần đầu tiên là một protein kinase được hoạt hóa nhờ canxi chịu trách nhiệm cho đáp ứng tế bào kéo dài và phần thứ hai liên quan đến yếu tố điều hòa calmodulin chịu trách nhiệm cho đáp ứng cấp thời.
Calmodulin được tìm thấy ở tất cả các tế bào động vật và thực vật, vì thế nó là một protein rất cổ xưa. Đây là một chuỗi polypeptide đơn gồm 148 amino acid, có cấu trúc và chức năng tương tự như troponin C, một chất gắn vào canxi khi có thắt cơ tạo thuận lợi cho sự tương tác giữa actin và myosin. Phân tử calmodulin có 4 vị trí gắn với canxi để có tác dụng sinh lý. Một tế bào điển hình có chứa hơn 10 triệu phân tử calmodulin, chiếm 1% tổng số protein tế bào. Là một protein điều hòa canxi, nó hoạt động như một thụ thể canxi nội bào và điều chỉnh sự vận chuyển canxi, hoạt động enzyme, điều hòa canxi trong chuyển hóa nucleotide vòng và glycogen, trong các quá trình như chế tiết và chuyển động tế bào. Vì vậy calmodulin đóng vai trò như troponin để điều hòa hoạt động canxi trong các mô không có co thắt. CAMP cùng với canxium và calmodulin điều hòa hoạt động chuyển hóa nội bào.
3.3 Các thụ thể kinase
Thụ thể màng tế bào của insulin, insulin like growth factor (IGF), epidermal growth factor (EGF), platelet derived growth factor (PDGF) và fibroblast growth factor là các tyrosine kinase. Tất cả các thụ thể tyrosine kinase có cấu trúc tương tự nhau: một domain ngoại bào để gắn kết, một domain xuyên màng và một domain bào tương. Một chuỗi amino acid duy nhất xác định hình dạng 3 chiều tạo nên tính đặc hiệu gắn kết. Domain xuyên màng không được ổn định cao. Domain bào tương đáp ứng với sự gắn kết bên ngoài bằng cách thay đổi hình dạng và tự phosphoryl hóa. Cấu trúc của các thụ thể insulin và IGF rất phức tạp với 2 tiểu đơn vị alpha và 2 tiểu đơn vị beta, tạo nên 2 domain xuyên màng liên kết bên ngoài tế bào nhờ cầu nối disulphide. Thụ thể của activin và inhibin, các yếu tố tự điều hòa và điều hòa lân cận quan trọng hoạt động như những protein kinase đặc hiệu serine.
4 ĐIỀU HÒA HORMON HƯỚNG SINH DỤC
Kiểu tác động của hormon peptid này là một hệ thống sinh lý quan trọng Làm tăng đáp ứng của mô đích. Sự điều hòa hormon hướng sinh dục được chia Làm 4 thành phần chính:
Các yếu tố tự điều hòa và điều hòa lân cận.
Tính không đồng nhất của hormone.
Điều hòa tăng - giảm thụ thể.
Điều hòa adenylate cyclase.
4.1 Cơ chế điều hòa ngược
Sự giải phóng GnRH phụ thuộc vào sự tương tác phức tạp và hiệp đồng của các hormon giải phóng, các hormon thần kinh, gonadotropin tuyến yên và steroid sinh dục. Ảnh hưởng của điều hòa ngược này gồm cả kích thích dương tính và ức chế âm tính.
Vòng điều hòa ngược dài: Ảnh hưởng của nồng độ hormon tuyến đích trong tuần hoàn (androgen và estrogen) lên vùng dưới đồi – tuyến yên.
Vòng điều hòa ngược ngắn: Điều hòa ngược âm tính của hormon tuyến yên lên chính sự chế tiết của nó thông qua điều hòa ngược âm tính lên sự giải phóng hormone & vùng dưới đồi.
Vòng điều hòa ngược cực ngắn: Sự ức chế của các hormon giải phóng lên chính sự tổng hợp của chúng (sự chế tiết của vùng dưới đồi tác động ngược trực tiếp tại vùng dưới đồi).
4.1.1 Hệ thống tự điều hoà/điều hòa lân cận tuyến yên
Các cytokine và yếu tố tăng trưởng tuyến yên tạo hệ thống tự điều hoà/điều hòa lân cận cho việc điều hòa phát triển các tế bào tuyến yên cũng như tổng hợp và chế tiết hormone tuyến yên. Tuyến yên chứa các chất có thể gặp khắp nơi trong cơ thể gồm interleukin, epidermal growth factor, fibroblast growth factor, insulin-like growth factor, nerve growth factor, activin, inhibin và nhiều chất khác.
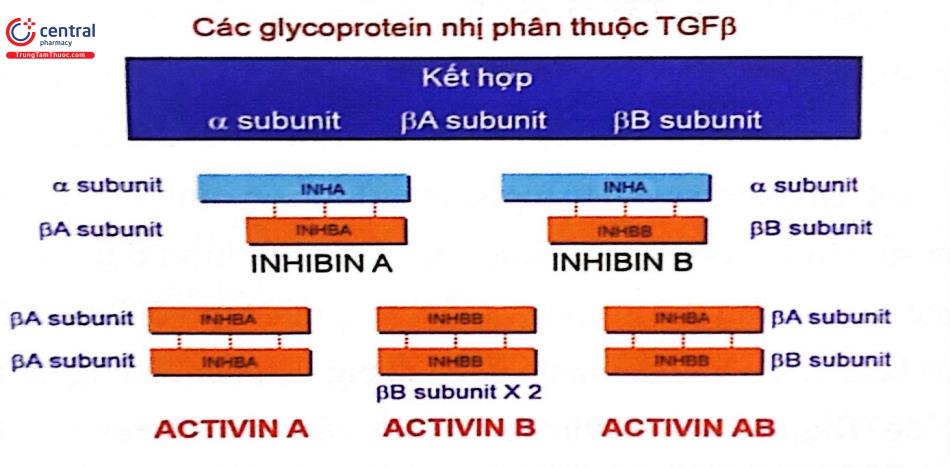
Activin và inhibin là các peptit của gia đình growth factor ß chuyển dạng Inhibin gồm 2 peptit (tiểu đơn vị α và β) gắn kết bằng liên kết disulfide tạo thành 2 dạng inhibin A và B. Inhibin ức chế chọn lọc sự chế tiết FSH nhưng không ức chế LH mà có thể làm tăng hoạt động LH. Các tế bào hoạt hóa tổng hợp LH đáp ứng với inhibin bằng cách tăng số thụ thể GnRH. Inhibin chỉ có rất ít hoặc không có tác dụng lên sự sản xuất growth hormone, ACTH, prolactin.
Activin cũng như Inhibin được chế tiết bởi tế bào hạt. Có 3 dạng activin A, activin B và activin AB. Activin làm tăng sự chế tiết FSH và ức chế đáp ứng prolactin, ACTH và GH. Activin làm tăng đáp ứng tuyến yên với GnRH, có thể bằng cách tăng hình thành các thụ thể GnRH. Hiệu quả của activin bị ngăn chặn bởi inhibin và follistatin.
Follistatin là một peptit được chế tiết bởi các tế bào khác nhau của tuyến yên và được xem là một protein ức chế tiết FSH do khả năng ức chế tổng hợp và chế tiết FSH cũng như đáp ứng của FSH với GnRH, có thể bằng cách gắn vào activin và làm giảm hoạt động của activin. Activin kích thích sản xuất follistatin còn inhibin thì ngăn chặn hiện tượng này.
Nói tóm lại, GnRH kích thích tổng hợp và chế tiết gonadotropin, cũng như activin, inhibin và follistatin. Activin làm tăng và follistatin ức chế hoạt động GnRH. Bằng chứng in vivo và in-vitro đều cho thấy gonadotropin đáp ứng với GnRH cần có hoạt động activin. Tăng tần số xung GnRH ban đầu làm tăng sản xuất FSH, sau đó kích thích GnRH tần số cao và liên tục sẽ làm tăng sản xuất follistatin.
Insulin like growth factor (IGF) còn được gọi là somatomedin là các polypeptide chuỗi đơn tương tự như insulin trong cấu trúc và chức năng. Các yếu tố này phân bố rộng rãi đáp ứng với GH trong sự phát triển và biệt hóa, như một yếu tố điều hòa chuyển hóa tại chỗ của tế bào. IGF II nổi bật hơn trong giai đoạn phôi, còn IGF I hoạt động hơn trong giai đoạn sau sinh. Gan tạo ra nhiều IGF I hơn so với buồng trứng. Các nghiên cứu trên động vật cho thấy, cả IGF I và IGF II đều do tế bào hạt buồng trứng sản xuất. IGF I khuếch đại hoạt động của gonadotropin. Thụ thể IGF I trên tế bào hạt tăng lên do FSH, LH và sự hỗ trợ của estrogen. Trên tế bào vỏ, IGF I làm tăng sinh hormone steroid. Trên tế bào hạt, IGF-I làm tăng thụ thể FSH, LH, làm sinh hormone steroid, chế tiết inhibin và trưởng thành noãn. Hoạt động của cả IGF I và IGF II có thể được điều hòa bởi thụ thể IGF type I có cấu trúc tương tự như thu the insulin.
Các tế bào hạt cũng chứa các thụ thể của insulin và insulin có thể gắn vào thụ thể IGF I. Vì vậy, nó có thể điều hòa chức năng tế bào buồng trứng hoặc thông qua thụ thể của chính nó hoặc thông qua thụ thể IGF I. Nồng độ IGF I và IGF II lưu hành trong máu với nồng độ lớn gấp 1.000 lần so với insulin. Tuy nhiên, phần lớn chúng được kết hợp với IGFBP (insulin like growth factor binding protein). Đây là các protein gắn kết IGF trong tuần hoàn và làm thay đổi đáp ứng tế bào. Có 6 loại IGFBP (IGFBP 1-6) được phát hiện trong huyết thanh và trong mô. IGFBP và các Protease của nó tạo nên cơ chế tác động đặc hiệu mô của IGF. Các IGFBP khác nhau có tác động khác nhau và cách biểu hiện riêng tùy vào loại tế bào và mô đặc hiệu.
4.2 Tính không đồng nhất của hormone
Các glycoprotein như FSH và LH, không phải là một protein đơn độc, mà được xem là một tập hợp các dạng biến đổi của các hoạt động miễn dịch và sinh lý khác nhau. Các đồng dạng này (isoform) xuất hiện theo nhiều cách khác nhau, gồm tác động hoạt hóa DNA khác nhau, thay đổi ghép nối RNA, đột biến điểm và thay đổi carbohydrate sau giải mã. Kết quả của những biến đổi này là làm thay đổi cấu trúc và mức độ chuyển hóa, vì vậy thay đổi khả năng gắn kết và hoạt động. Các đồng dạng này có trọng lượng phân tử, thời gian bán hủy và hoạt tính sinh học khác nhau. Trong một chu kỳ kinh nguyệt, ít nhất 20 – 30 isoform của FSH và LH hiện diện trong tuần hoàn. Vì vậy, tất cả hoạt động của glycoprotein là do tổng hợp các ảnh hưởng của hỗn hợp các dạng isoform này đi đến và gắn kết vào mô đích.
Các tiền chất của hormon glycoprotein được tổng hợp tại lưới nội bào hạt, sau đó sẽ được glycosyl hóa. Các tiểu đơn vị đã được glycosyl hóa này sẽ gắn với nhau và được vận chuyển đến thể Golgi để tiếp tục cấu thành carbohydrate. Sự gắn kết các đơn vị này tạo nên dị nhị trùng kết hợp. Phần protein của dị nhị trùng sẽ gắn vào thụ thể mô đích đặc hiệu, còn phần carbohydrate sẽ đóng vai trò chính trong gắn kết với phức hợp thụ thể-hormone cho hoạt động adenylate cyclase.
Thành phần hóa học chính xác của hormon hướng sinh dục là một yếu tố cần thiết để xác định khả năng hormone kết hợp với thụ thể. Các glycopeptid (FSH, LH, TSH và hCG) là nhị trùng hợp của hai tiểu đơn vị polypeptide được glycosyl hóa: α và β. Hai tiểu đơn vị này liên kết với nhau chặt chẽ. Cấu trúc 3 chiều và dạng hoạt động của nó được duy trì nhờ các liên kết disulphide bên trong. Tất cả các glycopeptide ở người có cùng chuỗi a, một cấu trúc gồm 92 amino acid. Chuỗi khác nhau ở cả amino acid và phần carbohydrate, liên quan đến tính đặc hiệu với thụ thể. Vì vậy, tính đặc hiệu sinh lý của hormone glycopeptide nhờ vào tiểu đơn vị β.
β-hCG là tiểu đơn vị β lớn nhất, nó có phần carbohydrate lớn hơn và 145 amino acid với nhóm carboxyl tận duy nhất chứa 24 amino acid. Đây là phần duy nhất của cấu trúc hCG cho phép sản xuất kháng thể đặc hiệu cao và có thể phát hiện nhờ các xét nghiệm miễn dịch đặc hiệu cao. Những khác biệt về cấu trúc này được kết hợp với những khác nhau về vị trí khởi động và vị trí giải mã nằm trên gen tiểu đơn vị β hCG so với vị trí trên gen tiểu đơn vị β của LH. Tiểu đơn vị hCG không chứa các yếu tố đáp ứng hormone, cho phép hCG thoát khỏi ảnh hưởng điều hòa ngược của hormone sinh dục, khác với FSH và LH.
Thời gian bán hủy của β hCG là 6-8 phút, của toàn bộ hCG sản xuất từ bánh nhau khoảng 24 giờ. Các thành phần carbohydrate của phân tử glycoprotein gồm Fructose, galactose, mannose, galactosamine, glucosamine và sialic acid. Mặc dù chúng đều cần thiết cho hoạt động của hormone, nhưng chỉ acid sialic quyết định thời gian bán hủy. Nếu tách acid sialic khỏi hCG, FSH và LH thì chúng sẽ nhanh chóng bị thải ra khỏi tuần hoàn.
FSH gồm tiểu đơn vị α với 92 amino acid và tiểu đơn vị β 118 amino acid. Nó có 4 chuỗi bên carbohydrate, mỗi tiểu đơn vị chứa 2 chuỗi. Tiểu đơn vị β của LH gồm 121 amino acid, với 3 chuỗi bên carbohydrate và một vị trí glycosyl hóa. Lượng acid sialic ít hơn một nửa so với FSH. Vì vậy, thời gian bán hủy ban đầu của LH khoảng 20 phút so với của FSH là 3-4 giờ.
4.3 Sự khác biệt về carbohydrate
Các hormone glycopeptid có thể thấy trong tuyến yên ở nhiều dạng khác nhau, do carbohydrate (oligosaccharide) của chúng quyết định. Các đồng dạng của gonadotropin bị ảnh hưởng về cả chất lượng và số lượng bởi GnRH và sự điều hòa ngược của hormone sinh dục. Tính không đồng nhất về cấu trúc biểu hiện một cơ chế kiểm soát của nội tiết để điều hòa thời gian bán hủy và hoạt động sinh học.
Thành phần carbohydrate tác dụng lên mô đích theo hai cách: (1) mức độ chuyển hóa và thời gian bán hủy (2) hoạt động sinh học. Cách sau tập trung vào hai chức năng của phức hợp hormone - thụ thể gắn kết và hoạt hóa. Một domain có vai trò quan trọng trong sự gắn kết và một domain khác để kích thích đáp ứng sinh học, Carbohydrate, đặc biệt là sialic acid ít quan trọng trong gắn kết. Thật sự, các chuỗi carbohydrate không có vai trò trong gắn kết của gonadotropin vào thụ thể của nó. Tuy nhiên, nếu lấy bỏ phần carbohydrate sẽ làm thoái giáng hoạt tính của gonadotropin. Như vậy, carbohydrate là phần ảnh hưởng lên tác dụng sinh học của phức hợp hormone - thụ thể sau khi gắn kết. Thời gian bán hủy của gonadotropin trong tuần hoàn chủ yếu phụ thuộc vào khối lượng sialic acid. Sự khác biệt chuỗi amino acid cũng góp phần quan trọng vào tính ổn định toàn bộ hormon.
4.4 Điều hòa tăng - giảm thụ thể
Sự điều hòa kích thích hay ức chế các thụ thể do các hormone tương đồng được xem là điều hòa tăng và giảm. Người ta còn ít biết về cơ chế điều hòa tăng. Tuy nhiên, các hormone như prolactin và GnRH có thể làm tăng mật độ thụ thể của bản thân chúng trên màng tế bào.
Về mặt lý thuyết, sự bất hoạt phức hợp hormone - thụ thể gây ra do sự phân tách phức hợp hay mất thụ thể từ tế bào, hoặc do tách (bên ngoài) hay do nội hóa các thụ thể vào trong tế bào. Quá trình nội hóa là cơ chế sinh học chính mà nhờ đó các hormone polypeptide điều hòa giảm các thụ thể của nó và hạn chế hoạt động của hormone. Nói chung, khi nồng độ hormon hướng sinh dục thừa ra, như GnRH hay LH, thì sẽ kích thích quá trình nội hóa, làm mất thụ thể trên màng tế bào và giảm đáp ứng sinh lý. Ngày nay chúng ta đều biết rằng, lý do chính của việc tiết hormon theo dạng xung là để duy trì thụ thể của nó, tránh tình trạng điều hòa giảm. Vì vậy, tần số của xung chế tiết là yếu tố chính để điều hòa số lượng thụ thể.
Các thụ thể đi vào trong màng tế bào một cách ngẫu nhiên sau khi tổng hợp nội bào. Thụ thể có 3 phần: vị trí gắn kết bên ngoài đặc hiệu cho hormone polypeptide, vùng xuyên màng và một vị trí bên trong giữ vai trò trong quá trình nội hóa. Khi thụ thể được gắn vào hormone polypeptide và khi nồng độ hormone tuần hoàn cao, phức hợp hormone thụ thể sẽ di chuyển qua màng tế bào. Phức hợp này được chuyển đến một vùng đặc hiệu của màng tế bào gọi là hố bao bọc. Các phức hợp hormone thụ thể đi vào được tập trung tại hố này cho phép tế bào tăng khả năng nội hóa các phức hợp.
Khi đã chứa đầy, các hố bọc lại và đi vào tế bào như một nang còn gọi là receptosome. Các nang này được chuyển vào lysosome để được giáng hóa cấu trúc, giải phóng các chất (như hormone polypeptide) và các thụ thể. Các thụ thể có thể được tái phục hồi như đưa trở lại màng tế bào. Cách khác, thụ thể và hormone có thể được chuyển hóa làm giảm hoạt động sinh học của hormone. Các hormone được nội hóa cũng có thể điều hòa phản ứng sinh học bằng cách ảnh hưởng lên bào quan nội bào như thể golgi, lưới nội bào và cả nhân.
Bên cạnh tác dụng điều hòa giảm các thụ thể hormone polypeptide, quá trình nội hóa có thể thực hiện đối với các hoạt động khác của tế bào như để chuyển vào tế bào các chất quan trọng như Sắt hay vitamin.
4.5 Điều hòa adenylate cyclase
Hoạt động sinh học của polypeptide hay hormone glycoprotein (như FSH, LH) có thể thay đổi do các yếu tố tự điều hòa và điều hòa lân cận; tính không đồng nhất của các phân tử; điều hòa tăng và giảm thụ thể; và cuối cùng là điều hòa hoạt động enzyme adenylate cyclase.
4.6 Hệ thống protein G
Adenylate cyclase được tạo thành bởi 3 đơn vị protein: thụ thể, đơn vị điều hòa guanyl nucleotide và một đơn vị xúc tác. Đơn vị điều hòa là một protein liên kết, được điều hòa bởi guanine nucleotide (đặc biệt là GTP) và vì vậy được gọi là protein liên kết GTP (GTP binding protein) hay protein. Đơn vị xúc tác là một enzyme chuyển ATP thành AMP vòng. Thụ thể và đơn vị điều hòa nucleotide được liên kết nhau về cấu trúc, nhưng vẫn bất hoạt cho đến khi hormone gắn vào thụ thể. Khi được gắn kết, phức hợp hormone, thụ thể và đơn vị điều hòa nucleotide được hoạt hóa dẫn đến sự thu nhận guanosine 5-triphosphate (GTP) vào đơn vị điều hoà. Sự hoạt hóa và thu nhận GTP tạo ra một enzyme có thể chuyển ATP thành AMP vòng Hoạt động của enzyme kết thúc khi GTP bị thủy phân thành GDP trở về trạng thái bất hoạt.
Protein được cấu thành bởi các tiểu đơn vị α-, β- và γ-, mỗi tiểu đơn vị tạo ra nhiều gen khác nhau. Tiểu đơn vị β- và γ- không hoàn toàn giống nhau, chúng tác dụng chọn lọc lên thụ thể đặc hiệu. Mỗi protein có một tiểu đơn vị α- duy nhất. GDP trong trạng thái bất hoạt được gắn với tiểu đơn vị α. Sự tương tác giữa hormone – thụ thể và sự gắn kết làm thay đổi hình dạng tiểu đơn vị α, GTP sẽ thay thế GDP trên tiểu đơn vị α, giải phóng tiểu đơn vị β- và γ-, cho phép phức hợp GTP - tiểu đơn vị a gắn vào đơn vị xúc tác của adenylate cyclase, tạo thành enzyme hoạt động. Hoạt động của GTPase nhanh chóng thủy phân GTP-α thành GDP-α. Tính đặc hiệu chức năng do tiểu đơn vị a quyết định khác nhau giữa các protein G.
4.7 Thụ thể protein G
Có hơn 200 thụ thể liên kết với protein G. Thụ thể gonadotropin chứa một vùng xuyên màng có cấu trúc của thụ thể gắn với protein và một domain ngoại bào lớn. Phần domain ngoại bào này là vị trí nhận biết và gắn kết gonadotropin đặc hiệu. Sự gắn kết làm thay đổi hình dạng và phosphoryl hóa dẫn đến sự tương tác với protein làm hoạt hóa hệ thống tin thứ hai, hoặc là enzyme hoặc kênh ion.
LH và hCG gắn vào các thụ thể thông thường, các thụ thể này có tính ổn định cao, Kết hợp với protein C, sự hoạt hóa thụ thể LH/hCG kích thích hệ thống thông tin canxi. Thụ thể FSH rất tương tự với thụ thể LH/CG nhưng khác về cấu trúc. Nó cũng được điều hòa bởi môi trường nội tiết, đặc biệt là nồng độ FSH và estradiol.
5 KẾT LUẬN
Các cơ quan nội tiết của hệ sinh sản từ trục dưới đồi, tuyến yên và buồng trứng hoạt động một cách nhịp nhàng với sự kiểm soát nghiêm ngặt do những cơ chế hoạt động và điều hòa đặc biệt. Mặc dù mỗi cơ quan có đặc điểm riêng về cấu trúc giải phẫu, hoạt động sinh lý, sản phẩm chế tiết và cơ chế điều hoà, nhưng mục đích chính của chúng vẫn là duy trì khả năng sinh sản của người phụ nữ trong giới hạn sinh lý, biểu hiện với sự hoạt động ngoại tiết (phóng noãn) và nội tiết (sản xuất hormone sinh dục) của buồng trứng. Nếu có rối loạn ở một vị trí bất kỳ trong hệ thống này thì sẽ ảnh hưởng trực tiếp đến tình trạng của buồng trứng và vì thế biểu hiện rối loạn phóng noãn và thiếu sót ở mô đích do rối loạn hormone sinh dục.
6 TÀI LIỆU THAM KHẢO
1. Bernichtein S, Touraine P, Goffin V: New concepts in prolactin biology, J Endocrinol 2010; 206:1-11.
2. Butcher AJ, Kong KC, Prihandoko R, et al: Physiological role of G-protein coupled receptor phosphorylation, Handb Exp Pharmacol 2012; 79–94.
3. Chan YM, Butler JP, Pinnell NE, Pralong FP, Crowley WF Jr, Ren C, Chan KK, Seminara SB: Kisspeptin resets the hypothalamic GnRH clock in men, The Journal of Clinical Endocrinology and Metabolism 2011; 96: 908–915.
4. Clarke IJ, Smith JT, Henry BA, Oldfield BJ, Stefanidis A, Millar RP, Sari IP, Chng K, Fabre-Nys C, Caraty A, Ang BT, Chan L, Fraley GS: Gonadotropin- inhibitory hormone is a hypothalamic peptide that provides a molecular switch between reproduction and feeding, Neuroendocrinology 2012; 95: 305-316.
5. Craig ZR, Wang W, Flaws JA: Endocrine-disrupting chemicals in ovarian function: effects on steroidogenesis, metabolism and nuclear receptor signaling, Reproduction 2011; 142: 633-646.
6. Foster PA, Purohit A: Steroid sulfatase inhibitors for estrogen- and androgen-dependent cancers, J Endocrinol 2012; 212 (2): 99-110.
7. Hekimsoy Z, Kafesçiler S, Güçlü, et al: The prevalence of hyperprolactinaemia in overt and subclinical hypothyroidism, Endocrine J 2010; 57: 1011-1015.
8. Hong JW, Lee MK, Kim SH, et al: Discrimination of prolactinoma from hyperprolactinemic non-functioning adenoma, Endocr 2010; 37: 140-147.
9. Hrabovszky E, Ciofi P, Vida B, Horvath MC, Keller E, Caraty A, Bloom SR, Ghatei MA, Dhillo WS, Liposits Z, Kallo I: The kisspeptin system of the human hypothalamus: sexual dimorphism and relationship with gonadotropin-releasing hormone and neurokinin B neurons, The European Journal of Neuroscience 2010; 31: 1984-1998.
10. Karligiotou E, Kollia P, Papaggeli P, et al: FSH modulatory effect on human granulosa cells: a gene-protein candidate for gonadotropinin surge- attenuating factor, Reprod Biomed Online 2011; 23: 440-448.
11. Kennet JE, McKee DT: Oxytocin: an emerging regulator of prolactin secretion in the female rat, J Neuroendocrinol 2011; 24: 403-412.
12. Kohalmy K, Vrzal R: Regulation of phase II biotransformation enzymes by steroid hormones, Curr Drug Metab 2011; 12 (2): 104-123.
13. Kratschmar DV, Vuorinen A, Da Cunha T, et al: Characterization of activity and binding mode of glycyrrhetinic acid derivatives inhibiting characterization of dehydrogenase type 2, J Steroid Biochem Mol Biol 2011; 125 (1-2): 129-142.
14. Mazziotti G, Mancini T, Mormando M, et al: High prevalence of radiological vertebral fractures in women with prolactin-secreting pituitary adenomas, Pituitary 2011; 14: 299-306.
15. McCartney CR: Maturation of sleep-wake gonadotropinin-releasing hormone secretion across puberty in girls: potential mechanisms and relevance to the pathogenesis of polycystic ovary syndrome, Journal of Neuroendocrinology 2010; 22: 701-709.
16. Melmed S, Casanueva FF, Hoffman AR, et al: Diagnosis and treatment of hyperprolactinemia: An Endocrine Society clinical practice guideline, J Clin Endocrinol Metab 2011; 96: 273–288.
17. Miller WL, Auchus RJ: The molecular biology, biochemistry, and physiology of human steroidogenesis and its disorders, Endocr Rev 2011; 32 (1): 81-151.
18. Navarro VM, Castellano JM, McConkey SM, Pineda R, Ruiz-Pino F, Pinilla L, Clifton DK, Tena-Sempere M, Steiner RA: Interactions between kisspeptin and neurokinin B in the control of GnRH secretion in the female rat, American Journal of Physiology. Endocrinology and Metabolism 2011; 300: 202-210.
19. Ojeda SR, Lomniczi A, Sandau U: Contribution of glial-neuronal interactions to the neuroendocrine control of female puberty, The European Journal of Neuroscience 2010; 32: 2003-2010.
20. Okamura H, Murata K, Sakamoto K, Wakabayashi Y, Ohkura S, Takeuchi Y, Mori Y: Male effect pheromone tickles the gonadotropininreleasing hormone pulse generator, Journal of Neuroendocrinology 2010; 22: 825-832.

