Ý nghĩa, hạn chế của chỉ số NON-HDL trên nguy cơ các biến cố tim mạch

Bài viết biên soạn dựa theo
Do Bs. Lê Bảo Trung biên soạn
1 Ý NGHĨA CỦA CHỈ SỐ NON-HDL
1.1 I. Tóm tắt
Dù không phải là một chỉ số mới nhưng cho tới những năm trở lại đây, chỉ số non-HDL mới được các hướng dẫn về quản lý nguy cơ tim mạch, rối loạn lipid máu sử dụng như một yếu tố đánh giá nguy cơ bệnh tim mạch do xơ vữa. Với giá trị tiên đoán cao hơn LDL-C, dễ áp dụng thường quy ngay trong thực tiễn, non-HDL có tiềm năng trở thành chỉ số thay thế LDL-C trong tương lai. Bài viết nhằm mục đích làm rõ giá trị vủa non-HDL và phân tích tiềm năng ứng dụng của chỉ số này.
1.2 II. Khi chất chỉ điểm cũ không theo kịp kỳ vọng
Cho tới hiện tại, LDL-C vẫn là mục tiêu chính trong các hướng dẫn về quản lý lipid máu. Tuy nhiên cùng với thời gian, chúng ta nhận ra còn một phần đáng kể nguy cơ tim mạch tồn dư mặc dù đã kiểm soát đầy đủ LDL-C, huyết áp và đường huyết [5]. Một số nghiên cứu cho thấy ở những đối tượng đang được điều trị đầy đủ bằng statin mà chưa có biến cố tim mạch do xơ vữa, nguy cơ tim mạch do xơ vữa tồn dư vẫn là khoảng 20% chỉ sau một thập kỉ, thậm chí là 40% ở một số đối tượng nguy cơ rất cao [8]. Trước tiên cần phải khẳng định rằng có nhiều yếu tố tham gia vào quá trình xơ vữa mạch máu và thúc đẩy biến cố tim mạch ngoài rối loạn mỡ máu như: bệnh thận mạn, stress, môi trường sống độc hại,... Nhưng bên cạnh việc tìm cách can thiệp vào những cơ chế khác, chúng ta cũng cần xem xét lại rằng liệu LDL- C có còn đủ tốt hay không? Tại sao và phương án thay thế là gì?
1.2.1 1. Bắt đầu từ sự khác biệt giữa LDL-C và LDL-P
Sau khi thiết bị xét nghiệm phân loại được LDL dựa trên tỉ trọng của hạt, số lượng LDL thường được ước tính gián tiếp bằng cách tính toán số lượng Cholesterol trong những hạt này mà chúng ta thường thấy nó trên lâm sàng là chỉ số LDL-C (LDL Cholesterol). Lý do phải sử dụng một chỉ số gián tiếp vì đo trực tiếp LDL rất khó, phải được đo bằng phổ cộng hưởng từ hạt nhân (NMR). Ngày nay ‘LDL-C’ trở thành chỉ số đại diện cho ‘LDL’ trong đánh giá nguy cơ tim mạch và chúng ta thường coi như chúng là một.
Tuy nhiên thực tế là lượng Cholesterol trong các ‘hạt LDL’ (LDL-P) là khác nhau ở từng cá thể. Điều này dẫn tới việc với cùng một lượng cholesterol, những người có ít cholesterol trong hạt LDL hơn thì kích thước hạt LDL của họ nhỏ hơn và số lượng hạt LDL của họ cũng sẽ nhiều hơn (nhưng LDL-C thì vẫn bằng với người khác do tổng lượng Cholesterol ngang nhau). Ngược lại, có những trường hợp Cholesterol trong LDL nhiều hơn bình thường thì cùng một lượng LDL-C, người đó có số lượng LDL ít hơn và kích thước hạt LDL của họ cũng lớn hơn. Chúng ta gọi đây là sự ‘bất tương xứng LDL-C và LDL-P’. Nhưng nó gây ra vấn đề gì?
1.2.2 2. Thuyết “bẫy”
Đây là một giả thuyết đóng vai trò quan trọng trong hiểu biết cơ chế xơ vữa mạch máu ngày nay. Sự xơ vữa gây ra bởi tình trạng ‘mắc bẫy’ của LDL và các hạt lipoprotein khác chứa Apolipoprotein B (ApoB) vào thành động mạch. Giả thuyết này cho rằng có ba lý do chính ảnh hưởng lên khả năng gây xơ vữa của các hạt Lipoprotein: kích thước hạt, tần suất và thời gian phơi nhiễm. Cụ thể, những hạt càng nhỏ thì khả năng đâm xuyên qua lớp nội mạc mạch máu và mắc bẫy của nó cao hơn, những hạt có số lượng lớn hơn thì tần suất tiếp xúc với thành mạch nhiều hơn kéo theo nguy cơ mắc bẫy cao hơn và cuối cùng là theo thời gian, số lượng hạt bị mắc bẫy sẽ tích lũy ngày càng nhiều hơn (Hình 1). Do sinh lý chuyển hóa, LDL là loại Lipoprotein mang ApoB chủ yếu lưu hành trong tuần hoàn, lên đến 90% [15]. Dù vậy, các hạt Lipoprotein mang ApoB khác như VLDL, IDL, kể cả Chylomicron và các hạt tàn dư của những Lipoprotein này cũng góp phần gây ra sự xơ vữa.
Hạt tàn dư hay đầy đủ hơn là hạt tàn dư của các Lipoprotein giàu Triglycerid (TRL) là thuật ngữ để chỉ những hạt Chylomicron, VLDL mà sau quá trình lưu hành trong tuần hoàn, hàm lượng Triglycerid của chúng giảm đi do quá trình thủy phân của Lipoprotein Lipase [16]. Nhưng qua quá trình lưu hành, chúng cũng được làm giàu Cholesterol Ester, tức là chúng mang nhiều Cholesterol hơn. Với kích thước nhỏ hơn và mang nhiều Cholesterol hơn, chúng dễ bị mắc bẫy và gây xơ vữa hơn. Các hạt tàn dư này đã được chứng minh có giá trị tiên lượng nguy cơ tim mạch do xơ vữa độc lập với các yếu tố khác [2].
Một trong những vấn đề được đặt ra là: liệu số lượng hạt hay số lượng Cholesterol trong mỗi hạt sẽ quan trọng hơn trong việc gây ra sự xơ vữa cũng phần nào được giải đáp gần đây, rằng mặc dù lượng Cholesterol lớn sẽ gây ra phản ứng viêm mạnh và thúc đẩy quá trình xơ vữa mạnh hơn nhưng những hạt nghèo Cholesterol lại nhỏ hơn và dễ mắc bẫy trong lòng mạch hơn. Do vậy xét về nguy cơ ròng thì nguy cơ gây xơ vữa của chúng gần như là ngang nhau. Một nghiên cứu gần đây cũng gợi rằng tất cả các Lipoprotein chứa ApoB bất kể là VLDL, tàn dư của VLDL hay LDL đều có nguy cơ gây xơ vữa như nhau [11].
Do vậy, việc chỉ đánh giá bằng LDL đã bỏ lại một khoảng trống cho các hạt Lipoprotein chứa ApoB khác góp phần tạo ra nguy cơ tim mạch tồn dư.
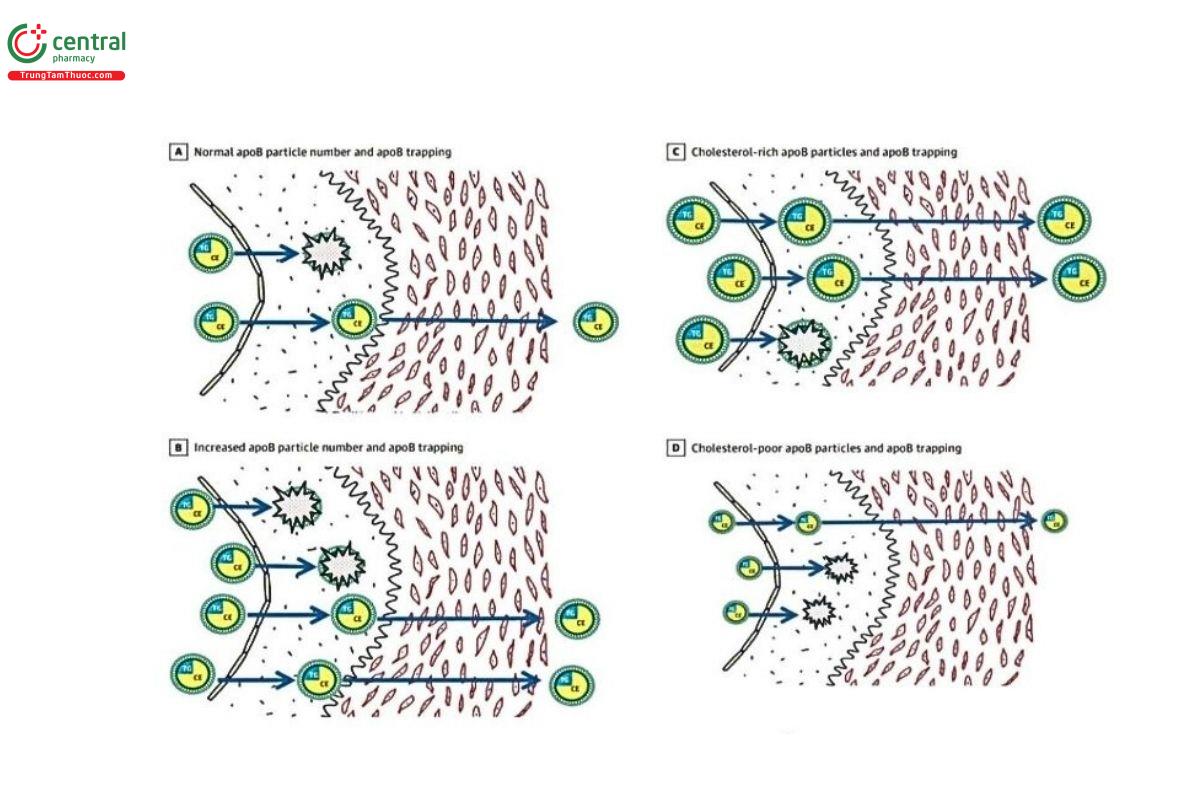
vữa. A: các hạt Lipoprotein chứa ApoB bị mắc bẫy. B: Số lượng hạt tăng lên thì số
lượng hạt bị mắc bẫy cũng tăng theo. C: Các hạt Lipoprotein giàu Cholesterol thì
lớn hơn và khó mắc bẫy hơn. D: Các hạt Lipoprotein nghèo Cholesterol thì nhỏ
hơn và dễ mắc bẫy hơn.
1.2.3 3. Bất tương xứng LDL-C và LDL-P
Quay lại với chủ đề bất 'tương xứng LDL-C và LDL-P, cần nhắc lại yếu tố quan trọng ở đây đó là ở những bệnh nhân có hạt LDL mang ít Cholesterol hơn bình thường thì: (1) hạt LDL của họ nhỏ hơn và (2) lượng LDL-P của họ cao hơn những người khác có cùng lượng Cholesterol. Dựa trên giả thuyết bẫy chúng ta hiểu rằng LDL của họ có nguy cơ gây xơ vữa tim mạch cao hơn và chỉ số LDL-C không phản ánh được đầy đủ nguy cơ tim mạch của bệnh nhân. Nghiên cứu của Cromwell và cộng sự đã cho thấy tỉ lệ sống còn mà không có biến cố tim mạch sẽ tương quan với chỉ số LDL-P hơn là LDL-C ở những trường hợp có bất tương xứng LDL-C và LDL- P (Hình 2) [3]. Kết quả cũng tương tự với tỉ lệ biến cố tim mạch tích lũy trong nghiên cứu Otvos DJ và cộng sự (Hình 3) [7].
Như vậy, chỉ số LDL-C thậm chí không thể hiện được chính xác nguy cơ mà các hạt LDL gây ra. LDL-P là chỉ số thể hiện chính xác ảnh hưởng của LDL hơn nhưng việc đo lường nó lại khó khăn và tốn kém, thiếu khả năng sử dụng rộng rãi trên lâm sàng.
![Hình 2. Tỉ lệ sống sót không có biến cố giữa 4 nhóm: (1) LDL-P thấp và LDL-C thấp (đỏ), (2) LDL-P thấp và LDL-C cao (xanh lá cây), (3) LDL-P cao và LDL- C cao (xanh dương) và (4) LDL-P cao và LDL-C thấp (vàng) [3]. Có thể thấy ở 2 nhóm có sự bất tương xứng LDL-P và LDL-P (xanh lá cây và vàng) thì tỉ lệ sống còn không có biến cố tương quan với LDL-P chứ không phải LDL-C.](/images/item/Y-nghia-cua-chi-so-non-hdl-2.jpg)
thấp (đỏ), (2) LDL-P thấp và LDL-C cao (xanh lá cây), (3) LDL-P cao và LDL-
C cao (xanh dương) và (4) LDL-P cao và LDL-C thấp (vàng) [3]. Có thể thấy ở
2 nhóm có sự bất tương xứng LDL-P và LDL-P (xanh lá cây và vàng) thì tỉ lệ
sống còn không có biến cố tương quan với LDL-P chứ không phải LDL-C.
![Hình 3. Tỉ lệ biến cố tim mạch tích lũy ở 3 nhóm: Bất tương xứng LDL-P>LDL-C (đỏ), bất tương xứng LDL-P < LDL-C (xanh), tương xứng (đen) [7]](/images/item/Y-nghia-cua-chi-so-non-hdl-3.jpg)
(đỏ), bất tương xứng LDL-P < LDL-C (xanh), tương xứng (đen) [7]
1.3 III. Vai trò của Apolipoprotein B
Tất cả các Lipoprotein chứa ApoB đều mang một và chỉ một ApoB, hơn nữa chúng không bị trao đổi giữa các Lipoprotein [1]. Điều đó có nghĩa là khi chúng ta định lượng ApoB, thực tế là chúng ta đang đếm số lượng tất cả các hạt Lipoprotein chứa ApoB. Có 2 loại Apolipoprotein B là Apolipoprotein B100 và Apolipoprotein B48. Dù vậy, ApoB48 chỉ có ở các Chylomycron và tàn dư của nó, vốn chiếm rất ít trong tuần hoàn nên định lượng ApoB chủ yếu vẫn là ApoB100 có ở LDL, Lp(a), IDL cùng VLDL và tàn dư của nó (Hình 4). Với đặc tính có mặt một cách cố định với số lượng cố định trên từng hạt Lipoprotein gây xơ vữa khiến cho ApoB có khả năng trở thành một chất chỉ điểm sinh học hàng đầu trong dự báo nguy cơ tim mạch do xơ vữa. Nhiều nghiên cứu gần đây đã chứng minh ApoB có giá trị cao hơn LDL-C một cách rõ ràng trong dự đoán các biến cố tim mạch [14].
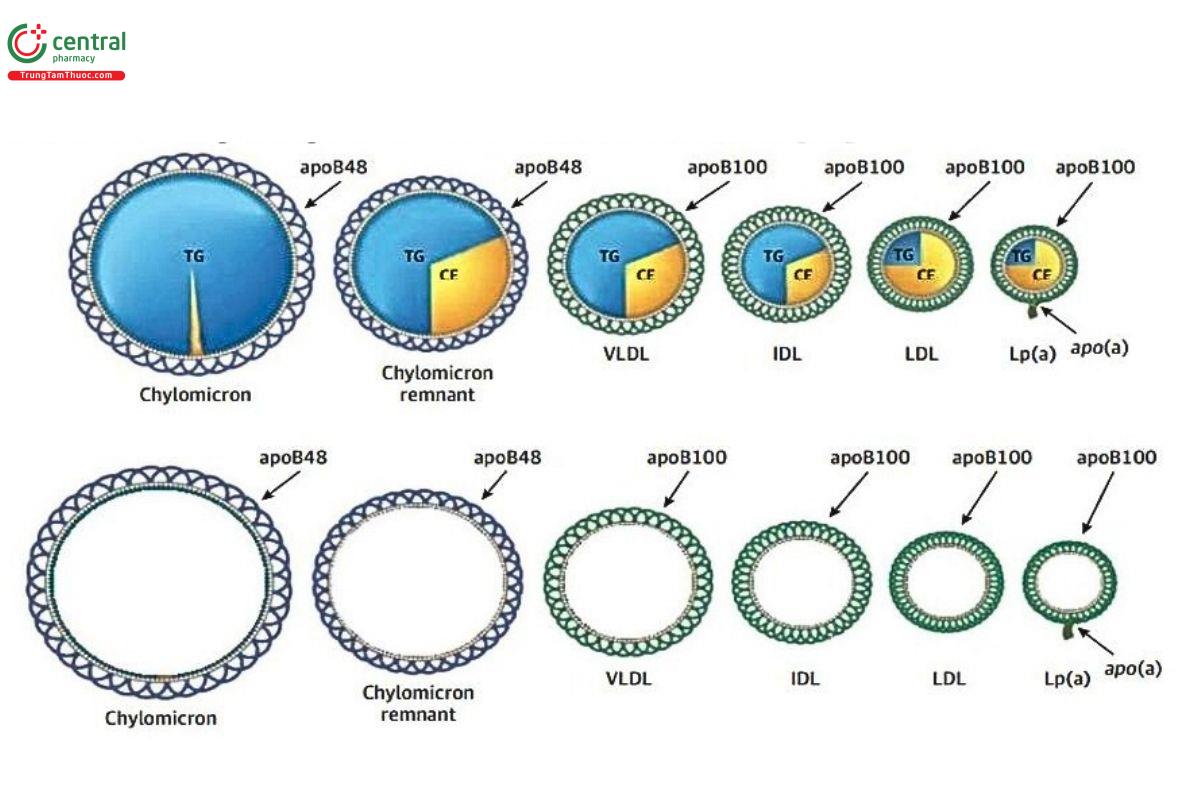
hạt tàn dư của chúng. Mỗi phân tử ApoB chỉ có ở một hạt Lipoprotein và sẽ luôn đi
theo các Lipoprotein này trong suốt vòng đời của chúng.
Tuy nhiên, việc định lượng ApoB vẫn là một vấn đề. Định lượng ApoB là một Xét nghiệm miễn dịch đo độ đục (nguyên lý là ApoB phản ứng đặc hiệu với kháng thể kháng ApoB tạo hợp chất không tan làm đục môi trường. Mật độ quang của môi trường phản ứng sẽ tỷ lệ với nồng độ Apo B trong mẫu bệnh phẩm) [10]. Giá của xét nghiệm định lượng ApoB cao gấp 4 lần so với xét nghiệm bộ Bilan lipid đầy đủ [18]. Giá thành cao và độ chính xác của xét nghiệm có thể thay đổi tùy thuộc phương pháp đo độ đục làm cho chỉ số này khó khả thi trong việc áp dụng rộng rãi trên lâm sàng đến mức thay thế được LDL-C [10].
1.4 IV. Ý nghĩa của non-HDL
Non-HDL là phép đo tính tổng lượng Cholesterol chứa trong các Lipoprotein ngoại trừ HDL. Nó được tính toán đơn giản dựa vào Bilan lipid mà chúng ta thực hiện hàng ngày, bằng cách lấy Cholesterol toàn phần trừ HDL-C. Nói cách khác, nó biểu thị tổng lượng Cholesterol trong các Lipoprotein chứa ApoB. Nghĩa là ngoài LDL-C, non-HDL cũng đại diện cho các Lipoprotein quan trọng khác như Lp(a), IDL,VLDL, và các hạt tàn dư của nó.
Nghiên cứu của Jonhansen và cộng sự cho thấy tỉ lệ bất tương xứng giữa LDL-C và ApoB là 13% trong khi giữa LDL-C và non-HDL là 8% [13]. Điều này tạo cảm giác giá trị tiên đoán nguy cơ tim mạch của non-HDL sẽ nằm giữa LDL-C và ApoB. Tuy nhiên các bằng chứng chứng minh sự vượt trội của ApoB so với non-HDL vẫn chưa đủ chắc chắn.
Không có gì ngạc nhiên khi các nghiên cứu cho thấy non-HDL có giá trị tiên đoán nguy cơ tim mạch do xơ vữa mạnh hơn so với LDL-C. Trong một nghiên cứu với dữ liệu trên 62,154 bệnh nhân đang điều trị statin cho thấy những đối tượng có LDL-C đạt mục tiêu (<100 g/dL) nhưng không đạt mục tiêu non-HDL (>130g/dL) thì nguy cơ xuất hiện biến cố tim mạch cao hơn 32% so với đối tượng đạt cả 2 mục tiêu [HR1.32 (95% CI: 1.17–1.50)] (Hình 5), và thậm chí giá trị dự đoán nguy cơ biến cố tim mạch của non-HDL còn cao hơn ApoB trong kết quả của phân tích này [9]. Trong một phân tích tổng hợp khác dựa trên dữ liệu của 68 nghiên cứu, non-HDL là yếu tố dự báo tốt nhất trong tất cả các chỉ số Cholesterol đối với các biến cố mạch vành và đột quỵ [4].
![Hình 5. Nguy cơ các biến cố tim mạch lớn theo 2 mục tiêu LDL-C và non-HDL [9]](/images/item/Y-nghia-cua-chi-so-non-hdl-5.jpg)
Một nghiên cứu khác trên 13,015 bệnh nhân đang điều trị statin cũng cho thấy cả ApoB và non-HDL đều phản ánh nguy cơ tim mạch tồn dư tốt hơn LDL-C [13]. Đáng chú ý, nghiên cứu này cho thấy có một tỉ lệ bất tương xứng giữa non-HDL và ApoB. Khi phân tích sâu hơn, đánh giá ở nhóm bất tương xứng này cho thấy, ApoB đã dự đoán chính xác hơn tỉ lệ tử vong do mọi nguyên nhân, trong khi tỉ lệ nhồi máu cơ tim là không có sự khác biệt (Hình 6) [13].
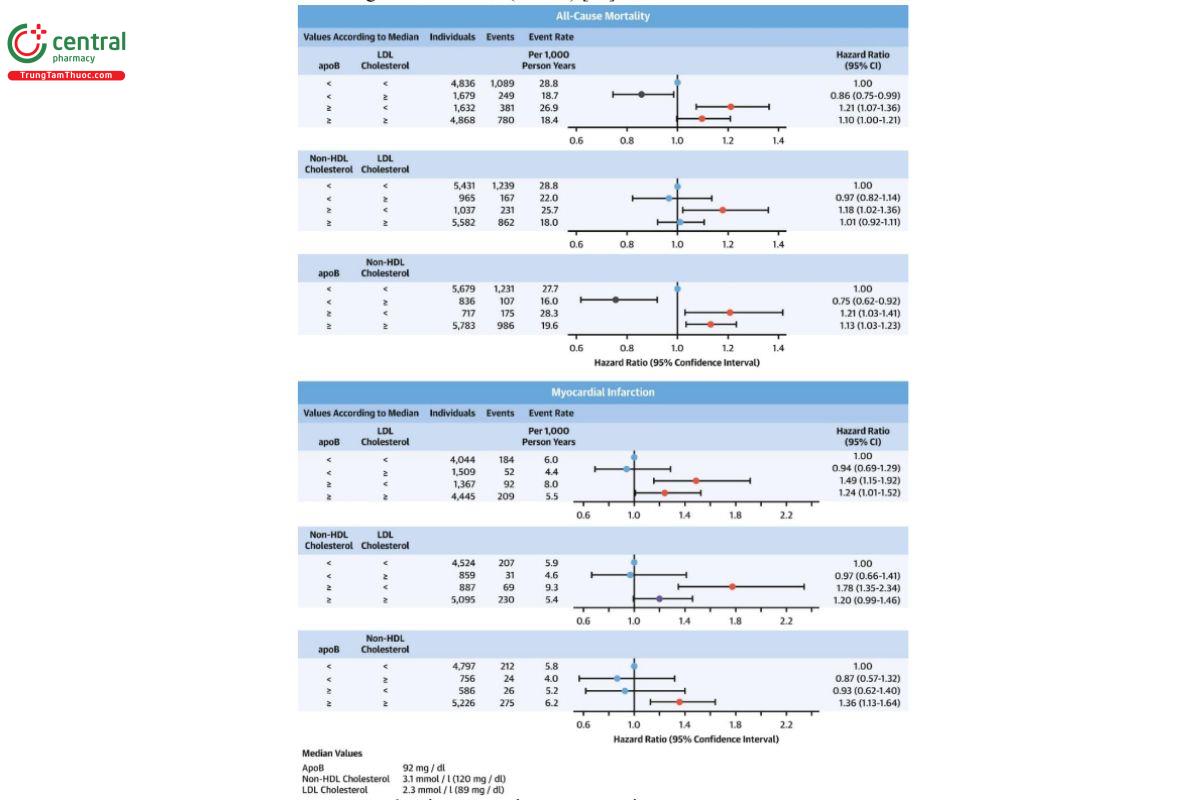
nhân và nhồi máu cơ tim so sánh giữa các nhóm tương xứng và có bất tương xứng
giữa LDL-C, non-HDL, ApoB ở bệnh nhân đang điều trị statin
Về tính khả thi và kinh tế, Non-HDL được tính toán ngay trên xét nghiệm bilan lipid thông thường, không cần chỉ định thêm xét nghiệm và vì thế không gây tốn kém thêm bất kì một chút nào.
Về mặt sinh lý chuyển hóa, hầu hết thời gian sống chúng ta ở trạng thái ‘không nhịn đói’. Điều này khiến chúng ta lập luận rằng, bilan lipid bất kì mới thực sự phản ánh đúng nguy cơ tim mạch chứ không phải bilan lipid lúc đói. Chỉ số LDL-C có thể bị sai số khi có tình trạng tăng Triglyceride (vốn dễ biến động sau bữa ăn) nên thường được chỉ định thực hiện khi đói [17]. Trong khi non-HDL được tính toán dựa trên Cholesterol toàn phần và HDL-C không bị ảnh hưởng bởi nồng độ Triglyceride nên có thể sử dụng với xét nghiệm bilan lipid bất kì hay đói đều được, mang lại nhiều thuận tiện cho bệnh nhân và các cơ sở y tế.
1.5 V. Hạn chế của non-HDL
Dù vậy non-HDL không phải là không có điểm yếu. Mục tiêu của non-HDL-C được khuyến cáo hiện nay cao hơn khoảng 30 mg/dL (0,8 mmol/L) so với ngưỡng của LDL-C. Nguyên lý thêm 30 mg/dL vào LDL-C bắt nguồn từ tỷ lệ trọng lượng Triglyceride: Cholesterol là 5:1 trong các hạt VLDL. Vì ngưỡng Triglyceride mục tiêu khi nhịn ăn là < 150 mg/dl nên mức VLDL-C bình thường có thể được ước tính là < 30 mg/dl. Tuy nhiên, cách ước tính ngưỡng non-HDL-C này gây tranh cãi vì không xem xét đến lượng Cholesterol từ các hạt tàn dư (những hạt này có tỉ lệ Triglyceride: Cholesterol khác với VLDL nguyên bản). Do đó, cần có các nghiên cứu trong tương lai để đưa ra sự đồng thuận về ngưỡng non-HDL-C và mục tiêu điều trị chuẩn mực hơn.
Hơn nữa, một số báo cáo cho thấy có một tỉ lệ sai số nhất định trong định lượng HDL-C, điều này có thể dẫn tới những sai số trong tính toán non-HDL [6]. Trong khi đó, định lượng Cholesterol toàn phần được xem là đáng tin cậy và không gây ra sai số trong việc tính toán non-HDL. Những nhược điểm hay hạn chế này của non-HDL đều có thể khắc phục được về mặt kĩ thuật và dữ liệu.
1.6 VI. Những khuyến cáo hiện hành
Non-HDL thực sự không phải là một chỉ số mới, nó lần đầu tiên được coi là mục tiêu đánh giá thứ phát nguy cơ tim mạch do xơ vữa trong hướng dẫn của Chương trình Giáo dục toàn quốc về Cholesterol năm 2001 tại Hoa Kỳ [19].
Non-HDL-C (≥190 mg/dL) và ApoB đã được nêu bật trong hướng dẫn của AHA/ACC (2018) là các yếu tố nguy cơ bệnh tim mạch do xơ vữa bổ sung và là một trong những yếu tố quyết định các liệu pháp điều trị tích cực bao gồm chất ức chế PCSK9 [12].
Xét đến tính liên quan và tính hữu ích của non-HDL-C, Hướng dẫn gần đây của ESC về dư phòng bệnh tim mạch (2021) cũng sử dụng non-HDL-C như một trong những tiêu chuẩn đầu vào cho thang điểm đánh giá nguy cơ tim mạch mới (SCORE-2) (Hình 7) [17].
Non-HDL cũng được khuyến cáo như một mục tiêu thứ cấp sau khi đạt mục tiêu LDL-C nhằm tối ưu hóa việc giảm nguy cơ tim mạch tồn lưu ở đối tượng có nguy cơ tim mạch trung bình (<3.4 mmol/L), cao (<2.6 mmol/L) và rất cao (<2.2 mmol/L) trong khuyến cáo của ESC và Khuyến cáo điều trị rối loạn lipid máu của Hội Tim mạch học Việt Nam.
Với những ưu điểm rõ ràng của mình, cộng với sự tăng lên về dữ liệu bằng chứng và cải thiện chất lượng xét nghiệm, non-HDL hoàn toàn khả thi trong việc thay thế chỉ số LDL-C trong đánh giá nguy cơ tim mạch và mục tiêu điều trị trong tương lai.
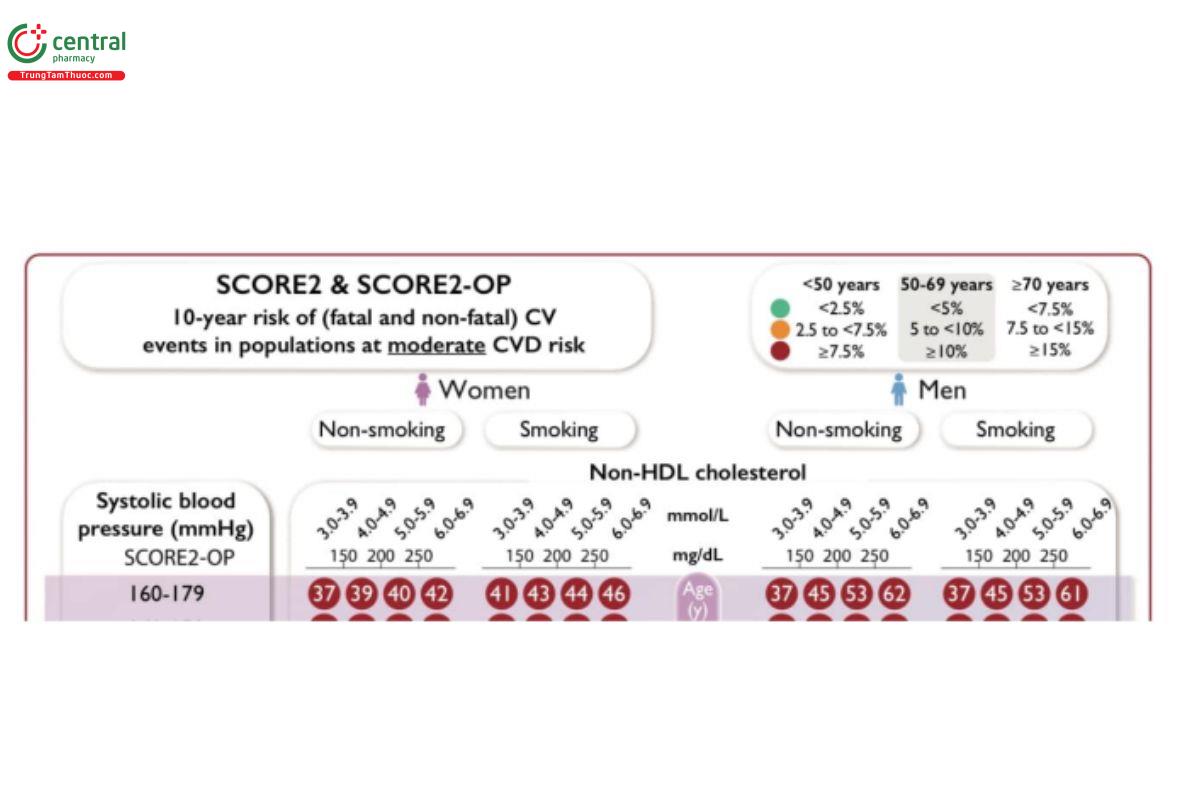
dữ liệu đầu vào cho thang điểm đánh giá nguy cơ tim mạch mới (SCORE2 và
SCORE2 OP) mà ESC sử dụng trong các khuyến cáo của mình.
TÀI LIỆU THAM KHẢO
1. Behbodikhah, J., Ahmed S., Elyasi A., et al. (2021). Apolipoprotein B and Cardiovascular Disease: Biomarker and Potential Therapeutic Target. Metabolites, 11(10). doi:10.3390/metabo11100690
2. Chen, X., & Li L. H. (2023). Remnant Cholesterol, a Valuable Biomarker for Assessing Arteriosclerosis and Cardiovascular Risk: A Systematic Review. Cureus, 15(8), e44202. doi:10.7759/cureus.44202
3. Cromwell, W. C., Otvos J. D., Keyes M. J., et al. (2007). LDL Particle Number and Risk of Future Cardiovascular Disease in the Framingham Offspring Study - Implications for LDL Management. J Clin Lipidol, 1(6), 583-592. doi:10.1016/j.jacl.2007.10.001
4. Di Angelantonio, E., Sarwar N., Perry P., et al. (2009). Major lipids, apolipoproteins, and risk of vascular disease. Jama, 302(18), 1993-2000. doi:10.1001/jama.2009.1619
5. Libby, P. (2005). The forgotten majority: unfinished business in cardiovascular risk reduction. J Am Coll Cardiol, 46(7), 1225-1228. doi:10.1016/j.jacc.2005.07.006
6. Miller, W. G., Myers G. L., Sakurabayashi I., et al. (2010). Seven direct methods for measuring HDL and LDL cholesterol compared with ultracentrifugation reference measurement procedures. Clin Chem, 56(6), 977-986. doi:10.1373/clinchem.2009.142810
7. Otvos, J. D., Mora S., Shalaurova I., et al. (2011). Clinical implications of discordance between low-density lipoprotein cholesterol and particle number. J Clin Lipidol, 5(2), 105-113. doi:10.1016/j.jacl.2011.02.001
8. Wong, N. D., Zhao Y., Quek R. G. W., et al. (2017). Residual atherosclerotic cardiovascular disease risk in statin-treated adults: The Multi-Ethnic Study of Atherosclerosis. J Clin Lipidol, 11(5), 1223-1233. doi:10.1016/j.jacl.2017.06.015
9. Boekholdt, S Matthijs, Arsenault Benoit J, Mora Samia, et al. (2012). Association of LDL cholesterol, non–HDL cholesterol, and apolipoprotein B levels with risk of cardiovascular events among patients treated with statins: a meta-analysis. Jama, 307(12), 1302-1309.
10. Cao, Jing, Steffen Brian T, Guan Weihua, et al. (2018). A comparison of three apolipoprotein B methods and their associations with incident coronary heart disease risk over a 12-year follow-up period: The Multi-Ethnic Study of Atherosclerosis. Journal of Clinical Lipidology, 12(2), 300-304.
11. Ference, Brian A, Kastelein John JP, Ray Kausik K, et al. (2019). Association of triglyceride-lowering LPL variants and LDL-C–lowering LDLR variants with risk of coronary heart disease. Jama, 321(4), 364-373.
12. Grundy, Scott M, Stone Neil J, Bailey Alison L, et al. (2019). 2018 AHA/ACC/AACVPR/AAPA/ABC/ACPM/ADA/AGS/APhA/ASPC/NLA/PCNA guideline on the management of blood cholesterol: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. Journal of the American College of Cardiology, 73(24), e285-e350.
13. Johannesen, Camilla Ditlev Lindhardt, Mortensen Martin Bødtker, Langsted Anne, et al. (2021). Apolipoprotein B and Non-HDL Cholesterol Better Reflect Residual Risk Than LDL Cholesterol in Statin-Treated Patients. Journal of the American College of Cardiology, 77(11), 1439-1450. doi:doi:10.1016/j.jacc.2021.01.027
14. Sniderman, Allan D, Thanassoulis George, Glavinovic Tamara, et al. (2019). Apolipoprotein B particles and cardiovascular disease: a narrative review. JAMA cardiology, 4(12), 1287-1295.
15. Sniderman, Allan, Vu Hai, & Cianflone Katherine. (1991). Effect of moderate hypertriglyceridemia on the relation of plasma total and LDL apo B levels. Atherosclerosis, 89(2-3), 109-116.
16. Stürzebecher, Paulina E, Katzmann Julius L, & Laufs Ulrich. (2023). What is ‘remnant cholesterol’? European Heart Journal, 44(16), 1446-1448. doi:10.1093/eurheartj/ehac783
17. Visseren, Frank LJ, Mach François, Smulders Yvo M, et al. (2021). 2021 ESC Guidelines on cardiovascular disease prevention in clinical practice: Developed by the Task Force for cardiovascular disease prevention in clinical practice with representatives of the European Society of Cardiology and 12 medical societies With the special contribution of the European Association of Preventive Cardiology (EAPC). European Heart Journal, 42(34), 3227-3337.
18. Welsh, Paul, & Sattar Naveed. (2023). To ApoB or not to ApoB: new arguments, but basis for widespread implementation remains elusive. In (Vol. 69, pp. 3-5): Oxford University Press US.
19. Detection, N. E. P. O. (2001). Evaluation. AND Treatment OF High Blood Cholesterol IN Adults: Executive summary of the third report of the National Cholesterol Education Program (NCEP)(Adult treatment Panel III) JAMA, 2486-2497.

