Chẩn đoán và điều trị Hội chứng gan phổi - Tăng áp cửa phổi - EASL 2018
Trungtamthuoc.com - Sự liên quan giữa bệnh gan mạn tính với các triệu chứng hô hấp và giảm oxy máu hiện nay được công nhận khá rộng rãi với nhiều biến chứng xảy ra. Bài viết này sẽ đề cập đến triệu chứng, sinh lý bệnh, chẩn đoán, điều trị hội chứng gan phổi (HPS) và tăng áp cửa phổi (PPHT).
1 ĐỊNH NGHĨA VÀ TRIỆU CHỨNG LÂM SÀNG
Sự liên quan giữa bệnh gan mạn tính với các triệu chứng hô hấp và giảm oxy máu hiện nay được công nhận khá rộng rãi. Bốn biến chứng chính về hô hấp có thể xuất hiện ở những bệnh nhân có bệnh gan mạn bao gồm: viêm phổi, tràn dịch màng phổi do gan, hội chứng gan phối (HPS) và tăng áp cửa phối (PPHT). Trong phạm vi bài này sẽ đề cập đến hội chứng gan phổi (HPS) và tăng áp cửa phối (PPHT).
Hội chứng gan phổi (Hepatopulmonary Syndrome - HPS) được định nghĩa là một rối loạn oxy hóa máu, gây ra bởi sự giãn mạch máu tại phổi, ít phổ biến hơn là thông nối động tĩnh mạch phổi và màng phổi, xảy ra trong bối cảnh lâm sàng của tăng áp cửa. HPS thường gặp nhất ở những bệnh nhân xơ gan tăng áp cửa nhưng cũng có thể gặp ở những bệnh nhân tăng áp cửa trước gan, với tắc nghẽn tĩnh mạch mà không có xơ gan, và thậm chí ở những bệnh nhân có viêm gan cấp hoặc mạn.
HPS được báo cáo trong 10% bệnh nhân viêm gan virus mạn, 15-23% bệnh nhân xơ gan và 28% bệnh nhân hội chứng Budd-Chiari. Biểu hiện lâm sàng của HPS ở những bệnh nhân bệnh gan mạn chủ yếu là khó thở và khó thở khi ngồi. Khó thở là triệu chứng hô hấp phổ biến nhất ở bệnh nhân HPS nhưng lại không đặc hiệu, thường khởi phát âm thầm và xảy ra khi gắng sức. Khó thở khi ngồi được định nghĩa là khó thở khởi phát khi ngồi dậy và cải thiện khi nằm ngửa, tuy kém nhạy nhưng lại rất đặc hiệu cho HPS (do ở tư thế này, có sự gia tăng shunt phổi và bất tương hợp V/Q ở vùng đáy của phổi). Giảm oxy máu khi gắng sức hoặc khi nghỉ ngơi khá phổ biến và khởi phát ở tư thế ngồi hoặc đứng thẳng (giảm oxy máu tư thế). Không có dấu hiệu thực thể nào của HPS khi khám lâm sàng. Tuy nhiên, thở nhanh, ngón tay dùi trống và/hoặc xanh tím ở những bệnh nhân có dấu hiệu của bệnh gan mạn là rất gợi ý cho sự hiện diện của HPS.
2 SINH LÝ BỆNH HỌC
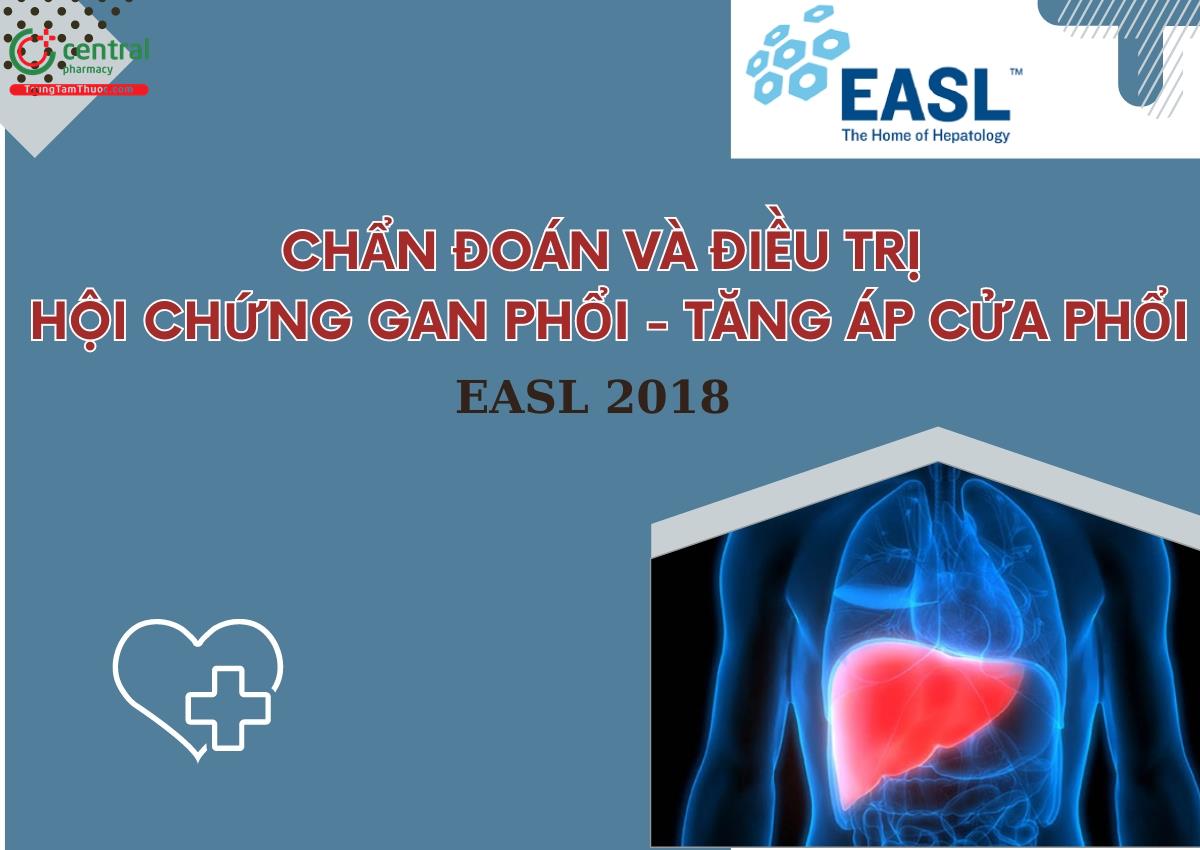
Sinh lý bệnh của HPS đặc trưng bởi tình trạng giãn mạch (tiền và hậu mao mạch) xảy ra trong tuần hoàn phổi (Intrapulmonary Vasodilation - IPVD) ở khu vực phế nang, đường kính của các mạch máu này bình thường là 8-15µm, khi có HPS, đường kính này tăng lên đến 15-500µm.
Sự bất thường về khí máu được giải thích thông qua 3 cơ chế chính:
- Sự bất tương xứng thông khí – tưới máu (V/Q): sự giãn tiền mao mạch làm tăng lưu lượng máu đến các phế nang được thông khí bình thường, dẫn đến làm giảm tỷ V/Q, làm gia tăng AaO2 và/hoặc giảm oxy máu động mạch.
- Hiệu ứng shunt: sự hình thành các thông nối động tĩnh mạch làm máu đi qua các phế nang không thông khí dẫn đến giảm oxy máu.
- Thay đổi khả năng khuếch tán oxy: được giải thích có lẽ là do sự gia tăng khoảng cách giữa phế nang và mao mạch, làm giảm DLCO.
Sinh bệnh học của IPVD có khả năng do nhiều yếu tố cấu thành (Hình 2). Sự giải phóng NO, một chất gây giãn mạch, đóng một vai trò quan trọng trong sự tiến tiến của HPS. Sự tăng giải phóng của NO trong tuần hoàn phổi có liên quan đến sự gia tăng biểu hiện và hoạt động của hai đồng phân của nitric oxide synthase (NOS), đó là NOS nội mạc (eNOS) và NOS cảm ứng (iNOS). Trong khi đó, du khuẩn huyết và nội độc tố máu liên quan đến du khuẩn huyết và đáp ứng tiền viêm cũng góp phần vào sự tích luỹ đại thực bào trong vi tuần hoàn phổi. Sự hoạt hoá nội mạc của fractalkine (CX3CL1) - một chemokine ở phổi có thể thúc đẩy sự kết dính của bạch cầu mono trong vi tuần hoàn phổi. Các bạch cầu mono biểu hiện INOS và sản xuất heme oxygenase-1 (HO), dẫn đến tăng sản xuất carbon monoxide (CO), càng làm giãn mạch mạnh hơn.

3 CHẨN ĐOÁN
Bảng 1: Tiêu chuẩn chẩn đoán của hội chứng gan phổi
Giảm oxy máu với áp suất Oxy riêng phần (PaO2) < 80 mmHg hoặc gradient oxy phế nang-động mạch (AaO2) ≥ 15 mmHg điều kiện khí trời (≥ 20mmHg ở bệnh nhân >65 tuổi).
Khiếm khuyết mạch máu phổi với các dấu hiệu dương tính trên siêu âm tim tăng cường tương phản hoặc sự hấp thụ phóng xạ bất thường ở não (>6%) với chụp xạ hình tưới máu phổi.
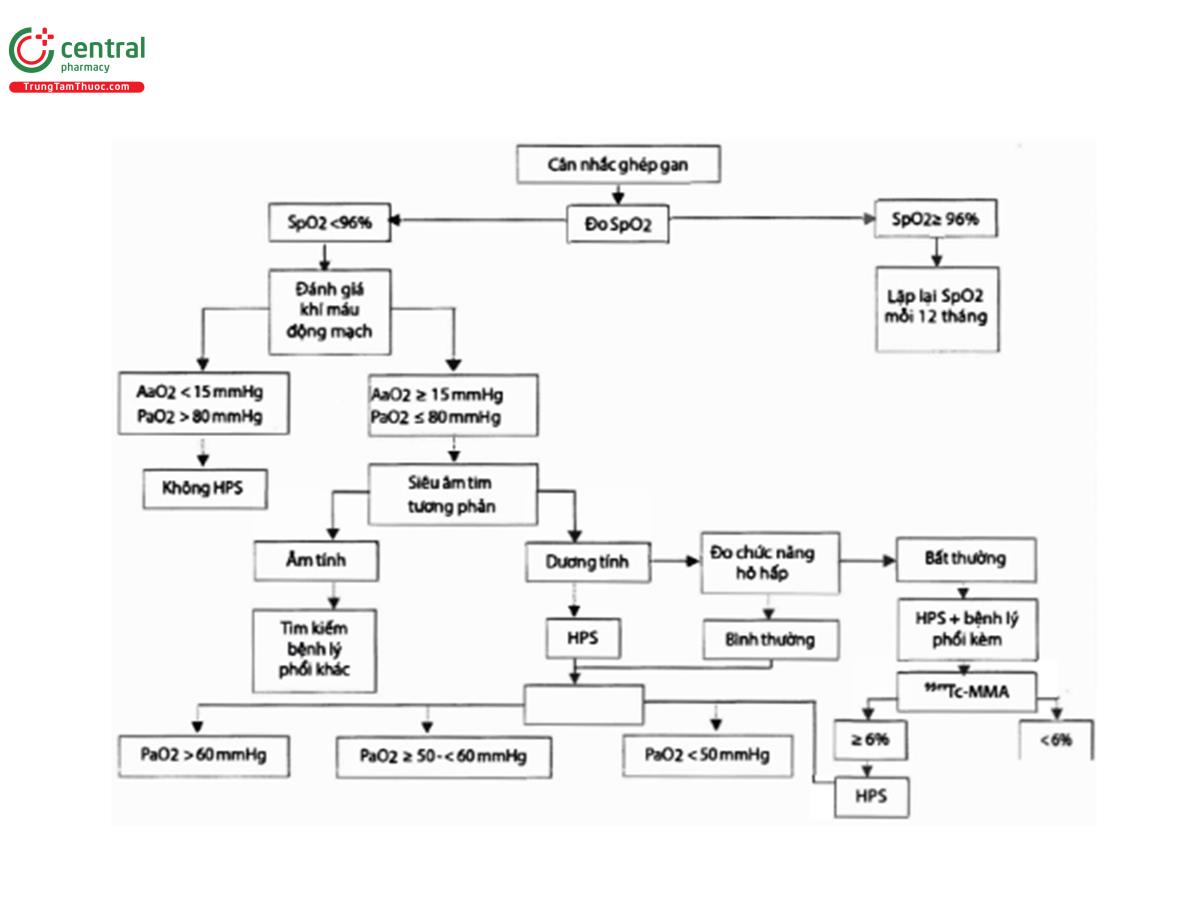
Tất cả tiêu chuẩn được xác định thông qua siêu âm tim tăng cường tương phản. Dựa vào PaO2, HPS có thể được chia thành các mức nhẹ (PaO2 ≥80 mmHg), trung bình (PaO2 60-79 mmHg), nặng (PaO2 50-59 mmHg), và rất nặng (PaO2 <50 mmHg). Cần nhấn mạnh rằng, mặc dù các tiêu chí về PaO2 và AaO2 được thiết lập tốt, cho phép thống nhất các phương pháp chẩn đoán và hiểu rõ hơn về căn bệnh này, nhưng chúng vẫn chỉ là những tiêu chuẩn dựa trên sự đồng thuận của các chuyên gia. Đo gián tiếp độ bão hoà oxy (SpO2), là một phương thức không xâm lấn và có thể hữu dụng trong chẩn đoán HPS ở người lớn vì SpO2 < 96% được thấy rằng rất nhạy (100%) và đặc hiệu (88%) để xác định HPS ở những bệnh nhân có PaO2 <70 mmHg. Các phép đo SpO2 liên tiếp có thể hữu ích để theo dõi tình trạng giảm oxy máu theo thời gian ở bệnh nhân mắc HPS.
Siêu âm tim tăng cường tương phản qua thành ngực với nước muối (lắc để tạo ra các vi bóng có đường kính > 10 µm) là phương pháp hữu ích nhất để phát hiện giãn mạch máu phổi. Sau khi cho nước muối được xử lý qua đường tĩnh mạch ngoại biên, sự xuất hiện của các vi bóng trong nhĩ trái sau 3-6 chu chuyển tim tính từ khi xuất hiện các vi bóng ở nhì phải chứng tỏ rằng các vi bóng đã đi qua một giường mao mạch bị giãn, bởi vì các vi bóng sẽ không thể đi qua được mao mạch thông thường.
Tiêm các thể tụ tập Albumin (Macro-aggregated Albumin - MAA) có đánh dấu technetium-99m qua tĩnh mạch ngoại biên để xạ hình phổi (chụp MAA) là một thủ thuật chẩn đoán thay thế tiềm năng mặc dù nó xâm lấn nhiều hơn và ít nhạy hơn. Các hạt với kích thước 20-50µm, thoát qua các mao mạch bất thường ở phổi (IPVD) và bị giữ lại trong các giường mao mạch hệ thống như não, thận và lách. Sự hấp thụ các hạt này của não được gọi là bất thường khi ≥ 6%. Hình ảnh mang tính định lượng của chụp MAA trong não và phổi cho phép tính toán mức độ của shunt. Việc đo shunt khi chụp MAA có thể hữu ích như một công cụ chẩn đoán bổ sung ở bệnh nhân HPS trong hai tình huống lâm sàng: đầu tiên, ở những bệnh nhân bị giảm oxy máu nặng, có HPS cùng tồn tại với bệnh phổi nội tại thì shunt > 6% khi chụp MAA chứng tỏ sự đóng góp chính của HPS vào tình trạng thiếu oxy máu; thứ hai, ở bệnh nhân bị HPS và giảm oxy máu rất nặng (PaO2 <50 mmHg), sự hiện diện của shunt > 20% có liên quan đến dự hậu xấu sau ghép gan. Mặc dù xạ hình tưới máu phổi có vai trò tiềm năng trong việc tiên lượng ở bệnh nhân xơ gan và IPVD, độ chính xác chẩn đoán của nó đối với HPS vẫn còn được xem xét.
Cuối cùng, cả siêu âm tim tăng cường tương phản lẫn chụp MAA đều không thể phân biệt rạch ròi thông nổi động tĩnh mạch phổi (do giãn mao mạch và tiền mao mạch lan toả) với shunt trong tim. Thông nổi động tĩnh mạch phổi có thể được phát hiện bằng phương pháp chụp động mạch phổi. Shunt trong tim có thể được phát hiện bằng phương pháp siêu âm tim tăng cường tương phản qua thực quản cho thấy trực tiếp vách ngăn trong tâm nhĩ.
Chụp mạch phổi không nên được thực hiện ở tất cả các bệnh nhân nghi ngờ mắc HPS, nhưng chỉ ở: a) bệnh nhân bị giảm oxy máu nặng (PaO2 <60 mmHg) đáp ứng kém với oxy 100% và b) bệnh nhân nghi ngờ cao (bằng một CT scan ngực) của việc có thông nối động tình mạch mà dự định thực hiện nút mạch.
KHUYẾN CÁO CỦA EASL 2018 • Trong bối cảnh bệnh gan mạn, nếu có thở nhanh, ngón tay dùi trống | và/hoặc xanh tím, HPS nên được nghi ngờ và đánh giá (II-2,1). • Đo SpO2 là một công cụ sàng lọc HPS ở những bệnh nhân người lớn, chứ không áp dụng cho bệnh nhi. Với những bệnh nhân có SpO2 < 96%, nên thực hiện phân tích khí máu động mạch. Khi PaO2 thấp hơn 80 mmHg và/hoặc gradient oxy phế nang- động mạch (P[A-a]02) ≥15 mmHg khi thở khí trời thì nên khảo sát thêm. Với bệnh nhân ≥ 65 tuổi nên dùng điểm cất cho P[A-a]O2 là ≥ 20 mmHg (II-2,1). • Khuyến cáo sử dụng siêu âm tim tăng cường tương phản bằng vi bóng để chẩn đoán HPS (II-2;1). • Có thể thực hiện siêu âm tim tăng cường tương phản qua thực quản để loại trừ chắc chắn các shunt trong tim, mặc dù kỹ thuật này vẫn tiềm ẩn nguy cơ (11-2;2). • Chụp MAA nên được xem như là một công cụ bổ trợ để xác định mức độ shunt ở bệnh nhân giảm oxy máu nặng và bệnh phổi nội tại cùng tồn tại, hoặc để đánh giá tiên lượng ở bệnh nhân mắc HPS và giảm oxy rất nặng (PaO2 <50 mmHg) (II-2;1). • Cả siêu âm tim tăng cường tương phản lẫn chụp MAA đều không thể phân biệt chắc chắn thông nối động tĩnh mạch phổi và các shunt trong tim. Chụp động mạch phổi chỉ nên thực hiện ở những bệnh nhân có giảm oxy máu nặng (PaO2 < 60 mmHg), đáp ứng kém với oxy 100%, và ở những người nghi ngờ cao có thông động tĩnh mạch mà được xem xét thực hiện nút mạch (II-2;1). |
Bảng 2: Các phương tiện chẩn đoán hội chứng gan phổi (HPS)
| Phương tiện chẩn đoán | Dấu hiệu | Hạn chế | Mục đích |
| Khí máu động mạch | AaO2 ≥15mmHg hoặc ≥20mmHg ở bệnh nhân >65 tuổi | Tiêu chuẩn đồng thuận chuyên gia, là XN xâm nhập. | Chẩn đoán HPS |
| SpO2 | <96% | Độ nhạy thấp | Sàng lọc và theo dõi HPS |
| Siêu âm tim tăng tương phản | Hiện diện vi bóng trong nhĩ trái sau 3-6 chu chuyến tim. | Khác biệt các chất được dùng làm vi bóng, khác biệt siêu âm qua thành ngực và thực quản | Chẩn đoán IPVD |
| 99m Tc-MAA | Hấp thụ ở não ≥6% | Độ nhạy thấp | Chẩn đoán và định lượng IPVD |
| X-quang ngực | Dấu hiệu kê vùng thấp của phổi do dân mạch | Không đặc hiệu | Loại trừ các bệnh lý phổi đi kèm |
| CT-scan ngực | Đo đường kính động mạch vùng ngoại biên và đánh giá mối quan hệ phế quản – động mạch và hình thái mạch máu. | Số nghiên cứu chứng minh sự có lợi còn ít | Loại trừ các bệnh lý phổi đi kèm |
| Chụp mạch phổi | Đánh giá mạch máu | Xâm nhập, độ nhạy thấp. | Nghi ngờ thông động tĩnh mạch, xem xét nút mạch. |
| Đo chức năng hô hấp | Bình thường hoặc giảm FVC hoặc FEV1, giảm DLCO. | Không đặc hiệu, độ nhạy thấp | Loại trừ các bệnh lý phổi đi kèm. |
Bảng 3: Tiến triển tự nhiên của hội chứng gan phổi
| Chẩn đoán | Không HPS | HPS sớm? | HPS | ||||
| Mức độ | Nhẹ | Trung bình | Nặng | Rất nặng | |||
| Triệu chứng | Không triệu chứng | Có triệu chứng | |||||
| Dấu hiệu | Xơ gan | Giãn mạch phổi giai đoạn sớm | Bằng chứng mạnh của giãn mạch phổi | Thay đổi AaO2 | Giảm oxy máu nhẹ - trung bình | Giảm DLCO | Giảm oxy máu nặng |
| Test chấn đoán | Siêu âm tim tăng cường tương phản qua thực quân | Siêu âm tim tăng cường tương phản qua thành ngực | Phân tích khí máu động mạch | Đo SpO2 Đo chức năng hô hấp 99mTc-MAA | |||
4 TIẾN TRIỂN TỰ NHIÊN
Tiến triển tự nhiên của IPVD cũng như là HPS cho đến nay vẫn chưa rõ ràng. Hầu hết bệnh nhân bị IPVD duy trì trao đổi khí bình thường qua thời gian, và không rõ lý do tại sao một nhóm nhỏ bệnh nhân IPVD phát triển HPS. Chẩn đoán HPS có liên quan đến kết quả tối về cả tỷ lệ sống còn và chất lượng cuộc sống. Về khả năng sống sót, cần nhấn mạnh rằng ở những bệnh nhân được đánh giá ghép gan, tỷ lệ tử vong cao gần gấp đôi ở bệnh nhân mắc HPS so với bệnh nhân xơ gan không có HPS, độc lập với các yếu tố dự đoán tử vong tiềm tàng khác như tuổi, MELD score và bệnh kèm.
5 ĐIỀU TRỊ
5.1 Điều trị nội khoa
KHUYẾN CÁO CỦA EASL 2018 • Liệu pháp oxy dài hạn được khuyến cáo ở những bệnh nhân HPS kèm giảm oxy máu nặng. Tuy nhiên, không có dữ liệu nào liên quan đến hiệu quả, dung nạp, chi phí, tuân thủ và ảnh hưởng đến tỷ lệ sống của liệu pháp này (II-2;1). • Không có khuyến cáo nào có thể được đề xuất liên quan đến việc sử dụng thuốc hoặc đặt TIPS để điều trị HPS (1;1). |
5.2 Ghép gan
KHUYẾN CÁO CỦA EASL 2018 • Bệnh nhân với HPS có PaO2 < 60mmHg nên được đánh giá ghép gan vì đó là • Điều trị duy nhất cho HPS mà được chứng minh là có hiệu quả cho tới nay (II-2;1). • Do tình trạng giảm oxy máu nặng (PaO2 < 45-50 mmHg) có liên quan đến tăng tỷ lệ tử vong sau ghép gan, nên tiến hành phân tích khí máu 6 tháng một lần để tạo điều kiện tối ưu cho ghép gan (II-2;1). |
6 TĂNG ÁP CỬA PHỔI
6.1 Định nghĩa và chẩn đoán
Chẩn đoán tăng áp cửa phổi (Portopulmonary Hypertension - PPHT) nên được xem xét ở bệnh nhân có tăng áp cửa kèm tăng áp phổi mà không có các nguyên nhân khác làm tăng áp động hoặc tĩnh mạch phổi, như là: huyết khối thuyên tắc mạn tính, giảm oxy máu/ bệnh phổi mạn tính; bệnh tim trái mạn tính.
Bệnh nhân có thể không có triệu chứng nhưng thường xuất hiện khó thở khi gắng sức và có những dấu hiệu lâm sàng của suy tim phải khi bệnh tiến triển từ mức độ vừa đến nặng.
Phân loại độ nặng dựa trên áp lực động mạch phổi trung bình (mPAP) và giả sử có sức cản mạch máu phổi cao (PVR). PPHT được xếp loại nhẹ (mPAP ≥ 25 và <35 mmHg); trung bình (mPAP ≥ 35 và <45 mmHg) và nặng (mPAP ≥ 45 mmHg). Chẩn đoán cũng đòi hỏi phải có áp lực phổi bít bình thường, để loại trừ tăng áp lực phổi do tăng áp lực đổ đầy thất trái. Siêu âm Doppler tim qua thành ngực (TDE) là công cụ sàng lọc chính để đánh giá sự hiện diện của PPHT khi sàng lọc bệnh nhân có nguy cơ cao, chẳng hạn như những bệnh nhân được xem xét dặt TIPS hoặc ghép gan.
6.2 Sinh lý bệnh
Ở những bệnh nhân bị tăng áp cửa, PPHT được cho là phát sinh do lưu lượng máu bị hạn chế trong tuần hoàn động mạch phổi do co mạch. Nhiều yếu tố được cho là chịu trách nhiệm về việc này bao gồm: thay đổi các chất vận mạch nội sinh; tăng endothelin 1 và giảm prostacyclin synthase từ các tế bào nội mô phổi; tăng sinh của các tế bào cơ trơn/kích hoạt nội mạc và kết tập tiểu cầu.
6.3 Tiến triển tự nhiên và tiên lượng
Từ các nghiên cứu ở những bệnh nhân được đánh giá ghép gan, tỷ lệ mắc bệnh được cho là nằm trong khoảng 3-10% dựa trên các tiêu chí huyết động. Hơn nữa, giới tính nữ và bệnh gan tự miễn trước đó được cho là các yếu tố nguy cơ độc lập. Sự thay đổi di truyền về mức độ oestradiol có thể làm tăng khuynh hướng dẫn đến co mạch máu phổi. Thật vậy, phụ nữ có nguy cơ cao gấp ba lần so với nam giới. Ngoài ra, còn có sự liên quan giữa bệnh nhân có PPHT mức độ vừa đến nặng với sự tồn tại của shunt cửa chủ. Tuy nhiên, không có mối liên quan rõ ràng giữa độ nặng của bệnh gan hoặc tăng áp cửa với sự tiến triển của PPHT mức độ nặng. Các nghiên cứu trích dẫn tỷ lệ sống sót sau một năm trong khoảng 35-46% mà không cần điều trị đặc hiệu. Tử vong thường liên quan đến các biến chứng khác của bệnh gan như ung thư tế bào gan, nhiễm trùng huyết, xuất huyết tiêu hoá và suy thất phải. Áp lực nhĩ phải cao và chỉ số tim thấp có liên quan đến việc làm tăng tỉ lệ tử vong.
6.4 Điều trị nội khoa
Cơ sở bằng chứng cho các liệu pháp dược lý trong PPHT bị hạn chế, hầu hết dữ liệu được ngoại suy từ các nghiên cứu về tăng áp phổi không liên quan đến bệnh gan. Các loại thuốc để thúc đẩy giăn mạch cấp tính trong quá trình đánh giá thông tim phải, về mặt lý thuyết có thể gây khó chịu vì chúng có nguy cơ làm giảm thêm chỉ số tim. Cho nên, còn thiếu dữ liệu để làm rõ vấn đề này. Ngược lại, trong khi bệnh nhân tăng áp phổi tiến triển có thể được điều trị bằng thuốc chẹn beta, thì liệu pháp ngưng chẹn beta có thể giúp tăng cung lượng tim và do đó giúp điều trị chứng khó thở khi gắng sức ở những bệnh nhân mắc PPHT tiến triển.
- Thuốc đối kháng thụ thể Endothelin: Bosentan đã được chứng minh cải thiện huyết động động mạch phổi và khả năng dung nạp của bệnh nhân mắc PPHT, độc lập với mức độ nghiêm trọng của bệnh gan. Tuy nhiên ở một số ít bệnh nhân, có xuất hiện tăng aminotransferases khi giảm liều hoặc ngưng thuốc nên cần thận trọng khi sử dụng nhóm thuốc này ở những bệnh nhân bị rối loạn chức năng gan tiến triển.
- Thuốc ức chế Phosphodiesterase subtype-5: Ức chế phosphodiesterase-5 tạo điều kiện thuận lợi cho tác dụng giãn mạch của oxit nitric, thông qua giảm chuyến hóa cGMP. Báo cáo các ca lâm sàng nhỏ cho thấy Sildenafil cải thiện dung tích cặn chức năng và tăng cung lượng tim. Nhưng cũng cần chú ý rằng sildenafil có thế làm dễ chảy máu từ các tĩnh mạch trướng, đặc biệt là khi gắng sức.
- Prostacyclin analogue: Prostacyclin analogue có nhiều lợi ích tiềm năng bao gồm giãn mạch, giảm sự tăng sinh cơ trơn mạch máu và chống huyết khối. Báo cáo hàng loạt case lâm sàng gợi ý cải thiện huyết động phổi với epoprostenol. TM và khả năng cải thiện tỷ lệ sống thêm 5 năm so với dữ liệu đăng ký trong tăng áp V (70 so với 40%). Đề nghị sử dụng liều thấp hơn so với liều dùng trong tăng áp phổi vô căn để giảm khả năng bị giảm tiểu cầu và lách to.
- Tác động của việc kiểm soát các biến chứng khác của bệnh xơ gan: Cần thận trọng khi xem xét đặt TIPS để điều trị các biến chứng khác của xơ gan ở bệnh nhân PPHT. Sự gia tăng dự kiến về áp lực đồ đầy thất phải và cung lượng tim có thể làm gia tăng đáng kể kháng lực mạch phổi và quá tải áp lực thất phải. PPHT mức độ vừa (mPAP >35 và <45 mmHg) là một chống chỉ định tương đối cho việc đặt TIPS, trong khi đó PPHT mức độ nặng là chống chỉ định tuyệt đối.
KHUYẾN CÁO CỦA EASL 2018 • Sàng lọc PPHT nên thông qua Siêu âm Doppler tim qua thành ngực ở những bệnh nhân được coi là đối tượng tiềm năng cho TIPS hoặc ghép gan; ở những người có xét nghiệm sàng lọc dương tính, nên thực hiện đặt catheter tim phải (II- 1;1). • Ở những bệnh nhân mắc PPHT nằm trong danh sách chờ ghép gan, nên lặp lại siêu âm tim, mặc dù, khoảng thời gian cụ thể thì không rõ ràng (III;1). • Trong trường hợp đã chẩn đoán PPHT, nên dừng thuốc chẹn beta và điều trị tĩnh mạch trướng bằng liệu pháp nội soi (II-3;1). • Các liệu pháp đã được chấp nhận trong tăng áp phổi nguyên phát có thể có lợi trong PPHT để cải thiện huyết động và khả năng gắng sức. Tuy nhiên, thuốc đối kháng endothelin nên được sử dụng thận trọng vì lo ngại về suy gan (II-2; 1). • Không nên sử dụng TIPS ở những bệnh nhân PPHT (II-3;1). |
6.5 Ghép gan
Trong lịch sử, PPHT nặng là một chống chỉ định tương đối cho ghép gan vì kết quả rất kém. Tuy nhiên, với sự ra đời của các thuốc kiểm soát huyết động như prostacyclin TM, hàng loạt trường hợp cho thấy huyết động phổi vẫn bình thường gần hai năm sau ghép gan.
KHUYẾN CÁO CỦA EASL 2018 • Nếu mPAP <35 mmHg và chức năng thất phải được bảo tồn, nên xem xét ghép gan (II-2.1). mPAP ≥45 mmHg nên được coi là chống chỉ định tuyệt đối với ghép gan bất kể liệu pháp nào đã được áp dụng (III,1). • Điều trị để giảm mPAP và cải thiện chức năng thất phải được bắt đầu ở những bệnh nhân có mPAP 235 mmHg. Chức năng tâm thất nên được đánh 1 giá định kỳ (II-2.1). |
7 TÀI LIỆU THAM KHẢO CHÍNH
1. EASL 2018
2. World J Gastroenterol. 2016 Jul 7;22(25):5728- 41.doi:10.3748/wjg.v22.125.5728. Hepatopulmonary syndrome: What we know and what we would like to know.

