Tìm hiểu cấy máy tạo nhịp tái đồng bộ cơ tim (CRT)

Nguồn: Sách tim mạch can thiệp
Chủ biên: PGS.TS.BS. Phạm Mạnh Hùng
Tham gia biên soạn:
ThS.BSNT Đặng Minh Hải
TS.BSNT Trần Song Giang
ThS.BSNT Đào Minh Đức
ThS. BSNT Bùi Văn Thường
ThS.BSNT Trịnh Văn Nhị
Các nội dung về giải phẫu hệ tĩnh mạch chi trên và tĩnh amchj vành, chỉ định, chống chỉ định cảu máy tạo nhịp rung tái đồng bộ cơ tim, các nội dung liên quan đến máy CRT,... sẽ được Trung Tâm Thuốc Central Pharmacy (trungtamthuoc.com) gửi đến bạn đọc trong bài này.
1 Đại cương
Số lượng bệnh nhân bị suy tim mạn tính gia tăng một cách nhanh chóng cùng với sự phát triển của nền kinh tế công nghiệp. Phần lớn chi phí điều trị suy tim liên quan chủ yếu đến việc nhập viện. Hàng năm có khoảng một triệu ca nhập viện vì suy tim trong đó có 300.000 ca tử vong do suy tim ở Hoa Kỳ cũng như châu Âu. Nguyên nhân tử vong là do suy bơm hoặc đột tử do tim. Suy tim được đặc trưng bởi tình trạng tái cấu trúc cơ học và điện học của tim, nguyên nhân chính tử vong do tim mạch là do suy bơm. Ngược lại, rối loạn điện học đóng vai trò quan trọng dẫn đến tình trạng suy tim nặng hơn, số lượng ca đột tử tăng lên ở bệnh nhân bị suy tim tiến triển và QRS giãn rộng, chiếm tới một phần ba số ca tử vong. Theo nghiên cứu Framingham tỷ lệ tử vong ở nữ 24% và nam 55% trong vòng 4 năm sau khi phát hiện suy tim. Các liệu pháp kết hợp thuốc (thuốc chẹn beta, thuốc ức chế men chuyển, thuốc chẹn thụ thể angiotensin/sacubitril, thuốc đối kháng thụ thể mineralocorticoid và thuốc ức chế SGLT2) đã làm giảm đáng kể tỷ lệ tử vong do suy tim tiến triển. Bất chấp những tiến bộ trong điều trị y học, suy tim vẫn là nguyên nhân gây tử vong hàng đầu.
Cơ chế chính của suy tim là do giảm sức co bóp cơ tim trong thì tâm thu dẫn đến dày và giãn thất trái, rối loạn về mặt điện học trong hệ thống dẫn truyền và cơ tim ở các mức độ khác nhau cũng làm giảm sức bóp cơ tim. Block nhánh trái thường đi kèm với giảm chức năng tâm thu thất trái do hậu quả của việc chậm dẫn truyền trong thành cơ tim thất trái. Mất đồng bộ dẫn truyền thất phải – thất trái cũng như trong hệ His-Purkinje dẫn tới mất đồng bộ co bóp của hai tâm thất. Sự mất đồng bộ này càng làm giảm hiệu quả co bóp, giảm thể tích tống máu.
Máy tạo nhịp tái đồng bộ cơ tim (CRT) được cấy vào cơ thể người bệnh đầu tiên vào những năm 1990. Kể từ đó CRT là một trong những phương pháp hiệu quả nhất trong điều trị suy tim. CRT có 3 dây điện cực là các dây điện cực đặt vào buồng thất phải, thất trái (qua xoang tĩnh mạch vành) và nhĩ phải để thất phải, thất trái co bóp cùng một lúc (đồng bộ). CRT đã được chứng minh cải thiện chức năng tâm thu, giảm tái cấu trúc thất trái, giảm tử vong và tái nhập viện vì suy tim. Ở cấp độ tế bào, CRT kích thích thụ thể adrenergic đáp ứng với tín hiệu kích thích, cải thiện chức năng kênh ion, kích thích ty thể sinh năng lượng. Hơn nữa CRT làm tăng huyết áp tâm thu, cho phép tăng liều thuốc ức chế men chuyển/ức chế thụ thể angiotensin – giúp chống tái cấu trúc thất trái.
2 Giải phẫu hệ tĩnh mạch chi trên và tĩnh mạch vành
2.1 Giải phẫu hệ tĩnh mạch chi trên (xin xem phần ICD)
2.2 Giải phẫu hệ tĩnh mạch vành
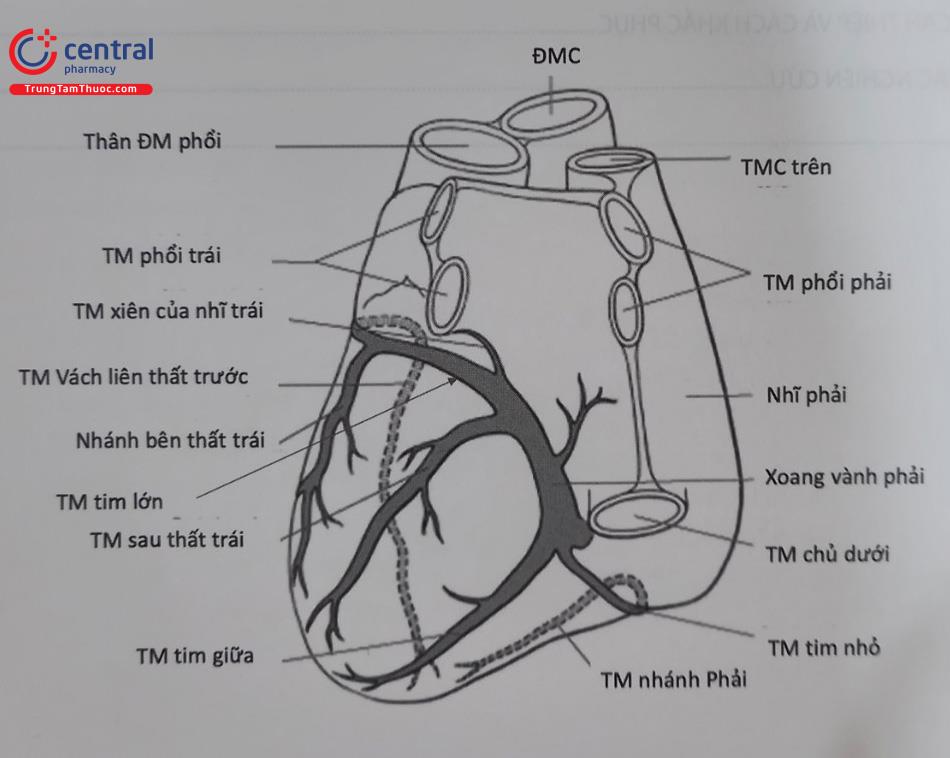
Hệ tĩnh mạch vành bắt đầu từ tĩnh mạch vách liên thất trước, chạy dọc theo rãnh vách liên thất, hợp với tĩnh mạch bên thất trái đổi tên thành tĩnh mạch tim lớn, tĩnh mạch tim lớn chạy trong rãnh vành hợp với tĩnh mạch sau bên thất trái. Tĩnh mạch tim lớn chạy đến chỗ đổ vào của tĩnh mạch xiên (tĩnh mạch marshall) đổi tên thành xoang tĩnh mạch vành, máu từ xoang tĩnh mạch vành hội lưu với máu trở về từ tĩnh mạch tim giữa đổ vào thành sau nhĩ phải (Hình 53.1). Dây điện cực thất trái được đặt vào các nhánh tĩnh mạch phù hợp để đồng bộ 2 thất. Khoảng 60% dây điện cực thất trái được đặt vào tĩnh mạch tim giữa để đi tới thành sau vách thất trái. Thông thường các nhánh trước bên, bên, sau bên và tĩnh mạch tim giữa đều có thể đặt được điện cực. Thành tự do thất trái thường có hoạt động điện muộn nhất và dễ gây mất đồng bộ nhất. Vậy nên, đặt điện cực ở đoạn xa của nhánh bên, sau bên để tái đồng bộ tối đa. Một số trường hợp tĩnh mạch vành quá lớn, không thể cố định được điện cực hoặc xuất phát bất thường hoặc ở bệnh nhân tim bẩm sinh có cấu trúc tim bất thường, sẽ rất khó khăn cho việc đặt điện cực thất trái.
3 Chỉ định và chống chỉ định của máy tạo nhịp tái đồng bộ cơ tim
Hiệu quả của cấy CRT trong điều trị suy tim đã được chứng minh trong nhiều thử nghiệm lâm sàng. Theo khuyến cáo của Hội Tim mạch học châu Âu năm 2021 cấy máy tái đồng bộ cơ tim được chỉ định trong các trường hợp sau (Bảng 53.1, 53.2).
Bảng 53.1. Khuyến cáo CRT ở bệnh nhân suy tim nhịp xoang
| Lựa chọn bệnh nhân | Mức khuyến cáo | Mức bằng chứng |
|---|---|---|
Suy tim, EF ≤ 35%, nhịp xoang, độ rộng QRS ≥ 150 ms, kèm block nhánh trái hoàn toàn mặc dù đã điều trị nội khoa tối ưu để cải thiện triệu chứng, tỷ lệ tái nhập viện và tử vong. | I | A |
Suy tim, EF ≤ 35%, nhịp xoang, độ rộng QRS 130-149 ms, kèm block nhánh trái hoàn toàn mặc dù đã điều trị nội khoa tối ưu để cải thiện triệu chứng,tỷ lệ tái nhập viện và tử vong. | IIA | B |
CRT nên được cân nhắc ở bệnh nhân suy tim có triệu chứng, nhịp xoang, EF ≤ 35%, độ rộng QRS ≥ 150 ms, không phải block nhánh trái hoàn toàn mặc dù đã điều trị nội khoa tối ưu để cải thiện triệu chứng và tỷ lệ tử vong. | IIA | B |
| Suy tim có triệu chứng, EF ≤ 35%, nhịp xoang, QRS ≥ 130-149 ms, không block nhánh trái hoàn toàn mặc dù đã điều trị nội khoa tối ưu. | IIB | B |
| CRT không được chỉ định ở bệnh nhân suy tim, độ rộng QRS < 130 ms mà không có chỉ định tạo nhịp. | III | A |
Chú thích: CRT: Cấy máy tái đồng bộ cơ tim; ICD: Cấy máy phá rung tự động; EF: Phân suất tống máu thất trái.
Bảng 53.2. Chỉ định cấy CRT trong các trường hợp khác
| Lựa chọn bệnh nhân | Mức khuyến cáo | Mức bằng chứng |
|---|---|---|
Suy tim, EF ≤ 35% NYHA III hoặc IV, mặc dù đã điều trị nội khoa tối ưu, nếu bệnh nhân có rung nhĩ và độ rộng QRS ≥ 130 ms, cân nhắc tạo nhịp 2 buồng thất để cải thiện triệu chứng và giảm tiến triển bệnh và tỷ lệ tử vong | IIA | C |
| Đốt nút nhĩ thất được cân nhắc khi tạo nhịp 2 thất < (90-95%) do rung nhĩ. | IIA | B |
| Bệnh nhân rung nhĩ có triệu chứng, không kiểm soát được nhịp thất có kế hoạch đốt nút nhĩ thất, CRT được khuyến cáo ở bệnh nhân HFrEF (< 40%) | IA | C |
| CRT nên được cân nhắc hơn tạo nhịp thất phải ở bệnh nhân HFmrEF và có chỉ định đốt nút nhĩ thất vì rung nhĩ đáp ứng thất nhanh | IIA | B |
| CRT có thể cân nhắc ở bệnh nhân đốt nút nhĩ thất có HFpEF | IIB | C |
| Bệnh nhân có chỉ định tạo nhịp thất phải và suy tim HFrEF (< 40%) nên cấy CRT hơn máy tạo nhịp thông thường | IA | A |
| Bệnh nhân là ứng viên cấy ICD, có chỉ định cấy CRT, cấy CRT-D được khuyến cáo | IA | A |
Chú thích: CRT: Liệu pháp tái đồng bộ cơ tim; CRT-D: Liệu pháp tái đồng bộ tim với máy tạo nhịp tim và phá rung tự động; ICD: Cấy máy phá rung tự động; EF: Phân suất tống máu thất trái. HFrEF: Suy tim EF giảm; HFmrEF: Suy tim EF trung bình; HFpEF: Suy tim EF bảo tồn (> 50%).
4 Các khái niệm cơ bản của máy CRT
4.1 Cấu tạo của máy CRT và dụng cụ hỗ trợ cấy máy cấu tạo của máy CRT
Cấu tạo của máy CRT
Cấu tạo của máy CRT gồm có 3 điện cực, một điện cực nhĩ, một điện cực thất phải và một điện cực thất trái đặt qua xoang tĩnh mạch vành hoặc thượng tâm mạc trong trường hợp giải phẫu hệ tĩnh mạch vành không phù hợp. Máy CRT có kích thước lớn hơn máy tạo nhịp hai buồng tim, nhưng nhỏ hơn máy phá rung tự động. Các máy CRT hiện đại có thời gian pin trung bình lớn hơn 8 năm.
Cấu tạo của máy CRT, CRT-D cũng tương tự như máy phá rung tự động bao gồm bộ phận phát xung và bộ phận kết nối, tuỳ theo thế hệ các máy khác nhau mà đầu kết nối của máy tạo nhịp tái đồng bộ cơ tim khác nhau, chủ yếu bao gồm đầu kết nối với nhĩ phải, điện cực thất trái, điện cực thất phải với máy CRT, điện cực sốc với máy CRT-D. Cấu tạo phần bảng mạch, vỏ máy và pin tương tự như máy phá rung tự động.
Cấu tạo của điện cực nhĩ phải và thất phải giống với máy tạo nhịp vĩnh viễn hai buồng tim, hoặc máy ICD hai buồng tim trong trường hợp bệnh nhân cấy CRT-D.
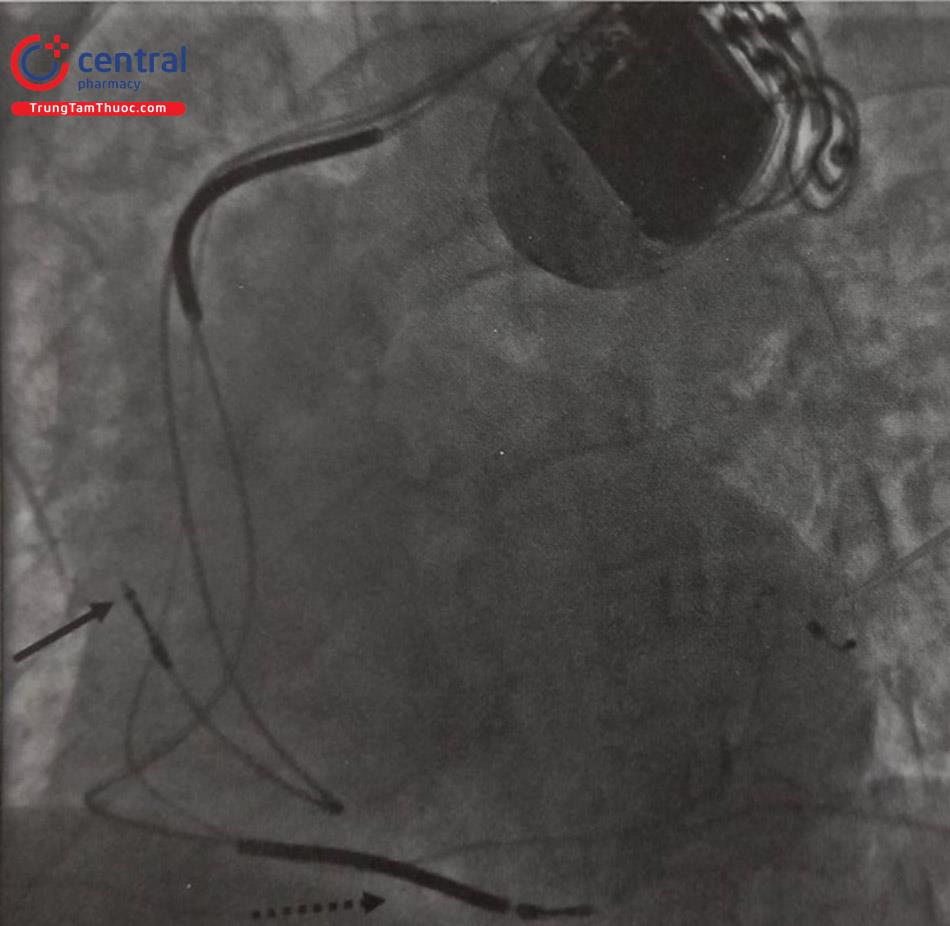
Chú thích: CRT-D: Liệu pháp tái đồng bộ tim với máy tạo nhịp tim và phá rung tự động. Mũi tên chỉ vị trí các điện cực.
4.1.1 Dụng cụ hỗ trợ đặt điện cực thất trái
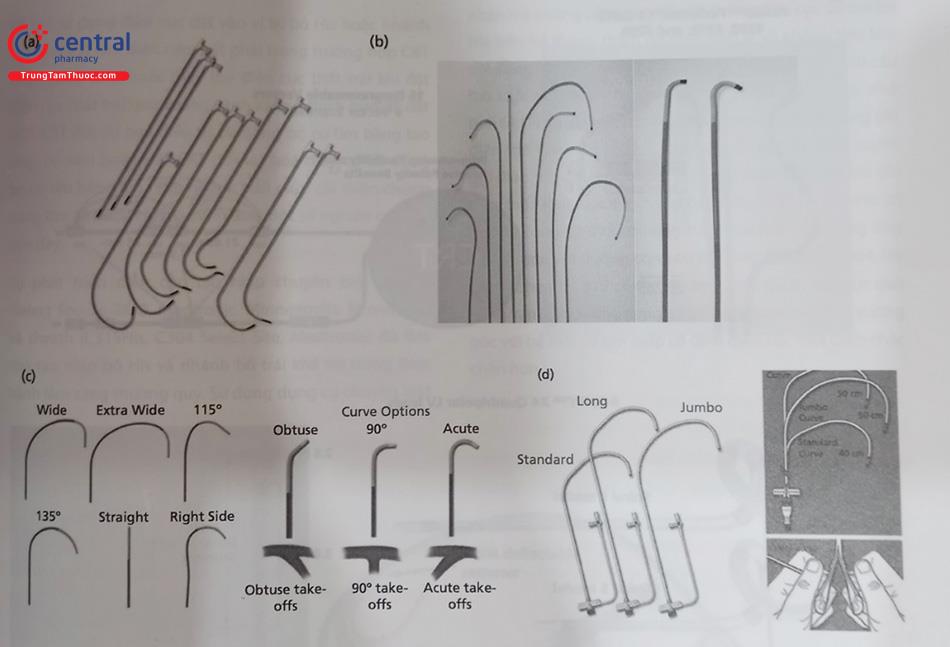
(a) Hệ thống sheath mẹ – con của hãng Medtronic, (b) Boston Scientific, (c) St. Jude Medical, (d) Pressure Product.
Hình 53.3 cho thấy sự đa dạng của các hệ thống sheath hỗ trợ để đặt điện cực thất trái. Hệ thống sheath hỗ trợ thất trái của Medtronic (Hình 53.3a) có kích thước 8 Fr và có dạng thẳng và cong. Nhiều loại ống thông nhỏ hơn 7Fr có sẵn ở các hình dạng và góc độ khác nhau ở đầu ống. Bộ phân sheath hỗ trợ đặt điện cực thất trái của (Boston Scientific; Hình 53.3b) có nhiều hình dạng và chiều dài khác nhau, với việc có thể uốn góc một cách đơn giản. Ngoài ra các sheath hỗ trợ của hãng St.Jude Medical, Biotronik cũng có hình dạng và các góc khác nhau giúp hỗ trợ tốt nhất để đặt điện cực thất trái qua xoang vành.
4.1.2 Điện cực tạo nhịp thất trái
Điện cực thất trái của hãng tạo nhịp khác nhau với đầu điện cực có hình dạng khác nhau như hình thẳng, cong hình chữ S, hình L, điện cực 2 cực hoặc 4 cực với 16 vector. Điện cực của Boston có dạng cố định mỏ neo, dạng xoáy (Hình 53.4).
Điện cực Abbott với 14 vectơ của điện cực 4 cực, làm tăng sự lựa chọn vector tạo nhịp thất trái so với điện cực hai cực. Dây điện cực thất trái thường có kích thước nhỏ hơn so với dây điện cực thất phải hoặc nhĩ phải.
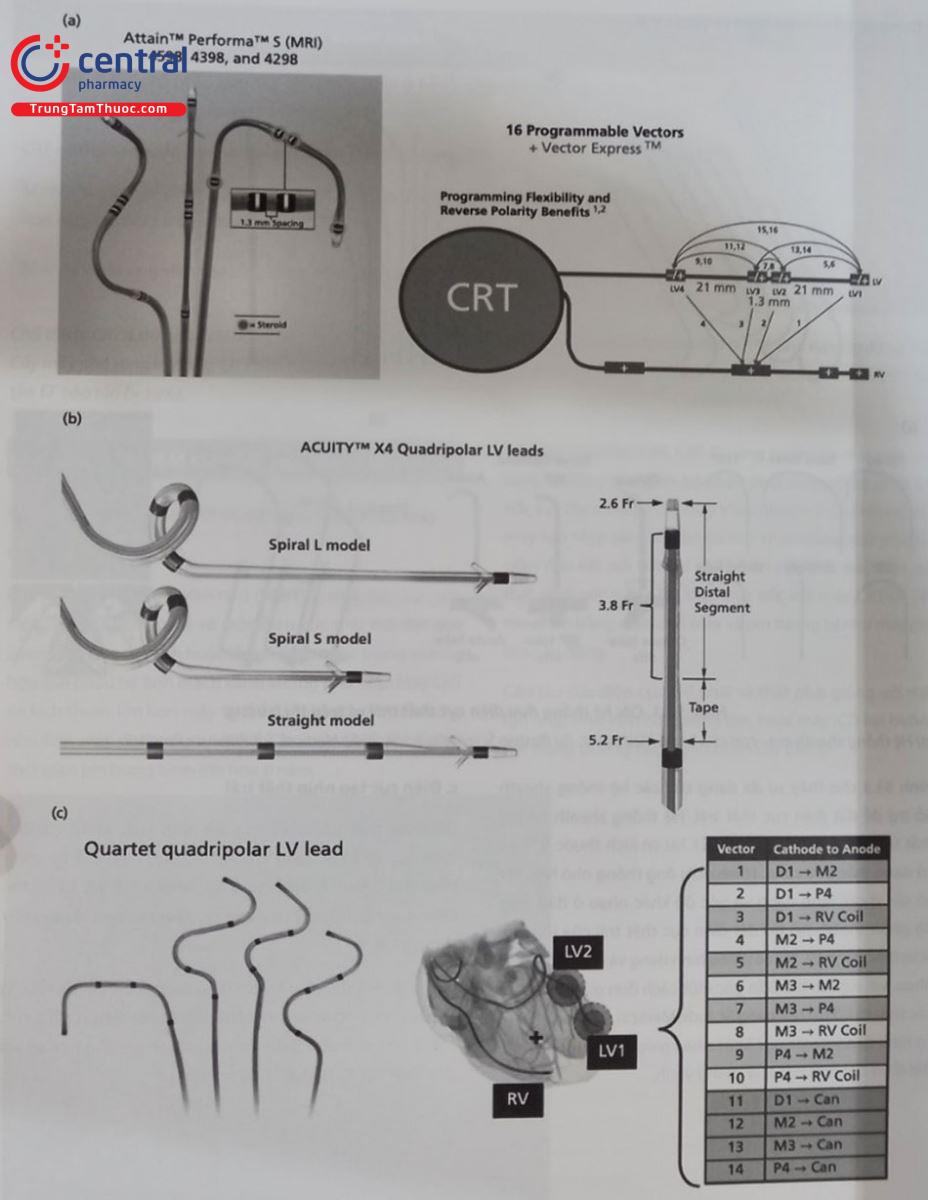
Loại Attain Performa 4 cực của Medtronic, có dạng cong hoặc thẳng. Loại này có 16 hình thái vector có thể lập trình. (b) Loại ACUITY X4 của Boston Scientific có nhiều cỡ, loại này có dạng xoắn và có mấu cố định ở đầu (c) Loại Abbott Quartet 4 cực của Abbott, có 4 dạng khác nhau, cho 14 vectơ khử cực.
4.1.3 Điện cực tạo nhịp bó His
Có thể sử dụng điện cực đặt vào vị trí bó His hoặc nhánh trái thay thế cho điện cực thất phải trong trường hợp CRT không đáp ứng, hoặc thay thế điện cực thất trái khi đặt điện cực thất trái qua xoang vành không thích hợp để đặt HOT-CRT (tối ưu hoá điều trị tái đồng bộ cơ tim bằng tạo nhịp bó His) hoặc LOT-CRT (tối ưu hoá điều trị tái đồng bộ cơ tim bằng tạo nhịp nhánh trái) giúp cải thiện chứng năng tim đã được chứng minh qua một số nghiên cứu lớn gần đây.
Sự phát triển điện cực tạo nhịp chuyên biệt bó His (Select Secure 3830, Medtronic, Minneapolis, Minnesota) và sheath (C315His, C304 Select Site, Medtronic) đã làm cho tạo nhịp bó His và nhánh bó trái khả thi trong thực hành lâm sàng thường quy. Sử dụng dụng cụ chuyên biệt này đã tạo nhịp vùng bó His thành công ở trên 95% bệnh nhân mà không cần dùng đến hệ thống điện cực dò tìm bó His trên hệ thống thăm dò điện sinh lý và không làm kéo dài đáng kể thời gian của thủ thuật. Điện cực SS 3830 cấu tạo khác với các điện cực tiêu chuẩn khác là điện cực nhỏ hơn (4,1F) và lò xo được xoay sẵn ra ngoài với tác dụng ghi điện thế vùng bó his, các phẫu thuật viên thường xuyên ghi điện thế đơn cực do tín hiệu ghi được lớn hơn khi ghi điện thế lưỡng cực. Hệ thống ống dẫn đường C 315-His có đường cong cố định thường hiệu quả hơn hệ thống ống dẫn đường với đường cong có thể thay đổi được C304. Hệ thống sheath C315 có đường cong gần giúp điện cực qua vòng van 3 lá, đường cong xa giúp điện cực tiếp xúc vuông góc với bề mặt cơ tim giúp cố định điện cực một cách chắc chắn hơn.

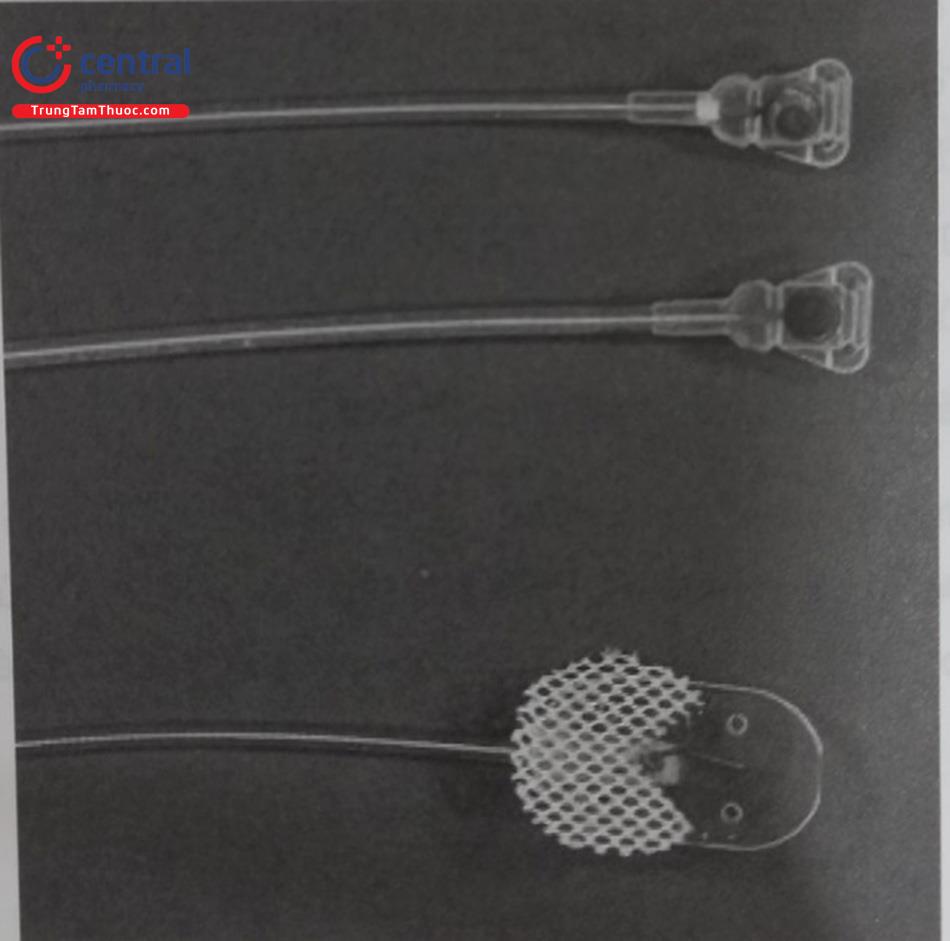
4.1.4 Điện cực thượng tâm mạc
Cấy CRT với điện cực thất trái đặt ở thượng tâm mạc qua đường mở ngực nhỏ khi đặt điện cực thất trái qua đường tĩnh mạch xoang vành không thành công. Hai nguyên nhân hay gặp nhất là giải phẫu hệ tĩnh mạch xoang vành không phù hợp, ngưỡng tạo nhịp quá cao.
Điện cực thượng tâm mạc thường ngắn và to hơn điện cực nội tâm mạc, có 2 loại điện cực xoáy và cài vào cơ tim, trên đầu xa của điện cực có 2 lỗ để đính vào vùng thượng tâm mạc cơ tim giúp điện cực cố định tốt hơn.
5 Kỹ thuật cấy máy CRT
5.1 Chuẩn bị bệnh nhân
Trước khi cấy máy cần đánh giá toàn diện bệnh nhân. Những vấn đề cần lưu ý bao gồm: tiền sử bệnh tật, những thuốc đã và đang sử dụng đặc biệt là thuốc chống đông, thuốc chống ngưng tập tiểu cầu, nên dùng dao điện để mở ổ máy giúp hạn chế chảy máu. Chỉ định cấy máy CRT phải tuân theo hướng dẫn của ESC/AHA.
Việc cân nhắc lựa chọn cấy máy tái đồng bộ cơ tim có hoặc không kèm theo phá rung. Cấy CRT truyền thống hay HOT-CRT, LOT-CRT tuỳ vào trường hợp cụ thể.
Một số vấn đề cần xem xét đặc biệt khi đánh giá và chuẩn bị bệnh nhân:
5.1.1 Nhiễm trùng
Bác sĩ cần hỏi và thăm khám cẩn thận tình trạng nhiễm trùng của bệnh nhân. Cấy máy CRT không phải là thủ thuật cấp cứu, nên cần trì hoãn cấy máy đến khi tình trạng nhiễm trùng của bệnh nhân hoàn toàn ổn định.
Để phòng ngừa nhiễm trùng khi cấy máy, theo khuyến cáo của ESC 2021 kháng sinh dự phòng đường tĩnh mạch nên được cho trước khi cấy máy 1 giờ để dự phòng nhiễm khuẩn.
5.1.2 Bệnh thận
Những bệnh nhân suy thận mạn tính cần phải được xem xét cẩn thận. Bởi vì, trong cấy CRT cần sử dụng thuốc cản quang, thuốc cản quan có thể làm nặng thêm tình trạng suy thận của bệnh nhân. Nên cấy máy đối diện với bên làm cầu tay ở người bệnh chạy thận nhân tạo chu kỳ giúp làm giảm nguy cơ chảy máu ổ máy do tăng áp lực của tĩnh mạch, cũng như không thể sử dụng cầu lọc sau này do tăng nguy cơ hẹp hoặc tắc tĩnh mạch dưới đòn và giảm nguy cơ nhiễm khuẩn cho người bệnh.
5.1.3 Các thuốc kháng kết tập tiểu cầu
Những bệnh nhân dùng thuốc kháng kết tập tiểu cầu kép trước khi cấy máy CRT. Theo khuyến cáo năm 2021 của Hội nhịp học châu Âu về sử dụng thuốc kháng tiểu cầu kép khi có chỉ định cấy máy tạo nhịp. Những bệnh nhân nguy cơ tắc mạch cao thì tiếp tục dùng thuốc kháng kết tập tiểu cầu kép, những bệnh nhân nguy cơ tắc mạch thấp có thể ngừng thuốc kháng P2Y12 trước khi cấy máy CRT.
Bệnh nhân dùng thuốc kháng vitamin K: hiện nay phác đồ được lựa chọn cho bệnh nhân đang uống warfarin cần cấy máy tạo nhịp là không ngừng thuốc. Có nhiều nghiên cứu chỉ ra khi INR < 2,6 biến chứng tụ máu và chảy máu tương tự nhóm INR< 1,5.
Đối với thuốc chống đông trực tiếp đường uống (DOAC) hiện chưa có khuyến cáo cụ thể trường hợp nào nên ngừng, việc ngừng thuốc phụ thuộc vào đánh giá nguy cơ chảy máu và tắc mạch của phẫu thuật viên.
5.1.4 Nguy cơ gây lock nhĩ thất khi cấy máy CRT
Bác sĩ cấy máy cần cân nhắc xem có cần phải đặt tạo nhịp tạm thời trước khi tiến hành cấy máy tái đồng bộ cơ tim để dự phòng nguy cơ gây block nhĩ thất hoàn toàn khi đặt điện cực vĩnh viễn. Những bệnh nhân block nhánh trái hoàn toàn khi cấy máy nguy cơ điện cực gây chấn thương cơ học nhánh dẫn đến block nhĩ thất.
5.2 Chuẩn bị bệnh nhân và dung cụ trong phòng cấy máy
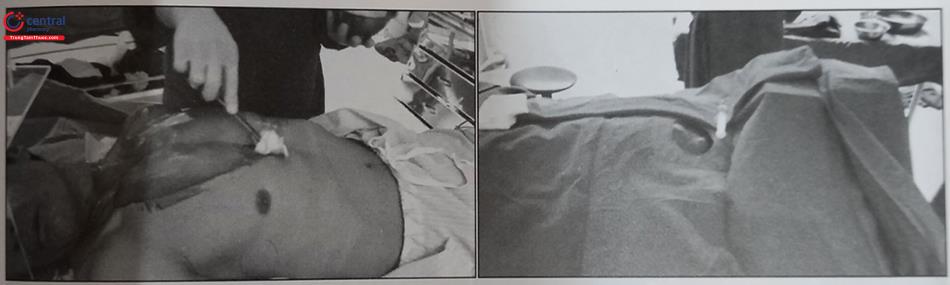
Khi vào phòng thủ thuật, bệnh nhân nằm ngửa trên bàn thủ thuật có thể soi màn tăng sáng. Thiết lập các phương tiện theo dõi các chức năng sống như: điện tâm đồ, đo huyết áp không xâm nhập tự động, đo độ bão hòa oxy máu… để có thể theo dõi các chức năng sống, phát hiện và xử lý các rối loạn nhịp xảy ra trong thủ thuật.
Bác sĩ thường sử dụng một tấm mica hình chữ U ở vùng đầu bệnh nhân để sau khi trải và che phủ bằng các tấm vải vô khuẩn sẽ không ảnh hưởng tới hô hấp của bệnh nhân. Sát khuẩn rộng vị trí sẽ đặt máy nhiều lần bằng dung dịch sát khuẩn có iodine như Povidone-iodine hoặc chlorhexidine. Sau khi sát khuẩn tiến hành che phủ người bệnh bằng các tấm vải vô khuẩn và vùng đặt máy thường được che phủ bằng tấm vải có “cửa sổ” đã được làm sẵn trước hoặc che bằng các tấm vải để tạo ra trường phẫu thuật cấy máy ở vùng dưới xương đòn.
5.3 Vị trí cấy máy tái đồng bộ cơ tim
Việc đặt các điện cực trong cấy CRT thường được thực hiện qua một số tĩnh mạch như tĩnh mạch dưới đòn, tĩnh mạch nách. Thông thường, việc lựa chọn vị trí đường vào tĩnh mạch sẽ quyết định vị trí làm túi máy để đặt thân máy tái đồng bộ cơ tim.
Thông thường nhất, vùng dưới đòn bên trái được lựa chọn vì thuận lợi cho đặt điện cực thất trái qua xoang vành vì góc giữa tĩnh mạch dưới đòn, tĩnh mạch tay-đầu và tĩnh mạch chủ trên ít gập góc hơn bên phải vì vậy việc đưa dây điện cực vào tĩnh mạch vành, buồng tim phải thuận lợi hơn. Một bất lợi khi sử dụng bên trái là có một tỷ lệ nhỏ khoảng 0,3-0,5% bệnh nhân tồn tại tĩnh mạch chủ trên trái đổ vào xoang vành làm khó khăn cho việc đặt các điện cực. Siêu âm cản âm và chụp tĩnh mạch sẽ xác nhận chẩn đoán tồn tại tĩnh mạch chủ trên trái.
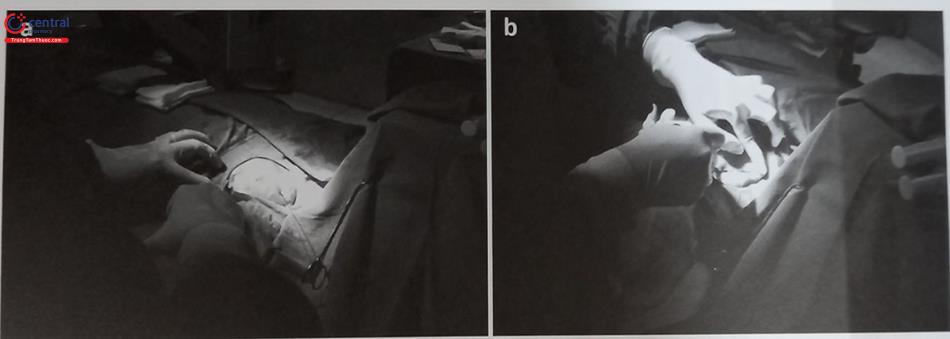
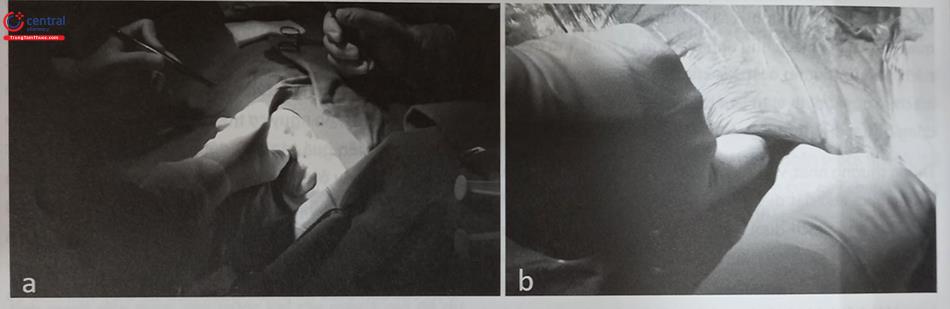
5.4 Đường vào tĩnh mạch và tạo ổ máy
Đường vào tĩnh mạch trong cấy CRT ưu tiên đường vào tĩnh mạch nách hơn tĩnh mạch dưới đòn vì giảm nguy cơ đứt gãy điện cực khi người bệnh vận động mạnh. Với mỗi vị trí đường vào tĩnh mạch khác nhau thì vị trí tạo ổ máy khác nhau. Ví dụ, vị trí tạo ổ máy ở rãnh cơ delta ngực trong trường hợp đường vào tĩnh mạch nách.
Kỹ thuật làm túi máy: gây tê tại chỗ tổ chức dưới da vùng dự định làm túi máy, sau đó phẫu tích bóc tách dần cho đến bao cân mặt trước cơ ngực lớn. Túi máy nên được làm ở trên bao cân cơ ngực lớn và dưới tổ chức mỡ dưới da. Hướng tách cân cơ làm túi máy tốt nhất là nên chếch vào bên trong để tránh nguy cơ trôi thân máy về phía nách làm ảnh hưởng đến quá trình cử động của tay và gây rò. Việc tạo một túi máy ở quá nông ngay dưới lớp da có thể dẫn tới rò rỉ túi máy hoặc hội chứng đau và cần phải làm lại túi máy. Túi máy nên ở ngay phía trên bao cân cơ ngực lớn và cần đủ rộng rãi để đủ chỗ cho cả thân máy và phần dây điện cực còn thừa lại phía ngoài. Nếu túi máy quá nhỏ có thể làm căng phần tổ chức trên thân máy khi khâu đóng ổ máy, ngược lại nếu ổ máy quá lớn lại có thể gây ra sự “trôi”, dịch chuyển thân máy. Cần tăng cường giảm đau bằng các thuốc giảm đau tác dụng nhanh đường tiêm truyền trong giai đoạn tạo túi máy là cần thiết vì đây là thời điểm đau nhất của thủ thuật. Cần chú ý cầm máu trong quá trình tạo ổ máy, với những chảy máu nhỏ thường tự cầm hoặc cầm bằng dao điện, trong chảy máu lớn có thể khâu để cầm máu. Việc cầm máu hết sức quan trọng vì tụ máu sau cấy máy làm tăng nguy cơ nhiễm trùng cho bệnh nhân. Trong một số trường hợp thành ngực quá mỏng cần làm ổ máy trong cơ ngực lớn, tránh trồi máy sau thủ thuật.
5.5 Kỹ thuật đặt điện cực
Phương pháp phổ biến nhất để đặt CRT là qua đường tĩnh mạch thông qua các dụng cụ đặc biệt để đưa điện cực vào nhánh của xoang tĩnh mạch vành, thất phải và nhĩ phải. Nếu đường tĩnh mạch thất bại, điện cực thất trái có thể đặt ở ngoại mạc bằng đường mở ngực trái.
Trong chương này chúng tôi trình bày kỹ thuật đặt điện cực thất trái, kỹ thuật đặt điện cực thất phải và nhĩ phải xin xem ở phần cấy máy tạo nhịp hai buồng.
5.5.1 Kỹ thuật đặt điện cực thất trái
Ống thông để đặt điện cực
Có nhiều cách để đặt ống thông vào xoang vành:
- Cách 1: Dùng guidewire 0,035’’ ngậm nước có đầu mềm chữ J (Terumo) để lái vào.
- Cách 2: dùng long sheath ống thông mẹ-con có wire dẫn đường để đưa vào xoang vành. Khi đặt đầu ống thông gần lỗ xoang vành, rút nhẹ lại và xoay ngược chiều kim đồng hồ, sau đó đẩy ống thông con vào trong xoang vành, kiểm tra chắc chắn bằng cách tiêm một ít thuốc cản quang, sau đó đẩy ống thông mẹ trượt trên ống con vào. Chụp cản quang chọn lọc xoang vành để xác định nhánh phù hợp (Hình 10).
- Cách 3: Dùng điện cực thăm dò điện sinh lý mềm, lái vào xoang vành để trợ lực cho ống thông cứng hơn. Biện pháp này rất hiệu quả khi không thể lái wire vào xoang vành và ống thông khá cứng (Hình 11).
Khi các biện pháp đặt theo mốc giải phẫu này thất bại, không thể xác định được lỗ xoang vành, chụp nhĩ phải cản quang hoặc chụp ĐMV cản quang để lấy hình ảnh xoang vành thì tĩnh mạch giúp xác định rõ lỗ xoang vành.
Có rất nhiều loại ống thông để đưa điện cực vào xoang vành. Tuỳ từng hãng sản xuất mà hình thái, độ cứng, kĩ thuật đưa có thể khác nhau.
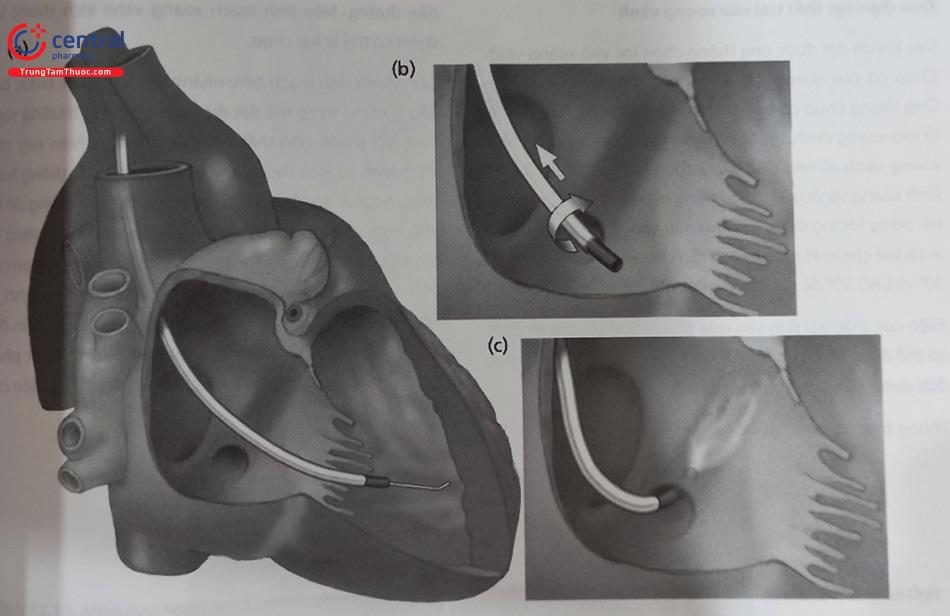
(a) hệ thống được đẩy tới thất phải gần vòng van ba lá thông qua wire, (b) rút nhẹ hệ thống lại, xoay ngược chiều kim đồng hồ để ghé vào miệng lỗ xoang vành, (c) đưa vào trong miệng lỗ và bơm cản quang
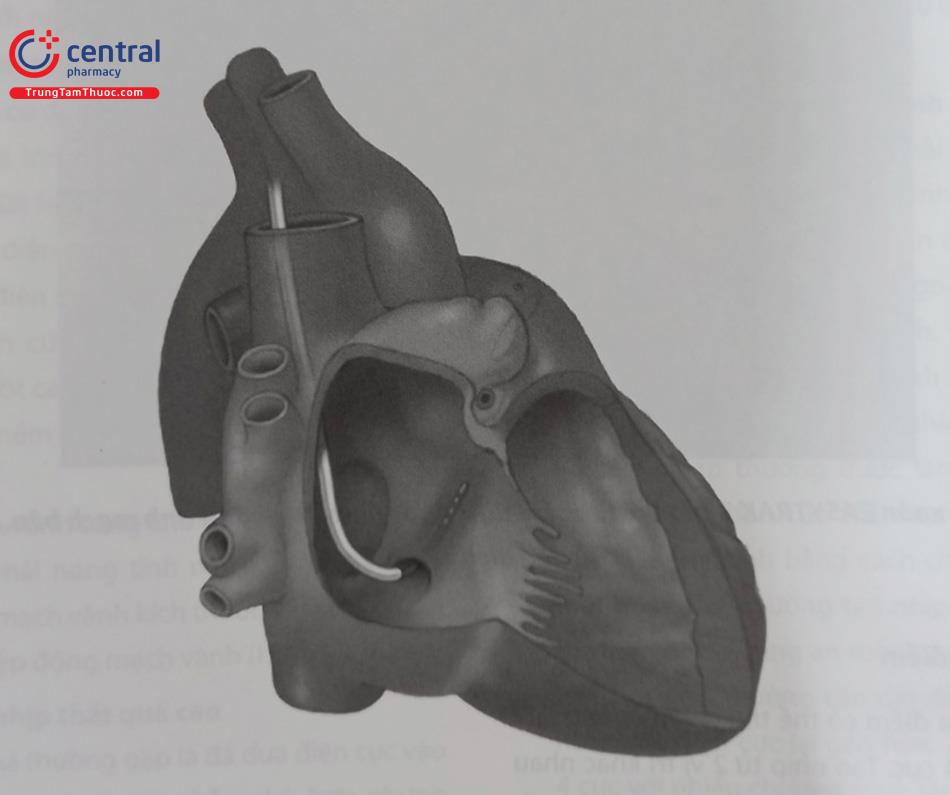
Đưa điện cực thất trái vào xoang vành
Sau khi đã đặt được ống thông chọn lọc vào xoang vành. Chụp có cản quang để xác định giải phẫu xoang vành. Ống thông chụp có bóng ở đầu, khi bơm lên, bóng sẽ bịt lỗ vào xoang vành, thuốc cản quang sẽ đi vào và hiện hình xoang vành rõ nét. Cần lưu ý chọn bóng vừa với đường kính xoang vành gần lỗ để không bị bơm quá to hoặc quá bé. Bóng không được đẩy quá sâu vào trong xoang vành vì có thể che mất nhánh đích cần chụp. Chụp ở 2 góc RAO 300 và LAO 300 để xác định rõ các nhánh.
Điện cực thất trái đưa vào qua ống thông tới nhánh đích, có thể dùng stylet hoặc hệ thống over-the-wire giống như đưa dụng cụ trong can thiệp động mạch vành.
Thông thường điện cực đưa vào với guidewire mềm 0,014” dẫn đường. Nếu tĩnh mạch xoang vành kích thước lớn stylet có thể là lựa chọn.
Các nhánh tĩnh mạch bên: nhánh sau bên, bên, trước bên đều là các vị trí có thể đặt điện cực vì chúng thường song song với thành bên thất trái. Các điện cực hiện nay trên thị trường có kích thước từ 2,6 đến 6,0 Fr, đầu thẳng hoặc cong, hoặc xoắn hình chữ S. Điện cực thẳng thường dễ lái, phù hợp với tĩnh mạch ngoằn ngoèo, chúng thường có các mấu để cố định. Điện cực cong, xoắn thường chọn cho tĩnh mạch lớn, thẳng, dài, làm tăng khả năng cố định và tiếp xúc với ngoại mạc thất trái (Hình 7, 4). Cần đặc biệt lưu ý rằng điện cực xoắn thường phải đặt hết phần xoắn sâu vào xoang vành, nếu không dễ bị tuột điện cực (Hình 12).
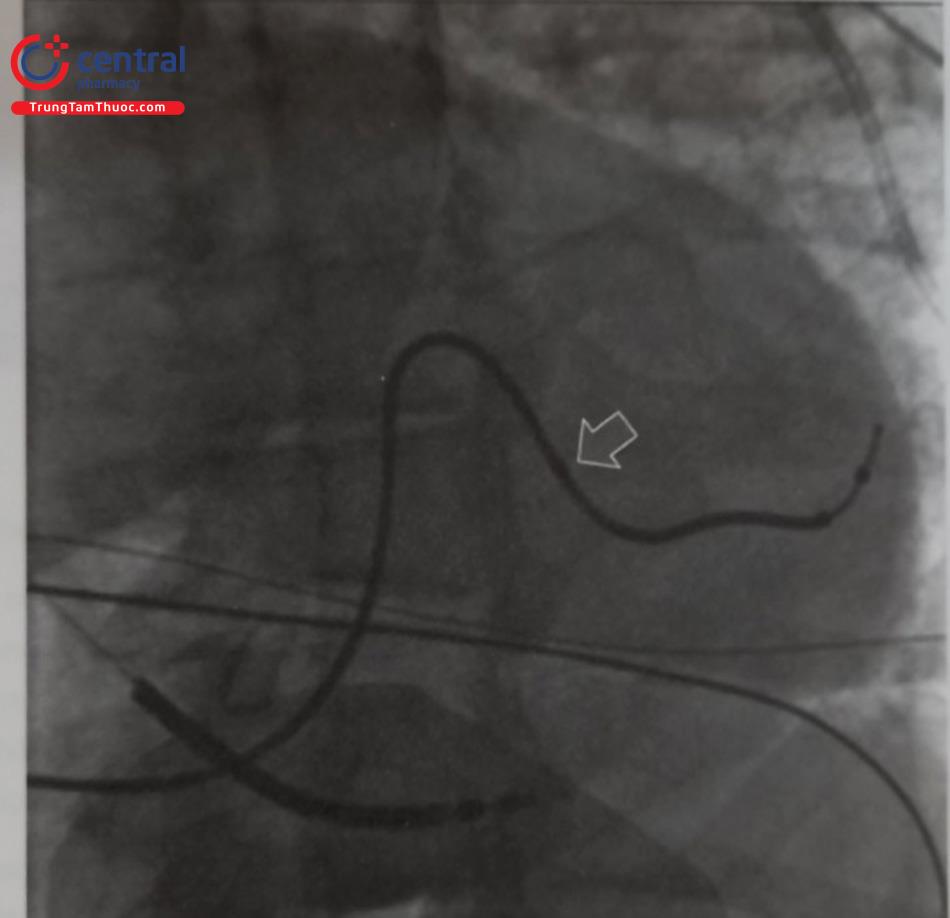
Tạo nhịp thất trái đa điểm
Chức năng tạo nhịp đa điểm có thể thực hiện ở máy CRT với điện cực thất trái 4 cực. Tạo nhịp từ 2 vị trí khác nhau tạo 2 vector tạo nhịp, cho phép cơ thất trái đồng bộ tốt hơn (Hình 13).
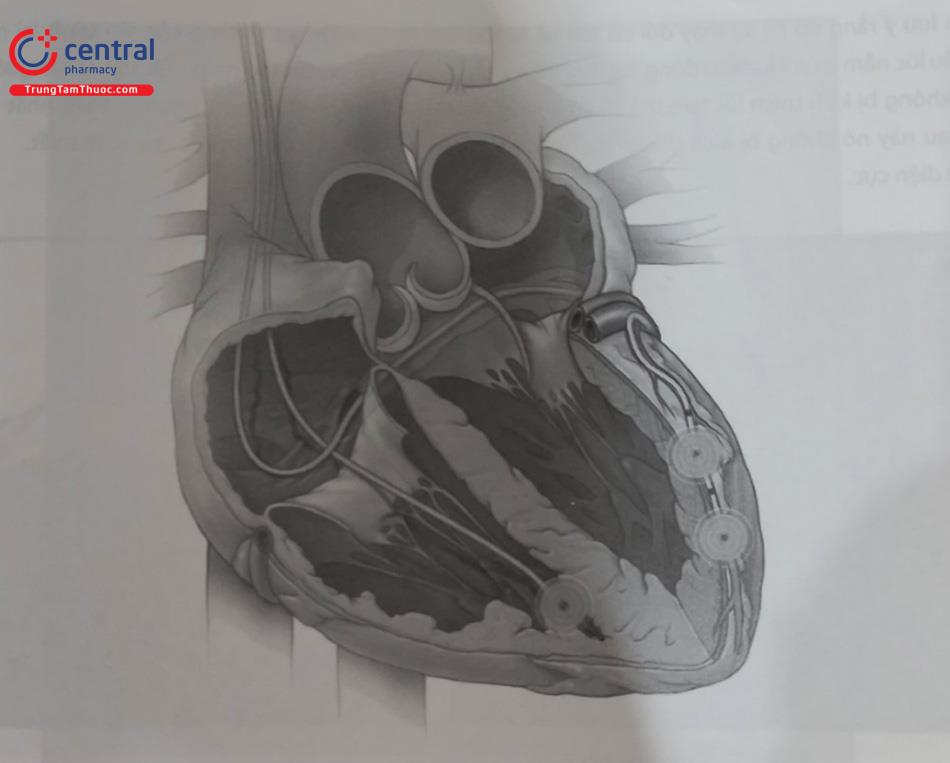
Các trường hợp khó đặt điện cực thất trái:
- Giải phẫu không phù hợp
Có tới 20% bệnh nhân không có nhánh tĩnh mạch vành vươn tới thành tự do thất trái để tối ưu hoá Một số trường hợp có đủ nhánh nhưng quá nhỏ để đặt điện cực, hoặc quá lớn để cố định điện cực tốt. Một trường hợp khó nữa là tĩnh mạch quá xoắn, góc gập lớn, không thể lái điện cực vào được. Tuy nhiên cũng có vài mẹo để lái điện cực trong trường hợp khó như: dùng wire có thân cứng, đầu mềm, hoặc 2 wire để duỗi tĩnh mạch. Một cách khác là dùng ống thông con (inner), nhỏ hơn, mềm hơn để đặt chọn lọc vào nhánh bên (Hình 14).
Hẹp tĩnh mạch vành cũng không quá hiếm, trường hợp này có thể phải nong tĩnh mạch. Thường dùng bóng nong động mạch vành kích thước 3-4 mm, giống như trong can thiệp động mạch vành (Hình 15).
Ngưỡng tạo nhịp thất quá cao
Một vấn đề khá thường gặp là đã đưa điện cực vào được nhánh bên, có vị trí giải phẫu phù hợp nhưng ngưỡng tạo nhịp quá cao. Có thể do lớp mỡ ngoại mạc hoặc sẹo cơ Đặt điện cực vào nhánh bên khác cạnh đó thường là giải pháp đầu tiên. Tuy nhiên với nhồi máu cơ tim và sẹo cơ tim vùng thành trước, vách, thành dưới hoặc mỏm, thành tự do thất trái là lựa chọn khả dĩ.
Kích thích thần kinh hoành
Thần kinh hoành trái và phải chạy dọc 2 bên trung thất giữa (Hình 16). Thần kinh hoành trái đi dọc bờ ngoài thất trái, chia nhánh vận động tới cơ hoành và nhánh cảm giác tới màng ngoài tim, lá tạng màng phổi và phúc mạc mặt hoành. Điện cực thất trái có thể kích thích thần kinh hoành khi nó đi gần đó. Tạo nhịp với ngưỡng cao để kích thích thần kinh hoành là nghiệm pháp thường được làm. Khác biệt đáng kể giữa ngưỡng dẫn của thần kinh hoành với thất trái có thể điều chỉnh bằng cách chỉnh ngưỡng tạo nhịp thất trái. Tăng ngưỡng tạo nhịp thất trái mạn tính có thể làm mất khoảng an toàn này. Khi thần kinh hoành bị kích thích, thường cần đặt điện cực ra nhánh khác hoặc kéo điện cực lại gần hơn. Dùng điện cực 2 hoặc 4 cực với nhiều chương trình lập trình khác nhau giúp tránh kích thích thần kinh hoành.
Cần lưu ý rằng do có sự thay đổi rất lớn về tư thế giải phẫu lúc nằm so với lúc vận động, hít thở, thần kinh hoành không bị kích thích lúc làm thủ thuật không có nghĩa sau này nó không bị kích thích nữa hoặc thậm chí tuột điện cực.
Thông thường cần lập trình lại ngưỡng tạo nhịp và vector tạo nhịp thất trái. Nếu ngưỡng kích thích cơ hoành thấp hơn ngưỡng thấp nhất để thất trái dẫn, việc đặt lại điện cực chưa cần thiết.
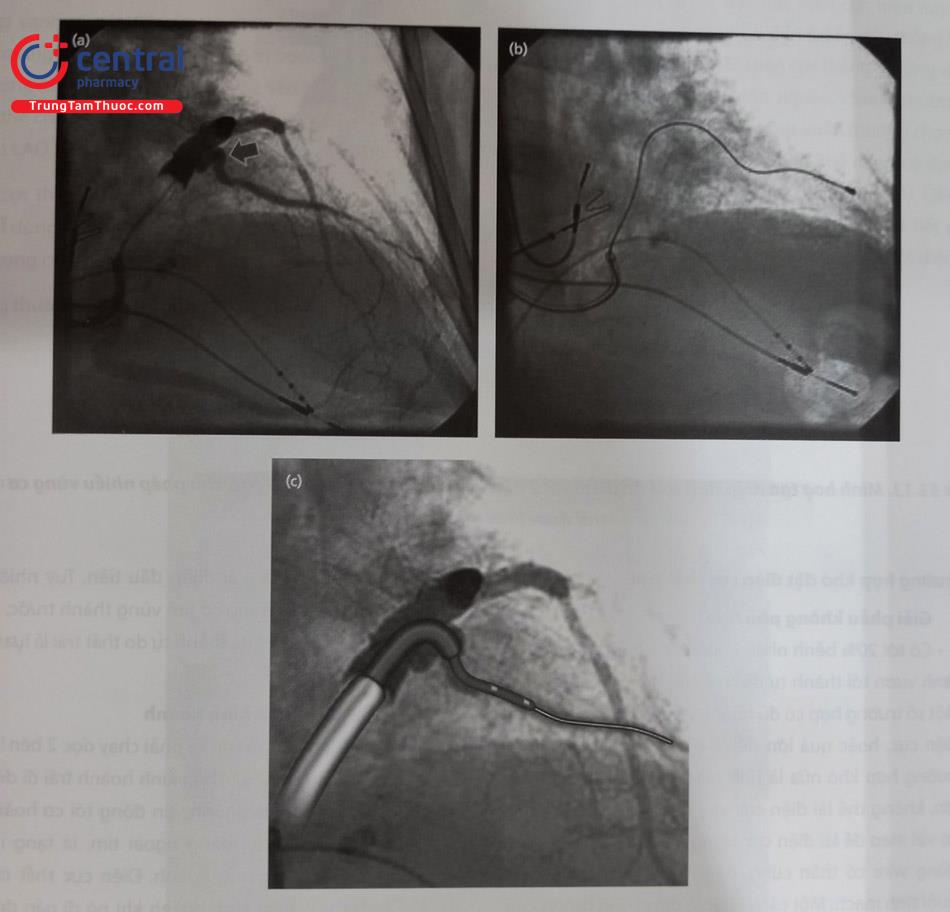
(a) Không thể đẩy điện cực 4-Fr over-the-wire vào được. (b) Dùng long sheath mẹ con để đẩy sheath con vào miệng lỗ nhánh bên hoặc vào hẳn nhánh bên, sau đó mới đẩy điện cực 4-Fr over-the-wire vào được.
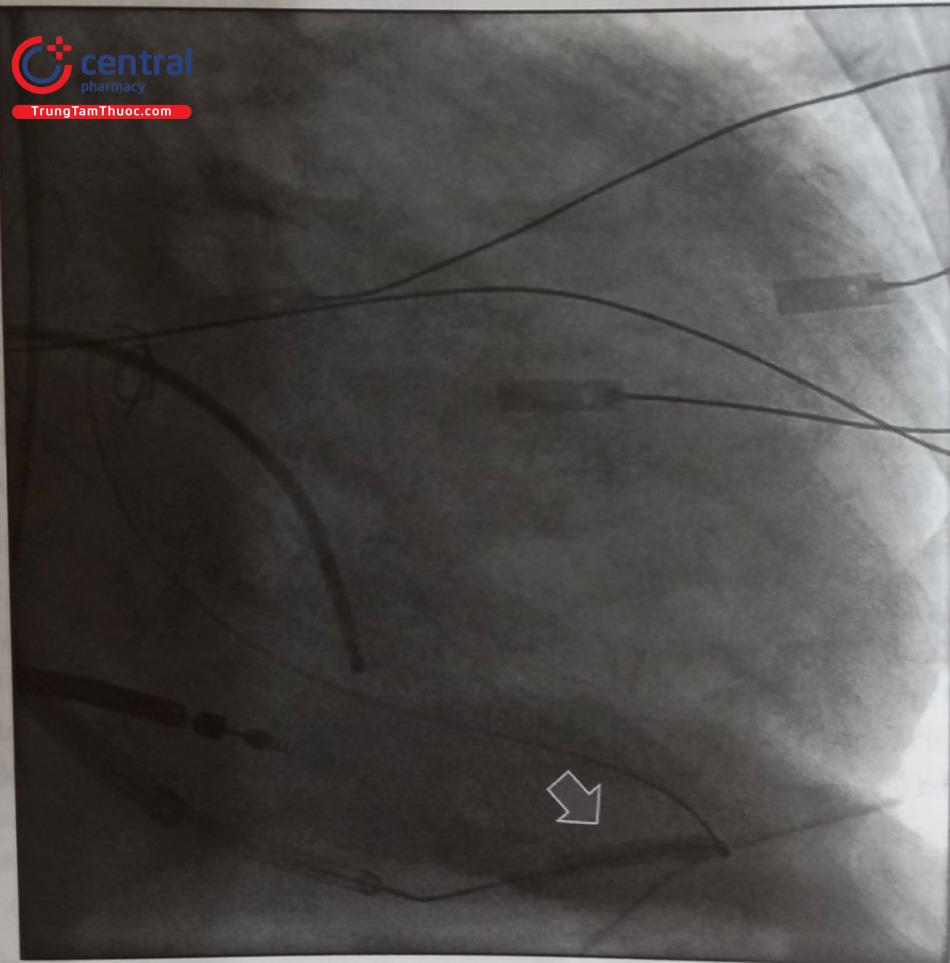
Dùng sheath can thiệp mạch thận 7-Fr và sheath con 5-Fr để đưa wire mềm 0,014” vào tĩnh mạch tim giữa. Dùng bóng cỡ 3,0×20 mm để nong. Sau đó đẩy điện cực 4-Fr qua được.
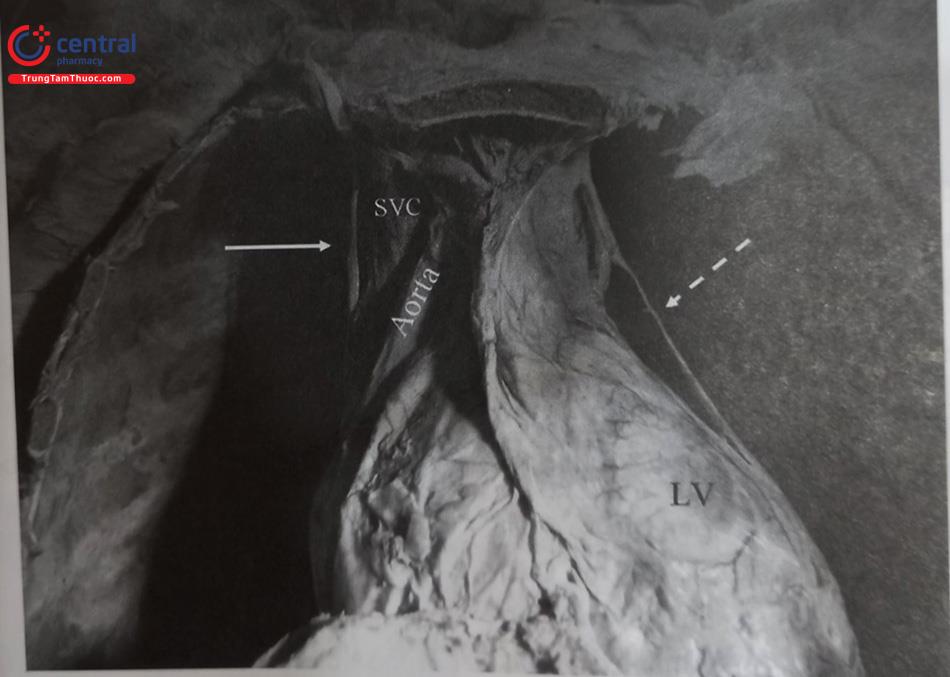
5.5.2 Kỹ thuật tạo nhịp bó His và nhánh trái
Những bệnh nhân không đáp ứng với CRT có thể cân nhắc thay thế điện cực thất phải bằng điện cực His đặt vào bó His hoặc nhánh bó trái. Nghiên cứu HOT-CRT với điện cực thất phải đặt ở vị trí bó His và nghiên cứu LOT-CRT điện cực thất phải cấy vào vị trí bó His trái đã chứng minh cải thiện chức năng tim và độ rộng QRS so với CRT truyền thống. Ngoài ra, trong khi thất bại với đặt điện cực thất trái (do ngưỡng tạo nhịp cao, giải phẫu không phù hợp), cân nhắc thay thế điện cực thất trái bằng điện cực bó His hoặc nhánh trái thay vì phải đặt điện cực thượng tâm mạc.
Kỹ thuật tạo nhịp bó His
Bước (1): Đường vào tĩnh mạch: chọc 2 đường vào tĩnh mạch riêng biệt, tạo ổ máy, đưa sheath C315HIS vào buồng thất phải dưới sự trợ giúp của dây dẫn 0,035. Rút dây dẫn và dilator ra ngoài, vừa rút sheath C315 vừa quay ngược chiều kim đồng hồ đến gần vòng van ba lá gần vị trí bó His. Luồn điện cực 3830 (điện cực cấy his) đến đầu xa của sheath, đầu gần kết nối unipolar với máy lập trình và hệ thống thăm dò điện sinh lý để tín hiệu điện thế rõ nét hơn. Thường sử dụng thử ngưỡng kênh nhĩ của máy lập trình để nhìn rõ hơn điện thế His và mức độ nhận cảm tốt hơn.
Bước (2): Tìm vị trí bó his: cẩn thận đưa đầu điện cực ra bên ngoài sheath C315 để ghi điện thế trong buồng tim, điều chỉnh sheath C315 theo chiều ngược kim đồng đồ để áp vào vùng vách, di chuyển sheath đến khi điện thế bó His có thể quan sát được. Đo khoảng His-QRS xác định vị trí điện cực trên bó His chung hay bó His phải. Sau đó đẩy sheath xa nhất có thể phủ điện cực, giúp cố định tốt hơn trong khi xoáy điện cực.
Bước (3): Xoáy điện cực
Điện cực His được xoáy bằng tay, xoáy 4-5 vòng theo chiều kim đồng hồ, trong khi xoáy giữ sheath C315 cố định vào cơ tim giúp điện cực His cố định tốt hơn. Khi thả ra điện cực xoay ngược trở lại theo chiều ngược kim đồng hồ 2-3 vòng. Rút sheath lại khoảng 2-4 cm để test độ ổn định của điện cực. Nếu khi vị trí không đạt chuẩn thì xoay điện cực theo chiều ngược kim đồng hồ để tháo xoắn, không được rút lại trực tiếp để tránh gây xé cơ tim.
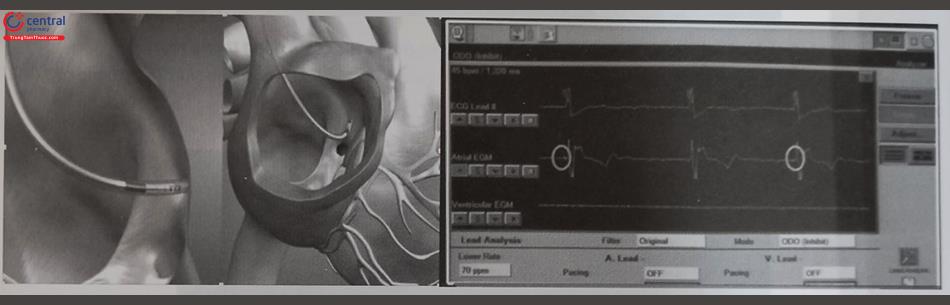
Bước (4): Thử ngưỡng tạo nhịp bó his.
Thử ngưỡng nhận cảm sóng R: sóng R có thể thấp 1-2 mV có thể được chấp nhận, nhưng cần tránh nhiễu trường xa.
Trên điện tâm đồ 12 chuyển đạo, đo độ rộng QRS và đoạn HV trong khi tạo nhịp với năng lượng cao 5V/1ms. Điện thế tạo nhịp giảm dần, trong khi giảm, quan sát ngưỡng tạo nhịp bó His chọn lọc, ngưỡng tạo nhịp không chọn lọc, ngưỡng tạo nhịp thất phải. Tuỳ vào giải phẫu của bó His mà cách chuyển dạng tạo nhịp khác nhau (tạo nhịp His không chọn lọc → tạo nhịp His chọn lọc – tạo nhịp thất phải) hay chỉ có tạo nhịp không chọn lọc bó His – tạo nhịp thất phải ở type 3 (bó His nằm sâu).
Ngưỡng yêu cầu tối thiểu tạo nhịp bó His chọn lọc, không chọn lọc là 1,5- 2V/1ms. Nếu ngưỡng cao hơn cần được xem xét chuyển sang vị trí tốt hơn.
Bước (5): Cắt sheath
Trước khi cắt sheath, kéo sheath ra tâm nhĩ phải, để điện cực His có độ chùng vừa phải. Cắt sheath bằng dao cắt chuyên biệt, sau khi cắt sheath cần đánh giá lại thông số tạo nhịp của điện cực His, nên đánh giá lại bằng cả unipolar và bipolar. Một điểm cần lưu ý, khi quan sát được sóng tổn thương của bó his, ngưỡng tạo nhịp bó His có thể giảm xuống sau 15-20 phút cố định điện cực. Cố định điện cực.
Bước (6): Chọn máy tạo nhịp phù hợp
Lập trình máy tạo nhịp ngưỡng an toàn cho cả ngưỡng tạo nhịp và ngưỡng nhận cảm của bó His/ thất phải.
Máy tạo nhịp cấy trong bó His thường yêu cầu ngưỡng nhận cảm 1 mV.
Kỹ thuật đặt điện cực nhánh bó trái
Trong tạo nhịp nhánh bó trái, điện cực thất ở phía sâu trong vách liên thất 10-15mm và từ đoạn xa của bó His tới nhánh trái và các phân nhánh. Tạo nhịp nhánh trái thành công được mô tả bởi các tiêu chuẩn sau:
Sử dụng điện cực Medtronic (sheath C315, điện cực cấy His 3830) hoặc điện cực Biotronik (dây điện cực Solia 60 và sheath Selectra 3D) và hệ thống thăm dò điện sinh lý ghi điện tâm đồ trong buồng tim và điện tâm đồ 12 chuyển đạo.
Đường vào tĩnh mạch bên trái, xác định vị trí tạo nhịp nhánh bó trái: vị trí nhánh bó trái được xác định phía dưới vùng bó His 10-15mm đường nối từ vị trí bó His đến mỏm thất phải khi nghiêng phải 300. Hình ảnh “W” ở chuyển đạo V1, QRS dương ở DII và 2 pha ở DIII khi tạo nhịp. Tuy nhiên 20% bệnh nhân không có notch ở
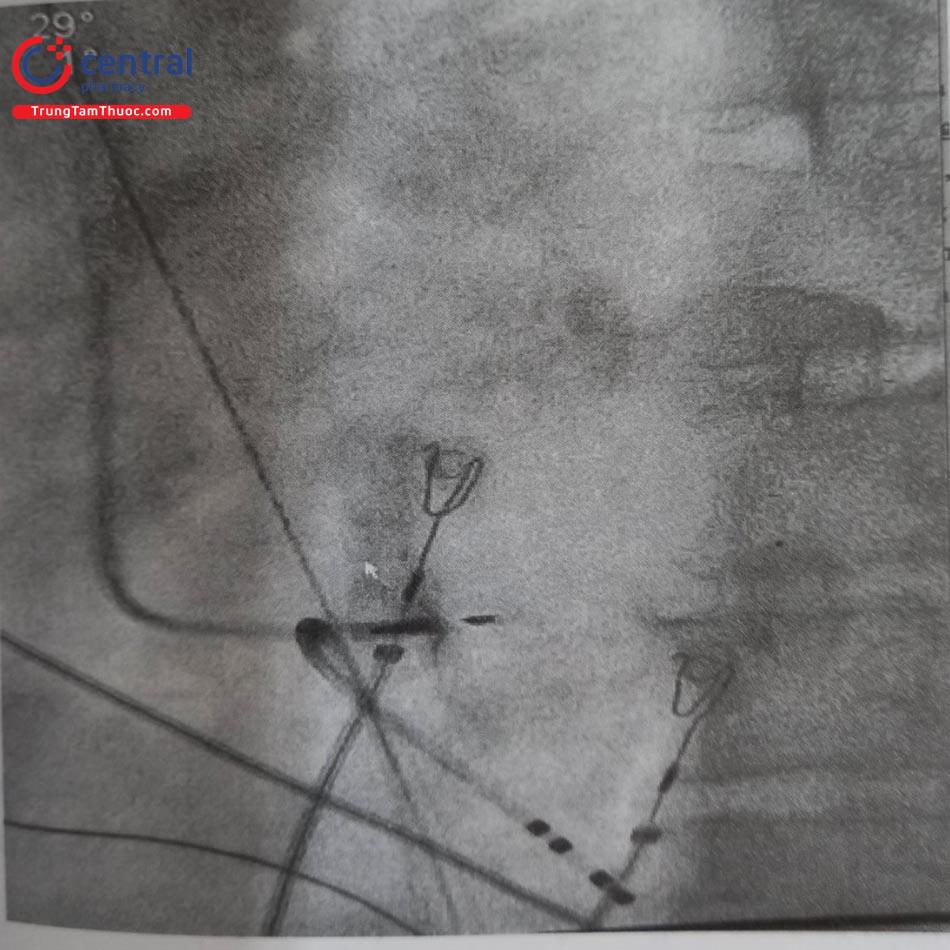
Khi xác định được vùng tạo nhịp nhánh trái, quay sheath C315 ngược chiều kim đồng hồ để duy trì hướng của đầy sheath vuông góc với vách liên thất. Kiểm tra vị trí tạo nhịp bằng chụp cản quang, xoay điện cực nhanh cùng chiều kim đồng hồ bằng cả hai tay, đầu điện cực tiến sâu vào vách liên thất. Trong quá trình xoáy điện cực theo dõi.
Trên đạo trình V1: khía trên chữ W ở sóng V1 chuyển dần sang sóng
Trở kháng tạo nhịp đơn cực tăng dần lên, trước khi giảm 100-200 Ω dấu hiệu điện cực tiến sang nội mạc cơ tim bên trái.
Tổn thương nhánh trái gặp ở 70% các trường hợp.
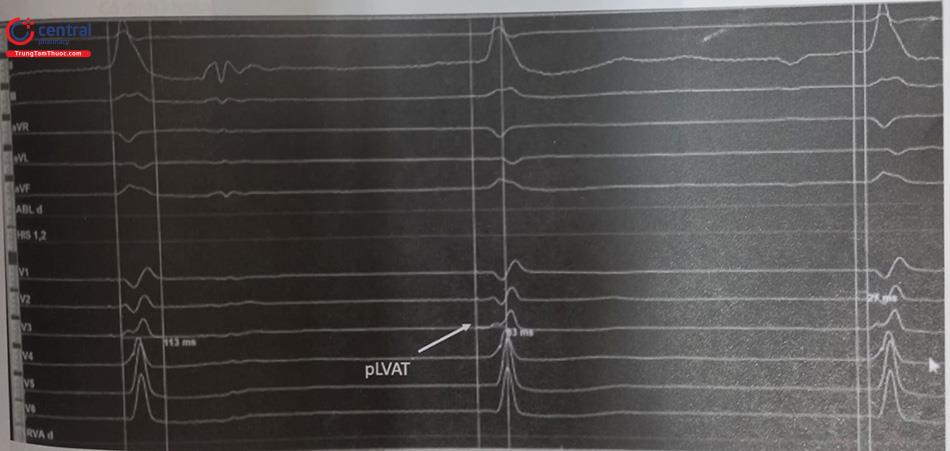
Xác định vị trí tối ưu của điện cực: vị trí điện cực tối ưu dựa vào các thông số pLVAT, trở kháng đơn cực, điện thế nhánh trái. Nhìn chung, pLVAT ngắn và không đổi (< 80 ms) ở ngưỡng tạo nhịp khác nhau trong khi hình dạng QRS ở V1 dạng qR hoặc rSR. Điện thế nhánh trái rất quan trọng ở bệnh nhân phức bộ QRS hẹp hoặc RBBB. Trở kháng đơn cực tạo nhịp khoảng 500-550 Ω với ngưỡng tạo nhịp < 1V ở độ rộng xung 0,5ms. Vách liên thất dầy 1,4 ± 0,23 cm. Trong trường hợp điện cực bị xuyên qua vách liên thất thì phải rút điện cực lại bằng cách xoay ngược chiều kim đồng hồ và đặt lại tại vị trí khác.
Cắt sheath và cố định điện cực: kéo sheath ra ngoài tâm nhĩ và cắt sheath, để điện cực độ chùng vừa phải để tránh bị kéo ra hoặc gây thủng vách liên thất muộn về sau. Sau khi cắt sheath cần kiểm tra lại ngưỡng tạo nhịp cả chế độ đơn cực và lưỡng cực.
Cài đặt chế độ tạo nhịp: ngưỡng tạo nhịp đơn cực, lưỡng cực và cực dương (anodal capture thresholds) nên được ghi lại trước khi lập trình. Cài đặt độ trễ nhĩ thất phụ thuộc vào dẫn truyền nhĩ thất tự nhiên.
6 Tiêu chí đánh giá thành công của thủa thuật
6.1 Đánh giá vị trí tạo nhịp thất trái phù hợp nhất
Theo kinh nghiệm, thường đặt điện cực thất trái vào các nhánh bên – nhánh chia vào thành bên thất trái, trong khi đó nhánh trước vách không tối ưu cho tạo nhịp. Khi đặt điện cực, soi dưới Xquang ở nhiều góc khác nhau để đánh giá vị trí phù hợp nhất. Vị trí điện cực thất phải – thất trái càng xa nhau càng tốt. Lâm sàng suy tim càng cải thiện khi đặt điện cực ở vùng đáy và thành bên so với vùng mỏm (Hình 19).
Điện đồ bề mặt là phương pháp đơn giản, hiệu quả để đánh giá vị trí tạo nhịp đã tối ưu chưa. Khi tạo nhịp thất phải, khử cực thất từ phải qua trái, làm DI dương cao. Khi tạo nhịp thất trái, vectơ khử cực ngược lại với QS ở DI. Chuyển đạo DIII giúp xác định hướng vector hướng lên (tạo nhịp từ thành trước) hay hướng ra trước (tạo nhịp từ thành dưới). Điện cực thất phải thường đặt ở vách liên thất gần mỏm, làm DIII âm sâu. Điện cực thất trái thường đặt ở thành bên và trước bên, làm hướng vector đi xuống dưới, làm DIII có dạng QS. Khi tạo nhịp 2 buồng (vách mỏm thất phải và thành bên thất trái) tạo ra vector tổng hợp với trục phải trên mạnh với hình thái qR hoặc Qr ở DI ở 90% các ca CRT. Mất Q hoặc q ở DI chứng tỏ điện cực thất trái tuột, mất dẫn hoặc chậm dẫn truyền.
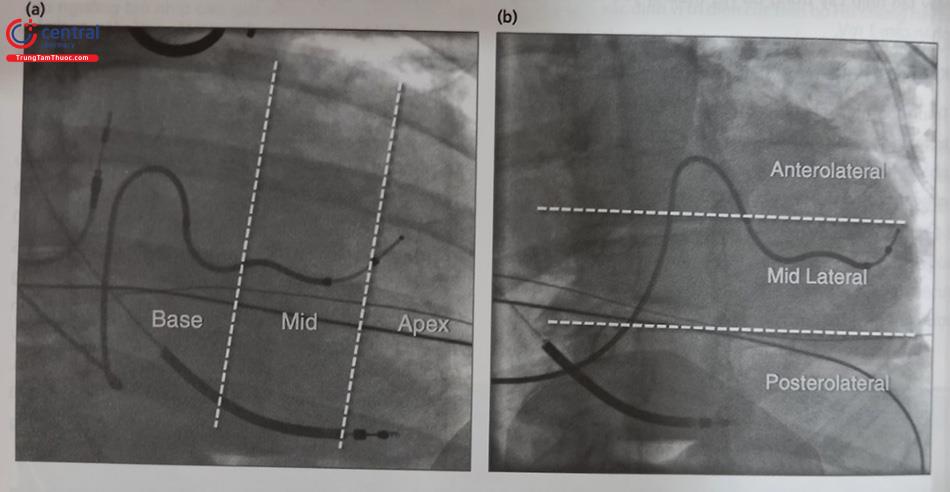
(a) góc chụp RAO chia thất trái thành 3 vùng: đáy, giữa, mỏm. (b) góc chụp LAO chia thành bên thất trái thành các phần: trước bên, giữa bên, sau bên.
Hình 20a là ví dụ về hình thái QRS khi tạo nhịp tương ứng với vị trí điện cực trên hình 20b.
Bảng 53.3. Tổng hợp các cách để đặt điện cực tối ưu
| Chụp chọc lọc tĩnh mạch vành giúp xác định rõ nhánh tối ưu để đặt điện cực |
| Điện cực thất trái có thể đặt qua nhánh bên, sau bên, trước bên hoặc tĩnh mạch tim giữa |
| Soi dưới màn tăng sáng góc RAO và hình thái QS ở DI là cách nhanh và dễ dàng để đánh giá vị trí điện cực ở thành bên thất trái |

6.2 Tiêu chí đánh giá vị trí tạo nhịp bó His và nhánh trái
6.2.1 Tiêu chí đánh giá tạo nhịp bó His thành công
Tạo nhịp bó His chọn lọc: sự kích hoạt tâm thất xảy ra chỉ do hệ thống his-purkinje. Tạo nhịp bó His chọn lọc gồm các tiêu chuẩn sau.
- S-QRS (vị trí tạo nhịp đến phức bộ QRS) = H-QRS (điện thế bó His đến phức bộ QRS) với đoạn đẳng điện.
- Điện đồ trong buồng tim với S-V=H-V.
- QRS tạo nhịp giống QRS tự nhiên.
- Một ngưỡng tạo nhịp bó
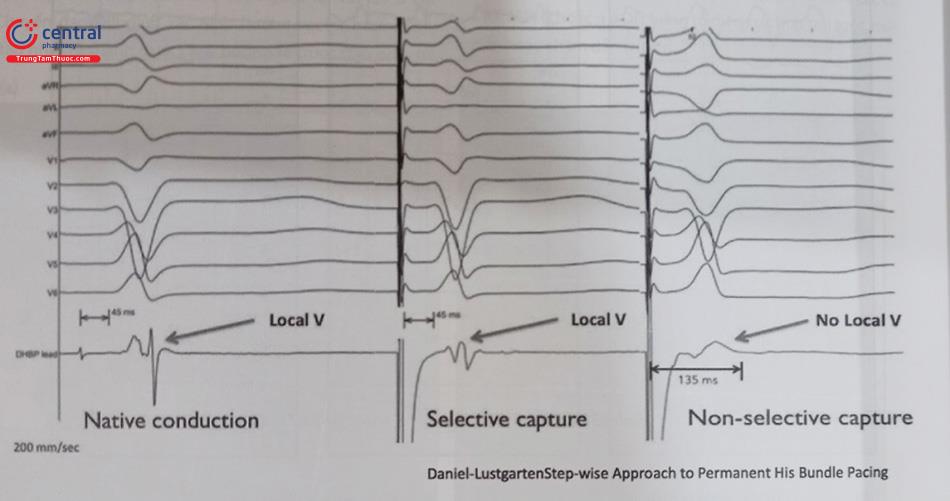
Tạo nhịp bó His không chọn lọc: kích thích một phần cơ thất tại vị trí tạo nhịp và cả bó His. Tạo nhịp bó His không chọn lọc gồm các tiêu chuẩn sau.
- S-QRS < H-QRS. Không có đoạn đẳng điện giữa vị trí tạo nhịp và
- Xuất hiện điện đồ thất ngay sau spike tạo nhịp.
- QRS tạo nhịp thường rộng hơn QRS tự nhiên.
- Hai ngưỡng tạo nhịp (ngưỡng tạo nhịp bó His và ngưỡng tạo nhịp thất phải).
6.2.2 Tiêu chí đánh gía tạo nhịp thất trái thành công
Trong tạo nhịp nhánh bó trái, điện cực thất ở phía sâu trong vách liên thất 10-15 mm và từ đoạn xa của bó His tới nhánh trái và các phân nhánh. Tạo nhịp nhánh trái thành công được mô tả bởi các tiêu chuẩn sau:
Hình dạng QRS khi tạo nhịp: dạng block nhánh phải (RBBB) với dạng qR hoặc Qr ở V1khi điện cực đặt phía dưới vị trí block nhánh trái. RBBB thường không hoàn toàn và nó phụ thuộc vào vị trí tạo nhịp như: đoạn xa của bó His, đoạn gần của nhánh trái và bệnh lý dẫn truyền His – Purkinje. Tuy nhiên, một mình hình dạng QRS không phải là yếu tố tiên lượng tốt cho dẫn truyền nhánh trái bởi vì RBBB cũng có thể quan sát được khi tạo nhịp vách liên thất trái mà không có dẫn truyền nhánh trái.
pLVAT đo từ spike tạo nhịp đến đỉnh sóng R ở V5, V6. Khi tạo nhịp thành công vào nhánh trái pLVAT thường < 80 ms và ổn định ở các ngưỡng tạo nhịp khác nhau. pLVAT tăng khi tạo nhịp từ 10V đến dưới 2V chỉ ra rằng điện cực ở xa vùng nhánh trái, tiếp tục xoáy điện cực tiến đến nhánh trái. Ngoài ra, pLVAT cũng bị ảnh hưởng bởi bệnh lý đường dẫn truyền và bệnh cơ
Điện thế nhánh trái (LBB potential): điện thế nhánh trái thường ghi được ở bệnh nhân không có block nhĩ thất hoàn toàn hoặc block nhánh trái hoàn toàn. Khoảng cách từ điện thế nhánh trái đến QRS khoảng 15-30 ms, ngoài ra nó cho phép xác định độ sâu của điện cực và vị trí bị block (Hình 22).
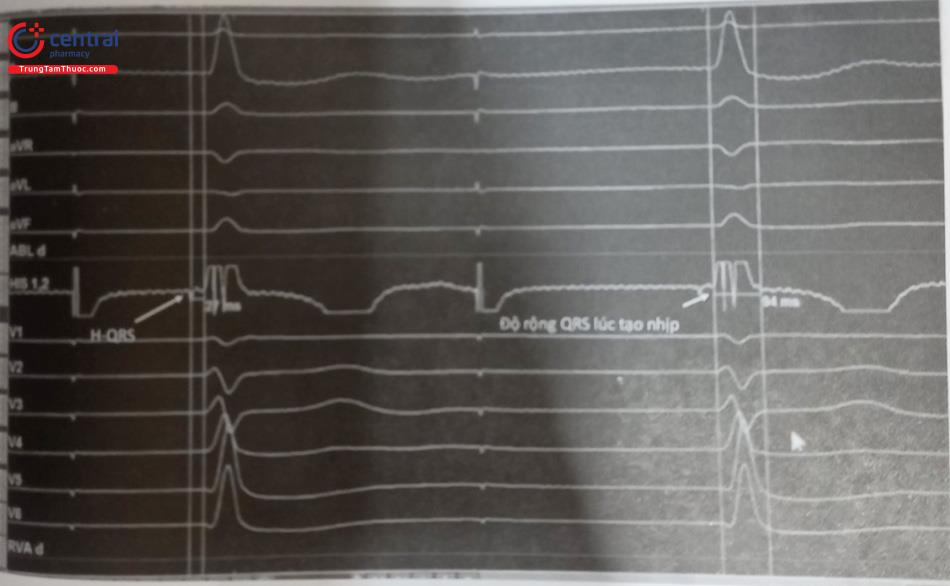
Tạo nhịp nhánh trái chọn lọc và không chọn lọc: tạo nhịp chọn lọc nhánh trái tức là chỉ dẫn truyền nhánh trái nên từ spike đến QRS có đoạn đẳng điện. Tạo nhịp nhánh trái không chọn lọc tức là ngoài dẫn truyền nhánh trái còn dẫn truyền cả cơ xung quanh dẫn đến không có đoạn đẳng điện giữa spike đến QRS. Thông thường cả tạo nhịp nhánh trái chọn lọc và không chọn lọc khi tạo nhịp ở năng lượng khác nhau thì pLVAT đều không đổi (hình 23).
7 Biến chứng của thủ thuật cấy CrT và xử trí
7.1 Biến chứng liên quan tới đặt điện cực thất trái và cách xử trí
7.1.1 Lóc tách/thủng xoang vành
Các thống kê cho thấy tỷ lệ biến chứng lóc tách xoang vành là 1,3% và tràn máu màng tim là 0,4%. Tỷ lệ biến chứng ngày càng ít đi do kinh nghiệm của phẫu thuật viên.
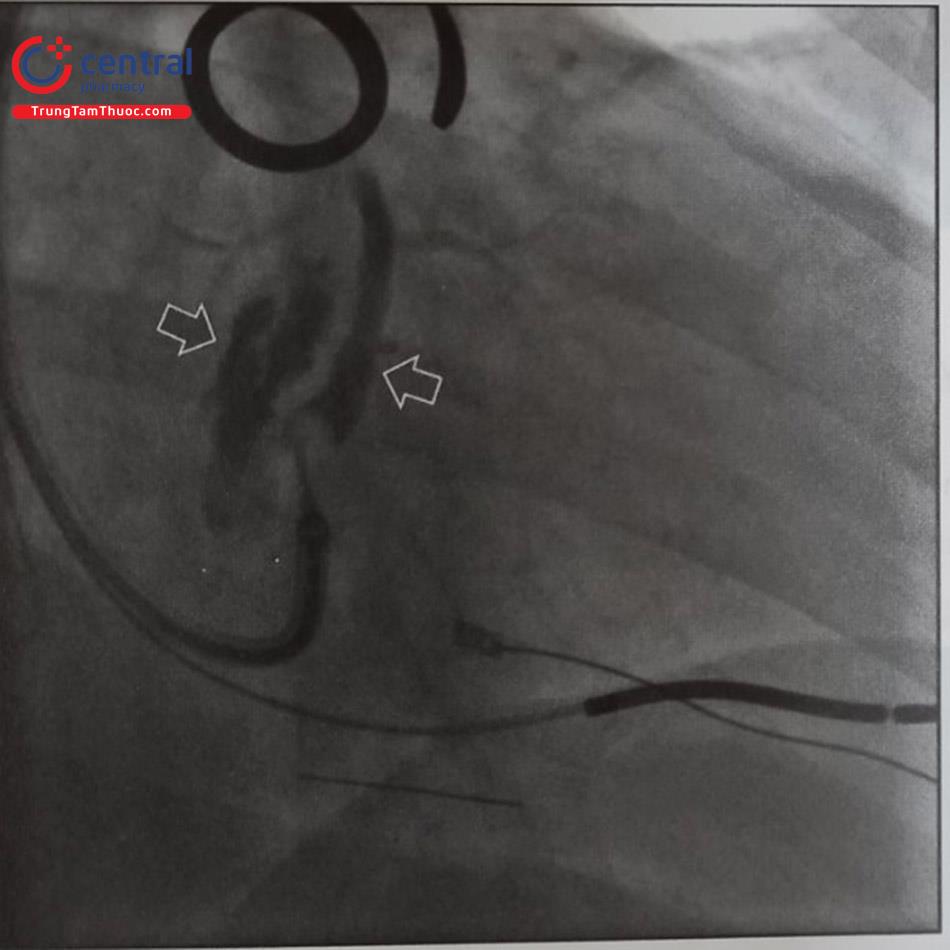
Lóc tách xoang tĩnh mạch thường do khi đưa ống thông vào hoặc đẩy wire gây lóc vào lớp nội mạc. Đẩy ống thông vào mà không có wire dẫn đường hoặc ống thông con trợ lực có thể tăng biến chứng lóc tách, do bóng bơm lúc chụp cản quang. Đẩy bóng không có wire đi trước, bơm bóng quá mức, đẩy bóng vào tĩnh mạch Marshall, đẩy bóng vào nhánh nhỏ là các nguyên nhân chủ yếu. Cần thao tác rất nhẹ nhàng, bơm nhẹ một ít cản quang trước để xác định chính xác vị trí bóng sau đó mới bơm căng bóng và chụp (Hình 53.24). Guidewire hoặc introducer sheath có thể bị kẹt trong lòng giả của tĩnh mạch bị lóc tách. Cần nhẹ nhàng rút wire và sheath lại, dùng cản quang bơm thử ở lỗ vào xoang vành để xác định lòng thật lòng giả, có thể tiếp tục thủ thuật nếu xác định được rõ.
Vỡ xoang vành có thể gây tràn máu màng tim hoặc không. Khi có tràn máu màng tim, dẫn lưu màng tim khẩn cấp. Một số trường hợp thủng xoang vành do dầu wire đâm xuyên, những trường hợp này thường không gây tràn nhiều máu màng tim và mất huyết động.
7.1.2 Tuột điện cực thất trái
Tuột điện cực thất trái gặp cao hơn hẳn tuột điện cực thất phải từ 2,8 đến 10,6%. Các nguyên nhân phổ biến gồm: không đủ chiều dài điện cực phần nằm trong nhĩ phải, vị trí đầu xa không ổn định, không đẩy đầu xa đủ sâu vào nhánh xoang vành, đặt điện cực xoắn vào nhánh quá nông.
Kiểm tra lại máy và chụp lại Xquang sau 24 giờ hết sức cần thiết. Nếu điện cực tuột hẳn, thất trái mất dẫn, khi đặt lại cần chọn nhánh khác, ví dụ sâu hơn, đặt xa hơn, góc tốt hơn. Một số trường hợp điện cực nhiều cực bị tuột không hoàn toàn, có thể chấp nhận không đặt lại nếu chỉnh được các vector và ngưỡng tạo nhịp hợp lý, vẫn đảm bảo được chức năng máy.
7.1.3 Tăng ngưỡng và bật điệnc cực bó His và nhánh trái
Tỷ lệ bật điện cực His là 2% trong các nghiên cứu lớn gần đây. Tăng ngưỡng tạo nhịp chọn lọc và không chọn lọc hay gặp ở người bệnh đặt tạo nhịp bó His. Tuy nhiên, cùng với sự phát triển của điện cực tạo nhịp bó His và kinh nghiệm của phẫu thuật viên, tỷ lệ này ngày càng thấp hơn.
Tạo nhịp nhánh trái về mặt bản chất giống tạo nhịp của thất phải ở vị trí vùng cao của vách liên thất. Ngoài biến chứng gây thủng vách liên thất, các biến chứng còn lại giống như biến chứng tạo nhịp thất phải. Khi xoáy điện cực nhánh trái gây thủng vách liên thất, cần xoay ngược chiều kim đồng hồ và đặt điện cực tại vị trí khác. Phần lớn các biến chứng gây thủng vách liên thất trong tạo nhịp nhánh bó trái không cần xử lý gì.
7.2 Biến chứng liên quan đến chọc mạch, điện cực thất phải và nhĩ phải, máy CRT (Xem thêm cấy máy rung tự động (ICD))
8 Theo dõi kết quả sau can thiệp và cách khắc phục
8.1 Lập trình để tối ưu hoá CRT
8.1.1 Tối ưu hoá AV và VV
Tối ưu hóa các thông số được lập trình có vai trò quan trọng để tối đa hóa đáp ứng điều trị. Cả hai khoảng thời gian AV và VV đã chứng minh lợi ích huyết động cấp tính. Tuy nhiên, các nghiên cứu đa trung tâm cho đến nay vẫn chưa cho thấy lợi ích lâm sàng lâu dài. Phương pháp lập trình tối ưu hoá CRT dưới hướng dẫn của siêu âm tim được sử dụng nhưng chưa chứng minh được hiệu quả rõ ràng. Do đó, vai trò và hiệu quả của tối ưu hóa AV và VV trong việc cải thiện kết quả lâm sàng ở CRT vẫn chưa rõ ràng. Hiện tại, tối ưu hóa AV và VV được sử dụng trên cơ sở cá nhân hóa.
8.1.2 Tạo nhịp hai thất trái tối đa
Tỷ lệ tạo nhịp hai thất là một yếu tố dễ bị bỏ qua. Mục tiêu lý tưởng là tạo nhịp 2 thất 100%, thường không khó đạt được trong nhịp xoang. Tuy nhiên, trong rung nhĩ (AF), tỷ lệ tạo nhịp hai thất phụ thuộc vào tần số thất và tốc độ tạo nhịp. Thường thấy các nhịp dẫn truyền nội tâm thất không liên tục, làm giảm hiệu quả của CRT. Không có tỷ lệ phần trăm xác định được tạo nhịp hai thất không đáp ứng. Trong trường hợp rung nhĩ bác sĩ nên cắt đốt nút nhĩ thất để tăng tỷ lệ tạo nhịp hai thất.
Bảng 53.4. Tối ưu hoá liệu pháp tái đồng bộ cơ tim (CRT)
| Thông số | Cái đặt tiêu chuẩn | Tối ưu hoá CRT | Lợi ích lâm sàng (so với tiêu chuẩn) |
| Độ trễ nhĩ thất | Cố định khoảng AV 120ms (100-120ms) | Siêu âm Doppler: thời gian trễ AV ngắn nhất mà không cắt ngắn sóng A (Phương pháp Ritter) hoặc thay đổi chức năng tâm thu thất trái. Thuật toán trên máy CRT (Smart delay, Quick-opt) | Không chắc chắn hoặc ít (một vài ng- hiên cứu nhỏ cho thấy lợi ích) Không chắc chắn (2 nghiên cứu ngẫu nhiên cho kết quả âm tính) |
| Độ trễ VV |
Tạo nhịp 2 thất | Siêu âm: mất đồng bộ thất trái Siêu âm Doppler: thể tích nhát bóp lớn nhất. Điện tâm đồ: tạo nhịp LV có QRS hẹp nhất; sự khác biệt giữa tạo nhịp 2 thất và QRS trước cấy. Các thuật toán trên thiết bị (Expert ‐ Ease, Quick Opt, Tăng tốc nội tâm mạc đỉnh điểm) | Không chắc chắn hoặc ít Không chắc chắn (một RCT âm tính, một nghiên cứu dương tính) Không biết (không có nghiên cứu so sánh) Không chắc chắn hoặc ít (3 RCT). |
| Tạo nhịp thất trái đơn độc | Đồng thời hai thất | Không thua kém |
Chú thích: LV: Thất trái; RCT: Thử nghiệm lâm sàng ngẫu nhiên có đối chứng.
Lập trình trong HOT-CRT (tối ưu hoá điều trị tái đồng bộ cơ tim bằng tạo nhịp bó His) và LOT-CRT (tối ưu hoá điều trị tái đồng bộ cơ tim bằng tạo nhịp nhánh trái):
Tối ưu hoá lập trình trong HOT-CRT và LOT-CRT khác với CRT truyền thống. Trong CRT truyền thống, VV delay thường được lập trình với tạo nhịp thất trái trước tạo nhịp thất phải 10-40 ms. Trong HOT-CRT, điện cực đặt ở vị trí bó His sẽ khử cực thất phải theo bó His bên phải nên giữ được đồng bộ trong thất phải. S-QRS trong HOT-CRT thường 35- 55 ms (His-QRS). Do vậy, trong HOT-CRT cài đặt độ trễ VV với tạo nhịp bó His sớm hơn thất trái 40-60 ms. Trong tạo nhịp LOT-CRT, thời gian từ spike-QRS khoảng 20 ms dẫn đến độ trễ VV cài đặt tạo nhịp nhánh trái sớm hơn thất trái 20-40 ms.
8.2 Trường hợp không đáp ứng với CRT
Đáp ứng lâm sàng của CRT bao gồm: cải thiện NYHA lớn hơn 1 mức độ, cải thiện khoảng cách đi bộ 6 phút trên 10% hoặc trên 50 mét, cải thiện phân suất tống máu thất trái (EF) hoặc các thang đo chất lượng sống. Đa số các trường hợp đặt CRT đáp ứng tốt, tuy nhiên có 30% bệnh nhân không đáp ứng CRT. Tiêu chuẩn của không đáp ứng tuỳ thuộc vào tiêu chuẩn lâm sàng nào được lựa chọn. Bảng đánh giá các yếu tố ảnh hưởng đến hiệu quả của
Bảng 53.5. Các yếu tố ảnh hưởng tới hiệu quả của CRT
| Yếu tố | Dễ đáp ứng tốt | Kém đáp ứng |
|---|---|---|
| Đặc điểm của bệnh nhân: | ||
Bệnh cơ tim Giới | Không do thiếu máu cục bộ Nữ | Do thiếu máu cục bộ Nam |
Độ rộng QRS Hình thái QRS Thể tích thất trái cuối tâm trương | >150 ms Block nhánh trái hoàn toàn 180-240 ml | <150 ms Block nhánh phải >240 mL |
| Mất đồng bộ thất | Có | Không |
Sẹo cơ tim Giãn, suy chức năng thất phải | Ít sẹo, không xuyên thành Không | Có nhiều, xuyên thành Có |
| Yếu tố có thể thay đổi được: | ||
| Vị trí điện cực thất trái | Thành bên, đáy thất trái | Thành trước, vách thất, mỏm |
| Mức độ tạo nhịp | 99 – 100% | < 99%, rung nhĩ, ngoại tâm thu |
| Tối ưu hoá A-V và V-V | Tối ưu | Không tối ưu |
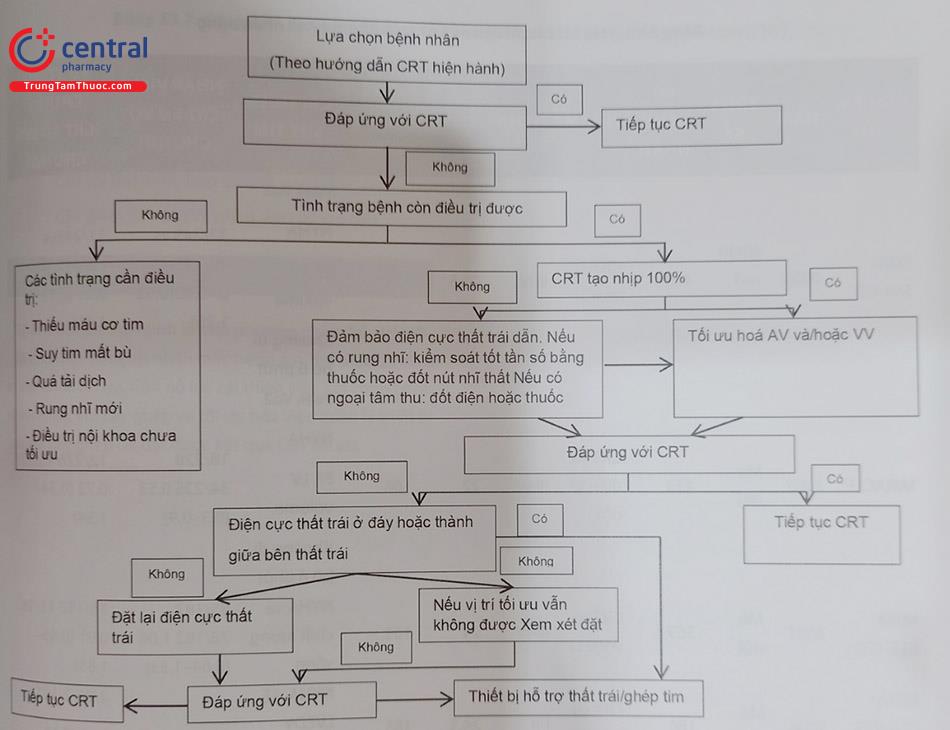
Khi gặp một bệnh nhân không đáp ứng hoặc đáp ứng kém với CRT, cần đánh giá những yếu tố liên quan như bệnh nền cần điều trị, lập trình lại CRT. Hình 53.25 là phác đồ tiếp cận với trường hợp không đáp ứng với CRT.
9 Kết quả cấy CRT qua các nghiên cứu
9.1 Lợi ích lâm sàng
Dữ liệu từ hơn 10 thử nghiệm lâm sàng trên 8000 bệnh nhân cho kết quả không thể bàn cãi về lợi ích của CRT cho bệnh nhân suy tim (Bảng 53.6). Mức độ lợi ích không đồng nhất ở các nhóm bệnh nhân khác nhau. Bao gồm cải thiện NYHA, cải thiện chất lượng cuộc sống, Peak Vo2, khoảng cách đi bộ 6 phút, nhập viện và tử vong vì suy tim.
Bảng 53.6. Tóm tắt các dữ liệu về CRT trên nhóm bệnh nhân nặng
| Nghiên cứu | Năm | Thiết kế | Số bệnh nhân | Nhóm | NYHA | EF(%) | QRS trung bình | Cải thiện suy tim | Nhập viện (CRT so với chứng) | Tử vong chung (CRT so với chứng) |
| CON- TAK-CD | 2000 | Nhãn mở | 490 | CRT-D và ICD | II-IV | 21,5 | 158 | Peak Vo2 NYHA EF, LV volume Khoảng đi bộ 6 phút | 32/245 vs 39/245, p=0,82(0,53- 1,26) | 11/245vs 16/245, p= 0,69 (0,33- 1,45) |
| MIRACLE | 2002 | Mù đôi | 453 | CRT và điều trị nội | III-IV | 22 | 166 | Peak Vo2 NYHA EF, LV volume Khoảng đi bộ 6 phút | 18/228 34/225 0,53 (0,3–0,9) | 12/228 16/225 0,73 (0,34– 1,54) |
| MIRA- CLE-ICD | 2003 | Mù đôi | 369 | CRT so với ICD | III-IV | 24 | 163 | NYHA và chất lượng sống | 85/187 78/182 1,06 (0,84–1,33) | 14/187 15/182 0,91 (0,45– 1,83) |
| MIRA- CLE-ICD II | 2004 | Mù đôi | 186 | CRT so với ICD | I-II | 24,5 | 165 | NYHA, EF, LVEDV | 2/85 2/101 1,19 (0,17– 8,26) | |
| RAF |
9.2 Lợi ích đối với suy tim nặng
Các nghiên cứu đầu tiên về CRT đều trên nhóm bệnh nhân suy tim nặng.
9.3 Độ rộng QRS ảnh hưởng đến tiên lượng
Độ rộng QRS trên điện đồ bề mặt vẫn là tiêu chuẩn chủ yếu cho chỉ định CRT. Các nghiên cứu đã chỉ ra rằng, CRT có lợi ích hơn ở bệnh nhân có QRS trên 150 ms, trong khi những bệnh nhân QRS dưới 150 ms ít lợi ích hơn.
Cần nhấn mạnh rằng QRS rộng không phải tất cả đều đi đôi với mất đồng bộ cơ học. Trong trường hợp này, kể cả QRS rất rộng nhưng CRT không cải thiện được nhiều sức bóp cơ tim. Ngược lại một số trường hợp QRS không quá rộng nhưng bằng chứng trên siêu âm hoặc MRI thấy mất đồng bộ, lợi ích của CRT vẫn rất rõ ràng.
9.4 Hình thái QRS ảnh hưởng tới hiệu quả điều trị
Phần lớn ứng viên cho CRT đều có block nhánh trái hoặc block nhánh trái do tạo nhịp thất. Khi có block nhánh trái, bệnh nhân đáp ứng tốt hơn với CRT và là yếu tố ảnh hưởng độc lập, bên cạnh độ rộng QRS. Tạo nhịp thất trái kích thích sớm vùng thành bên thất trái bị chậm dẫn truyền sẽ làm cải thiện đồng bộ cơ thất. Bệnh nhân block nhánh trái hoàn toàn thường cải thiện NYHA, cải thiện tiên lượng sống và EF tốt hơn bệnh nhân có block nhánh phải.
Bảng 53.7. Các lợi ích lâm sàng chủ yếu của liệu pháp tạo nhịp tái đồng bộ cơ tim (CRT)
| QRS rộng trên 150 ms và/hoặc block nhánh trái là yếu tố thuận lợi cho CRT |
| CRT có hiệu quả ở cả bệnh nhân suy tim vừa đến nặng |
| CRT cải thiện triệu chứng, khả năng gắng sức và chất lượng sống |
| CRT cải thiên sức bóp cơ thất trái, giảm tái cấu trúc thất trái |
| CRT giảm tử vong và nhập viện do suy tim |
10 Kết luận
CRT đã được chứng minh là một phương pháp điều trị hiệu quả cho một số bệnh nhân mắc bệnh suy tim mặc dù điều trị nội khoa tối ưu. Cần nỗ lực cải thiện việc lựa chọn bệnh nhân trước khi cấy ghép và tối ưu hóa việc quản lý thiết bị sau khi cấy ghép để đạt được kết quả CRT tối ưu.
11 Tài liệu tham khảo
- Joseph Marine, Charles J. Love, and Jeffrey A. Brinker. Techniques of pacemaker and ICD implantation and removal. Cardiac Pacing and ICDs. Willey Blạckwell 2020, 131-206.
- Michael Field and Michael R. Gold .The implantable cardioverter–defibrillator. Cardiac Pacing and ICDs. Willey Blạckwell 2020, 315-356.
- Yong-Mei Cha and Ammar M. Killu .Cardiac resynchronization therapy, Cardiac Pacing and ICDs. Willey Blạckwell 2020, 357 -394.
- Kevin Jackson . ICD follow-up and troubleshooting, Cardiac Pacing and ICDs. Willey Blạckwell 2020, 395-416.
- Conrad N, Judge A, Tran J, et al. Temporal trends and pat- terns in heart failure incidence: a population‐based study of 4 million individuals. Lancet 2018;391(10120):572–580.
- Gheorghiade M, Pang Acute heart failure syndromes. J Am Coll Cardiol 2009;53(7):557–573.
- TournouxFB,ManzkeR,ChanRC,etal.Integratingfunc- tional and anatomical information to facilitate cardiac resynchronization Pacing Clin Electrophysiol2007;30(8):1021–1022.
- Linde C, Abraham WT, Gold MR, et al. Randomized trial of cardiac resynchronization in mildly symptomatic heart failure patients and in asymptomatic patients with left ventricular dysfunction and previous heart failure J Am Coll Cardiol 2008;52(23):1834–1843.
- Tang ASL, Wells GA, Talajic M, et Cardiac‐ resynchronization therapy for mild‐to‐moderate heart failure. N Engl J Med 2010;363(25): 2385–2395.
- Moss AJ, Hall WJ, Cannom DS, et al. Cardiac‐ resynchronization therapy for the prevention of heart‐ failure events. N Engl J Med 2009;361(14):1329–1338.
- Yu CM, Chau E, Sanderson JE, et al. Tissue Doppler echocardiographic evidence of reverse remodeling and improved synchronicity by simultaneously delaying regional contraction after biventricular pacing therapy in heart failure. Circulation 2002;105(4):438–445.
- Chakir K, Depry C, Dimaano VL, et al. Gαs‐biased β2‐ adrenergic receptor signaling from restoring synchro- nous contraction in the failing heart. Sci Transl Med2011;3(100):100ra88.
- Wang S‐B, Foster DB, Rucker J, et al. Redox regulation of mitochondrial ATP synthase: novelty and significance. Circ Res 2011;109(7): 750–757.
- Aiba T, Hesketh GG, Barth AS, et al. Electrophysiological consequences of dyssynchronous heart failure and its restoration by resynchronization therapy. Circulation2009;119(9):1220–1230.
- Epstein AE, DiMarco JP, Ellenbogen KA, et al. ACC/AHA/ HRS 2008 guidelines for device‐based therapy of cardiac rhythm abnormalities. Circulation 2008;117(21):e350 –e408.

