Cấy máy phá rung tự động - Một phương pháp hồi sinh tim phổi
Nguồn: Sách Tim mạch can thiệp
Chủ biên
PGS.TS.BS.Phạm Mạnh Hùng
Tác giả
TS.BSNT.Trần Song Giang
ThS.BSNT.Đặng Minh Hải
ThS.BSNT.Đào Minh Đức
ThS.BSNT.Bùi Văn Thường
ThS.BSNT.Trịnh Văn Nhị
Cấy máy phá rung tự động (ICD) như một phương pháp hồi sinh tim phổi. Kỹ thuật đó như thế nào? Hãy cùng Trung Tâm Thuốc Central Pharmacy (trungtamthuoc.com) tìm hiểu trong bài viết sau đây.
1 Đại cương
Rung thất (Ventricular Fibrillation-VF) là nguyên nhân chủ yếu gây đột tử do tim (Sudden Cardiac Death-SCD). Rung thất có thể xuất hiện ngay từ đầu hoặc có thể xuất hiện sau cơn nhịp nhanh thất. Các biện pháp hồi sinh tim phổi như: ép tim ngoài lồng ngực, thông khí nhân tạo có thể hỗ trợ tuần hoàn trong một khoảng thời gian nhất định cho bệnh nhân ngừng tim, những phương pháp duy nhất có hiệu quả để cắt cơn VF là phá rung tim. Sự thành công của việc sốc điện ngoài lồng ngực trong cấp cứu bệnh nhân rung thất, máy phá rung tự động cấy trong cơ thể người (Implantable Cardioverter Defibrillator – ICD) đã được nghiên cứu và phát triển.
Năm 1980, lần đầu tiên máy ICD được cấy vào trong cơ thể người. Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) đã phê duyệt để sử dụng trên lâm sàng vào năm 1985, ban đầu chỉ để phòng ngừa thứ phát ở những bệnh nhân sống sót sau ngừng tim. Tỷ lệ thành công cao trong việc cắt cơn VF/VT (Rung thất/Nhanh thất) cùng với kết quả giảm tỷ lệ tử vong qua một số thử nghiệm lâm sàng lớn, thì ICD được coi là lựa chọn đầu tiên trong dự phòng đột tử thứ phát và tiên phát ở bệnh nhân có nguy cơ đột tử do VT/VF.
Các máy ICD đầu tiên rất lớn, đòi hỏi phải phẫu thuật lồng ngực để đặt miếng dán điện cực vùng thượng tâm mạc và máy được cấy vào ổ bụng. Phẫu thuật phức tạp này dẫn đến tình trạng tái nhập viện sau phẫu thuật trung bình khoảng 1 tuần. Các máy phát xung có tuổi thọ pin dưới 2 năm và hầu như không có khả năng chẩn đoán hoặc tạo nhịp tim. Những thiết bị ban đầu này chỉ được FDA chấp thuận sử dụng ở những bệnh nhân sống sót sau nhiều lần ngừng tim. Trong những thập kỷ tiếp theo, công nghệ ICD đã phát triển để cung cấp thông tin chi tiết về hình thái và tỷ lệ rối loạn nhịp tim, điện đồ trong buồng tim được lưu trữ (EGM) trước, trong và sau khi điều trị, cũng như thông tin chẩn đoán để đánh giá tính toàn vẹn của điện cực và trạng thái sinh lý hoạt động của quả tim.
Ngày nay, mặc dù giảm đáng kể kích thước và tăng khả năng chẩn đoán, nhưng thời gian pin của ICD vẫn là vấn đề phức tạp. Trong khi đó, bên cạnh vai trò cơ bản của các ICD là để điều trị và dự phòng đột tử do tim, chúng còn có vai trò trong một số bệnh lý khác bao gồm rối loạn nhịp tim chậm, rối loạn nhịp nhĩ và suy tim bằng liệu pháp tái đồng bộ tim (CRT-D). Gần đây, kĩ thuật cấy máy ICD dưới da (S-ICD) được phát triển nhằm thay thế cho ICD truyền thống ở bệnh nhân có bất thường đường vào tĩnh mạch hoặc có rối loạn nhịp thất đơn thuần không cần phải tạo nhịp.
2 Chỉ định và chống chỉ định cấy máy ICD
Cấy máy ICD được chỉ định nhằm mục đích phòng ngừa đột tử tiên phát (cho những bệnh nhân có nguy cơ đột tử do tim cao, mặc dù chưa có cơn nhịp nhanh thất hoặc rung thất) và phòng ngừa đột tử thứ phát (cho những bệnh nhân đã bị các rối loạn nhịp tim đe dọa tính mạng như: nhịp nhanh thất hoặc rung thất).
Theo khuyến cáo của Hội tim mạch học Hoa Kỳ/ Trường môn tim mạch học Hoa Kỳ/ Hội nhịp tim Hoa Kỳ năm 2017 (AHA/ACC/HRS) và Hội tim mạch châu u (ESC) 2021, cấy máy ICD được chỉ định trong các trường hợp bệnh cơ tim do thiếu máu, bệnh cơ tim không do thiếu máu (Bảng 52.1) và trong một số bệnh lý rối loạn nhịp tim, bệnh lý cơ tim ít gặp hơn (Bảng 2).
Bảng 1. Các chỉ định cấy ICD ở bệnh nhân bị bệnh cơ tim do thiếu máu hoặc không do thiếu máu
| Dự phòng thứ phát | |
| Loại I | Ngưng tuần hoàn do nhịp nhanh thất hoặc rung nhĩ được cứu sống hoặc nhịp nhanh thất có huyết động không ổn định (bằng chứng B) hoặc nhịp nhanh thất không phải do nguyên nhân có thể đảo ngược(bằng chứng B). Ngất không rõ nguyên nhân ở bệnh nhân có bênh cơ tim do thiếu máu và thăm dò điện sinh lý tim gây được cơn nhịp nhanh thất bền bỉ(bằng chứng B). |
| Loại II | Ngất được cho là nhịp nhanh thất ở bênh nhân bệnh cơ tim do thiếu máu có phân suất tống máu thất trái (LVEF) không phù hợp do dự phòng tiên phát ICD(bằng chứng B). |
| Loại I | Bệnh cơ tim do thiếu máu hoặc không thiếu máu với phân số tống máu <35% và suy tim mức độ NYHA III hoặc NYHA II mặc dù điều trị nội khoa tối ưu (Bằng chứng A). Bệnh cơ tim do thiếu máu với LEVF < 30%, suy tim NYHA I mặc dù điều trị nội khoa tối ưu (Bằng chứng A). Bênh cơ tim do thiếu máu, có nhịp nhanh thất không bền bỉ, LVEF <40% và gây ra nhịp nhanh thất hoặc rung thất khi thăm dò điện tim (Bằng chứng B). |
| Loại IIa | Bệnh nhân suy tim giai đoạn cuối có kế hoạch ghép tim hoặc đặt dụng cụ hỗ trợ thất trái. |
| Loại IIb | Bệnh cơ tim không do thiếu máu vưới LVEF <35% mặc dù đã điều trị nội khoa tối ưu và suy tim NYHA (Bằng chứng B). |
Chú thích: Khuyến cáo Loại I (ICD được khuyến cáo); Loại IIa (ICD nên cấy); Loại IIb (ICD có thể cân nhắc); ICD: Máy phá rung tự động; NYHA: Phân độ suy tim theo Hiệp hội Tim mạch New York.
Bảng 2. Chỉ định ICD cho một số bệnh lý ít gặp hơn
Loại I (ICD được khuyến cáo) | Loạn sản thất phải có kèm theo yếu tố tăng nguy cơ đột tử (ngừng tuần hoàn được cứu sống, nhịp nhanh thất bền bỉ, suy chức năng tâm thất với RVEF hoặc LVEF ≤ 35% (bằng chứng B- NR). Bệnh cơ tim phì đại đã bị ngừng tim được cứu sống hoặc nhịp nhanh thất bền bỉ gây rối loạn huyết động hoặc gây ngất. (bằng chứng B-NR). Bệnh lý bất thường kênh ion của tim đã có ngừng tuần hoàn được cứu sống (bằng chứng B-NR). Nhịp nhanh thất đa hình thái do cường catecholamin và nhịp nhanh thất bền bỉ tái phát hoặc ngất mặc dù đã điều trị thuốc chẹn beta liều tối ưu (Liệu pháp thay thế cho ICD bao gồm kết hợp chẹn beta và flecainide hoặc điều trị cắt/đốt hệ giao cảm tim trái) (bằng chứng B-NR). Hội chứng Brugada type I có ngừng tuần hoàn hoặc nhịp nhanh thất bền bỉ hoặc tiền sử ngất do nhịp nhanh thất (bằng chứng B-NR). Bệnh cơ tim do nhiễm Sarcoidosis có nhịp nhanh thất bền bỉ hoặc ngừng tuần hoàn hoặc LVEF ≤ 35% (bằng chứng B-NR). Hội chứng QT dài có triệu chứng, nguy cơ cao nhưng không đáp ứng hoặc không dung nạp với chẹn beta (bằng chứng B-NR). |
Loại IIa (ICD nên cấy) | Loạn sản thất phải và ngất được nghi ngờ do rối loạn nhịp thất (bằng chứng B-NR). Bệnh cơ tim phì đại kèm theo một hoặc nhiều yếu tố nguy cơ sau: Thành thất trái dày nhất ≥ 30 mm (bằng chứng B-NR). Tiền sử gia đình có người đột tử tiên đoán do bệnh cơ tim phì đại. Một trong nhiều lần bị ngất không giải thích được nguyên nhân trong vòng 6 tháng (bằng chứng C-NR). Bệnh cơ tim phì đại với nhịp nhanh thất không bền bỉ xuất hiện tự phát (bằng chứng C-LD) hoặc huyết áp phản ứng bất thường khi gắng sức (bằng chứng B-NR) ở người có nguy cơ đột tử trung bình hoặc Bệnh cơ tim do nhiễm sarcoidosis và LVEF > 35% có bằng chứng của ngất hoặc sẹo cơ tim trên phim chụp MRI hoặc PET CT, và hoặc có chỉ định tạo nhịp vĩnh viễn (bằng chứng NR). Bệnh cơ tim do nhiễm sarcoidosis và LVEF > 35% có nhịp nhanh thất bền bỉ gây ra khi thăm dò điện sinh lý tim (bằng chứng C-LD). Bệnh thiểu sản cơ có liên quan đến tiến triển cơ tim (bằng chứng B-NR). |
| Loại IIb (ICD có thể cấy) | Bệnh nhân mắc hội chứng QT kéo dài không có triệu chứng và QTc lúc nghỉ > 500ms trong khi đã điều trị bằng thuốc chẹn beta (điều trị thay thế bao gồm tăng cường diều trị nội khoa bằng thuốc cắt bỏ hệ thần kinh giao cảm tim trái)(bằng chứng B-NR) Thiếu dưỡng cơ type 1 có chỉ định cấy máy tạo nhịp vĩnh viễn (bằng chứng B-NR) |
a: ICD được chỉ định ở tất cả bệnh nhân có kỳ vọng sống > 1 năm. LVEF: phân suất tống máu thất trái, RVEF: phân suất tống máu thất phải. CT: Cắt lớp vi tính; MRI: Cộng hưởng từ.
3 Cấu tạo và chức năng của máy ICD
3.1 Cấu tạo của máy ICD
Bộ máy ICD gồm 2 phần: máy ICD và dây điện cực. Thân máy ICD là bộ phận phát xung điện và dây điện cực có chức năng dẫn truyền xung động điện đến tim.
3.1.1 Bộ phận phát xung
Các máy ICD thế hệ đầu có kích thước khá lớn (115 đến 145 cm3) với trọng lượng từ 195 đến 235g. Vì vậy, các thiết bị này bắt buộc phải cấy ở ổ bụng, dưới da vùng cơ thẳng bụng bên trái. Cấy máy ICD ở ổ bụng và phải gây mê khi phẫu thuật có thể là nguyên nhân làm tỷ lệ biến chứng cao hơn, đặc biệt là nhiễm trùng và nhiễm độc chì.
Máy ICD hiện nay đã giảm đáng kể về kích thước và trọng lượng (kích thước từ 30-39 cm3 và trọng lượng từ 70-84 g) nên có thể cấy dưới da vùng ngực như cấy máy tạo nhịp tim thông thường. Các máy phá rung thế hệ đầu có pin với thời gian sử dụng ngắn chỉ được 2 năm nhưng với sự cải tiến của việc thiết kế pin và giảm mức tiêu hao dòng điện trong theo dõi và phát hiện rối loạn nhịp, nhiều máy ICD hiện đại ngày nay thời gian pin lớn hơn 8 năm thậm chí có dòng pin kéo dài tới 14 năm, góp phần quan trọng để giảm chi phí điều trị.
Máy ICD cấu tạo gồm 2 phần chính là: mạch điện tử và pin. Mạch điện tử với các chương trình rất phức tạp cho phép máy thực hiện các chức năng của mình như: điện tâm đồ trong buồng tim, thời gian tạo nhịp tim, trở kháng sốc và ngưỡng tạo nhịp của dây điện cực có thể được theo dõi thông qua thiết bị không xâm lấn và đánh giá chức năng của điện cực sốc.
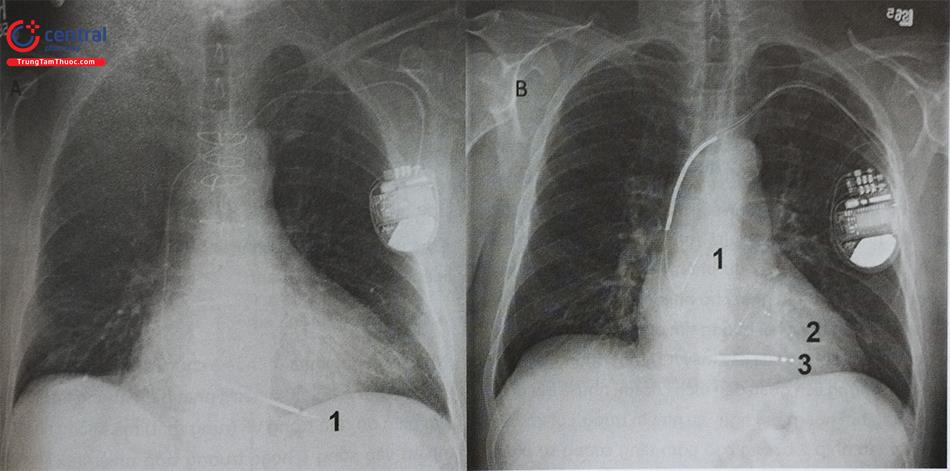
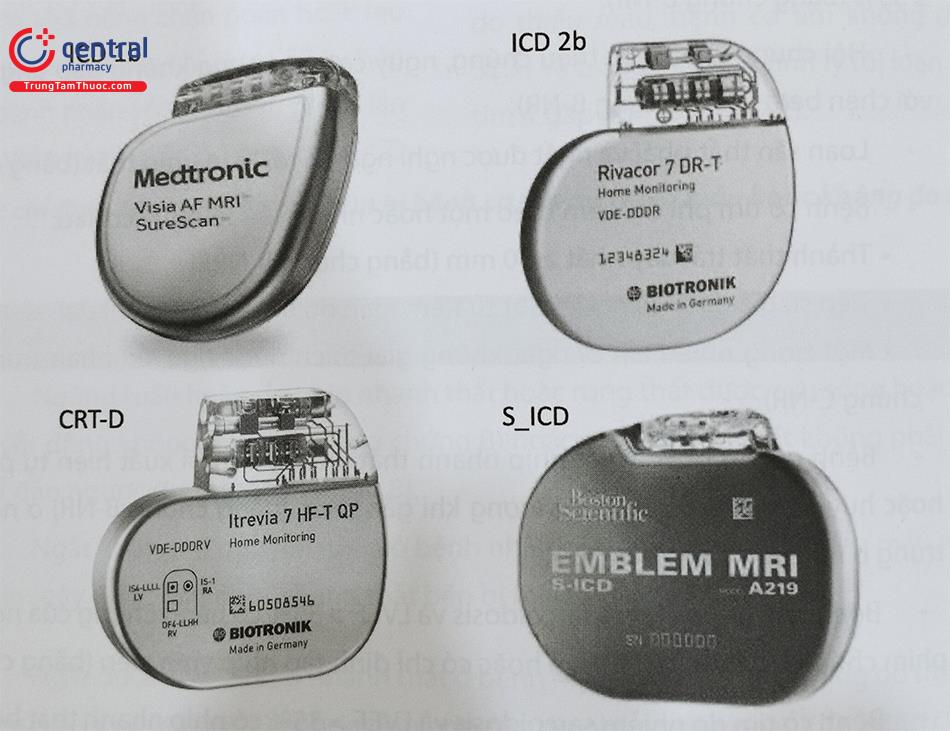
Có 2 loại máy phá rung chính: máy phá rung cấy điện cực qua đường tĩnh mạch, máy phá rung cấy điện cực dưới da (Hình 1).
Máy phá rung cấy điện cực qua đường tĩnh mạch gồm máy phá rung 1 buồng tim, máy phá rung 2 buồng tim và máy phá rung kết hợp với điều trị suy tim (CRT-D).
Máy phá rung điện cực cấy dưới da (S-ICD), chỉ có loại máy một buồng tim, S-ICD không có chức năng tạo nhịp.
3.1.2 Điện cực phá rung
Dây điện cực phá rung luôn có hai chức năng cơ bản là chức năng tạo nhịp và nhận cảm. Máy ICD hiện nay thường sử dụng điện cực sốc lưỡng cực, đầu xa của điện cực (TIP) để xoáy vào cơ tim là đầu âm, cực thứ hai hình vòng tròn cách đầu TIP vài milimet là cực dương để tạo thành điện cực lưỡng cực. Các điện cực lưỡng cực cung cấp ngưỡng nhận cảm chính xác, năng lượng cao và điện tâm đồ hẹp. Một số điện cực lưỡng cực của ICD sử dụng một cực là đầu xa của của điện cực (TIP) và cực còn lại cuộn dây sốc ở đầu xa. Ngoài khả năng nhận cảm được cải thiện, điện cực lưỡng cực của ICD còn giảm nguy cơ nhiễu từ bên ngoài dẫn đến máy phá rung hoạt động không thích hợp (ví dụ: nhát sốc nhầm do nhận cảm cả hoạt động điện của bó cơ).
Chức năng phá rung của điện cực yêu cầu diện tích bề mặt tương đối lớn và vị trí của điện cực trong buồng tim để tối ưu hoá dòng điện chạy qua tâm thất. Các hệ thống ICD hiện đại sử dụng cuộn sốc kéo dài chạy dọc theo điện cực thất làm điện cực phá rung chính, nó cải thiện được hiệu quả phá rung và ngưỡng phá rung. Các hệ thống ICD hiện đại có hai đến ba cực phá rung, cùng với cuộn sốc ở đầu xa của điện cực nằm trong buồng thất phải (RV coil), một số máy ICD sử dụng cuộn sốc thứ hai nằm ở tĩnh mạch chủ trên và nhĩ phải (SVC coil), ngoài ra vỏ kim loại của máy ICD cũng đóng vai trò như một điện cực chống sốc (Hình 2).
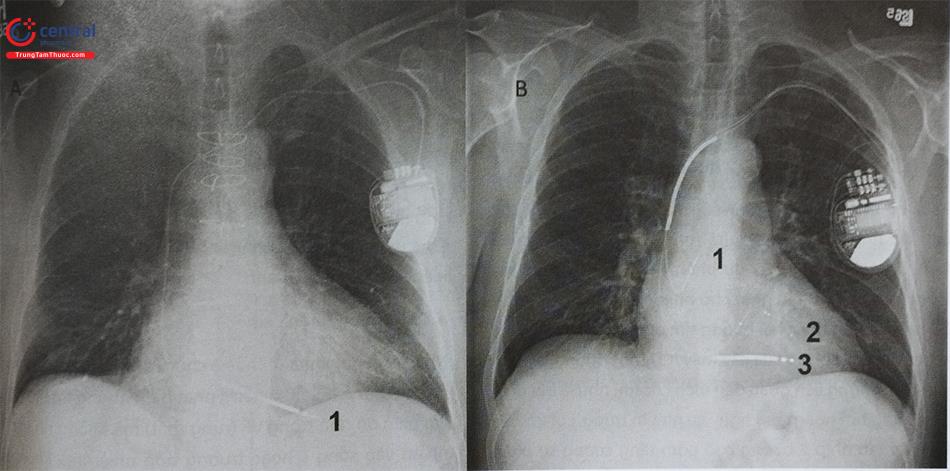
Chú thích: EGM: điện tâm đồ trong buồng tim; RV coil: Cuộn dây sốc ở thất phải. SVC coil: Cuộn dây sốc ở tĩnh mạch chủ trên.
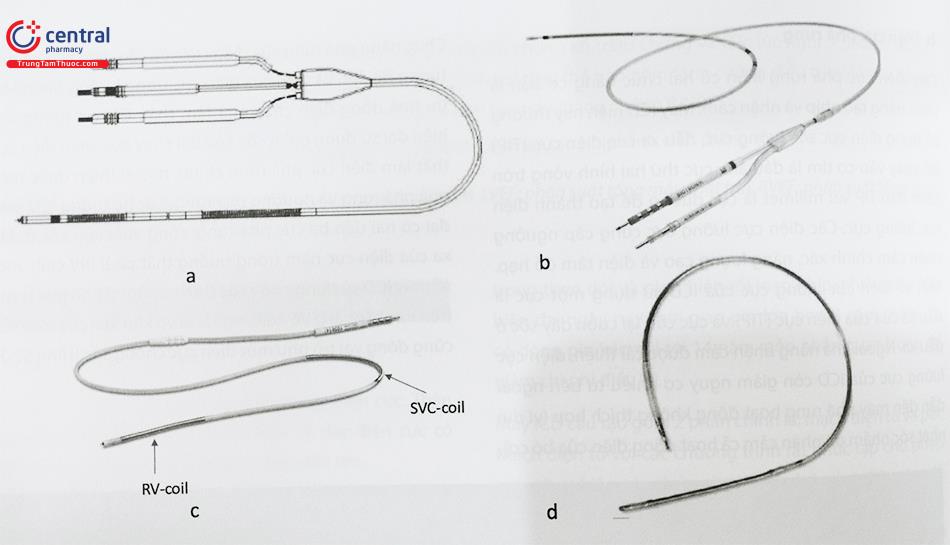
Hiện nay có 4 loại điện cực phá rung chính (Hình 3).
- Dây điện cực DF1 (Hình 3a) gồm 2 cuộn sốc và 3 đầu kết nối với máy ICD. Đây là dây điện cực phá rung thế hệ cũ, hiện ít được dùng cho bệnh nhân, nhược điểm của dây sốc này là kích thước máy ICD đi cùng to hơn.
- Hình 3b: dây sốc biotronic, dây sốc điện này có 1 cuộn sốc thất phải, ở nhĩ phải có hai vòng tròn khi cấy máy tỳ vào nhĩ có thể nhận cảm được sóng nhĩ, nhưng không có khả năng tạo nhịp. Nó được chỉ định ở bệnh nhân có chỉ định cấy máy phá rung tự động nhưng không cần tạo nhịp nhĩ, ưu điểm giúp phân biệt rối loạn nhịp thất chính xác hơn ICD 1 buồng
- Hình 3c: Dây ICD thế hệ mới (DF-4), kích thước dây nhỏ hơn, có loại có 1 hoặc 2 cuộn sốc. đây là dây sốc được dùng phổ biến hiện
- Hình 3d: Dây sốc điện dùng để cấy dưới da ở bệnh nhân có chỉ định cấy S-ICD, chỉ có duy nhất một cuộn sốc dài.
3.2 Lựa chọn máy phá rung
3.2.1 Máy ICD 1 buồng hay ICD 2 buồng tim
Tất cả bệnh nhân có chỉ định cấy máy phá rung và cần tạo nhịp do nhịp chậm, máy phá rung hai buồng được lựa chọn. Trong khi, cấy ICD dự phòng đột tử tiên phát mà không có chỉ định tạo nhịp cho nhịp chậm, lựa chọn máy ICD một buồng hoặc hai buồng tim đều có lợi ích và nguy cơ khác nhau. Lợi ích của cấy máy ICD một buồng là giảm tỷ lệ biến chứng liên quan đến điện cực nhĩ như là bật điện cực, thủng tim hoặc tăng nguy cơ nhiễm trùng. Lợi ích của đặt máy tạo nhịp 2 buồng bao gồm tăng cường sự phân biệt giữa rối loạn nhịp nhĩ và rối loạn nhịp thất làm giảm tỷ lệ nhát sốc không tương thích.
3.2.2 Máy phá rung dưới da với ICD (S-ICD)
Cấy máy phá rung dưới da, máy được cấy vào vùng ngực trái của bệnh nhân, không có chức năng tạo nhịp vượt tần số mà chỉ có chức năng phá rung, nên máy S-ICD được chỉ định trong một số trường hợp.
Cấy máy ICD dưới da (S-ICD) được khuyến cáo ưu tiên làm trong các trường hợp sau:
- Không thể hoặc rất khó tiếp cận đường tĩnh mạch (do tắc hoặc dị dạng tĩnh mạch dưới đòn).
- Nguy cơ cao biến chứng từ hệ thống tĩnh mạch (lọc máu, trẻ con, suy giảm miễn dịch).
- Tiền sử nhiễm trùng máy tạo nhịp trước đấy.
- Viêm nội tâm mạch nhiễm khuẩn.
3.3 Chức năng của máy phá rung
Chức năng của máy phá rung bao gồm: nhận cảm, phát hiện, cắt cơn nhịp nhanh.
3.3.1 Chức năng nhận cảm
Nhận cảm nhịp nhanh thất là chức năng cực kỳ quan trọng của hệ thống ICD. Khả năng phát hiện những tín hiệu điện với biên độ nhỏ trong VF (rung thất) mà không nhận cảm nhầm vào sóng T hoặc trường hợp nhiễu mà không có nhịp nhanh là yếu tố cần thiết trong chức năng của máy ICD. Không giống như máy tạo nhịp tim sử dụng cảm biến khuếch đại cố định, tất cả các máy ICD sử dụng điều chỉnh tự động của bộ khuếch đại hoặc ngưỡng cảm biến để đảm bảo phát hiện được các rối loạn nhịp thất thích hợp (Hình 4).
ICD làm tăng độ nhận cảm bộ khuếch đại theo thời gian giữa nhận cảm và tạo nhịp thất để tìm kiếm điện thế rung thất biên độ thấp có thể ở dưới ngưỡng nhận cảm, trong khi vẫn giữ các cài đặt tương đối không nhạy ngay sau nhận cảm sóng EGM thất để ngăn chặn nhận cảm sóng T.
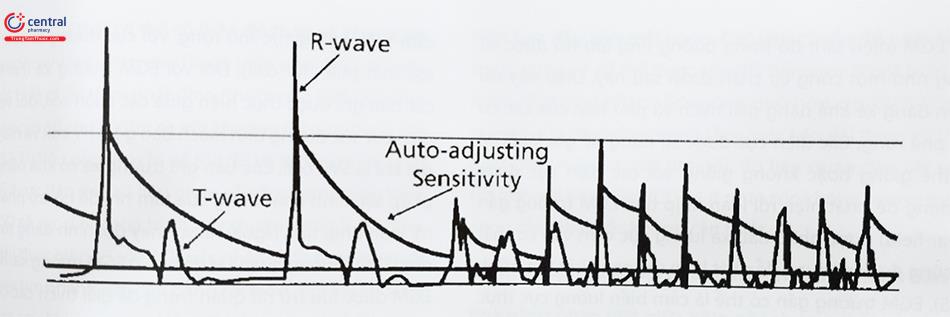
Trong nhịp xoang độ nhận cảm tăng chậm để tránh nhậm cảm nhầm sóng T. Tuy nhiên, với sự khởi phát của rung thất, độ nhạy cao được duy trì để giảm thiểu sự nhận cảm dưới ngưỡng.
Nhận cảm kém (undersensing) VF hiếm khi được ghi nhận với điện cực thượng tâm mạc hoặc điện cực lưỡng cực qua đường tĩnh mạch sau khi tăng độ nhạy hoặc độ nhận cảm tự động được sử dụng. Thông thường, biên độ nhận cảm sóng R lớn hơn 5 mV ở nhịp cơ bản (nhịp xoang hoặc rung nhĩ) là đủ để đảm bảo nhận cảm được VF.
Mặc dù việc nhận cảm kém với nhịp nhanh thất thường không phổ biến với các thế hệ điện cực và máy ICD hiện đại, nhưng việc nhận cảm quá mức vẫn là một vấn đề. Độ nhận cảm tối đa của máy ICD qua đường tĩnh mạch được tăng lên (lên đến 0,15 mV) với các bộ khuếch đại tiếng ồn thấp hiện đại và các giá trị này thậm chí còn thấp hơn đối với các thiết bị đặt dưới da. Điều này có thể dẫn đến việc nhận cảm quá mức với nhiễu điện từ hoặc các nguồn nhiễu âm ngoài khác. Một lần nữa, điều này thường có thể tránh được bằng lập trình thiết bị, bao gồm việc sử dụng các thuật toán giám sát sóng T tự động, giảm độ nhạy tối đa, kéo dài thời gian trơ hoặc giảm tính tích cực của thuật toán độ nhạy tự động. Tần số giám sát nhận cảm quá mức sóng T khác nhau giữa các thiết bị của các nhà sản xuất khác nhau, nhưng thường được chú ý nhất với S ‐ ICD.
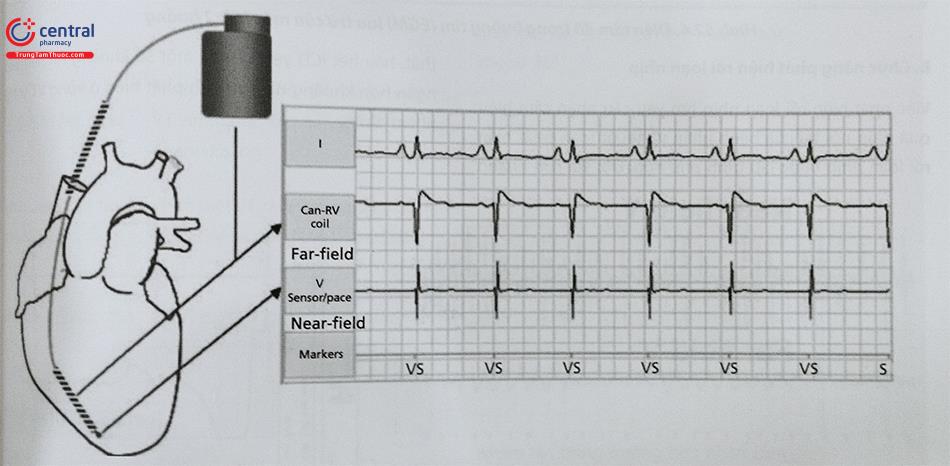
Chú thích: EGM: điện tâm đồ trong buồng tim; RV coil: Cuộn dây sốc ở thất phải.
Các EGM (điện tâm đồ trong buồng tim) lưu trữ được sử dụng như một công cụ chẩn đoán sau này. Điều này cải thiện đáng kể khả năng giải thích sự phù hợp của các cú sốc phá rung. Các điện cực được sử dụng để ghi lại EGM có thể giống hoặc không giống với các điện cực được sử dụng để phát hiện rối loạn nhịp tim. EGM trường gần (Near-field) được ghi ở đầu xa lưỡng cực cắm vào cơ thất và cũng được sử dụng để phát hiện rối loạn nhịp tim (Hình 5). EGM trường gần có thể là cảm biến lưỡng cực thực sự, với điện cực âm ở đầu điện cực sốc gắn vào cơ tim và điện cực dương là vòng tròn cách đó vài milimet, hoặc cảm biến lưỡng cực mở rộng, với cực dương là cuộn dây sốc thất phải (RV coil). Đối với EGM trường xa (Far-field), các bản ghi được thực hiện giữa các cuộn sốc, đối với ICD điện cực sốc đường tĩnh mạch bao gồm RV coil và máy ICD, đôi khi là SVC coil. Các bản ghi trường xa có khả năng cho phép xác định hoạt động của tâm nhĩ để hỗ trợ phân loại rối loạn nhịp tim. Ngoài ra, sự thay đổi hình dạng rối loạn nhịp thất thường quan sát dễ hơn ở EGM trường xa. Nguồn EGM được lưu trữ rất quan trọng để giải thích các cơn rối loạn nhịp tim, đặc biệt là nhát sốc không tương thích (Hình 6).
3.3.2 Chức năng phát hiện rối loạn nhịp
Việc phát hiện rối loạn nhịp tim yêu cầu nhận cảm hiệu quả nhịp nội tại của bệnh nhân và thuật toán phát hiện rối loạn nhịp được lập trình phù hợp. Đối với cơn nhanh thất, hầu hết ICD yêu cầu có một số khoảng RR liên tiếp ngắn hơn khoảng nhịp nhanh phát hiện ở vùng VT (nhịp nhanh thất).
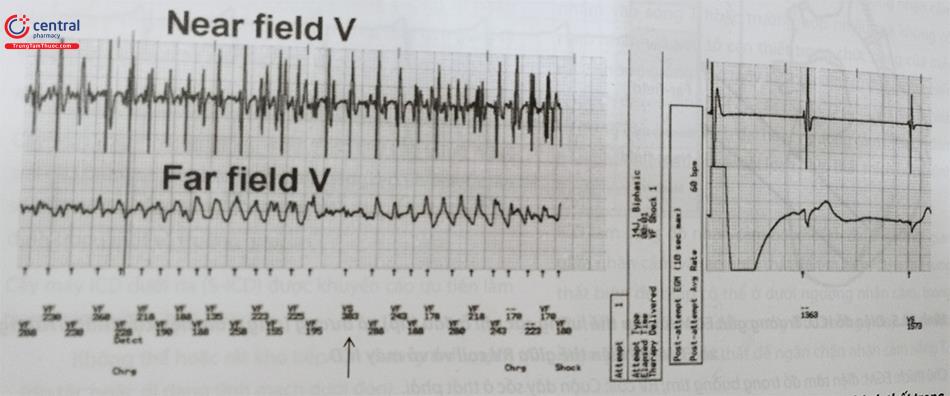
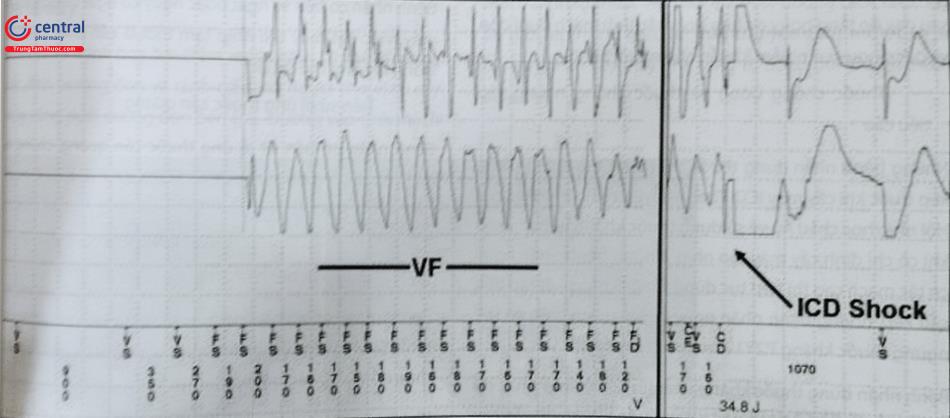
VF và VS chỉ ra khoảng thời gian nhận cảm trong vùng VF và vùng nhịp xoang tương ứng. Rung thất được phát hiện, ICD được sạc điện và nhát sốc được đưa ra để phá cơn rung thất (VF).
Vì EGM của rung thất có thể có biên độ thấp và nhận cảm kém (undersensing), nên các thuật toán phát hiện VF yêu cầu một tỷ lệ phần trăm nhất định (thường là 75%) khoảng RR trong cửa sổ chu kỳ tim so với khoảng RR của VF cài đặt (Hình 7). Nếu các tiêu chí về tốc độ và thời gian để phát hiện VF được đáp ứng và liệu pháp sốc được tính toán theo tỷ lệ, ICD sẽ sạc điện, quá trình này thường mất 5–12 giây. Trước khi thực hiện cú sốc, ICD xác nhận rằng tình trạng rối loạn nhịp tim nhanh vẫn còn bằng cách đo một vài khoảng thời gian sau khi sạc xong. Nếu VT (nhịp nhanh thất) hoặc VF (rung thất) không còn nữa thì sốc được hủy bỏ. Sau mỗi lần sốc điện, máy ICD phải xác định liệu nhịp tim nhanh đã được chấm dứt hay chưa. Tiêu chuẩn xác định cơn VT/VF lại sau khi điều trị thường yêu cầu hơn so với tiêu chí phát hiện ban đầu cho mỗi vùng. Các tiêu chuẩn để phát hiện trong vùng VT có thể được sửa đổi bằng các thuật toán để ngăn chặn liệu pháp sốc không phù hợp cho SVT. Nhiều nghiên cứu đã chứng minh rằng việc kéo dài đáng kể thời gian phát hiện và giới hạn tốc độ liên quan đến kết quả tốt hơn với hệ thống ICD và ít nhát sốc không tương thích cũng như nhát sốc không cần thiết.
3.3.3 Phân biệt giữa nhịp nhanh trên thất và nhanh thất
Khả năng phân biệt giữa nhịp nhanh trên thất và nhanh thất đặc biệt quan trọng trong chức năng của máy phá rung, các loại máy phá rung sử dụng thuật toán khác nhau để phân biệt cơn nhịp nhanh, nhưng chủ yếu dựa vào các tiêu chuẩn phổ biến sau (Bảng 3).
Bảng 3. Phân biệt cơn nhịp nhanh thất và nhanh trên thất của máy ICD
| Tiêu chuẩn phân biệt | Mục đích | Giới hạn | Vai trò của ICD 2 buồng | |
| V=A | V<A | |||
| Thất (ICD một hoặc hai buồng) | ||||
| Độ ổn định VV | Phân biệt nhịp nhanh thất đơn dạng với rung nhĩ | Không chắc chắn nhịp nhanh thất tần số > 170 chu kỳ/ phút. Không phát hiện được nhịp nhanh thất không đều. | + | |
| Xuất hiện đột ngột | Phân biệt sự khởi phát đột ngột của VT với sự gia tăng dần tốc độ của nhịp nhanh xoang | SVT khởi phát đột ngột. | + | |
| Hình dạng của nhịp nhanh thất | Phân biệt VT dựa trên sự thay đổi hình thái EGM so với trạng thái cơ bản. | Gặp trong dẫn truyền lệch hướng. | + | + |
| Độ rộng phức bộ QRS | Phân biệt VT dựa trên sự thay đổi độ rộng phức bộ QRS so với cơ sở. | Đo độ rộng phức bộ QRS trên EGM không được chính xác, bệnh nhân bị block nhánh có thể không tăng độ rộng phức bộ QRS trong nhanh thất. | + | + |
| Nhĩ thất (ICD 2 buồng) | ||||
| So sánh tần số nhĩ và thất | Chẩn đoán nhanh thất nếu tần số nhĩ < tần số thất | Nhầm lẫn trong trường hợp nhận cảm kém ở sóng nhĩ và nhận cảm quá mức ở sóng thất. | + | + |
| Phân ly nhĩ thất | Phân ly nhĩ thất thường nghĩ đến nhanh thất. | Nhanh thất với dẫn truyền ngược thất nhĩ 1:1, rung nhĩ với đáp ứng tần số thất nhanh. | + | |
| Vị trí khởi phát | Phân biệt nhịp nhanh khởi phát từ tâm nhĩ hay tâm thất | Nhận cảm kém hoặc nhận cảm quá mức ở 1 buồng tim có thể dẫn đến chẩn đoán nhầm | + | |
| Khởi phát đột ngột | Phân biệt VT dựa trên sự thay đổi đột ngột của tần số thất và khoảng thời tạo nhịp thất gian AV | Không đáng tin cậy nếu nhịp cơ bản là tạo nhịp thất | + | |
| Nhĩ (ICD 2 buồng) | ||||
| Tần số nhĩ | Phát hiện rung nhĩ | Nhận cảm kém/quá mức nhĩ gây ra nhầm lẫn. VT/VF có thể xảy ra trong rung nhĩ. | + | |
| Phân biệt trong cơn nhịp nhanh | ||||
| Tạo nhịp nhĩ, thất, nhĩ thất trong cơn nhịp nhanh | Có thể cắt cơn nhịp nhanh, phân biệt dẫn truyền 1:1 vẫn tồn tại nhịp nhanh đoạn AV sau tạo nhịp | + | ||
Chú thích: VT: Nhịp nhanh thất; SVT: Nhịp nhanh trên thất; VF: Rung thất; V: Thất; A: Nhĩ.
Độ ổn định của đoạn RR
Độ ổn định để phân biệt giữa nhịp nhanh thất đơn dạng với rung nhĩ có đáp ứng tần số thất nhanh. Tiêu chuẩn của sự ổn định đoạn VV có thể loại trừ rung nhĩ nếu tần số thất nhỏ hơn 170 nhịp/phút khi không sử dụng thuốc chống loạn nhịp. Ở tần số cao hơn, chúng ta không thể phân biệt rung nhĩ với nhanh thất một cách hiệu quả bởi vì đoạn VV trong rung nhĩ trở nên đều hơn. Tiêu chuẩn phân biệt này có thể giúp nhận biết nhịp nhanh thất đơn dạng vì nhịp thất có thể không đều sau khi dùng Amiodarone hoặc thuốc chống loạn nhịp nhóm Ic.
Khởi phát đột ngột
Phân biệt khởi phát đột ngột của cơn nhanh thất với sự gia tăng dần tốc độ của nhịp nhanh xoang. Tính chất khởi phát đột ngột có độ đặc hiệu cao để loại trừ nhịp nhanh xoang. Tuy nhiên khi sử dụng riêng biệt, nó ngăn chặn việc phát hiện nhịp nhanh thất bắt nguồn từ cơn nhịp nhanh trên thất (SVT) hoặc nhanh thất bắt đầu đột ngột với tốc độ ban đầu thấp hơn giới hạn phát hiện nhịp nhanh thất (VT). Trong trường hợp thứ hai, ICD phân loại nhầm sự khởi phát đột ngột của rối loạn nhịp tim là sự gia tốc dần dần của nhịp nhanh thất qua ngưỡng phát hiện nhịp nhanh thất. Hầu hết các máy ICD 1 hoặc 2 buồng đều đánh giá lại khả năng phân loại cơn nhịp nhanh đang diễn ra, nhưng tiêu chuẩn “khởi phát đột ngột” chỉ phân loại nó 1 lần khi nó đi qua vùng ranh giới nhịp xoang và nhanh thất. Bởi vì cả lý do trên và phân biệt bằng hình dạng QRS có độ chính xác cao hơn để loại trừ nhịp nhanh xoang, tính chất khởi phát đột ngột không nên được sử dụng như tiêu chuẩn duy nhất.
Hình thái điện tâm đồ trong buồng tim (EGM)
Sử dụng hình thái điện tâm đồ thất để phân loại cơn nhịp nhanh trên thất với cơn nhanh thất, nếu đặc điểm EGM ban đầu giống EGM trong cơn thì chẩn đoán cơn nhịp nhanh trên thất và chẩn đoán là nhanh thất nếu không giống. Máy ICD 1 buồng có thể phân loại cơn SVT một cách chính xác. Bao gồm cả tính chất xuất hiện đột ngột, cơn SVT đều với dẫn truyền nhĩ thất 1:1 hoặc cơn cuồng nhĩ. Do đó, nó là thuật toán nền tảng của máy ICD 1 buồng hiện đại.
Các thuật toán về hình thái điện tâm đồ để phân biệt cơn VT-SVT đều có chung các bước (Hình 8).
- Ghi lại một mẫu EGM của nhịp cơ bản.
- Xây dựng và lưu trữ đại diện định lượng của mẫu này.
- Ghi lại các EGM từ nhịp tim nhanh không rõ.
- Thời gian giữa EGM mẫu và các EGM nhịp tim
- Xây dựng định lượng, đo thời gian phục hồi bình thường của mỗi EGM cơn tim
- So sánh hình thái của từng EGM cơn nhịp tim nhanh với EGM mẫu để xác định mức độ giống nhau về hình thái.
- Phân loại mỗi EGM nhịp tim nhanh là giống hoặc không giống EGM mẫu.
- Phân loại nhịp tim nhanh là VT hoặc SVT dựa trên hình thái cơn nhịp nhanh giống hay không giống EGM mẫu.
Các bước 3-8 được thực hiện trong thời gian thực.
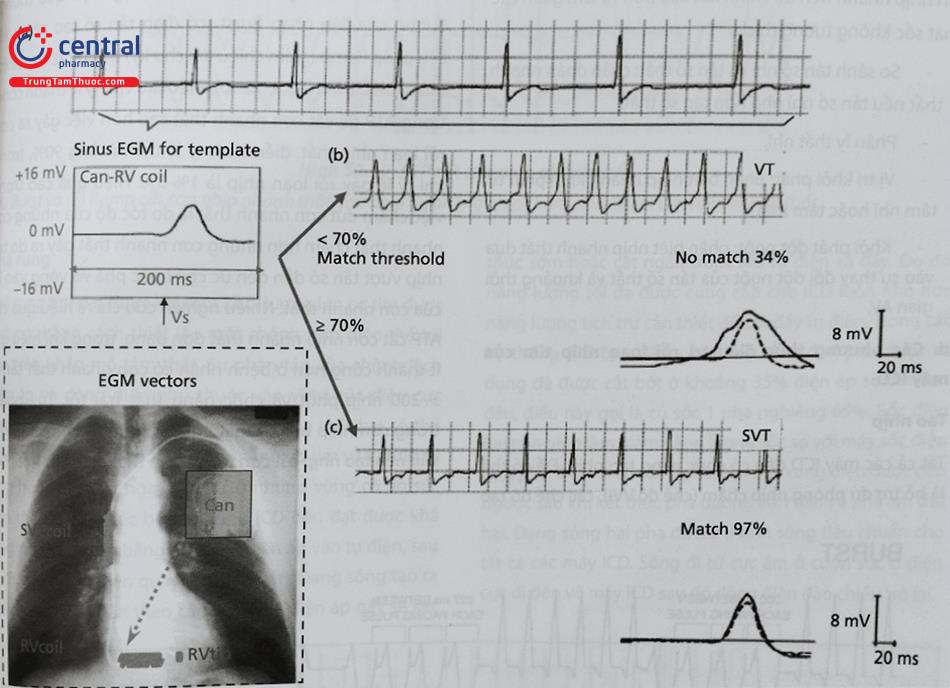
EGM: Điện tâm đồ trong buồng tim; RV coil: Cuộn dây sốc ở thất phải; SCV coil: Cuộn dây sốc ở tĩnh mạch chủ trên.
Mặc dù thuật toán dựa vào hình thái của EGM có độ đặc hiệu cao nhưng nó vẫn có nhiều nhược điểm có thể dẫn đến phân biệt nhầm cơn VT-SVT.
- EGM mẫu không chính xác bởi vì EGM mẫu có thể thay đổi (sau cấy máy hoặc block nhánh mới xuất hiện) hoặc EGM mẫu ghi lúc xuất hiện block nhánh thoáng qua, ngoại tâm thu thất.
- Cắt ngắn điện đồ: cắt ngắn EGM xảy ra khi biên độ tín hiệu của EGM ghi được vượt quá phạm vi bộ khuếch đại EGM, thường xảy ra khi thay đổi tư thế.
- Các lỗi căn chỉnh: xảy ra khi một đặc điểm của điện tâm đồ trong buồng tim cơn nhịp nhanh được căn chỉnh với một đặc điểm khác của EGM mẫu, điều đó dẫn đến sự phù hợp giữa EGM của cơn nhịp nhanh với EGM mẫu.
- Tín hiệu bị nhiễu trong cơn nhịp
- Tốc độ liên quan đến dẫn truyền lệch hướng.
- Cơn SVT xuất hiện ngay sau phát sốc: Sau một cú sốc, các thuật toán phát hiện của ICD được phân loại và hồi phục sau khoảng vài giây, nhưng sự biến dạng sau sốc của hình thái EGM vẫn tồn tại trong 30 giây đến vài phút. Nếu rối loạn nhịp nhanh trên thất bắt đầu sau khi nhịp đã được phân loại là xoang, nhưng trước phát sốc sau EGM biến dạng không hoạt động, phân biệt hình thái học sẽ phân loại nhầm SVT thành
Máy ICD 2 buồng có thêm nhiều thuật toán để phân loại cơn nhịp nhanh nên độ chính xác cao hơn và làm giảm các nhát sốc không tương thích.
- So sánh tần số nhĩ và tần số thất: chẩn đoán nhanh thất nếu tần số nhĩ nhỏ hơn tần số thất.
- Phân ly thất nhĩ.
- Vị trí khởi phát: phân biệt nhịp nhanh khởi phát từ tâm nhĩ hoặc tâm thất.
- Khởi phát đột ngột: phân biệt nhịp nhanh thất dựa vào sự thay đổi đột ngột của tần số thất và khoảng thời gian
3.3.4 Các phương thức điều trị rối loạn nhịp tim của máy ICD
Tạo nhịp
Tất cả các máy ICD đều có chức năng tạo nhịp. Để có thể là hỗ trợ dự phòng nhịp chậm (chế độ VVI), các chế độ tạo
nhịp sinh lý hơn có hoặc không có đáp ứng tần số (ví dụ: DDDR) hoặc tạo nhịp vượt tần số để chấm dứt nhịp nhanh thất hoặc loạn nhịp nhanh trên thất (SVT hoặc cuồng nhĩ).
Tạo nhịp vượt tần số
Tạo nhịp vượt tần số (ATP) rất hiệu quả trong cắt cơn nhịp nhanh thất. Các thuật toán tương thích được sử dụng, trong khi tần số tạo nhịp được cài đặt dựa vào chu kỳ của mỗi cơn nhịp nhanh.
Các nghiên cứu ngẫu nhiên chỉ ra rằng hiệu quả tương đương của liệu pháp Burst (cố định tần số tạo nhịp) và liệu pháp Ramp (giảm chiều dài chu kỳ) trong cắt cơn nhịp nhanh thất (Hình 52.9, 52.10). Điều thú vị là tỷ lệ thành công trong ATP để cắt cơn nhanh thất cao hơn việc gây ra cơn rối loạn nhịp thất, điển hình tỷ lệ thành công 90%, trong khi tỷ lệ gây rối loạn nhịp là 1%-3%. Hiệu quả cao trong việc chấm dứt cơn nhanh thất là do tốc độ của những cơn nhanh thất chậm hơn những cơn nhanh thất gây ra do tạo nhịp vượt tần số dẫn đến ức chế hoặc phá vỡ vòng vào lại của cơn nhanh thất. Nhiều nghiên cứu chỉ ra hiệu quả của ATP cắt cơn nhịp nhanh thất đơn dạng, trong khi hiệu quả ít thành công hơn ở bệnh nhân có cơn nhanh thất tần số 200 nhịp/phút và chức năng thất trái tồi. Tuy nhiên, trong cơn nhịp nhanh thất với tần số rất nhanh chúng ta vẫn nên tạo nhịp cắt cơn tim nhanh thất để giảm nhát sốc.
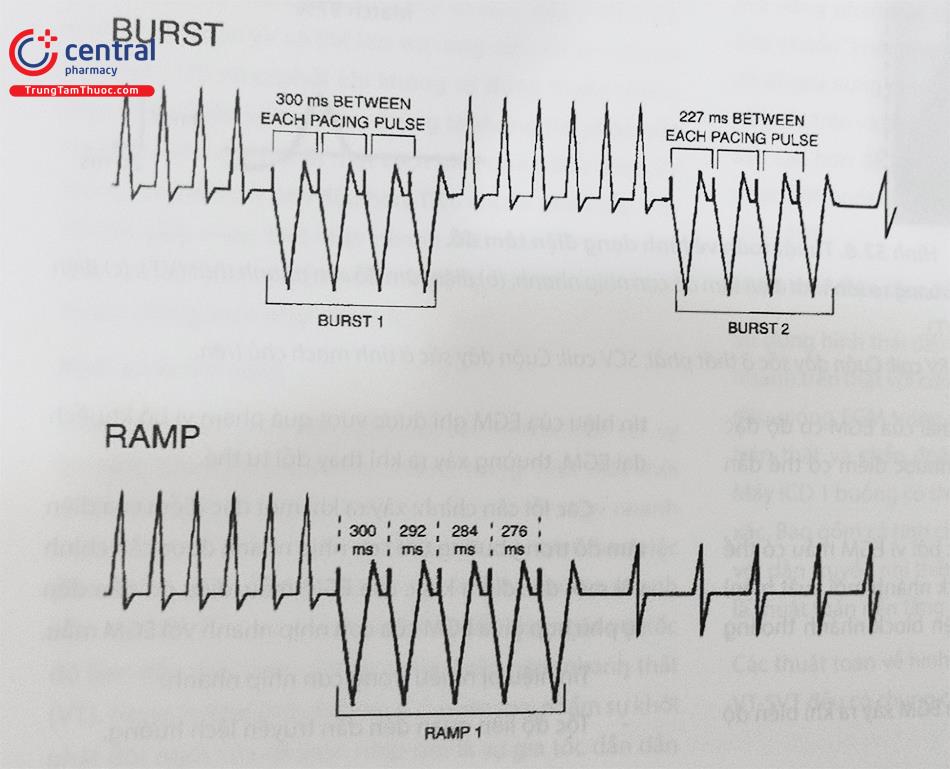
Hình trên: bốn nhịp đầu tiên nhịp nhanh thất sau đó BURST (ATP) ở tần số 300 ms trong bốn nhịp. Nhịp nhanh vẫn tiếp tục, BURST 2 với tần số nhanh hơn BURST 1 là 227ms. Hình dưới: Ramp ATP có sự giảm nhịp độ giữa các lần kích thích liên tiếp.
Phá rung
Phá rung tim đạt được khi một khối lượng lớn cơ tim được khử cực bằng cách thiết lập một chênh lệch điện thế tới hạn trên khắp mô tâm thất. Sự phân tán của chênh lệch điện áp và dòng điện phụ thuộc vào vị trí của điện cực trong và/hoặc xung quanh tim. Phá rung thất bại có thể do còn tồn tại một khối lượng lớn mô cơ tim vẫn đang bị rung hoặc tái phát ngay lập tức ở những vùng có độ sốc điện thấp. Tất cả các bộ tạo xung ICD đều đạt được khả năng phá rung tim bằng cách đặt điện áp vào tụ điện, sau đó được phóng điện qua hệ thống dẫn. Dạng sóng tạo ra là điện áp giảm dần theo cấp số nhân, điện áp này sẽ kết thúc sớm hoặc cắt ngắn trước khi tụ điện xả đầy. Do đó, năng lượng tối đa được cung cấp cho ICD luôn nhỏ hơn năng lượng tích trữ cần thiết để sạc đầy tụ điện. Trong các hệ thống ICD ban đầu, các dạng sóng đơn pha được sử dụng đã được cắt bớt ở khoảng 35% điện áp so với ban đầu, điều này gọi là cú sốc 1 pha nghiêng 65%. Sốc điện hai pha giúp làm giảm năng lượng sốc so với máy sốc điện một pha. Đối với cú sốc 2 pha, cực của xung điện được đảo ngược sau khi kết thúc pha dương ban đầu và pha âm thứ hai. Dạng sóng hai pha đã trở thành sóng tiêu chuẩn cho tất cả các máy ICD. Sóng đi từ cực âm ở cuộn sốc ở điện cực đi đến vỏ máy ICD sau đó dòng điện đảo chiều trở lại.
4 Kỹ thuật cấy máy ICD
4.1 Chuẩn bị bệnh nhân
Trước khi cấy máy ICD, nên đánh giá kỹ tình trạng của người bệnh. Xem xét hồ sơ y tế, tiền sử của bệnh nhân (bao gồm các loại thuốc hiện tại, đặc biệt là thuốc chống đông, thuốc chống ngưng tập tiểu cầu, tiền sử phản ứng hoặc dị ứng với thuốc cản quang) khám tổng quát và làm các xét nghiệm cơ bản để phẫu thuật.
Các trường hợp đặc biệt
- Nhiễm trùng
Bác sĩ cần phải hỏi và thăm khám cẩn thận tình trạng nhiễm trùng của bệnh nhân. Cấy máy ICD không phải là thủ thuật cấp cứu, nên chúng ta cần trì hoãn cấy máy đến khi tình trạng nhiễm trùng của bệnh nhân hoàn toàn ổn định.
Để phòng ngừa nhiễm trùng khi cấy máy, theo khuyến cáo của ESC 2021 kháng sinh dự phòng đường tĩnh mạch nên được cho trước khi cấy máy 1 giờ để dự phòng nhiễm khuẩn.
- Suy thận
Những bệnh nhân suy thận mạn tính cần phải được xem xét cẩn thận. Bởi vì, trong cấy ICD có thể cần sử dụng thuốc cản quang, thuốc cản quang có thể làm nặng thêm tình trạng suy thận của bệnh nhân. Chúng ta nên cấy máy đối diện với bên làm cầu tay ở người bệnh chạy thận nhân tạo chu kỳ giúp làm giảm nguy cơ chảy máu ổ máy do tăng áp lực của tĩnh mạch, cũng như không thể sử dụng cầu lọc sau nay do tăng nguy cơ hẹp hoặc tắc tĩnh mạch dưới đòn và giảm nguy cơ nhiễm khuẩn cho người bệnh.
- Thuốc chống đông và thuốc chống ngưng tập tiểu cầu
Những bệnh nhân dùng thuốc chống ngưng tập tiểu cầu kép trước khi cấy máy ICD. Theo khuyến cáo năm 2021 của Hội nhịp học châu Âu về sử dụng thuốc kháng tiểu cầu kép khi có chỉ định cấy máy tạo nhịp. Những bệnh nhân nguy cơ tắc mạch cao thì tiếp tục dùng thuốc kháng kết tập tiểu cầu kép, những bệnh nhân nguy cơ tắc mạch thấp có thể ngừng thuốc kháng P2Y12 trước khi cấy máy ICD.
Bệnh nhân dùng thuốc kháng vitamin K: hiện nay phác đồ được lựa chọn cho bệnh nhân đang uống Warfarin cần cấy máy tạo nhịp là không dừng thuốc. Có nhiều nghiên cứu chỉ ra khi INR < 2,6 biến chứng tụ máu và chảy máu tương tự nhóm INR < 1,5.
Đối với thuốc chống đông trực tiếp đường uống (DOAC): hiện chưa có khuyến cáo cụ thể trường hợp nào nên dừng, việc ngừng thuốc phụ thuộc vào đánh giá nguy cơ chảy máu và tắc mạch của phẫu thuật viên.
Để hạn chế chảy máu trong khi cấy máy phá rung tự động, dao điện nên được sử dụng một cách thường quy.
- Đánh giá đường vào
Việc đánh giá đường vào nên được thực hiện trước khi cấy máy, những bệnh nhân có bất thường tĩnh mạch dưới đòn, đặt đường truyền tĩnh mạch trung tâm, điện cực cũ hoặc tiền sử gãy xương đòn. Giải pháp đặt ra trong trường hợp này chúng ta có thể chụp tĩnh mạch và thay đổi vị trí chọc khi cần thiết.
- Tiền sử phẫu thuật cắt tuyến vú
Bệnh nhân có tiền sử phẫu thuật cắt tuyến vú do ung thư, nói chung vị trí cấy máy nên ở bên đối diện do lo ngại tình trạng sưng tấy nặng hơn ở cánh tay do hẹp, tắc tĩnh mạch dưới đòn sau cấy ICD.
- Bệnh van ba lá
Bệnh nhân có tình trạng hở van ba lá nặng, việc cấy máy phá rung có thể làm cho tình trạng hở van ba lá và suy thất phải nặng hơn. Đặc biệt ở bệnh nhân thay van ba lá cơ học, việc cấy ICD đường tĩnh mạch là chống chỉ định. Chúng ta có thể cân nhắc đặt S-ICD.
- Nguy cơ ngất
Bệnh nhân có tiền sử ngất hoặc nguy cơ ngất trong khi cấy máy, việc đặt máy tạo nhịp tạm thời là cần thiết trước và trong khi làm thủ thuật.
- Tiền sử dị ứng thuốc cản quang
Bệnh nhân có tiền sử dị ứng thuốc cản quang, chúng ta có thể chọc mù hoặc chọc tĩnh mạch dưới đòn, tĩnh mạch nách dưới hướng dẫn của siêu âm trong một số trường hợp khó khăn.
- Chuẩn bị bệnh nhân trước cấy máy
Bệnh nhân cần đặt đường truyền tĩnh mạch phía bên dự định đặt máy, truyền dịch trước 8 giờ để giảm nguy cơ suy thận do thuốc cản quang.
Kháng sinh dự phòng làm giảm nguy cơ nhiễm trùng ổ máy, kháng sinh được dùng trước cấy máy 1 đến 2 giờ để đạt được nồng độ đỉnh trong lúc cấy máy, sau cấy máy tiếp tục dùng 3 đến 5 ngày. Kháng sinh được dùng chủ yếu là kháng sinh dự phòng tụ cầu.
Trong một số trường hợp đặc biệt bệnh nhân được yêu cầu gây mê, việc khám tiền mê là cần thiết.
4.2 Thủ thuật cấy máy phá rung
4.2.1 Giải phẫu hệ tĩnh mạch chi trên
Tĩnh mạch nách là một tĩnh mạch sâu của chi trên được hình thành bởi sự hợp nhất của các tĩnh mạch cánh tay
và tĩnh mạch nền. Nó bắt đầu ở đường viền dưới của cơ tròn lớn đi lên hội lưu với tĩnh mạch đầu, khi đến xương sườn thứ nhất thì đổi tên thành tĩnh mạch dưới đòn, tĩnh mạch nách nằm trước động mạch nách, chồng lên nó một phần. Tĩnh mạch dưới đòn đi qua xương sườn đầu tiên chui xuống phía dưới xương đòn phía gần khớp ức đòn tại đây nó kết hợp với tĩnh mạch cảnh trong đổi tên thành thân tĩnh mạch cánh tay đầu để đi vào tĩnh mạch chủ trên, đổ vào tâm nhĩ phải của tim (Hình 52.12).
4.2.2 Vị trí chọc mạch
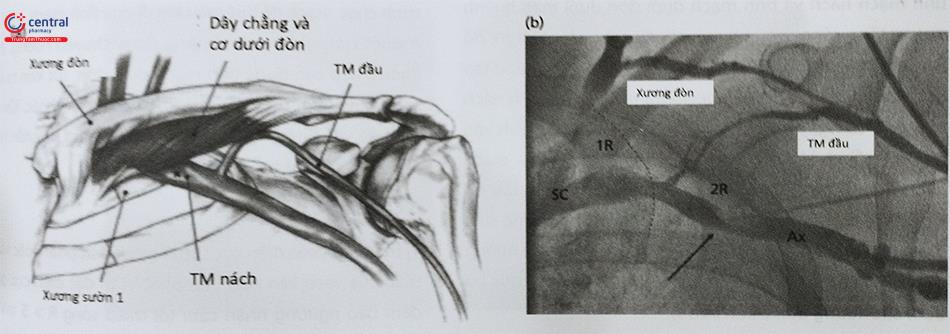
Đường vào tĩnh mạch ở bệnh nhân cấy máy phá rung chủ yếu bên trái do năng lượng sốc thấp hơn và hiệu quả nhát sốc cao hơn bên phải. Nhiều vị trí đường chọc tĩnh mạch có thể tiếp cận bao gồm: tĩnh mạch dưới đòn, tĩnh mạch đầu, tĩnh mạch nách.
Mở túi máy
Hình 13 minh hoạ hai điểm mốc chính có thể dễ dàng xác định (xương đòn và rãnh cơ delta ngực) cho vị trí cấy máy vùng dưới xương đòn bên trái. Đường vào tĩnh mạch công qua đường rạch này. Gây tê vùng dưới da với chiều dài từ 4-6 cm. Nếu tĩnh mạch đầu được sử dụng, đường rạch bắt đầu khoảng 0,5 cm phía bên tới rãnh cơ delta ngực và kéo dài ra giữa. Đường rạch này cho phép bộc lộ đầy đủ đường vào tĩnh mạch đầu và tĩnh mạch dưới đòn.
Một vài phẫu thuật viên bắt đầu với đường rạch nhỏ, sau đó mới rạch rộng hơn. Túi máy chủ yếu được mở trong cơ ở bệnh nhân cấy máy phá rung tự động bởi vì kích thước máy lớn.
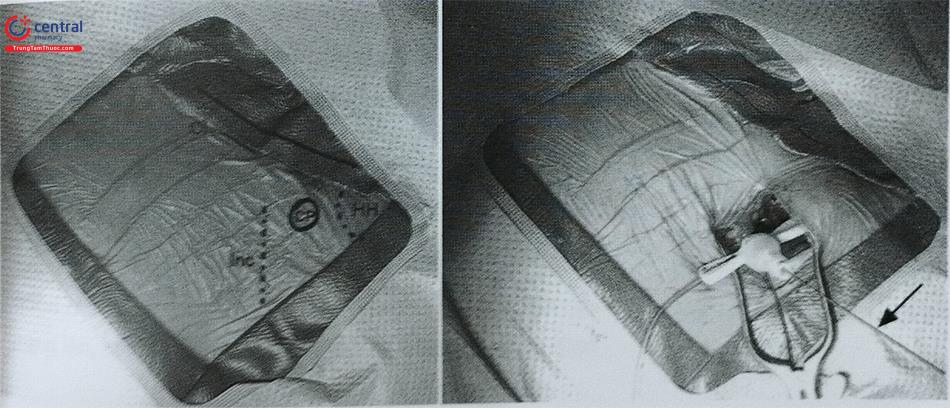
Kỹ thuật chọc tĩnh mạch nách
Việc bất lợi trong việc chọc tĩnh mạch dưới đòn ở bệnh nhân cấy máy phá rung dẫn đến sự phát triển các kỹ thuật tiếp cận tĩnh mạch nách. Phương pháp này có vẻ an toàn, hiệu quả và thành công hơn biện pháp bộc lộ tĩnh mạch đầu. Truyền dịch tĩnh mạch cùng bên làm tăng khả năng chọc mạch, sử dụng thuốc cản quang đánh giá đường đi của tĩnh mạch và vị trí chọc mạch hiệu quả.
Bơm 10-20ml thuốc cản quang qua đường tĩnh mạch cùng bên, cho dịch chảy và ngay lập tức theo dõi đường đi của tĩnh mạch nách và tĩnh mạch dưới đòn dưới màn huỳnh quang tăng sáng. Nếu túi máy đã được bộc lộ dưới cơ, đó là vị trí tốt nhất để vào tĩnh mạch, giúp cho hạn chế sự tạo góc quá mức giữa vị trí chọc và túi máy. Tĩnh mạch nách rất nông và ngay dưới ổ máy nên cần cẩn thận tránh vào màng phổi và khoang màng phổi. Vị trí chọc tĩnh mạch nách ở rãnh cơ delta ngực, hướng kim 60-90 độ, sau đó kim chọc đi dưới hướng dẫn của màn huỳnh quang đến điểm giữa bờ ngoài của xương sườn số 1 mà tại đó đường viền bên của xương sườn đầu tiên dường như vượt qua bờ dưới của xương đòn (Hình 12).
Sau khi chọc vào tĩnh mạch đưa dây dẫn cong hình chữ J vào đến tĩnh mạch chủ dưới để tránh gây rối loạn nhịp tim khi đầu dây dẫn kích thích vào buồng tim. Quá trình này được nhắc lại với nhiều dây dẫn hơn tuỳ thuộc vào loại cấy máy phá rung.
Kỹ thuật chọc tĩnh mạch dưới đòn
Mặc dù được sử dụng rộng rãi trong quá khứ, nhưng phương pháp chọc tĩnh mạch dưới đòn được sử dụng ít hơn phương pháp chọc tĩnh mạch nách ở bệnh nhân cấy máy phá rung tự động.
Chuẩn bị bệnh nhân tương tự như phương pháp tiếp cận qua tĩnh mạch nách, chụp cản quang tĩnh mạch qua tĩnh mạch cánh tay cùng bên có thể hữu ích trong việc xác định tính thông suốt của tĩnh mạch, cấu trúc giải phẫu của nó có thể khác nhau ở các bệnh nhân khác nhau. Cánh tay của bệnh nhân nên được giang ra để cho xương đòn thẳng ra và giảm gù vai. Kim chọc mạch được gắn với bơm tiêm 5-10ml có chứa thuốc gây tê hoặc nước muối. Chọc qua vị trí ổ máy, kim chọc được nâng cao, đầu kim chọc ở vị trí 1/3 giữa xương đòn hướng về khớp ức đòn. Ngoài ra, kim được di chuyển từ trước ra sau dọc theo xương đòn bằng cách sử dụng ngón tay cái của bàn tay không thuận để giữ kim hoặc bơm tiêm. Khi đã ở dưới xương đòn, kim và ống tiêm nên được giữ song song với lồng ngực; điều này ngăn không cho kim đâm về phía sau nhiều hơn như khi kim được nâng cao. Hút áp lực âm liên tục trong quá trình chọc mạch để hút máu khi đi qua tĩnh mạch. Một khi ở dưới xương đòn, kim không được chuyển hướng. Nếu không tiếp cận được tĩnh mạch dưới đòn, rút kim ra làm sạch bằng nước muối lặp lại và đi theo hướng khác. Khi xác định đã vào được tĩnh mạch dưới đòn, trượt dây dẫn hình chữ J vào như đã mô tả ở trên.
4.2.3 Cấy điện cực
Vị trí ưu tiên của điện cực sốc là mỏm thất phải hoặc vùng thấp của vách liên thất bên phải. Vị trí đặt điện cực phải đảm bảo ngưỡng nhận cảm tối thiểu sóng R > 5 mV và ngưỡng tạo nhịp < 1 V. Nếu cấy máy ICD 2 buồng tim thì chúng ta đặt thêm điện cực nhĩ với thông số nhận cảm và tạo nhịp thích hợp. Chỉ có điện cực lưỡng cực mới được chỉ định trong hệ thống ICD. Đối với máy ICD 2 buồng, điện cực nhĩ nên cấy xa vòng ban ba lá để giảm nguy cơ nhận cảm trường xa của điện đồ thất. Đối với máy CRT-D, thêm một điện cực được cấy vào thất trái thông qua hệ thống tĩnh mạch xoang vành. Các điện cực này được cố định một cách thụ động và có thể sử dụng điện cực đơn cực hoặc lưỡng cực.
Kỹ thuật cấy điện cực sốc vào thất phải
Bước 1: Điện cực sốc được đưa vào vùng thấp của nhĩ phải hoặc tĩnh mạch chủ dưới, stylet thẳng được rút lại 1 vài cm để cho phép đầu điện cực chạm vào thành nhĩ phải, sau đó chúng ta đẩy điện cực sốc vào sẽ tạo ra hình chữ J, sau đó xoay nhẹ hướng vào vòng van ba lá (Hình 14).
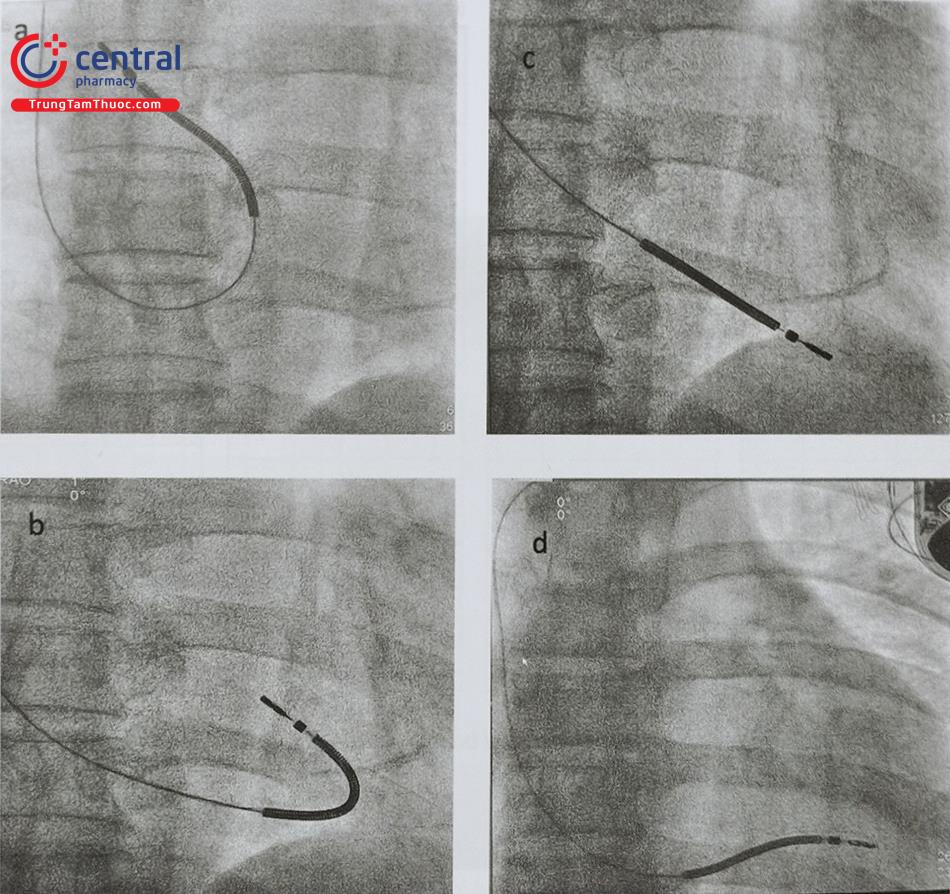
Bước 2: Tiếp tục đẩy nhẹ điện cực chui qua vòng van 3 lá, đầu điện cực thường bật vào đường ra thất phải hoặc động mạch phổi, phải đảm bảo chắc chắn rằng điện cực không chui vào xoang tĩnh mạch vành. Việc đầu điện cực vào động mạch phổi xác định rằng điện cực không ở trong xoang tĩnh mạch vành và nhĩ phải.
Bước 3: Đẩy stylet vào giúp đầu điện cực đi dần về phía mỏm tim, trong lúc đó ta có thể rút nhẹ điện cực quay cùng chiều kim đồng hồ.
- Kỹ thuật đưa điện cực sốc qua vòng van ba lá kiểu này giúp tránh tổn thương van ba lá.
- Nếu muốn lái điện cực vào vùng thấp của vách liên thất, ta có thể uốn stylet hơi cong và đầu xa của stylet uống hình chữ L với chiều cong hướng sang trái. Thay stylet thẳng bằng stylet vừa mới tạo hình, đầy stylet tối đa và quay cùng chiều kim đồng hồ thì đầu điện cực sốc tiến vào vùng thấp của vách liên thất.
- Ngoài ra còn một số kỹ thuật khác như uốn cong stylet hình chữ J, khi luồn vào điện cực thì đầu điện cực nâng lên, sau đó hơi kéo stylet lại để đảm bảo đầu điện cực mềm không gây tổn thương van ba lá trong quá trình đưa qua nó.
Bước 4: Khi vào được vị trí thích hợp, tạo nhịp ở mức năng lượng 10V để loại trừ các kích thích vùng cơ hoành, nếu có cần chuyển điện cực ra vị trí khác.
Bước 5: Cố định điện cực, trong quá trình cố định nên xem dưới dạng phóng đại để theo dõi đầu điện cực bắt vào cơ tim, sau đó kéo stylet lại 1 vài cm.
Bước 6: Kiểm tra các thông số của điện cực. Kết nối đầu gần điện cực với hệ thống lập trình để kiểm tra.
- Có sóng tổn thương hay không (Hình 15).
- Kiểm tra ngưỡng nhận cảm của điện cực.
- Kiểm tra trở kháng và ngưỡng tạo nhịp.
Trong một số trường hợp không có sóng tổn thương chúng ta nên chắc chắn rằng điện cực đã được bám chắc vào cơ tim. Vị trí đặt điện cực thích hợp khi ngưỡng nhận cảm của bệnh nhân ít nhất lớn hơn 5 mV, ngưỡng tạo nhịp < 1 V, trở kháng trong giới hạn từ 400 đến 1200 Ω.
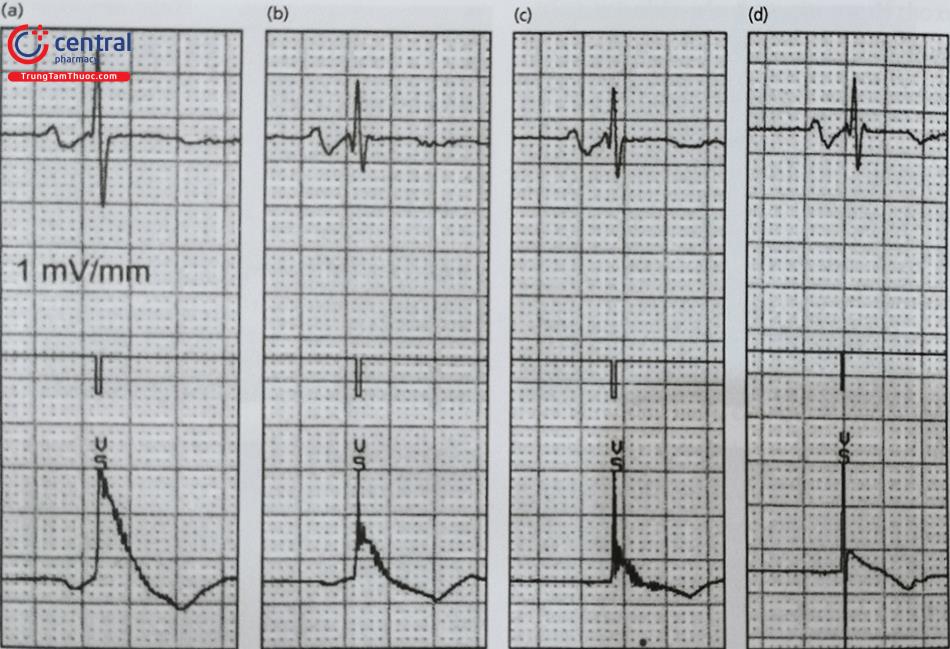
Bước 7: Kiểm tra độ bám chắc của điện cực và đặt điện cực tư thế phù hợp sao cho 2 cuộn sốc ở trong thất phải và tĩnh mạch chủ trên.
Bước 8: Cố định điện cực, kết nối mới máy phát xung, kiểm tra lại thông số một lần nữa (trở kháng sốc, trở kháng dây, ngưỡng tạo nhịp và ngưỡng nhận cảm).
Bước 9: Chúng ta nên khâu cố định máy vào tổ chức cơ trong ổ máy để hạn chế máy di động về sau này. Đóng da 2 lớp.
4.3 Máy ICD dưới da (S-ICD)
Đối với hệ thống ICD thông thường, điện cực sốc là thành phần dễ bị hỏng hóc và biến chứng nhiều nhất bao gồm: bật, thủng tim, đứt dây và nhiễm trùng. Để giải quyết những hạn chế của điện cực sốc tĩnh mạch, S-ICD với điện cực cấy dưới da được phát triển và được FDA công nhận năm 2013.
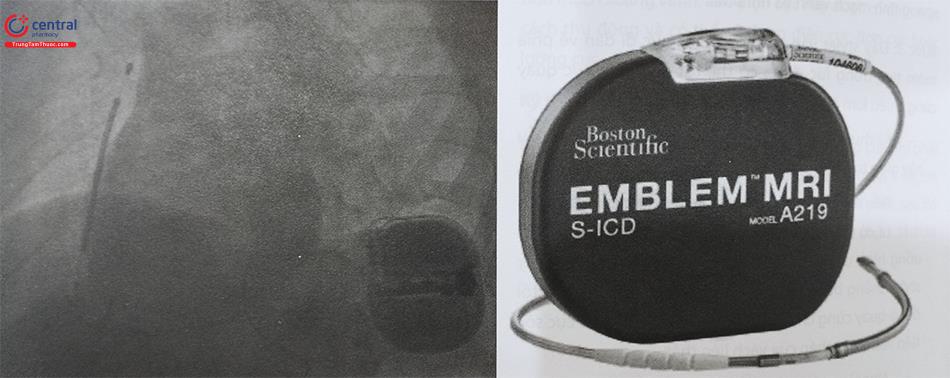
Kỹ thuật cấy máy S-ICD
Bước 1: Xác định vị trí làm ổ máy và vị trí đặt điện cực sốc dưới da vùng cạnh ức bên trái (Hình 52.17).
Bước 2: Vị trí rạch da để cấy máy S-ICD ở vùng khoang liên sườn 5-6 đường nách trước, song song với xương sườn (Hình 17). Mở túi máy cẩn thận theo từng lớp cơ, để máy S-ICD hoạt động hiệu quả thì mở túi máy càng ra phía sau càng tốt.
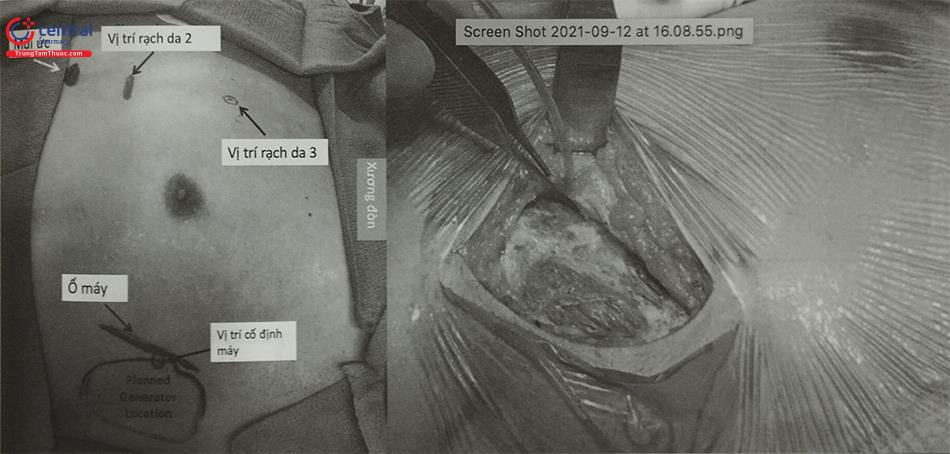
Bước 3: Tiếp theo là đường mở nhỏ thành bên cạnh mũi ức. Khâu 2 sợi chỉ số 0 chờ sẵn.
Dụng cụ tạo đường hầm để tạo đường hầm từ đường mở nhỏ cạnh mũi ức, song song với mặt cân cơ vào ổ máy.
Buộc đầu điện cực sốc bằng chỉ số 0 và kết nối với dụng cụ tạo đường hầm, kéo điện cực qua đường hầm về phía mũi ức và cố định điện cực bằng 2 sợi chỉ khâu chờ trước (Hình 18).
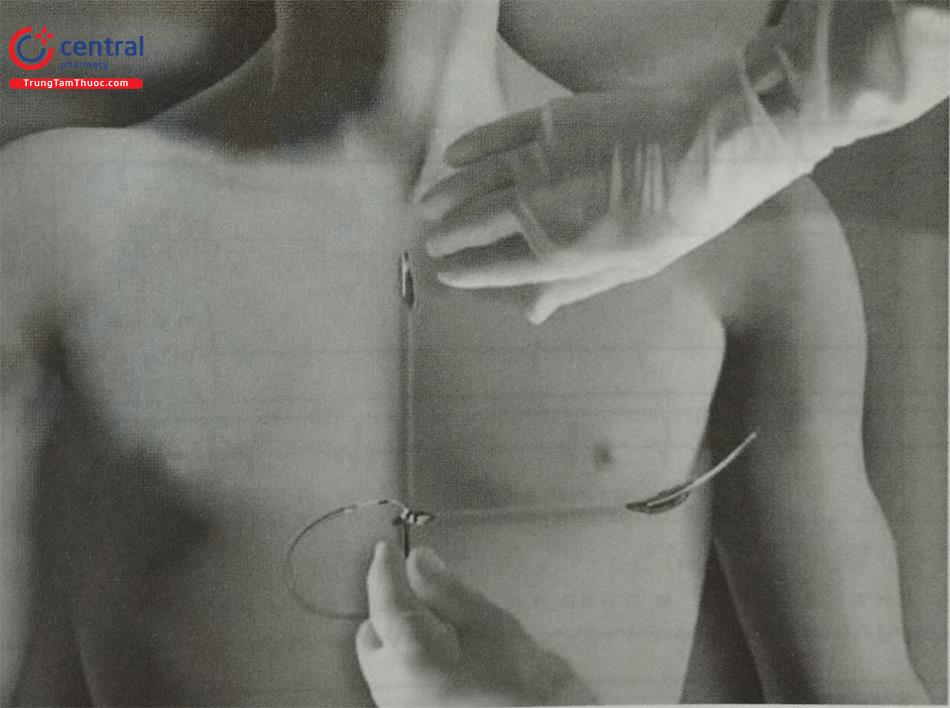
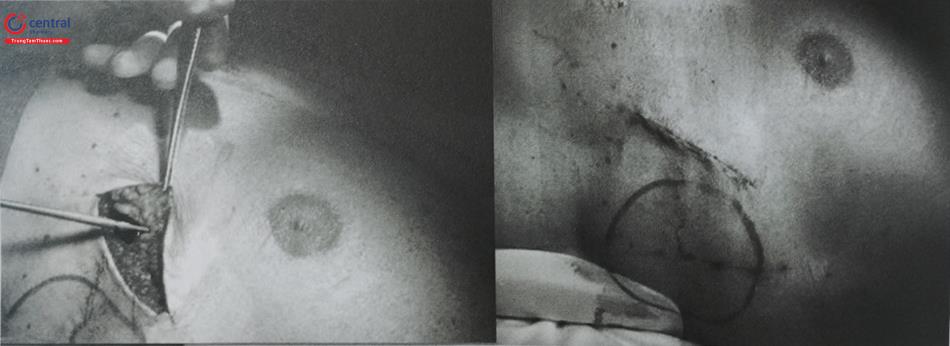
Với kỹ thuật ba đường rạch truyền thống, một vết rạch nhỏ ở gần phần hõm trên xương ức và bên cạnh đường giữa xương ức dọc theo mặt phẳng cân cơ.
Luồn đầu xa của điện cực sốc dọc theo xương ức, cố định điện cực.
Kết nối với máy ICD và đóng da (Hình 19).
5 Kiểm tra ngưỡng sốc và lập trình máy ICD
5.1 Kiểm tra độ pha srung cấp tính (DFT)
Kiểm tra ngưỡng sốc được chỉ định ở bệnh nhân dự phòng đột tử thứ phát. Không cần kiểm tra ngưỡng sốc ở người bệnh có chỉ định cấy máy phá rung dự phòng tiên phát.
Kiểm tra ngưỡng sốc bằng cách gây cơn rung thất bằng sốc với năng lượng 1-2 J vào đỉnh sóng T (Hình 52.20) hoặc kích thích thất bằng nghiệm pháp Burst để gây cơn rung thất (Hình 52.21). Sau đó tìm ngưỡng sốc điện cắt thành công cơn rung thất.
Kiểm tra độ phá rung tim cấp tính (DFT) được thực hiện để chắc chắn mức độ an toàn và hiệu quả điều trị rối loạn nhịp thất. Ngưỡng phá rung (DFT) được định nghĩa là năng lượng thấp nhất giúp chấm dứt thành công cơn rung thất. Tuy nhiên không giống với ngưỡng tạo nhịp, DFT không phải là một giá trị tuyệt đối, mà trên ngưỡng phá rung tim luôn luôn thành công và dưới ngưỡng đó sẽ luôn thất bại.
Bệnh nhân cần được gây mê khi làm DFT, chuẩn bị sốc ngoài nếu test phá rung không thành công. Nếu nhiều nhát test sốc được thực hiện, các lần test sốc tiếp theo nên được thực hiện cách nhau mỗi 5 phút.
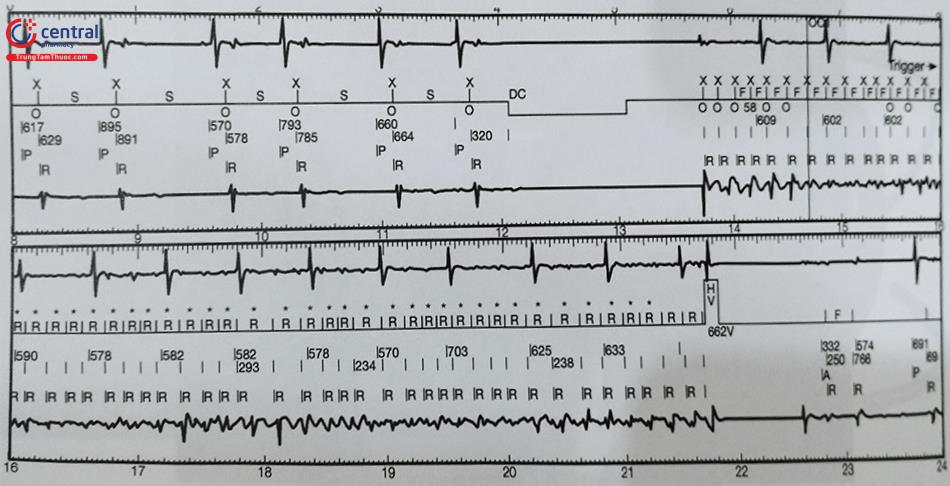
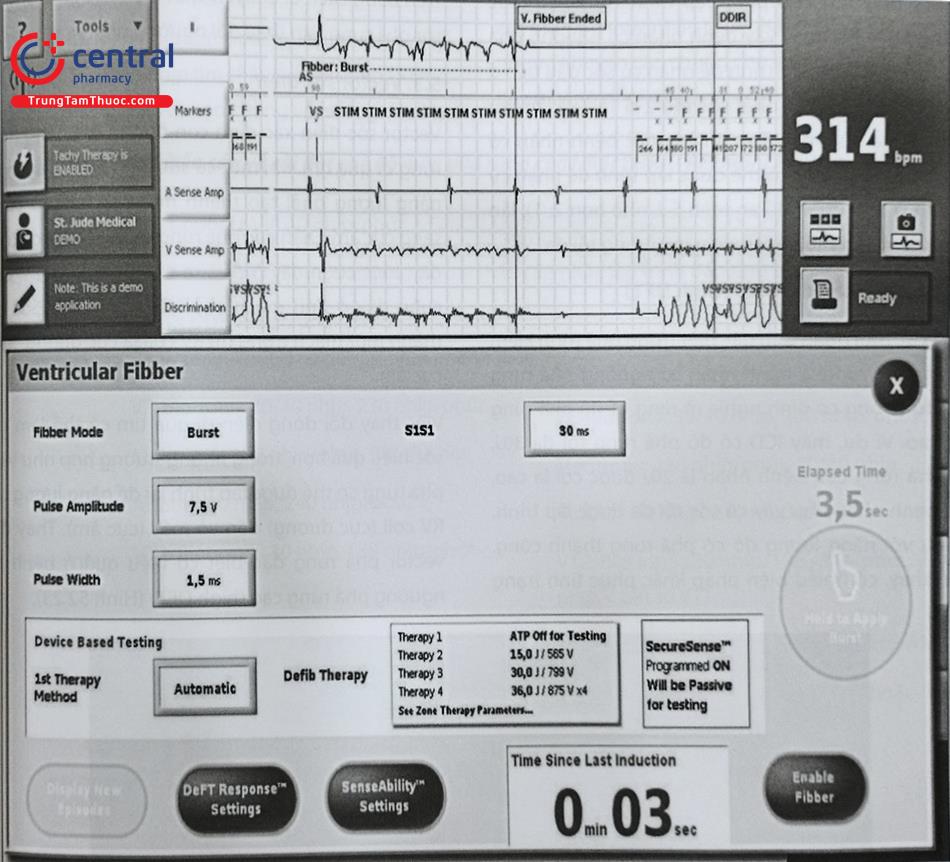
Mỗi bệnh nhân có ngưỡng năng lượng phá rung thành công khác nhau, ngưỡng sốc còn phụ thuộc tình trạng bệnh lý, thuốc điều trị rối loạn nhịp và nhiều yếu tố khác nữa. Qua các phân tích gộp chúng tôi thấy có mối quan hệ giữa xác suất phá rung tim thành công so với năng lượng được cung cấp tạo ra hình cong (Hình 22).
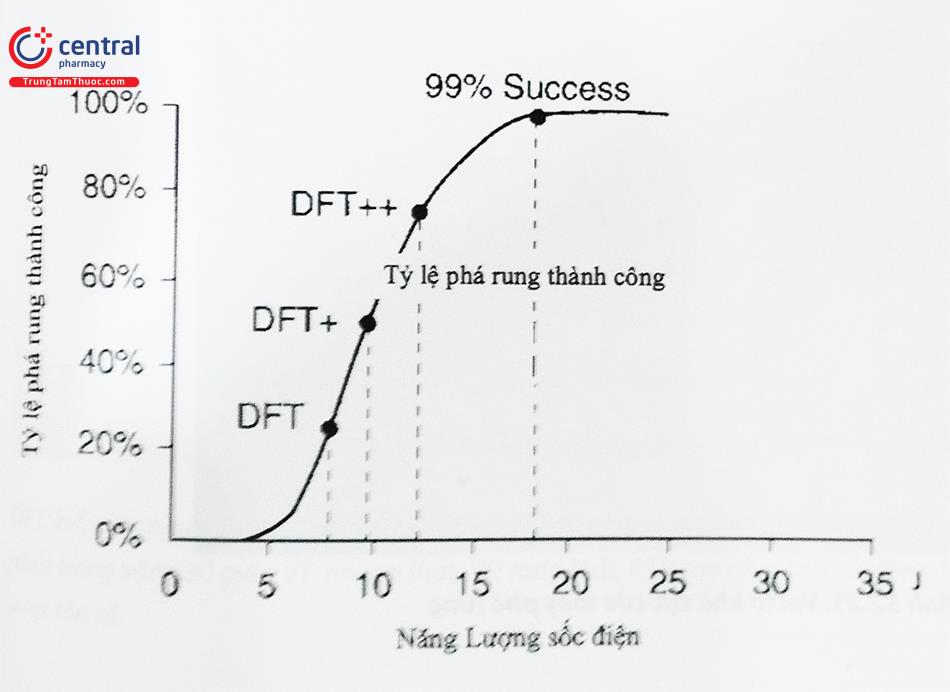
Hầu hết các máy ICD cho phép lập trình với nhiều mức năng lượng khác nhau, vì vậy bệnh nhân có ngưỡng phá rung là 5 J có thể được lập trình để nhận cú sốc đầu tiên ở 10 J (biên độ an toàn 2:1), nhát sốc thứ 2 là 15 J và lần thứ ba ở mức tối đa của máy. Tuy nhiên, một bệnh nhân có ngưỡng phá rung là 10 J có thể được lập trình để nhận cú sốc đầu tiên ở 15 J (biên độ an toàn 5 J, nhỏ hơn 2: 1), lần thứ hai ở 20 J và lần thứ ba ở mức năng lượng tối đa.
5.2 Độ phá rung cấp tính cao (HIGH DFT)
Một trong các mối quan tâm đặc biệt trong quá trình kiểm tra ngưỡng phá rung là bệnh nhân có ngưỡng phá rung cao, mặc dù không có định nghĩa rõ ràng về độ phá rung cấp tính cao. Ví dụ, máy ICD có độ phá rung tối đa 30J, ngưỡng phá rung của bệnh nhân là 20J được coi là cao, ở những bệnh nhân như vậy cú sốc tối đa được lập trình, nhưng liệu với năng lượng đó có phá rung thành công. May mắn thay, có nhiều biện pháp khắc phục tình trạng trên bằng cách di chuyển vị trí điện cực phá rung, đổi vec- tor phá rung làm thay đổi ngưỡng phá rung.
5.3 Vector sốc điện
Vector sốc điện xác định con đường mà năng lượng phá rung đi qua tim. Khi một cú sốc điện được truyền đến tim, năng lượng phải tạo thành một mạch đi từ cực dương sang cực âm. Điện cực phá rung thông thường có hai cuộn dây, một cuộn dây ở đầu xa của thất phải (RV Coil), một cuộn dây ở tĩnh mạch chủ trên (SVC coil). Sốc điện tạo thành một mạch trong đó RV coil là cực dương, SVC coil là cực âm.
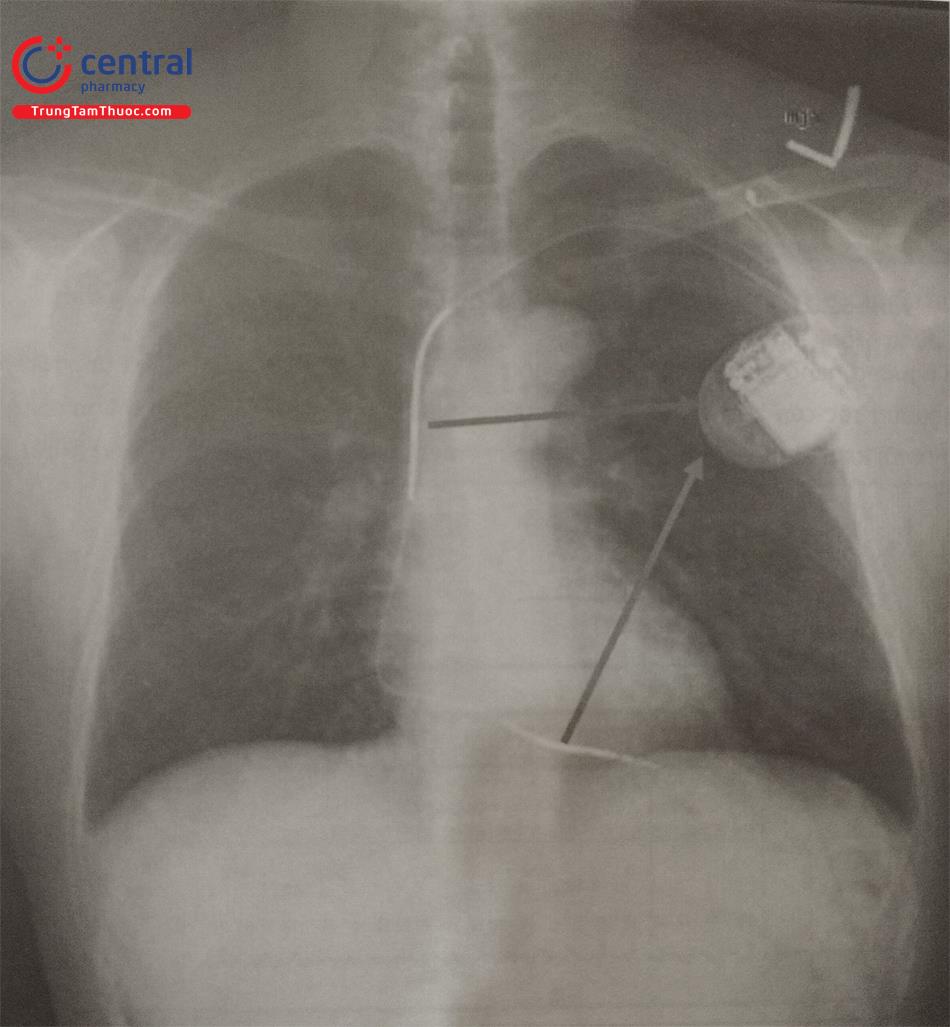
Việc thay đổi dòng điện đi qua tim có thể làm cho nhát sốc hiệu quả hơn, trong những trường hợp như vậy vector phá rung có thể được lập trình lại để năng lượng truyền từ RV coil (cực dương) đến vỏ máy (cực âm). Thay đổi chiều vector phá rung đặc biệt có hiệu quả ở bệnh nhân có ngưỡng phá rung cao (high DFT) (Hình 23).
5.4 Lập trình máy phá rung tự động
Năm 2019, Hội rối loạn nhịp tim Hoa Kỳ, Hội rối loạn nhịp tim châu Âu, Hội rối loạn nhịp tim châu Á – Thái Bình Dương đã thống nhất đưa ra khuyến cáo chung về hướng dẫn lập trình máy phá rung tự động. Tuy các hãng khác nhau có các phương thức nhận cảm phát hiện và cắt cơn khác nhau nhưng khuyến cáo chung cho lập trình máy ICD được trình bày ở bảng dưới đây.
Bảng 4. Khuyến cáo về cài đặt chế độ máy phá rung của HRS/ EHRA/ APHRS/ LAHRS năm 2019
| Nhịp chậm | ICD 1 buồng: VVI 40 nhịp/phút ICD 2 buồng: DDD, ưu tiên nhịp nội tại thất, cân nhắc lập trình đáp ứng tần số CRTD: DDD ± Đáp ứng tần số | |
| Phát hiện nhịp nhanh | Bệnh nhân không có tiền sử nhịp nhanh thất VF: Biotronik 30/40 nhịp, 230 nhịp/phút Medtronic 188 nhịp/phút, 30/40 nhịp Abbott: 30 nhịp, 240 nhịp/phút VT2: Biotronik: 30 nhịp, 188 nhịp/phút
Medtronic: Off Abbott: 30 nhịp, 187 nhịp/phút VT1: theo dõi | Bệnh nhân biết tần số cơn nhịp nhanh thất VF: Biotronik 30/40 nhịp, 230 nhịp/phút Medtronic 188 nhịp/phút, 30/40 nhịp Abbott: 30 nhịp, 240 nhịp/phút VT2: Biotronik: 30 nhịp, 188 nhịp/phút, (hoặc 10-20 nhịp < tần số VT) Medtronic: 24 nhịp, 10-20 nhịp < tần số VT Abbott: 30 nhịp, 187 nhịp/phút (hoặc 10-20 nhịp < tần số VT) VT1: theo dõi |
| Điều trị | VF: ATP trong khi sạc 8 nhịp/85% CL VT, sốc năng lượng cao nhất ( trừ khi có DFT) VT2: ATP (burst, ramp), chẩn đoán lại nếu còn VT sốc điện. Năng lượng phụ thuộc vào DFT VT1: Vùng theo dõi hoặc ATP cắt cơn nhịp nhanh | |
| Phân biệt SVT | Máy ICD 1 buồng
Máy ICD 2 buồng
| |
| S-ICD | Vùng sốc: khi tần số ≥ 230 nhịp/phút Vùng điều kiện: ≥ 200 nhịp/phút hoặc 10-20 nhịp < tần số VT ( nếu có cơn nhanh thất trước đó) PSP ( post shock pacing) ON | |
DFT: kiểm tra ngưỡng sốc, PSP: máy S-ICD cho phép phóng ra dòng điện 200mA qua thành ngực để tạo nhịp tim 50 chu kỳ trên phút trong vòng 30 giây. VT: nhanh thất, VF: rung thất, PSP: tạo nhịp sau sốc điện, SVT: cơn tim nhanh trên thất, ATP: tạo nhịp vượt tần số.
6 Biến chứng của thủ thuật và xử trí
6.1 Biến chứng liên quan đến chọc mạch
Biến chứng chọc mạch phụ thuộc vào kỹ năng của phẫu thuật viên và giải phẫu hệ của bệnh nhân. Các biến chứng thường gặp liên quan đến chọc mạch bao gồm làm tổn thương các tổ chức xung quanh tĩnh mạch là phổi, động mạch dưới đòn, thần kinh và ống ngực, là nguyên nhân thường nhất của biến chứng cấy máy tạo nhịp. Biết được giải phẫu hệ tĩnh mạch dưới đòn bằng cách chụp tĩnh mạch giúp chọc mạch hiệu quả và giảm biến chứng.
6.1.1 Tràn khí màng phổi
Thường không có triệu chứng và phát hiện bằng chụp Xquang tim phổi sau cấy máy, hiếm khi xuất hiện tràn khí màng phổi gây suy hô hấp trong quá trình can thiệp. Triệu chứng đau kiểu màng phổi, ho, khó thở là các triệu chứng gợi ý của tràn khí màng phổi.
Theo dõi độ bão hòa oxy, mạch nhanh, theo dõi khí máu và kiểm tra dưới màn tăng sáng hai trường phổi cũng nên làm trong quá trình cấy máy.
Điều trị tràn khí màng phổi phụ thuộc vào mức độ nghiêm trọng của triệu chứng kèm theo. Bệnh nhân có tình trạng suy hô hấp cấp cần phải đặt nội khí quản cấp cứu, nếu tràn khí màng phổi số lượng ít, đôi khi chỉ cần theo dõi, thở oxy và chụp Xquang liên tiếp đánh giá mức độ tiến triển của tràn khí. Khi tràn khí gây triệu chứng suy hô hấp cần chọc dẫn lưu khí và hút áp lực âm liên tục.
6.1.2 Chọc và động mạch dưới đòn và tràn máu màng phổi
Tràn máu màng phổi là biến chứng hiếm gặp khi chọc tĩnh mạch nách và tĩnh mạch dưới đòn, thường do tổn thương động mạch và tĩnh mạch dưới đòn và các mạch máu khác trong lồng ngực. Việc chọc vào động mạch dưới đòn có thể không để lại biến chứng nếu kim được rút ra và ép vào vị trí đi vào dưới xương đòn. Vấn đề trở nên nghiêm trọng nếu phần vát của kim làm cho động mạch bị rách hoặc lỡ luồn sheath vào động mạch (Hình 25).
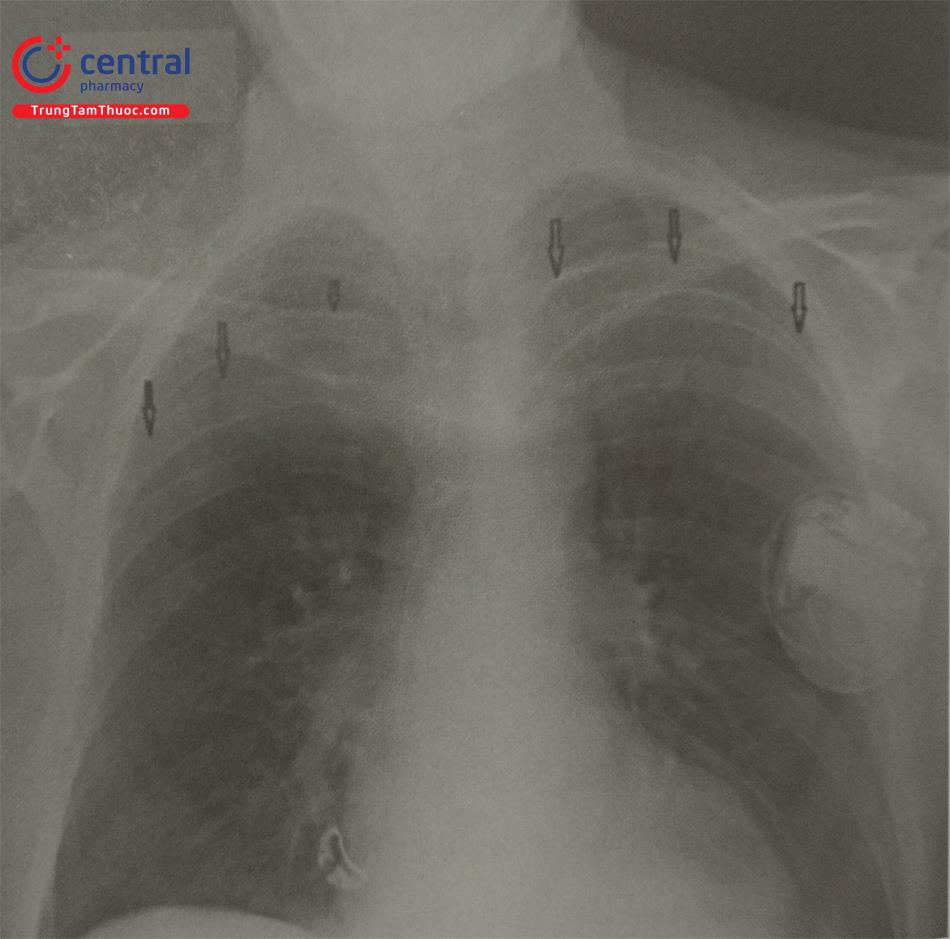
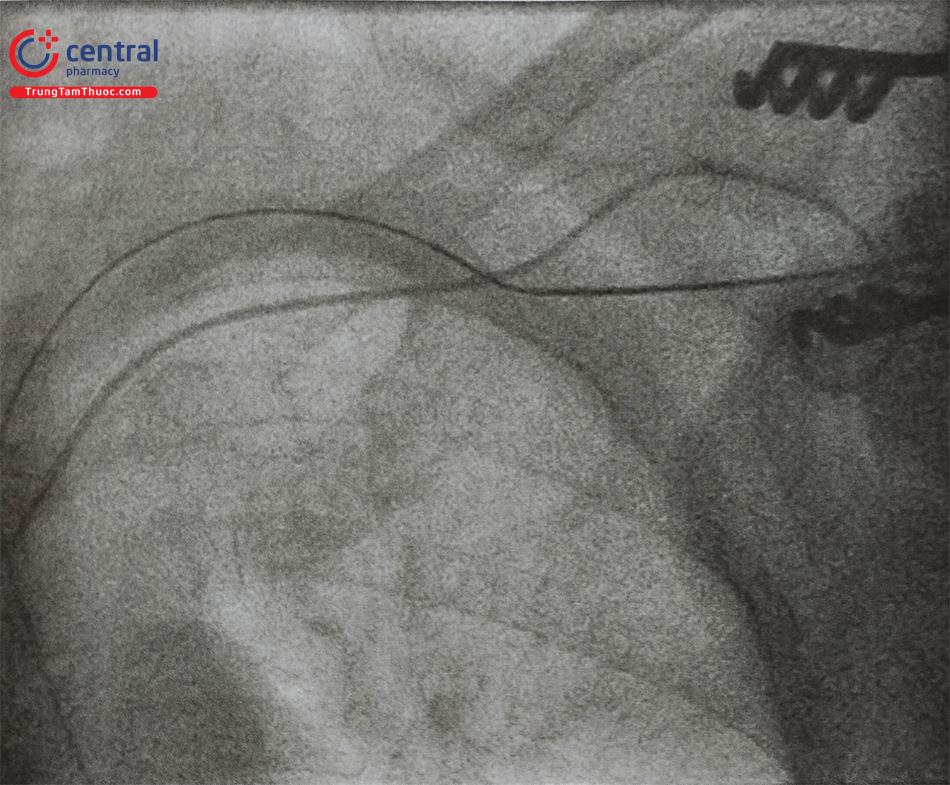
Nếu tình trạng chảy máu nhiều chúng ta có thể sử dụng một số biện pháp để cầm máu như, bơm bóng chèn vào vị trí rách, đặt stent có màng bọc hoặc thậm chí bít bằng coil. Ngừng hoặc trung hoà các thuốc chống đông và chống ngưng tập tiểu cầu đang dùng, nếu tràn máu màng phổi nhiều chúng ta có thể dẫn lưu.
Trong một số trường hợp cần đến sự can thiệp của ngoại khoa, nếu vị trí chọc mạch ở vùng động mạch nách chúng ta có thể cầm máu từ bên ngoài, nhưng vị trí ở vùng dưới đòn việc mở ngực có thể phải đặt ra khi tình trạng mất máu của bệnh nhân vẫn tiếp diễn mặc dù đã dùng các biện pháp can thiệp và điều trị nội khoa.
6.1.3 Thuyên tắc khí
Thuyên tắc khí có thể xảy ra khi đưa sheath vào, khí được đưa vào bởi áp lực âm của lồng ngực ở bệnh nhân ngủ ngáy nặng hít thở sâu (Hình 26).
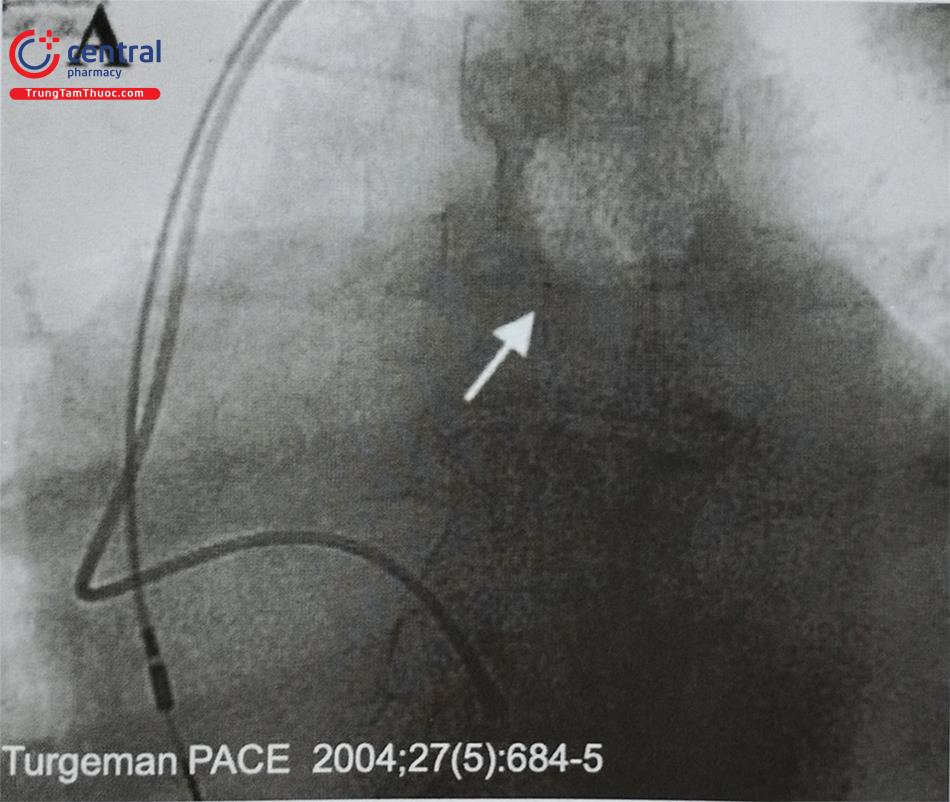
Hầu hết trường hợp lượng khí đưa vào ít, nhưng cũng có thể gây suy hô hấp, đau ngực, độ bão hòa oxy giảm nếu có sự tắc nghẽn đáng kể của dòng chảy và động mạch phổi.
Điều trị thuyên tắc khí bao gồm thở oxy, hút khí bằng ống thông, và điều trị hỗ trợ nếu cần thiết.
Các biện pháp phòng ngừa thuyên tắc khí: tăng áp lực tĩnh mạch trung tâm bằng cách truyền dịch, gác chân cao. Đánh thức bệnh nhân tránh hít sâu. Sử dụng introducer sheath có van.
Các biến chứng hiếm gặp khác: tắc ống dẫn ngực, tổn thương động mạch vú.
6.2 Biến chứng liên quan đến điện cực
6.2.1 Việc đưa, lái và đặt điện cực trong buồng tim có thể gây ra các biến chứng
Rối loạn nhịp
Gây nhịp chậm do cường phế vị, sử dụng thuốc gây tê quá mức, tổn thương đường dẫn truyền (ví dụ: chấn thương nhánh His bên phải gây điện tâm đồ dạng block nhánh phải), việc đặt máy tạo nhịp tạm thời hoặc dùng isoproterenol rất hữu ích.
Rối loạn nhịp tim nhanh có thể xảy ra trong quá trình cấy máy, nó thường là kết quả của điện cực kích thích vào cơ tim. Rung nhĩ có thể xảy ra trước và trong khi đặt điện cực nhĩ dẫn đến chúng ta không kiểm tra được thông số của nhĩ, một số trường hợp cần chuyển nhịp bằng thuốc hoặc sốc điện. Rối loạn nhịp thất là phổ biến, đặc biệt ở bệnh nhân suy tim là do đầu điện cực kích thích vào buồng thất, nhưng hiếm khi bền bỉ. Rút điện cực ra khỏi vị trí gây rối loạn nhịp hầu hết cắt được cơn nhịp nhanh, một số trường hợp có thể dẫn đến cơn rung thất hoặc xoắn đỉnh, nên việc luôn luôn dự phòng sẵn bằng máy sốc điện ngoài cơ thể rất quan trọng ở bệnh nhân cấy máy phá rung tự động.
Thủng tim
Quả tim có thể bị thủng bởi các điện cực phá rung, có thể cấp tính hoặc bán cấp, phần đầu xoáy bám vào cơ tim có thể gây thủng tim đặc biệt ở bệnh nhân có tiền sử nhồi máu thất phải khi đó thành thất mỏng và bệnh nhân uống thuốc chống ngưng tập tiểu cầu làm tăng nguy cơ tràn máu màng tim (Hình 27).
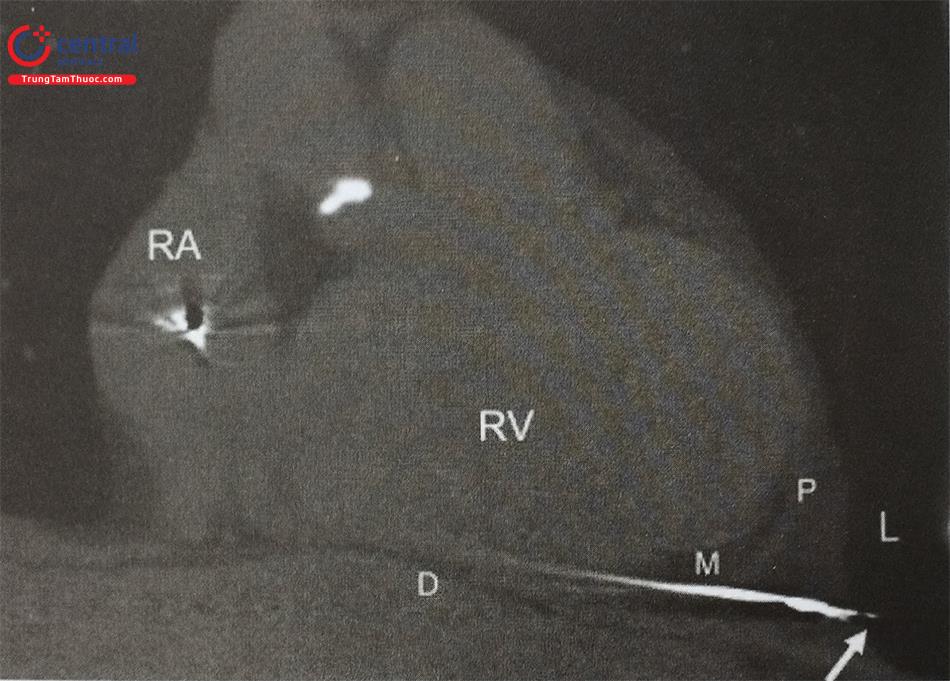
Khi cấy máy phá rung tự động, ngưỡng nhận cảm và ngưỡng tạo nhịp kém các bác sĩ thường rút điện cực lại và lỗ thủng thường được bịt kín. Có trường hợp tiến triển tràn máu màng tim đặc biệt ở bệnh nhân đang dùng thuốc chống đông, việc theo dõi huyết động và siêu âm tim, theo dõi tiến triển của dịch màng tim bằng cách nghiêng trái (LAO) để theo dõi bóng tim rất hữu ích. Chọc dẫn lưu dịch màng tim tư thế LAO giúp thủ thuật trở nên dễ dàng hơn, ngừng thuốc chống ngưng tập tiểu cầu, đảo ngược chống đông nếu cần thiết.
6.2.2 Các biến chứng liên quan đến điện cực khác
Tổn thương van ba lá
Trong quá trình cấy ICD có thể gây rách hoặc tổn thương van ba lá dẫn đến tình trạng hở ba lá, tăng nguy cơ nhiễm trùng và viêm nội tâm mạc .
Bản thân của dây dẫn cũng có thể bị hư hỏng do tác động vật lý trong quá trình cấy ghép hoặc do mắc kẹt trong hệ thống cơ xương. Mất tính toàn vẹn của lớp cách điện thường được biểu hiện bằng trở kháng thấp, gây dòng điện cao. Khi đứt điện cực dẫn điện điện trở dây tăng cao. Việc đứt gãy điện cực dẫn đến bệnh nhân có những nhát sốc không tương thích (Hình 28).

Giải pháp cho trường hợp này là cố gắng rút dây điện cực cũ và thay bằng dây điện cực mới.
Bật điện cực
Tỷ lệ bật điện cực trong các nghiên cứu khoảng 2-3%, nguy cơ của biến chứng này được giảm thiểu bằng cách đặt điện cực ở vị trí ổn định, để điện cực chùng vừa phải và điện cực ít di chuyển theo sự đóng mở của van ba lá (Hình 29).
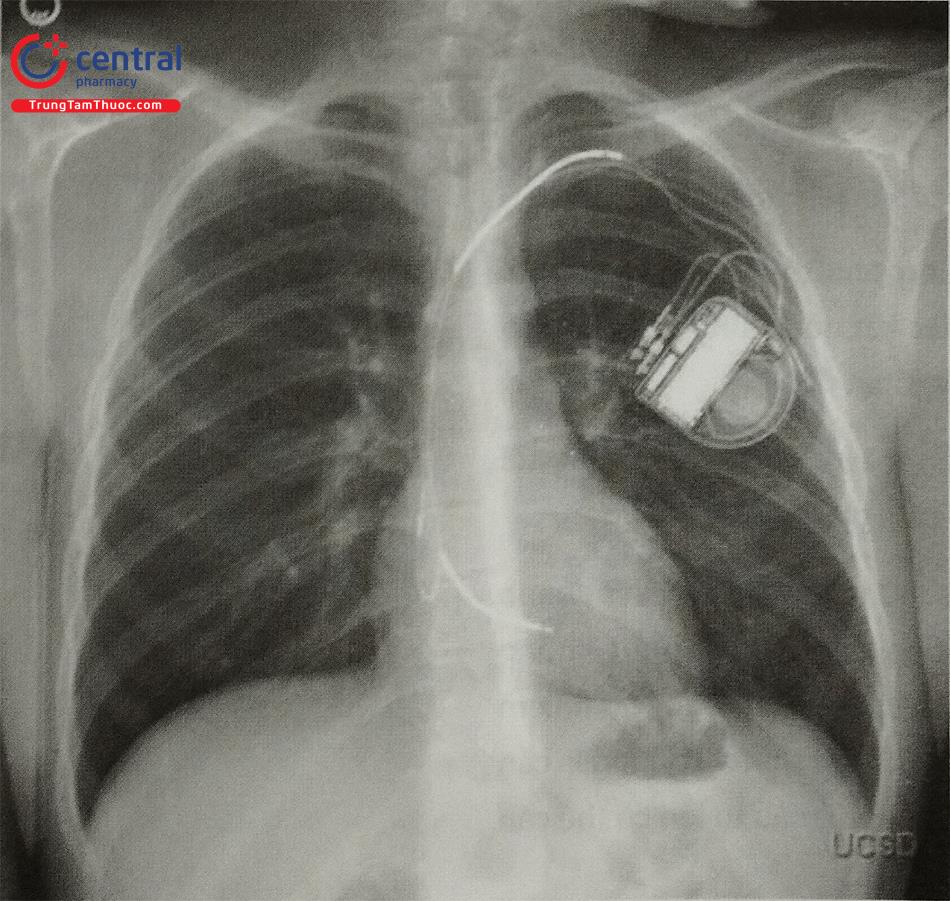
Huyết khối tĩnh mạch
Một trong các biến chứng của cấy máy phá rung tự động đường tĩnh mạch là huyết khối gây tắc tĩnh mạch dưới đòn. Huyết khối tĩnh mạch dưới đòn có thể xuất hiện cấp tính hoặc bán cấp (Hình 30). Biểu hiện lâm sàng hạn chế, đôi khi xuất hiện dấu hiệu sưng nóng đỏ đau chi trên bên cấy máy, thường xuất hiện vài tuần sau khi cấy máy. Huyết khối có thể lan đến tĩnh mạch chủ trên, cấu trúc bên cạnh, thậm chí gây huyết khối tĩnh mạch não. Siêu âm doppler mạch và chụp tĩnh mạch có thể biết được tình trạng của huyết khối. Sử dụng thuốc chống đông đường uống, đặc biệt thuốc chống đông thế hệ mới được ưu tiên, thuốc được duy trì trong 3-6 tháng.
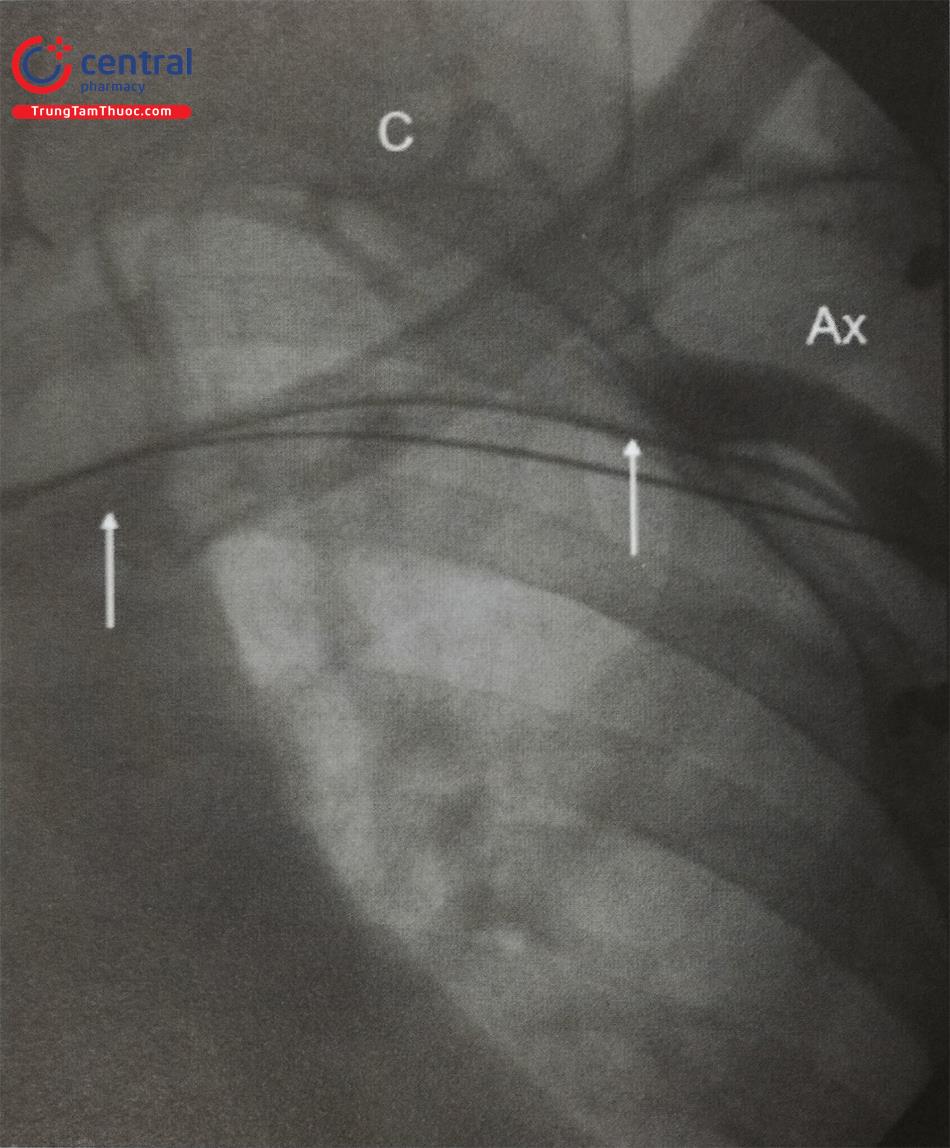
6.3 Biến chứng liên quan đến máy phá rung
Chức năng của máy phá rung phụ thuộc vào sự kết nối điện cực và máy ICD, nếu việc kết nối không tốt, dẫn đến điện trở tăng cao, máy không hoạt động.
Làm túi máy quá to dẫn đến máy bị di chuyển trong túi máy, làm cho bệnh nhân có cảm giác đau khi cử động.
Tụ máu trong ổ máy là biến chứng hay gặp đặc biệt bệnh nhân đang dùng thuốc chống đông hoặc thuốc chống ngưng tập tiểu cầu, việc tụ máu làm tăng nguy cơ nhiễm trùng máy tạo nhịp, việc dùng kháng sinh dự phòng là cần thiết, trong một số trường hợp khối máu tụ lớn có thể cân nhắc lấy khối máu tụ (Hình 31).
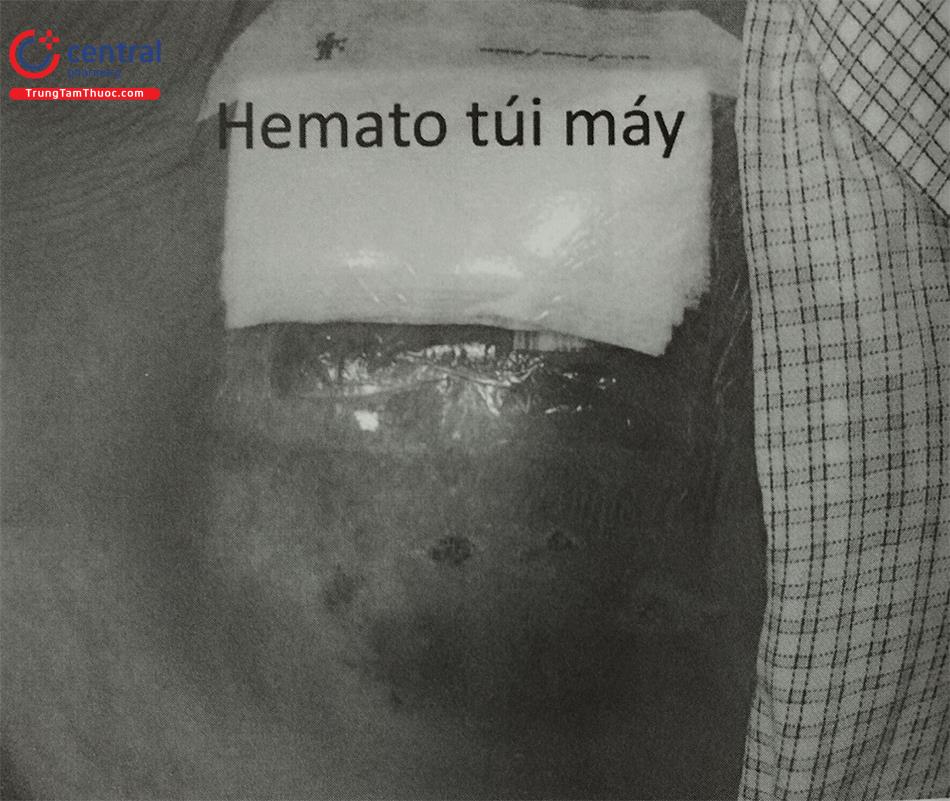
6.4 Biến chứng nhiễm trùng
Nhiễm trùng máy phá rung, viêm nội tâm mạc nhiễm khuẩn ở bệnh nhân có cấy ghép dụng cụ là biến chứng để lại nhiều hậu quả nặng nề. Việc tháo máy và rút bỏ toàn bộ dây ra là cần thiết để điều trị kháng sinh có hiệu quả. Nếu việc cấy máy phá rung lại là bắt buộc nên cấy máy bên đối diện khi tình trạng nhiễm trùng đã được kiểm soát. (Hình 32).
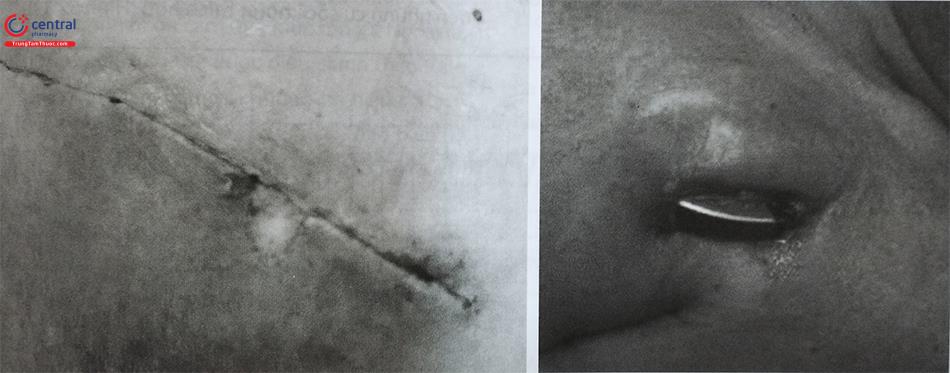
7 Theo dõi sau cấy máy, các sự cố và cách khắc phục của máy phá rung
Để đảm bảo hoạt động đúng và lập trình phù hợp của máy ICD, việc theo dõi thường xuyên là rất cần thiết. Với các thiết bị hiện đại, điều này có thể đạt được thông qua sự kết hợp giữa các lần kiểm tra máy trực tiếp và giám sát từ xa. Theo khuyến cáo, người bệnh theo dõi máy lần đầu trong vòng 2 đến 12 tuần sau khi cấy ghép ICD. Trong lần theo dõi máy này, vết mổ cần được kiểm tra xem có dấu hiệu nhiễm trùng và tháo chỉ khâu nếu có. Lập trình ICD được thực hiện để đánh giá chức năng của thiết bị và các thông tin chẩn đoán và các thông số của máy để tối ưu hóa lập trình. Các cảnh báo âm thanh và rung nên được thử nghiệm để bệnh nhân có thể nhận biết. Sau đó, việc thực hiện đánh giá thiết bị nên được thực hiện sau mỗi 3 -6 tháng hoặc qua các lần kiểm tra máy trực tiếp và giám sát từ xa.
Bảng 5. Nội dung theo dõi máy ICD (mỗi 3-6 tháng)
| Điện áp pin (và trở kháng) |
Thời gian sạc tụ Ngưỡng nhận cảm của các điện cực Ngưỡng tạo nhịp của các điện cực |
Trở kháng của các điện cực tạo nhịp và bản cực Phần trăm tạo nhịp ở các buồng tim |
| Cơn loạn nhịp thu thập bởi thiết bị |
Liệu pháp điều trị để cắt cơn SVT/VT/VF (Nhịp nhanh trên thất/Nhanh thất/Rung thất) Xem xét các thông số lập trình chính |
| Xem xét lại các cảnh báo từ thiết bị |
| Xem xét các phép đo huyết động (nếu có thể) |
7.1 Tính toàn vẹn của điện cực
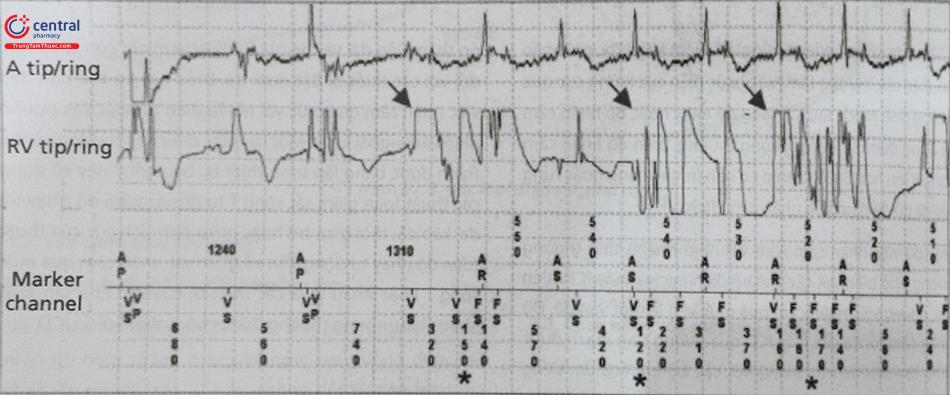
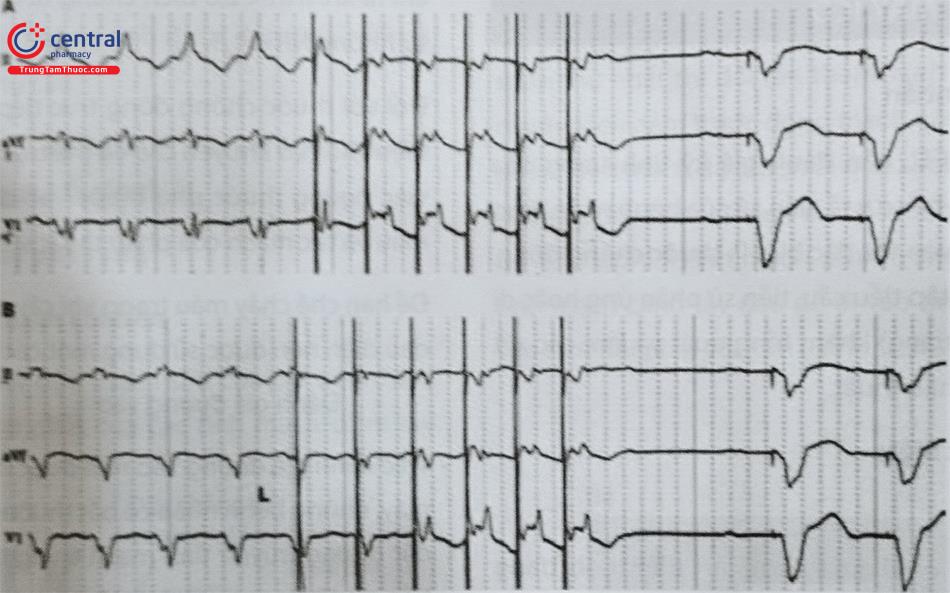
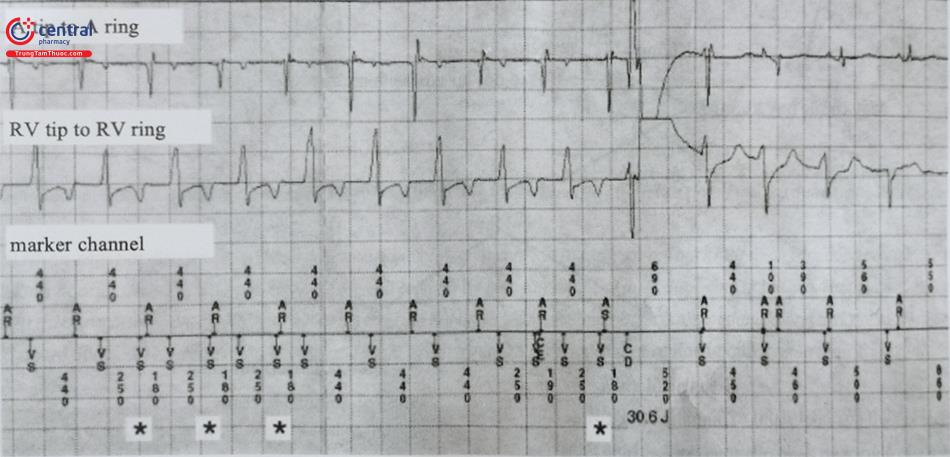
Liên kết yếu nhất trong một hệ thống ICD là điện cực sốc, do đó phải theo dõi chặt chẽ tính toàn vẹn của dây dẫn và cuộn dây sốc. Nhiễu không liên tục thường đi trước những thay đổi quan sát được trong các thông số tiêu chuẩn của điện cực (ví dụ: trở kháng, nhận cảm, ngưỡng tạo nhịp). Do đó, các điện đồ trong buồng tim (EGM) của các sự kiện đảo ngược nhiễu (Noise Reversion Event) và cơn nhanh thất không bền bỉ nên được xem xét chi tiết. Tín hiệu Make-Break có thể được thấy ở những điện cực gãy, dẫn đến những cú sốc không thích hợp (Hình 33).

Ghi lại từ một máy ICD tạo nhịp hai thất (CRT-D) với một điện cực ICD bị gãy. Các bệnh nhân bị nhiều cú sốc ICD. Bản ghi cho thấy bệnh nhân có rung nhĩ ở kênh nhĩ và nhịp hai thất ở bảng giữa. Có những khoảng thời gian không sinh lý đột ngột (khoảng RR <130 ms) với các điện đồ bất thường loại Make-Break và độ bão hòa của kênh khuếch đại (*). Điều này phù hợp với sự mất toàn vẹn của điện cực. Lưu ý sự khác biệt giữa một bản ghi sóng rung trong kênh nhĩ so với nhiễu trên kênh thất. Mặc dù một số khoảng thời gian ngắn có thể được nhìn thấy ngay cả khi rung nhĩ (hoặc V-V trong tâm thất) (#), các đặc điểm của tín hiệu khác nhau rõ rệt. A: Cực âm (tip)- Cực dương (Ring); V: Cực âm (tip)- Cực dương (Ring).
7.2 Nhận cảm kênh thất
Trái ngược với nhận cảm cố định của máy tạo nhịp tim truyền thống, độ nhạy nhận cảm kênh thất trong máy ICD là động. Nó tự điều chỉnh theo biên độ sóng R và tăng độ nhạy theo thời gian để đạt độ nhạy được tối đa đã lập trình, đồng thời tránh nhận cảm quá mức sóng T. Ngoài ra, độ khuếch đại tín hiệu có thể được điều chỉnh theo từng nhịp để điều chỉnh nhận cảm với những tín hiệu có biên độ thay đổi. Kinh nghiệm lâu năm cho thấy rằng biên độ sóng R lớn hơn 5 mV thường là đủ để đảm bảo phát hiện thích hợp cơn rung thất (VF). Nhận cảm quá mức kênh thất ở bệnh nhân cấy ICD có thể có âm cảnh báo bệnh nhân nghe được, cảnh báo khi theo dõi máy hoặc nghiêm trọng hơn là một hoặc nhiều cú sốc không thích hợp. Nguyên nhân sinh lý gồm nhận cảm quá mức sóng T, đếm kép các phức bộ QRS, nhận cảm tín hiệu điện cơ hoành (Hình 34) và nhận cảm quá mức sóng P khi điện cực ở gần van ba lá. Nhận cảm quá mức do nguyên nhân không sinh lý bao gồm: Gãy điện cực, đầu kết nối có vấn đề (Nhiễu dạng Make-Break), hoặc nhiễu điện từ trường.
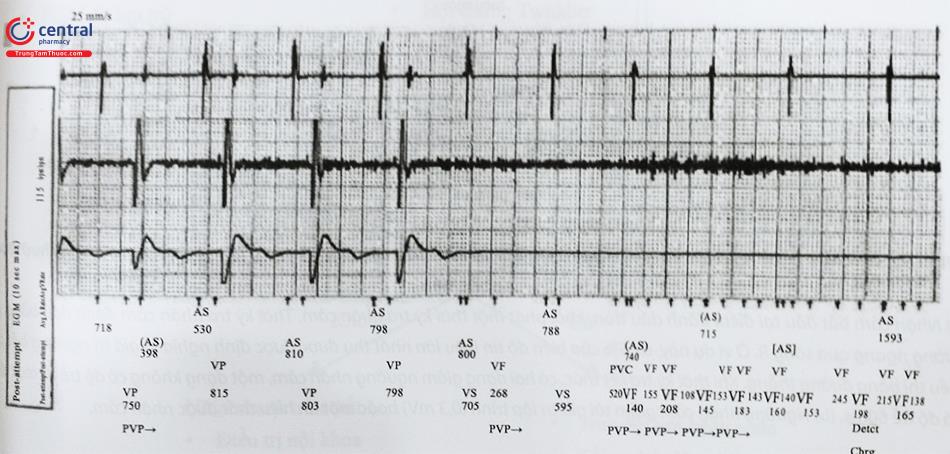
Dữ liệu trừ trên xuống: Điện tâm đồ trong buồng nhĩ, điện tâm đồ trong buồng thất và kênh điện đồ thất trường xa (Bản cực sốc). Nhịp xoang đều đang được hiển thị trong suốt đoạn dữ liệu. Tín hiệu điện cơ hoành được nhận cảm dẫn tới ức chế xung tạo nhịp thất, Cơn VF được máy phát hiện và tụ đắt đầu sạc.
Giải pháp cho nhận cảm quá mức phụ thuộc vào nguyên nhân. Lập trình lại nhận cảm của máy ICD sang cài đặt ít nhạy hơn có thể là một tùy chọn trong trường hợp nhận cảm quá mức trường gần (sóng R và sóng T). Điều này phải được cân bằng với nguy cơ tiềm ẩn máy bỏ sót cơn VT hoặc VF thực sự. Một phương pháp khác để điều chỉnh độ nhạy cảm là thay đổi độ trễ phân rã và ngưỡng bắt đầu. Bất kỳ khi nào các thông số nhận cảm được thay đổi, bác sĩ phải đánh giá xem có cần thực hiện đo ngưỡng phá rung tim để đảm bảo việc phát hiện VF hay không. Trong trường hợp không thể khắc phục được việc giám sát bằng lập trình (ví dụ: sóng R nhỏ, sóng T lớn), nên xem xét can thiệp lại.
Nhiễu điện từ trường
Ở bệnh nhân ICD, nhận cảm quá mức nhiễu điện từ trường (EMI) có thể dẫn đến phát hiện rối loạn nhịp thất không thích hợp và gây sốc (Hình 35). Ở những bệnh nhân phụ thuộc máy tạo nhịp tim, EMI có thể dẫn đến việc ức chế xung tạo nhịp dẫn đến chóng mặt hoặc ngất.
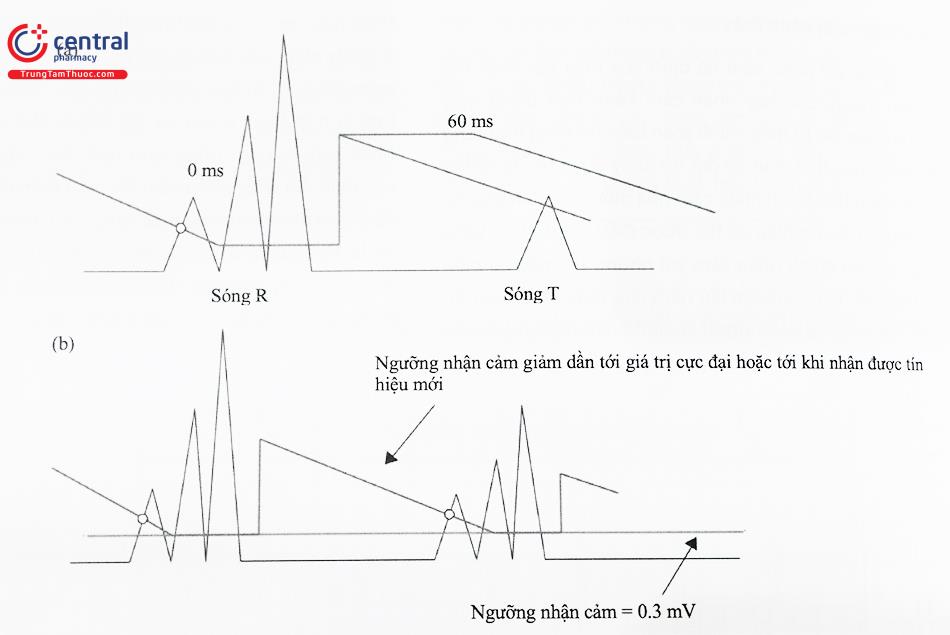
Nhận cảm bắt đầu tại điểm đánh dấu tròn, khởi phát một thời kỳ trơ nhận cảm. Thời kỳ trơ nhận cảm đánh dấu bằng một đường ngang qua sóng Ở ví dụ này, 62,5% của biên độ tín hiệu lớn nhất thu được được định nghĩa là giá trị ngưỡng bắt đầu, biểu thị bằng đường thẳng. Khi thời kỳ trơ kết thúc, có hai dạng giảm ngưỡng nhận cảm, một dạng không có độ trễ và một dạng có độ trễ 60ms. (b) Ngưỡng nhận cảm giảm tới giá trị lập trình (0,3 mV) hoặc một tín hiệu thất được nhận cảm.
8 Khắc phục sự cố
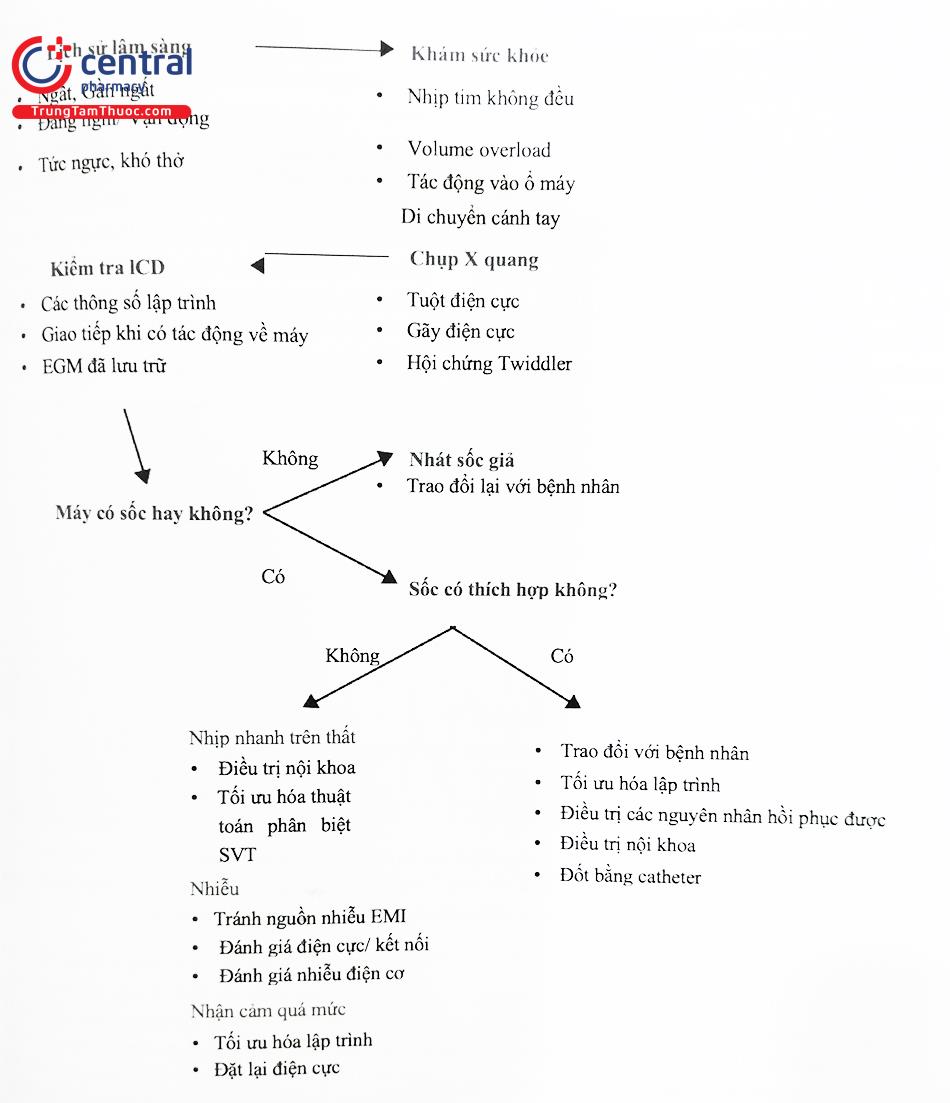
Mỗi cá thể bệnh nhân có những rủi ro riêng về sự cố ICD hoặc liệu pháp ICD (thích hợp hoặc không phù hợp). Tuy nhiên, việc xử lý sự cố được hướng dẫn bởi một số nguyên tắc chung, bao gồm tiền sử lâm sàng xung quanh sự kiện, khám sức khỏe, chụp Xquang và kiểm tra thiết bị (Hình 36). Ngoài ra, hiểu rõ về thuật toán của thiết bị là rất cần thiết khi xác định lý do liệu pháp được cung cấp hoặc ngăn chặn. Việc cung cấp các lần sốc không phù hợp hoặc không có sốc thích hợp thường gặp nhất là do lập trình không đúng hoặc không hiểu đầy đủ về các thuật toán của thiết bị (Bảng 6).
8.1 Đánh giá bệnh nhân
Sau một cú sốc duy nhất, bệnh nhân không có triệu chứng có thể không cần đến ngay hoặc thông báo cho phòng khám máy tạo nhịp tim/ ICD. Tuy nhiên, trong trường hợp có triệu chứng hoặc bị nhiều cú sốc, cần đánh giá tại khoa cấp cứu để xử trí nhanh chóng. Tiền sử lâm sàng xung quanh các cú sốc nên được khai thác. Các cú sốc không thích hợp do nhận cảm quá mức thường được gợi ý do thiếu các triệu chứng báo trước. Nhát sốc của ICD khi vận động có thể là thích hợp do VT hoặc không thích hợp do nhịp nhanh xoang hoặc rung nhĩ đáp ứng thất nhanh. Các cú sốc của máy ICD liên quan đến chuyển động của cánh tay hoặc vị trí cơ thể gợi ý gãy dây, dây dẫn không ổn định hoặc lỏng kết nối máy và điện cực. Đánh trống ngực trước khi điều trị ICD có thể do nhịp tim nhanh trên thất (SVT) hoặc VT.
8.2 Nhát sốc đơn
Khi một cú sốc được thực hiện, cần phải xác định xem nó là thích hợp (do VT/ VF) hay không thích hợp. Các cú sốc không thích hợp có thể được phân loại thêm là do SVT, nhận cảm quá mức trong buồng tim (sóng P, R, hoặc T) hoặc nhận cảm quá mức ngoài tim (ví dụ như điện cơ, EMI, gãy dây dẫn).
Điện đồ được lấy từ bộ nhớ của thiết bị. Nhận cảm quá mức sóng T được nhận biết bằng các sự kiện nhận cảm thất tương ứng với sóng T (*) và đếm kép. Do nhịp nhanh xoang ban đầu, những đợt nhận cảm quá mức này dẫn đến sốc ICD.
8.3 Nhiều cơn sốc
Nhiều cơn sốc có thể là thích hợp do cơn VT / VF liên tục hoặc lặp đi lặp lại hoặc không thích hợp do SVT, nhận cảm quá mức hoặc hỏng dây dẫn. Các cú sốc của máy ICD, dù thích hợp hay không, đều có liên quan đến việc tăng tỷ lệ tử vong. Hơn nữa, chúng thường xuyên gây ra căng thẳng tâm lý đáng kể cho bệnh nhân. Việc xảy ra nhiều cú sốc điện là một trường hợp cấp cứu y tế và cần được đánh giá và nhập viện nhanh chóng để tiến hành công việc chẩn đoán cũng như quản lý và hỗ trợ bệnh nhân. Phác đồ xử trí bệnh nhân có nhiều cơn sốc (Bảng 6).
8.4 Sốc không thành công
Việc không phát hiện hoặc điều trị rối loạn nhịp thất một cách thích hợp có thể do chức năng ICD, lập trình ICD không thích hợp hoặc do bệnh lý nền của bệnh nhân. Trong trường hợp có một cú sốc không thành công, tất cả các kịch bản tiềm năng phải được xem xét. Tính toàn vẹn của hệ thống ICD cần được xác minh, bao gồm pin, dây dẫn và cuộn dây sốc (HV). SVT phải được loại trừ. Khi phân tích một cú sốc không thành công, cần hiểu bản chất xác suất của việc phá rung tim. Tuy nhiên, trong trường hợp có nhiều cú sốc tối đa năng lượng không thành công, nên đánh giá lại chất nền (ví dụ như thiếu máu cục bộ/sẹo, suy tim tiến triển) và nên xem xét những thay đổi trong điều trị bằng thuốc như thêm amiodaron hoặc thuốc chẹn kênh natri. Sau một thời gian thải trừ thích hợp, ngưỡng sốc (DFT) phải được đánh giá (lại) trong phòng điện sinh lý.
Trong trường hợp DFT cao liên tục, các tùy chọn bao gồm thay đổi dạng sóng sốc (ví dụ: cực tính, độ rộng dạng sóng hoặc độ nghiêng) và thử nghiệm các vectơ sốc khác (thêm hoặc loại bỏ cuộn dây sốc ở tĩnh mạch chủ trên hoặc “vỏ máy”). DFT dưới mức tối ưu có thể xảy ra trong cài đặt của một vỏ máy bị di chuyển xuống, do đó làm thay đổi vectơ sốc. Các tùy chọn bổ sung bao gồm đặt lại dây dẫn, thay đổi sang máy phát công suất cao, thêm cuộn dây sốc (ví dụ: tĩnh mạch chủ trên, xoang vành, tĩnh mạch vô danh, điện cực dưới da dạng mảng) hoặc sử dụng thuốc (ví dụ: dofetilide, sotalol) để giúp giảm DFT.
8.5 Không phát hiện hoặc điều trị cơn tim nhanh thất (VT) bền bỉ
Hệ thống ICD không phát hiện được cơn VT thường do nguyên nhân cơn VT có tần số cơn chậm hơn ngưỡng phát hiện nhanh thất . Điều này có thể xảy ra ở những bệnh nhân có tần số phát hiện VT được lập trình cao hoặc phổ biến hơn do tần số VT bị chậm lại sau khi điều trị bằng thuốc chống loạn nhịp. Các vấn đề về nhận cảm của điện cực có thể ảnh hưởng đến việc phát hiện VT/ VF. Nhận cảm dưới mức có thể xảy ra khi có sóng VF nhỏ. Ít phổ biến hơn, các thuật toán phân biệt có thể dẫn đến không phát hiện được VT. Khi các thuật toán phân biệt SVT được lập trình “bật”, các tiêu chí khác ngoài tần số tim phải được đáp ứng để kích hoạt các liệu pháp điều trị trong vùng VT. Các yếu tố phân biệt phổ biến, bao gồm sự khởi phát đột ngột (Onset) và độ ổn định (Stability), có thể ngăn chặn điều trị sai, với cơn VT tăng tốc dần tới tần số phát hiện VT, hoặc khi tần số VT không đều. Chúng ta cần lập trình lại tần số phát hiện VT, tăng độ nhạy, có thể phải đặt lại điện cực, tắt chương trình phân biệt SVT nếu cần thiết.
Một số trường hợp máy ICD không điều trị được cơn rung thất và nhanh thất, thường do nguyên nhân thay đổi chất nền cơ tim (bệnh tim thiếu máu cục bộ, suy tim), ngưỡng sốc cao hoặc quá tải điện, trong những trường hợp này chúng ta cần điều trị nguyên nhân, đặt lại điện cực dây sốc, thay máy ICD.
Bảng 6. Nguyên nhân và xử lý các sự cố của máy phá rung
| Cơn VT/VF (nhanh thất/rung thất) liên tục hoặc lặp lại | Sử dụng nam châm hoặc lập trình tắt chức năng điều trị của ICD Điều trị nội khoa cho VT (thuốc chẹn beta tiêm tĩnh mạch, amiodarone) Thay thế điện giải (K+, Mg2+) Điều trị chứng thiếu máu cục bộ hoặc các yếu tố khác như suy tim Bơm bóng vào động mạch chủ hoặc hỗ trợ huyết động để hạ huyết áp Đặt nội khí quản và an thần cho bệnh nhân Chẹn giao cảm bằng phong tỏa hạch hình sao ở những bệnh nhân được chọn Triệt đốt bằng catheter |
| Nhịp nhanh trên thất (SVT) | Sử dụng nam châm hoặc lập trình tắt chức năng điều trị của ICD Điều trị nội khoa cho SVT (thuốc chẹn beta tiêm tĩnh mạch, thuốc chẹn kênh Canxi) Lập trình tần số phát hiện và/ hoặc tần số phân biệt SVT cao hơn nếu có thể Triệt đốt bằng catheter |
| Hỏng điện cực | Tắt chức năng phát hiện loạn nhip và chuẩn bị thay điện cực |
| Kết nối lỏng giữa máy | Kết nối lại máy và điện cực và điện cực |
| Nhận cảm quá mức sóng T | Lập trình lại nếu có thể Đặt lại điện cực Ưu tiên tạo nhịp nếu nhận cảm quá mức sóng T không xuất hiện khi tạo nhịp và bệnh nhân không thích hợp để thay điện cực |
| Nhiễu điện cơ hoành | Thay đổi độ nhạy nhận cảm và kiểm tra lại chức năng nhận cảm khi bệnh nhân có VF Đặt lại điện cực |
| Nhận cảm quá mức sóng P | Có thể khó lập trình vì thường dây dẫn ở gần vòng van ba lá hoặc do sự tuột điện cực Đặt lại điện cực |
| Nhận cảm quá mức sóng R | Thay đổi độ nhạy nhận cảm và kiểm tra lại chức năng nhận cảm khi bệnh nhân có VF Điều chỉnh thời kỳ trống nếu có thể Đặt lại điện cực |
| Nhiễu điện từ trường (EMI) | Phát hiện nguồn EMI Tránh tiếp xúc nguồn EMI |
8.6 Rối loạn nhịp do thiết bị
Lập trình tạo nhịp vượt tần số cho ICD là phương pháp điều trị hiệu quả để giảm tần suất các cú sốc ICD. Tuy nhiên, trong một số trường hợp, tạo nhịp vượt tần số có thể gây ra cơn nhanh thất, rung thất nếu được thực hiện không thích hợp. Các cú sốc điện đối với VT hoặc SVT, đặc biệt là các cú sốc năng lượng thấp, có thể gây ra VF. Khi nhiều sự kiện liên tiếp được ghi lại, việc phân tích cơn đầu tiên rất quan trọng, ngoài việc phân tích cơn ATP và các cú sốc tiếp theo. Rất hiếm khi, tạo nhịp chống nhịp chậm có thể gây ra rối loạn nhịp thất.
8.7 Máy ICD dưới da
Máy ICD dưới da (S ‐ ICD) sử dụng các điện cực có khoảng cách lớn có chức năng nhận cảm gần giống với máy phá rung tim ngoài hơn là hệ thống điện cực trong tĩnh mạch. Vì S ‐ ICD không có chức năng tạo nhịp, thiết bị không bắt buộc phải nhận cảm và phân loại từng EGM. Thay vào đó, thiết bị sử dụng một thuật toán cảm biến bao gồm giai đoạn phát hiện, giai đoạn xác nhận và giai đoạn quyết định. Trong nghiên cứu quan trọng của Hoa Kỳ, 99,8% các cơn VT/VF được phát hiện thích hợp. Nhận cảm quá mức có thể xảy ra, đặc biệt khi sóng T và sóng R có biên độ tương tự, và quy trình sàng lọc để đánh giá khả năng này là bắt buộc trước khi cấy. Nếu việc nhận cảm quá mức sóng T xảy ra sau khi cấy, các nguyên nhân như có khí dưới da xung quanh điện cực, sự thay đổi chuyển hóa như tăng Kali máu, hoặc sự di lệch của điện cực hoặc máy phải được nghiên cứu. Việc lập trình lại sử dụng một vectơ thay thế có sóng R lớn hơn hoặc tỷ lệ sóng R trên sóng T lớn hơn có thể loại bỏ được vấn đề.
9 Kết quả cấy ICD theo các nghiên cứu
Rất nhiều nghiên cứu đã chứng minh hiệu quả của máy phá rung tự động so với điều trị thuốc ở bệnh nhân bị bệnh cơ tim do thiếu máu hoặc không do thiếu máu và các bệnh lý hiếm gặp khác. Dẫn đến việc sử dụng máy phá rung để phòng đột tử cả tiên phát và thứ phát trở nên thường quy. Bảng 7 tổng hợp các nghiên cứu điển hình trong cấy máy phá rung tự động.
Bảng 7. Tổng hợp các nghiên cứu điển hình trong cấy máy phá rung tự động
| Năm | Nghiên cứu | Dự phòng | Bệnh nhân | Chỉ định | Kết quả |
| 1996 | MADIT | Tiên phát | 196 | Bệnh cơ tim do thiếu máu, LVEF≤35, NYHA I-III, NSVT hoặc VT do EPS | Giảm 54% nguy cơ đột tử với ICD |
| 1997 | AVID | Thứ phát | 1013 | VT có triệu chứng, ngừng tim cứu sống, LVEF ≤ 40% | Giảm 31% nguy cơ tử vong với ICD trong 3 năm |
| 1999 | MUSTT | Tiên phát | 704 | Bệnh cơ tim do thiếu máu, LVEF < 40, NSVT không triệu chứng | Giảm 51% nguy cơ tử vong với ICD |
| 2000 | CASH | Thứ phát | 288 | Ngừng tim cứu sống, nhanh thất ảnh hưởng huyết động | Giảm 23% nguy cơ tử vong với ICD |
| 2002 | MADIT-II | Tiên phát | 1232 | Bệnh cơ tim do thiếu máu, LVEF < 30, lớn hơn 30 ngày sau NMCT | Giảm 31% nguy cơ tử vong với ICD |
| 2004 | DEFINITE | Tiên phát | 458 | Bệnh cơ tim không do thiếu máu, LVEF ≤ 35% NSVT hoặc PVC | ICD giảm tỷ lệ chết do mọi nguyên nhân (7,9% với 14% ở năm thứ 2) |
| 2004 | DINAMIT | Tiên phát | 674 | Bệnh cơ tim do thiếu máu, NMCT từ 4-40 ngày; LVEF ≤ 35% | Không làm giảm tỷ lệ tử vong do mọi nguyên nhân với p=0,66 nhưng làm giảm rối loạn nhịp gây tử vong với p= 0,009 |
| 2004 | COMPANION | Tiên phát | 1520 | Bệnh cơ tim do thiếu máu hoặc không thiếu máu, NYHA III-IV, LVEF≤ 35, QRS> 120 ms | Giảm khoảng 20% nguy cơ tái nhập viện do suy tim hoặc đột tử so với cấy CRT |
| 2005 | SCD-HeFT | Tiên phát | 2521 | Bệnh cơ tim do thiếu máu hoặc không thiếu máu, NYHA II-III, LVEF < 35 | Giảm 23% nguy cơ tử vong với ICD |
| 2016 | DANISH | Tiên phát | 1116 | Bệnh cơ tim không do thiếu máu, LVEF ≤ 35%; NYHA II-III (IV nếu CRT-D); điều trị nội khoa tối ưu | Không giảm tử vong với ICD |
10 Tài liệu tham khảo
- Joseph Marine, Charles J. Love, and Jeffrey A. Brinker. Techniques of pacemaker and ICD implantation and removal. Cardiac Pacing and ICDs. Willey Blạckwell 2020, 131-206.
- Michael Field and Michael R. Gold .The implantable cardioverter–defibrillator. Cardiac Pacing and ICDs. Willey Blạckwell 2020, 315-356.
- Yong-Mei Cha and Ammar M. Killu .Cardiac resynchronization therapy, Cardiac Pacing and ICDs. Willey Blạckwell 2020, 357 -394.
- Kevin Jackson . ICD follow-up and troubleshooting, Cardiac Pacing and ICDs. Willey Blạckwell 2020, 395-416.
- Anantha Narayanan M, Vakil K, Reddy YN, et al. Efficacy of implantable cardioverter‐defibrillator therapy in patients with nonischemic cardiomyopathy: a systematic review and meta‐analysis of randomized controlled trials. JACC Clin Electrophysiol 2017;3(9):962–970.
- Sroubek J, Buxton AE. Primary prevention implantable cardiac defibrillator trials: what have we learned? Card Electrophysiol Clin 2017;9(4):761–773.
- Birnie DH, Sauer WH, Bogun F, et al. HRS expert con sensus statement on the diagnosis and management of arrhythmias associated with cardiac sarcoidosis. Heart Rhythm 2014;11(7):1305–1323.
- PrioriSG,WildeAA,HorieM,etal.HRS/EHRA/APHRS expert consensus statement on the diagnosis and man agement of patients with inherited primary arrhythmia syndromes: document endorsed by HRS, EHRA, and APHRS in May 2013 and by ACCF, AHA, PACES, and AEPC in June 2013. Heart Rhythm 2013;10(12): 1932–1963.
- Koneru JN, Jones PW, Hammill EF, Wold N, Ellenbogen KA. Risk factors and temporal trends of complications associated with transvenous implantable cardiac defibril lator leads. J Am Heart Assoc 2018;7(10):e007691.
- Wilkoff BL, Fauchier L, Stiles MK, et al., editors. 2015 HRS/EHRA/APHRS/SOLAECE expert consensus state ment on optimal implantable cardioverter‐defibrillator programming and testing. Heart Rhythm 2016;13(2): e50–e86.

