Cập nhật Chẩn đoán và Điều trị thuốc trong COPD

TS. BS. NGUYỄN VĂN THÀNH
PCT Hội Phổi VN, PCT Hội Hô hấp VN
Xem và tải PDF tại đây
1 1. CHẨN ĐOÁN VÀ ĐÁNH GIÁ
1.1 1.1. Định nghĩa và phân loại
Hút thuốc lá, thu hẹp đường thở, khí phế thũng và hạn chế luồng khí có phải là một lộ trình bệnh lý cố định, nhất quán trong COPD? Câu trả lời là không. Phân tích trên những người hút thuốc lá đã chứng minh điều này. Một phân tích nhóm trong nghiên cứu đoàn hệ lớn COPDGene (Genetic Epidemiology of COPDGene) đã cho thấy có khí phế thũng ở 44% người tham gia được xem là GOLD 0 (không bất thường về chức năng hô hấp theo định nghĩa COPD). Theo dõi 5 năm từ những người ban đầu biểu hiện khí phế thũng rõ ràng bằng mắt thường có những thay đổi lớn hơn đáng kể ở nhiều thông số đặc trưng của COPD, bao gồm cả tỷ lệ FEV1/FVC. Tuy nhiên, những cá nhân này hiện nay không được xem là COPD vì dựa trên các tiêu chuẩn đo chức năng hô hấp.
Bên cạnh việc phát hiện khí phế thũng bằng chụp X-quang, giảm khả năng khuếch tán carbon monoxide (DLCO) cũng cho thấy đây là một yếu tố nguy cơ tử vong không phụ thuộc vào mức độ hạn chế luồng khí. Những phát hiện này là bằng chứng mạnh mẽ để xem những người bị khí phế thũng, bất kể kết quả đo chức năng hô hấp như thế nào, là người bị COPD. Ngoài ra, có một tỷ lệ những người hút thuốc lá trong suốt cuộc đời (10-20 gói/năm hoặc hơn), nhưng không có tắc nghẽn luồng khí vẫn có các triệu chứng hô hấp đặc trưng của COPD, trong đó bao gồm cả các đợt cấp cần được điều trị bằng thuốc giãn phế quản.
Một nhóm người khác hiện đang bị loại khỏi định nghĩa về COPD đáng được xem xét: những người có tỷ lệ FEV1/FVC bảo tồn nhưng suy giảm chức năng hô hấp (preserved ratio impaired spirometry, PRISm) còn được gọi là chức năng hô hấp hạn chế (restrictive spirometry). Nhóm này thường được định nghĩa là FEV1/FVC >0,7 và FEV1% dự đoán <80%, mặc dù đã sử dụng giới hạn thấp của tiêu chuẩn bình thường (lower limit of normal, LLN). Điều này cho thấy các ngưỡng cắt cứng nhắc dựa trên các giá trị đo chức năng hô hấp có thể phân loại sai. Thí dụ, một số cá nhân có giá trị FVC cao không cân xứng so với FEV1 của họ (cũng vẫn trong phạm vi bình thường) sẽ được chẩn đoán theo tiêu chuẩn GOLD là mắc COPD nhẹ thay vì là một dạng bình thường. Vấn đề này liên quan chặt chẽ đến độ tuổi. So với định nghĩa tỷ lệ cố định, ngưỡng dựa trên giới hạn thấp của giá trị bình thường đối với FEV1/FVC chẩn đoán COPD ít gặp hơn ở người cao tuổi và thường gặp hơn ở những người khoảng 45 tuổi. PRISm là phổ biến trong phân nhóm của nghiên cứu COPDGene (12,3%). Nhiều người trong nhóm này ban đầu có vẻ có biểu hiện lâm sàng tương tự như COPD, và sau đó nhiều người trong số họ chuyển sang COPD thực sự theo thời gian, thường ở giai đoạn GOLD 2 hoặc nặng hơn. Tỷ lệ sống sót ở những người PRISm thấp hơn so với những người mắc GOLD 0, tức là những người hút thuốc không bị tắc nghẽn luồng khí. Trong một nghiên cứu khác sau đó cho thấy thấy tỷ lệ sống sót của người trong nhóm PRISm tương tự so với những bệnh nhân mắc COPD trung bình và xấu hơn so với những người mắc GOLD nhẹ.
Hiện nay chúng ta thừa nhận rằng chẩn đoán COPD bằng phương pháp đo chức năng hô hấp hiện tại có độ đặc hiệu đáng kể nhưng độ nhạy thấp, điều này đã dẫn đến đề xuất công nhận một nhóm rộng hơn những cá nhân có phơi nhiễm nguy cơ, có triệu chứng hô hấp là tiền COPD (pre- COPD). Do đó, định nghĩa hiện tại về COPD ngày càng được công nhận là không đầy đủ. Thế tiến thoái lưỡng nan là làm thế nào để thay thế nó. Phân tích nhóm trong nghiên cứu COPDGene đã cố gắng nắm bắt tính không đồng nhất của COPD bằng cách sử dụng phương pháp đo chức năng hô hấp, kết hợp hình ảnh CT, các triệu chứng và yếu tố phơi nhiễm. Dựa trên các mô hình hồi quy kết quả thực tế, các tác giả đề xuất một danh mục chẩn đoán COPD, bao gồm: Không COPD, Có thể (xác suất xảy ra thấp), Có khả năng (xác suất xảy ra cao) và Xác định COPD. Do đó, một định nghĩa lại toàn diện dường như khó có thể có trong tình trạng hiểu biết hiện nay của chúng ta về bệnh lý COPD. Một quan điểm thay thế là ngừng coi COPD là một bệnh đơn nhất và thay vào đó chấp nhận nó như một hội chứng lâm sàng có thể sẽ hợp lý hơn nếu nhìn từ góc độ tiếp cận điều trị sớm.
COPD là một bệnh mạn tính, tiến triển của đường thở và phổi, đặc trưng bởi tình trạng tắc nghẽn luồng khí không thể hồi phục hoàn toàn khi dùng thuốc giãn phế quản. Có hai kiểu hình chính: Kiểu đường thở, là kiểu chiếm ưu thế và được đặc trưng bởi viêm phế quản mạn tính với biểu hiện ho, khạc đờm nổi trội. Kiểu khí phế thũng ưu thế với biểu hiện chủ yếu là giảm khả năng gắng sức.
COPD cũng được xem xét phân loại theo nguyên nhân như theo kiểu gen (Genetic COPD, COPD-G), theo kiểu khuyết tật phát triển phổi (COPD due to abnormal lung development, COPD-D), theo kiểu tác động từ ô nhiễm môi trường (Environmental COPD, do thuốc lá - COPD-C, do bụi khói- COPD-P), theo kiểu nhiễm trùng (COPD due to infections , COPD-I), theo kiểu do hen (COPD and asthma, COPD-A), và theo kiểu không xác định được căn nguyên (COPD of unknown cause, COPD-U).
Trong quá trình diễn biến, COPD có những đợt cấp, trong đó các triệu chứng tăng nặng làm mất đi trạng thái ổn định của người bệnh. Đợt cấp làm cho diễn biến COPD xấu đi nhanh hơn và tiên lượng xấu hơn và thường là một dạng kiểu hình. Cách tiếp cận điều trị COPD nhiều đợt cấp cũng khác và do vậy phân loại COPD cũng bao gồm cả ít đợt cấp và nhiều đợt cấp.
Sau khi chẩn đoán COPD, bệnh nhân nên được xác định mức độ tắc nghẽn luồng khí (từ nhẹ đến rất nặng) bằng cách sử dụng FEV1 sau khi dùng thuốc giãn phế quản. Các tài liệu hướng dẫn Vietnam Fanpage of Respirology thường khuyến cáo sử dụng các thang điểm để đánh giá mức độ triệu chứng (thí dụ thang điểm CAT, mMRC). Tuy nhiên, trong thực tế, thực hành có thể linh hoạt đánh giá mức độ ít hay nhiều triệu chứng, mức độ khó thở bằng nhưng câu đơn giản và thực tế phù hợp bối cảnh cụ thể hơn.
Số lượng đợt cấp trong khoảng thời gian 12 tháng trước cần được xác định để phân loại bệnh nhân thuộc nhóm ít hay nhiều đợt cấp. Khi có điều kiện, bệnh nhân nên được xét nghiệm công thức máu để xác định tỷ lệ bạch cầu ái toan. Tăng bạch cầu ái toan máu là dấu hiệu sinh học cho thấy bệnh nhân có khả năng đáp ứng với điều trị kháng viêm corticosteroids dạng hít (ICS).
1.2 1.2. Chẩn đoán
Trong lâm sàng, nên nghi ngờ COPD ở bất kỳ bệnh nhân nào than phiền khó thở, ho mạn tính hoặc khạc đờm và/hoặc có tiền sử tiếp xúc với các yếu tố nguy cơ mắc bệnh. Tuy nhiên, cần phải thực hiện đo chức năng hô hấp gắng sức để chứng minh FEV1/FVC sau khi dùng thuốc giãn phế quản <0,7. Đo chức năng hô hấp gắng sức là phép đo xác định tắc nghẽn luồng khí khách quan nhất.
Những bệnh nhân đang điều trị bằng thuốc giãn phế quản không cần phải ngừng thuốc để đo chức năng hô hấp. Cần nhớ là chụp X-quang ngực không thể chẩn đoán được COPD. Tuy nhiên, chụp X-quang ngực có thể hữu ích trong việc loại trừ các chẩn đoán khác và phát hiện những thay đổi liên quan đến COPD như tình trạng tăng sáng, biến dạng lồng ngực. CT ngực cũng không phải là điều kiện tiên quyết để chẩn đoán COPD. Tuy nhiên, nó được sử dụng như một công cụ để phát hiện u phổi, bệnh phổi đồng mắc và sàng lọc ung thư phổi ở những bệnh nhân mắc COPD. CT ngực cũng có thể cung cấp thông tin có liên quan lâm sàng tiềm ẩn bao gồm sự hiện diện, mức độ nghiêm trọng và phân bố của khí phế thũng cũng như các bệnh đi kèm tiềm ẩn hoặc bất thường về đường thở.
Do đó, tài liệu GOLD khuyến cáo sử dụng CT ngực ở những bệnh nhân được xác nhận mắc COPD có các đợt cấp dai dẳng, tắc nghẽn luồng khí đáng kể, các triệu chứng không phù hợp với mức độ nặng của bệnh hoặc các đặc điểm đáp ứng các tiêu chí sàng lọc ung thư phổi. CT ngực có tầm quan trọng bổ sung trong việc ra quyết định liên quan đến phẫu thuật giảm thể tích phổi hoặc đặt van nội phế quản điều trị trong COPD.
Phân tích khí máu có thể được sử dụng để chẩn đoán suy hô hấp. Khả năng khuếch tán carbon monoxide (DLCO) hít vào có thể cung cấp thông tin có giá trị về mức độ nặng của khí phế thũng. Tài liệu GOLD hiện tại đề xuất thuật ngữ “tiền COPD” cho những bệnh nhân có các triệu chứng về hô hấp và những thay đổi về cấu trúc đã có từ trước, thí dụ họ có thể có những thay đổi về khí phế thũng nhưng vẫn bảo tồn chức năng hô hấp. Vì lý do này, bệnh nhân có các triệu chứng điển hình của COPD và nguy cơ phơi nhiễm nhưng không được chẩn đoán COPD vì lý do không thỏa mãn tiêu chuẩn đo chức năng hô hấp nên được giới thiệu để tham vấn một lần với bác sĩ chuyên khoa phổi, với khả năng xét nghiệm chẩn đoán chức năng phổi mở rộng hơn.
Ngoài tiền sử phơi nhiễm, hút thuốc lá, bệnh nhân nên được hỏi về các triệu chứng hô hấp bao gồm cả các đợt cấp và khám lâm sàng (các dấu hiệu gợi ý như thì thở ra kéo dài, ngực hình thùng hoặc khi thở ra có tiếng khò khè). Về phân tích chức năng phổi, chẩn đoán dựa trên tình trạng tắc nghẽn đường thở không hồi phục với giá trị FEV1/FVC sau khi dùng thuốc giãn phế quản thấp hơn giới hạn dưới của mức bình thường hoặc FEV1/FVC < 0,7.
1.3 1.3. Các bệnh đi kèm ở phổi
Các bệnh phổi đi kèm làm giảm chất lượng cuộc sống kém hơn, tăng nguy cơ nhập viện nhiều lần và tỷ lệ tử vong cao hơn. Trung bình, hơn 90% bệnh nhân mắc COPD có ít nhất một bệnh đi kèm và gần 50% có nhiều hơn ba bệnh. Bệnh đi kèm có thể được chia thành bệnh phổi và bệnh ngoài phổi. Phương pháp điều trị cơ bản cho bệnh đi kèm nên được thực hiện tốt bởi các hướng dẫn lâm sàng từ các hiệp hội chuyên khoa tương ứng. Bệnh đi kèm phổi chính là hen phế quản và giãn phế quản.
Hen phế quản là bệnh đi kèm phổi phổ biến nhất. Tỷ lệ mắc hội chứng chồng lấp hen - COPD (ACO) ước tính là 27% trong các nghiên cứu quan sát nhưng khái niệm ACO không được chấp nhận rộng rãi. Các đặc điểm hen kết hợp bao gồm chẩn đoán lâm sàng hen, xu hướng dị ứng, tắc nghẽn đường thở thay đổi và tăng bạch cầu ái toan ngoại biên (>300 tế bào/mm3). Nhóm bệnh nhân này nên được điều trị sớm bằng corticosteroids dạng hít (ICS), đặc biệt nếu xảy ra đợt cấp. Giãn phế quản kết hợp COPD với tỷ lệ chưa xác định, dao động 4% đến 72%. Giãn phế quản có ý nghĩa lâm sàng liên quan đến ho có đờm, nhiễm trùng phế quản và giãn bất thường về mặt hình thái phế quản được xác nhận bằng chụp CT. Ở những bệnh nhân bị COPD, giãn phế quản có liên quan đến giảm chỉ số khối cơ thể và tuổi cao hơn, tăng tạo đờm và đợt cấp. Những bệnh nhân này cũng cho thấy tình trạng quần cư (colonization) hoặc nhiễm trùng giới hạn với P. aeruginosa, tăng các dấu hiệu viêm tại chỗ và toàn thân, tăng tỷ lệ tử vong (HR=2,54). Việc xác định tình trạng giãn phế quản có ý nghĩa lâm sàng (trái ngược với những thay đổi giãn phế quản chỉ rõ ràng trên CT khi không có các dấu hiệu lâm sàng tương ứng) là rất quan trọng. Đối với tình trạng giãn phế quản cần điều trị, các xét nghiệm chẩn đoán tiếp theo bao gồm nghiên cứu vi sinh đờm để tìm vi khuẩn lao điển hình và không điển hình, loại trừ thiếu hụt α1-antitrypsin và Xét nghiệm miễn dịch học để loại trừ nhiễm trùng lao. Không vì có chẩn đoán giãn phế quản mà ngưng ICS nếu chỉ định ICS đã được xác lập cho điều trị hen hoặc COPD
1.4 1.4. Tầm soát COPD
Không khuyến cáo sàng lọc bằng đo chức năng hô hấp để chẩn đoán COPD ở những người không có triệu chứng, không tiếp xúc đáng kể với thuốc lá hoặc không có các yếu tố nguy cơ khác. Tuy nhiên, nên cân nhắc việc phát hiện ca bệnh chủ động bằng cách đo chức năng hô hấp ở những người có các triệu chứng giống COPD hoặc các yếu tố nguy cơ như hút thuốc lá hơn 20 gói-năm, nhiễm trùng hô hấp dưới tái phát và/hoặc các sự kiện đầu đời (bao gồm cả việc mẹ hút thuốc trong thời kỳ mang thai, sinh non, trẻ nhẹ cân và/hoặc tiếp xúc với khói thuốc lá thụ động trong thời kỳ trẻ sơ sinh). Các nhà nghiên cứu đã phát hiện ra rằng việc kết hợp các bảng câu hỏi với các phép đo chức năng hô hấp đơn giản có thể xác định COPD, một căn bệnh trước đây thường bị chẩn đoán thiếu, bao gồm cả một tỷ lệ đáng kể bệnh nhân mắc bệnh nhẹ. Khuyến cáo của GOLD là những bệnh nhân chụp cắt lớp vi tính (CT) liều thấp để sàng lọc ung thư phổi nên được đánh giá COPD thông qua đánh giá triệu chứng và đo chức năng hô hấp, vì hai tình trạng này có nhiều yếu tố nguy cơ chung. Hơn nữa, khi những bệnh nhân có các yếu tố nguy cơ COPD khác ngoài hút thuốc, chẳng hạn như những bệnh nhân có các yếu tố nguy cơ phát triển hoặc di truyền hoặc tiếp xúc với môi trường, chụp phổi để kiểm tra các triệu chứng hô hấp, thì bất kỳ phát hiện bất thường nào có thể chỉ ra COPD đều phải được đánh giá các triệu chứng và cân nhắc đo chức năng hô hấp.
2 2. ĐIỀU TRỊ THUỐC
2.1 2.1. Tác động của thuốc điều trị lên bệnh lý COPD
Cần nhấn mạnh rằng, trái ngược với bệnh hen, điều trị bằng corticosteroids ở COPD ổn định không hiệu quả trong việc giảm viêm đường thở và suy giảm chức năng phổi. Tuy nhiên, corticosteroids dạng hít (ICS) như Budesonide và Fluticasone, dùng riêng lẻ hoặc kết hợp với LABA, có liên quan đến việc tăng nguy cơ mắc các biến cố viêm phổi. Điều này cho thấy ICS có thể làm thay đổi phản ứng miễn dịch ở phổi COPD, làm tăng khả năng mắc các bệnh nhiễm trùng do vi khuẩn. Có rất ít dữ liệu nghiên cứu về những thay đổi trong bệnh lý miễn dịch sau khi điều trị bằng corticosteroids dạng hít bằng sinh thiết phế quản và/hoặc rửa phế quản phế nang (BAL) ở bệnh nhân COPD ổn định. Một tổng quan hệ thống gần đây cho thấy ICS có hiệu quả trong việc giảm số lượng tế bào CD4 và CD8 trong sinh thiết phế quản và làm giảm số lượng bạch cầu trung tính và tế bào lympho nhưng làm tăng số lượng đại thực bào trong dịch rửa phế quản - phế nang (BAL). Một số nghiên cứu cũng quan sát thấy sự giảm đáng kể các chất trung gian gây viêm trong dịch BAL như CXCL8 và PGE2, 6kPGF1α và PGF2α. Dữ liệu thu được từ phân tích đờm phù hợp với một số ít quan sát được báo cáo đối với sinh thiết phế quản và trong dịch BAL. Salmeterol/fluticasone propionate sử dụng trong ba tháng làm giảm tế bào CD8+ và CD68+ trong sinh thiết phế quản của bệnh nhân COPD trung bình/nặng so với nhóm dùng giả dược trong khi điều trị trong 6 đến 30 tháng có hoặc không có thuốc giãn phế quản bổ sung cho thấy số lượng tế bào CD3+, CD4+ và tế bào mast giảm ở bệnh nhân COPD trung bình/nặng so với nhóm dùng giả dược. Mặc dù các cuộc tìm kiếm thuốc điều trị mới nhắm vào các cơ chế khác nhau nhưng hầu hết các thuốc ứng viên đều không đạt đến giai đoạn thử nghiệm lâm sàng. Do đó, việc quản lý COPD vẫn phụ thuộc vào việc sử dụng thuốc giãn phế quản và corticosteroids.
Hạn chế luồng khí xảy ra do mất độ đàn hồi và tăng sức cản đường thở. Mặc dù hạn chế luồng khí là đặc điểm đặc trưng của COPD, triệu chứng chính là khó thở, liên quan đến tăng công hô hấp để đối phó với gia tăng sức cản đường thởi. Tiến triển của bệnh và tình trạng phổi tăng căng phồng phổi động làm tăng dần thể tích còn lại sau khi thở ra, làm cản trở quá trình hít vào. Thuốc giãn phế quản làm giảm khó thở bằng cách giảm công cản trở và sức cản đường thở. Đo chức năng hô hấp cung cấp đánh giá toàn diện hơn về hạn chế luồng khí, trong khi chụp cắt lớp vi tính cho phép hình dung vị trí giải phẫu của bệnh, cho phép mô tả đặc điểm hình thái và phân tích định lượng mức độ nghiêm trọng góp phần vào việc phân loại kiểu hình. Việc tập trung vào các đặc điểm cá nhân cụ thể đã thúc đẩy nghiên cứu về các phương pháp điều trị nhắm vào các cơ chế bệnh cơ bản. Không có phương pháp điều trị dược lý hiệu quả cụ thể nào cho bệnh khí phế thũng, ngoại trừ những phương pháp nhắm vào tình trạng thiếu hụt α1 antitrypsin.
Corticosteroids (một trong những phương pháp điều trị chính được sử dụng trong COPD), được sử dụng bằng đường uống hoặc hít, là thuốc chống viêm có hiệu quả cao đối với bệnh hen. Sự ức chế gen do corticosteroids gây ra làm giảm hoạt động của NF-kB. Tuy nhiên, điều trị bằng corticoid không cho thấy tác dụng chống viêm ở bệnh nhân COPD. Kháng corticosteroids chủ yếu là do bất hoạt HDAC2.
Chất chống oxy hóa và chất ức chế tổng hợp oxit nitric có thể phục hồi độ nhạy cảm với corticosteroids ở người bị COPD. Vì là thuốc điều hòa miễn dịch và ức chế miễn dịch, sử dụng corticosteroids điều trị kéo dài có thể làm tăng nguy cơ viêm phổi ở bệnh nhân mắc COPD nặng, tuổi cao, có các bệnh đi kèm, chẳng hạn như bệnh tim mạch, teo cơ xương, ung thư phổi và loãng xương, hoặc có tiền sử viêm phổi mới được chẩn đoán. Tình trạng viêm đường thở mạn tính trong COPD theo truyền thống được đặc trưng bởi tình trạng viêm bạch cầu trung tính. Tuy nhiên, một nhóm bệnh nhân COPD có kiểu hình tăng bạch cầu ái toan (BCAT), xác định dựa trên số lượng bạch cầu ái toan trong máu ngoại vi hoặc trong đờm tăng. Ở bệnh nhân COPD, số lượng bạch cầu ái toan trong máu tăng có liên quan đến tăng nguy cơ mắc các đợt cấp và điều trị bằng corticosteroids dạng hít làm giảm nguy cơ này. Nhiều nghiên cứu xác định mối liên quan giữa tăng BCAT với hiệu quả điều trị bằng ICS và tăng BCAT đã được chứng minh là một dấu ấn sinh học chẩn đoán, dự đoán đáp ứng điều trị với corticosteroids dạng hít.
Thuốc giãn phế quản, như chất chủ vận beta2 tác dụng kéo dài (LABA) và chất đối kháng muscarinic tác dụng kéo dài (LAMA), có tác dụng cải thiện tình trạng thông khí, cải thiện khả năng gắng sức. Trong các đợt cấp COPD, LAMA tốt hơn LABA, ngay cả khi LABA kết hợp với corticosteroids dạng hít. Điều này giải thích cơ chế thực sự của tác dụng “giãn phế quản” của LAMA trong sinh bệnh học COPD là cải thiện tình trạng khí cạm và căng phồng phổi quá mức do tăng trương lực phó giao cảm hơn là làm giãn cơ trơn.
Ở bệnh nhân bị hen, tăng bạch cầu ái toan nặng, ba kháng thể đơn dòng nhắm vào trục IL-5/thụ thể IL-5 đã được chứng minh là làm giảm đáng kể tỷ lệ đợt cấp. Trong hai thử nghiệm lâm sàng ngẫu nhiên, mù đôi, có đối chứng giai đoạn III (METREX và METREO), tiêm dưới da hàng tháng mepolizumab có liên quan đến tỷ lệ đợt cấp thấp hơn so với giả dược ở những bệnh nhân COPD có kiểu hình tăng bạch cầu ái toan. Tuy nhiên, hiệu quả điều trị mepolizumab trong COPD thấp hơn so với hen. Một số cơ chế có thể là cơ sở cho tác dụng rất khiêm tốn của mepolizumab ở những bệnh nhân bị COPD tăng bạch cầu ái toan, trong đó vai trò của bạch cầu ái toan trong việc gây ra các đợt cấp ở COPD có thể ít nổi bật hơn so với bệnh hen và tình trạng viêm tăng bạch cầu ái toan có thể do các chất trung gian khác ngoài IL-5 thúc đẩy.
Điều trị COPD bằng thuốc chống viêm vẫn là một thách thức do tình trạng viêm phức tạp và các bệnh đi kèm liên quan. Thuốc giãn phế quản có thể làm giảm viêm, nhưng là hiệu quả ngắn hạn và không hiệu quả ở bệnh nhân COPD do các biến đổi đã trở thành mạn tính. Hiện tại, không có liệu pháp nào có hiệu quả đảo ngược bệnh lý COPD, thay vào đó, giảm thiểu sự tiến triển của COPD là một chiến lược duy nhất. Giảm stress oxy hóa và viêm có thể cải thiện chất lượng cuộc sống và tăng khả năng sống sót. Bổ sung, quản lý điều trị và/hoặc sử dụng nhiều chất chống oxy hóa có thể có lợi cho bệnh nhân COPD bằng cách tăng mức độ chống oxy hóa nội sinh.
Hiện nay, phương pháp tiếp cận chính là xử lý các triệu chứng hạn chế luồng khí do các triệu chứng nêu trên gây ra để cải thiện tình trạng khó thở thông qua thuốc, điều trị oxy và liệu pháp phục hồi chức năng. Tuy nhiên, hiện tại không có cách nào để ngăn ngừa sự tiến triển của bệnh. Một loạt các loại thuốc điều trị nhắm mục tiêu phân tử mới để ngăn chặn sự tiến triển của COPD đang được phát triển và vẫn còn trong giai đoạn thử nghiệm lâm sàng.
2.2 2.2. Vai trò của từng thuốc điều trị với COPD
2.2.1 2.2.1. Thuốc giãn phế quản
Là thuốc hiện đang được sử dụng như là trị liệu cơ bản để điều trị cho bệnh nhân COPD nhằm cải
thiện các triệu chứng của bệnh.
Các thụ thể beta2-adrenergic có trong các cơ trơn phế quản và được ghép nối với protein G
trong màng tế bào, khi được kích thích, chúng làm tăng hoạt động của adenyl cyclase, một loại
enzyme xúc tác quá trình chuyển đổi ATP thành Adenosine monophosphate vòng (cAMP). cAMP
ức chế giải phóng Canxi nội bào, làm giảm dòng canxi đi vào qua màng, làm giãn cơ trơn và làm
giãn đường thở. Các chất chủ vận thụ thể adrenergic có thể là thuốc giãn phế quản tác dụng ngắn
(SABA), chẳng hạn như albuterol, được sử dụng để làm giảm nhanh các triệu chứng cấp tính hoặc
thuốc giãn phế quản tác dụng kéo dài (LABA), chẳng hạn như Formoterol, indacaterol, salmeterol,
được sử dụng để làm giảm các triệu chứng phổ biến và dai dẳng nhất, chẳng hạn như ho và khó
thở.
Thuốc đối kháng muscarinic là thuốc tác dụng ngắn (SAMA), chẳng hạn như Ipratropium, hoặc
thuốc tác dụng dài (LAMA), chẳng hạn như Tiotropium, glycopyrrolate, umeclidinium và revefenacin.
Thuốc nhóm kháng muscarinic ngăn chặn hoạt động của các thụ thể acetylcholine muscarinic
(mAChRs). Các thụ thể muscarinic là các protein tham gia vào quá trình truyền tín hiệu qua một số
bộ phận nhất định của hệ thần kinh và thuốc đối kháng thụ thể muscarinic có tác dụng ngăn chặn
quá trình truyền tín hiệu này xảy ra. Đáng chú ý là thuốc đối kháng muscarinic làm giảm hoạt động
của hệ thần kinh phó giao cảm làm giảm trương lực phó giao cảm ở phổi. Có năm phân nhóm thụ
thể muscarinic, trong đó M1 và M3 là những mục tiêu chính của thuốc để tạo tác dụng cải thiện tình
trạng co thắt phế quản và giảm tiết chất nhầy, dẫn đến cải thiện chức năng phổi và khó thở.
2.2.2. Thuốc kháng viêm corticosteroids
Thuốc có thể ức chế sản xuất chất nhầy và làm giảm tắc nghẽn đường thở do ức chế biểu hiện
mRNA của protein mã hóa gen MUC5AC. Thuốc được sử dụng để điều trị COPD trong liệu pháp
kết hợp với thuốc giãn phế quản và cải thiện các triệu chứng ở những bệnh nhân có tiền sử nhiều
đợt cấp nặng. Việc kích hoạt các thụ thể beta2-adrenergic làm tăng cường tác dụng chống viêm của corticosteroids bằng cách tăng sự chuyển vị của thụ thể glucocorticosteroids từ tế bào chất vào
nhân. Việc kết hợp liệu pháp corticosteroids với thuốc giãn phế quản đã được chứng minh là có lợi
trong điều trị các triệu chứng và đợt cấp của bệnh nhân COPD.
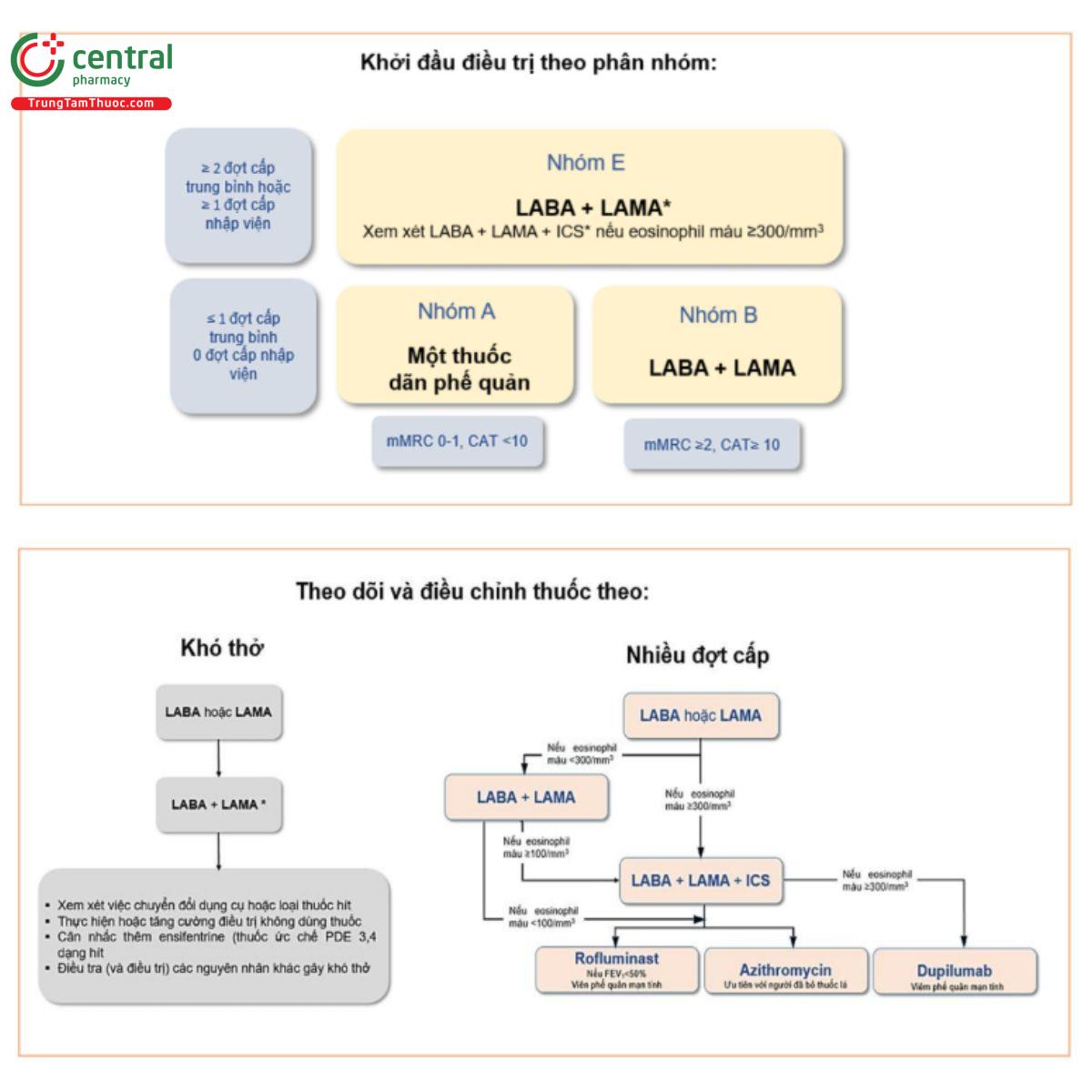
Tài liệu GOLD đề xuất một phương pháp tiếp cận phù hợp để bắt đầu điều trị dựa trên mức
độ triệu chứng và nguy cơ đợt cấp. Có thể tăng/giảm điều trị dựa trên sự hiện diện của các triệu
chứng chủ yếu (đặc điểm có thể điều trị) là khó thở và hạn chế vận động và tình trạng tiếp tục cơn
cấp trong khi đang điều trị duy trì. Cơ sở cho các khuyến cáo này một phần bắt nguồn từ bằng
chứng thu được từ các nghiên cứu lâm sàng ngẫu nhiên có đối chứng. Tuy nhiên, các khuyến cáo
này nhằm mục đích hỗ trợ bác sĩ lâm sàng đưa ra quyết định và cũng cần kết hợp với lời khuyên
của chuyên gia dựa trên kinh nghiệm lâm sàng (Hình 1). Trị liệu thuốc ban đầu nên dựa trên phân
nhóm nhóm GOLD (A, B, E) của bệnh nhân. Bệnh nhân nên được hướng dẫn và theo dõi về việc
tự quản lý tình trạng khó thở và stress. Các bệnh đi kèm nên được quản lý theo các hướng dẫn
đặc thù, bất kể có COPD hay không.
2.2.2 2.2.3. Chất chống oxy hóa (antioxidant)
Căng thẳng oxy hóa (oxidative stress) đóng vai trò quan trọng trong quá trình sinh bệnh của COPD.
Thông qua các nghiên cứu in vivo, chất chống oxy hóa đã được chứng minh là có tác dụng ức chế
khởi phát COPD. N-acetylcysteine (NAC) và các glutamine khác đã được thử nghiệm lâm sàng về
hiệu quả trên cơ chế này. Mặc dù có bằng chứng về vai trò có lợi của NAC trong COPD, hiệu quả
điều trị của nó trong việc quản lý lâm sàng COPD vẫn còn gây tranh cãi do Sinh khả dụng thuốc
dạng uống thấp và bản chất a-xít của nó không cho phép sử dụng ở dạng hít. Ngoài ra, việc thiếu
sự đảm bảo rằng sẽ có nồng độ Glutathione (hợp chất hữu cơ có vai trò chống các gốc oxy hóa tự
do quan trọng) trong phổi là một lý do chính khác khiến không đạt được hiệu quả điều trị mong
muốn. Tài liệu GOLD ghi nhận NAC, Carbocysteine có thể giảm đợt cấp trên bệnh nhân không đang
điều trị ICS. Tuy nhiên, chưa có bằng chứng cho phép chọn quần thể bệnh nhân nào có lợi khi sử
dụng thuốc này.
2.2.3 2.2.4. Macrolides
Kháng sinh nhóm macrolide chứa cấu trúc vòng lactone 14-16 thành phần, có nhiều chức năng. Nó
không chỉ có chức năng kháng sinh mà còn có tác dụng chống viêm, ức chế tiết chất nhầy và điều
hòa miễn dịch. Chức năng chống viêm và điều hòa miễn dịch chủ yếu là vòng lactone. Về mặt lâm
sàng, chúng được sử dụng để điều trị lâu dài các bệnh phổi viêm mạn tính như COPD. Cơ chế
chống viêm của kháng sinh nhóm macrolide rất phức tạp và chưa được làm sáng tỏ đầy đủ. Thuốc
có thể làm giảm tình trạng viêm của COPD bằng cách ức chế việc sản xuất các cytokine gây viêm.
Các mô hình thực nghiệm trên động vật cung cấp thêm bằng chứng cho thấy Clarithromycin có tác
dụng ức chế sự phát triển của khí phế thũng và liều dùng của thuốc này gần như tương đương với
liều dùng trên lâm sàng. Lợi ích tiềm năng của một loại kháng sinh mới, solithromycin đã được
nghiên cứu để điều trị COPD lâu dài nhưng chưa đủ dữ liệu nghiên cứu lâm sàng. Các loại
macrolide khác không có hoạt tính kháng khuẩn đang được phát triển như thuốc chống viêm và
các thử nghiệm lâm sàng dự kiến sẽ diễn ra trong tương lai. Cũng đã có một số nghiên cứu sử dụng macrolide (azithromycin, Erythromycin) liều thấp kéo dài làm giảm đợt cấp trên người COPD
có nhiều đợt cấp và đã ngưng thuốc lá. Tài liệu GOLD cũng khuyến cáo sử dụng Azithromycin nếu
đã tối đa trị liệu thuốc cơ bản vẫn còn nhiều đợt cấp và bạch cầu ái toan <100/mm3
2.2.4 2.2.5. Kháng PDE4
Chất ức chế PDE4 có tác dụng ức chế chọn lọc đối với PDE4 đặc hiệu biểu hiện trên các tế bào
biểu mô và cơ trơn đường thở bị viêm. Tác dụng sinh học chính là ức chế chọn lọc PDE4, dẫn đến
tăng nồng độ cAMP trong các tế bào viêm, điều chỉnh hoạt động của các tế bào viêm và điều chỉnh
giải phóng các yếu tố gây viêm từ đó có tác dụng chống viêm. Chúng đã được phát triển như thuốc
chống viêm mới cho COPD và hen từ những năm 1980. Chất ức chế PDE4 roflumilast đã được
Cục FDA Mỹ chấp thuận là phương pháp điều trị COPD. Roflumilast làm giảm khí phế thũng lan
tỏa do thuốc lá gây ra ở chuột so với nhóm đối chứng. Các nghiên cứu khác đã thấy rằng roflumilast
ức chế tình trạng xơ phổi do Bleomycin gây ra ở chuột và làm giảm tái tạo mạch máu phổi. Các thử
nghiệm lâm sàng đã chứng minh rằng roflumilast làm giảm các triệu chứng khó thở ở bệnh nhân
COPD và làm giảm tần suất các cơn cấp. Việc dùng roflumilast một lần mỗi ngày cải thiện đáng kể
giá trị FEV1 và làm giảm các đợt cấp, đặc biệt ở những bệnh nhân mắc bệnh nặng. Tuy nhiên thuốc
có các tác dụng phụ như buồn nôn, nôn và đau đầu. Sự phát triển của các chế phẩm mới đặc hiệu
cho phân nhóm PDE4B được mong đợi, và các chất hít để giảm tác dụng phụ toàn thân cũng đang
được phát triển. Tài liệu GOLD cũng khuyến cáo sử dụng roflumilast cho những trường hợp có
nhiều đợt cấp, FEV1 <50% và có kiểu hình viêm phế quản mạn tính mặc dù đã điều trị tối đa trị liệu
thuốc cơ bản.
2.2.5 2.2.6. Các thuốc điều trị khác và khả năng sử dụng thuốc sinh học
Sinh bệnh học trong COPD, theo quan niệm truyền thống, đặc trưng bởi tình trạng viêm bạch cầu
trung tính. Tuy nhiên, một nhóm bệnh nhân COPD có kiểu hình ái toan, dựa trên số lượng ái toan
trong máu ngoại vi tăng hoặc tỷ lệ phần trăm bạch cầu ái toan trong đờm tăng. Số lượng ái toan
trong máu tăng ở bệnh nhân COPD có liên quan đến nguy cơ tăng các đợt cấp và điều trị bằng
corticosteroids dạng hít làm giảm nguy cơ này. Sự hiện diện của tình trạng viêm đường thở tăng ái
toan (bằng chứng là tăng nồng độ ái toan trong máu) đã được chứng minh là một dấu ấn sinh học
chẩn đoán, dự đoán phản ứng điều trị với corticosteroids dạng hít.
Câu hỏi tiếp theo là liệu phương pháp tiếp cận y học chính xác sử dụng các chất sinh học cụ
thể nhắm mục tiêu vào tình trạng viêm ái toan có thành công ở bệnh nhân COPD như ở bệnh nhân
hen hay không? Thật vậy, ở những bệnh nhân bị hen nặng tăng bạch cầu ái toan, ba kháng thể
đơn dòng nhắm vào trục IL-5/ thụ thể IL-5 đã được chứng minh là làm giảm đáng kể tỷ lệ đợt cấp.
Mepolizumab và reslizumab ức chế phối tử IL-5, trong khi benralizumab liên kết với thụ thể IL-5
biểu hiện trên bạch cầu ái toan và bạch cầu ái kiềm, gây ra quá trình apoptosis và do đó làm cạn
kiệt các tế bào này. Tuy nhiên, trái với các kết quả thu được từ các thử nghiệm lâm sàng hen, các
thử nghiệm lâm sàng PHA III trên COPD sử dụng mepolizumab (ức chế IL-5) và benralizumab (ức
chế thụ thể IL-5) cho các kết quả rất hạn chế mặc dù đã thu tuyển những bệnh nhân nhiều đợt cấp
và tăng bạch cầu ái toan máu. Cho tới nay đã có dupilumab (dupixent) kháng IL-4/IL-13,
mepolizumab (nucala) kháng IL-5 được FDA (Mỹ) phê duyệt sử dụng trong COPD. Chỉ định các
thuốc trên để điều trị duy trì bổ sung cho người lớn bị COPD không kiểm soát được và có kiểu hình
tăng bạch cầu ái toan
2.3 2.3. Quan điểm điều trị thuốc cơ bản cập nhật
Theo tài liệu GOLD, điều trị thường quy bằng LABA + ICS không được khuyến cáo kể từ năm 2023
và vị trí của thuốc chủ vận beta2 tác dụng kéo dài (LABA) + thuốc đối kháng muscarinic tác dụng
kéo dài (LAMA) trong điều trị cũng đã được thay đổi theo chiều hướng tăng chỉ định sử dụng. Theo
GOLD (Hình 1), tất cả bệnh nhân trong nhóm A nên được chỉ định điều trị bằng thuốc giãn phế
quản tác dụng ngắn hoặc tác dụng kéo dài. Đối với bệnh nhân trong nhóm B, nên bắt đầu điều trị
bằng phối hợp LABA + LAMA. Nếu LABA + LAMA không được coi là phù hợp, việc lựa chọn giữa
LABA hoặc LAMA tùy thuộc vào mức độ giảm triệu chứng được cảm nhận ở từng bệnh nhân. Đối
với bệnh nhân trong nhóm E, LABA + LAMA được ưu tiên, tuy nhiên, nếu số lượng bạch cầu ái
toan của bệnh nhân ≥300 tế bào/mm3 thì việc sử dụng ICS cũng được chỉ định cho phác đồ cuối cùng là LABA + LAMA + ICS.
Đối với những bệnh nhân đang dùng liệu pháp đơn trị bằng LABA hoặc LAMA nhưng đang bị
đợt cấp, nên cân nhắc thay đổi phác đồ thành LABA + LAMA đối với những bệnh nhân có số lượng
bạch cầu ái toan trong máu <300 tế bào/mm3 và thành LABA + LAMA + ICS đối với những bệnh
nhân có số lượng bạch cầu ái toan từ 300 tế bào/mm3 trở lên. Đối với những bệnh nhân đang được
điều trị bằng LABA + LAMA nhưng đang bị đợt cấp, có thể thêm ICS vào phác đồ đối với những
bệnh nhân có số lượng bạch cầu ái toan trong máu từ 100 tế bào/mm3 trở lên hoặc có thể cân nhắc
thêm roflumilast hoặc azithromycin đối với những bệnh nhân có số lượng bạch cầu ái toan trong
máu <100 tế bào/mm3. Đối với những bệnh nhân đang được điều trị bằng LABA + LAMA + ICS
nhưng vẫn bị đợt cấp, nên cân nhắc bổ sung roflumilast, bổ sung macrolide và/hoặc (trong một số
trường hợp) ngừng ICS. Đối với những bệnh nhân bị khó thở khi đang dùng LABA hoặc LAMA,
nên cân nhắc tăng liều lên LABA + LAMA. Cũng có thể cân nhắc thay đổi dụng cụ phân phối hoặc
dạng thuốc hít, xem xét các biện pháp can thiệp không dùng thuốc và đánh giá các nguyên nhân
khác gây khó thở. Trong quá trình theo dõi, điều quan trọng là phải xem xét các triệu chứng, nguy
cơ đợt cấp, kỹ thuật hít và tuân thủ thuốc để hướng dẫn điều chỉnh phù hợp.
Với sự cải tiến để tạo điều kiện thuận lợi nhất, hiệu quả nhất trong việc sử dụng thuốc trên
bệnh nhân COPD, các dạng dụng cụ phân phối thuốc hít hiện nay đóng vai trò không nhỏ trong
hiệu quả đưa thuốc vào phổi và tuân thủ điều trị. Hầu hết các phương pháp điều trị COPD đều là
thuốc hít. Hiện nay (theo GOLD 2024) có 33 liệu pháp hít khác nhau chứa thuốc giãn phế quản tác
dụng ngắn hoặc tác dụng dài và ICS, dùng đơn độc hoặc kết hợp. Hơn nữa, có ít nhất 22 loại thiết
bị hít khác nhau, và cũng khác nhau về cách sử dụng. Do đó, khi chọn thuốc, điều quan trọng là
phải xem xét từng bệnh nhân và khả năng tuân thủ của họ với từng loại dụng cụ phân phối thuốc,
đặc biệt là xem xét các trở ngại như các yếu tố kinh tế xã hội và tình trạng sẵn có của thuốc.
3 3. KẾT LUẬN
Bệnh phổi tắc nghẽn mạn tính đặc trưng bởi tình trạng hạn chế luồng khí thở ra không hồi phục
hoàn toàn. Đo chức năng hô hấp là tiêu chuẩn tham chiếu để chẩn đoán và đánh giá mức độ nặng
của bệnh. Tất cả bệnh nhân cần được tư vấn và áp dụng các biện pháp phòng bệnh như cai thuốc lá và tiêm vắc-xin. Việc điều trị nên dựa trên mức độ nặng của suy giảm chức năng phổi, các triệu
chứng như khó thở, ho và lượng đờm, cũng như tần suất bị đợt cấp. Khi khó thở làm hạn chế hoạt
động hoặc chất lượng cuộc sống, COPD nên được điều trị bằng thuốc giãn phế quản kháng
cholinergic tác dụng kéo dài và thuốc chủ vận beta2, liều duy trì một hoặc hai lần mỗi ngày. Bệnh
nhân có nhiều đợt cấp có thể được hưởng lợi từ việc bổ sung corticosteroids dạng hít, đặc biệt là
những bệnh nhân có bạch cầu ái toan máu cao. Bên cạnh điều trị thuốc, phục hồi chức năng phổi,
bao gồm rèn luyện thể lực và sức bền, cùng với hỗ trợ giáo dục, dinh dưỡng và tâm lý xã hội, giúp
cải thiện các triệu chứng và khả năng chịu đựng khi tập thể dục nhưng chưa được sử dụng hết. Bổ
sung oxy cho bệnh nhân bị giảm oxy máu khi nghỉ ngơi (được định nghĩa là SpO2 <89%) giúp cải
thiện khả năng sống sót.
Bệnh nhân bị các đợt kịch phát thường xuyên làm giảm chất lượng cuộc sống và đẩy nhanh
tiến triển của bệnh. Liệu pháp điều trị phù hợp với thuốc giãn phế quản duy trì đã được chứng minh
là làm giảm tần suất các đợt cấp nhưng thực tế chưa được sử dụng đúng mức, điều này cho thấy
nhu cầu nâng cao nhận thức về các khuyến cáo điều trị cho bác sĩ điều trị và các tổ chức chăm sóc
sức khỏe, từ đó cải thiện việc chăm sóc bệnh nhân. Các tiếp cận điều trị dựa trên đặc điểm có khả
năng điều trị được đơn giản hóa bằng phân loại bệnh nhân theo triệu chứng, mức độ tần suất đợt
cấp và số lượng bạch cầu ái toan máu đang là cách hợp lý và được khuyến cáo mạnh nhất hiện
nay.
4 Tài liệu tham khảo
1. Jeffrey L Curtis. Understanding COPD Etiology, Pathophysiology, and Definition. Respir Care 2023;68(7):859-870
2. Lowe KE, Regan EA, Anzueto A, et al. COPDGene 2019: redefining the diagnosis of chronic obstructive pulmonary disease. Chronic Obstr Pulm Dis. 2019;6(5):384-399.
3. Kahnert K, Jörres RA, Behr J, Welte T: The diagnosis and treatment of COPD and its comorbidities. Dtsch Arztebl Int 2023; 120: 434-44
4. Polverino E, Goeminne PC, McDonnell MJ, et al. European Respiratory Society guidelines for the management of adult bronchiectasis. Eur Respir J 2017; 50: 1700629 ).
5. Nisa Patel,. An update on COPD prevention, diagnosis, and management: The 2024 GOLD Report. The Nurse Practitioner • Vol. 49, No. 6
6. Gaetano Caramori et al. COPD immunopathology. Semin Immunopathol (2016) 38:497-515.
7. Rodrigues, S.d.O.et al. Mechanisms, Pathophysiology and Currently Proposed Treatments of Chronic Obstructive Pulmonary Disease. Pharmaceuticals 2021, 14, 979.
8. Corry-Anke Brandsma et al. Recent advances in chronic obstructive pulmonary disease pathogenesis: from disease mechanisms to precision medicine. J Pathol 2020; 250: 624-635
9. Cuixue Wang et al. Progress in the mechanism and targeted drug therapy for COPD. Signal Transduction and Targeted Therapy (2020) 5:248
10. GOLD report 2025
11. Craig M. Riley et al. Diagnosis and Outpatient Management of Chronic Obstructive Pulmonary DiseaseA Review. Published Online: February 26, 2019 2019;321;(8):786-797. doi:10.1001/jama.2019.0131
12. Suzanne G. Bollmeieret al. Management of chronic obstructive pulmonary disease: A review focusing on exacerbations. Am J Health-Syst Pharm. 2020; 77:259-268
13. Mullard A. FDA approves first monoclonal antibody for COPD. Nature Reviews Drug Discovery 23, 805 (2024)

