Can thiệp tim mạch: Can thiệp động mạch chi dưới
Nguồn: Sách can thiệp tim mạch
Chủ biên: PGS.TS.BS. Phạm Mạnh Hùng
Tham gia biên soạn
ThS.BSNT Đinh Huỳnh Linh
ThS.BSNT Lê Tuấn Minh
ThS.BSNT Phạm Đình Vụ
ThS.BSNT Trần Đình Tuyên
ThS.BSNT Trương Đình Phi
PGS. TS.BS Phạm Mạnh Hùng
Các nội dung về tiếp cận bệnh nhân, lựa chọn dụng cụ, thực hiện can thiệp động mạch chi dưới, các biến chứng có thể gặp phải sẽ được Trung Tâm Thuốc Central Pharmacy (trungtamthuoc.com) xin gửi đến các bạn đọc trong bài đăng dưới đây.
1 Đại cương
Bệnh động mạch chi dưới nằm trong bệnh cảnh chung của xơ vữa động mạch, với các yếu tố nguy cơ tương tự bệnh mạch vành, như tuổi cao, giới tính nam, đái tháo đường, hút thuốc lá, tăng huyết áp, rối loạn lipid máu. Khi dân số ngày càng già đi, tỷ lệ bệnh nhân bệnh động mạch chi dưới cũng tăng lên. Nhiều nghiên cứu cho thấy tổn thương động mạch chi dưới là một yếu tố tiên lượng các biến cố tim mạch như tử vong, nhồi máu cơ tim, đột quỵ não.
Chiến lược điều trị bệnh động mạch chi dưới cần được đặt trong tổng thể đánh giá diễn biến bệnh, các yếu tố nguy cơ, và triệu chứng lâm sàng của bệnh nhân. Các biện pháp điều trị bao gồm dự phòng thứ phát biến cố tim mạch, cải thiện triệu chứng, và tái tưới máu chi.
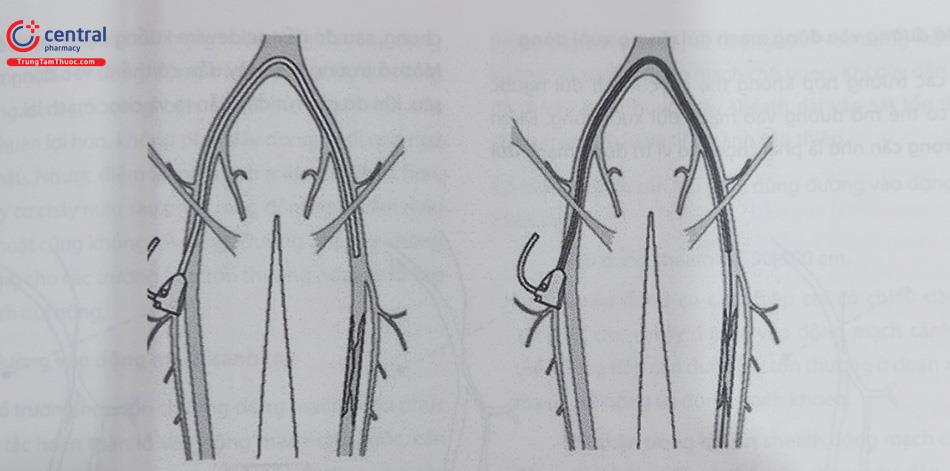
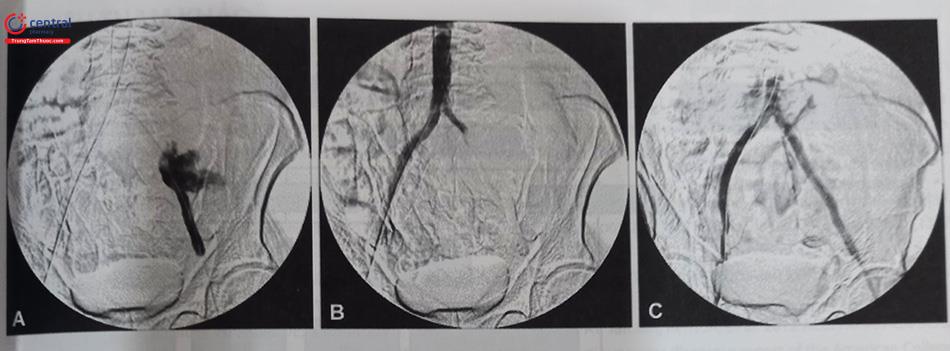
Lịch sử can thiệp nội mạch điều trị tổn thương mạch máu chi dưới được khởi đầu năm 1964, khi bác sĩ Charles Dotter sử dụng các ống nong có đường kính tăng dần để nong rộng động mạch đùi của một bệnh nhân nữ 82 tuổi có hoại tử chi. Thủ thuật thành công đã giúp người bệnh tránh được phẫu thuật cắt cụt chi, và có thể đi lại tương đối bình thường cho đến cuối đời. Đây cũng là ca can thiệp mạch máu dưới màn tăng sáng đầu tiên trên thế giới, làm cơ sở cho sự ra đời của can thiệp động mạch vành và chuyên ngành tim mạch can thiệp.
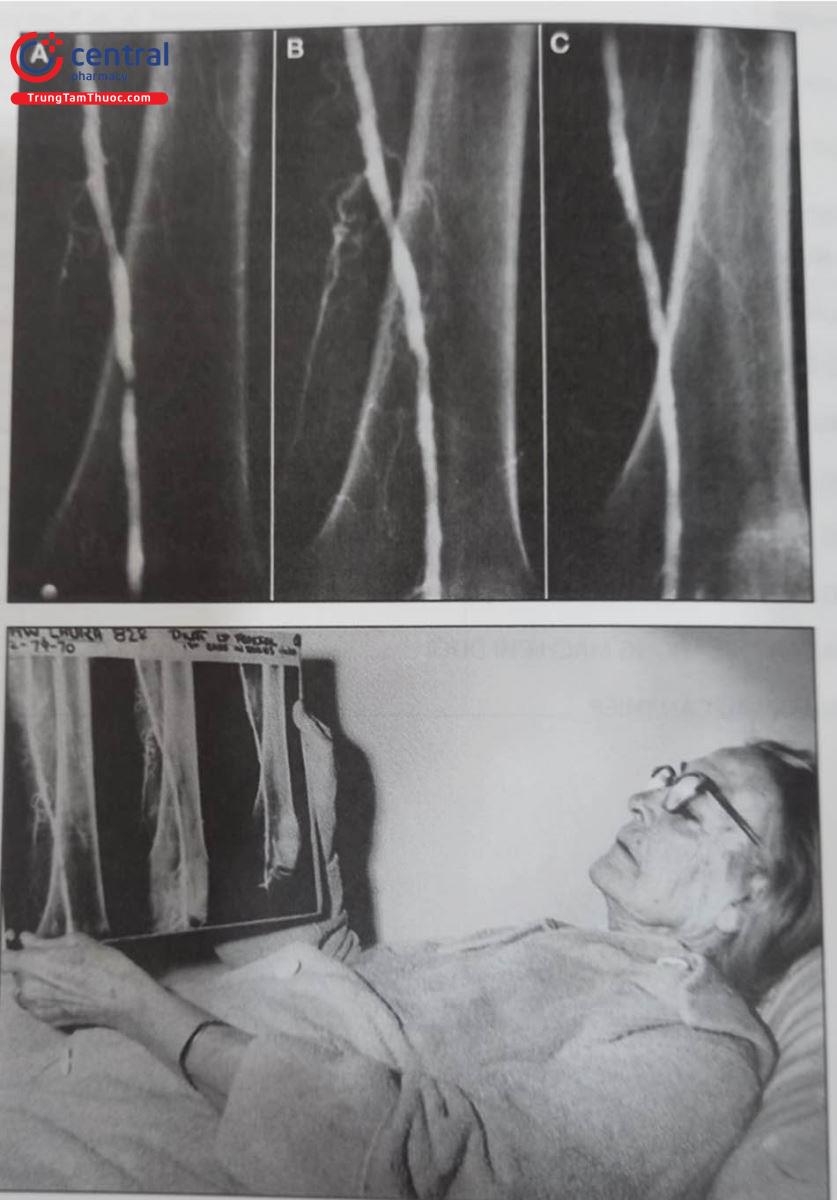
A. Trước khi nong động đùi chung trái, B. Ngay sau khi nong bóng và C. Ba tuần sau can thiệp.
Để điều trị tổn thương hẹp, tắc động mạch chi dưới, can thiệp nội mạch đã được chứng minh có tỷ lệ thành công không kém phẫu thuật bóc tách nội mạc hoặc làm cầu nối, đặc biệt với những tổn thương tầng trên gối. Ngoài ra, so với phẫu thuật, can thiệp nội mạch có một số ưu điểm:
- Gây tê tại chỗ cho phép thực hiện trên bệnh nhân có nguy cơ cao với gây mê toàn thân.
- Tỷ lệ biến chứng và tử vong thấp hơn so với phẫu thuật tái thông mạch.
- Bệnh nhân có thể trở lại hoạt động bình thường trong vòng 24-48 giờ.
- Có thể can thiệp lại nếu cần thiết. Can thiệp lần 2 không khó khăn hơn và cũng không làm tăng nguy cơ cho bệnh nhân.
- Can thiệp nội mạch không loại trừ hoàn toàn phẫu thuật sau này nếu cần.
Cùng với những tiến bộ về kỹ thuật và công nghệ trong chuyên ngành tim mạch can thiệp, can thiệp nội mạch dần trở thành lựa chọn được ưu tiên trong thực hành lâm sàng, giúp cải thiện triệu chứng lâm sàng và chất lượng cuộc sống cho người bệnh, cũng như giảm đáng kể tỷ lệ cắt cụt chi. Hiện nay, có nhiều biện pháp để tái thông mạch máu chi dưới như nong bóng đơn thuần, nong bóng phủ thuốc, đặt stent tự nở, đặt stent phủ thuốc và đặt stent có màng bọc. Xu thế hiện nay là dịch chuyển dần từ phẫu thuật mở sang thủ thuật can thiệp nội mạch ít xâm lấn.
Trước đây, thủ thuật can thiệp mạch máu chi dưới thường được tiến hành bởi các bác sĩ điện quang can thiệp hoặc phẫu thuật viên mạch máu. Tuy nhiên, sự phức tạp của tổn thương mạch máu, cùng các bệnh nội khoa phổ biến ở người bệnh, như nhiễm khuẩn nặng, bệnh ĐMV, suy tim, suy thận, đòi hỏi tiếp cận đa chuyên khoa để đạt hiệu quả điều trị tối ưu nhất, với sự tham gia ngày càng nhiều hơn của các bác sĩ tim mạch can thiệp. Theo thống kê, các bác sĩ tim mạch can thiệp thực hiện khoảng 50-80% số ca can thiệp động mạch chi dưới.
2 Tiếp cận bệnh nhân động mạch chi dưới
2.1 Thiếu máu chi cấp tính
Khi đánh giá bệnh nhân có đau chi dưới, cần trả lời bệnh nhân thiếu máu chi cấp tính hay thiếu máu chi mạn tính. Thiếu máu chi cấp tính có thể xuất hiện do tắc mạch trên nền mạch máu xơ vữa nặng, tương tự biến cố nhồi máu cơ tim ở bệnh nhân có hẹp ĐMV. Tuy nhiên, căn nguyên thường gặp hơn gây thiếu máu chi cấp tính là do cục máu đông từ tim trôi xuống. Các dấu hiệu gợi ý tắc mạch cấp tính do cục máu đông bao gồm:
- Bệnh nhân có tình trạng thuận lợi cho hình thành huyết khối buồng tim như rung nhĩ hoặc chức năng thất trái giảm nhiều.
- Bệnh nhân trẻ tuổi, không có nhiều yếu tố nguy cơ của xơ vữa mạch máu.
- Tắc mạch thường gặp ở vị trí chỗ chia nhánh như động mạch đùi chung chỗ chia động mạch đùi nông – đùi sâu, động mạch khoeo chỗ tách ra các nhánh tầng cẳng chân.
- Thăm dò chẩn đoán hình ảnh cho thấy các đoạn mạch khác tương đối bình thường, hệ thống tuần hoàn bàng hệ không phong phú.
Ngoài ra, một nguyên nhân khác có thể gặp là tắc động mạch chi cấp tính sau can thiệp nội mạch (nong bóng, đặt stent).
Mặc dù chẩn đoán hình ảnh mạch máu là cần thiết để quyết định hướng điều trị, cần nhớ chẩn đoán tắc mạch chi cấp tính là chẩn đoán lâm sàng, dựa vào thời điểm xuất hiện và diễn biến bệnh. Không được phép để các thăm dò cận lâm sàng như siêu âm, chụp MSCT, chụp MRI mạch máu làm chậm trễ quá trình xử trí người bệnh. Triệu chứng lâm sàng kinh điển của tắc mạch chi cấp tính là dấu hiệu 6P:
- Pain: Đau
- Pale: Nhợt
- Poikilothermia: Lạnh
- Pulseless: Mất mạch
- Paresthesia: Rối loạn cảm giác
- Paralysis: Giảm vận động
Nếu được chẩn đoán tắc mạch chi cấp tính, cần phân độ giai đoạn bệnh và chỉ định tái tưới máu càng sớm càng tốt, đồng thời truyền Heparin đường tĩnh mạch. Phân độ Rutherford dựa trên lâm sàng chia các bệnh nhân tắc mạch chi cấp tính thành 3 nhóm: còn bảo tồn (Rutherford I), đe doạ mất chi (Rutherford II), và thiếu máu chi không phục hồi (Rutherford III). Bảng phân độ này có giá trị tiên lượng bệnh nhân để lựa chọn biện pháp điều trị phù hợp nhất.
Trong bệnh cảnh tắc mạch chi cấp tính, thiếu máu chi không phải là mối đe dọa duy nhất đối với người bệnh. Bệnh nhân hoại tử có thể bị tiêu cơ vân cấp dẫn đến suy thận cấp, biểu hiện là nồng độ CK và creatinin máu tăng cao. Cùng với đó là tình trạng nhiễm trùng nhiễm độc toàn thân và toan chuyển hoá. Vì vậy, nếu xác định bệnh nhân không còn khả năng cứu chi, cắt cụt chi sớm để tránh các biến cố toàn thân đe doạ tính mạng.
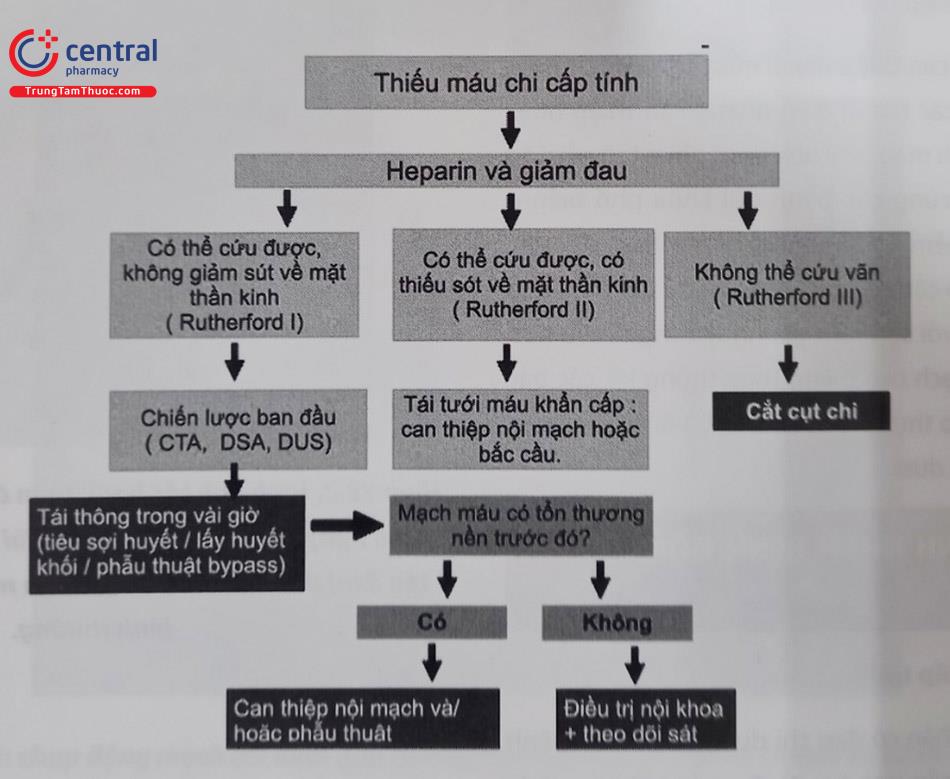
(Chú thích: CTA: Chụp cắt lớp vi tính mạch máu; DSA: Chụp mạch số hóa xóa nền; DUS: Siêu âm Doppler mạch chẩn đoán.)
Trước đây, phẫu thuật mở mạch máu lấy huyết khối kết hợp làm cầu nối là phương pháp được ưu tiên trong các trường hợp tắc mạch do cục máu đông. Hiện nay, những kỹ thuật can thiệp nội mạch như hút huyết khối qua đường ống thông, truyền thuốc tiêu sợi huyết tại chỗ, nong bóng và đặt stent có thể giúp tái thông dòng chảy hiệu quả trong bệnh cảnh tắc mạch chi cấp tính. Nhiều nghiên cứu cho thấy can thiệp nội mạch có hiệu quả lâu dài tương đương phẫu thuật, trong khi tỉ lệ tử vong quanh chu phẫu lại thấp hơn. Tuy nhiên, cần có sự hội chẩn giữa bác sĩ nội khoa tim mạch, bác sĩ tim mạch can thiệp, phẫu thuật viên mạch máu để lựa chọn chiến lược điều trị tối ưu cho người bệnh.
Tương tự phẫu thuật, mục đích của can thiệp nội mạch là tái thông dòng chảy càng sớm càng tốt. Thủ thuật được tiến hành tương tự trường hợp tắc mạch chi mạn tính. Do chủ yếu tổn thương do huyết khối mới hình thành, việc lái dây dẫn qua tổn thương không quá khó khăn. Sau đó tiến hành nong bóng như các ca can thiệp thông thường.
Biện pháp tối ưu nhất tái thông mạch máu là hút huyết khối bằng dụng cụ. Do mạch máu ngoại biên có kích cỡ lớn hơn động mạch vành (đường kính động mạch chậu khoảng 8-10 mm, đường kính động mạch đùi nông 4-8 mm), các dụng cụ chuyên dụng như AngioJet sẽ đảm bảo hút huyết khối triệt để hơn. Nếu không có máy hút huyết khối, có thể hút huyết khối bằng bơm áp lực âm. Sau khi hút huyết khối, có thể cần nong lại mạch máu bằng bóng hoặc đặt stent.
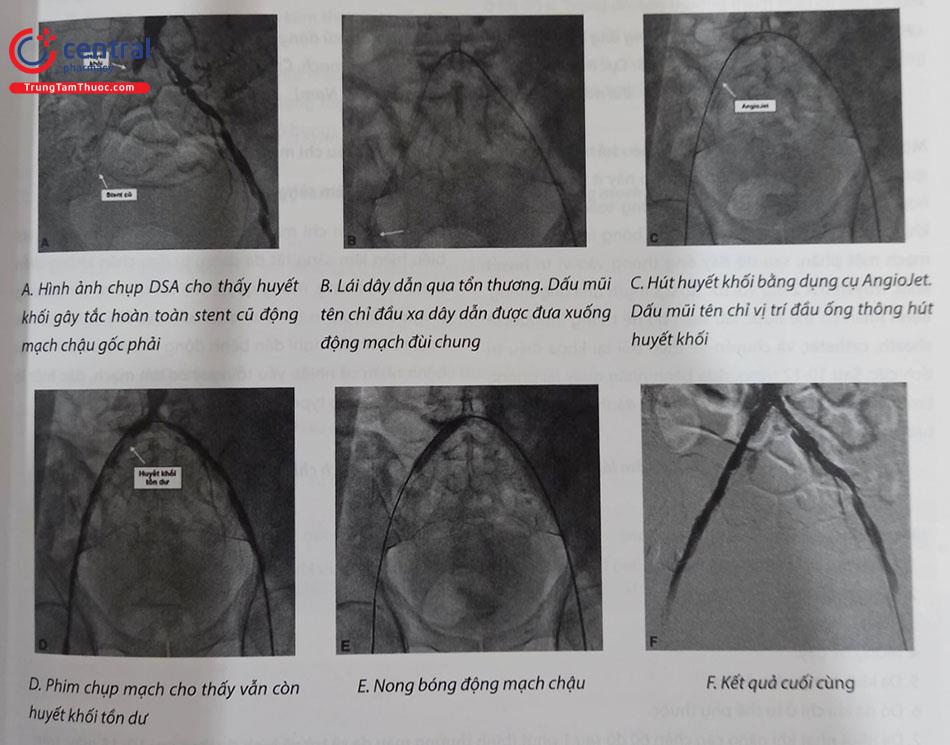
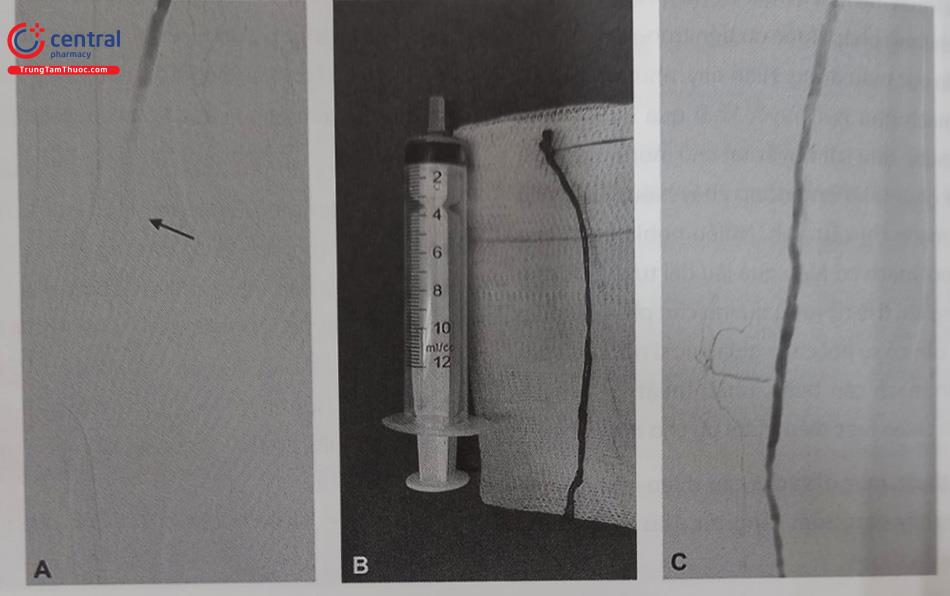
Một biện pháp khác là truyền thuốc tiêu sợi huyết trực tiếp qua đường ống thông. Phương pháp này ít tác dụng phụ hơn dùng thuốc tiêu sợi huyết đường toàn thân. Trước khi bơm thuốc tiêu sợi huyết, nong bóng tái thông lòng mạch một phần, sau đó đẩy ống thông vào vị trí huyết khối. Truyền tPA 2 mg với tốc độ 0,5 mg/h qua ống thông. Bệnh nhân có thể được lưu toàn bộ hệ thống introducer sheath, catheter, và chuyển về theo dõi tại khoa điều trị tích cực. Sau 10-12 tiếng, đưa bệnh nhân quay lại phòng tim mạch can thiệp để chụp mạch và đánh giá tình trạng tưới máu chi.
2.2 Thiếu máu chi mạn tính
2.2.1 Đánh giá lâm sàng
Hẹp, tắc mạch chi mạn tính thường diễn biến từ từ, với biểu hiện lâm sàng rất đa dạng, từ đau chân không điển hình, nấm móng, móng quặp, teo cơ, dị cảm, vết thương chi khó lành, cho tới đau cách hồi, đau khi nghỉ, loét và hoại tử chi. Cần nghĩ đến bệnh động mạch chi dưới ở mọi bệnh nhân có nhiều yếu tố nguy cơ tim mạch, đặc biệt là đái tháo đường type 2 và tiền sử hút thuốc lá.
Bảng 28.1. Khám lâm sàng bệnh nhân bệnh động mạch chi dưới mạn tính
Khám chi (và so sánh với chi bên lành):
|
Do biểu hiện lâm sàng rất đa dạng, nhiều bệnh nhân bệnh động mạch chi dưới mạn tính đến viện ở giai đoạn muộn, khi đó khả năng tái tưới máu rất khó khăn. Theo khuyến cáo Hội Tim mạch châu Âu (ESC) năm 2017 về chẩn đoán và điều trị bệnh động mạch ngoại biên, thầy thuốc lâm sàng cần tiến hành sàng lọc tổn thương mạch máu chi dưới bằng chỉ số huyết áp cổ chân – cánh tay (ABI) ở những đối tượng sau:
- Người có triệu chứng lâm sàng gợi ý bệnh động mạch chi dưới.
- Người không triệu chứng nhưng có yếu tố nguy cơ cao:
- Người ≥ 65 tuổi.
- Tuổi 50-64, có ít nhất một yếu tố nguy cơ (đái tháo đường, hút thuốc lá, rối loạn lipid máu).
- Tuổi < 50, có đái tháo đường kèm theo một yếu tố nguy cơ xơ vữa mạch máu khác.
- Bệnh nhân có bệnh lý xơ vữa mạch máu (động mạch vành, động mạch cảnh, động mạch dưới đòn, động mạch thận, động mạch chủ bụng).
Chỉ số ABI < 0,9 là cơ sở để chỉ định các thăm dò chẩn đoán hình ảnh để chẩn đoán xác định, định khu, đánh giá giai đoạn tổn thương động mạch chi dưới. Nhiều nghiên cứu cho thấy số đo ABI có tương quan nghịch với tỷ lệ các biến cố tim mạch như tử vong, nhồi máu cơ tim, đột quỵ não, cắt cụt chi. Đo ABI cả khi nghỉ ngơi và sau gắng sức rất hữu ích, đặc biệt ở người có nguy cơ cao. Ngoài ra, có thể đo chỉ số ngón chân – cánh tay (TBI) cho các bệnh nhân thành mạch quá cứng (như người cao tuổi, suy thận mạn, đái tháo đường).
2.2.2 Các thang điểm lâm sàng
Có nhiều thang điểm lâm sàng được sử dụng để đánh giá bệnh nhân bệnh động mạch chi dưới. Thang điểm Rutherford chia tình trạng lâm sàng của bệnh nhân từ độ 0 tới độ 6. Trong đó, tổn thương mạch máu có Rutherford 4 trở lên được xếp vào giai đoạn thiếu máu chi trầm trọng. Nếu người bệnh có thiếu máu chi trầm trọng, tỷ lệ sống sau 1 năm với hai chân còn nguyên vẹn chỉ là 50%.
2.2.3 Các thang điểm lâm sàng
Có nhiều thang điểm lâm sàng được sử dụng để đánh giá bệnh nhân động mạch chi duwois. thâng điểm Rutherford chia tình trạng lâm sàng của bệnh nhân từ độ 0 đến 6. Trong đó, tổn thương mạch máu có Rutherford 4 trở lên được xếp vào giai đoạn thiếu máu chi trầm trọng. Nếu người bệnh có thiếu máu chi trầm trọng, tỷ lệ sống sau 1 năm với 2 chân còn nguyên vẹn chỉ là 50%.
Bảng 28.2. Phân độ Rutherford cho bệnh nhân bệnh động mạch chi dưới mạn tính& ;
| Rutherford 0 ; | Không có triệu chứng lâm sàng |
| Rutherford 1 | Đau cách hồi mức độ nhẹ |
| Rutherford 2 | Đau cách hồi mức độ trung bình |
| Rutherford 3 | Đau cách hồi mức độ nặng |
| Rutherford 4 | Đau chân khi nghỉ |
| Rutherford 5 | Loét đầu chi, mất mô ít |
| Rutherford 6 | Thiếu máu chi nặng, loét chi nhiều, hoại tử chi |
Một bảng phân loại khác cũng thường được sử dụng trong thực hành lâm sàng là phân loại WIFI. Bảng phân loại này đánh giá tình trạng bàn chân của bệnh nhân theo 3 yếu tố: loét (Wound), thiếu máu (Ischemia), và nhiễm trùng bàn chân (Foot Infection). Dựa vào đó sẽ phân tầng nguy cơ cắt cụt chi là rất thấp, thấp, trung bình, hay cao.
Bảng 28.3. Thang điểm WIFI đánh giá nguy cơ cắt cụt chi
| THÀNH PHẦN | ĐIỂM | MÔ TẢ | |||
|---|---|---|---|---|---|
W | 0 | Không có vết loét (đau ngay cả khi nghỉ do thiếu máu chi) | |||
1 | Vết loét nhỏ, nông ở đoạn xa chi hoặc bàn chân, không có hoại tử | ||||
2 | Vết loét sâu, (bộc lộ xương) khớp và gân, không hoặc có hoại tử giới hạn ở ngón chân | ||||
3 | Vết loét sâu rộng, loét hết độ dày gót chân có thể bao gồm xương gót, hoại tử rộng | ||||
; I |
| ABI | Tưới máu mắt cá (mmHg) | Tưới máu ngón chân hoặc TcPO2 | |
0 | ≥ 0,80 | > 100 | ≥ 60 | ||
1 | 0,60 – 0,79 | 70 -100 | 40 – 59 | ||
2 | 0,4 – 0,59 | 50 – 70 | 30 -39 | ||
3 | < 0,40 | < 50 | < 30 | ||
fI | 0 | Không có triệu chứng/ dấu hiệu của nhiễm trùng | |||
| 1 | Nhiễm trùng khu trú chỉ ở da hoặc mô dưới da | ||||
2 | Nhiễm trùng nằm sâu hơn da hoặc mô dưới da | ||||
3 | Hội chứng đáp ứng viêm hệ thống | ||||
Chú thích: TcPO2 (Transcutaneous Oxygen): Áp lực riêng phần oxy đo qua da, W (Wound): Vết thương, I (Ischemia): Thiếu máu, fI ( foot Infection): Nhiễm trùng bàn chân
2.2.4 Bàn chân đái tháo đường
Đái tháo đường làm tăng nguy cơ cắt cụt chi lên 20 lần ở các bệnh nhân bệnh động mạch chi dưới. Điểm đặc trưng của tổn thương mạch máu trong bệnh lý bàn chân đái tháo đường là tiến triển nhanh, kèm theo vôi hoá nhiều lớp áo giữa. Động mạch tổn thương thường là tầng dưới gối.
Hẹp mạch máu trên nền đái tháo đường thường đi kèm bệnh lý thần kinh ngoại biên. Hệ quả là giảm cảm giác, teo cơ, biến dạng bàn chân, dẫn tới bàn chân dễ bị viêm loét ngay cả khi tình trạng hẹp tắc động mạch không quá trầm trọng. Nhiều bệnh nhân đái tháo đường không biểu hiện đau, vì thế triệu chứng đầu tiên của bệnh thường là loét khó liền.
Do mạch máu vôi hoá nhiều nên đo ABI có thể cho kết quả âm tính giả. Khi đó, chỉ số ngón chân – cánh tay (TBI: Toe Brachial Index) là một thông số đáng tin cậy hơn về tình trạng tưới máu chi, đặc biệt ở các bệnh nhân đái tháo đường và suy thận mạn vì các mạch nhỏ của ngón chân thường không bị vôi hóa nội mạc. TBI đặc biệt có giá trị khi ABI lớn hơn 1,4. Các bệnh nhân ABI tăng giả tạo có nguy cơ cắt cụt chi cao ngang bệnh nhân ABI thấp.
Bảng 28.4. Khuyến cáo về đánh giá bệnh nhân bệnh động mạch chi dưới mạn tính giai đoạn thiếu máu chi đe doạ, theo Hiệp hội Tim mạch châu Âu (ESC) năm 2017.
CÁC KHUYẾN CÁO | NHÓM | MỨC ĐỘ CHỨNG CỨ |
|---|---|---|
Phát hiện sớm dấu hiệu mất mô và/hoặc nhiễm trùng và giới thiệu người bệnh đến các bác sĩ chuyên khoa mạch máu là bắt buộc để cải thiện việc bảo tồn chi thể. |
I |
C |
Với bệnh nhân có thiếu máu mạn tính chi đe dọa, đánh giá nguy cơ cắt cụt được chỉ định. |
I |
C |
Với bệnh nhân có thiếu máu mạn tính chi đe dọa kèm theo đái tháo đường, kiểm soát đường máu tối ưu được khuyến cáo. |
I |
C |
Để bảo tồn chi, tái tưới máu được chỉ định bất cứ khi nào có thể. | I | B |
Ở bệnh nhân thiếu máu chi mạn tính với tổn thương dưới gối, chụp mạch đánh giá tổn thương nên được xem xét trước khi tái tưới máu. |
IIa |
C |
Ở bệnh nhân thiếu máu mạn tính chi, liệu pháp tế bào/gen không được chỉ định. |
III |
B |
2.2.5 Thăm dò chẩn đoán hình ảnh
Chẩn đoán hình ảnh mạch máu giữ vai trò quan trọng giúp thầy thuốc đề ra chiến lược tái tưới máu phù hợp nhất. Lý tưởng nhất, tất cả các bệnh nhân dự định can thiệp nội mạch cần được chụp MSCT động mạch chi dưới, đặc biệt là các trường hợp tổn thương tầng chủ chậu. Tuy nhiên, tuỳ vào từng bệnh nhân cụ thể, cũng như điều kiện thực tế của bệnh viện để đưa ra chỉ định thăm dò chẩn đoán hình ảnh phù hợp.
2.2.6 Siêu âm Doppler mạch máu
Siêu âm mạch máu là thăm dò cơ bản cần được chỉ định cho mọi bệnh nhân bệnh động mạch chi dưới. Siêu âm cho phép đánh giá vị trí, hình thái mảng xơ vữa, mức độ vôi hóa, đánh giá tình trạng hẹp hay tắc toàn bộ lòng động mạch, huyết khối trong lòng động mạch, phình động mạch, kích thước đoạn mạch tổn thương và đoạn mạch lành. Phổ Doppler mạch máu cho phép lượng hóa mức độ hẹp lòng động mạch cũng như ảnh hưởng huyết động lên dòng chảy sau vị trí hẹp.
Ưu điểm lớn nhất của siêu âm là không xâm nhập, gọn nhẹ, trong khi giá trị chẩn đoán cao. Siêu âm mạch máu không cần dùng thuốc cản quang, không có tia X, do đó có thể dùng cho các bệnh nhân suy thận. Do tính đơn giản của nó, đây là thăm dò được sử dụng để theo dõi tái hẹp sau can thiệp mạch máu chi dưới. Tuy nhiên, siêu âm không cho phép đánh giá sâu các đặc điểm giải phẫu của động mạch tầng chậu, như sự xoắn vặn mạch máu. Thăm dò này cũng phụ thuộc nhiều vào kinh nghiệm của người làm siêu âm.
2.2.7 Chụp MSCT mạch máu
Chụp MSCT mạch máu cho phép dựng hình toàn bộ hệ mạch máu. Kết quả MSCT mô tả tổn thương động mạch, các đặc điểm giải phẫu, cũng như hệ thống tuần hoàn bàng hệ, tình trạng tưới máu đoạn xa. Một ca chụp MSCT mạch chi dưới thường cần khoảng 100 mL thuốc cản quang, vì thế có thể gây suy thận.
2.2.8 Chụp cộng hưởng từ mạch máu
Các bệnh nhân suy thận có thể được chỉ định chụp MRI mạch máu bằng gadolinium. Mặc dù có giá trị chẩn đoán cao, MRI thường có xu hướng ước tính quá nặng mức độ hẹp, và không mô tả tình trạng vôi hóa mạch máu.
2.2.9 Chụp mạch số hoá xoá nền (DSA)
Đây là tiêu chuẩn vàng để đánh giá tổn thương mạch máu chi dưới. Tuy nhiên nhược điểm là thăm dò gây chảy máu và phải sử dụng thuốc cản quang.
2.2.10 Phân độ TASC II
Dựa trên thăm dò hình ảnh mạch máu, đánh giá mức độ phức tạp của tổn thương bằng bảng phân loại theo đồng thuận liên Đại Tây Dương lần 2 (TransAtlantic Inter- Society Consensus 2, viết tắt TASC 2). Các tổn thương được chia ra làm 3 nhóm: tầng chủ chậu, tầng đùi khoeo, tầng dưới gối. Trong mỗi nhóm, mức độ tổn thương mạch máu được phân ra từ A-D, trong đó TASC A là tổn thương khu trú, không phức tạp, còn TASC D là những tổn thương lan toả, bao gồm nhiều mạch máu, kèm theo tình trạng vôi hoá nhiều. Trước đây, can thiệp nội mạch chỉ được ưu tiên cho những trường hợp TASC A hay TASC B, còn TASC C và TASC D là chỉ định phẫu thuật. Những tiến bộ về thiết bị và kỹ thuật đã nâng tỉ lệ thành công của can thiệp nội mạch đồng thời giảm tỉ lệ biến chứng, do đó đã mở rộng chỉ định của thủ thuật can thiệp cho cả những tổn thương phức tạp TASC C-D.
Bảng 28.5. Thang điểm TASC II đánh giá tổn thương động mạch chậu

Bảng 28.6. Thang điểm TASC II đánh giá tổn thương động mạch đùi nông

Bảng 28.7. Phân loại TASC II với tổn thương tầng dưới gối

2.2.11 Điều trị nội khoa với bệnh động mạch chi dưới mạn tính
Thay đổi lối sống
Nếu bệnh nhân tiếp tục hút thuốc, nguy cơ tiến triển của xơ vữa động mạch sẽ tiếp tục gia tăng, kèm theo đó là các biến cố như nhồi máu cơ tim, đột quỵ não, mất chi, và tử vong tim mạch. Vì thế, bỏ thuốc lá là chỉ định tuyệt đối cho tất cả các bệnh nhân.
Tập vận động cũng được chứng minh có hiệu quả ở những bệnh nhân còn có thể đi bộ. Bệnh nhân được hướng dẫn tập luyện ít nhất 30 – 45 phút mỗi ngày, tối thiểu 3 lần/ tuần trong khoảng thời gian ít nhất là 12 tuần, sau đó đánh giá lại và tiếp tục vận động thường quy.
Điều trị rối loạn lipid máu
Statin được chỉ định cho tất cả các bệnh nhân, nhằm phòng ngừa biến cố tim mạch. Bệnh nhân bệnh động mạch chi dưới được coi là nguy cơ cao đến rất cao, do vậy cần sử dụng statin có cường độ cao như rosuvastatin (20 – 40 mg); Atorvastatin (40 – 80 mg), hoặc có thể phối hợp statin với ezetimibe.
Chỉ định dùng statin bất kể nồng độ LDL-C ban đầu là bao nhiêu, với đích LDL-C dưới 1,4 mmol/l, hoặc ít nhất giảm được một nửa mức ban đầu. Kháng thể đơn dòng ức chế PCSK9 có thể cân nhắc cho những bệnh nhân đã sử dụng liều statin và ezetimibe tối đa mà vẫn chưa đạt LDL mục tiêu.
Điều trị đái tháo đường
Ở bệnh nhân có tổn thương động mạch chi dưới kèm theo đái tháo đường type 2, bên cạnh Metformin, thuốc ức chế thụ thể SGLT2 (như Empagliflozin, Dapagliflozin) và/hoặc thuốc đồng vận GLP-1 (liraglutide) được khuyến cáo sử dụng. Mục tiêu là đạt HbA1c ≤ 7,0%.
Điều trị tăng huyết áp
Kiểm soát huyết áp tích cực, mục tiêu là HA < 140/90 mmHg, hoặc dưới 130/80 mmHg nếu bệnh nhân có đái tháo đường hoặc suy thận. Trong số các thuốc điều trị THA, nên có một thuốc ức chế men chuyển hoặc thuốc chẹn thụ thể angiotensin.
Liệu pháp kháng huyết khối
Thuốc kháng tiểu cầu đơn (SAPT) được chỉ định dùng dài hạn cho mọi bệnh nhân có triệu chứng, gồm cả những bệnh nhân được tái thông mạch chi (can thiệp nội mạch hoặc phẫu thuật bắc cầu nối bằng đoạn mạch nhân tạo). Không cần dùng thuốc kháng tiểu cầu ở bệnh nhân không triệu chứng.
Liệu pháp kháng tiểu cầu kép, phối hợp giữa Aspirin (75 – 100 mg) với Clopidogrel (75 mg), được chỉ định cho bệnh nhân sau tái tưới máu, với thời gian kéo dài tối thiểu là 1 tháng. Ngoài ra, ở các bệnh nhân nguy cơ xuất huyết thấp, có thể kết hợp aspirin (100 mg/ngày) với thuốc chống đông đường uống Rivaroxaban liều thấp (2,5 mg x 2 lần/ngày) để giảm biến cố tim mạch, biến cố lớn trên chi đặc biệt là giảm tỉ lệ cắt cụt chi cho người bệnh
Chăm sóc tại chỗ vết loét
Để điều trị tối ưu bệnh nhân thiếu máu chi trầm trọng, tái tưới máu là không đủ. Chăm sóc vết loét cũng giữ vai trò quan trọng tương tự. Có thể cần phẫu thuật cắt lọc vùng mô hoại tử, giảm tiến triển của nhiễm khuẩn. Các biện pháp trị liệu khác bao gồm hút áp lực âm, tiêm yếu tố tăng trưởng mô, đảm bảo vết loét khô và liền thương tốt. Những bệnh nhân nhiễm khuẩn nặng cần dùng kháng sinh toàn thân liều cao.
Điều trị tái tưới máu với bệnh động mạch chi dưới mạn tính
Chỉ định tái tưới máu dựa trên tình trạng cụ thể của người bệnh, có cân nhắc các bệnh mạch máu khác kèm theo (bệnh ĐMV, bệnh động mạch cảnh), cũng như nguy cơ cắt cụt chi.
Ở bệnh nhân có đau cách hồi, tái tưới máu giúp giảm triệu chứng và cải thiện chất lượng cuộc sống, đồng thời hạn chế tiến triển của tổn thương mạch máu chi dưới. Ở những bệnh nhân thiếu máu chi trầm trọng (giai đoạn Rutherford 4 trở lên), tái tưới máu có giảm triệu chứng đau, giúp liền vết thương, và giảm tỉ lệ cắt cụt chi. Trong một số trường hợp, khi không thể tránh khỏi việc cắt cụt chi, tái tưới máu tốt phần chi phía trên giúp cắt cụt ít hơn, tăng tỷ lệ bảo tồn mô, đồng thời đảm bảo mỏm cụt liền sẹo và hồi phục tốt.
3 Dụng cụ sử dụng trong can thiệp động mạch chi dưới
Thủ thuật can thiệp động mạch chi dưới có thể tiến hành với hệ thống chụp mạch tương tự can thiệp ĐMV. Tuy nhiên do đặc thù tổn thương, nó đòi hỏi một số dụng cụ chuyên biệt hơn.
3.1 Sheath dài (long sheath)
Với can thiệp ĐMV, dụng cụ mở đường vào mạch máu (sheath) thường có độ dài 10-15 cm. Tuy nhiên, nhiều trường hợp can thiệp mạch chi dưới sử dụng sheath có độ dài từ 45-100 cm. Sheath dài có hai tác dụng: (1) Nó đi qua các đoạn mạch xoắn vặn, tiếp cận gần tổn thương, giúp bác sĩ can thiệp thao tác dễ dàng hơn; (2) Dụng cụ sử dụng trong can thiệp mạch chi dưới thường có kích cỡ lớn hơn dụng cụ can thiệp ĐMV, vì thế đòi hỏi ống thông can thiệp kích cỡ lớn hơn. Trong trường hợp này, sheath dài đóng vai trò như ống thông can thiệp. Sheath kích cỡ 6Fr có đường kính trong tương đương một ống thông can thiệp kích cỡ 8Fr, nhờ đó giảm các biến cố liên quan đường vào mạch máu.
Đa số các ca can thiệp mạch máu chi dưới có thể tiến hành với sheath cỡ 6Fr. Một số trường hợp đòi hỏi dụng cụ kích cỡ lớn hơn như khi can thiệp động mạch chậu cần stent lớn, dùng stent có màng bọc, hay dùng dụng cụ khoan phá mảng xơ vữa, có thể cần sheath cỡ 7Fr hay 8Fr. Thủ thuật viên cần nắm vững các thông số kỹ thuật của dụng cụ, từ đó lựa chọn dụng cụ mở đường vào mạch máu phù hợp.
Không phải lúc nào cũng có thể đẩy sheath dài trong lòng mạch một cách dễ dàng. Khi đó, có thể sử dụng kỹ thuật“mẹ bồng con” (mother-and-child). Thủ thuật viên đẩy que nong (dilator), ống thông, hoặc bóng vào trong sheath để tăng lực hỗ trợ, nhờ đó có thể đẩy sheath đi xa hơn. Ngoài ra cũng có thể dùng kĩ thuật mỏ neo (anchor). Bóng được đẩy đến mạch máu đoạn xa, đẩy sheath đi trong lòng mạch khi bơm căng bóng.

3.2 Dây dẫn can thiệp
Can thiệp động mạch vành chỉ sử dụng dây dẫn đường kính 0,014”, còn can thiệp mạch chi dưới có thể cần các dây dẫn đường kính 0,035” hay 0,018”. Dây dẫn sử dụng trong can thiệp mạch chi dưới thường cứng hơn, độ đâm xuyên cao hơn, hỗ trợ đẩy dụng cụ tốt hơn. Nhược điểm là không mềm mại và khó điều khiển hơn dây dẫn can thiệp ĐMV.
Bóng và stent dùng trong can thiệp mạch ngoại biên thường là loại over-the-wire, vì thế dây dẫn can thiệp cần có độ dài tối thiểu 260-300 cm (khác với dây dẫn trong can thiệp động mạch vành chỉ dài 180 cm). Bảng 28.8 tổng hợp ưu nhược điểm của từng loại dây dẫn sử dụng trong can thiệp mạch chi dưới.
Bảng 28.8. Tổng hợp ưu và nhược điểm của các loại dây dẫn được sử dụng trong can thiệp mạch chi dưới
DÂY DẪN
| 0.035” | 0.018” | 0.014” |
|---|---|---|---|
Kỹ thuật | Tái thông dưới nội mạc | Tái thông trong lòng mạch | Tái thông trong lòng mạch |
Ưu điểm | Thời gian thủ thuật ngắn | Kiểm soát tốt không gâybóc tách nội mạc | Kiểm soát tốt |
Nhược điểm | Gây bóc tách kéo dài Đôi khi không thể quay lại lòng thật | Đôi khi không lái qua được tổn thương Có thể gây thủng mạch máu | Yếu, không lái qua được tổn thương Hỏng guidewire |
Khi nào sử dụng | Tổn thương CTO kéo dài | Lựa chọn đầu tay trong đa số trường hợp | Tổn thương dưới gối |
CTO: Tắc hoàn toàn mạn tính
3.3 Bóng nong
Bóng nong mạch chi dưới có cấu tạo cơ bản tương tự bóng nong ĐMV, ngoại trừ chiều dài và đường kính lớn hơn, và thường là loại ít giãn nở (non-compliant). Đặc tính ít giãn nở cho phép bóng nở căng nhưng kích cỡ lại không tăng nhiều, làm nở rộng mạch máu nhưng không gây vỡ mạch. Điều này đặc biệt có ý nghĩa với các tổn thương vôi hoá nhiều. Bóng ít giãn nở cũng dồn lực khu trú vào một điểm, thay vì dàn đều lực căng ra toàn bộ thành mạch, nhờ vậy giảm nguy cơ bóc tách ở những đoạn mạch máu lân cận.
Vật liệu chế tạo bóng ngoại biên thường là polyethylene terephthalate (PET) hoặc polyurethane được gia tăng độ cứng bằng nylon. Nhiều bóng ngoại biên có thể chịu được áp lực lên tới 30 atm. Các bóng ngoại biên tương thích dây dẫn cỡ 0,014”, 0,018”, hoặc 0,035”. Thủ thuật viên cần nắm vững đặc tính của bóng để lựa chọn dây dẫn phù hợp.
3.4 Stent
3.4.1 Stent tự nở và stent gắn trên bóng
Stent mạch ngoại biên hoạt động theo hai cơ chế: gắn trên bóng hoặc tự nở. Điểm khác biệt cơ bản giữa hai loại stent này là vật liệu chế tạo. Stent gắn trên bóng thường được làm từ hợp kim cobalt-chrome hoặc chrome với kền (nickel). Trong khi đó, stent tự nở được làm từ nitinol, là hợp kim titan (55%) với kền (45%).
So với stent gắn trên bóng, stent tự nở có hai ưu điểm. Thứ nhất là cấu hình nhỏ gọn, nhờ đó có thể đi trong lòng mạch khá dễ dàng. Một số stent nitinol có thể đi vừa sheath 4Fr. Thứ hai, vật liệu nitinol có đặc tính nhớ hình tốt, nên khi bung stent sẽ áp sát thành mạch, dù các đoạn mạch có thể có kích cỡ khác nhau. Nhược điểm của stent tự nở là khó căn chỉnh chính xác vị trí đặt stent, đồng thời độ cứng kém hơn stent nở bằng bóng. Do vậy, có thể gặp tình trạng gãy stent nếu mạch vôi hoá nặng, hoặc stent phải chịu nhiều lực chèn ép từ bên ngoài. Một nghiên cứu cho thấy gãy stent làm tăng nguy cơ tái hẹp (59%, so với tỉ lệ 16% ở nhóm không gãy stent).
Với các thế hệ thuốc chống ngưng kết tiểu cầu mới, tỉ lệ tái hẹp hay tắc lại stent của cả hai loại stent tự nở và nở trên bóng đều rất thấp. Ưu tiên lựa chọn stent gắn trên bóng cho các tổn thương tại lỗ vào động mạch chậu vì có thể căn vị trí chính xác, hoặc các tổn thương vôi hoá nhiều. Ngược lại, khả năng nhớ hình giúp stent tự nở có thể uốncong theo mạch máu, phù hợp với những đoạn mạch xoắn vặn như động mạch đùi nông.
Khi đặt stent tự nở, nên chọn đường kính stent tối thiểu lớn hơn 1 mm so với đường kính lòng mạch, để đảm bảo stent được cố định tốt. Do stent tự nở rất khó căn chính xác vị trí mong muốn như stent gắn trên bóng, nên chủ động lựa chọn stent dài để đảm bảo che phủ hết tổn thương (ví dụ chọn stent dài 60 mm cho các tổn thương dài 40 mm). Khi đặt nhiều stent, các stent cần gối nhau ít nhất 5 mm.
3.4.2 Stent có màng bọc
Stent có màng bọc là loại stent gắn trên bóng nhưng có lớp graft bằng ePTFE gắn trên khung thép, che phủ các mắt stent. Thông thường, stent có màng bọc được sử dụng cho các trường hợp tắc hoàn toàn động mạch chậu, do nguy cơ vỡ mạch máu cao. Ngoài ra, stent có màng bọc còn được sử dụng cho các tổn thương phình mạch, giả phình, hoặc để cấp cứu khi vỡ mạch máu. Do cấu hình lớn, khó đẩy trong lòng mạch, stent có màng bọc chỉ có độ dài tối đa 60 mm. Stent có màng bọc cũng cần sheath kích cỡ lớn hơn.
Stent có màng bọc có thể bị co ngắn lại khi bơm bóng, dẫn đến không che phủ hoàn toàn tổn thương. Một nguy cơ khác là lớp graft sẽ hạn chế sự nội mạc hoá, dẫn đến tăng nguy cơ huyết khối gây tắc stent. Tuy vậy, các nghiên cứu đa trung tâm so sánh stent có màng bọc với stent thường (loại tự nở hoặc gắn trên bóng) cho thấy stent có màng bọc có tỉ lệ tái hẹp thấp hơn cả.
3.5 Dụng cụ phủ thuốc
Tương tự can thiệp ĐMV, nhược điểm lớn của nong bóng đơn thuần và đặt stent thường là tỉ lệ tái hẹp cao, đặc biệt với tổn thương tầng đùi khoeo hoặc tầng dưới gối. Bóng nong phủ Paclitaxel đã được đưa vào ứng dụng, với mục đích cải thiện tỷ lệ tái thông mạch máu theo thời gian. Hiện nay có rất nhiều bóng phủ thuốc khác nhau, với kích cỡ đa dạng, đường kính 2-7 mm, chiều dài 40-120 mm.
Trong các thử nghiệm lâm sàng THUNDER và FemPac, nong bóng phủ thuốc động mạch đùi nông được chứng minh giảm tỷ lệ tái can thiệp so với nong bóng thường, bất kể là với tổn thương mới (de novo) hay tổn thương tái hẹp.
Hiện nay có hai loại stent phủ thuốc sử dụng cho động mạch đùi nông, Zilver PTX của hãng Cook và Eluvia của hãng Boston Scientific. Đây đều là các loại stent không cópolymer, được phủ paclitaxel. Kết quả nghiên cứu cho thấy stent phủ thuốc làm giảm đáng kể tỷ lệ tái hẹp so với stent thường. Với các tổn thương khu trú tầng dưới gối, một số tác giả đã sử dụng stent động mạch vành (ví dụ Xience của hãng Abbott) cho kết quả tốt.
Năm 2018, một phân tích gộp của Katsanos trên các bệnh nhân bệnh động mạch chi dưới cho thấy dụng cụ bóng hoặc stent phủ paclitaxel làm tăng 7% tỉ lệ tử vong so với dụng cụ không phủ thuốc, trong thời gian theo dõi 5 năm. Tuy nhiên, nhiều tác giả phản biện rằng nhóm bệnh nhân dùng dụng cụ phủ thuốc thường có nhiều bệnh phối hợp hơn, dẫn đến gia tăng tỉ lệ tử vong, chứ không phải do dụng cụ phủ thuốc. Gần đây, nghiên cứu SWEDEPAD theo dõi trong 2,5 năm cho thấy tỉ lệ biến cố lâm sàng (bao gồm tử vong và cắt cụt chi) của hai nhóm dùng hoặc không dùng dụng cụ phủ thuốc không có sự khác biệt.
4 Mở đường vào mạch máu
Mở đường vào mạch máu là bước đầu tiên của mọi thủ thuật tim mạch. Với can thiệp mạch chi dưới, bước này có vai trò hết sức quan trọng. Lựa chọn đường vào mạch máu phù hợp có thể chiếm 30% thành công của thủ thuật.
Các đường vào mạch máu thường được sử dụng là động mạch đùi chung ngược dòng, động mạch đùi chung xuôi dòng, động mạch cánh tay, động mạch quay, đoạn xa động mạch đùi nông, động mạch khoeo, động mạch mu chân. Nhiều trường hợp cần phối hợp nhiều đường vào mạch máu. Thủ thuật viên cần thành thạo kỹ thuật mở đường vào mạch máu, cũng như nắm được các biến cố có thể gặp. Chọc mạch máu nhiều khi không đơn giản, do động mạch phía trên bị hẹp, tắc nên mạch nảy rất yếu, hoặc không thể bắt được mạch. Siêu âm hoặc chọc mạch dưới màn tăng sáng có thể hữu ích trong các trường hợp này.
Bảng 28.9. Các đường vào mạch máu đối với các vùng mạch can thiệp khác nhau
ĐƯỜNG VÀO | ĐỘNG MẠCH CẦN CAN THIỆP |
|---|---|
Động mạch đùi chung ngược dòng | Động mạch chậu cùng bên hoặc bên đối diện, động mạch đùi – khoeo bên đối diện |
Động mạch đùi chung xuôi dòng | Động mạch đùi nông cùng bên, động mạch tầng dưới gối |
Động mạch cánh tay | Thận, mạc treo, chậu |
Mạch khoeo ngược dòng | Đùi nông và chậu |
Mạch mu chân ngược dòng | Dưới khoeo, khoeo, đùi nông |
4.1 Đường vào động mạch đùi chung ngược dòng
Đây vẫn là đường vào phổ biến nhất trong can thiệp mạch chi dưới, nhờ đơn giản và dễ kiểm soát các biến cố. Đường vào động mạch đùi chung ngược dòng cho phép tiếp cận các tổn thương động mạch chậu (cùng bên và đối bên), tổn thương tầng đùi khoeo bên đối diện, và đôi khi cả tổnthương tầng dưới gối bên đối diện. Vì thế đường vào này cho phép thủ thuật viên can thiệp nhiều tầng mạch máu trong cùng một thì.
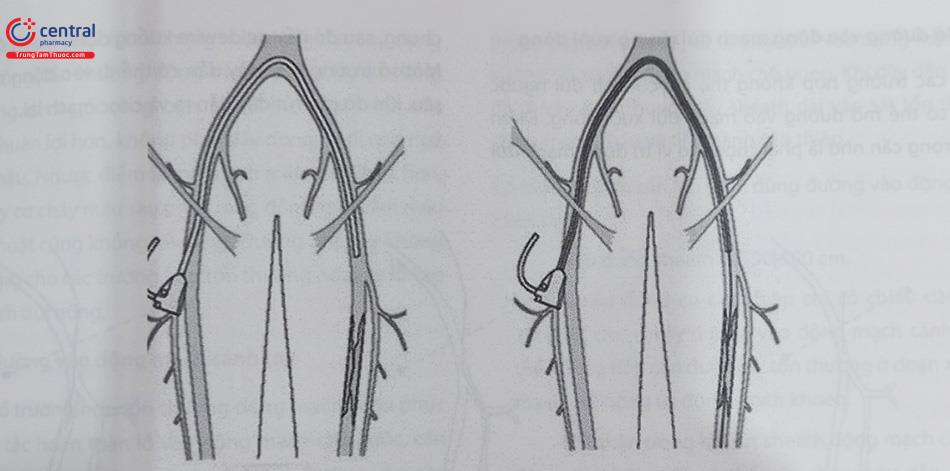
Một số trường hợp không nên hoặc không thể sử dụng đường vào động mạch đùi chung ngược dòng:
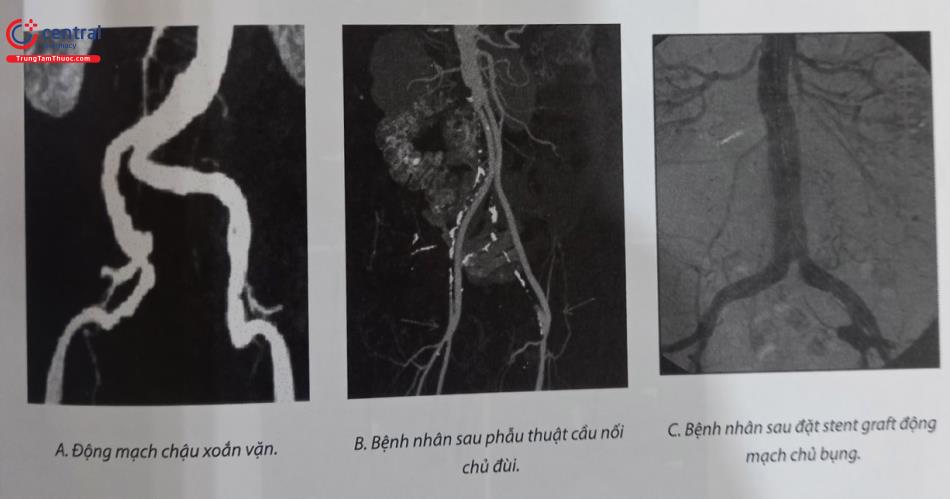
- Đặc điểm giải phẫu động mạch chậu không thuận lợi: góc tại ngã ba chủ chậu là góc nhọn, hoặc động mạch chậu xoắn vặn nhiều.
- Bệnh nhân đã phẫu thuật bắc cầu nối chủ – đùi.
- Bệnh nhân đặt stent graft động mạch chủ bụng – động mạch chậu.
- Bệnh nhân đã đặt stent động mạch chậu (cùng bên hoặc đối bên) nhô vào trong động mạch chủ bụng.
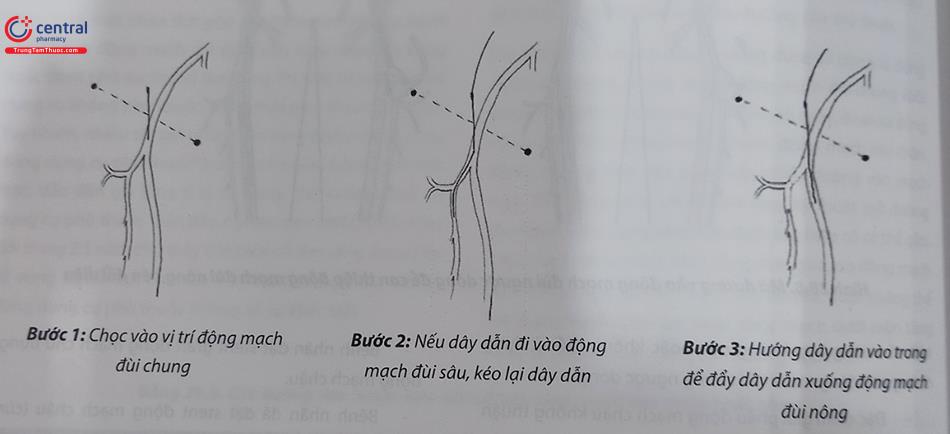
4.2 Mở đường vào động mạch đùi chung xuôi dòng
Trong các trường hợp không thể chọc mạch đùi ngược dòng, có thể mở đường vào mạch đùi xuôi dòng. Điểm quan trọng cần nhớ là phải chọc vào vị trí động mạch đùichung, sau đó đẩy guidewire xuống động mạch đùi nông. Một số trường hợp dây dẫn có thể đi vào động mạch đùi sâu. Khi đó cần rút dây dẫn ra và chọc mạch lại.
4.2.1
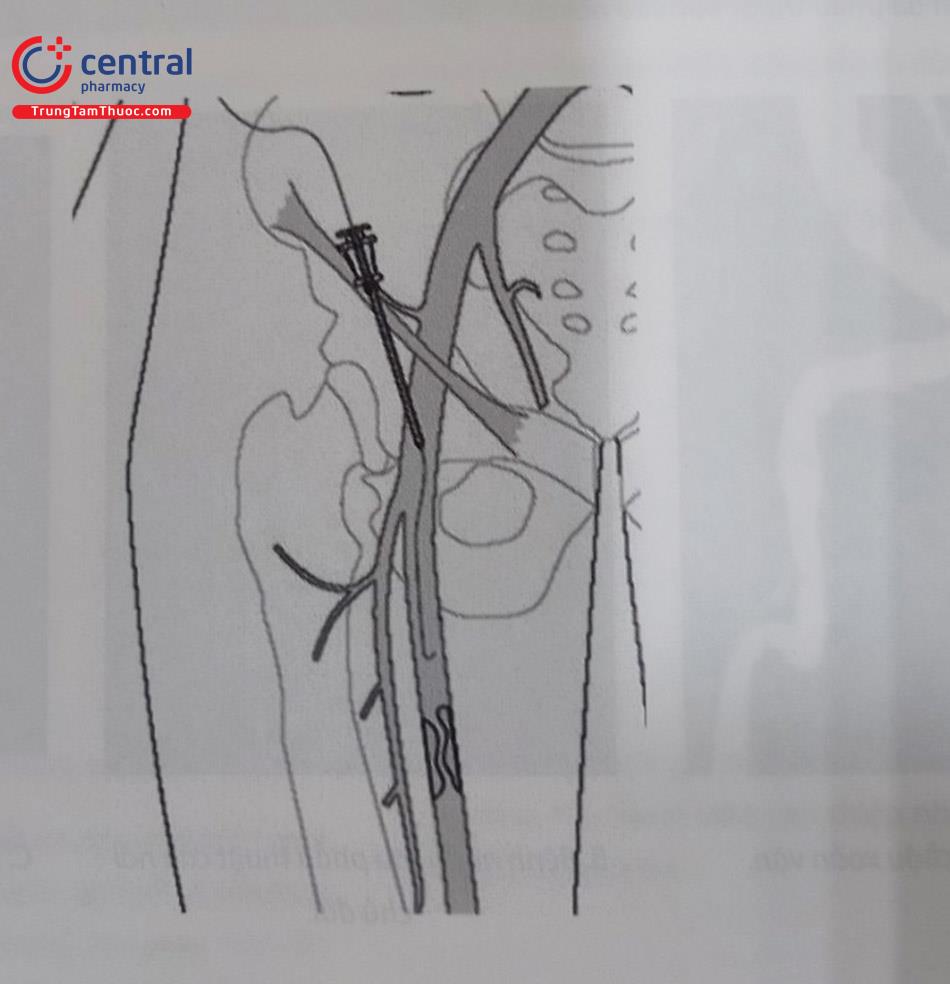
Đường vào động mạch đùi chung xuôi dòng được sử dụng để tái thông tổn thương động mạch đùi nông và động mạch tầng dưới gối cùng bên. Ưu điểm là tiếp cận tổn thương thuận lợi hơn, không phải đẩy dụng cụ đi qua ngã ba chủ chậu. Nhược điểm là mở mạch máu khó khăn hơn, tăng nguy cơ chảy máu sau phúc mạc, đồng thời cầm máu sau thủ thuật cũng không dễ dàng. Đường vào này không thể sử dụng cho các trường hợp tổn thương ngay từ lỗ vào động mạch đùi nông.
4.3 Mở đường vào động mạch cánh tay
Với một số trường hợp tổn thương động mạch chậu phức tạp, ví dụ tắc hoàn toàn lỗ vào động mạch chậu gốc, cần sử dụng đường vào động mạch cánh tay. Đường vào này cho phép dây dẫn can thiệp có thể tiếp cận trực tiếp tổn thương, tăng khả năng dây dẫn đi qua tổn thương.
Thường sử dụng đường vào động mạch cánh tay bên trái thay vì bên phải, do dụng cụ có thể dễ dàng đi xuống động mạch chủ bụng. Dây dẫn từ đường động mạch cánh tay có thể đi thẳng vào động mạch chủ lên. Khi đó, dùng ốngthông pigtail hoặc AL để lái dây dẫn vào động mạch chủ xuống, và xuống động mạch chủ bụng. Khi dây dẫn 0,035” đã đi vào ĐMC bụng, đẩy sheath dài vào sát tổn thương động mạch chậu và tiến hành can thiệp.
Có một số điểm cần lưu ý khi dùng đường vào động mạch cánh tay:
- Nên dùng sheath dài 90-100
- Nhiều dụng cụ can thiệp chỉ có chiều dài tối đa 120-135 cm, vì vậy đường vào động mạch cánh tay có thể không tiếp cận được các tổn thương ở đoạn xa động mạch đùi nông và động mạch
- Rất thận trọng khi rút sheath động mạch cánh Băng ép không đủ có thể gây chảy máu dẫn đến hội chứng khoang. Băng ép quá chặt sẽ gây tắc động mạch cánh tay do huyết khối.
- Không dùng dụng cụ đóng mạch chuyên dụng (Perclose, AngioSeal) với động mạch cánh tay, do động mạch cánh tay có kích cỡ nhỏ hơn động mạch đùi.
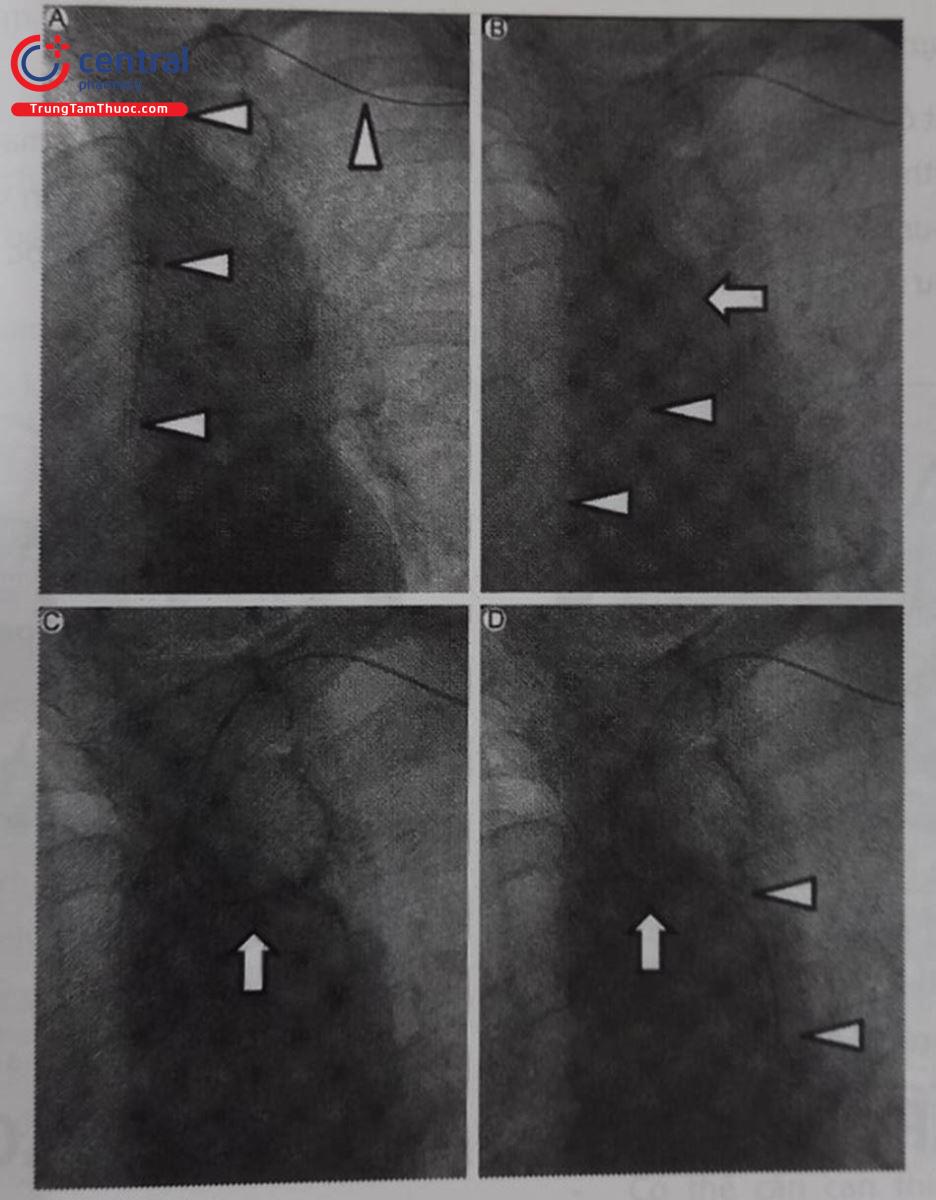
Chú thích: A. Dây dẫn từ động mạch cánh tay trái đi vào động mạch chủ (ĐMC) lên. B. Đẩy ống thông AL theo dây dẫn vào vị trí quai ĐMC. C. Rút dây dẫn về, ống thông AL hướng về phía ĐMC xuống. D. Đẩy dây dẫn qua ống thông để đi vào ĐMC xuống và ĐMC bụng.
5 Chụp mạch máu ngoại biên
Khác với động mạch vành di chuyển theo từng nhịp đập của tim, động mạch ngoại biên cố định chứ không di chuyển. Vì thế ưu tiên chụp mạch máu ngoại biên bằng chế độ chụp số hoá xoá nền (DSA), hơn là chế độ số hoá thông thường (DA). Chế độ DSA cung cấp hình ảnh với độ phân giải cao hơn và xoá bỏ các phần không liên quan đến mạch máu (xương, phần mềm), giúp bộc lộ tổn thương tốt hơn. Thường chụp DSA với tốc độ 5 hình một giây (5 fps) với tầng chủ chậu, 3 fps với tầng đùi khoeo, 1,5-2 fps với tầng dưới gối.
Nhược điểm của chế độ chụp DSA là không được phép di chuyển bàn trong lúc chụp, vì thế có thể cần nhiều cúp chụp liên tiếp để đánh giá một đoạn mạch dài (như động mạch đùi nông). Với bệnh nhân suy giảm chức năng thận, chuyển sang chế độ chụp DA để di chuyển bàn và đánh giá mạch máu với một lần chụp duy nhất. Thủ thuật viên cũng cần dặn người bệnh không di chuyển chân trong lúc chụp DSA.
5.1 Chụp động mạch chủ bụng không chọn lọc
Sau khi đặt sheath 4 – 6Fr, một ống thông pigtail được đưa vào vị trí ngang động mạch thận (khoảng mức đốt sống L1) để thực hiện chụp ĐMC bụng không chọn lọc. Ưu tiên dùng ống thông có lỗ bên như pigtail thay vì ống thông lỗ;tận (end-hole catheter), để giảm nguy cơ lóc tách và chấn thương mạch máu.
5.2 Chụp mạch máu chọn lọc
Chụp mạch chọn lọc là tiêm thuốc cản quang trực tiếp vào mạch máu cần quan sát qua ống thông. Lái ống thông chọn lọc vào mạch máu bị tổn thương. Trước khi bơm thuốc cản quang, đầu ống thông nên được di chuyển tự do và các sóng huyết động phải bình thường và cố định, tránh hiện tượng “tì đầu” gây tụt áp lực. Tiêm thuốc cản quang khi tụt sóng áp lực sẽ gây lóc tách mạch máu. Thao tác thiếu thận trọng với ống thông khi không có dây dẫn sẽ tăng nguy cơ tổn thương thành mạch.
Tương tự chụp động mạch vành, chụp chọn lọc mạch máu ngoại biên cũng đòi hỏi các góc chụp khác nhau để đánh giá chính xác tổn thương.
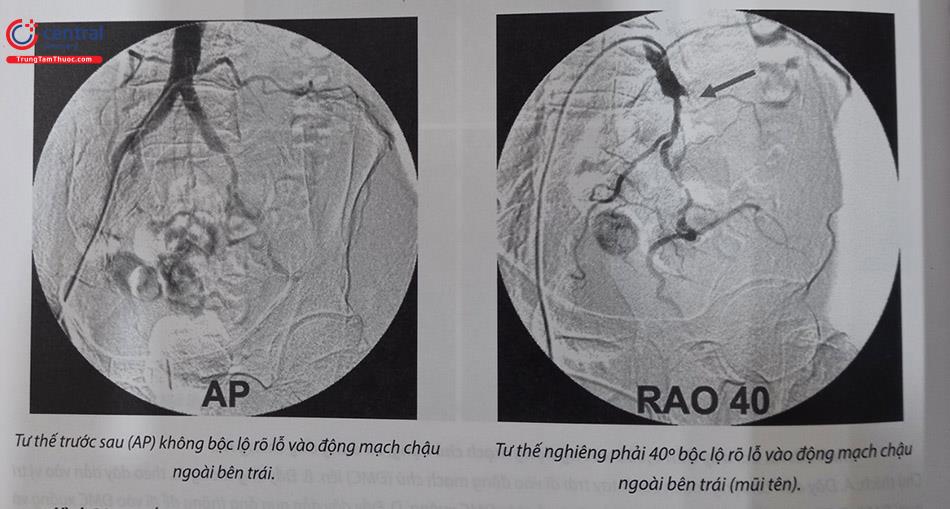
- Tổn thương ngã ba chủ chậu, gốc và thân động mạch chậu chung: góc chụp tư thế
- Tổn thương động mạch chậu ngoài: tư thế chếch 30º đối bên.
- Tổn thương động mạch đùi-khoeo: tư thế chếch 30-45º cùng bên.
- Tổn thương động mạch tầng dưới gối: tư thế chếch 30º cùng bên. Cần chọn góc chụp tách được 2 xương cẳng chân để có thể bộc lộ 3 nhánh động mạch dưới gối rõ nhất.
6 Can thiệp động mạch chậu
Can thiệp động mạch chậu không chỉ giúp cải thiện dòng máu đến chi dưới, mà còn có vai trò đảm bảo đường vào mạch máu để hỗ trợ điều trị các bệnh tim mạch, ví dụ như can thiệp động mạch vành qua đường động mạch đùi, đặt bóng đối xung động mạch chủ, đặt stent graft động mạch chủ .
Tái thông nội mạch động mạch chậu cho kết quả dài hạn tương đương với phẫu thuật, và cần cân nhắc lựa chọn biện pháp điều trị dựa trên đặc điểm giải phẫu của tổn thương (phân loại TASC II), cũng như tình trạng lâm sàng của người bệnh.
Đối với bệnh nhân có chỉ định can thiệp động mạch chậu, nên đánh giá kỹ giải phẫu tổn thương bằng MSCT, để dự kiến đường vào mạch máu và có chiến lược can thiệp tối ưu, cũng như những dụng cụ có thể cần sử dụng trong thủ thuật.
6.1 Chỉ định
Chỉ định can thiệp động mạch chậu cho các bệnh nhân đau cách hồi với những đặc điểm giải phẫu phù hợp theo khuyến cáo của ESC 2017.
Bảng 28.10. Các khuyến cáo điều trị tổn thương động mạch chậu theo ESC 2017.
KHUYẾN CÁO CAN THIỆP TÁI TƯỚI MÁU TỔN THƯƠNG HẸP TẮC TẦNG CHỦ – CHẬU |
LOẠI | MỨC ĐỘ BẰNG CHỨNG |
|---|---|---|
Chiến lược can thiệp nội mạch được chỉ định đầu tay cho các tổn thương hẹp ngắn (< 5 cm) |
I |
C |
Bệnh nhân phù hợp với phẫu thuật, bắc cầu nối chủ đùi nên được xem xét trong tắc chủ – chậu |
IIa |
B |
Chiến lược can thiệp nội mạch nên được xem xét đầu tiên trong các tổn thương dài và/hoặc 2 bên ở bệnh nhân có nhiều bệnh phối hợp kèm theo |
IIa |
B |
Can thiệp nội mạch có thể xem xét đầu tiên cho tổn thương tắc chủ chậu, nếu tiến hành bởi đội ngũ có kinh nghiệm và các lựa chọn phẫu thuật không thích hợp |
IIb |
B |
6.2 Đường vào mạch máu
6.2.1 Động mạch đùi chung cùng bên ngược dòng
Mở đường vào ngược dòng động mạch đùi chung cùng bên là đường tiếp cận tốt nhất để tái thông động mạch chậu chung và chậu ngoài. Ưu điểm của hướng tiếp cận này là dễ thao tác, có thể áp dụng cho cả các trường hợp tắc ngay lỗ vào động mạch chậu gốc. Tuy nhiên, đường vào mạch máu này có 3 nhược điểm chính:
- Mạch chậu hẹp/tắc nên động mạch đùi nảy yếu hoặc không bắt được, mở đường vào mạch máu khó khăn.
- Các trường hợp tổn thương lan xuống động mạch chậu ngoài, sau khi đặt sheath động mạch đùi sẽ không đủ vùng đệm (landing zone) để nong bóng hay đặt stent.
- Nếu trong quá trình can thiệp gây bóc tách mạch máu, có thể bóc tách lan lên động mạch chủ bụng.
6.2.2 Động mạch đùi chung đối bên ngược dòng
Đi từ động mạch đùi bên đối diện là hướng tiếp cận an toàn và đơn giản hơn. Đường vào này cũng giúp thủ thuật viên có thể can thiệp động mạch chậu và động mạch đùi đối bên trong cùng một thì. Nếu quá trình can thiệp có gây bóc tách mạch máu, cũng là bóc tách xuống động mạch đùi nông và ít gây ảnh hưởng đến động mạch chủ bụng.
Các hạn chế của đường vào mạch đùi đối bên bao gồm:
- Có thể cần can thiệp cả hai động mạch chậu cùng lúc
- Không phải lúc nào cũng dễ dàng đẩy dụng cụ (sheath dài, bóng, stent) qua ngã ba chủ chậu. Điều này đặc biệtquan trọng trong những ca can thiệp đòi hỏi dụng cụ kích cỡ lớn, như stent có màng bọc
- Khó can thiệp trong những trường hợp tắc ngay tại lỗ vào động mạch chậu gốc
KHUYẾN CÁO | LOẠI | MỨC ĐỘ BẰNG CHỨNG |
|---|---|---|
Trong trường hợp thiếu máu chi mạn tính đe dọa, việc tái tưới máu dưới khoeo được chỉ định để cứu vãn chi. |
I |
A |
Bắc cầu dùng tĩnh mạch hiển lớn được chỉ định để tái thông mạch máu tầng dưới gối |
I |
A |
Can thiệp nội mạch nên được cân nhắc để tái thông mạch máu tầng dưới gối |
IIa |
B |
6.2.3 Động mạch chi trên
Chọn đường vào động mạch cánh tay hoặc động mạch quay trong trường hợp tắc hoàn toàn mạn tính gốc động mạch chậu (xem ca lâm sàng hình 28.15). Đường vào động mạch cánh tay thường dùng hơn động mạch quay nhờ hai đặc điểm. Thứ nhất, động mạch cánh tay lớn hơn nên có thể dùng sheath cỡ 7F hay 8F. Thứ hai, với bệnh nhân thân hình cao, đường vào động mạch quay đôi khi sẽ không đủ để tiếp cận tổn thương, do dụng cụ không đủ dài.
6.2.4 Phối hợp nhiều đường tiếp cận tổn thương
Đôi khi cần phối hợp nhiều đường vào, như động mạch đùi chung cả hai bên, động mạch đùi và động mạch cánh tay, để hình ảnh chụp mạch rõ nét nhất và để tạo thuận lợi cho cả đường xuôi dòng và ngược dòng bắt chéo, giúp quan sát rõ hơn vị trí tắc nghẽn.
6.3 Quy trình can thiệp động mạch chậu
6.3.1 Sheath
Cân nhắc sử dụng sheath dài hơn (23-30 cm) đối với tổn thương động mạch chậu chung để quan sát tổn thương, đồng thời đưa bóng và stent vào vùng có cấu trúc giải phẫu khá phức tạp.
Kích thước sheath phụ thuộc vào kích cỡ mạch máu can thiệp. Nhiều stent đường kính lớn (9-10 mm) đòi hỏi sheath 7Fr. Tất cả các ca can thiệp động mạch chậu đều tiềm tàng nguy cơ thủng mạch máu dẫn tới tử vong trong vài phút do sốc mất máu, vì thế cần chuẩn bị sẵn sàng cho trường hợp phải sử dụng stent có màng bọc. Chọn sheath đủ lớn để có thể đưa stent có màng bọc vào vùng can thiệp, ví dụ stent có màng bọc đường kính 10 mm cần sheath 9-10Fr.
6.3.2 Dây dẫn
Ưu tiên sử dụng dây dẫn kích cỡ 0,035” với các tổn thương động mạch chậu. Có thể dùng dây dẫn đầu thẳng hoặc đầu cong. Dây dẫn đầu thẳng có khả năng đâm xuyên tốt hơn nhưng lại khó đi qua các tổn thương gập góc, xoắn vặn.
Có thể sử dụng dây dẫn nhỏ hơn (0,018; 0,014 inch), với ưu điểm ít gây sang chấn mạch máu. Nhưng thường cácdây dẫn này khá mềm và yếu, vì thế không tạo ra đủ hỗ trợ cần thiết để đi qua tổn thương, khi qua tổn thương rồi cũng khó đẩy bóng và stent. Do vậy, sau khi lái dây dẫn qua tổn thương, tráo dây dẫn siêu cứng 0,035 inch (Supracore, Lunderquist, hoặc Amplatz) để đẩy dụng cụ dễ dàng hơn.
6.3.3 Nong bóng
Nong tổn thương bằng bóng có đường kính bằng đoạn mạch tham chiếu hoặc sử dụng áp lực thấp nhất có thể để bóng nở hoàn toàn. Đánh giá kết quả nong bóng bằng cách chụp mạch máu qua ống thông hoặc qua sheath. Luôn nhớ rằng nong bóng sẽ tiềm ẩn nguy cơ vỡ mạch chậu, vì thế không nên bơm bóng áp lực quá cao. Tốt nhất dùng bóng có kích thước nhỏ hơn đường kính đoạn mạch tham chiếu.
6.3.4 Đặt stent
Đặt stent được chỉ định cho đa số các trường hợp can thiệp động mạch chậu, do nong bóng có tỉ lệ hẹp tồn lưu cao, hoặc gây lóc tách mạch máu gây hạn chế lưu lượng dòng chảy. Ưu tiên lựa chọn stent nở bằng bóng khi cần phải đặt stent chính xác (tổn thương tại vị trí lỗ vào động mạch chậu gốc). Stent tự nở được lựa chọn nếu không cần thiết phải đặt chính xác, hoặc mạch máu có kích thước không đồng đều. Với đặc điểm xoắn vặn của động mạch chậu (đặc biệt là động mạch chậu ngoài), stent tự nở nitinol sẽ linh hoạt và phù hợp hơn. Khi đặt stent tự nở, thường chọn stent có kích thước lớn hơn kích thước mạch ít nhất là 1-2 mm. Ở những trường hợp nguy cơ thủng hoặc vỡ mạch cao (hẹp vôi hóa/tắc hoàn toàn mạn tính), chủ động lựa chọn stent có màng bọc để đảm bảo an toàn tối đa.
Đối với stent nở bằng bóng (có hoặc không có màng bọc), khung stent có thể rơi ra khỏi bóng do mắc phải đoạn mạch vôi hoá hoặc tổn thương phức tạp. Để tránh biến cố này, nên sử dụng sheath động mạch đủ dài để vượt qua vùng tổn thương, tránh biến dạng stent. Khi stent đã đi qua tổn thương, rút sheath lại rồi bơm thuốc cản quang để khẳng định stent đã nằm đúng vị trí.
Có thể nong lại bằng bóng áp lực cao nếu stent chưa giãn nở hoàn toàn. Cần lưu ý rằng không nhất thiết phải có hình ảnh chụp mạch hoàn hảo, hẹp tồn dư dưới 30% với chênh áp qua tổn thương < 5 mmHg là kết quả chấp nhận được. Nong bóng quá tích cực với kỳ vọng có hình ảnh tối ưu sẽ đối mặt với nguy cơ vỡ mạch chậu cao.
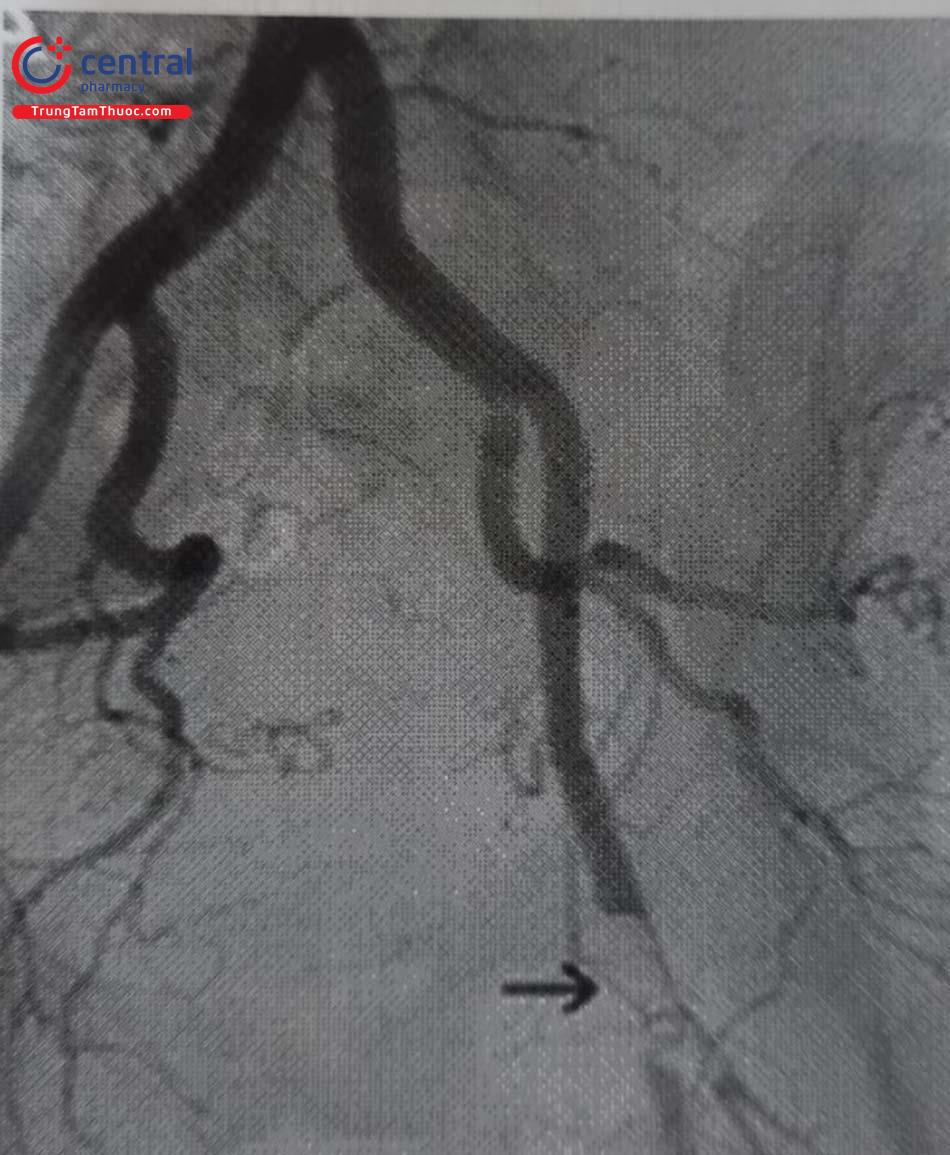
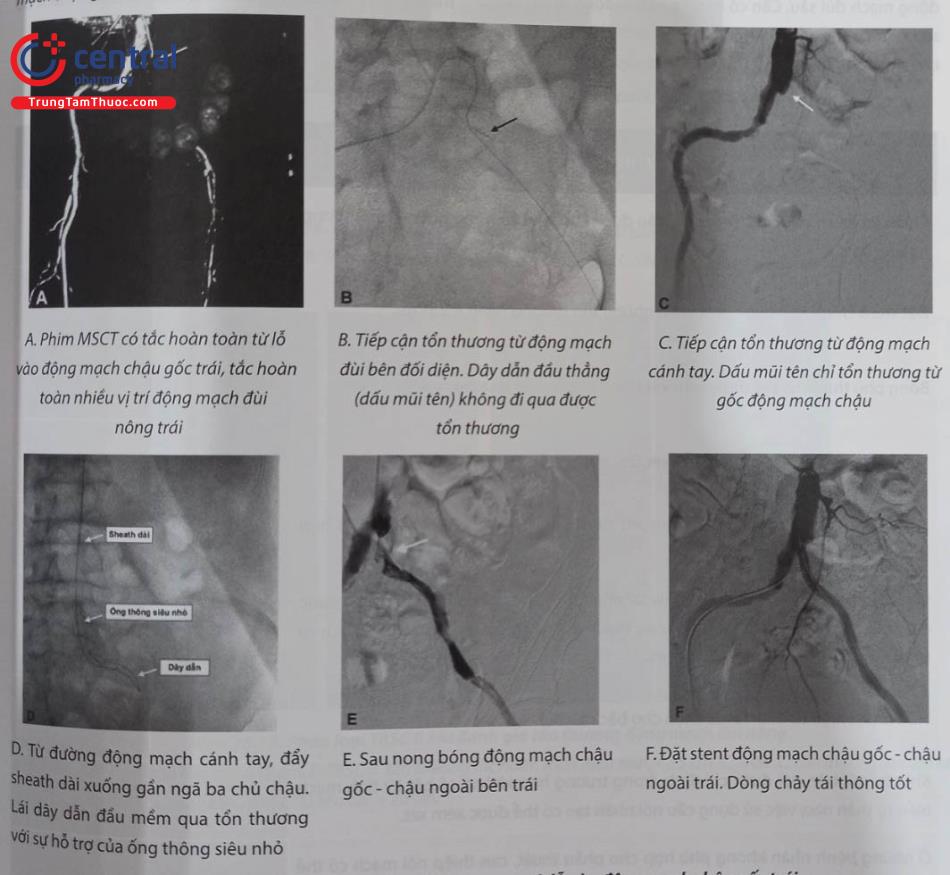
.jpg)
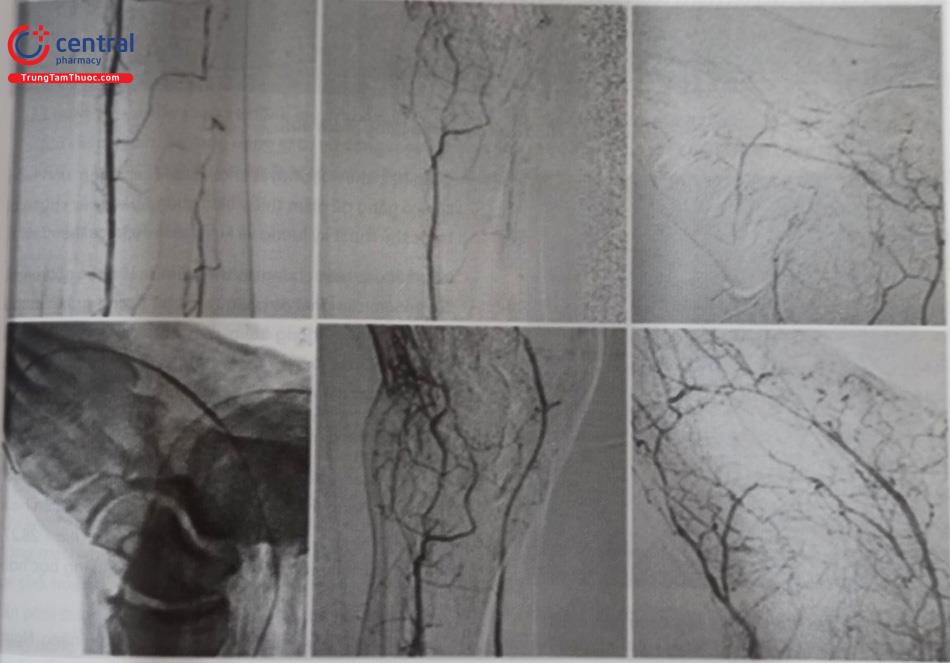
(Hình A: Mũi tên chỉ hình ảnh tắc hoàn toàn động mạch chậu gốc bên trái. Hình B: Hình ảnh sau can thiệp tái tưới máu động mạch chậu gốc – chậu ngoài bên trái)
7 Can thiệp động mạch tầng đùi - khoeo
7.1 Can thiệp động mạch đùi chung
Động mạch đùi chung chạy qua dây chằng bẹn và bị đè ép khá nhiều. Động tác gập khớp háng cũng dễ gây biến dạng nếu đặt stent vùng này. Vì vậy, động mạch đùi chung được coi là vùng “không đặt stent”. Biện pháp tái tưới máu thường được lựa chọn là phẫu thuật bóc nội mạc động mạch đùi chung, hoặc phẫu thuật làm cầu nối. Tuy nhiên, tái thông nội mạch vẫn có thể được thực hiện bằng nhiều kĩ thuật không stent: khoan cắt mảng xơ vữa, nong bóng động mạch đùi chung.
Thành phần quan trọng của động mạch đùi chung là gốc động mạch đùi sâu. Cần cố gắng bảo tồn động mạch đùi sâu nếu có thể, vì tuy không phải nhánh chính cấp máu cho chi dưới, nhưng nó thường cung cấp hệ thống tuần hoàn bàng hệ phong phú trong trường hợp động mạch đùi nông bị tắc. Không nên sử dụng kỹ thuật tái thông dưới nội mạc khi lái dây dẫn qua tổn thương động mạch đùi chung, do nguy cơ bóc tách mạch máu làm giảm tưới máu động mạch đùi sâu.
7.2 Can thiệp động mạch đùi nông – động mạch khoeo
7.2.1 Tổng quan
Can thiệp nội mạch đối với tổn thương động mạch tầng đùi khoeo có tỉ lệ thành công cao (khoảng 95%), đồng thời tỉ lệ biến cố rất thấp, vì thế được chỉ định rộng rãi cho các bệnh nhân hẹp, tắc mạch máu tầng đùi khoeo. Về mặt giải phẫu, động mạch đùi nông chạy từ trước ra sau, nó chịu nhiều lực tác động do có nhiều đoạn gập dưới cơ, vì thế stent tự nở bằng nitinol được ưu tiên hơn stent nở bằng bóng.
Bảng 28.11. Các khuyến cáo điều trị tổn thương tầng đùi khoeo theo ESC 2017
| CÁC KHUYẾN CÁO | LOẠI | MỨC ĐỘ BẰNG CHỨNG |
|---|---|---|
| Chiến lược can thiệp nội mạch thì đầu được khuyến cáo trong những tổn thương ngắn < 25 cm. | I | C |
| Đặt stent chính nên được xem xét ở những tổn thương ngắn < 25 cm. | IIa | A |
| Bóng phủ thuốc có thể được xem xét trong những tổn thương ngắn < 25 cm. | IIa | A |
| Stent phủ thuốc có thể được xem xét cho những tổn thương ngắn < 25 cm. | IIb | B |
| Bóng phủ thuốc có thể được xem xét để điều trị những trường hợp tái hẹp trong stent. | IIb | B |
| Ở những bệnh nhân không có nguy cơ phẫu thuật cao, phẫu thuật bắc cầu được chỉ định cho những tổn thương động mạch đùi nông dài ≥ 25 cm, tĩnh mạch tự thân sẵn có và kỳ vọng sống > 2 năm. | I | B |
| Tĩnh mạch hiển tự thân là lựa chọn cho bắc cầu đùi – khoeo. | I | A |
| Khi cầu nối trên gối được chỉ định, trong trường hợp không có bất kỳ tĩnh mạch hiển tự thân nào, việc sử dụng cầu nối nhân tạo có thể được xem xét. | IIa | A |
| Ở những bệnh nhân không phù hợp cho phẫu thuật, can thiệp nội mạch có thể xem xét ở những tổn thương dài ≥ 25 cm. | IIb | C |
7.2.2 Quy trình kỹ thuật
- Chụp động mạch đùi
- Sau khi mở đường vào mạch máu, ống thông được đưa vào động mạch đùi chung bên tổn thương để chụp chọn lọc mạch máu. Phim chụp mạch phải đảm bảo đánh giá được lỗ vào động mạch đùi nông, mức độ hẹp, tắc mạch máu, cũng như tình trạng tưới máu của hệ mạch đoạn xa.
- Khi chụp mạch máu, có thể đặt một thước cản quang để ước tính chiều dài đoạn mạch tổn thương.
- Nếu tầng dưới gối chỉ còn duy nhất một mạch máu còn thông, cần sử dụng lưới lọc trước khi can thiệp động mạch đùi nông, do quá trình nong bóng có thể làm huyết khối hay mảng xơ vữa trôi xuống gây tắc mạch đoạn xa.
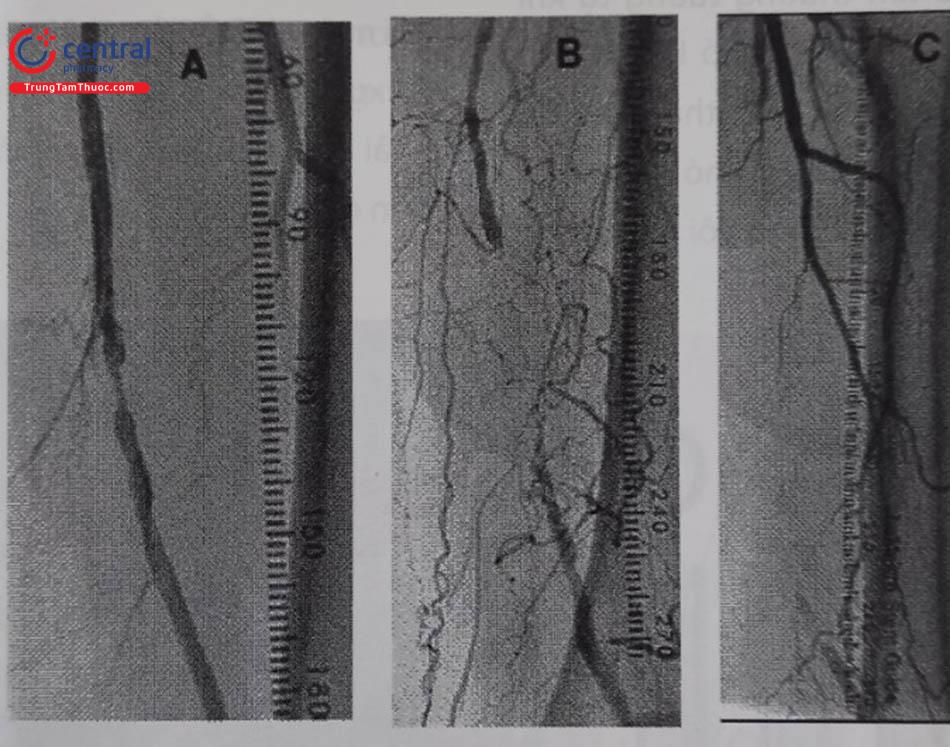
Hình A: Hẹp trên đoạn dài 3 mm; Hình B: Tắc hoàn toàn trên đoạn dài 7 cm; Hình C: Tắc hoàn toàn trên đoạn dài 16 cm
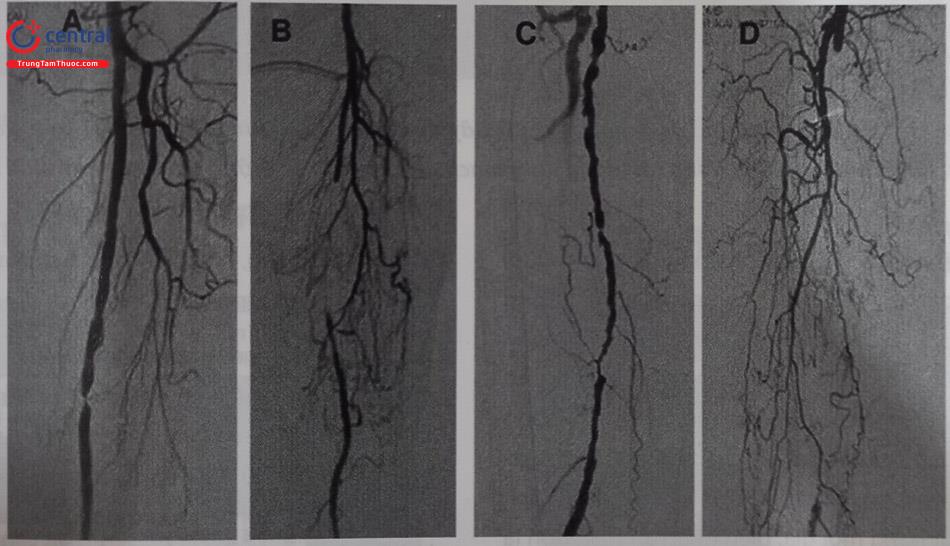
A: TASC A, tổn thương khu trú, < 10 cm. B: TASC B, tổn thương tắc hoàn toàn mạn tính, < 15 cm. C: TASC C, tổn thương lan toả kéo dài > 15 cm. D: TASC D, tổn thương CTO kéo dài > 20 cm.
- Đưa dây dẫn qua tổn thương
- Dây dẫn can thiệp động mạch đùi nông có thể dùng loại 0,018” hoặc 0,035”. Tốt nhất là dùng dây dẫn ngậm nước (hydrophilic). Có hai kỹ thuật chính để đưa dây dẫn qua tổn thương động mạch đùi nông là tái thông trong lòng mạch và tái thông dưới nội mạc.
- Ưu tiên sử dụng kỹ thuật lái guidewire trong lòng mạch trước. Guidewire được đẩy qua tổn thương tương tự khi can thiệp động mạch vành. Ưu điểm của nó là bảo tồn mạch máu và các nhánh bên, ít gây bóc tách thành mạch. Tuy nhiên, kỹ thuật này có thể gặp nhiều khó khăn nếu tổn thương tắc nghẽn lâu ngày, tổn thương vôi hoá, đồng thời tăng nguy cơ bong mảng xơ vữa và huyết khối gây tắc mạch đoạn xa.
- Biện pháp thay thế khi kỹ thuật tái thông trong lòng mạch thất bại là tái thông dưới nội mạc. Chỉ dùng kỹ thuật can thiệp dưới nội mạc nếu như đoạn xa mạch máu còn lành lặn. Dây dẫn (thường là loại 0,035”) được uốn cong đầu sẽ đi vào lớp dưới nội mạc, qua tổn thương tắc nghẽn, rồi quay trở lại lòng thật ở đoạn lành. Mặc dù can thiệp dưới nội mạc có thể giảm thời gian tiến hành thủ thuật, nó cũng có xu hướng gây bóc tách lan toả động mạch, hệ quả là phải đặt stent kéo dài dù tổn thương ban đầu chỉ khu trú trên đoạn ngắn.
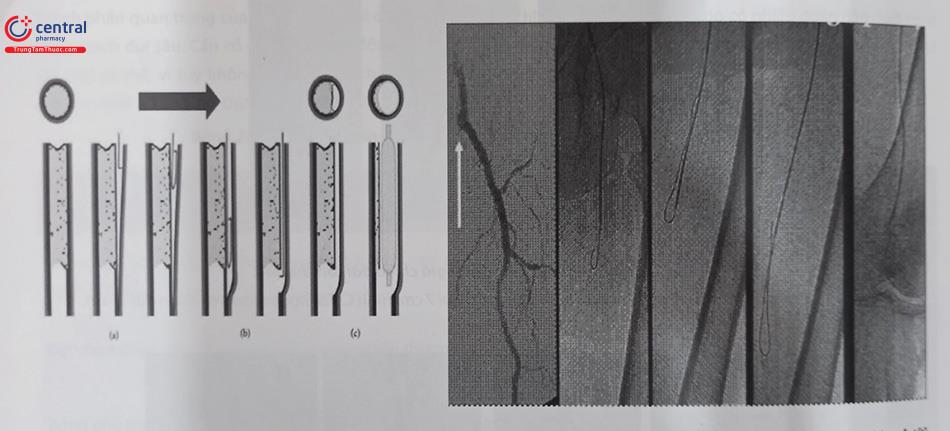
- Một vấn đề kỹ thuật có thể gặp phải khi tái thông dưới nội mạc là dây dẫn từ lòng giả không quay lại được lòng thật, đặc biệt trong các trường hợp động mạch đùi nông vôi hoá nhiều. Để tránh bóc tách mạch máu lan rộng, cố gắng giữ cho vòng cong của dây dẫn nhỏ. Tuyệt đối không nong bóng nếu chưa khẳng định chắc chắn dây dẫn đã nằm trong lòng thật hay chưa. Thay vì cố gắng tìm cách quay lại lòng thật bằng mọi giá, biện pháp an toàn hơn là mở đường vào động mạch đùi nông đoạn xa.
– Mở đường vào động mạch đùi nông đoạn xa
- Đây không phải đường tiếp cận thường quy để tái thông động mạch đùi nông. Tuy nhiên, nếu tiếp cận xuôi dòng không thành công, hoặc gây bóc tách mạch máu kéo dài, có thể cần mở đường vào động mạch đùi nông đoạn xa.
- Chọc động mạch đùi nông đoạn trong ống Hunter khi bệnh nhân ở tư thế nằm ngửa, với sự hỗ trợ của siêu âm Doppler hoặc màn huỳnh quang tăng sáng. Dùng kim chọc mạch kích cỡ 21G, chiều dài 10-15 cm. Quay C-arm ở tư thế 30-45º đối bên tổn thương. Sau đó từ từ đưa kim chọc mạch qua da, đảm bảo kim đồng trục với mạch máu. Khi kim đi qua da và lớp mô dưới da, quay C-arm sang góc 30-45º cùng bên tổn thương, đưa kim hướng về phía động mạch đùi nông cho đến khi thấy máu đi ra. Đẩy một dây dẫn 0,018” qua kim vào lòng mạch.
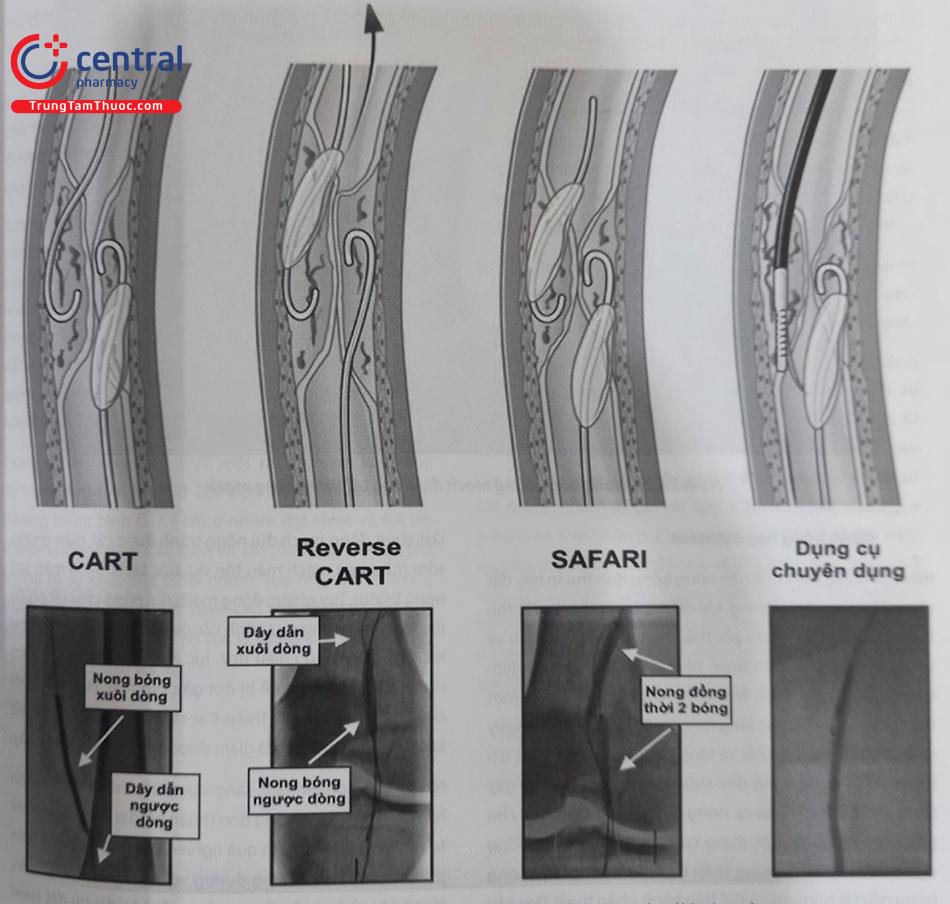
- Sau khi đưa guidewire 0,018” vào lòng mạch đoạn xa, có thể tái thông bằng kỹ thuật CART (Controlled Antegrade and Retrograde Subintimal Tracking: tái thông dưới nội mạc xuôi dòng và ngược dòng có kiểm soát). Thủ thuật viên sẽ đưa bóng nong xuôi chiều xuống đến tổn thương, nong rộng lòng giả, tạo thông thương giữa đoạn gần và đoạn xa mạch máu, qua đó đẩy dây dẫn ngược dòng vào lòng thật ở đoạn gần động mạch đùi nông.
- Một biến thể khác của CART là Reverse CART. Thay vì nong bóng xuôi dòng, bác sĩ can thiệp đẩy bóng qua đường mở;mạch đùi ngược dòng, nong lòng giả tạo thông thương đầu, rồi đẩy dân dẫn từ đầu gần xuống mạch đoạn xa. Hoặc có thể nong đồng thời cả xuôi dòng lẫn ngược dòng (kỹ thuật SAFARI).
- Giải pháp cuối cùng là dùng dụng cụ ống thông chuyên dụng để lái dây dẫn từ lòng giả quay lại lòng thật. Tuy nhiên, những ống thông này (ví dụ Outback Catheter) có chi phí khá cao và tỉ lệ thành công chỉ ở mức trung bình.
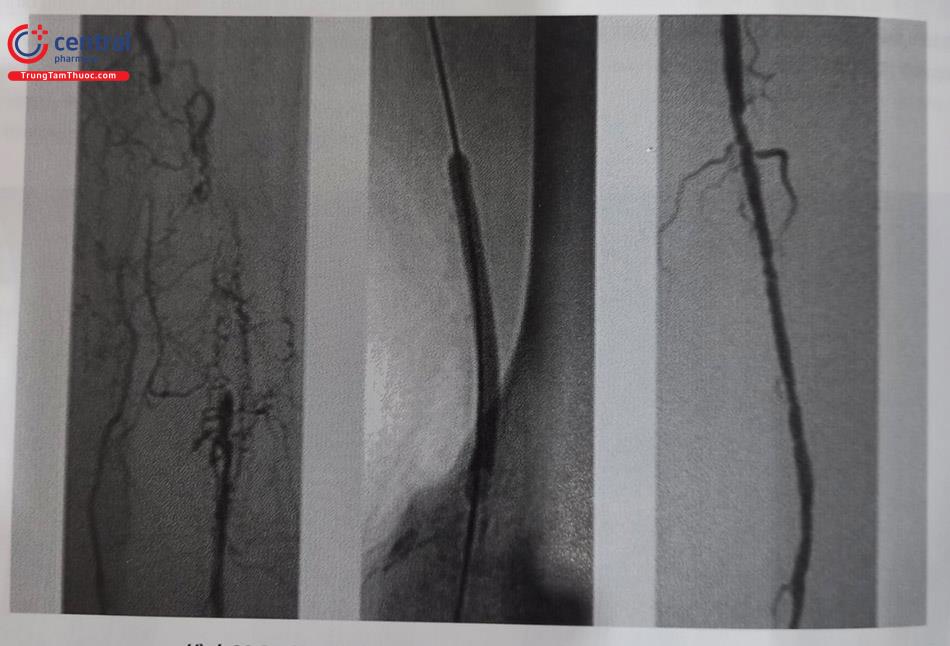
– Nong bóng
Sau khi đưa dây dẫn qua tổn thương, tiến hành nong bóng tạo hình động mạch đùi nông. Bóng nong là loại bóng áp lực cao (non-compliant balloon), áp lực bơm bóng có thể tăng lên rất cao mà kích cỡ bóng không nở ra quá nhiều. Lựa chọn độ lớn của bóng dựa theo kích cỡ lòng mạch tham chiếu đoạn xa, kích cỡ bóng thường bằng 80% kích cỡ mạch máu. Để tránh vỡ mạch, không nên lựa chọn bóng quá lớn hay bơm bóng áp lực quá cao. Bơm bóng quá căng cũng có thể làm vỡ bóng, hậu quả là gây tắc mạch đoạn xa do khí hoặc các thành phần của bóng trôi xuống. Cần bơm bóng với thời gian đủ dài (tối thiểu 60 giây), đảm bảo bóng nở căng hoàn toàn.
- Nong bóng hay đặt stent
Vẫn còn nhiều tranh cãi nên nong bóng đơn thuần hay đặt stent động mạch đùi nông. Ưu điểm của nong bóng là thủ thuật đơn giản và có chi phí thấp hơn. Nong bóng bảo vệ các nhánh bên và tuần hoàn bàng hệ trong khi vẫn đảm bảo tưới máu chi dưới. Nó cũng tránh việc phải đặt một dụng cụ ngoại lai trong lòng mạch máu, qua đó giảm nguy cơ hình thành huyết khối và tăng sản lớp nội mạc. Một ích lợi khác của nong bóng đơn thuần là tránh tình trạng gãy stent ở vùng đùi. Ngoài ra, nong bóng động mạch đùi cho phép can thiệp với các dụng cụ kích cỡ nhỏ (4Fr), đồng nghĩa với tỉ lệ biến chứng thấp hơn. Cuối cùng, sau nong bóng nếu tái hẹp vẫn có thể tiến hành phẫu thuật làm cầu nối hoặc can thiệp qua da, điều không dễ thực hiện nếu có stent động mạch đùi.
Đặt stent động mạch đùi nông tránh được các biến chứng sớm (như hẹp mạch máu tồn dư, bóc tách mạch máu sau nong bóng). Tuy nhiên, động mạch đùi nông chịu rất nhiều lực tác động trong quá trình các cơ vùng đùi làm việc, như lực kéo giãn theo chiều dọc, lực ép, lực xoắn vặn, lực co rút,… dẫn đến stent dễ bị đứt gãy, nứt mắt. Hậu quả cuối cùng là tái hẹp sau can thiệp. Các stent thế hệ mới, với thiết kế và vật liệu tốt hơn, đã giảm được một phần nguy cơ này.
Nhiều thử nghiệm lâm sàng được tiến hành để so sánh hiệu quả của nong bóng đơn thuần với đặt stent (loại stent tự nở bằng nitinol). Kết quả nghiên cứu cho thấy, hai biện pháp có hiệu quả tương đương với các tổn thương ngắn, trong khi những tổn thương hẹp tắc kéo dài thì đặt stent ưu việt hơn.
Nghiên cứu FAST so sánh đặt stent và nong bóng ở 244 bệnh nhân có đau cách hồi. Chiều dài tổn thương trung bình là 4,4 cm ở nhóm đặt stent và 4,5 cm ở nhóm nong bóng. Tỉ lệ tử vong, tỉ lệ cắt cụt chi, thay đổi phân độ Rutherford, ở hai nhóm ngang bằng nhau. Tỉ lệ tái hẹp ở nhóm nong bóng có xu hướng cao hơn nhóm đặt stent (38,6% so với 31,7%), tuy nhiên khác biệt chưa có ý nghĩa thống kê. Ở cả hai nhóm đều có sự cải thiện về quãng đường đi bộ tối đa cũng như chỉ số ABI, và sự cải thiện này được duy trì bền vững sau 12 tháng .
Một phân tích gộp của Kasapis và cộng sự, đánh giá 10 thử nghiệm lâm sàng, trong đó 724 trường hợp được đặt stent thường quy (chiều dài tổn thương trung bình 4,6 cm) và 718 trường hợp được nong bóng, chỉ đặt stent nếu có bóc tách mạch máu (chiều dài tổn thương trung bình 4,3 cm) cho thấy tỉ lệ cần phải tái can thiệp sau 24 tháng là tương đương nhau ở cả hai nhóm (20% ở nhóm đặt stent thường quy; 20,2% ở nhóm nong bóng, p = 0,89).
Schillinger tiến hành so sánh nong bóng với đặt stent ở 104 bệnh nhân có đau cách hồi nặng. Chiều dài tổn thương trung bình là 13,2 cm ở nhóm đặt stent, so với 12,7 cm ở nhóm nong bóng. Sau 12 tháng, tỉ lệ tái hẹp trên siêu âm Doppler ở nhóm nong bóng cao hơn đáng kể so với nhóm đặt stent (63% so với 37%, p = 0,01). Tại thời điểm 12 tháng, quãng đường đi bộ tối đa ở nhóm nong bóng cũng ngắn hơn đáng kể (267 m, so với 387 m, p = 0,04).
Trong nghiên cứu RESILIENT, một thử nghiệm lâm sàng đa trung tâm tiến hành ở 206 bệnh nhân, chiều dài tổn thương trung bình là 7,7 cm ở nhóm đặt stent và 6,4 cm ở nhóm nong bóng. Các biến cố lớn (tử vong, cắt cụt chi) không có sự khác biệt ở hai nhóm. Tuy nhiên, tỉ lệ thông mạch máu của nhóm đặt stent cao hơn đáng kể, tại thời điểm sau 6 tháng (94,2% so với 47,4%; p < 0,0001) và sau 12 tháng (81,3% so với 36,7%).
Các tiến bộ về công nghệ cho phép stent động mạch tầng đùi khoeo chịu được áp lực xoắn vặn lớn hơn, đồng thời cải thiện tỉ lệ tái hẹp sau đặt stent. Hiện tại, đặt stent là biện pháp được ưu tiên cho các trường hợp tắc động mạch đùi nông.
– Vai trò của bóng phủ thuốc và stent phủ thuốc
Nghiên cứu PACIFIER so sánh bóng phủ paclitaxel IN.PACT Pacific với bóng thường ở các bệnh nhân tổn thương động mạch đùi nông chiều dài trung bình 6,6-7,0 cm. Kết quả theo dõi cho thấy sau 12 tháng: bóng phủ thuốc có tỉ lệ tái hẹp thấp hơn (8,6% so với 32,4%, p = 0,01), cũng như tỉ lệ biến cố đích (tử vong, cắt cụt chi, tái can thiệp) thấp hơn (7,1% so với 27,9%, p = 0,02).
Thử nghiệm THUNDER chứng minh bóng phủ thuốc làm giảm đáng kể tỉ lệ phải tái can thiệp trong 5 năm khi so với bóng thường (21% so với 56%, p = 0,0005), đồng thời không làm tăng nguy cơ tổn thương thành mạch do thuốc (xơ hoá, phình mạch). Bóng phủ thuốc cũng được chứng minh hiệu quả trong các trường hợp tái hẹp trong stent.
Tại Viện Tim mạch Việt Nam, nghiên cứu của Đinh Huỳnh Linh và cộng sự cho thấy tỉ lệ tái hẹp sau nong bóng phủ thuốc động mạch đùi nông là 28% sau 12 tháng theo dõi.
Thử nghiệm SIROCCO được tiến hành trên 93 bệnh nhân tổn thương động mạch đùi TASC C. Trong đó 46 bệnh nhân được đặt stent thường (stent SMART) và 47 bệnh nhân được đặt stent phủ sirolimus. Kết quả theo dõi sau 24 tháng cho thấy, nhóm đặt stent phủ thuốc có ABI trung bình 0,96 (so với 0,87 ở nhóm stent thường, p 0,05) và tỉ lệ tái hẹp 22,9% (so với 21,1% ở nhóm stent thường, p > 0,05). Tỉ lệ tử vong và cần phải tái thông mạch máu ở hai nhóm cũng tương đương nhau. Thử nghiệm SIROCCO cho thấy trong thời gian 24 tháng, stent phủ thuốc sirolimus chưa chứng minh được ưu điểm khi so sánh với stent thường.
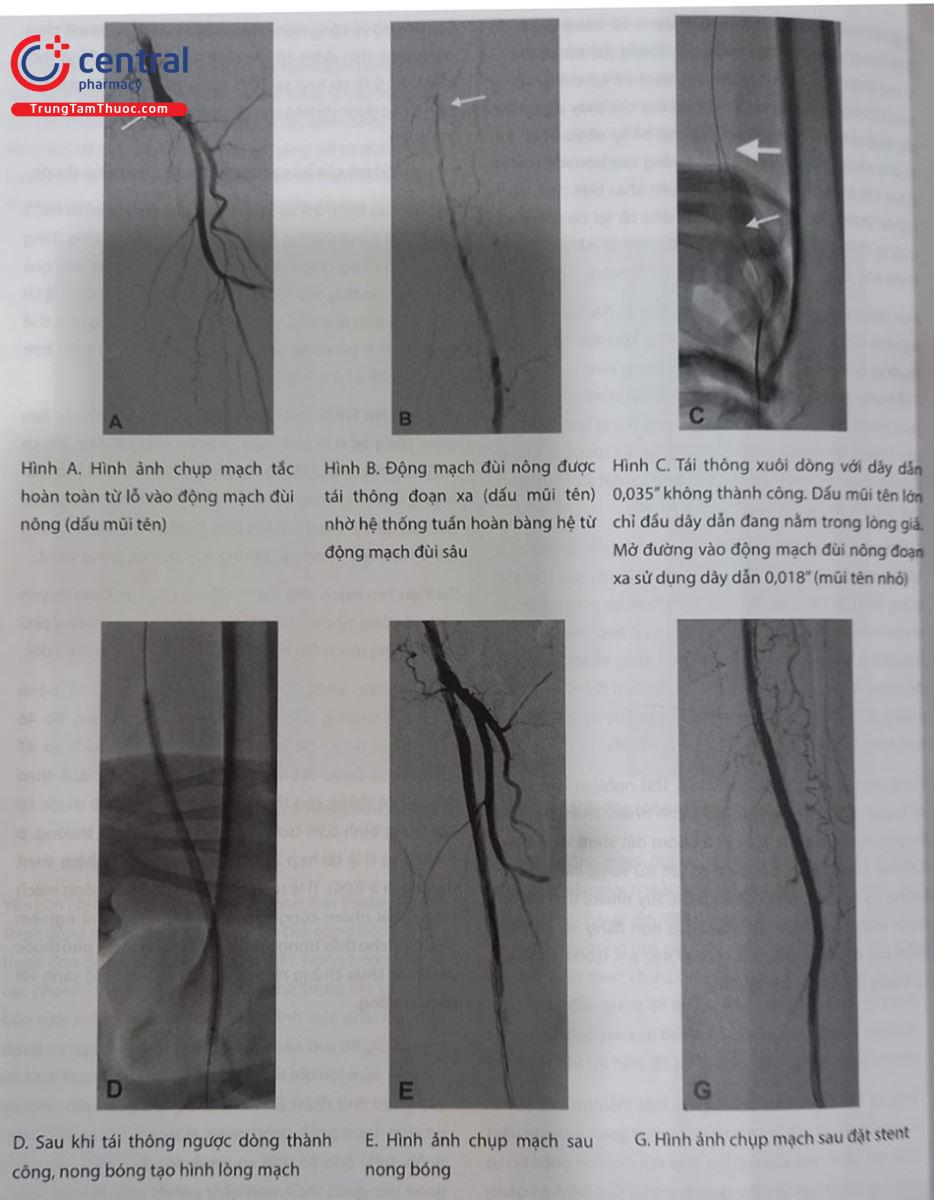
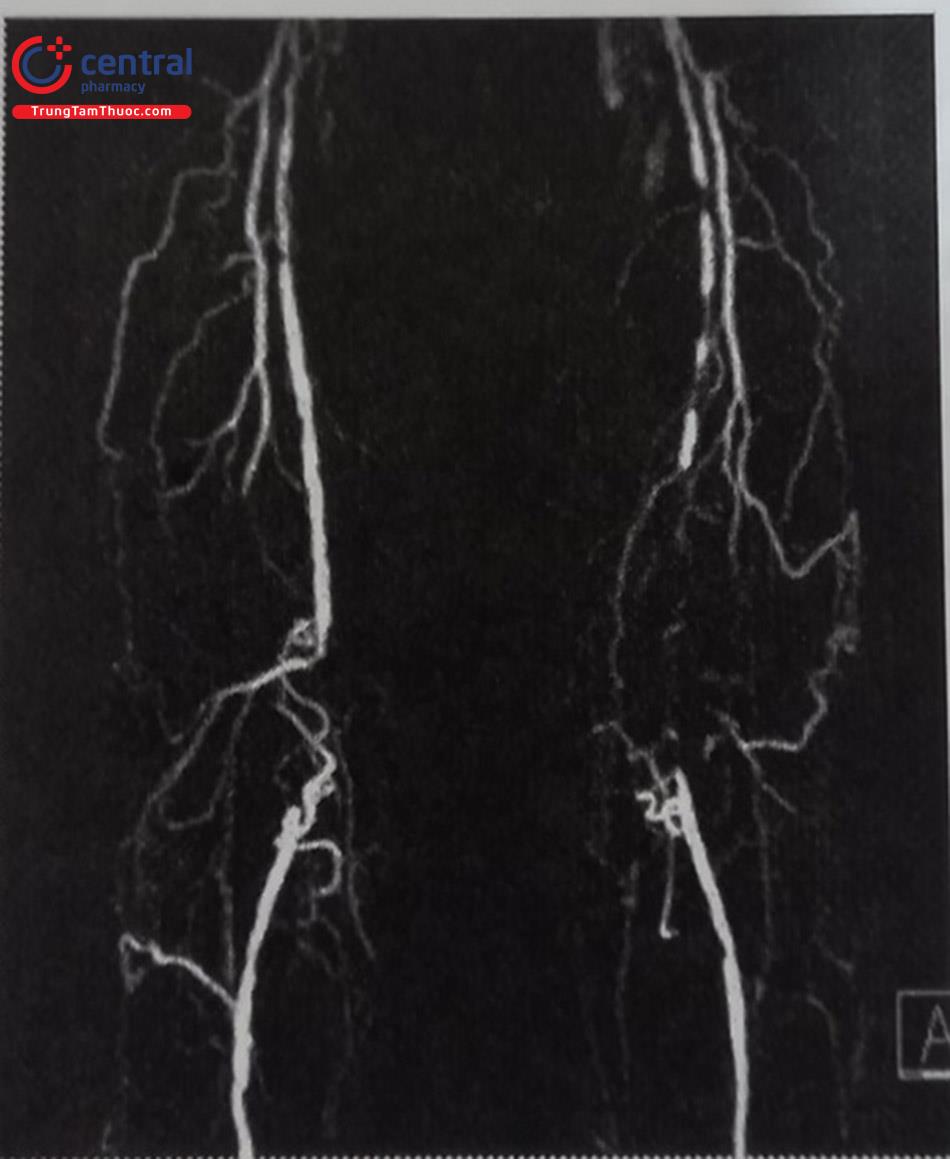
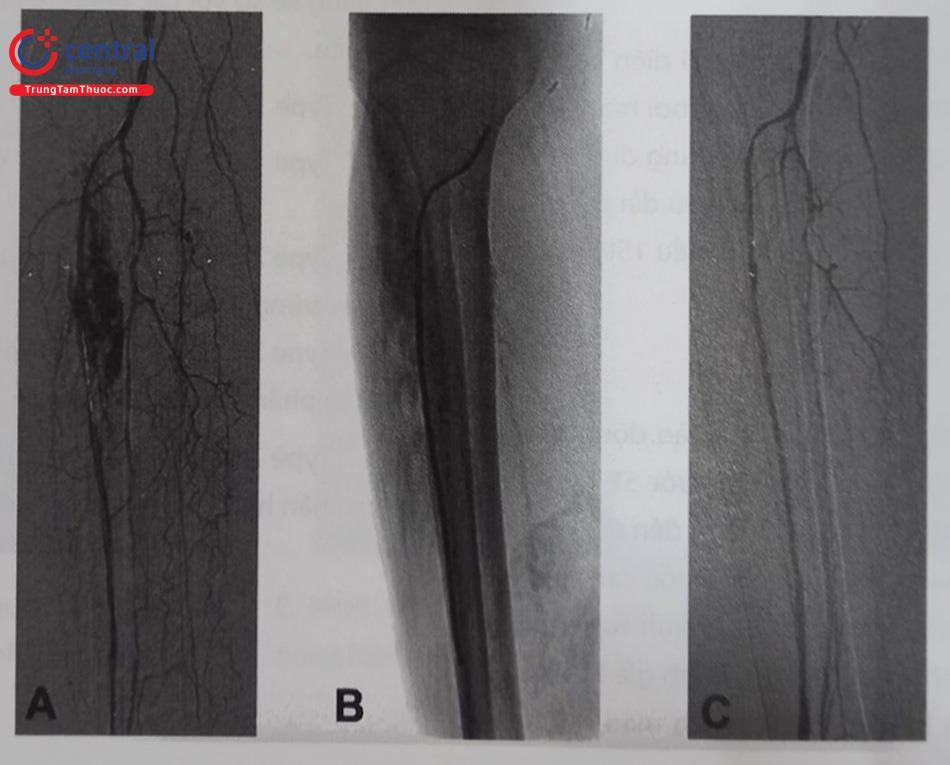
Hình A. Hình ảnh chụp mạch tắc hoàn toàn từ lỗ vào động mạch đùi nông (dấu mũi tên)
Hình B. Động mạch đùi nông được tái thông đoạn xa (dấu mũi tên) nhờ hệ thống tuần hoàn bàng hệ từ động mạch đùi sâu
Hình C. Tái thông xuôi dòng với dây dẫn 0,035” không thành công. Dấu mũi tên lớn chỉ đầu dây dẫn đang nằm trong lòng giả. Mở đường vào động mạch đùi nông đoạn xa sử dụng dây dẫn 0,018” (mũi tên nhỏ)
8 Can thiệp động mạch tầng dưới gối
8.1 Tổng quan
Động mạch tầng dưới gối thường là các mạch máu nhỏ, với tổn thương lan toả, phức tạp. Những mạch máu này có kích thước tương tự như mạch vành, ngoại trừ chiều dài dài hơn. Với tổn thương tầng dưới gối, can thiệp nội mạch đặc biệt có ý nghĩa khi không thấy dòng chảy đoạn xa ở gan chân và mu chân (do đó không thể phẫu thuật làm cầu nối). Những tiến bộ về kỹ thuật và công nghệ, như mở đường vào ngược dòng (động mạch mu chân, đoạn xa động mạch chày sau), các thiết bị cấu hình nhỏ của thời đại mạch vành, hoàn toàn có thể can thiệp các mạch máu tầng dưới gối một cách hiệu quả.
Mặc dù can thiệp mạch máu tầng dưới gối có tỉ lệ tái hẹp và tái can thiệp cao, lợi ích giảm cắt cụt chi của can thiệp nội mạch tương đương phẫu thuật làm cầu nối.
Bảng 28.12. Khuyến cáo điều trị tổn thương tầng dưới gối (theo ESC 2017)
| Khuyến cáo | Loại | Mức độ bằng chứng |
|---|---|---|
| Trong trường hợp thiếu máu chi mạn tính đe dọa, việc tái tưới máu dưới khoeo được chỉ định để cứu vãn chi | I | A |
| Bắc caafu dùng tĩnh mạch hiển lớn được chỉ định để tái thông mạch máu tầng dưới gối | I | A |
| Can thiệp nội mạch nên được cân nhắc để tái thông mạch máu tầng dưới gối | IIa | B |
8.2 Quy trình kỹ thuật
8.2.1 Đường vào mạch máu
Ưu tiên đường vào động mạch đùi chung cùng bên (mở mạch xuôi dòng), giúp tiếp cận gần như trực tiếp với các mạch máu dưới khoeo.
Đường vào động mạch đùi chung bên đối diện cũng có lợi, đặc biệt là khi dự định tái thông đồng thời mạch chậu hoặc động mạch tầng đùi khoeo. Khi sử dụng đường vào bên đối diện, thủ thuật viên cần lưu ý chiều dài dụng cụ. Ống thông và bóng cần có chiều dài tối thiểu 150 cm mới đủ để tới được các mạch máu dưới khoeo.
8.2.2 Chụp mạch máu
Dây dẫn đầu mềm 0,035 inch được đưa vào động mạch khoeo đoạn xa. Sau đó ống thông kích thước 5F hoặc 6F hoặc sheath dài được đưa vào qua dây dẫn đến đoạn giữa hoặc đoạn xa động mạch khoeo. Bơm thuốc cản quang qua ống thông hoặc sheath để đánh giá tình trạng hẹp, tắc mạch máu. Hình ảnh chụp DSA cần đánh giá kỹ lưỡng dòng chảy đoạn xa và hiện hình các mạch máu dưới cổ chân và cung gan chân.
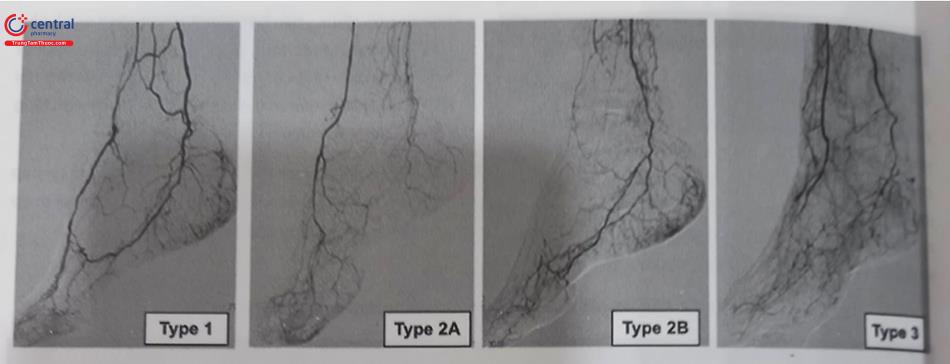
Dựa vào hình ảnh cung gan chân và cung mu chân, chia ra 3 type tổn thương mạch máu bàn chân. Tình trạng bảo tồn cung mạch bàn chân là một yếu tố tiên lượng tốt sau can thiệp tái tưới máu tầng dưới gối, với tỉ lệ thông mạch máu và cải thiện triệu chứng lâm sàng, giảm tỉ lệ cắt cụt chi, tốt hơn đáng kể so với các bệnh nhân không còn cung mạch bàn chân.
- Type 1: Cung mạch bàn chân còn bảo tồn tốt.
- Type 2: Cung mạch bàn chân được bảo tồn một phần.
- Type 2A: Còn mạch máu phần mu chân, mất mạch máu vùng gan chân.
- Type 2B: Còn mạch máu phần gan chân, mất mạch máu phần mu chân.
- Type 3: Không còn cung mạch bàn chân. Cấp máu bàn chân hoàn toàn qua hệ thống tuần hoàn bàng hệ.
8.2.3 Dây dẫn can thiệp
Dây dẫn can thiệp thường sử dụng kích cỡ 0,014” hoặc 0,018”. Do lợi thế đường tiếp cận xuôi dòng, có thể sử dụng dây dẫn chuyên dùng cho can thiệp CTO, với chiều dài 180 cm. Để tăng độ đâm xuyên của dây dẫn, sử dụng ống thông siêu nhỏ (micro-catheter) có kích cỡ tương ứng. Ưu tiên dùng kỹ thuật tái thông trong lòng mạch để tránh gây thủng mạch máu.
8.2.4 Nong bóng và đặt stent
Bóng nong có kích thước tương đương với đoạn mạch tham chiếu. Bóng thường được bơm bằng áp lực 6-8 atm hoặc để bóng nở hoàn toàn. Bơm nhiều lần, với thời gian với thời gian bơm bóng lâu (2-3 phút) để mạch máu giãn nở tốt. Các mạch máu tầng dưới gối thường co thắt nhiều, có thể tiêm Nitroglycerin nhiều lần qua ống thông. Một số trường hợp hẹp tồn lưu nhiều, lóc tách mạch máu cần đặt stent nếu tổn thương ở đoạn gần mạch máu.
Tương tự can thiệp các mạch máu khác, nong bóng động mạch tầng dưới gối cũng có thể gây vỡ mạch máu. Biến cố này đặc biệt nguy hiểm nếu không được phát hiện và xử trí kịp thời, vì tình trạng chảy máu nặng có thể gây hội chứng khoang vùng cẳng chân. Nếu phát hiện thoát thuốc cản quang ra ngoài lòng mạch, bơm bóng chèn khoảng 5-10 phút thường là đủ để cầm máu
Mặc dù kết quả nong mạch về lâu dài khá hạn chế nhưng vẫn còn đủ cấp máu để làm lành vết thương. Mục đích chính của tái thông mạch là hỗ trợ quá trình liền thương, tạo thuận lợi cho quá trình cắt lọc chi nếu cần thiết. Khi tình trạng thiếu máu chi được cải thiện, các liệu pháp vận động sẽ giúp phát triển hệ thống tuần hoàn bàng hệ cấp máu cho bàn chân.
Một phương pháp điều trị khác là đặt stent phủ thuốc (DES), sử dụng stent dùng cho động mạch vành. Một số nghiên cứu đã chứng minh lợi ích của loại stent này với bệnh lý mạch dưới khoeo thiếu máu cục bộ, lóc tách gây hạn chế dòng máu, và/ hoặc tắc nghẽn đột ngột. Khi đặt stent vào các động mạch dưới khoeo, bệnh nhân sẽ được điều trị bằng clopidogrel, liều nạp 300-600 mg khi kết thúc thủ thuật, sau đó liều 75 mg/ngày trong ít nhất 4 tuần.
9 Biến chứng của can thiệp động mạch chi dưới.
Các biến chứng thường gặp như các thủ thuật can thiệp mạch khác. Các biến chứng có thể xảy ra trong quá trình làm thủ thuật hoặc sau thủ thuật.
9.1 Biến chứng liên quan đường vào mạch máu
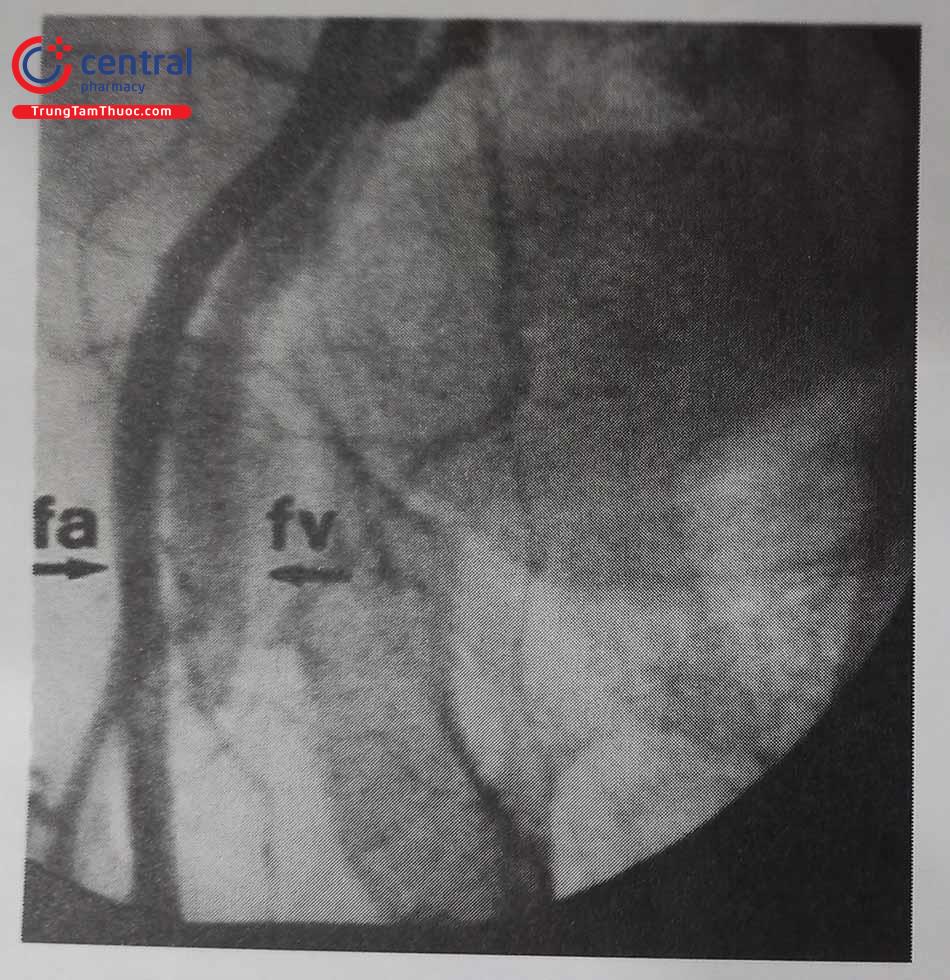
Biến chứng do đường vào bao gồm chấn thương động mạch đường vào (lóc tách, thủng mạch) dẫn tới chảy máu sau phúc mạc, giả phình mạch đùi hoặc tạo ra thông động tĩnh mạch(Xem thêm chương 10).

9.2 Biến chứng liên quan quá trình tiến hành thủ thuật
Nong bóng có nguy cơ gây biến chứng tại vị trí nong bao gồm lóc tách, thủng mạch và tắc mạch (do xơ vữa, vật chất dạng hạt, khí, hoặc huyết khối). Bác sĩ can thiệp luôn luôn cần cố gắng để giảm thiểu biến chứng bằng các chuẩn bị trước thủ thuật kỹ lưỡng và kiểm soát dụng cụ thật tỉ mỉ.
Hầu hết các biến chứng có thể kiểm soát được nội mạch. Tuy nhiên, cần phải có phẫu thuật hỗ trợ trong bất kì thủ thuật nào nếu không kiểm soát được biến chứng bằng đường nội mạch hoặc có hội chứng khoang kèm theo cần phải mở cân.
9.2.1 Thủng mạch máu
Phần lớn các trường hợp thủng mạch máu (động mạch đùi nông, động mạch dưới gối) do dây dẫn sẽ tự liền hoặc dùng bóng gây chèn ép vị trí thủng (xem hình 28.27). Với các lỗ thủng lớn, có thể dùng stent có màng bọc hoặc bít coil.
Thủng hay vỡ động mạch chậu là biến chứng nặng. Người bệnh có thể sốc mất máu nhanh. Xử trí cấp cứu bằng bơm bóng chèn trên động mạch chủ, bơm bóng tại chỗ gây bít tắc chỗ thủng, bù máu và dung dịch cao phân tử. Sau đó đặt stent có màng bọc tại vị trí thủng mạch máu.
9.2.2 Tắc mạch do huyết khối
Mọi bước của quá trình tái thông mạch máu chi dưới đều có thể gây bong mảng xơ vữa và huyết khối, dẫn đến tắc mạch đoạn xa. Tuy nhiên, phần lớn các trường hợp không ảnh hưởng đến tình trạng tưới máu chi đoạn xa và không biểu hiện triệu chứng lâm sàng. Các trường hợp dễ gây tắc mạch đoạn xa là: tổn thương huyết khối, tổn thương tắc hoàn toàn mạn tính, mảng xơ vữa giàu lipid.
Đánh giá nguy cơ tắc mạch đoạn xa bằng chụp mạch máu kỹ càng trước và sau thủ thuật, hiện hình rõ dòng chảy hệ động mạch mu chân và gan chân. Huyết khối hình thành tại chỗ hoặc do biến chứng làm tắc dòng chảy đoạn xa cần phải được điều trị khẩn trương. Có thể hút huyết khối bằng dụng cụ, hoặc bơm thuốc tiêu sợi huyết vào đoạn xa. Một lựa chọn điều trị huyết khối khác đó là nong bóng áp lực thấp và/ hoặc đặt stent để ép cục đông sang bên cạnh lòng mạch và phục hồi dòng chảy. Các kỹ thuật này tương tự với kỹ thuật sử dụng trong phục hồi tuần hoàn mạch vành.
10 Điều trị bệnh nhân sau can thiệp
Các thăm dò cần tiến hành sau thủ thuật bao gồm đo chỉ số huyết áp cổ chân – cánh tay (ABI) và làm siêu âm Doppler mạch máu. Theo dõi cẩn thận vị trí đường vào để dự phòng khối máu tụ và/ hoặc chảy máu sau phúc mạc.
Bệnh nhân cần được dùng thuốc kháng tiểu cầu kép (aspirin và clopidogrel) tối thiểu 1 tháng sau can thiệp, sau đó dùng aspirin liều thấp (75-100 mg) suốt đời. Nếu nguy cơ chảy máu thấp, bổ sung rivaroxaban liều thấp (2,5 mg x 2 viên/ngày) cùng với thuốc kháng kết tập tiểu cầu đã được chứng minh giảm tỉ lệ cắt cụt chi và tái can thiệp sau khi tái tưới máu động mạch chi dưới. Thời điểm dùng rivaroxaban thường là trong vòng 7 ngày sau khi tiến hành can thiệp nội mạch.
Bệnh nhân bệnh động mạch chi dưới thường có nhiều yếu tố nguy cơ xơ vữa mạch máu, kèm theo tổn thương hẹp tắc mạch các vị trí khác (mạch vành, mạch cảnh, mạch tạng), do đó cần điều trị dự phòng thứ phát các biến cố tim mạch chung. Các biện pháp điều trị khác bao gồm liệu pháp statin và thay đổi lối sống (bỏ thuốc lá tuyệt đối, thay đổi chế độ ăn, tập đi bộ, giảm các yếu tố nguy cơ). Những biện pháp này không chỉ giúp giảm tỉ lệ tái hẹp sau can thiệp tái tưới máu, mà còn giảm nguy cơ tim mạch tổng thể cho người bệnh.
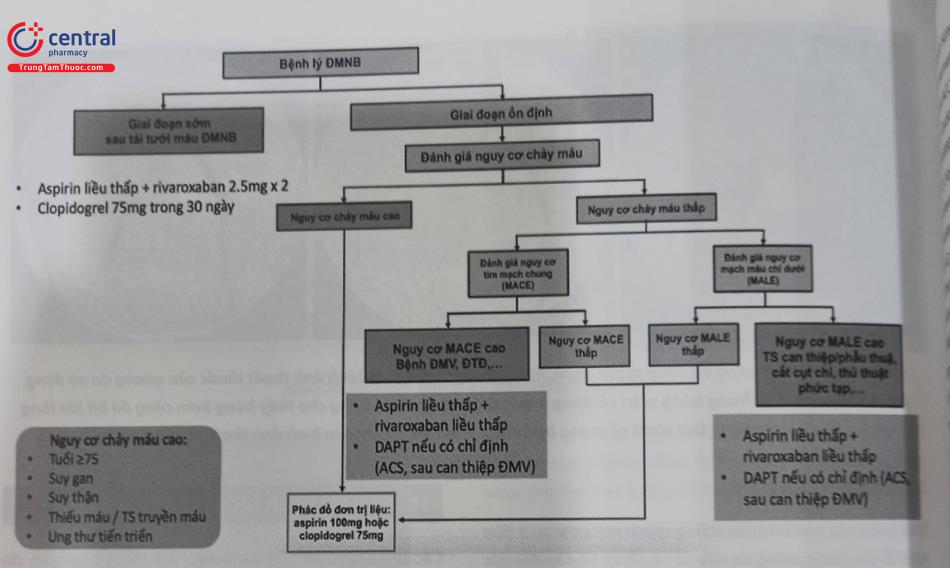
Chú thích: ĐMNB: Động mạch ngoại biên; DAPT (Dual Antiplatelet Therapy): Liệu pháp kháng kết tập tiểu cầu kép; ACS (Acute Coronary Syndrome): Hội chứng vành cấp; ĐMV: Động mạch vành; ĐTĐ: Đái tháo đường; TS: Tiền sử.
11 Tài liệu tham khảo
- Phạm Mạnh Hùng và Bệnh động mạch ngoại biên. Lâm sàng Tim Mạch. Nhà xuất bản Y học 2019.
- Gerhard-Herman MD, Gornik HL, Barrett C, Barshes NR, Corriere MA, Drachman DE, Fleisher LA, Fowkes FG, Hamburg NM, Kinlay S, et 2016 AHA/ACC guideline on the management of patients with lower extremity peripheral artery disease: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. Circulation. 2017;135:e726–e779. doi: 10.1161/CIR.0000000000000471 Crossref. PubMed.
- Hirsch AT, Criqui MH, Treat-Jacobson D, Regensteiner JG, Creager MA, Olin JW, Krook SH, Hunninghake DB, Comerota AJ, Walsh ME, et al. Peripheral arterial disease detection, awareness, and treatment in primary JAMA. 2001;286:1317–1324. doi: 10.1001/jama.286.11.1317 Crossref. PubMed.
- Pradhan AD, Aday AW, Beckman JA. The Big MAC attack on peripheral artery disease. Circulation. 2020;141:1211–1213. doi: 10.1161/ CIRCULATIONAHA.120.045627 Crossref.
- Creager MA, Belkin M, Bluth EI, Casey DE, Chaturvedi S, Dake MD, Fleg JL, Hirsch AT, Jaff MR, Kern JA, et al. 2012 ACCF/AHA/ACR/SCAI/ SIR/STS/SVM/SVN/SVS key data elements and definitions for peripheral atherosclerotic vascular disease: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Clinical Data Standards (Writing Committee to Develop Clinical Data Standards for Peripheral Atherosclerotic Vascular Disease). Circulation. 2012;125:395–467. doi: 10.1161/CIR.0b013e31823299a1
- McDermott MM. Lower extremity manifestations of peripheral artery disease: the pathophysiologic and functional implications of leg ischemia. Circ Res. 2015;116:1540–1550. doi: 10.1161/CIRCRESAHA.114.303517 Crossref.
- Fowkes FG, Rudan D, Rudan I, Aboyans V, Denenberg JO, McDermott MM, Norman PE, Sampson UK, Williams LJ, Mensah GA, et al. Comparison of global estimates of prevalence and risk factors for peripheral artery disease in 2000 and 2010: a systematic review and analysis. Lancet. 2013;382:1329–1340. doi: 10.1016/S0140-6736(13)61249-0 Crossref.
- Song P, Fang Z, Wang H, Cai Y, Rahimi K, Zhu Y, Fowkes FGR, Fowkes FJI, Rudan I. Global and regional prevalence, burden, and risk factors for carotid atherosclerosis: a systematic review, meta-analysis, and modelling study. Lancet Glob Health. 2020;8:e721–e729. doi: 10.1016/ S2214-109X(20)30117-0 Crossref.
- Conte MS, Bradbury AW, Kolh P, White JV, Dick F, Fitridge R, Mills JL, Ricco JB, Suresh KR, Murad MH; GVG Writing Group. Global vascular guidelines on the management of chronic limb-threatening ischemia. J Vasc Surg. 2019;69(6S):3S–125S.e40. doi: 10.1016/j.jvs.2019.02.016 Crossref.
- Mustapha JA, Katzen BT, Neville RF, Lookstein RA, Zeller T, Miller LE, Driver VR, Jaff MR. Critical limb ischemia: a threat to life and limb. Endovasc 2019;18:80–82.
- Aboyans V, Ricco JB, Bartelink MEL, Björck M, Brodmann M, Cohnert T, Collet JP, Czerny M, De Carlo M, Debus S, et al; ESC Scientific Document Group. 2017 ESC guidelines on the diagnosis and treatment of peripheral arterial diseases, in collaboration with the European Society for Vascular Surgery (ESVS): document covering atherosclerotic disease of extracranial carotid and vertebral, mesenteric, renal, upper and lower extremity Eur Heart J. 2018;39:763–816. doi: 10.1093/eurheartj/ehx095 Crossref. PubMed
- Schmidt, A., et al., Retrograde recanalization technique for use after failed antegrade angioplasty in chronic femoral artery occlusions. J Endovasc Ther, 19(1): p. 23-9.
- Pappy, , T.A. Hennebry, and M.S. Abu-Fadel, Retrograde access via the popliteal artery to facilitate the re-entry technique for recalcitrant superficial femoral artery chronic total occlusions. Catheter Cardiovasc Interv, 2011. 78(4): p. 625-31.
- Shi, , et al., Combined antegrade femoral artery and retrograde popliteal artery recanalization for chronic occlusions of the superficial femoral artery. J Vasc Interv Radiol, 2014. 25(9): p. 1363-8.
- Tokuda, , et al., A sheathless retrograde approach via the popliteal artery is useful and safe for treating chronic total occlusions in the superficial femoral artery. J Endovasc Ther, 2014. 21(2): p. 289-95.
- Soga, , et al., Contemporary outcomes after endovascular treatment for aorto-iliac artery disease. Circ J, 2012. 76(11): p. 2697-704.
- Soga, , et al., Initial and 3-year results after subintimal versus intraluminal approach for long femoropopliteal occlusion treated with a self-expandable nitinol stent. J Vasc Surg, 2013. 58(6): p. 1547-55.
- Krankenberg, H., et al., Nitinol stent implantation versus percutaneous transluminal angioplasty in superficial femoral artery lesions up to 10 cm in length: the femoral artery stenting trial (FAST). Circulation, 116(3): p. 285-92.
- Laird, J.R., et al., Nitinol stent implantation versus balloon angioplasty for lesions in the superficial femoral artery and proximal popliteal artery: twelve-month results from the RESILIENT randomized Circ Cardiovasc Interv, 2010. 3(3): p. 267-76.
- Schillinger, , et al., Balloon angioplasty versus implantation of nitinol stents in the superficial femoral artery. N Engl J Med, 2006. 354(18): p. 1879-88.
- Swee, et al., Managing Perforations of the Superficial Femoral Artery. Endovascular today, 2014. 10.

