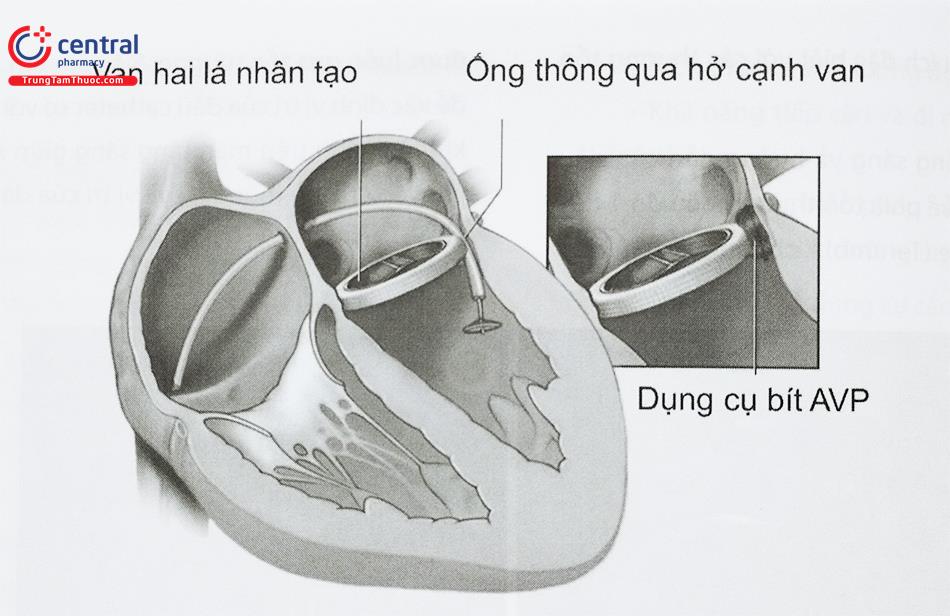
Can thiệp hở cạnh van nhân tạo - Một lựa chọn đầu tay
Nguồn: Sách Tim mạch can thiệp
Chủ biên
PGS.TS.BS.Phạm Mạnh Hùng
Tác giả
PGS.TS.BS.Phạm Mạnh Hùng
ThS.BSNT.Bùi Nguyên Tùng
ThS.BSNT.Lê Xuân Thận
Can thiệp hở cạnh van nhân tạo ngày nay là phương pháp an toàn cho bệnh nhân hở van tim. Kỹ thuật đó như thế nào? Hãy cùng Trung Tâm Thuốc Central Pharmacy (trungtamthuoc.com) tìm hiểu trong bài viết sau đây.
1 Đại cương
Hở cạnh van nhân tạo khá thường gặp, chiếm khoảng 5% – 10% ở các bệnh nhân phẫu thuật thay van tim nhân tạo và 40% – 70% ở nhóm bệnh nhân thay van tim qua đường ống thông. Bệnh nhân có hở cạnh van hầu hết không có triệu chứng. Tuy nhiên có một số ít bệnh nhân hở cạnh van nhân tạo có có các triệu chứng như suy tim hoặc có tình trạng thiếu máu do tan máu. Đối với nhóm bệnh nhân này, điều quan trọng là việc cần thiết của phẫu thuật mổ lại để sửa chữa tình trạng hở cạnh van nhân tạo. Tuy nhiên, những bệnh nhân này thường trong bệnh cảnh lâm sàng nặng do đó nguy cơ cho cuộc phẫu thuật rất cao. Hơn nữa, phẫu thuật mổ mở cũng có thể thất bại do đặc điểm của mô cơ tim tổn thương gây tình trạng hở cạnh van tiếp tục tiếp diễn.
Phương pháp sửa chữa hở cạnh van qua đường ống thông hiện nay đã được phát triển và cho thấy đây là một kỹ thuật an toàn và hiệu quả cho các bệnh nhân hở cạnh van tim nhân tạo được thực hiện bởi các nhà can thiệp có kinh nghiệm. Can thiệp qua đường ống thông là hướng đi của tương lai bởi đây là một can thiệp tương đối ít xâm lấn cho hở cạnh van và được xem như là lựa chọn đầu tay nếu điều kiện bệnh nhân cho phép.
2 Đánh giá giải phẫu tổn thương
Quy trình đánh giá bệnh nhân có hở cạnh van là toàn diện và tiếp cận đa chuyên khoa. Khai thác tiền sử và khám bệnh nhằm phát hiện các biểu hiện của viêm nội tâm mạc nhiễm khuẩn và thiếu máu tan máu cho tất cả các bệnh nhân. Nếu có tình trạng viêm nội tâm mạc đang hoạt động thì đó là chống chỉ định của can thiệp. Nếu bệnh nhân có tình trạng thiếu máu tan máu thì đòi hỏi thủ thuật phải thành công tối đa (tức là không còn dòng hở cạnh van).
Đánh giá giải phẫu hở cạnh van thường được thực hiện bằng các phương tiện chẩn đoán hình ảnh như siêu âm tim qua thành ngực, siêu âm tim qua thực quản, chụp cắt lớp vi tính đa dãy (MSCT), cộng hưởng từ (MRI) tim đối với loại van có thể chụp được cộng hưởng từ.
2.1 Siêu âm tim đánh giá hở cạnh van nhân tạo
Đánh giá tình trạng hở cạnh van tim chủ yếu bằng siêu âm tim. Siêu âm Doppler tim có vai trò xác định mức độ nghiêm trọng và vị trí của hở cạnh van (bao gồm cả kích thước và khoảng cách từ vòng van đến rìa ngoài của tổn thương), đường kính thất trái, sự có mặt của dòng hở van trung tâm và để loại trừ các trường hợp có chỉ định phẫu thuật tim mở thay lại van. Do đó các nghiên cứu chi tiết với nhiều cửa sổ siêu âm là rất cần thiết cũng như được thực hiện bởi nhiều phương thức khác nhau như siêu âm tim qua thành ngực, siêu âm tim qua thực quản.
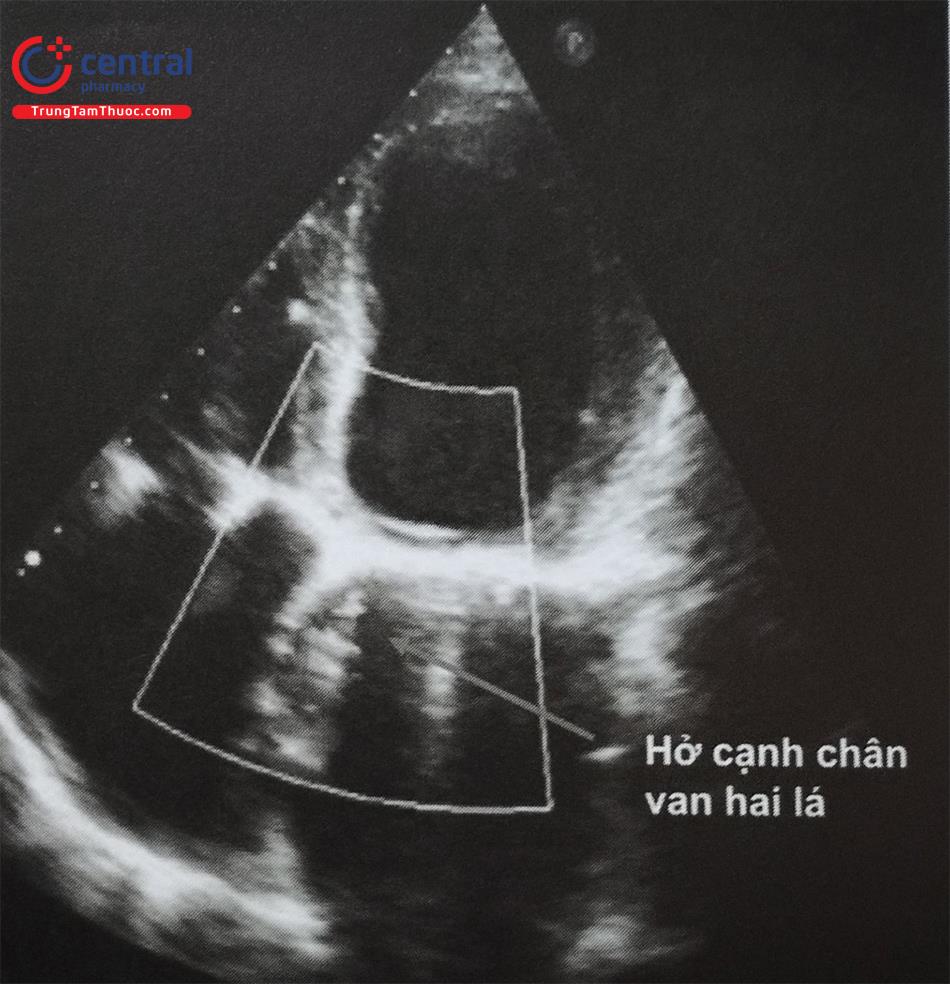
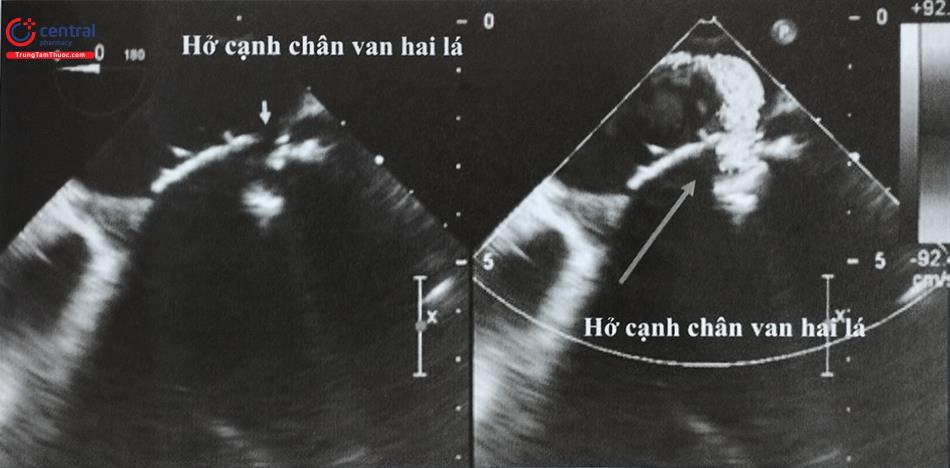
Siêu âm tim hai bình diện và Doppler tim được sử dụng như các phương pháp sàng lọc ban đầu. Ngoài ra, đối với bệnh nhân khó trong đánh giá van hai lá, siêu âm tim ba bình diện với phổ màu đặc biệt hữu ích trong đánh giá hình thái và lên kế hoạch chi tiết cũng như định hướng cho thủ thuật sửa chữa hở cạnh van. Đáng chú ý, mặc dù việc đánh giá mức độ hở van tự nhiên bằng siêu âm tim đã được thực hiện từ lâu và có tiêu chuẩn rõ ràng, thì các tiêu chí để xác định mức độ nghiêm trọng của hở cạnh van vẫn chưa được nghiên cứu nhiều.
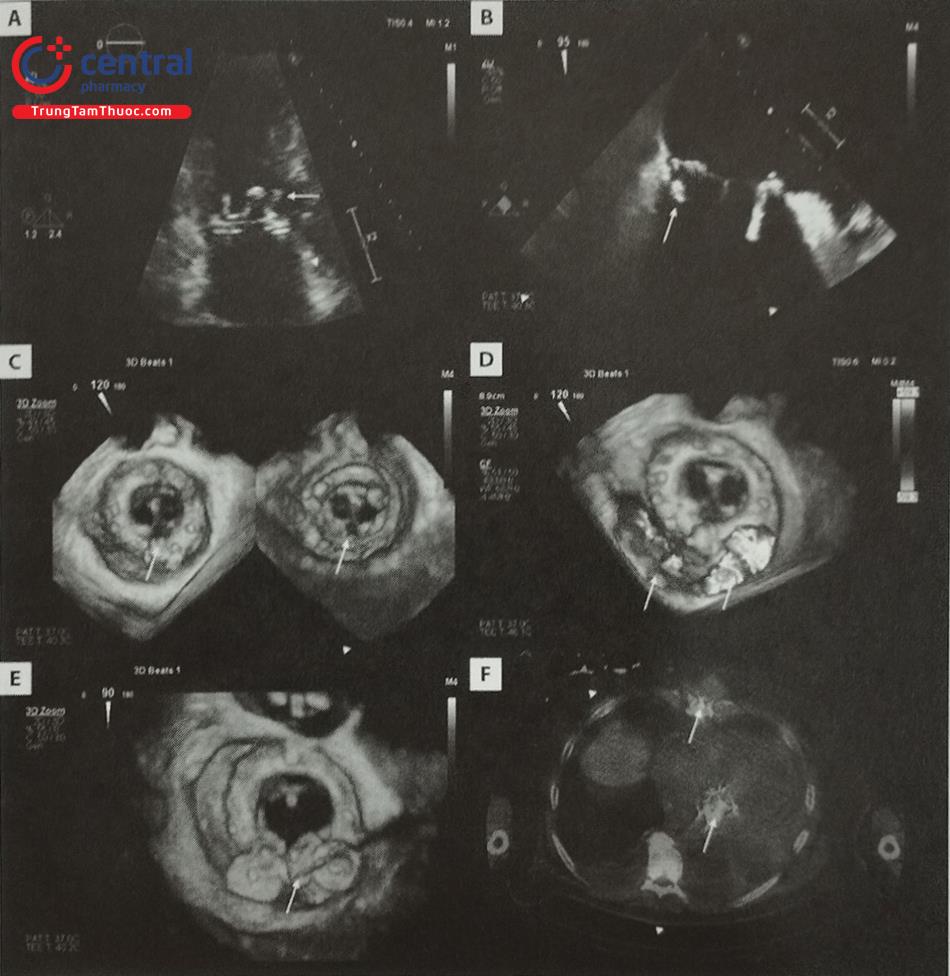
A, Hình ảnh hở cạnh van trên siêu âm tim qua thành ngực. B, Hình ảnh hở cạnh van trên siêu âm tim qua thực quản. C, Hình ảnh hở cạnh van trên siêu âm tim 3D.
2.2 Cộng hưởng từ đánh giá hở cạnh van nhân tạo
Hình ảnh cộng hưởng từ tim (MRI) có thể hỗ trợ cùng siêu âm tim để đánh giá một cách chính xác mức độ hở cạnh van vì MRI không bị ảnh hưởng nhiều bởi các yếu tố nhiễu. Bởi vì chẩn đoán hình ảnh không xâm lấn hiện nay vẫn còn nhiều thách thức và có thể là không tương đồng về kết quả giữa các phương pháp hình ảnh trong việc đánh giá tình trạng hở cạnh van, vì thế các tác giả đã đề xuất thêm các thăm dò xâm lấn nhằm đánh giá một cách chính xác mức độ hở van ở bệnh nhân chưa có triệu chứng lâm sàng. Vì vậy, thông tim thăm dò huyết động một cách chi tiết qua đường ống thông nên được thực hiện trong trường hợp này.
2.3 Thăm dò huyết động xâm lấn đánh giá hở cạnh van nhân tạo
Đối với tất cả bệnh nhân, đặc điểm lâm sàng liên quan đến mức độ nặng và các triệu chứng liên quan phải được đánh giá chi tiết. Những tổn thương không phải là tình trạng hở cạnh van nhiều nhưng nó vẫn có thể ảnh hưởng đến huyết động và có thể có lợi ích từ việc điều trị. Vậy nên, quyết định điều trị là phải cá thể hóa. Trong trường hợp này, thăm dò huyết động xâm lấn với đánh giá trực tiếp áp lực đổ đầy thất trái khi nghỉ và khi gắng sức có thể là hữu ích.
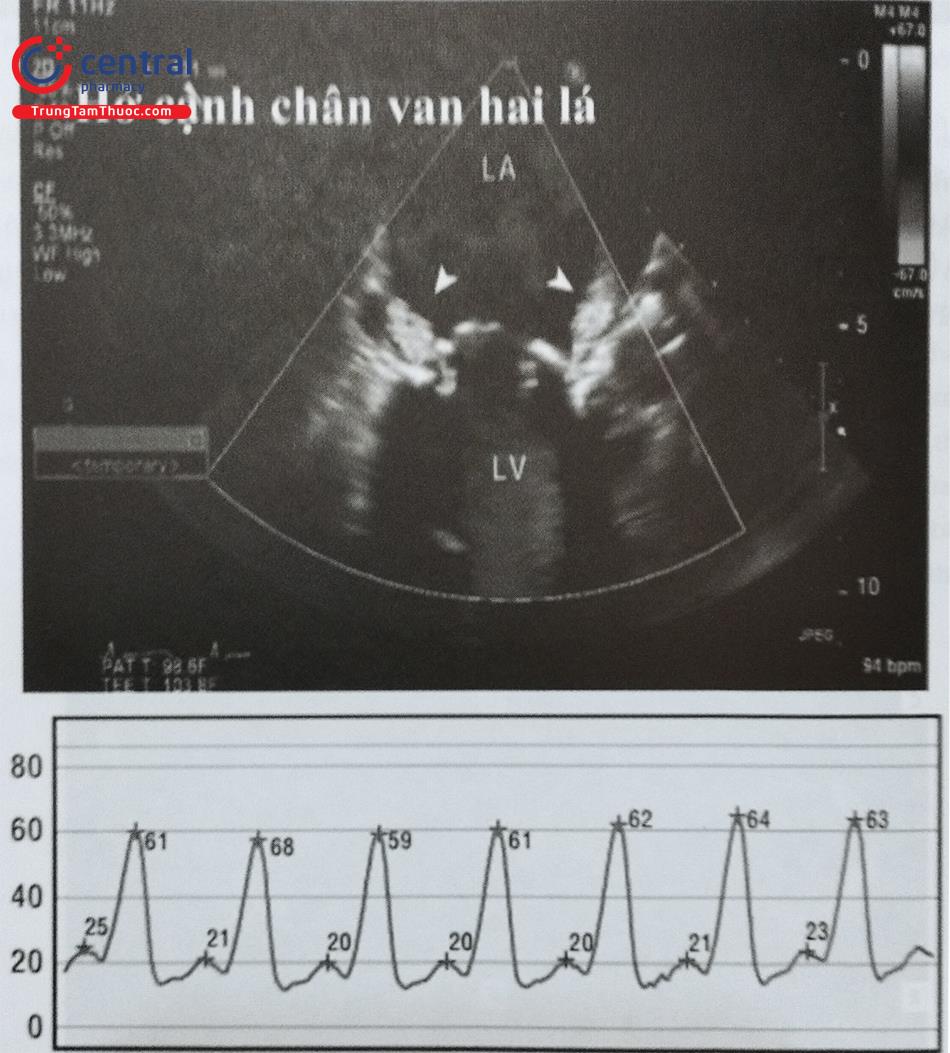
Dòng hở cạnh van được nhìn thấy rõ ở 2 bên của van hai lá sinh học (phía trên, đầu các mũi tên). Dòng hở từ nhẹ đến trung bình được đánh giá qua siêu âm tim thực quản. Tuy nhiên, đánh giá huyết động xâm lấn với trực tiếp áp lực nhĩ trái cao với sóng v rất lớn và áp lực trung bình là 38 mmHg (phía dưới).
2.4 Chụp cắt lớp vi tính đánh giá hở cạnh van nhân tạo
Chụp cắt lớp vi tính tim (CT) có giá trị chẩn đoán cao trong việc định hướng trục dòng hở và mức độ vôi hóa quanh van. Các hình ảnh cắt lớp cung cấp các thông tin chi tiết, hỗ trợ rất nhiều cho thành công của thủ thuật.
Các hình ảnh được dựng dựa trên hình ảnh cản quang đồng bộ với cổng điện tâm đồ, độ dày mỗi lớp cắt tối đa là 0,6 mm để đảm bảo độ phân giải tốt nhất. Dựa trên các thông tin từ siêu âm tim, các hình ảnh CT được dựng lại với các góc từ vị trí thoát của dòng hở cạnh van.
Các hình ảnh CT cũng có thể đánh giá được hình thái, tổn thương kèm theo của các lá van (ví dụ pannus) để đánh giá các yếu tố ảnh hưởng đến dòng hở. Điều này đặc biệt hữu dụng nếu hiện tượng bóng cản gây khó khăn trong việc đánh giá tổn thương bằng siêu âm. Ở một số trung tâm có CT đồng bộ hóa giúp cho thủ thuật tiến hành được thuận lợi hơn. Do các hình ảnh CT này sẽ được đồng bộ với các cấu trúc tim (buồng tim, van tim, mạch vành), sau đó đưa lên trên màn hình huỳnh quang. Hình ảnh CT đồng bộ được sử dụng để đưa dụng cụ (xuôi dòng qua vách liên nhĩ hoặc ngược dòng từ mỏm tim) đồng thời hỗ trợ khi lái dây dẫn qua tổn thương và khi thả dụng cụ.

3 Chỉ định và chống chỉ định can thiệp hở cạnh chân van nhân tạo
Trong các khuyến cáo về bệnh van tim, sửa chữa hở cạnh van qua đường ống thông được khuyến cáo cho bệnh nhân có triệu chứng nghiêm trọng hoặc có tan máu, những người có nguy cơ phẫu thuật cao, và những người có giải phẫu phù hợp (khuyến cáo mức độ IIa).
Ngoài ra, nhiều chuyên gia cũng xem xét điều trị qua đường ống thông cho các bệnh nhân không có triệu chứng nhưng có suy chức năng thất trái và cho bệnh nhân có nguy cơ cao của phẫu thuật. Sửa chữa qua đường ống thông có thể được coi là phương pháp tiếp cận ban đầu.
Do những thách thức về kỹ thuật, sửa chữa qua đường ống thông không nên được thực hiện trong các trung tâm chưa có kinh nghiệm. Chống chỉ định khác là đang có tình trạng viêm nội mạc nhiễm khuẩn, tình trạng van nhân tạo không ổn định, hoặc hở van trung tâm đáng kể cần phải mổ lại. Nguy cơ rơi dụng cụ có thể tương đối cao với tất cả van cơ học nhưng có thể xảy ra ở tất cả bệnh nhân.
Bảng 1. Khuyến cáo về Quản lý bệnh lý van tim của Trường môn tim mạch Hoa Kỳ và Hiệp hội Tim mạch Hoa Kỳ (AHA/ACC) 2020
Chẩn đoán hở van nhân tạo | ||
1 | B-NR | Ở những bệnh nhân nghi ngờ hở van tim nhân tạo, siêu âm tim qua thành ngực và siêu âm tim qua thực quản được khuyến cáo để xác định nguyên nhân và mức độ nặng của dòng hở, đánh giá chức năng thất, và áp lực động mạch phổi. |
1 | C-EO | Những bệnh nhân thực hiện bít hở cạnh van nhân tạo qua đường ống thông, siêu âm tim qua thực quản 3D được khuyến cáo để hướng dẫn quá trình thủ thuật. |
Xử trí hở van nhân tạo | ||
1 | B-NR | Những bệnh nhân có tan máu hoặc suy tim do hở van nhân tạo hoặc hở cạnh van nhân tạo, phẫu thuật nên được khuyến cáo trừ khi nguy cơ phẫu thuật cao hoặc có chống chỉ định. |
2a | B-NR | Những bệnh nhân hở van nhân tạo mức độ nặng nhưng không có triệu chứng và nguy cơ phẫu thuật thấp, phẫu thuật nên được thực hiện. |
2a | B-NR | Những bệnh nhân hở cạnh van nhân tạo có:
|
2a | B-NR | Bệnh nhân suy tim nặng do hở van sinh học nhưng có nguy cơ phẫu thuật cao, kỹ thuật đặt van trong van nên được thực hiện ở trung tâm hoàn chỉnh về bệnh Van tim. |
4 Dụng cụ bít hở cạnh van nhân tạo
Để bít hở cạnh van nhân tạo có nhiều dụng cụ khác nhau được sử dụng. Hầu hết các dụng cụ này được cấu tạo bởi phần eo và 2 đĩa ở hai đầu. Occlutech PLD có hai hình dạng đĩa là hình vuông và hình chữ nhật. Amplatzer Vascular Plug (AVP) được thiết kế đóng các mạch ngoại biên nhưng ngày nay được sử dụng rộng trong bít hở cạnh van nhân tạo. Dụng cụ bít ống động mạch, bít thông liên nhĩ, thông liên thất cũng có thể được lựa chọn. Trong các trường hợp thì việc lựa chọn dụng cụ dựa vào hình dạng và kích thước của hở cạnh van và kinh nghiệm của bác sĩ can thiệp. Dụng cụ AVPIII và Occlutech PLD thường được sử dụng cho các lỗ hở hình bầu dục do dụng cụ hình chữ nhật. Ngược lại, các dụng cụ hình vuông như AVPII hoặc Occlutech PLD có thể phù hợp cho các trường hợp lỗ hở hình trụ. Các lỗ hình liềm có thể phù hợp với dụng cụ hình chữ nhật. Về kích thước dụng cụ được khuyến cáo lớn hơn đường kính lớn nhất của lỗ hở cạnh van từ 1 – 2 mm, một số trường hợp hở cạnh van lớn có thể sử dụng 2 dụng cụ để bít.

(a): Amplatzer bít thông liên thất phần cơ. (b): Amplatzer bít còn ống động mạch. (c): Amplatzer Vascular Plug III. (d): Occlu- tech PLD (thiết kế hình vuông). (e): Amplatzer bít thông liên nhĩ. (f): Amplatzer Vascular Plug (g): Amplatzer Vascular Plug IV. (h): Occlutech PLD (thiết kế hình chữ nhật).
Dụng cụ bít phổ biến được sử dụng trong can thiệp qua da sửa chữa hở cạnh van nhân tạo là các loại Amplatzer plug thường được dùng bít mạch máu – AVP (St. Jude Medical, Fridley, MN). Chúng được chế tạo từ Nitinol tự nở, được thả thông qua các loại ống thông kích thước nhỏ (4Fr) có hoặc không có đường dẫn, duy trì hình dạng các cánh sau khi thả để giảm thiểu nguy cơ huyết khối thuyên tắc. Trong khi ở Mỹ sử dụng loại AVP-2, AVP-4 thì ở châu Âu loại AVP-3 được sử dụng. Một số loại dụng cụ thường gặp khác gồm Amplatzer để bít thông liên thất phần cơ (VSD) và bít ống động mạch (ADO và ADO-2) (St. Jude Medical, Fridley, MN). Các VSD và ADO có thể ứng dụng thành công trong một số trường hợp hở cạnh van đặc biệt, tuy nhiên cần hệ thống sheath lớn hơn để đưa các dụng cụ này. Trong khi đó ADO-2 là một loại dụng cụ bít mới, có đường kính phần eo lớn nhất chỉ 6 mm (phần đĩa 12 mm).
Một điểm quan trọng cần nhớ là loại ống thông nào phù hợp từng loại dụng cụ khác nhau không được các nhà sản xuất khuyến cáo rõ ràng trong hướng dẫn sử dụng. Một vài điểm chú ý được các hướng dẫn (được ban hành dựa trên các thử nghiệm và các ca lâm sàng có biến chứng) liệt kê bao gồm:
- Ống thông Multipurpose kích thước 6Fr (Cordis Co, Bridgewater, NJ) phù hợp với dụng cụ bít AVP-2.
- Ống thông Multipurpose chẩn đoán 4Fr (Terumo Medical Co, Somerset, NJ) phù hợp với dụng cụ bít AVP-4.
- Cook Flexor Shuttle sheath (Cook Medical, Bloomington, IN) 4Fr sẽ phù hợp với AVP-2 loại 8
- Cook Flexor Shuttle sheath đường kính 6Fr sẽ phù hợp với AVP-2 loại 12 mm đưa đồng thời với một dây dẫn Amplatz siêu cứng 0,035’’ hoặc 2 dây dẫn Amplatz siêu cứng 0,032’’ cùng sử dụng.
- Lựa chọn dụng cụ bít đến nay hầu hết vẫn dựa vào kinh nghiệm do việc nong bóng đo kích thước không được khuyến cáo. Bên cạnh đó hình dạng uốn khúc tự nhiên đặc trưng của hở cạnh van nên nhiều dụng cụ bít kích thước nhỏ nên được sử dụng hơn là một dụng cụ bít đơn độc.
Bảng 2. Các dụng cụ cho can thiệp sửa chữa hở cạnh van nhân tạo theo đường ống thông
| Các tổn thương ở van động mạch chủ |
2 introducer sheath 6Fr để mở đường vào động mạch. Sheath Gore Dryseal 12 Fr. Dây dẫn siêu cứng Glidewire 0,035 inch dài 260 cm, dây dẫn 0,018 inch có thể sử dụng trong một số trường hợp. Các dây dẫn siêu cứng Amplatz 0,032 inch, loại dài để thay thế ống thông là phù hợp nhất. Ống thông động mạch vành chẩn đoán: AL – 1,2 6Fr, multipurpose. Thòng lọng cổ ngỗng 15 hoặc 20 mm. Sheath Cook Flexor shuttle 4Fr đến 8Fr, dài 90 cm. Dụng cụ bít AVP-2 hoặc AVP-4 đường kính 6 – 14 mm, dụng cụ ADO-II hoặc VSD (thông liên thất) cũng có thể sử dụng. |
| Các tổn thương ở van hai lá |
Các introducer sheath 6Fr để mở đường vào tĩnh mạch và động mạch. Dụng cụ chọc vách liên nhĩ (tùy thuộc vào sự quen thuộc của thủ thuật viên). Sheath Gore Dryseal 20Fr. Dây dẫn siêu cứng Glidewire 0,035 inch dài 260 cm, dây dẫn 0,018 inch có thể sử dụng trong một số trường hợp. Các dây dẫn siêu cứng Amplatz 0,032 inch, loại dài để thay thế ống thông là phù hợp nhất. Các sheath Agilis (St. Jude Medical) có độ uốn cong ở đầu mức nhỏ đến trung bình, kích thước 8,5Fr. Ống thông chẩn đoán động mạch vành: multipurpose 5Fr, ống thông can thiệp động mạch vành: multipurpose 6Fr, JL, JR 6Fr. Thòng lọng cổ ngỗng 15 hoặc 20 mm. Sheath Cook Flexor shuttle 4Fr đến 8Fr, dài 90 cm. Dụng cụ bít AVP-2 hoặc AVP-4 đường kính 6 – 14 mm, dụng cụ ADO – II hoặc VSD (thông liên thất) cũng có thể sử dụng. |
5 Các bước tiến hành can thiệp
5.1 Các bước can thiệp hở cạnh van động mạch chủ nhân tạo
Phương án tiếp cận thông dụng nhất sửa chữa hở cạnh van động mạch chủ là đi đường ngược dòng qua động mạch đùi. Thủ thuật có thể tiến hành trong điều kiện an thần nhẹ hoặc gây mê truyền thống tùy thuộc vào phương thức siêu âm nào được sử dụng. Có nhiều cách thức siêu âm khác nhau để hướng dẫn can thiệp,
sự lựa chọn phụ thuộc vào vị trí thương tổn và mục đích nhằm tối thiểu hóa bóng cản của dòng hở gây ra (siêu âm thực quản cho các tổn thương phía sau, siêu âm qua thành ngực cho các tổn thương phía trước). Siêu âm trong buồng tim cũng có thể được sử dụng. Trong một số trường hợp, cần phải đưa ống thông siêu âm trong buồng tim đến vị trí đường ra thất phải để có thể đánh giá hình ảnh chi tiết mà các phương pháp siêu âm qua thực quản và qua thành ngực không cung cấp được.
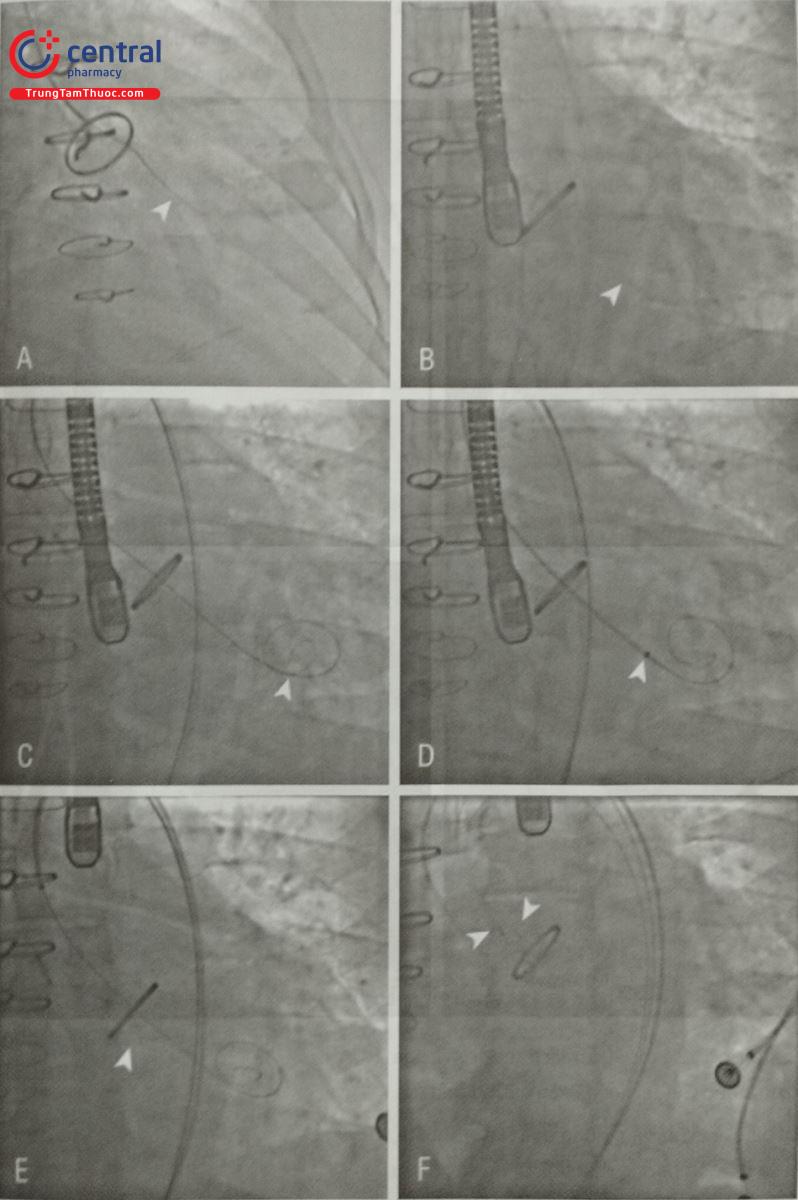
Ống thông chẩn đoán Multipurpose 6Fr (đầu mũi tên) được lái qua tổn thương phía sau, sau đó 1 dây dẫn siêu cứng, đầu cong, dài 260 cm được đưa (B) Ống thông Multipurpose (đầu mũi tên) được đưa vào trong thất trái. (C) Một dây dẫn Safari dài 260 cm được đưa qua tổn thương theo ống thông Multipurpose (đầu mũi tên). (D) Thông qua dây dẫn Safari, 1 Sheath 8Fr Cook Flexor Shuttle (đầu mũi tên) được đưa vào trong thất trái, theo sau đó là 2 dây dẫn siêu cứng Amplatz 0,032-inch . (E) Với dây dẫn cứng dùng để làm mỏ neo, nòng sheath được rút ra và dụng cụ bít AVP-2 kích thước 12 mm (đầu mũi tên ) được đặt tại vị trí tổn thương. (F) Flexor sheath được kéo ra và sau đó đẩy lại theo dây dẫn cứng. Dụng cụ bít AVP-2 12 mm thứ 2 được đưa vào và được đặt dọc theo dụng cụ bít đầu tiên. Hình ảnh đồng thời từ siêu âm và chụp động mạch chủ cho thấy dụng cụ bít ở vị trí thích hợp, an toàn, không còn dòng hở và không chèn vào cánh van nhân tạo. Các dụng cụ sau đó được thả ra.
Các bước trong can thiệp hở cạnh van động mạch chủ nhân tạo
Mở đường vào từ 2 động mạch đùi chung 2 bên (1 bên dùng sheath 12Fr Gore Dryseal, 1 bên dùng sheath 6Fr thông thường). Bên dùng sheath lớn nên được khâu chờ bằng 2 sợi chỉ (phẫu thuật hoặc dụng cụ đóng mạch).
Sử dụng 1 ống thông can thiệp động mạch vành kích thước 5Fr hoặc 6Fr đặt vào động mạch chủ lên (Multipurpose với thương tổn phía sau và Amplatz vành trái cho các vị trí phía trước).
Đầu dò siêu âm phải được điều hướng khéo léo để có thể loại bỏ được hiện tượng chồng hình giữa vị trí tổn thương và van nhân tạo. Nếu vị trí đầu dò không chính xác sẽ gây khó khăn cho phẫu thuật viên nếu dây dẫn đi từ tổn thương phía ngoài xuyên qua van nhân tạo. Vị trí đặt đầu dò có thể ước lượng (nghiêng trái chếch đầu với các tổn thương phía sau, nghiêng phải chếch chân với các tổn thương phía trước) hoặc xác định chính xác nhờ vào hình ảnh Nếu có siêu âm 2 bình diện thì đầu dò siêu âm thứ 2 thường được sử dụng để bộc lộ hình ảnh thẳng mặt của van nhân tạo nếu có thể, điều này giúp xác định được liệu dây dẫn có ở ngoài van hay không.
Lái ống thông đi qua tổn thương, thay dây dẫn bằng dây dẫn Guidewire đường kính 0,035 inch (Terumo) khi phần đầu ống thông qua được tổn thương vào trong buồng thất trái. Lưu ý cẩn thận tránh vướng dây dẫn vào các phần tổ chức của van hai lá. Bác sĩ can thiệp cũng cần tránh đưa wire vào các động mạch vành, tư thế nghiêng trước trái giúp việc thao tác dễ dàng hơn.
Một sheath Cook Flexor 90cm kích thước 4Fr đến 8Fr sẽ được trượt theo Guidewire để vào buồng thất trái.
Dụng cụ bít được đưa vào thông qua Flexor sheath, với phần đầu xa ở trong buồng thất trái. Dụng cụ bít sau đó được kéo ra sao cho phần đĩa nằm hoàn toàn trong thất trái và trong tổn thương, như dụng cụ AVP-4, sau khi được thả xong sẽ nằm hoàn toàn trong tổn thương.
Một phương án tiếp cận khác là khi Guidewire đi qua tổn thương, tiếp tục đưa ống thông can thiệp động mạch vành theo dây dẫn này vào buồng thất trái, sau đó thay thế dây dẫn này bằng một dây dẫn siêu cứng Amplatz 0,032 inch để tiếp đó đưa ống thông can thiệp vào. Trong tất cả các trường hợp việc lựa chọn ống thông đưa dụng cụ phụ thuộc vào:
- Kích thước và số lượng dụng cụ bít cần phải dùng.
- Khả năng tiếp cận và đi qua được tổn thương của ống thông.
- Sử dụng các biện pháp hỗ trợ như dây dẫn mỏ neo (anchor wire) hoặc đường ray tạo thuận (rail).
Trước khi thả dụng cụ cần phải đánh giá tình trạng hở tồn lưu cạnh van và có sự cản trở của dụng cụ với hoạt động của cánh van nhân tạo hay không. Đồng thời cần chụp lại động mạch chủ để loại trừ vấn đề tắc mạch do sử dụng dụng cụ lớn hoặc nhiều dụng cụ đồng thời, do xoang vành nhỏ, khoảng cách từ lỗ động mạch vành đến mặt phẳng van thấp, tổn thương gần với lỗ động mạch vành. Sau khi đánh giá kỹ càng các vấn đề nêu trên, dung cụ bít được giải phóng bằng cách xoay que thả ngược chiều kim đồng hồ.
5.2 Các bước can thiệp hở cạnh van hai lá nhân tạo
Với các bệnh nhân này, thủ thuật được tiến hành dưới hướng dẫn của siêu âm qua thực quản và bệnh nhân được gây mê theo phương pháp truyền thống. Các bước can thiệp phổ biến là thông qua tĩnh mạch đùi tiếp cận vách liên nhĩ, chọc vách sau đó đi xuôi dòng, luồn ống thông từ nhĩ trái xuống van hai lá nhân tạo. Các phương pháp tiếp cận có hiệu quả khác là đi vào trực tiếp từ mỏm tim hoặc ngược dòng thông qua động mạch đùi, ống thông đi từ buồng thất trái ngược lên.
Các bước trong can thiệp qua da sửa chữa hở cạnh van hai lá nhân tạo
- Đường vào từ tĩnh mạch đùi phải (chọc mạch theo phương pháp cơ bản) sau đó luồn 1 sheath Gore Dryseal kích thước 20Fr vào. Có thể khâu chỉ chờ tại vị trí này để thuận tiện cho việc cầm máu sau khi can thiệp
- Chọc vách liên nhĩ dưới màn hình tăng sáng và hướng dẫn của siêu âm để đi vào nhĩ trái. Với các thương tổn ở vị trí sau – giữa, vị trí chọc vách nên dịch về phía sau của vách liên nhĩ, nhằm tăng khoảng cách từ vị trí này đến van hai lá. Điều này giúp làm giảm độ gập góc gây nên khó khăn khi đưa ống thông tiếp cận tổn thương.
- Một hệ thống các ống thông thứ tự từ nhỏ đến to luồn vào nhau gồm ngoài cùng là 1 ống thông 8,5Fr (Agilis, St. Jude, Fridley, MN), tiếp đó là 1 ống thông Multipurpose 6Fr dài 100 cm, trong cùng là ống thông chẩn đoán Multipurpose 5Fr dài 125 cm. Ống thông ngoài cùng nên uốn nhẹ tạo thành 1 đoạn cong nhỏ hoặc vừa, điều này hữu ích đặc biệt với các thương tổn ở vị trí phía sau.
- Dưới màn hình tăng sáng và hướng dẫn của siêu âm, hệ thống được lái về phía tổn thương, sau đó 1 dây dẫn đầu cong Glidewire (Terumo) kích thước 0,035 inch được luồn qua tổn thương. Siêu âm tim 3D rất hữu dụng để xác định vị trí của đầu catheter so với van hai lá, trong khi hình ảnh trên màn tăng sáng giúp xác định vị trí, di chuyển của hệ thống lái và vị trí của dây dẫn bên ngoài vòng van.
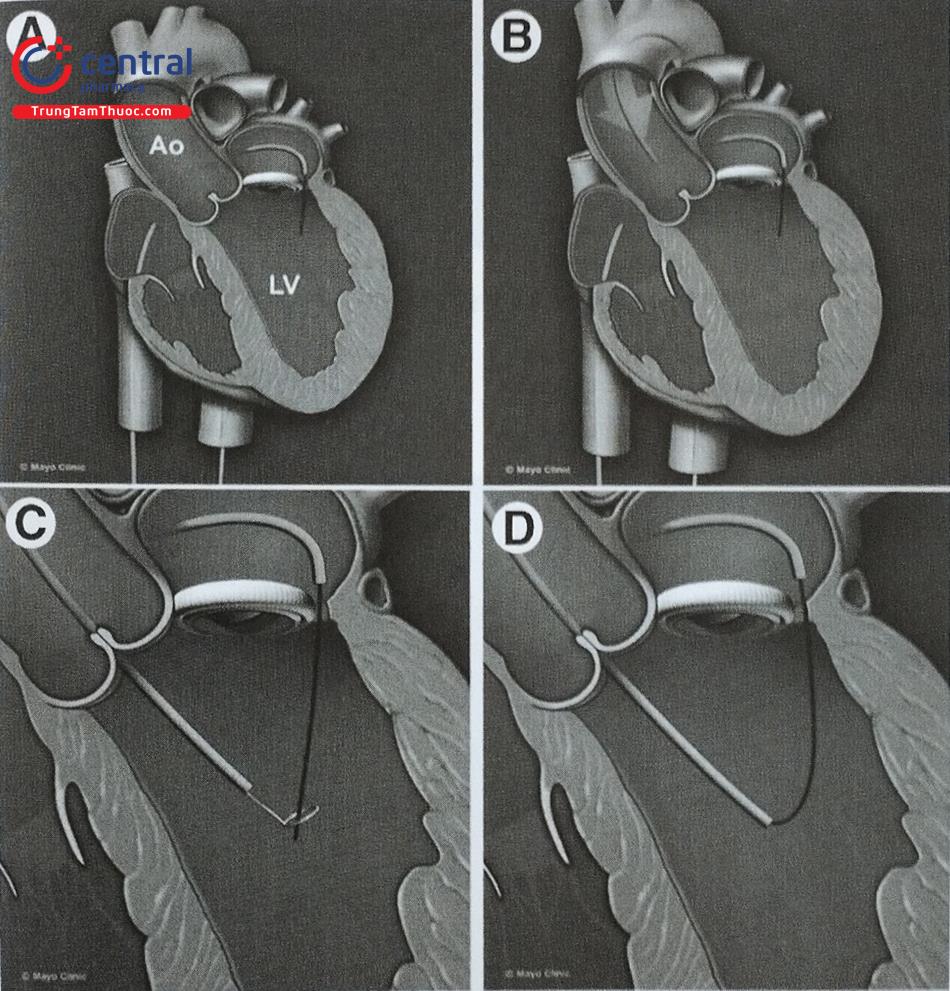
A. Đưa ống thông qua vách liên nhĩ; B. Hướng ống thông và đưa guidewire qua hở cạnh van; C. Dùng Snare bắt và giữ đầu wire; D. Đưa ống thông qua hở hai lá xuống thất trái
- Sau khi luồn 2 ống thông Multipurpose qua tổn thương để vào thất trái, ống thông Multipurpose chẩn đoán sẽ được rút
- Dụng cụ bít được đưa vào qua ống thông 6Fr, kích thước tối đa phù hợp với ống thông này của AVP – 2 là 12 mm. Có thể thay thế bằng ống thông kích thước to hơn (Cook Flexor Shuttle 6Fr đến 8Fr, 90 cm), sử dụng dây dẫn siêu cứng Amplatz 0,032 inch để thuận tiện cho việc thay ống thông. Sử dụng ống thông kích thước lớn giúp thủ thuật thuận lợi trong trường hợp phải dùng nhiều dụng cụ bít hoặc cần sử dụng kỹ thuật dây dẫn mỏ neo.
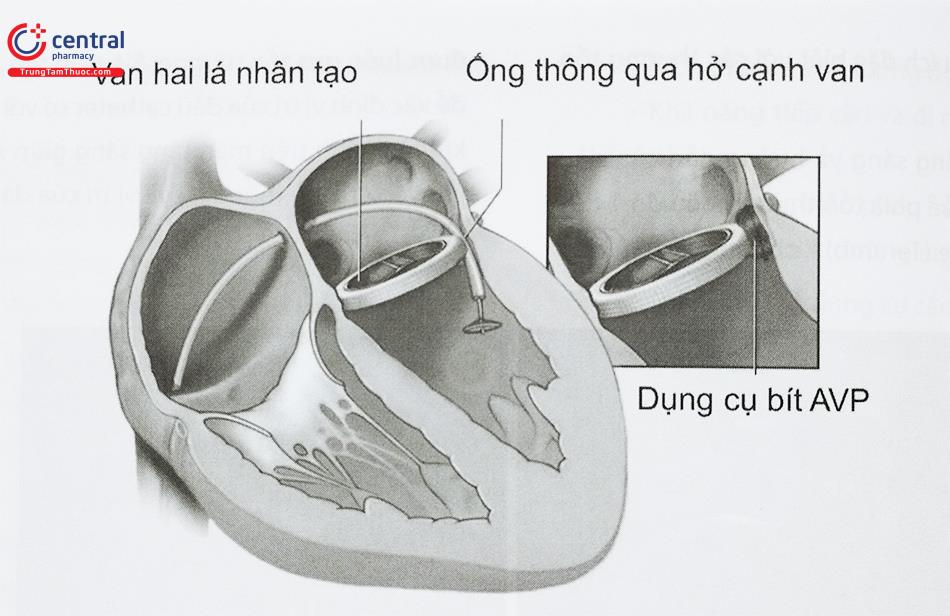
- Tương tự như trong can thiệp van động mạch chủ, phần cánh của dụng cụ bít được đẩy ra đầu ống thông vào trong thất trái, hệ thống sau đó được kéo về, dụng cụ bít sẽ nằm hoàn toàn trong tổn thương.
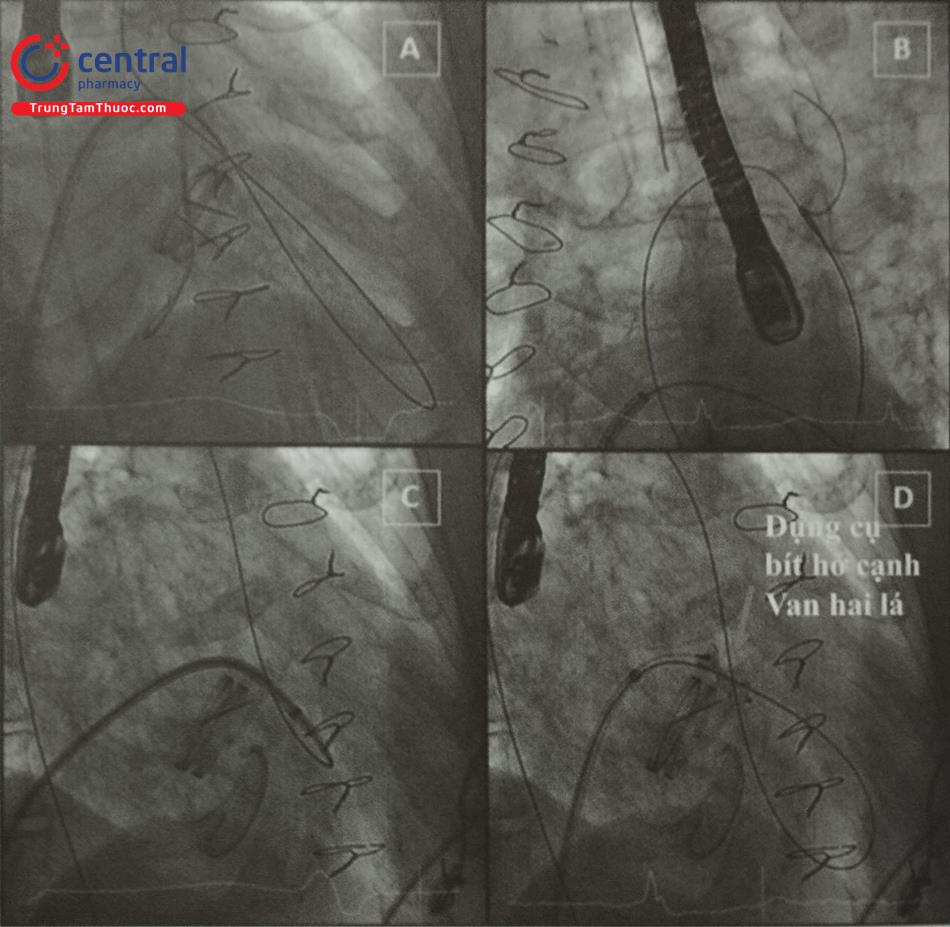
A. Đưa ống thông qua vách liên nhĩ và đưa wire qua hở cạnh van, B. Dùng Snare bắt và giữ đầu wire trên động mạch chủ, C. Đưa ống thông qua hở hai lá xuống thất trái , D. Bít hở cạnh van bằng dụng cụ
- Nếu kiểm tra thấy dụng cụ không làm cản trở hoạt động của cánh van qua siêu âm tim và màn hình tăng sáng, tiến hành thả dụng cụ.
- Siêu âm qua thực quản hướng dẫn can thiệp là yếu tố cần thiết cho sự thành công của thủ thuật. Người làm siêu âm và phẫu thuật viên cần phối hợp đồng bộ nhịp nhàng trong xác định vị trí thương tổn và điều chỉnh dụng cụ can thiệp. Thách thức trong vấn đề kết nối này là sự trái chiều của hình ảnh trên màn hình tăng sáng và siêu âm qua thực quản. Để thuận tiện, cần đánh giá theo các thuật ngữ giải phẫu ví dụ như trước với sau, giữa với bên, tam giác giữa van động mạch chủ (phía trước) với tiểu nhĩ trái (trước bên) và vách liên nhĩ (giữa). Trong trường hợp van cơ học, vị trí của mép van nhân tạo cũng giúp cho việc định hướng.
- Với phương pháp tiếp cận ngược dòng thông qua động mạch đùi, các ống thông dùng can thiệp động mạch vành (ống thông Judkin phải, Amplatz trái và phải, ống thông động mạch vú trong) sau khi đưa vào trong thất trái sẽ được lái hướng về phía sau để tiếp cận tổn thương. Kỹ thuật này đặc biệt hữu dụng trong trường hợp tổn thương khu trú ở vùng giữa và không thể tiếp cận được qua nhĩ trái. Nếu dây dẫn Guidewire quá cứng để đi qua tổn thương thì có thể dùng các loại dây dẫn 0,014 inch hoặc 0,018 inch mềm hơn để thao tác. Với kỹ thuật tiếp cận thông qua mỏm tim, cách thức đi qua tổn thương và đặt các dụng cụ cũng tương tự kỹ thuật đi xuôi dòng. Sử dụng hình ảnh CT đồng bộ hóa cũng giúp ích nhiều khi tiến hành chọc mỏm tim và lái dụng cụ qua tổn thương.
5.3 Đường dẫn hỗ trợ ống thông
Các thương tổn cạnh van thường uốn khúc và vôi hóa nhiều gây khó khăn cho việc đưa ống thông đi Do đó đường dẫn có thể được sử dụng để hỗ trợ thao tác này cũng như tránh việc phải lái dây dẫn nhiều lần qua tổn thương.
Các đường dẫn hỗ trợ ống thông ban đầu được sử dụng nhiều trong can thiệp các bệnh lý tim bẩm Các đường dẫn được tạo nên bằng việc sử dụng thòng lọng bắt lấy đầu xa của dây dẫn sau khi dây dẫn đi qua tổn thương, sau đó kéo đầu xa của dây dẫn ra phía ngoài, điều này giúp phẫu thuật viên có thể kiểm soát được cả 2 đầu dây dẫn. Các loại thòng lọng điển hình thường dùng là loại cổ ngỗng (với kích thước vòng 15 hoặc 20 mm). Thao tác bắt đầu xa dây dẫn thường tiến hành dễ dàng tại các vị trí mạch máu có khẩu kính bé (như đoạn động mạch chủ xuống), vì vậy, sau khi đi qua tổn thương dây dẫn nên được tiếp tục lái ra càng xa càng tốt. Với tổn thương cạnh van hai lá, các loại đường dẫn có thể là nhĩ trái – thất trái – động mạch chủ hoặc nhĩ trái – thất trái – mỏm tim. Trong khi với các tổn thương cạnh van động mạch chủ, các loại đường dẫn có thể là động mạch chủ thất trái – động mạch chủ, hoặc trong một vài trường hợp là động mạch chủ – thất trái – mỏm tim, nhĩ trái – thất trái – động mạch chủ.
Một khi đã tạo đường dẫn thành công, bác sĩ can thiệp có thể đưa ống thông đi qua với sự hỗ trợ của người phụ bằng cách kéo căng 2 đầu dây dẫn. Một khi lựa chọn được ống thông có kích thước hợp lý (ví dụ Flexor shuttle, 8Fr, 90 cm), dụng cụ bít có thể đưa vào dễ dàng bằng cách trượt theo đường dẫn. Thêm vào đó, đường dẫn sẽ giúp phẫu thuật viên thoải mái đưa được thử các loại dụng cụ bít, cũng như đưa được đồng thời nhiều dụng cụ vào vị trí tổn thương (xem thêm phần kỹ thuật mỏ neo phía dưới). Ví dụ, 1 ống thông Flexor shut- tle có thể đưa được cùng lúc 1 dụng cụ bít AVP – 2 kích thước 12 mm và 1 Glidewire kích thước 0,035mm.
Tuy nhiên, điều rất quan trọng là phải luôn chú ý đến việc gây tổn thương đến các cấu trúc xung quanh gây ra bởi độ căng và độ cứng của đường dẫn. Nó có thể gây nên các sang chấn nặng với cả van nhân tạo lẫn các cánh van tự nhiên, tổn thương cơ tim, các rối loạn nhịp chậm nguy hiểm do tác động lên nút nhĩ thất, thậm chí đứt các dây chằng, cột cơ của van hai lá. Do đó, các thao tác có sự góp mặt của đường dẫn hỗ trợ chỉ nên tiến hành nếu có sự theo dõi sát sao về huyết động cũng như của siêu âm.
5.4 Kỹ thuật dây dẫn mỏ neo và thả nhiều dụng cụ bít
Các thương tổn cạnh van thường không đồng tâm và nằm sát với các khu vực khâu đính vòng van nhân tạo. Trong những trường hợp này, nếu dụng cụ bít bị nhô ra quá nhiều có thể chèn và gây cản trở hoạt động các cánh van, đặc biệt là van cơ học. Để tránh hiện tượng này cũng như việc làm giảm dòng hở một cách tối ưu, một số lượng lớn các dụng cụ kích thước nhỏ có thể được sử dụng thông qua việc sử dụng dây dẫn mỏ
Với kỹ thuật này, một ống thông kích thước lớn (thường > 6Fr, dài 90 cm như Cook Flexor Shuttle) được đưa vào trong thất trái một khi dây dẫn ái nước đi qua được tổn thương. Loại ống thông này thuận lợi cho việc đưa nhiều dây dẫn siêu cứng, các dây dẫn này sau đó sẽ được sử dụng để đưa các ống thông thả dụng cụ bít vào, theo thứ tự hoặc cùng lúc. Trong kỹ thuật thả đồng thời, 2 dây dẫn siêu cứng được đưa qua tổn thương thông qua ống thông, sau đó 2 ống thông thả dụng cụ (thông thường là Multipurpose 6Fr) sẽ đưa vào theo 2 dây dẫn này. Dụng cụ bít sau đó sẽ được thả vào vị trí tổn thương đồng thời thông qua 2 ống thông này.
Với kỹ thuật thả tuần tự sử dụng dây dẫn mỏ neo, dụng cụ bít được đưa dọc theo dây dẫn (dụng cụ vẫn nằm trong ống thông). Dây dẫn này có thể cuộn tròn trong thất trái hoặc được bắt bằng thòng lọng đưa ra ngoài. Một khi dụng cụ bít đã ở đúng tại vị trí tổn thương, ống thông sẽ được kéo ra chỉ để lại que thả (cable) kết nối với dụng cụ phía ngoài ống thông và dây dẫn. Ống thông sau đó lại được đưa vào thông qua dây dẫn mỏ neo này. Thao tác trên lặp lại nếu phẫu thuật viên thấy cần đưa thêm dụng cụ bít vào. Khi các dụng cụ đã ở vị trí phù hợp và đáp ứng yêu cầu, các que thả sẽ được thao tác để tách ra khỏi dụng cụ.
Kỹ thuật này cũng rất hữu ích trong trường hợp phải giữa ổn định tại vị trí tổn thương nếu phẫu thuật viên muốn thay đổi dụng cụ bít hoặc cần phải thả nhiều dụng cụ hơn. Chú ý là khi sử dụng kỹ thuật này, phải sử dụng ống thông có kích thước lớn để có thể đưa được nhiều dây dẫn và ống thông thả dụng cụ. Loại ống thông Dryseal (W.L.Wore, Flagstaff, AZ) với một đầu có bóng cuff, là loại ống thông duy nhất thích hợp cho việc cầm máu trong trường hợp này.
6 Tiêu chí đánh giá thành công của thủ thuật
Siêu âm tim và chụp buồng tim xác nhận sau khi bít hở cạnh van, dụng cụ bít ở đúng vị trí hở cạnh van và ngăn dòng hở giảm ít nhất về hở mức độ 1 hoặc không có hở cạnh van đồng thời dụng cụ không ảnh hưởng đến các hoạt động của lá van.
Trường hợp bít hở cạnh van có biến chứng tan máu cần cân nhắc can thiệp lại bít kín hoàn toàn không còn dòng hở.
7 Biến chứng và xử trí
Biến chứng khá ít gặp, đánh giá tỷ lệ biến cố trong 30 ngày sau can thiệp có khoảng 2,6% bệnh nhân đột quỵ não, 1,7% bệnh nhân đột tử, 0,9% bệnh nhân cần phải can thiệp mổ cấp cứu, 5,2% cho chảy máu quanh thủ thuật và 0,5% cho tử vong. Chảy máu thủ thuật có thể do thủng tim, chọc mỏm tim, dùng các dụng cụ đường vào mạch máu quá lớn, dùng chống đông trong can thiệp. Đóng vị trí chọc mạch vùng mỏm tim bằng keo phẫu thuật hoặc dụng cụ bít mạch máu được sử dụng để tăng cường khả năng cầm máu.
Những nguyên nhân thất bại của thủ thuật là do dụng cụ bít chèn vào cánh van nhân tạo hoặc không có khả năng đưa dây dẫn hoặc đầu ống thông qua vị trí dò cạnh van. Chèn vào cánh van nhân tạo (khoảng 5% trường hợp) có thể xảy ra với bất kỳ loại van nhân tạo nào nhưng là phổ biến hơn trong các van cơ học. Đặc biệt việc đánh giá phải được thực hiện để đảm bảo các lá van tương thích với dụng cụ bít về chức năng của cả van sinh học và cơ học, dựa vào hình ảnh và huyết động (tức là tính chênh áp qua van). Cần lưu ý đến vấn đề lực tồn dư sau khi hệ thống đẩy giải phóng dụng cụ có thể dẫn đến việc làm di lệch vị trí dụng cụ bít. Vì vậy, cần đánh giá lại lần cuối có hay không dụng cụ bít chèn vào cánh van nhân tạo trước khi thả dụng cụ. Bên cạnh việc sử dụng nhiều dụng cụ bít kích thước nhỏ để làm giảm nguy cơ chèn vào cánh van, việc ổn định hệ thống thả cũng đóng vai trò rất quan trọng trong giảm di lệch. Xử trí trường hợp chèn ép dụng cụ vào cánh van có thể phải hiệu chỉnh lại vị trí, hoặc thu hồi dụng cụ để chuyển sang phẫu thuật.
Nhìn chung, tỉ lệ di lệch dụng cụ bít sau thủ thuật chiếm khoảng < 1% các ca. Để đề phòng sự di lệch, trước khi giải phóng dụng cụ cần được kiểm tra mức độ chắc chắn bằng cách đẩy dụng cụ và kéo đồng thời quan sát sự di chuyển dụng cụ trên màn tăng sáng. Những trường hợp di lệch có thể cần phải dùng thòng lọng (Snare) để lấy dụng cụ ra.
8 Kết quả lâm sàng qua các nghiên cứu
Thành công của thủ thuật sửa chữa hở cạnh chân van qua đường ống thông có tiêu chuẩn rất nghiêm ngặt. Bít hở cạnh van nhân tạo dòng hở cạnh van sau can thiệp ở mức độ nhẹ hoặc không còn dòng hở và không có các biến chứng lớn, đạt khoảng 80% bệnh nhân (và khoảng 90% có dòng hở sau can thiệp ở mức vừa hoặc ít hơn).
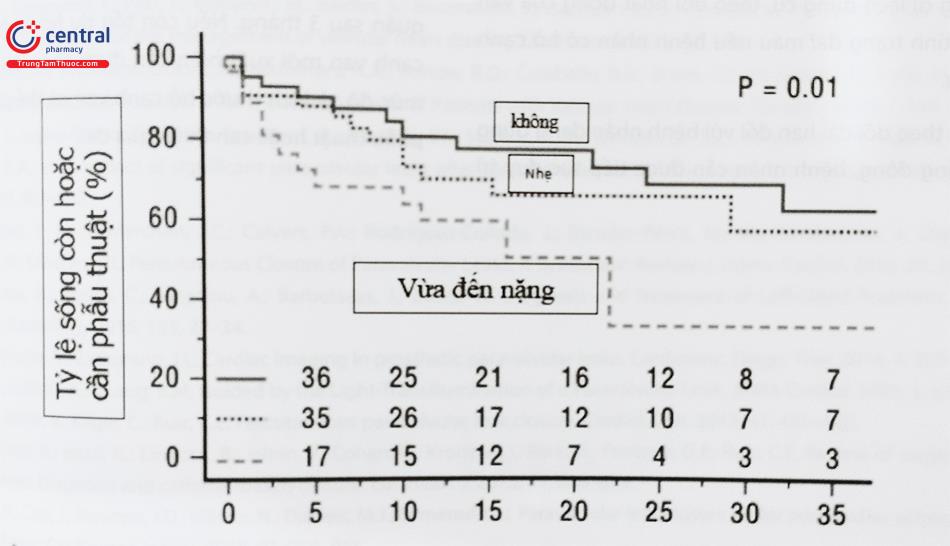
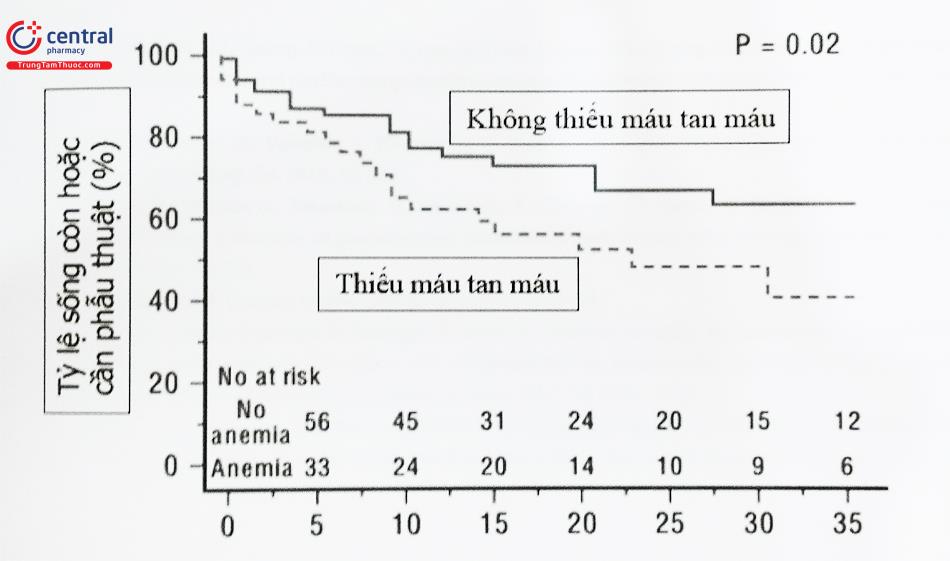
Mức độ hở cạnh van sau can thiệp càng ít, triệu chứng càng được cải thiện và tăng tỷ lệ sống còn. Trong một nghiên cứu theo dõi sau 3 năm, tỷ lệ sống sót sau 3 năm là 64%, và phân độ NYHA cũng được cải thiện tốt hơn ở nhóm bệnh nhân còn hở cạnh van mức độ nhẹ hoặc không còn hở cạnh van. Bệnh nhân có thiếu máu tan máu thì thủ thuật cần đạt mức độ gần hoặc hoàn toàn không còn hở cạnh van nhằm giảm tình trạng thiếu
máu tan máu. Kinh nghiệm của nhà tim mạch học can thiệp với sự phát triển của kỹ thuật trong những năm gần đây (như kỹ thuật mỏ neo, hình ảnh 3D, đường dẫn hỗ trợ) là những yếu tố dự báo quan trọng cho sự thành công của thủ thuật.
9 Theo dõi
Sau thủ thuật bệnh nhân cần được điều trị nội khoa theo dõi tình trạng huyết động các chỉ số sinh tồn và các biến chứng sau thủ thuật chung như biến chứng đường vào, biến chứng di lệch dụng cụ, theo dõi hoạt động của van nhân tạo, tình trạng đái máu nếu bệnh nhân có hở cạnh van tồn dư.
Điều trị và theo dõi dài hạn đối với bệnh nhân đang dùng thuốc chống đông, bệnh nhân cần được tiếp tục duy trì
thuốc chống đông sau thủ thuật. Những bệnh nhân không có chỉ định dùng thuốc chống đông trước thủ thuật thì sau thủ thuật chỉ định dùng thuốc chống ngưng kết tiểu cầu kép ít nhất 3 tháng. Sau thủ thuật cần siêu âm qua thực quản đánh giá kỹ vị trí của dụng cụ bít và mức độ hở cạnh van tồn dư đồng thời cần đánh giá lại siêu âm qua thực quản sau 3 tháng. Nếu còn tồn dư hở cạnh van hoặc hở cạnh van mới xuất hiện cần được theo dõi sát. Tuỳ theo mức độ và kích thước hở cạnh van có thể cần có chỉ định phẫu thuật hoặc can thiệp qua da.
10 Tài liệu tham khảo
- Desai, ; John, C. Messenger, Robert Quaife, John Carroll. Update in Paravalvular Leak Closure. Curr. Cardiol. Rep. 2021, 23, 122.
- Cruz-Gonzalez, I.; Rama-Merchan, J.C.; Rodríguez-Collado, J.; Martín-Moreiras, J.; Diego-Nieto, A.; Barreiro-Pérez, M.; Sánchez, L. Transcatheter closure of paravalvular leaks: State of the art. Neth. Heart J. 2017, 25, 116–124.
- Bernard, ; Yucel, E. Paravalvular Leaks-From Diagnosis to Management. Curr Treat. Options Cardiovasc. Med. 2019, 21, 67.
- Vahanian, A.; Beyersdorf, ; Praz, F.; Milojevic, M.; Baldus, S.; Bauersachs, J.; Capodanno, D.; Conradi, L.; De Bonis, M.; De Paulis, R.; et al. 2021 ESC/EACTS Guidelines for the management of valvular heart disease. Eur. Heart J. 2021, 43, 172.
- Writing Committee Members; Otto, C.M.; Nishimura, R.A.; Bonow, R.O.; Carabello, B.A.; Erwin, I.I.J.P.; Gentile, F.; Jneid, H.; Krieger, E.V.; Mack, M.; et al. 2020 ACC/AHA Guideline for the Management of Patients with Valvular Heart Disease. Circulation 2021, 143, e72–e227.
- Lopez-Pais, J.; Lopez-Otero, D.; Garcia-Touchard, A.; Coronel, B.I.; Muiños, J.A.; Mendioroz, X.C.; Pérez-Poza, M.; Garcia, Ó.O.; Peredo, C.G.M.; Flores, C.A.; et al. Impact of significant paravalvular leaks after transcatheter aortic valve implantation on anaemia and mortality. Heart 2020, 107, 497–502.
- Cruz-Gonzalez, I.; Rama-Merchan, J.C.; Calvert, A.; Rodríguez-Collado, J.; Barreiro-Pérez, M.; Martín-Moreiras, J.; Diego-Nieto, A.; Hildick-Smith, D.; Sánchez, P.L. Percutaneous Closure of Paravalvular Leaks: A Systematic Review. J. Interv. Cardiol. 2016, 29, 382–392.
- Lampropoulos, K.; Aggeli, C.; Megalou, A.; Barbetseas, J.; Budts, Diagnosis and Treatment of Left-Sided Prosthetic Paravalvular Regurgitation. Cardiology 2016, 133, 27–34.
- Lazaro, C.; Hinojar, R.; Zamorano, J.L. Cardiac imaging in prosthetic paravalvular leaks. Cardiovasc. Diagn. 2014, 4, 307–313.
- Karagodin, ; Shah, A.P.; Lang, R.M. Guided by the Light-Transillumination of a Paravalvular Leak. JAMA Cardiol. 2020, 5, e203260.
- Kumar, ; Jelnin, V.; Kliger, C.; Ruiz, C.E. Percutaneous paravalvular leak closure. Cardiol. Clin. 2013, 31, 431–440.
- Kliger, C.; Eiros, R.; Isasti, G.; Einhorn, B.; Jelnin, ; Cohen, H.; Kronzon, I.; Perk, G.; Fontana, G.P.; Ruiz, C.E. Review of surgical prosthetic paravalvular leaks: Diagnosis and catheter-based closure. Eur. Heart J. 2013, 34, 638–649.
- Ruparelia, ; Cao, J.; Newton, J.D.; Wilson, N.; Daniels, M.J.; Ormerod, O.J. Paravalvular leak closure under intracardiac echocardiographic guidance. Catheter. Cardiovasc. Interv. 2018, 91, 958–965.
- Suchá, D.; Symersky, ; Tanis, W.; Mali, W.P.; Leiner, T.; van Herwerden, L.A.; Budde, R.P. Multimodality Imaging Assessment of Prosthetic Heart Valves. Circ. Cardiovasc. Imaging 2015, 8, e003703.
- Orwat, S.; Diller, P.; Kaleschke, G.; Kerckhoff, G.; Kempny, A.; Radke, R.M.; Buerke, B.; Burg, M.; Schülke, C.; Baumgartner, H. Aortic regurgitation severity after transcatheter aortic valve implantation is underestimated by echocardiography compared with MRI. Heart 2014, 100, 1933–1938.
- Suh, J.; Hong, G.R.; Han, K.; Im, D.J.; Chang, S.; Hong, Y.J.; Lee, H.J.; Hur, J.; Choi, B.W.; Chang, B.C.; et al. Assessment of mitral paravalvular leakage after mitral valve replacement using cardiac computed tomography: Comparison with surgical findings. Circ. Cardiovasc. Imaging 2016, 9, e004153.
- Cruz-González, I.; Barreiro-Pérez, M.; Valverde, I. 3D-printing in Preprocedural Planning of Paravalvular Leak Closure: Feasibility/ Proof-of-concept. Rev. Esp. Cardiol. Engl. Ed. 2019, 72,
- Onorato, E.M.; Muratori, M.; Smolka, G.; Zakarkaite, D.; Mussayev, A.; Christos, P.; Bauer, F.; Gandet, T.; Luca, G.; Martinelli, M.D.; et al. Midterm procedural and clinical outcomes of percutaneous paravalvular leak closure with the Occlutech Paravalvular Leak Device. EuroIntervention 2020, 15, e1251–e1259.
- Sorajja, Mitral Paravalvular Leak Closure. Interv. Cardiol. Clin. 2016, 5, 45–54.
- García, E.; Arzamendi, D.; Jimenez-Quevedo, ; Sarnago, F.; Martí, G.; Sanchez-Recalde, A.; Lasa-Larraya, G.; Sancho, M.; Iñiguez, A.; Goicolea, J.; et al. Outcomes and predictors of success and complications for paravalvular leak closure: An analysis of the SpanisH real-wOrld paravalvular LEaks closure (HOLE)registry. EuroIntervention 2017, 12, 1962–1968.
- Calvert, A.; Northridge, D.B.; Malik, I.S.; Shapiro, L.; Ludman, P.; Qureshi, S.A.; Mullen, M.; Henderson, R.; Turner, M.; Been, M.; et al. Percutaneous Device Closure of Paravalvular Leak. Combined Experience From the United Kingdom and Ireland. Circulation 2016, 134, 934–944.

