Can thiệp điều trị hội chứng hậu huyết khối do tắc tĩnh mạch tầng chậu đùi
1 Nguồn: Sách tim mạch can thiệp
Chủ biên: PGS.TS.BS. Phạm Mạnh Hùng
Tham gia biên soạn
ThS. BSNT Nguyễn Tuấn Hải
BSNT Nguyễn Văn Đông
PGS.TS.BS Phạm Mạnh Hùng
Các nội dung về giải phẫu và hình thái tổn thương, chỉ định, chống chỉ định, quy trình can thiệp điều trị hội chứng hậu huyết khối do tắc tĩnh mạch tầng chậu đùi....sẽ được Trung Tâm Thuốc Central Pharmacy (trungtamthuoc.com) gửi đến bạn đọc trong bài viết dưới đây.
2 Đại cương
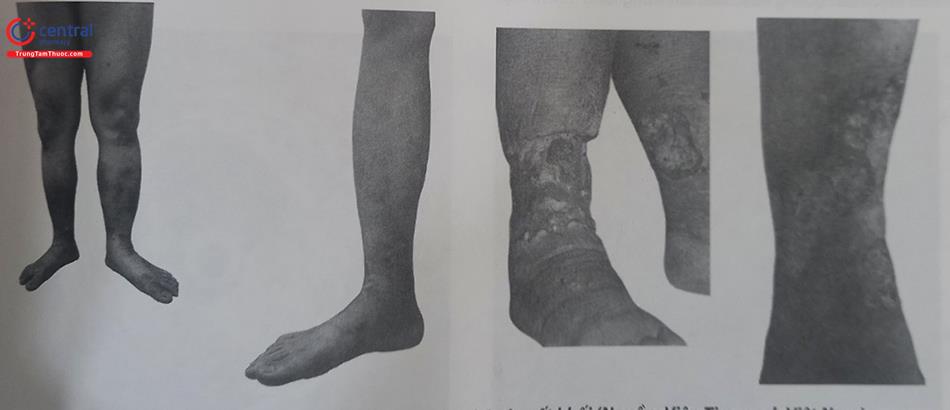
Hội chứng hậu huyết khối (HCHHK) tĩnh mạch (PTS/post thrombotic syndrome) tương ứng với các biểu hiện lâm sàng của suy tĩnh mạch mạn tính thứ phát sau huyết khối tĩnh mạch sâu chi dưới (HKTMSCD). Hội chứng hậu huyết khối không hiếm gặp, chỉ sau 2 năm bị HKTMSCD gần, kể cả khi được điều trị chống đông cũng như băng ép/tất áp lực đầy đủ, vẫn có từ 20 đến 50% bệnh nhân sẽ phát triển HCHHK và 5–10% ở mức độ nặng, ảnh hưởng đáng kể đến chất lượng cuộc sống, gây suy giảm chức năng vận động và làm tăng gánh nặng chi phí y tế. Tỷ lệ HCHHK có liên quan chặt chẽ với vị trí giải phẫu của huyết khối. Sự lan rộng của huyết khối đến tĩnh mạch tầng chậu đùi làm gia tăng tỷ lệ mắc HCHHK sau hai năm là trên 50%, với 44% đau cách hồi tĩnh mạch và 14% loạn dưỡng da. Chỉ có khoảng 20 – 30% trường hợp huyết khối tầng chậu được tái thông hoàn toàn, và tuần hoàn bàng hệ cũng chỉ phát triển ở khoảng 1/3 số bệnh nhân này, dẫn đến hậu quả lâu dài là tình trạng tăng áp lực tĩnh mạch mạn tính. Ngoài ra, HCHHK cũng xuất hiện thường xuyên hơn ở những bệnh nhân có huyết khối tồn dư hoặc dòng trào ngược bệnh lý trong tĩnh mạch khoeo.
Để điều trị HCHHK trầm trọng, liên quan đến tầng chậu đùi, đã có nhiều phương pháp điều trị khác nhau được đề xuất, trong đó có can thiệp nong tĩnh mạch qua da kết hợp với đặt stent tĩnh mạch. Tạo hình tĩnh mạch bằng can thiệp nội mạch đặt stent tĩnh mạch chậu đùi đã trở thành lựa chọn ưu tiên cho các tổn thương tắc nghẽn tĩnh mạch chậu đùi hậu huyết khối mức độ nặng. Thực tế cho thấy chỉ cần đặt stent mà chưa cần điều trị dòng trào ngược bệnh lý từ tĩnh mạch sâu đã có thể cải thiện đáng kể các triệu chứng. Do tỷ lệ biến chứng thấp và tỉ lệ thành công cao của các can thiệp nội mạch để làm giảm mức độ tắc nghẽn của dòng chảy tĩnh mạch sâu, can thiệp tĩnh mạch qua da đã dần dần thay thế phẫu thuật chuyển đoạn tĩnh mạch hay tạo hình van tĩnh mạch.
3 Giải phẫu và hình thái tổn thương
3.1 Giải phẫu
Giải phẫu chi tiết của hệ tĩnh mạch chi dưới được mô tả trong Chương 7: Giải phẫu và sinh lý hệ tĩnh mạch ứng dụng trong can thiệp. Chú ý đường đi của tĩnh mạch chậu ngoài bắt đầu từ dây chằng bẹn và kết thúc trước khớp xương cùng, ở vị trí nối với tĩnh mạch chậu trong để tạo thành tĩnh mạch chậu chung. Các tĩnh mạch chậu chung hợp lưu ở bên phải của đốt sống thắt lưng thứ 5 để tạo thành tĩnh mạch chủ dưới. Ngược lại với tĩnh mạch chậu chung phải, có đường đi tương đối thẳng với trục dọc của tĩnh mạch chủ dưới, tĩnh mạch chậu chung trái đi ngang và nằm dưới động mạch chậu chung phải, vì vậy có thể bị chèn ép vào cột sống (hội chứng May – Thurner). Tĩnh mạch chủ dưới đi lên phía trước, bên phải cột sống, qua gan và vào cơ hoành ở đốt sống ngực số 10 và sau đó đổ về tâm nhĩ phải.
Trong quá trình chụp tĩnh mạch cần chú ý đến các biến thể giải phẫu của tĩnh mạch chủ dưới (được mô tả chi tiết trong Chương 58: Can thiệp đặt lưới lọc tĩnh mạch chủ dưới).
3.2 Chẩn đoán hội chứng hậu huyết khối và hình thái tổn thương
Chẩn đoán HCHHK dựa vào lâm sàng, theo thang điểm Villalta.
Bảng 59.1. Thang điểm Villalta để chẩn đoán và đánh giá mức độ nặng của hội chứng hậu huyết khối.
| Triệu chứng lâm sàng | Không có | Nhẹ | Trung bình | Nặng |
|---|---|---|---|---|
| Triệu chứng cơ năng | ||||
| Đau chân | 0 | 1 | 2 | 3 |
| Chuột rút | 0 | 1 | 2 | 3 |
| Nặng chân | 0 | 1 | 2 | 3 |
| Ngứa | 0 | 1 | 2 | 3 |
| Dị cảm | 0 | 1 | 2 | 3 |
| Triệu chứng thực thể | ||||
| Phù | 0 | 1 | 2 | 3 |
| Da cứng | 0 | 1 | 2 | 3 |
| Đỏ da | 0 | 1 | 2 | 3 |
| Sạm da | 0 | 1 | 2 | 3 |
| Đau khi bóp cơ | 0 | 1 | 2 | 3 |
| Phân loại mức độ nặng | ||||
| Điểm Villalta | <5 | 5-9 | 10-14 | >14 hoặc có loét tĩnh mạch |
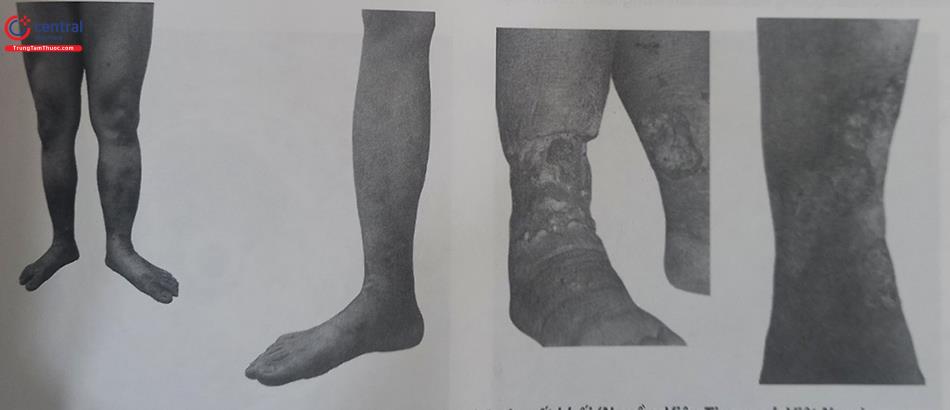
Siêu âm Doppler có thể làm rõ cơ chế của HCHHK (suy van hoặc tắc nghẽn) và xác định các dấu hiệu dự báo nguy cơ tiến triển thành HCHHK trầm trọng trong trường hợp tắc nghẽn tĩnh mạch đoạn gần (chậu, đùi). Ngay cả khi bệnh nhân chỉ bị huyết khối một bên, vẫn cần kiểm tra cả hai chân, và so sánh, đối chiếu để phát hiện suy tĩnh mạch không triệu chứng tồn tại từ trước. Các hội chứng chính trên siêu âm gồm:
- Hội chứng tắc nghẽn: tắc tĩnh mạch do huyết khối mạn tính
- Hội chứng hạn chế: thành tĩnh mạch dày, cứng, có di tích huyết khối bám vào
- Hội chứng thay thế: tuần hoàn tĩnh mạch nông thay thế
- Hội chứng tái thông: dòng trào ngược trong tĩnh mạch sâu
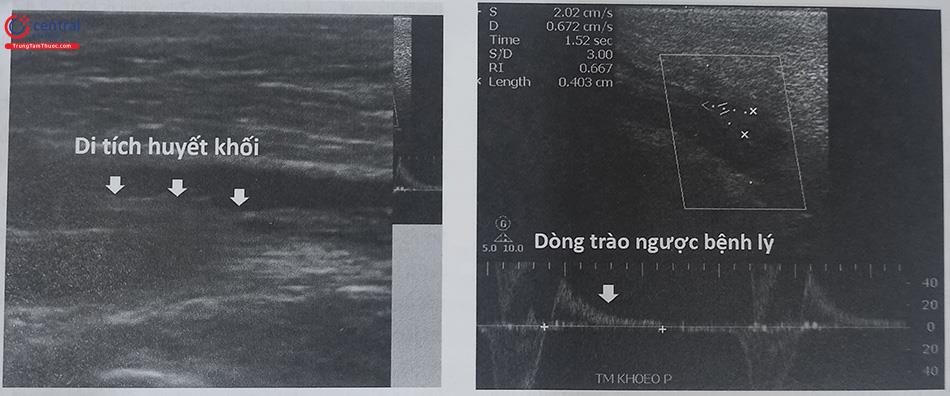
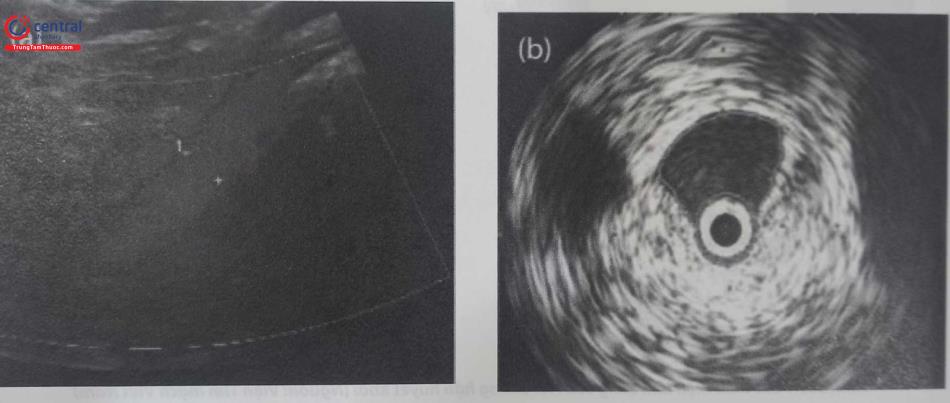
Chỉ định các biện pháp thăm dò hình ảnh khác phụ thuộc vào chiến lược điều trị và theo dõi. Nếu bệnh nhân đáp ứng tốt với điều trị bảo tồn, không hoặc rất ít triệu chứng thì chỉ cần định kỳ theo dõi lâm sàng và siêu âm. Nhưng nếu bệnh nhân có triệu chứng trầm trọng, dự kiến phải can thiệp, phẫu thuật, thì cần làm thêm cộng hưởng từ, chụp tĩnh mạch cản quang hoặc siêu âm trong lòng mạch. Mục tiêu của thăm dò hình ảnh trước khi tái thông mạch nhằm đảm bảo tính khả thi về mặt kỹ thuật và lập kế hoạch chính xác cho quy trình can thiệp. Yêu cầu phải xác định vị trí cực trên của huyết khối, đánh giá tình trạng của tĩnh mạch chủ dưới (giải phẫu, di chứng của huyết khối…), thăm dò các đoạn tĩnh mạch để xác định vị trí đặt stent.
4 Chỉ định, chống chỉ định can thiệp
Can thiệp nội tĩnh mạch không chứng minh được lợi ích ở những bệnh nhân không triệu chứng, ngay cả khi họ có tổn thương tắc hoặc hẹp nặng tĩnh mạch.
Chỉ định can thiệp ở những bệnh nhân HHKTM có triệu chứng cũng có sự khác biệt giữa các nghiên cứu lâm sàng. Bệnh nhân được lựa chọn, và đánh giá mức độ nặng dựa vào phân loại CEAP (xem thêm ở Chương 57: Can thiệp điều trị bệnh tĩnh mạch mạn tính chi dưới), thang điểm Villalta và r-VCSS. Giai đoạn lâm sàng từ C3 – C6 của phân loại CEAP thường coi là tiêu chí phổ biến nhất để xem xét khả năng can thiệp. Bên cạnh đó, thang điểm Villalta, tiêu chuẩn vàng hiện tại để chẩn đoán HCHHK, cũng được sử dụng để lựa chọn bệnh nhân trung bình (Villalta từ 10 – 14) hoặc nặng (Villalta ≥ 15 hoặc loét) trong can thiệp. Đau cách hồi nguyên nhân tĩnh mạch là triệu chứng chủ quan và không đủ tin cậy để làm căn cứ chỉ định can thiệp, nhưng lại là một trong những tiêu chí góp phần vào chỉ định, đồng thời đánh giá sự cải thiện triệu chứng sau can thiệp.
Ngoài lâm sàng, hẹp trên 50% lòng tĩnh mạch, được chẩn đoán dựa vào chụp tĩnh mạch, chụp cộng hưởng từ và/ hoặc siêu âm trong lòng mạch (IVUS) cũng là một tiêu chí góp phần vào chỉ định can thiệp nội tĩnh mạch.
Hội Tim mạch Hoa Kỳ (2014), và Diễn đàn tĩnh mạch Hoa Kỳ (2017) khuyến cáo can thiệp nong và đặt stent tĩnh mạch cho những bệnh nhân tắc/hẹp nặng tĩnh mạch chủ dưới hoặc tĩnh mạch chậu mạn tính, và trên lâm sàng có phù chi (C3), rối loạn sắc tố da có nguy cơ gây loét (C4b), loét tĩnh mạch đã lành (C5), hoặc loét tĩnh mạch đang tiến triển để làm vết loét chóng liền và giảm nguy cơ tái phát (I/B). Theo khuyến cáo của Hội phẫu thuật mạch máu châu Âu (2022):
Bảng 59.2. Khuyến cáo của Hội Phẫu thuật mạch máu châu Âu về chỉ định can thiệp tắc tĩnh mạch mạn tính tầng chậu đùi
| KHUYẾN CÁO | MỨC ĐỘ KHUYẾN CÁO | MỨC ĐỘ BẰNG CHỨNG |
|---|---|---|
Can thiệp nội tĩnh mạch nên là phương pháp điều trị được lựa chọn đầu tiên ở bệnh nhân tắc tĩnh mạch tầng chậu đùi có triệu chứng/dấu hiệu trầm trọng | IIa | B |
| Cân nhắc dùng siêu âm trong lòng mạch (IVUS) để hướng dẫn điều trị can thiệp cho bệnh nhân tắc nghẽn tầng chậu | IIa | C |
| Can thiệp hoặc phẫu thuật không được chỉ định cho bệnh nhân tắc nghẽn tầng chậu không có triệu chứng trầm trọng | III | C |
5 Quy trình can thiệp
5.1 Chuẩn bị bệnh nhân
Bệnh nhân được giải thích đầy đủ, làm xét nghiệm cơ bản và ký hồ sơ bệnh án.
Vô cảm trong can thiệp: Không giống như can thiệp động mạch, gây tê tại chỗ trong can thiệp nội tĩnh mạch có thể không đủ vì sức căng của thành tĩnh mạch trong quá trình can thiệp làm bệnh nhân rất đau, nhất là khi thủ thuật nong và đặt stent phải kéo dài. Vì vậy, bệnh nhân nên được gây tê bằng phong bế thần kinh, hoặc gây mê toàn thân trong quá trình can thiệp.
Chống đông trong can thiệp: ngay khi tiến hành can thiệp, tiêm Heparin không phân đoạn với liều từ 70 – 100 đơn vị/ kg. Sau khi thủ thuật tiến hành được 90 phút có thể tiêm tĩnh mạch bổ sung 2000 đơn vị.
Kháng sinh dự phòng nên được sử dụng một cách hệ thống.
5.2 Các bước tiến hành can thiệp
Bước 1: Chọc mạch và mở đường vào tĩnh mạch
Vị trí chọc mạch: Đường vào được sử dụng từ 1/3 giữa – trên của tĩnh mạch đùi, dưới hướng dẫn của siêu âm. Trong một số trường hợp, đường vào tĩnh mạch đùi không thành công, có thể chọc mạch ở các vị trí khác như tĩnh mạch đùi chung, tĩnh mạch đùi sâu, tĩnh mạch cảnh trong, tĩnh mạch khoeo, hoặc thậm chí tĩnh mạch hiển lớn. Sử dụng ống dẫn dài (long sheath) nếu đi đường tĩnh mạch cảnh trong phải để tránh làm ống thông cuộn lại trong tâm nhĩ phải gây rối loạn nhịp.
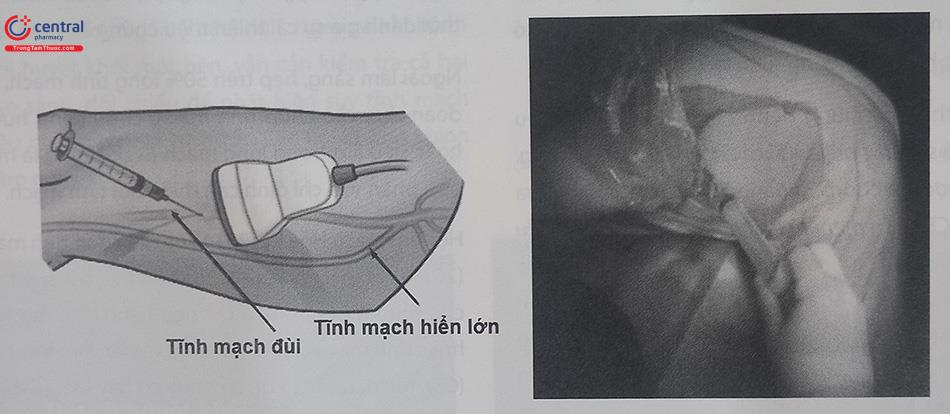
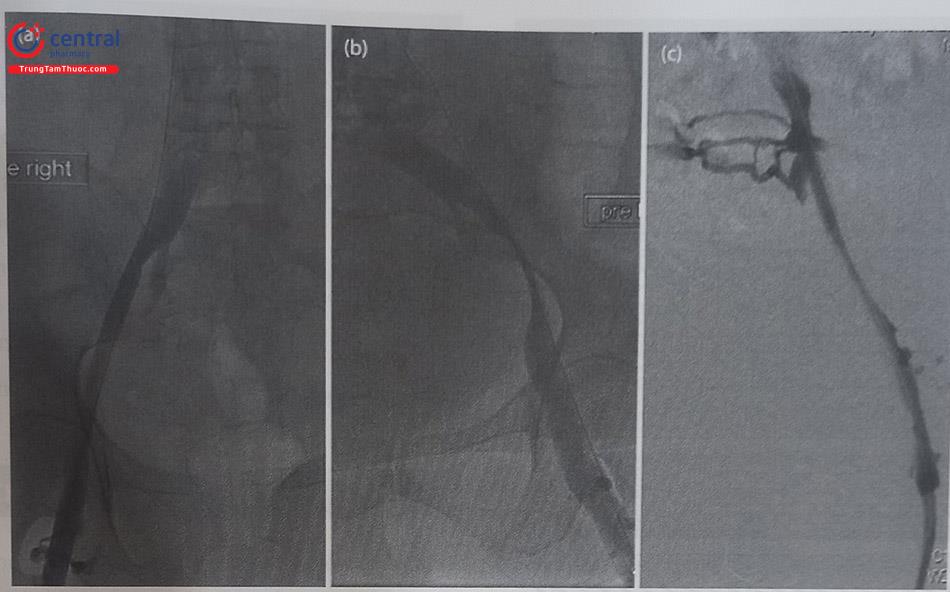
Bước 2: Chụp hệ tĩnh mạch và làm siêu âm trong lòng mạch (IVUS) để xác định mức độ tổn thương
Cả hai phương pháp chụp hệ tĩnh mạch cản quang và IVUS đều được thực hiện để hướng dẫn thủ thuật. Chụp hệ tĩnh mạch hướng dẫn đường đi trong thủ thuật, xác định tuần hoàn bàng hệ ở vùng chậu và cho hình ảnh dòng chảy liên tục trong tĩnh mạch. Có thể xác định dễ dàng dòng chảy chậm với sự thanh thải thuốc cản quang kém hoặc tĩnh mạch tắc hoàn toàn.
Tổn thương tắc tĩnh mạch sẽ cản trở dây dẫn và ống thông. Nên sử dụng sheath 6 Fr hoặc 7 Fr để hỗ trợ đi qua được tổn thương tắc hoàn toàn. Khác với kỹ thuật “subintimal j-wire” thường được sử dụng để đi qua tổn thương ở động mạch, đối với các tổn thương tĩnh mạch, ưu tiên sử dụng dây dẫn và ống thông nhỏ trong lòng mạch.
- IVUS được thực hiện khi dây dẫn đã đi qua được tổn thương tĩnh mạch hẹp hay tắc:
- IVUS phát hiện được tổn thương hẹp tĩnh mạch chậu, cả hẹp khu trú và lan tỏa với độ nhạy rất cao. Dòng chảy chậm dưới tổn thương tắc được thể hiện bằng hình ảnh “tuyết rơi” trên IVUS
- Đo đường kính và diện tích ở tĩnh mạch đùi chung, tĩnh mạch chậu ngoài, tĩnh mạch chậu chung, và TMCD để xác định mức độ của HCHHK. Các giá trị này sau đó được so sánh với chỉ số bình thường ở mỗi đoạn để xác định mức độ hẹp (đường kính và diện tích tham chiếu bình thường ở TM chậu chung, chậu ngoài, đùi chung lần lượt là 16, 14, 12 mm; và 200, 150, 125 mm2). Tổn thương hậu huyết khối thường xảy ra ở từng đoạn tĩnh mạch, ảnh hưởng đến toàn bộ tĩnh mạch chậu chung, tĩnh mạch chậu ngoài và/hoặc tĩnh mạch đùi chung. Vị trí chạc ba tĩnh mạch chậu cần được lưu ý. Ngoài ra, xác định vị trí “landing zone” của stent tại thời điểm IVUS ban đầu, trước khi bóng giãn nở làm co thắt mạch. “Landing zone” phải ở trong một đoạn tĩnh mạch bình thường, hoặc ít nhất là trong đoạn ít tổn thương nhất, trên vị trí chia đôi của tĩnh mạch đùi. Nếu có thể, ở những bệnh nhân hẹp tĩnh mạch nên tránh đặt stent mà không có “landing zone” phù hợp. Tuy nhiên, trong trường hợp có dòng tái thông ở bệnh nhân tắc mạn tính, đặt stent vào đoạn tĩnh mạch lành nhất có thể vẫn có lợi ích và duy trì được dòng chảy.
Trường hợp IVUS không xác định được tổn thương thì nên đo trực tiếp bằng bóng khi chụp mạch. IVUS có thể bỏ sót 15% bệnh nhân bị hẹp tĩnh mạch chậu. Trong nhóm này, hẹp được chẩn đoán bằng bóng và cần được đặt stent.
Bước 3: Nong bóng và đặt stent tĩnh mạch
Lựa chọn bóng: Quanh tĩnh mạch bị hẹp hoặc tắc thường có một lớp xơ đàn hồi khá cứng, vì vậy lựa chọn loại bóng phù hợp rất quan trọng. Nên chọn loại bóng áp lực cao và ít đàn hồi. Các đoạn tĩnh mạch điều trị cần được nong trước với bóng lớn (16 – 18 mm) ở áp lực cao, từ 14 đến 18 mmHg, được giữ ở mỗi đoạn trong 1-2 phút. Quy trình nong bóng được thực hiện tuần tự từ dưới lên trên để tránh gặp khó khăn khi đưa bóng qua đoạn hẹp. Bóng lớn cỡ 22 – 24 mm được sử dụng để tái thông
Lựa chọn và đặt stent: Sử dụng stent tự nở, chất liệu thép hoặc nitinol, loại dành riêng cho tĩnh mạch, như Wallstents (Boston Scientific, Nantick, MA), Abre (Medtronic), Gianturco Z-stent (Cook, Bloomington, IN)…, đường kính lựa chọn thường lớn hơn khoảng 20% đường kính tĩnh mạch đo trên
Đường kính và chiều dài của stent cần được lựa chọn cẩn thận, vì nguy cơ di lệch và trôi stent vào buồng tim phải. Đường kính stent thường lớn hơn 2 – 4 mm so với đường kính bóng, thay đổi từ 14 – 24 mm phụ thuộc vào đoạn tĩnh mạch cần đặt stent: trung bình 14 – 16 mm trong tĩnh mạch đùi và tĩnh mạch chậu ngoài, từ 14 đến 18 mm trong tĩnh mạch chậu chung và 16 đến 20 mm trong tĩnh mạch chủ dưới. Chiều dài tối thiểu của stent được khuyến cáo là 6 cm để tránh di lệch.
Quan trọng là stent phải phủ hết vị trí hẹp, tắc. Trong trường hợp phải đặt nhiều stent, các stent cần gối lên nhau khoảng 2 cm để tránh di lệch, gập góc giữa các stent, và tái hẹp ở vị trí tiếp giáp giữa hai
Một điểm khác so với stent động mạch là stent tĩnh mạch có thể tỳ trên khớp, mà không làm tăng nguy cơ hình thành huyết khối, chèn ép hoặc gãy Nếu tổn thương lan xuống tĩnh mạch đùi, stent có thể đặt qua cả nếp lằn bẹn. Trên thực tế, nguy cơ huyết khối lớn nhất là khi tổn thương không được stent phủ hết. Theo Neglen, sự thông thoáng của stent tầng chậu đùi không phụ thuộc vào vị trí của đầu dưới stent, phía trên hoặc phía dưới nếp lằn bẹn, mà phụ thuộc vào mức độ hẹp trước khi đặt stent, và sự tồn tại hay không của tổn thương tắc nghẽn không được can thiệp ở phía trên.

Bước 4: Kiểm tra lại bằng IVUS và kết thúc can thiệp
Tiến hành nong bóng sau đặt stent. IVUS nên được thực hiện lại để xác định đường kính tĩnh mạch chậu đùi đã trở về bình thường, hoặc sử dụng bóng lớn hơn để tiếp tục mở rộng thêm
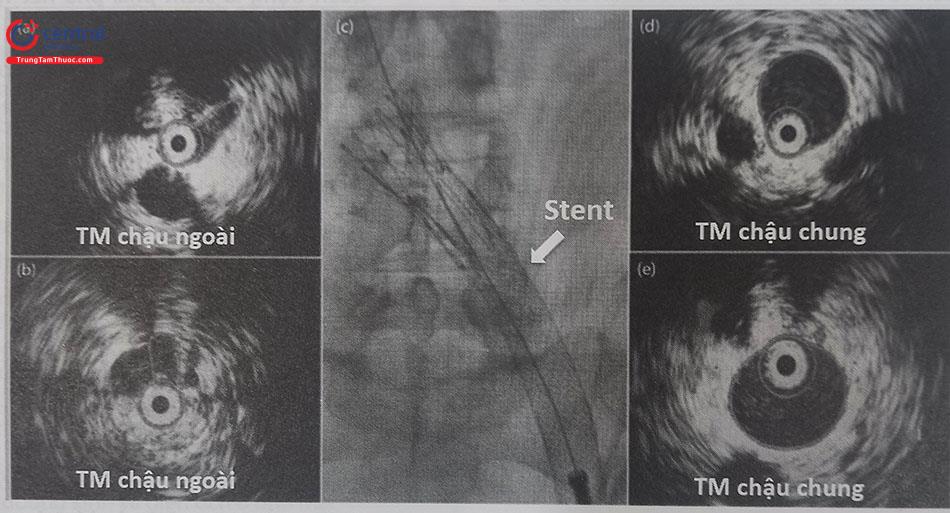
Chú thích: TM: Tĩnh mạch; IVUS: Siêu âm trong lòng mạch.
6 Tiêu chí đánh giá thành công
Can thiệp nong và đặt stent tĩnh mạch chậu đùi được đánh giá là thành công khi:
- Quá trình can thiệp diễn ra thuận lợi, không xảy ra biến chứng.
- Kiểm tra bằng siêu âm trong lòng mạch (IVUS) và chụp tĩnh mạch sau can thiệp thấy stent ở đúng vị trí, không còn hẹp lòng tĩnh mạch tồn dư.
- Bệnh nhân có thể xuất viện an toàn vào ngày hôm
7 Biến chứng và xử lý
Can thiệp nong và đặt stent tĩnh mạch điều trị HCHHK được coi là một kỹ thuật an toàn. Tổng hợp từ 1500 ca can thiệp, Raju S. (2013) ghi nhận không có trường hợp nào tử vong hoặc thuyên tắc phổi cấp. Tỷ lệ biến chứng tại vị trí chọc dò dưới 1% và tỷ lệ biến chứng chảy máu nghiêm trọng dưới 0,03%. Tỷ lệ tái huyết khối trong stent sau 5 năm xấp xỉ 25% và tỷ lệ thuyên tắc thứ phát là 75-90%.
8 Kết quả can thiệp theo một số nghiên cứu
Kết quả điều trị nội tĩnh mạch của HCHHK tương đối khó phân loại và đánh giá vì sự không đồng nhất giữa các nghiên cứu lâm sàng, về cả hệ thống phân loại bệnh, chỉ định và tiêu chuẩn can thiệp, cũng như quần thể bệnh nhân gộp chung cả tổn thương huyết khối mạn tính với cấp tính tầng chậu, đùi hay thống kê cả tổn thương tầng chậu không do huyết khối (NIVL/non-thrombotic iliac vein lesion). Tuy nhiên, những dữ liệu hiện có chỉ ra tỷ lệ tái thông tĩnh mạch thành công sau can thiệp 6 tháng ở bệnh nhân bị HCHHK vào khoảng 70 – 80%, thấp hơn so với bệnh nhân NIVL sau can thiệp (95 – 100%), chủ yếu liên quan đến đặc điểm tổn thương tĩnh mạch và chất lượng giường mạch trước can thiệp. Kết quả lâm sàng thậm chí còn khó đánh giá hơn. Bên cạnh những tiêu chuẩn rõ ràng như sự cải thiện thang điểm Villalta hay r-VCSS, khá nhiều nghiên cứu chỉ đề cập đến sự “giảm triệu chứng”, “giảm phù”, “cải thiện một phần”. Một số nghiên cứu khác đưa triệu chứng “đau cách hồi tĩnh mạch” vào cải thiện tình trạng lâm sàng nhưng cũng không có định nghĩa rõ ràng. Vì vậy, kết quả tổng hợp không đồng nhất, ví dụ tỷ lệ chữa lành vết loét sau can thiệp từ 56 – 100%, tỷ lệ loét tái phát từ 0 – 17%.
Bảng 59.3. Kết quả các nghiên cứu can thiệp tái thông tĩnh mạch chậu – đùi
| NGHIÊN CỨU | LOẠI | QUẦN THỂ BỆNH NHÂN | N | KẾT QUẢ |
|---|---|---|---|---|
| Neglen, 2007 | Thuần tập tiến cứu | HCHHK và không do HK | 982 | Giảm đau (62%), phù (32%), liền vết loét (58%) |
| Nayak, 2012 | Thuần tập hồi cứu | HCHHK | 45 | Giảm đau (42%), phù (55%), liền vết loét (86%) |
| Ozugkurt, 2008 | Thuần tập tiến cứu | HCHHK | 30 | “Giảm triệu chứng” (25%) |
| Raju, 2009 | Thuần tập tiến cứu | HCHHK và không do HK | 139 | Giảm đau (79%), phù (66%), liền vết loét (56%) |
| Rosales, 2010 | Thuần tập tiến cứu | HCHHK | 34 | Giảm VCSS ở nhóm CEAP C3 (9 xuống 1) và C6 (21 xuống 7) |
| Meng, 2011 | Thuần tập tiến cứu | Không do HK (NIVL) | 296 | Giảm phù (84%), liền vết loét (85%) |
| Alhadad, 2011 | Thuần tập hồi cứu | HCHHK | 70 | Giảm đau (41%), phù (24%), liền vết loét (80%) |
| Alhalbouni, 2012 | Thuần tập hồi cứu | HCHHK và không do HK | 56 | Liền vết loét (58%) |
| Ye, 2012 | Thuần tập hồi cứu | Không do HK (NIVL) | 224 | Giảm phù (89%), liền vết loét (82%) |
| Ye, 2012 | Thuần tập hồi cứu | HCHHK | 118 | Giảm đau (72%), phù (70%), liền vết loét (78%) |
Chú thích: HCHHK: Hội chứng hậu huyết khối; HK: Huyết khối.
Theo dõi 504 bệnh nhân có tắc nghẽn tầng chậu mạn tính kèm theo suy van tĩnh mạch sâu, được can thiệp nội tĩnh mạch, Raju S. đã chỉ ra kết quả giảm đau là 78%, giảm phù là 55% sau 5 năm. Điều này nhấn mạnh lợi ích của can thiệp đặt stent trong cải thiện các triệu chứng mặc dù vẫn tồn tại dòng trào ngược bệnh lý. Một nghiên cứu khác của Yin M., so sánh hai nhóm bệnh nhân HHKTM, gồm 122 người được điều trị nội mạch, và 94 người chỉ điều trị bảo tồn với băng ép áp lực (30 – 40 mmHg). Ở thời điểm 24 tháng, điều trị nội mạch có hiệu quả vượt trội ở nhóm HHKTM nặng nhất (Villalta 16,1 ± 4,9 so với 11 ± 5,9), trong khi không có hiệu quả ở nhóm HHKTM trung bình (Villalta 6,6 ± 2,4 so với 5,7 ± 3). Nhóm điều trị can thiệp có tỷ lệ lành vết loét cao hơn (86,6 so với 70,6%). Vì vậy, theo các khuyến cáo quốc tế hiện tại, can thiệp nong tĩnh mạch và đặt stent có thể được xem xét cho những bệnh nhân có triệu chứng tắc nghẽn tĩnh mạch chậu mạn tính (Villalta ≥ 10 hoặc triệu chứng đau kéo dài, loét, đau cách hồi chi dưới). Quản lý các bệnh nhân HHKTM giai đoạn nặng cần được thực hiện bởi nhóm đa ngành, tập hợp nhiều chuyên gia, phối hợp với bác sĩ can thiệp để hội chẩn, chỉ định và theo dõi cho từng trường hợp cụ thể.
9 Theo dõi sau can thiệp
9.1 Băng chun, tất áp lực
Sau can thiệp, bệnh nhân nên được sử dụng tất áp lực (30-40 mmHg) ít 80% thời gian trong ngày (tốt nhất là bắt đầu đeo từ sau khi ngủ dậy, và chỉ tháo ra trước lúc đi ngủ) kéo dài ít nhất 6 tháng. Bệnh nhân được khuyên nên vận động sớm, và đi bộ càng sớm càng tốt.
9.2 Thuốc chống đông
Hội Tim mạch Hoa Kỳ vào năm 2011 đề nghị sử dụng thuốc chống đông liều điều trị sau khi đặt stent tĩnh mạch (IIa/C), thậm chí phối hợp với thuốc chống kết tập tiểu cầu ở những bệnh nhân được coi là có nguy cơ tái phát huyết khối cao (IIb/C). Tuy nhiên, vẫn chưa có sự thống nhất về lựa chọn loại thuốc chống đông cũng như thời gian điều trị chống huyết khối sau nong và đặt stent tĩnh mạch.
Đồng thuận Delphi (International Delphi consensus) năm 2018 ghi nhận ý kiến của 106 chuyên gia với 12 quan điểm điều trị khác nhau sau khi nong và đặt stent tĩnh mạch, trong đó 1/3 đề nghị dùng kháng vitamin K kéo dài, 20% dùng NOACs kéo dài, 35% ngừng điều trị sau 6 – 12 tháng, 25% sử dụng thuốc chống kết tập tiểu cầu khi ngừng điều trị chống đông. Một số kết luận từ giai đoạn 2 của đồng thuận được tóm tắt dưới đây:
- Điều trị chống đông được ưu tiên hơn liệu pháp chống kết tập tiểu cầu sau khi đặt stent tĩnh mạch (72% đồng ý);
- Điều trị chống đông nên được ngừng sau 6 – 12 tháng kể từ lần thuyên tắc huyết khối tĩnh mạch đầu tiên (87% đồng ý);
- Điều trị chống đông cần duy trì nếu có nhiều đợt bị TT-HKTM (85% đồng ý).
Tuy nhiên, điều trị thuốc chống kết tập tiểu cầu vẫn chưa đạt được sự đồng thuận. Một phân tích hồi cứu từ năm 2008 đến năm 2017 đã đánh giá tác dụng của liệu pháp kháng tiểu cầu đối với tình trạng bệnh nhân sau khi đặt stent chủ chậu (n = 62), trong đó 54,8% bệnh nhân có tiền sử HKTMSCD. Tỷ lệ tái thông tiên phát và thứ phát sau 12 tháng lần lượt là 70 và 92,4%. Sau khi đặt stent, 97% bệnh nhân được điều trị chống đông (48,4% dùng warfarin, 62,9% dùng enoxaparin, 25,8% dùng kháng yếu tố Xa); 38 bệnh nhân (61,3%) cũng được điều trị chống kết tập tiểu cầu (aspirin 41,9%, Clopidogrel 12,9%, kháng tiểu cầu kép 6,4%); 36 trong số 38 bệnh nhân này được điều trị đồng thời thuốc chống đông. Phân tích đa biến chỉ ra liệu pháp kháng tiểu cầu là yếu tố dự báo duy nhất của tình trạng tắc stent (HR = 0,28, KTC 95%: 0,10–0,83 đối với tắc stent). Trong trường hợp không phối hợp liệu pháp chống kết tập tiểu cầu, phần lớn các trường hợp tái phát huyết khối xảy ra trong tháng đầu tiên, và còn kéo dài đến tháng thứ 15. Sáu trường hợp chảy máu đã được báo cáo, trong đó có ba trường hợp chảy máu nặng (một trường hợp khi chuyển tiếp kháng vitamin K và Aspirin, một trường hợp dùng Enoxaparin cùng aspirin, trường hợp thứ ba dùng rivarox- aban và thuốc kháng tiểu cầu kép).
9.3 Siêu âm mạch máu
Siêu âm Doppler được thực hiện vào ngày đầu tiên sau can thiệp. Vì huyết khối gây tắc stent có thể được tái thông bằng tiêu sợi huyết trong vòng 14 ngày sau khi xảy ra biến cố, và hầu hết các biến chứng huyết khối xảy ra ngay sau khi can thiệp, nên làm siêu âm lần hai trong vòng hai tuần sau khi đặt stent. Lịch theo dõi tiếp theo là thời điểm sau 3 tháng, 6 tháng, 12 tháng và định kỳ hàng năm. Tái hẹp trong stent trước tiên được xử trí bằng thay đổi hoặc tăng liều thuốc chống đông. Nếu có sự kết hợp giữa triệu chứng lâm sàng tăng lên, song song với việc giảm hiệu quả của stent qua từng giai đoạn theo dõi, bệnh nhân nên được làm lại IVUS, sau đó có thể nong bóng lại stent và/hoặc đặt thêm stent tùy thuộc vào tổn thương khi can thiệp lại.
10 Kết luận
Hội chứng hậu huyết khối tĩnh mạch là một biến chứng mạn tính khá phổ biến của huyết khối tĩnh mạch sâu chi dưới, có thể điều trị được nhưng không thể chữa khỏi hoàn toàn. Can thiệp nội tĩnh mạch qua da có thể được chỉ định cho những bệnh nhân có triệu chứng ở giai đoạn nặng, với nguy cơ biến chứng và tử vong rất thấp, giúp cải thiện triệu chứng, đặc biệt là giảm đau và phù, cũng như có hiệu quả chữa lành vết loét, nâng cao chất lượng cuộc sống, giảm đáng kể tình trạng suy giảm chức năng vận động do bệnh gây ra.
11 Tài liệu tham khảo
- Erin H. Murphy and Seshadri Raju. Endovascular treatment of post-thrombotic iliofemoral venous obstruction. Handbook of Venous and Lymphatic Disorders-Guidelines of the American Venous Forum-CRC Press (2017), 533-540.
- Marianne G De Maeseneer et European Society for Vascular Surgery (ESVS) 2022 Clinical Practice Guidelines on the Management of Chronic Venous Disease of the Lower Limb. Eur J Vasc Endovasc Surg (2022) 63, 184-267.
- Kahn S.R., Comerota A.J., Cushman M. American Heart Association Council on Peripheral Vascular Disease, Council on Clinical Cardiology, and Council on Cardiovascular and Stroke Nursing. The postthrombotic syndrome: evidence-based prevention, diagnosis, and treatment strategies: a scientific statement from the American Heart Association. Circulation. 2014;130:1636–1661.
- Villalta S., Bagatella , Piccioli A. Assessment of validity and reproducibility of a clinical scale for the postthrombotic syndrome. Haemostasis. 1994;24:158a.
- Neglen , Hollis K.C., Olivier J. Stenting of the venous outflow in chronic venous disease : long-term stent-related outcome, clinical, and hemodynamic result. J Vasc Surg. 2007;46:979–990.
- Nayak L., Hildebolt F., Vedantham S. Postthrombotic syndrome: feasibility of a strategy of imaging-guided endovascular intervention. J Vasc Interv Radiol. 2012;23:1165–1173.
- Raju S., Neglen Percutaneous recanalization of total occlusions of the iliac vein. J Vasc Surg. 2009;50:360–368.
- Rosales , Sandbaek G., Jorgensen J.J. Stenting for chronic post-thrombotic vena cava and iliofemoral venous occlusions: mid-term patency and clinical outcome. Eur J Vasc Endovasc Surg. 2010;40:234–240.
- Meng Y., Li X.Q., Qian A.M. Endovascular treatment of iliac vein compression syndrome. Chin Med J (Engl). 2011;124:3281–3284.
- Alhadad A., Kolbel , Herbst A. Iliocaval vein stenting: Long term survey of postthrombotic symptoms and working capacity. J Thromb Thrombolysis. 2011;31:211–216.
- Alhalbouni S., Hingorani A., Shiferson A. Iliac-femoral venous stenting for lower extremity venous stasis symptoms. Ann Vasc Surg. 2012;26:185–189.
- Ye , Lu X., Jiang M. Technical details and clinical outcomes of transpopliteal venous stent placement for postthrombotic chronic total occlusion of the iliofemoral vein. J Vasc Interv Radiol. 2014;25:925–932.
- Vedantham S., Sista A.K., Klein S.J. Quality improvement guidelines for the treatment of lower-extremity deep vein thrombosis with use of endovascular thrombus removal. J Vasc Interv Radiol. 2014;25:1317–1325.
- Raju S., Darcey R., Neglen Unexpected major role for venous stenting in deep reflux disease. J Vasc Surg. 2010;51:401–408.
- Yin , Shi H., Ye K. Clinical assessment of endovascular stenting compared with compression therapy alone in post-thrombotic patients with iliofemoral obstruction. Eur J Vasc Endovasc Surg. 2015;50:101–107.
- Raju Best management options for chronic iliac vein stenosis and occlusion. J Vasc Surg. 2013;57:1163–1169.

