Cách phân biệt và xử trí tắc nghẽn van tim nhân tạo ở người cao tuổi
Đại học Y Dược Thành phố Hồ Chí Minh - Bộ môn Lão khoa
Chủ biên PGS.TS.BS. Nguyễn Văn Tân
PGS.TS.BS. Nguyễn Văn Trí
TS.BS. Nguyễn Thanh Huân
Các tác giả tham gia biên soạn
Nguyễn Thanh Huân
Bệnh lý tim mạch là một trong những bệnh lý thường gặp ở người cao tuổi. Với sự phát triển của y học, đã có nhiều can thiệp nhân tạo để khắc phục những bệnh lý này, ví dụ như van tim nhân tạo. Tuy nhiên, người bệnh sử dụng van tim nhân tạo cần được theo dõi sát sao để tránh được biến chứng nguy hiểm như tắc van tim nhân tạo, nhất là do huyết khối. Trong bài viết này, Trung Tâm Thuốc Central Pharmacy (trungtamthuoc.com) xin gửi đến bạn đọc thông tin về cấp cứu tắc nghẽn van tim nhân tạo do huyết khối ở người cao tuổi.
1 Mở đầu
Bệnh lý van tim là một trong nhóm các bệnh lý tim mạch có thể gặp ở mọi lứa tuổi, bao gồm ở người cao tuổi. Mặc dù có những tiến bộ trong thay van tim qua ống thông, như thay van động mạch chủ qua ống thông (transcatheter aortic valve replacement, TAVR), phẫu thuật thay van tim nhân tạo (prosthetic heart valves) vẫn được tiến hành ở những bệnh nhân có chỉ định phù hợp. Dựa vào các tiêu chuẩn đánh giá, bệnh nhân sẽ được chỉ định thay van tim sinh học (bioprosthetic heart valves, BHVs) hoặc thay van tim cơ học (mechanical heart valves, MHVs). Tắc nghẽn van nhân tạo cơ học (mechanical valve obstruction, MVO) là một trong những biến chứng mặc dù hiếm gặp nhưng có thể đe dọa tính mạng của bệnh nhân, đặc biệt là kẹt van do huyết khối. Việc bỏ sót chẩn đoán hoặc điều trị sai biến chứng này có thể dẫn đến tình huống lâm sàng gây tử vong cho bệnh nhân. Do đó, bài trình bày này tập trung vào việc chẩn đoán và điều trị kẹt van tim nhân tạo cơ học, đặc biệt trên đối tượng người cao tuổi.
2 Tổng quan về van tim nhân tạo cơ học
2.1 Lịch sử phát triển và cấu tạo của van tim nhân tạo cơ học
Phẫu thuật van tim đầu tiên được thực hiện vào năm 1952. Trong năm 1957, Albert Starr và Lowell Edwards đã tạo ra van cơ học có cấu trúc hình lồng và bóng (ball-and-cage) và trở thành van nhân tạo đầu tiên được thương mại hóa. Vài thập kỷ sau đó là cuộc cách mạng của van tim nhân tạo cơ học 2 mảnh (bileaflet mechanical valve), được phát triển trong năm 1976. Tuy nhiên, hình thái và bề mặt van tim nhân tạo cơ học không sinh lý như van tim tự nhiên dẫn đến nguy cơ hình thành huyết khối. Đến nay, vấn đề tạo huyết khối van tim vẫn là biến chứng đáng quan ngại khi sử dụng van tim nhân tạo cơ học, đặc biệt trong 6 tháng đầu tiên sau phẫu thuật. Để giảm nguy cơ hình thành huyết khối, bệnh nhân cần được điều trị với thuốc kháng vitamin K (vitamin K antagonist, VKA) lâu dài. Nhưng điều này có thể dẫn đến nguy cơ chảy máu. Do đó, mặc dù được ghi nhận có độ bền cao hơn so với các van tim nhân tạo sinh học, thay thế van tim nhân tạo cơ học chỉ phù hợp cho nhóm bệnh nhân không chống chỉ định sử dụng thuốc kháng đông đường uống lâu dài.
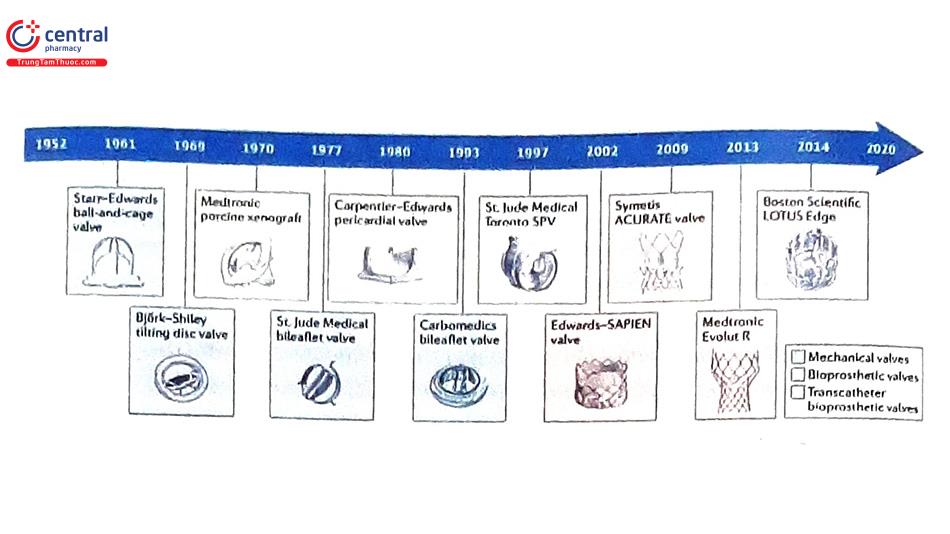
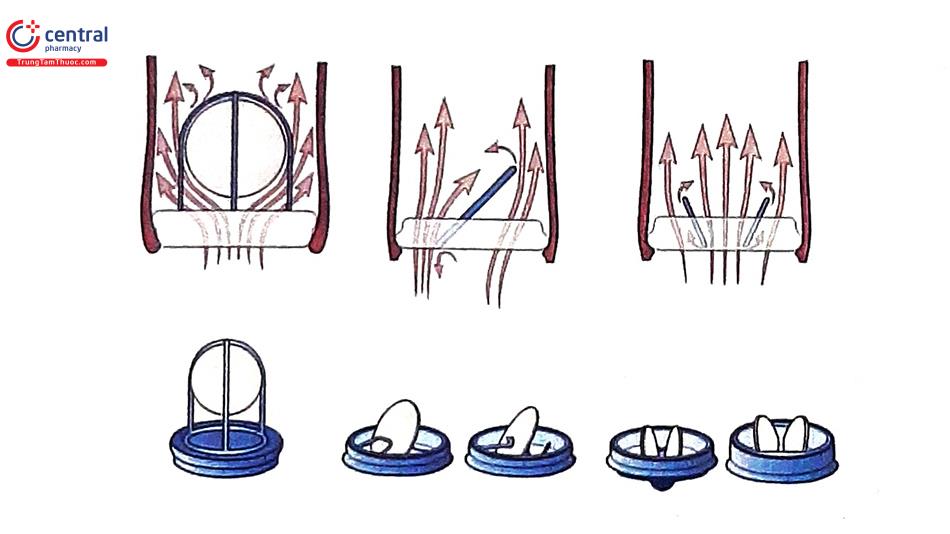
Hiện nay, gần như tất cả các trung tâm y khoa trên thế giới chỉ còn sử dụng van tim nhân tạo cơ học 2 mảnh để thay cho bệnh nhân có chỉ định thay van cơ học. Điều này liên quan đến chất lượng và huyết động học của loại van này. Các van cấu trúc dạng lồng và bóng có các dòng chảy qua van thiếu dòng trung tâm. Các van dạng đĩa nghiêng (tilting disc valves) tạo ra dòng máu rối loạn tại vị trí lỗ van nhỏ hơn. Trong khi đó, van tim cơ học 2 mảnh có các dòng chảy xuôi dòng tự nhiên hơn so với 2 loại trước.
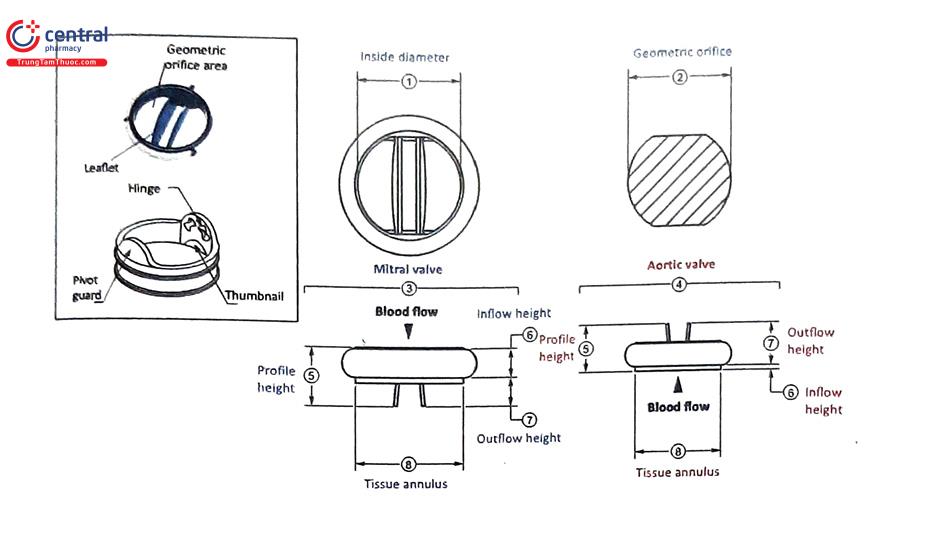
Về mặt cấu tạo, các van tim nhân tạo cơ học 2 mảnh được cấu thành từ vật liệu kim loại (titanium, cobalt và pyrolytic carbon) và polymers (polytetrafluorethylen, polyacetal, polyethylen terephthalate và Silicon). Trong đó, vật liệu pyrolytic carbon thường được lựa chọn do bề mặt vật liệu này có tính chất kháng hình thành huyết khối và không gây phản ứng phụ khi cấy vào cơ thể người. Vật liệu và kiểu dáng có thể khác nhau giữa các nhà sản xuất nhưng vẫn đảm bảo các thành phần cấu trúc cơ bản, bao gồm: 2 mảnh van bán nguyệt (semicircular leaflets) được gắn vào một giá đỡ vòng (annular stent) tại các điểm bản lề (hinge points); bao xung quanh giá đỡ vòng van là một vòng để khâu van tim vào vòng van (sewing ring). Các van tim nhân tạo cơ học 2 mảnh được thiết kế để có dòng chảy ngược (backflow) khi các lá van đóng, được gọi là các dòng hở rửa trôi (washing jets), được cho là có vai trò giảm nguy cơ hình thành huyết khối tại các điểm bản lề.
2.2 Chỉ định của van tim nhân tạo cơ học
Các yếu tố quyết định lựa chọn loại van nhân tạo phù hợp để thay thế cho bệnh nhân bao gồm: tuổi, kỳ vọng sống, lối sống, yếu tố môi trường, nguy cơ chảy máu và hình thành huyết khối liên quan thuốc kháng đông, nguy cơ phẫu thuật và quan trọng nhất là sự lựa chọn của bệnh nhân. Nhìn chung, van tim nhân tạo sinh học nên được lựa chọn cho các bệnh nhân có kỳ vọng sống được đánh giá ngắn hơn, có nhiều bệnh đồng mắc và có nguy cơ cao chảy máu liên quan đến dùng kháng đông. Đối với van cơ học, các chỉ định được trình bày trong Bảng 1.
Theo khuyến cáo năm 2021 của Hiệp hội Tim châu Âu (European Society of Cardiology, ESC) và Tổ chức Phẫu thuật Tim-lồng ngực châu Âu (European Association for Cardio-Thoracic Surgery, EACTS), van sinh học nên được xem xét ở các bệnh nhân >65 tuổi cho vị trí van động mạch chủ và >70 tuổi cho vị trí van 2 lá. Trong khi đó, van cơ học nên được xem xét ở các bệnh nhân <60 tuổi ở vị trí van động mạch chủ và bệnh nhân <65 tuổi ở vị trí van 2 lá. Như vậy, ở người cao tuổi, việc lựa chọn van sinh học được khuyến cáo hơn so với van cơ học. Tuy nhiên, trên thực tế, vẫn có một số tình huống bệnh nhân cao tuổi được thay van cơ học (ví dụ: sự lựa chọn của bệnh nhân) hoặc bệnh nhân được đặt van tim cơ học khi còn trẻ và vấn đề biến chứng xuất hiện khi bệnh nhân bước vào tuổi già, đặc biệt ở nhóm bệnh nhân thấp tim. Do đó, biến chứng huyết khối van tim nhân tạo cơ học vẫn có thể được ghi nhận ở người cao tuổi.
| Khuyến cáo | Nhóm | Mức độ bằng chứng |
| Van cơ học được khuyến cáo dựa trên mong muốn của bệnh nhân và nếu không có chống chỉ định dùng kháng đông lâu dài. | I | C |
| Van cơ học được khuyến cáo cho bệnh nhân có nguy cơ thoái hóa van cấu trúc (structural valve deterioration, SVD). | I | C |
| Van cơ học nên được xem xét ở các bệnh nhân đang dùng kháng đông do bệnh nhân đang có van cơ học ở vị trí khác. | IIa | C |
| Van cơ học nên được xem xét ở các bệnh nhân <60 tuổi ở vị trí van động mạch chủ và bệnh nhân <65 tuổi ở vị trí van 2 lá. | IIa | B |
| Van cơ học nên được xem xét ở các bệnh nhân với tuổi kỳ vọng sống hợp lý và có nguy cơ cao nếu phẫu thuật van tim lại hoặc thay van qua ống thông trong tương lai. | IIa | C |
| Van cơ học có thể được xem xét ở các bệnh nhân đang dùng kháng đông lâu dài liên quan bệnh nhân có nguy cơ cao của thuyên tắc huyết khối. | IIb | C |
3 Siêu âm tim đánh giá van tim nhân tạo cơ học
3.1 Siêu âm tim đánh giá hoạt động bình thường của van tim nhân tạo cơ học
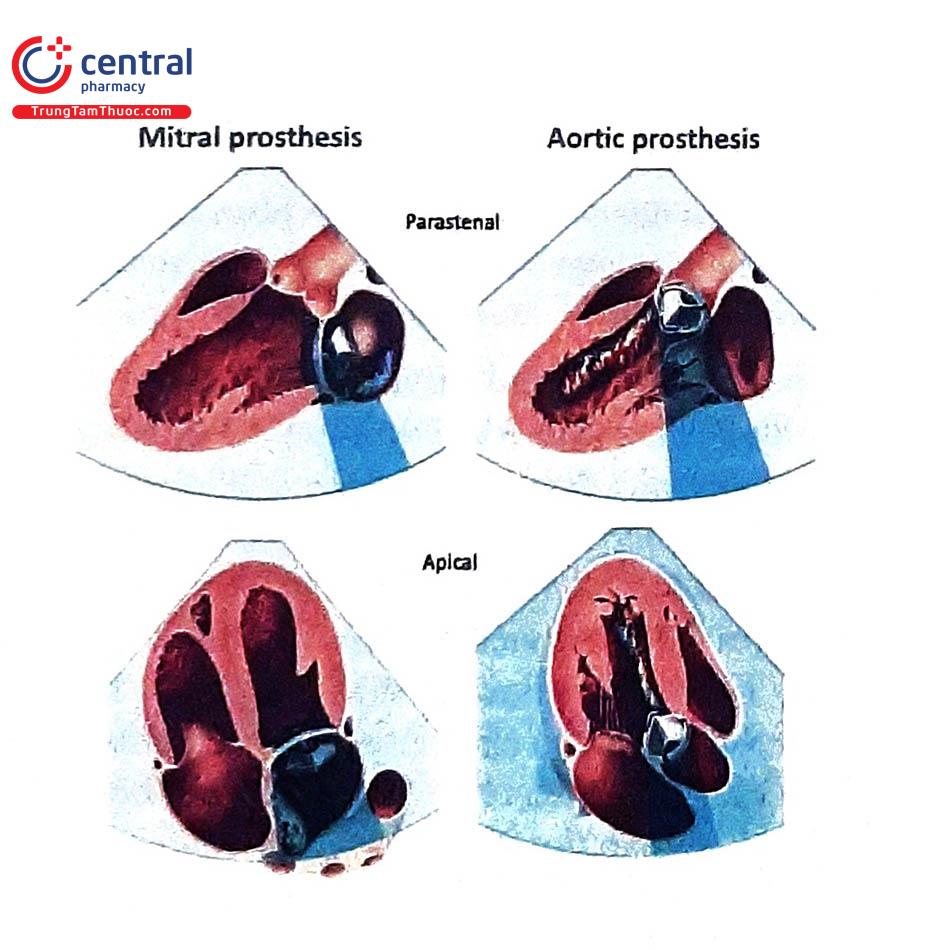
Siêu âm tim là một phương pháp chẩn đoán hình ảnh thường quy được sử dụng để đánh giá hoạt động van tim nhân tạo cơ học. Mặc dù vậy, do van tim cơ học có cấu trúc kim loại nên gây cản âm, dẫn đến khó khảo sát được cấu trúc sau van bị cản âm. Do đó, để đánh giá cấu trúc, hoạt động và chức năng của van tim nhân tạo cơ học, siêu âm tim cần thực hiện với nhiều mặt cắt khác nhau, kết hợp siêu âm tim 2D, 3D và Doppler. Trong một số trường hợp, bên cạnh siêu âm tim qua thành ngực (transthoracic echocardiography, TTE), bệnh nhân có thể cần được khảo sát siêu âm tim qua thực quản (transesophageal echocardiography, TEE) để đánh giá tốt hơn tình trạng của van tim nhân tạo cơ học.
.jpg)
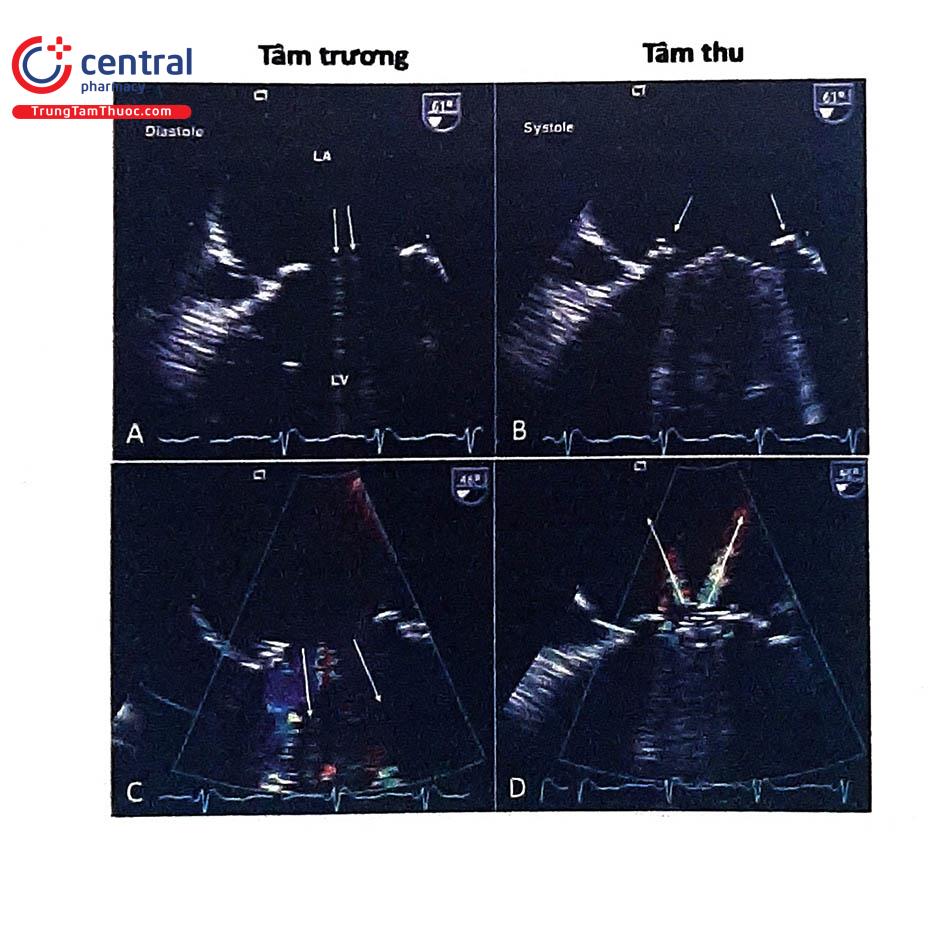
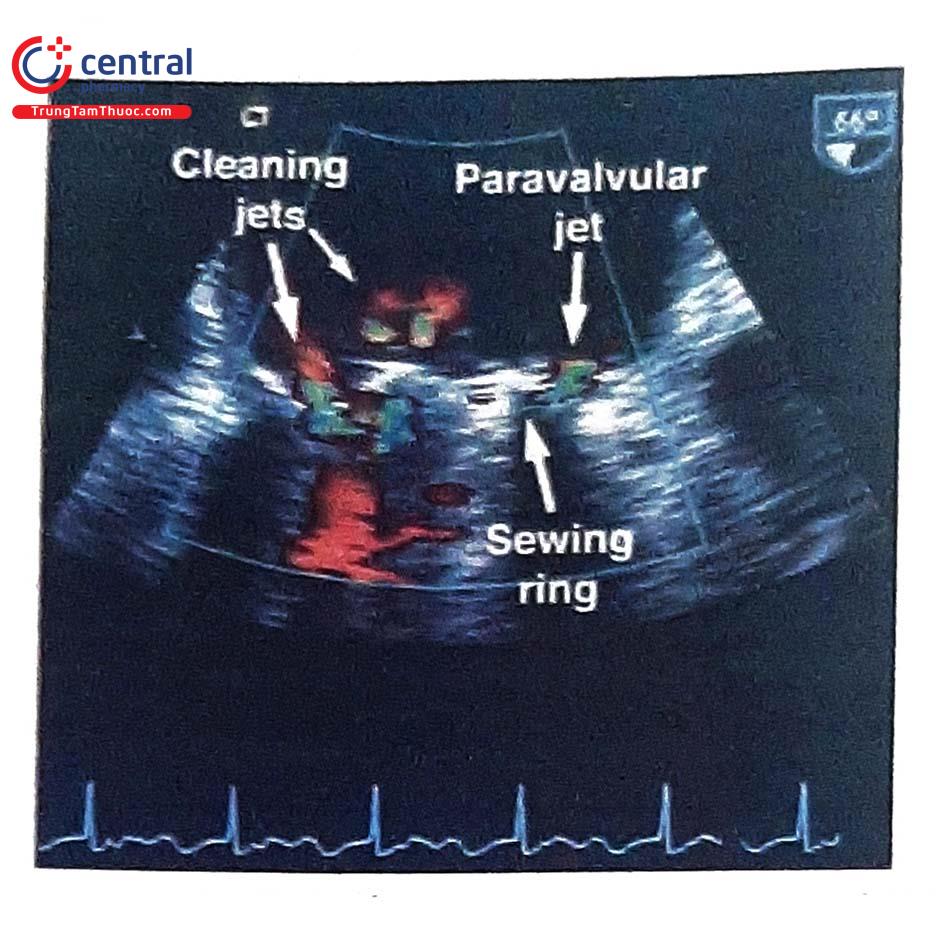
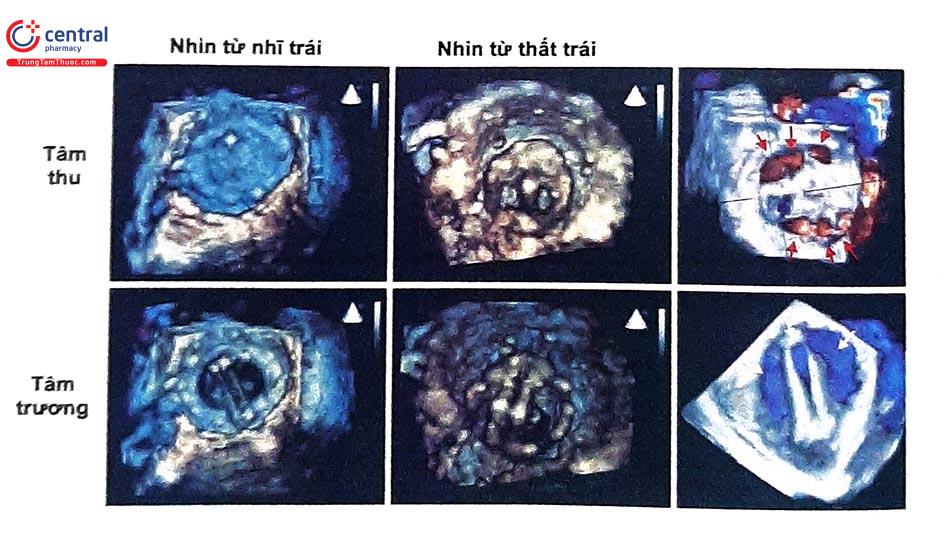
Bên cạnh khảo sát trên 2D và kết hợp 3D, quy trình siêu âm tim đánh giá tình trạng hoạt động và chức năng của van tim nhân tạo cơ học hay sinh học đều cần kết hợp với khảo sát Doppler với các đặc điểm cần khảo sát trình bày trong Bảng 2.
| Đặc điểm cần khảo sát | Van Động mạch chủ | Van 2 lá |
| Vận tốc đỉnh (peak velocity) | ✓ | ✓ |
| Chênh áp trung bình (mean gradient) | ✓ | ✓ |
| Đường viền vận tốc tống máu (contour of Jet velocity) | ✓ | |
| Thời gian gia tốc (acceleration time, AT) | ✓ | |
| Thời gian nửa áp lực (pressure half-time, PHT) | ✓ | |
| Diện tích lỗ van hiệu quả (effective orifice area, EOA) | ✓ | ✓ |
| Chỉ số vận tốc Doppler (Doppler velocity index, DVI) | ✓ | ✓ |
| Hở van sinh lý (physiologic regurgitation) | ✓ | ✓ |
| Tắc nghẽn/hẹp van tim nhân tạo | ✓ | ✓ |
Ở tình trạng bình thường, van tim nhân tạo có diện tích mở van thấp hơn so với van tim tự nhiên. Do đó, vận tốc ghi nhận ở van nhân tạo thường cao hơn so với vận tốc ở van tim tự nhiên. Mỗi van tim nhân tạo luôn có thông số riêng về kích thước van, vận tốc đinh, chênh áp trung bình và diện tích lỗ van hiệu quả. Do đó, tốt nhất cần biết được loại van tim nhân tạo bệnh nhân đã được cấy ghép nhằm tạo sự thuận lợi trong đánh giá van tim nhân tạo. Nếu không biết rõ thông số van tim nhân tạo của bệnh nhân, nghi ngờ hay chẩn đoán hẹp đáng kể van tim nhân tạo có thể dựa vào các mức thông số giới hạn cho phép (Bảng 3). Lưu ý, vận tốc đỉnh tăng đơn thuần không đủ để chẩn đoán xác định có tắc nghẽn van nhân tạo vì có thể gặp trong cung lượng tim cao hay bất tương hợp van-bệnh nhân (patient-prosthesis mismatch, PPM).
| Thông số | Bình thường | Nghi ngờ hẹp | Gợi ý hẹp đáng kể |
| Van động mạch chủ nhân tạo | |||
| Vận tốc đỉnh (m/s) | <3 | 3-4 | >4 |
| Chênh áp trung bình (mmHg) | <20 | 20-35 | >35 |
| Chỉ số vận tốc Doppler DVI | ≥0,30 | 0,29-0,25 | <0,25 |
| Diện tích lỗ van hiệu quả EOA (cm2) | >1,2 | 1,2-0,8 | <0,8 |
| Đường viền vận tốc tống máu | Hình tam giác, đỉnh đến sớm | Hình tam giác đến trung gian | Hình bo tròn, đối xứng |
| Thời gian gia tốc AT (ms) | <80 | 80-100 | >100 |
| Van 2 lá nhân tạo | |||
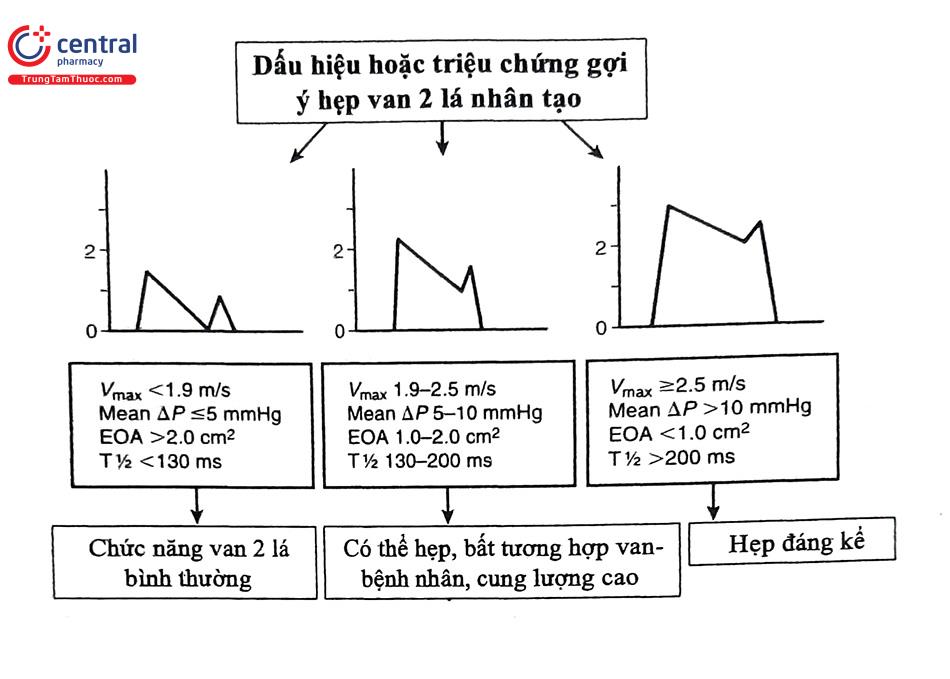
| Vận tốc đỉnh (m/s) | <1,9 | 1,9-2,5 | ≥2,5 |
| Chênh áp trung bình (mmHg) | ≤5 | 6-10 | >10 |
| Tỷ số VTIPrMV/VTILVO | <2,2 | 2,2-2,5 | >2,5 |
| Diện tích lỗ van hiệu quả EOA (cm2) | ≥2,0 | 1-2 | <1 |
| Thời gian nửa áp lực PHT | <130 | 130-200 | >200 |
.jpg)
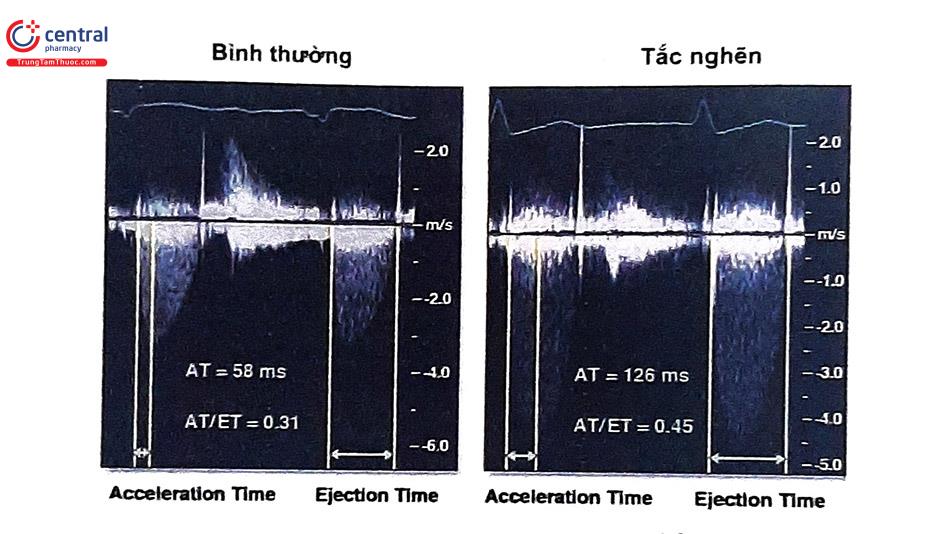
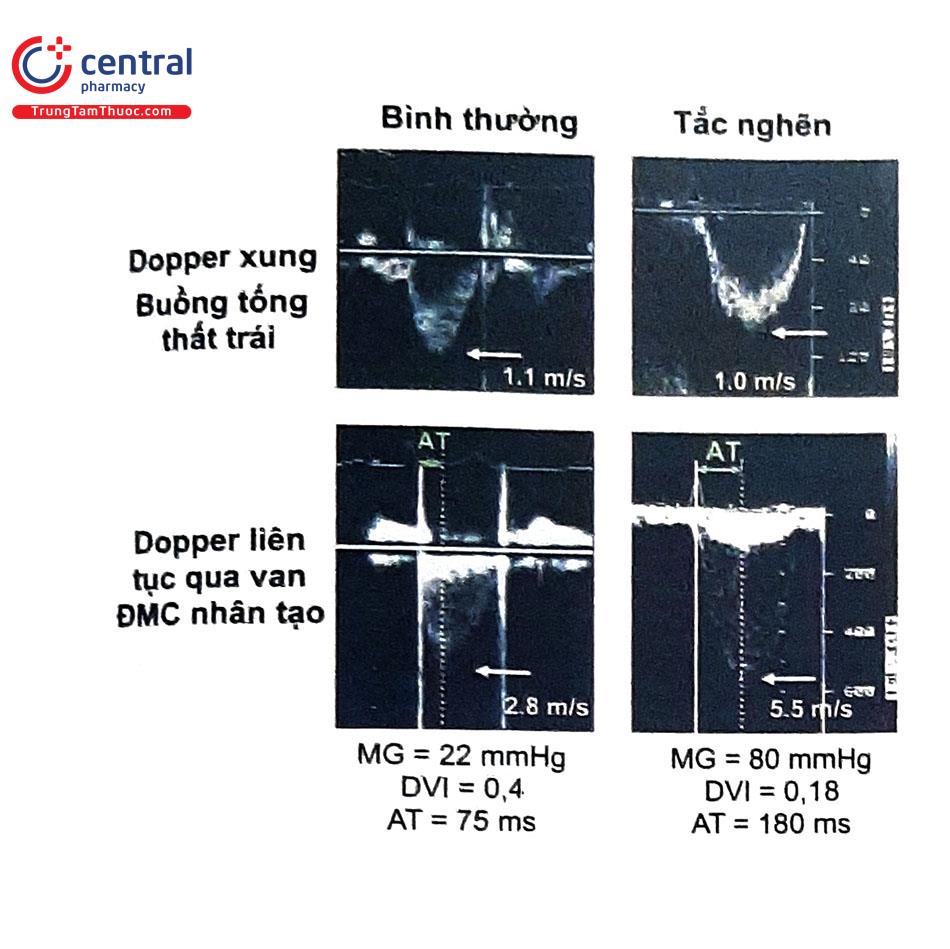
Trong đánh giá van 2 lá nhân tạo, vận tốc định có thể tăng trong các tình trạng tăng động tim, nhịp tim nhanh, kích thước van nhỏ hoặc có hở van 2 lá đi kèm. Trong van tim cơ học 2 mảnh bình thường, vận tốc đỉnh thường <1,9 m/s nhưng cũng có thể đạt đến 2,4 m/s. Chênh áp trung bình cao có thể liên quan tình trạng tăng động tim, nhịp tim nhanh hoặc bất tương hợp van-bệnh nhân, hở van 2 lá đi kèm hoặc hẹp van. Trong khi đánh giá van động mạch chủ nhân tạo cần khảo sát 2 thông số là AT và DVI, thì trong đánh giá van tim 2 lá nhân tạo cần khảo sát 2 thông số là thời gian nửa áp lực PHT và VT Im VTIvo PHT có thể không chính xác khi nhịp tim nhanh, blốc nhĩ thất độ I, khi sóng E và A hợp lại với nhau hoặc khi thời gian tâm trương quá ngắn. Tăng PHT khi khảo sát nhiều lần hoặc tăng đáng kể trong 1 lần đo (>200 ms) có thể là bằng chứng của tắc nghẽn van tim 2 lá nhân tạo.
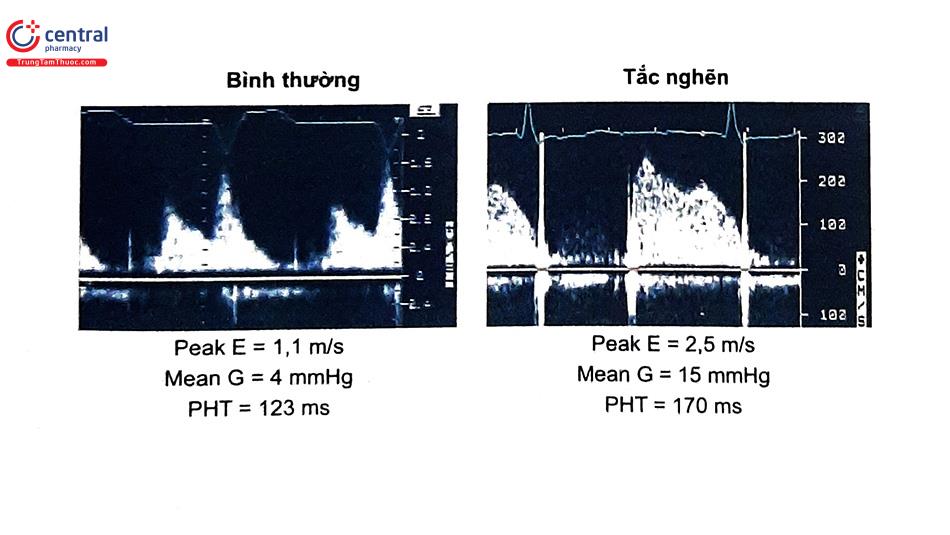
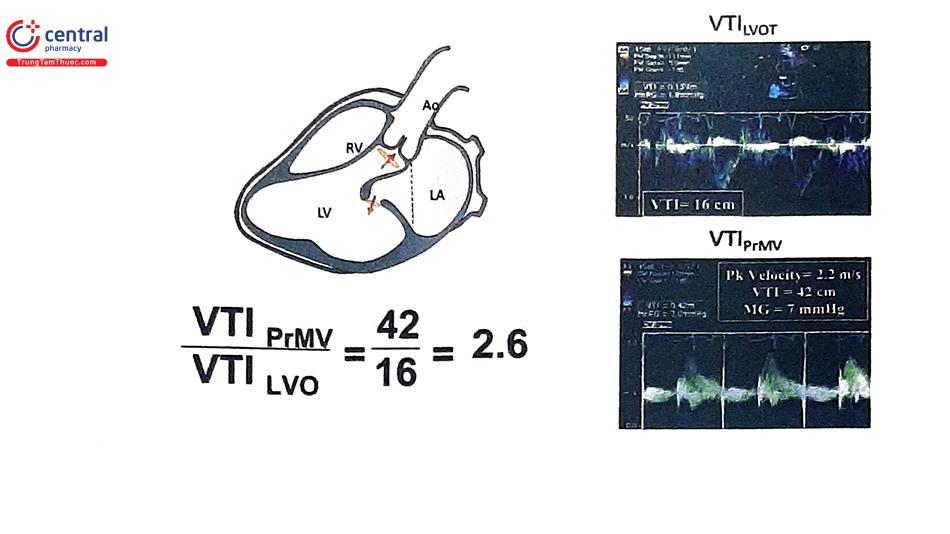
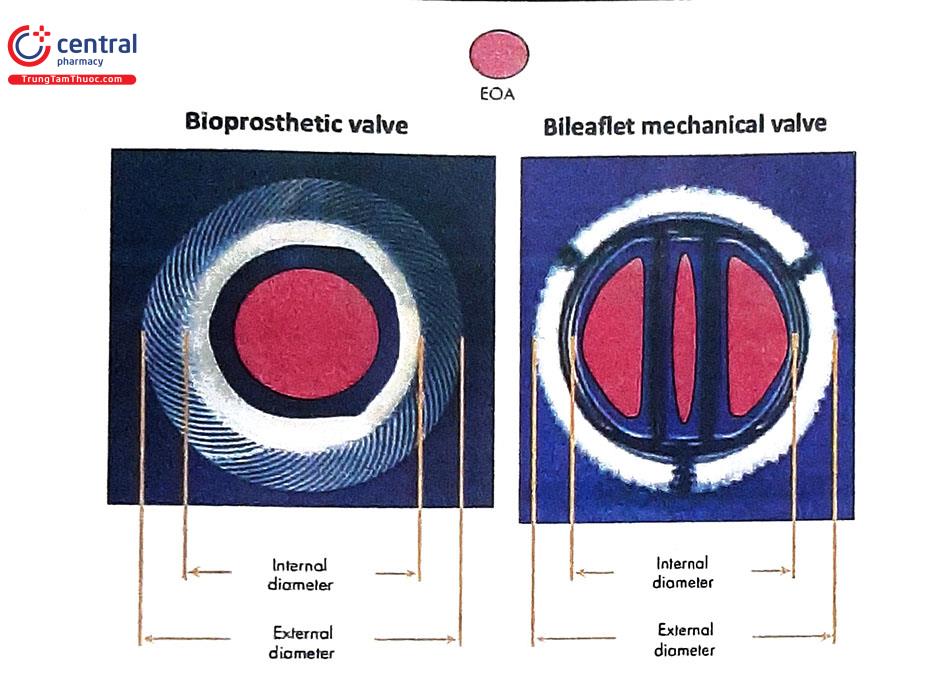
Một trong những thông số quan trọng trong đánh giá van tim nhân tạo là diện tích lỗ van hiệu quả (effective orifice area, EOA). EOA là thông số khác với thông số diện tích lỗ van hình học (geometric orifice area, GOA). GOA là diện tích lỗ van tim bên trong theo lý thuyết để dòng máu đi qua. GOA có thể được tính toán từ đường kính lỗ van bên trong (internal orifice diameter) của phần giá đỡ thuộc cấu trúc van nhân tạo và được cung cấp bởi nhà sản xuất. Trong khi đó, EOA luôn luôn nhỏ hơn GOA và phản ánh diện tích chức năng thật sự của van tim nhân tạo hơn do chênh áp qua van tim nhân tạo tương quan ναι EOA tốt hơn so với GOA. Ở cả van động mạch chủ hay 2 lá nhân tạo, EOA nên được tính toán dựa vào phương pháp phương trình liên tục (continuity equation method). Tính EOA từ thời gian nửa áp lực PHT có thể phù hợp cho van 2 lá tự nhiên nhưng không đúng khi áp dụng trên van 2 lá nhân tạo. Có hai vấn đề cần lưu ý khi đo EOA: (1) sai sót đo đạc các thành tố trong công thức tính EOA có thể dẫn đến sai số kết quả EOA và (2) ở van nhân tạo cơ học 2 mảnh, lỗ van trung tâm là nhỏ nhất với vận tốc cao hơn so với 2 lỗ 2 bên, dẫn đến đánh giá thấp giá trị EOA so với thực tế.
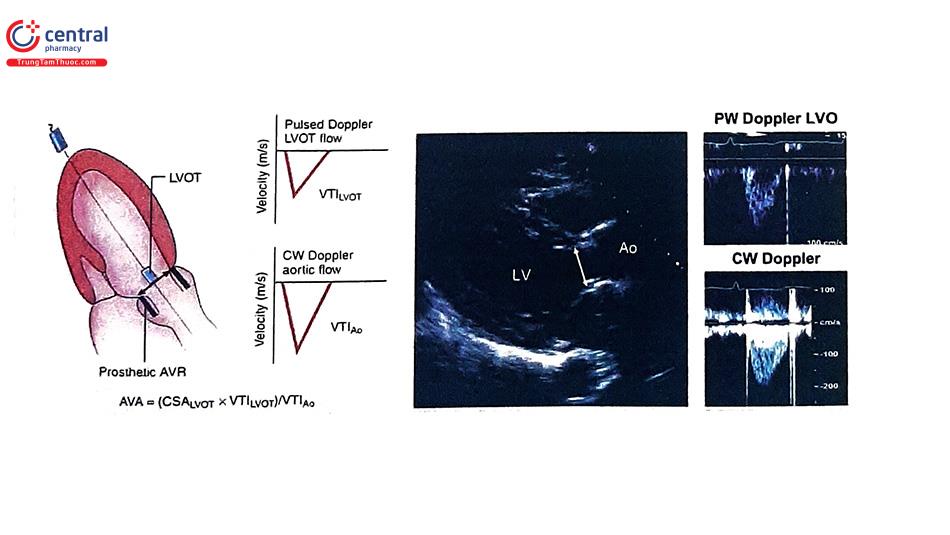
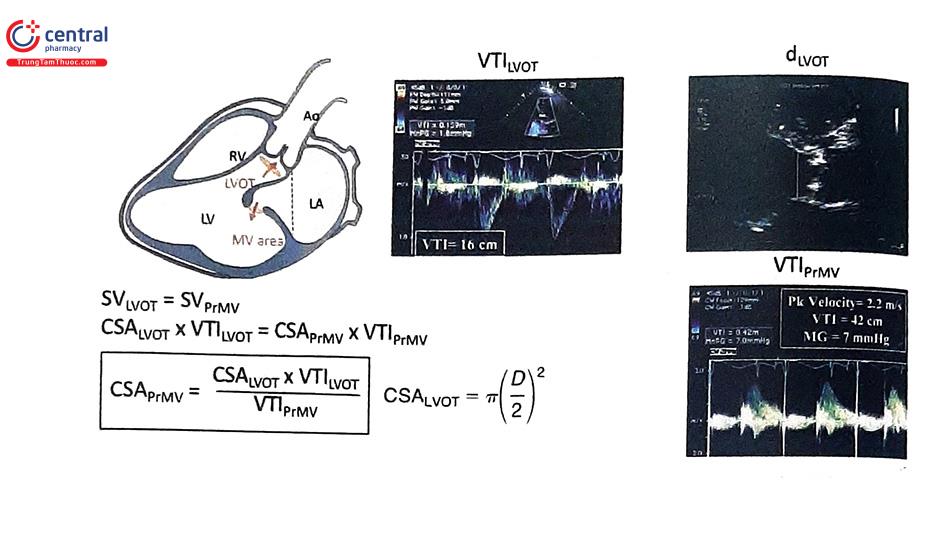
3.2 Siêu âm tim chẩn đoán tắc nghẽn/hẹp van tim nhân tạo cơ học
3.2.1 Chẩn đoán tắc nghẽn/hẹp van tim động mạch chủ cơ học
Bệnh nhân đang có van tim nhân tạo nếu xuất hiện âm thổi mới đi kèm với biểu hiện suy tim sung huyết thì cần thực hiện siêu âm tim qua thành ngực khẩn cấp để đánh giá van tim nhân tạo và nếu cần thì thực hiện siêu âm tim qua thực quản. Tuy nhiên, các nghi ngờ ban đầu của hẹp van nhân tạo có thể đến từ siêu âm tim thường quy ghi nhận có tăng vận tốc đỉnh bất thường qua van tim nhân tạo. Mặc dù vậy, một mình vận tốc cao không đủ để kết luận có tắc nghẽn/hẹp van nhân tạo vì có thể nằm trong tình huống tăng cung lượng tim hoặc bất tương hợp van-bệnh nhân (PPM). Ở chiều ngược lại, bệnh nhân có tắc nghẽn hẹp van nhân tạo có thể không có vận tốc đỉnh cao do tình trạng cung lượng tim thấp (ví dụ: bệnh nhân có phân suất tống máu thất trái giảm nặng). Ngoài ra, Doppler ghi nhận chênh áp có thể tăng giả tạo ở các van nhân tạo cơ học 2 mảnh do hiện tượng phục hồi áp lực (pressure recovery) tại mức van ở nhóm van tim này. Do đó, cần đánh giá nhiều thông số khi đo đạc (ví dụ: vận tốc, chênh áp, DVI và EOA), kết hợp với thông số van tim từ nhà sản xuất để đưa ra kết luận phù hợp trong chẩn đoán hẹp van nhân tạo. Nếu siêu âm tim qua thành ngực còn chưa rõ, có thể cần kết hợp thêm siêu âm tim qua thực quản, soi hoạt động van tim dưới tia X (fluoroscopy) hoặc chụp cắt lớp vi tính. Tuy nhiên, siêu âm tim qua thực quản có điểm hạn chế khi đánh giá van tim động mạch chủ cơ học do tính cản âm của van. Trong tình huống này, fluoroscopy và chụp cắt lớp vi tính có thể được chỉ định để đánh giá tính di động của mảnh van.
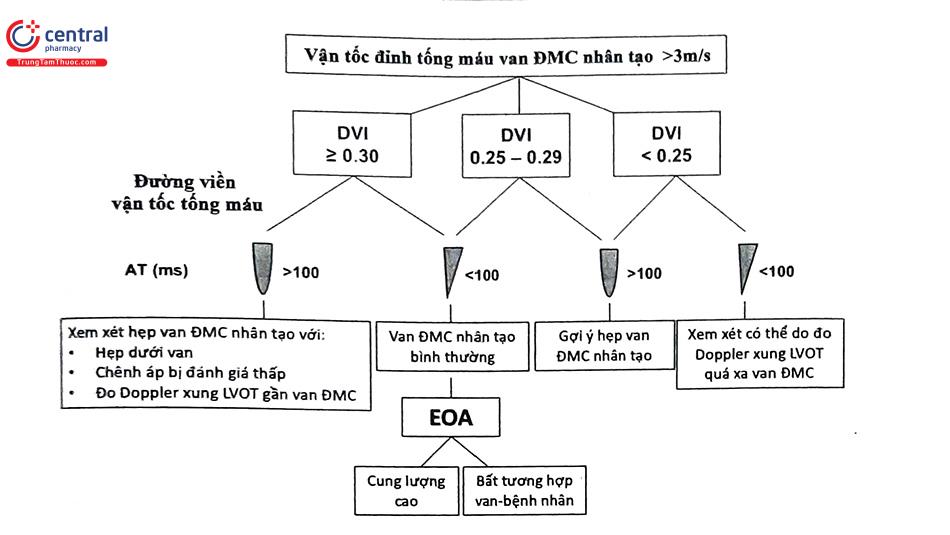
3.2.2 Chẩn đoán tắc nghẽn/hẹp van tim 2 lá cơ học
Tắc nghẽn van đáng kể có thể gợi ý khi thấy lá van dày hoặc giảm tính di động. Bên cạnh đó, các thông số vận tốc đỉnh E tăng, chênh áp trung bình tăng, thời gian nửa áp lực kéo dài và/hoặc tăng tỷ số VTIPrMV/VTIvo là những bằng chứng gợi ý có tắc nghẽn van tim nhân tạo 2 lá. Càng nhiều thông số bất thường càng gợi ý có tắc nghẽn van tim nhân tạo 2 lá. Tương tự như van động mạch chủ nhân tạo, vận tốc cao có thể nằm trong tình huống tăng cung lượng tim, bất tương hợp van-bệnh nhân (PPM) hoặc nhịp tim nhanh. Cần thiết có thể thực hiện siêu âm tim qua thực quản để đánh giá thêm. Khác với van động mạch chủ cơ học, siêu âm tim qua thực quản giúp có cái nhìn tốt hơn trong đánh giá van 2 lá cơ học.
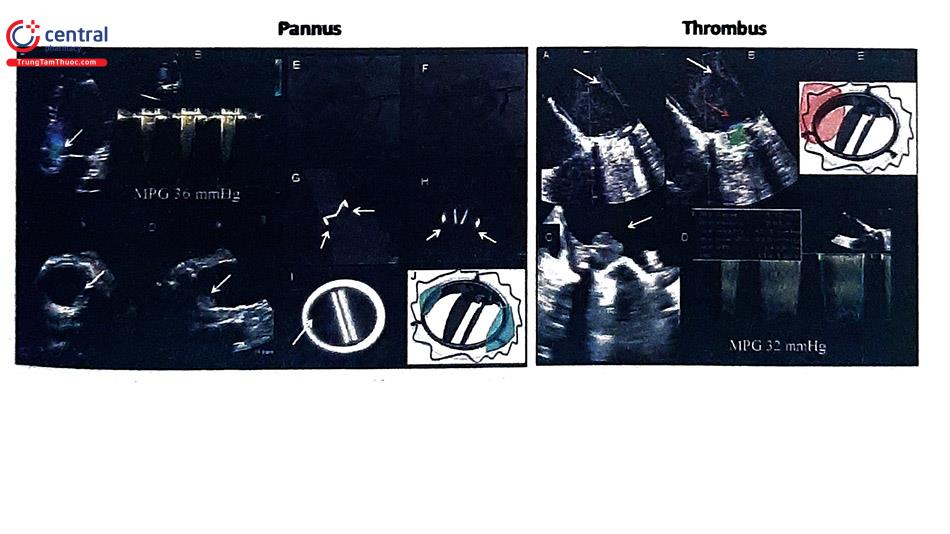
3.3 Phân biệt giữa huyết khối và pannus van tim nhân tạo
Huyết khối van tim nhân tạo hình thành liên quan chặt chẽ đến việc không kiểm soát tốt chống đông máu bằng thuốc kháng đông (ví dụ: INR thấp dưới ngưỡng điều trị). Thành phần chính của huyết khối là fibrin. Trong khi đó, pannus là một phản ứng viêm không liên quan miễn dịch của cơ thể đối với một vật thể lạ trong cơ thể là van nhân tạo. Thành phần chính của pannus là mô fibroelastic và Collagen. Huyết khối van nhân tạo thường gặp ở van cơ học hơn van sinh học. Huyết khối có thể gây tắc nghẽn van, gây kẹt lá van, gây hở van hoặc thuyên tắc nhưng cũng có thể được phát hiện khi siêu âm tim thường quy. Việc phân biệt giữa huyết khối và pannus có ý nghĩa quan trọng vì liên quan đến quyết định hướng điều trị cho bệnh nhân. Gần đây, thuốc tiêu sợi huyết được chứng minh có thể thay thế phẫu thuật trong điều trị tắc nghẽn van tim nhân tạo cơ học bên trái do huyết khối. Do đó, việc phân biệt hai cấu trúc này càng quan trọng nhằm tránh sử dụng thuốc tiêu sợi huyết cho pannus. Phân biệt hai cấu trúc này được trình bày trong Bảng 4.
| Pannus | Huyết khối | |
| Thời gian | Tối thiểu 12 tháng, thường >5 năm sau thay van tim | Xảy ra bất kỳ thời điểm nào (nếu trễ thường liên quan pannus) |
| Liên quan kháng đông (INR thấp) | Liên quan kém | Liên quan mạnh |
| Vị trí | Van 2 lá >van DMC | Van 3 lá >>van 2 lá = van DMC |
| Hình dạng | Khối nhỏ, hầu hết bám tại đường khâu chỉ, phát triển , hướng tâm, giới hạn ở mặt phẳng mảnh van, tăng sinh dưới mảnh van | Khối lớn hơn pannus, thường di động độc lập, có thể lan ngoài vòng van hướng phát triển vào nhĩ trái ở van 2 lá, có các thành phần có tính di động |
| Tỷ số video-intensity trên siêu âm | <0,7 (đặc hiệu 100%) | <0,4 |
| Giá trị attenuation trên CT tim | >200 HU | <200 HU |
| Tác động trên chênh áp | Van ĐMC >van 2 lá | Van 2 lá >Van DMC |
Tác động trên lỗ van | Van DMC >van 2 lá | Van 2 lá >Van DMC |
| Tác động trên di động mảnh van | Có/không | Có |
Tỷ số video-intensity: echo khối so với van nhân tạo cơ học. CT: computed tomography, ĐMC: động mạch chủ, HU: hounsfield units.
4 ĐIều trị tắc nghẽn van tim cơ học do huyết khối
4.1 Nghiên cứu điều trị tắc nghẽn van tim nhân tạo do huyết khối
Điều trị huyết khối van tim nhân tạo cơ học là một việc phức tạp và phụ thuộc vào nhiều yếu tố, bao gồm: vị trí van tim (bên trái hay bên phải), mức độ ảnh hưởng của huyết khỏi lên hoạt động van tim, tình trạng huyết động và lâm sàng của bệnh nhân, tình trạng sử dụng kháng đông, hội chứng tăng đông và các yếu tố khác có thể ảnh hưởng đến nguy cơ khi dùng liệu pháp tiêu sợi huyết (thrombolytic therapy) hay phẫu thuật. Liệu pháp tiêu sợi huyết, khi thành công, giúp bệnh nhân không phải chịu một cuộc phẫu thuật lấy huyết khối (thrombectomy) hoặc thay van nhân tạo khác. Tuy nhiên, có hai vấn đề đáng quan ngại: (1) có khoảng 15% bệnh nhân huyết khối trên van nhân tạo cơ học bên trái bị thuyên tắc huyết khối, bao gồm nhồi máu não do thuyên tắc khi được điều trị với thuốc tiêu sợi huyết Streptokinase hoặc tissue plasminogen activator (tPA) và (2) có khoảng 5% bệnh nhân có biến chứng xuất huyết khi được điều trị với thuốc tiêu sợi huyết.
Trong một phân tích gộp từ 48 nghiên cứu quan sát với 2.302 bệnh nhân có huyết khối van tim nhân tạo, tử vong do phẫu thuật là 18,1%, trong khi tử vong do liệu pháp tiêu sợi huyết là 6,6%. Tử vong do phẫu thuật tăng ở nhóm bệnh nhân có phân độ suy tim theo NYHA cao' Trong một phân tích gộp khác từ 7 nghiên cứu quan sát với 690 bệnh nhân có huyết khối van tim nhân tạo bên trái, 446 bệnh nhân được điều trị bằng phẫu thuật và 244 bệnh nhân được điều trị với thuốc tiêu sợi huyết. Kết quả ghi nhận không có sự khác biệt có ý nghĩa thống kê trong tiêu chí phục hồi hoàn toàn chức năng van tim và tử vong. Tuy nhiên, so với liệu pháp tiêu sợi huyết, phẫu thuật khẩn cấp có tỷ lệ thấp hơn trong thuyên tắc huyết khối, chảy máu lớn và tái phát huyết khối van tim nhân tạo'. Kết quả này gợi ý phẫu thuật lấy huyết khối nên được thực hiện hơn so với thuốc tiêu sợi huyết ở các bệnh nhân có huyết khối van tim nhân tạo bên trái.
Để đánh giá lại tính hiệu quả và an toàn của hai phương pháp điều trị này, Özkan và cộng sự thực hiện nghiên cứu quan sát, đa trung tâm HATTUSHA với 158 bệnh nhân có tắc nghẽn van nhân tạo do huyết khối (83 bệnh nhân dùng tiêu sợi huyết và 75 bệnh nhân được phẫu thuật). Điểm đặc biệt trong nghiên cứu này là thuốc tiêu sợi huyết tPA được truyền chậm (trong 6 giờ) hoặc siêu chậm (trong 25 giờ) với liều thấp, không dùng liều bolus và không dùng Heparin trong quá trình truyền tPA. Trong chế độ truyền chậm, 25 mg của tPA được truyền trong 6 giờ. Siêu âm tim đánh giá lại tình trạng huyết khối và hoạt động van tim được thực hiện sau truyền. Thuốc tPA có thể được lặp lại với liều và tốc độ như trên với tối đa 6 lần cho tổng liều 150 mg tPA nếu cần, phụ thuộc đánh giá huyết khối, tình trạng bệnh nhân và hoạt động van tim. Kết quả ghi nhận tỷ lệ thành công của thuốc tiêu sợi huyết là 90.4% với liều trung vị của tPA là 59 mg (IQR: 37,5-100 mg). Tỷ lệ tử vong trong 3 tháng của nhóm tiêu sợi huyết và phẫu thuật lần lượt là 2,4% và 18,7%. Tỷ lệ biến chứng thuyên tắc của nhóm tiêu sợi huyết và phẫu thuật lần lượt là 2,4% và 5,3%. Tỷ lệ tái lập huyết khối của nhóm tiêu sợi huyết và phẫu thuật lần lượt là 2,4% và 6,7%. Nghiên cứu này kết luận chế độ truyền chậm hoặc siêu chậm tPA có tỷ lệ tử vong và biến chứng thuyên tắc thấp, tỷ lệ thành công cao và nên được xem xét như một liệu pháp điều trị tắc nghẽn van nhân tạo do huyết khối 6 Chế độ truyền chậm và liều thấp thuốc tiêu sợi huyết cũng đã được ghi nhận hiệu quả và an toàn ở những phụ nữ có thai và có huyết khối van tim nhân tạo.
4.2 Khuyến cáo điều trị tắc nghẽn van tim cơ học do huyết khối
Hai khuyến cáo quan trọng trong điều trị bệnh lý van tim từ Mỹ của ACC/AHA (American College of Cardiology/American Heart Association) năm 2020 và châu Âu năm 2021 có đề cập đến điều trị huyết khối van tim nhân tạo. Theo ACC/AHA, bệnh nhân có huyết khối van tim cơ học cần được điều trị khẩn cấp. Hai phương pháp là thuốc tiêu sợi huyết hoặc phẫu thuật đều hiệu quả. Quyết định phương pháp nào phụ thuộc vào yếu tố lâm sàng từ bệnh nhân và kinh nghiệm tại đơn vị y tế. Quyết định phương pháp điều trị cho huyết khối van tim nhân tạo cơ học bên trái cần được cá thể hóa (Bảng D) Đối với thuốc tiêu sợi huyết, trong khi ACC/AHA ưu tiên dùng chế độ điều trị liều thấp, truyền chậm, không bolus thì ESC khuyến cáo dùng liều chuẩn, có bolus.
| Ưu tiên phẫu thuật | Ưu tiên thuốc tiêu sợi huyết |
| Đội phẫu thuật thành thạo, sẵn sàng | Đội phẫu thuật không thành thạo |
| Nguy cơ phẫu thuật thấp | Nguy cơ phẫu thuật cao |
| Chống chỉ định thuốc tiêu sợi huyết | Không chống chỉ định thuốc tiêu sợi huyết |
| Huyết khối van tim tái phát | Huyết khối van tim lần đầu tiên |
| NYHA độ IV | NYHA độ I, II, III |
| Kích thước huyết khối lớn (>0,8 cm2) | Kích thước huyết khối nhỏ (<0,8 cm2) |
| Có huyết khối nhĩ trái | Không có huyết khối nhĩ trái |
| Đồng mắc bệnh động mạch vành và cần tái thông mạch máu | Bệnh động mạch vành nhẹ hoặc không có |
| Bệnh van tim khác | Không có bệnh van tim khác |
| Khả năng là pannus | Huyết khối nhìn thấy rõ |
| Lựa chọn của bệnh nhân | Lựa chọn của bệnh nhân |
| Khuyến cáo của ACC/AHA 2020 | Nhóm | Mức độ bằng chứng |
| Ở bệnh nhân có huyết khối van tim nhân tạo cơ học và có triệu chứng tắc 1 nghẽn van tim, khuyến cáo điều trị ban đầu khẩn cấp với tiêu sợi huyết liều thấp, truyền chậm hoặc phẫu thuật cấp cứu | I | B-NR |
| Khuyến cáo của ESC 2021 | Nhóm | MĐBC |
| Thay thế van tim cấp cứu hay khẩn cấp được khuyến cáo cho huyết khối gây tắc nghẽn ở các bệnh nhân có bệnh cảnh nặng và không có bệnh đồng mắc nghiêm trọng | I | B |
| Thuốc tiêu sợi huyết (recombinant tPA 10 mg bolus + 90 mg trong 90 phút với heparin không phân đoạn hoặc streptokinase 1.500.000 IU trong 60 phút không kèm heparin không phân đoạn) nên được xem xét khi không thể thực hiện được phẫu thuật hoặc nguy cơ rất cao hoặc cho huyết khối tại van tim nhân tạo bên phải | IIa | B |
| Phẫu thuật nên xem xét cho huyết khối van nhân tạo không tắc nghẽn có kích thước lớn >10mm có biến chứng thuyên tắc | IIa | C |
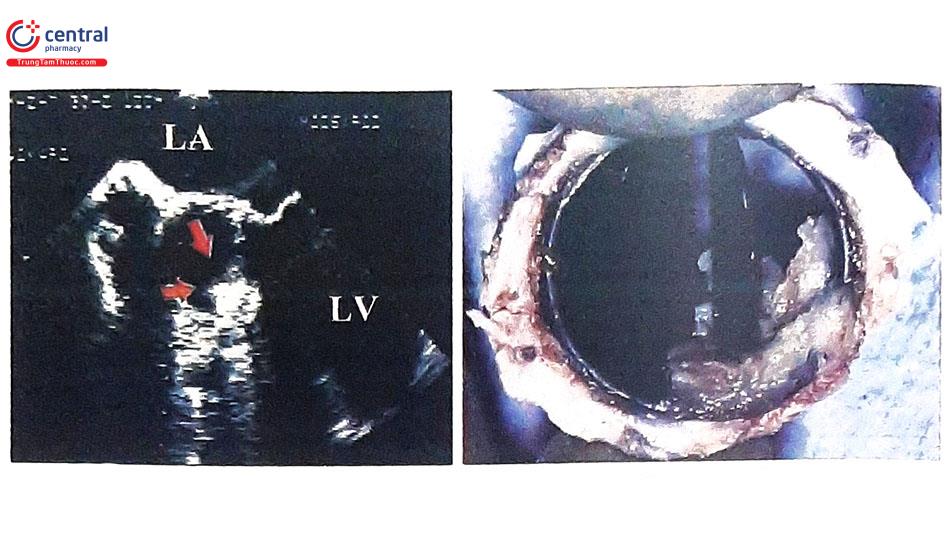
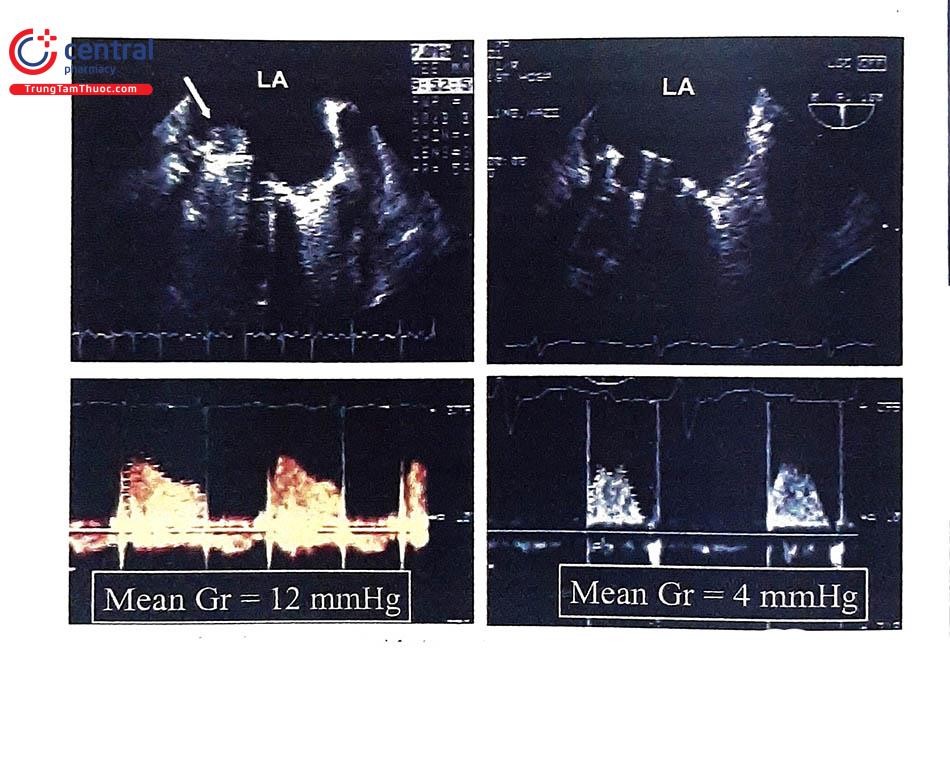
4.3 Minh họa trường hợp điều trị tắc nghẽn van cơ học do huyết khối
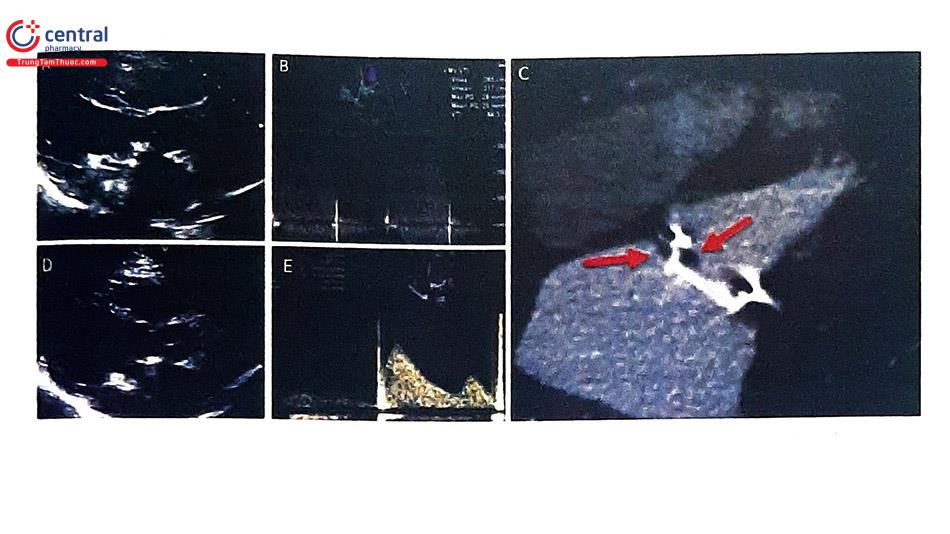
4.4 Các lưu ý trong điều trị tắc nghẽn van tim nhân tạo cơ học ở người cao tuổi
Cho đến hiện tại, chưa có một khuyến cáo hay nghiên cứu điều trị tắc nghẽn van tim nhân tạo cơ học ở nhóm dân số người cao tuổi. Việc lựa chọn phương pháp điều trị giữa thuốc tiêu sợi huyết hoặc phẫu thuật cần dựa vào các yếu tố theo khuyến cáo chung của ACC/AHA 2020 (Bảng 6). Tuy nhiên, dựa trên đặc điểm tuổi cao là một yếu tố làm tăng nguy cơ chảy máu/xuất huyết khi dùng các thuốc chống huyết khối, việc sử dụng thuốc tiêu sợi huyết cần xem xét chế độ liều thấp, truyền chậm hoặc siêu chậm theo từng đợt và đánh giá lại tình trạng lâm sàng, hoạt động van giữa các lần truyền thuốc.
5 Kết luận
Tắc nghẽn van tim nhân tạo cơ học do huyết khối là một biến chứng sau thay van tim nhân tạo. Biến chứng này có thể gặp ở người cao tuổi và dẫn đến rối loạn huyết động cấp tính và đe dọa mạng sống bệnh nhân nếu không được chẩn đoán và điều trị kịp thời. Việc quyết định phương pháp điều trị biến chứng này cần dựa vào nhiều yếu tố và sự lựa chọn của bệnh nhân. Ở bệnh nhân cao tuổi, nếu sử dụng phương pháp tiêu sợi huyết thì cần xem xét dùng liều thấp, truyền chậm hoặc siêu chậm.
6 Tài liệu tham khảo
- Nguyễn Văn Tân, Nguyễn Văn Trí, Nguyễn Thanh Huân (2023). “Tắc nghẽn van tim nhân tạo cơ học do huyết khối ở người cao tuổi”, Cấp cứu các bệnh thường gặp ở người cao tuổi. Nhà xuất bản Y học, trang 219-240. Tải bản PDF tại đây.
- Vahanian A, Beyersdorf F, Praz F, et al. (2022) 2021 ESC/EACTS Guidelines for the management of valvular heart disease. Eur Heart J.
- Fioretta ES, Motta SE, Lintas V, et al. (2021) Next-generation tissue-engineered heart valves with repair, remodelling and regeneration capacity. Nat Rev Cardiol.
- Soliman Hamad MA, van Eekelen E, van Agt T, et al. (2009) Self-management program improves anticoagulation control and quality of life: a prospective randomized study. Eur J Cardiothorac
- Pibarot P, Dumesnil JG.(2009) Prosthetic heart valves: selection of the optimal prosthesis and longterm management. Circulation.
- Fuster V, Harrington RA, Narula J, et al. (2017) Chapter 52: Prosthetic Heart Valves. Hurst's The Heart, 14th edition. McGraw-Hill
- Lancellotti P, Pibarot P, Chambers J, et al. (2016) Recommendations for the imaging assessment of prosthetic heart valves: a report from the European Association of Cardiovascular Imaging endorsed by the Chinese Society of Echocardiography, the InterAmerican Society of Echo- cardiography, and the Brazilian Department of Cardiovascular Imaging. Eur Heart J Cardiovasc Imaging
- Ellis JT, Yoganathan AP.(2000) A comparison of the hinge and near-hinge flow fields of the St Jude medical hemodynamic plus and regent bileaflet mechanical heart valves. J Thorac Cardiovasc Surg 2000;119(1):83-93.
- Hussain N, Rehman A, Cheema FH. (2014) Mechanical mitral valve thrombosis in an elderly patient. Int J Cardiovasc Imaging
- Otto CM. (2019) Chapter 13. Prosthetic Valves. Textbook of Clinical Echocardiography, 6th Edition.
- Zoghbi WA, Chambers JB, Dumesnil JG, et al. (2009) Recommendations for evaluation of pros- thetic valves with echocardiography and doppler ultrasound: a report From the American Society of Echocardiography's Guidelines and Standards Committee and the Task Force on Prosthetic Valves, developed in conjunction with the American College of Cardiology Cardiovascular Imaging Committee, Cardiac Imaging Committee of the American Heart Association, the European Association of Echocardiography, a registered branch of the European Society of Cardiology, the Japanese Society of Echocardiography and the Canadian Society of Echocardiography, endorsed by the American College of Cardiology Foundation, American Heart Association, European Association of Echocardiography, a registered branch of the European Society of Cardiology, the Japanese Society of Echocardiography, and Canadian Society of Echocardiography. J Am Soc Echocardiogr
- Zekry SB, Saad RM, Ozkan M, et al.(2011) Flow acceleration time and ratio of acceleration time to ejection time for prosthetic aortic valve function. JACC Cardiovasc Imaging
- Pibarot P, Dumesnil G. (2006) Prosthesis-patient mismatch: definition, clinical impact, and prevention. Heart
- Schaff HV. (2022) Progress in Management of Mechanical Valve Thrombosis. J Am Coll Cardiol
- Castilho FM, De Sousa MR, Mendonca AL, et al. (2014) Thrombolytic therapy or surgery for valve prosthesis thrombosis: systematic review and meta-analysis. J Thromb Haemost
- Karthikeyan G, Senguttuvan NB, Joseph J, et al. (2013) Urgent surgery compared with fibrinolytic therapy for the treatment of left-sided prosthetic heart valve thrombosis: a systematic review and meta-analysis of observational studies. Eur Heart J
- Ozkan M, Gunduz S, Guner A, et al. (2022) Thrombolysis or Surgery in Patients With Obstructive Mechanical Valve Thrombosis: The Multicenter HATTUSHA Study. J Am Coll Cardiol
- Ozkan M, Cakal B, Karakoyun S, et al. (2013) Thrombolytic therapy for the treatment of prosthetic heart valve thrombosis in pregnancy with low-dose, slow infusion of tissue-type plasmino- gen activator. Circulation
- Writing Committee M, Otto CM, Nishimura RA, et al. (2021) 2020 ACC/AHA Guideline for the Management of Patients With Valvular Heart Disease: A Report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. J Am Coll Cardiol
- Kapos I, Fuchs T, Tanner FC. (2020) Case report of successful low-dose, ultra-slow infusion thrombolysis of prosthetic mitral valve thrombosis in a high risk patient after redo-mitral valve replacement. Eur Heart J Case Rep.

