Cơ chế sinh lý và tiếp cận chẩn đoán các rối loạn kiềm-toan

Physiologic mechanisms and diagnostic approach to acid-base disorders
John G. Tejfaletti, PhD; Craig R. Rackley, MD
Blood Gases and Critical Care Testing, Chapter 2, 23-52
1 Toan chuyển hóa
Toan chuyển hóa được định nghĩa là một quá trình lâm sàng dẫn đến giảm pH máu (nhiễm toan máu) và giảm nồng độ HCO3-. Nguyên nhân là do tăng các hợp chất acid và/hoặc mất một base, thường là bicarbonate. Sự di chuyển của các chất điện giải cũng có thể đóng một vai trò trong cân bằng kiềm-toan, đôi khi được biểu hiện bằng việc tăng khoảng trống anion.
Cơ chế sinh lý của toan chuyển hóa:
- Trong tiêu chảy, dịch tiết của tụy vào ruột non có hàm lượng natri so với clorua tương đối cao, với nồng độ bicarbonate tương đối cao hơn. Mất các dịch tiêu hóa như vậy thường dẫn đến toan chuyển hóa.
- Trong toan hóa ống thận, nếu sự bài tiết natri và Kali vượt quá sự bài tiết clorua vào nước tiểu, anion đi kèm natri/kali thường là bicarbonate. Điều này có thể dẫn đến giảm bicarbonate huyết thanh và toan chuyển hóa.
- Tăng clo máu (Hyperchloremia) thường cho thấy có tình trạng toan chuyển hóa. Tăng clo do hấp thu qua Đường tiêu hóa hoặc truyền tĩnh mạch có thể gây tăng clo máu. Đây là một lĩnh vực phức tạp về mặt sinh lý, nhưng có một vài nguyên tắc:
Nếu nồng độ Cl- tăng và nồng độ Na+ giữ nguyên, một anion khác ngoài Cl- phải giảm. Anion này thường là bicarbonate.
Tăng clo máu có thể xảy ra khi mất các muối natri không chứa clorua từ đường tiêu hóa hoặc từ nước tiêu.
Tăng clo máu sẽ phát triển khi thêm các Dung dịch chứa muối clorua như natri, kali, calci, hoặc amoni.
- Tăng hoặc mất kali cũng có thể ảnh hưởng đến nồng độ natri, sau đó sẽ ảnh hưởng đến nồng độ clorua.
- Tăng khoảng trống anion có thể liên quan đến toan chuyển hóa. Các quá trình sau thường đi kèm với việc tăng khoảng trống anion:
Sản xuất lactat và acid từ chuyển hóa yếm khí. Nếu không có đủ oxy cho các mô (thiếu oxy), các điều kiện tế bào bắt đầu ưu tiên chuyển hóa yếm khí với việc chuyển đổi pyruvate thành lactat. Mặc dù các bác sĩ lâm sàng thường nghĩ rằng quá trình này tạo ra Acid Lactic, nhưng thực tế sản phẩm là lactat. Acid (H+) đến từ sự phân hủy một lượng lớn ATP mà không có sự tái tổng hợp.
Sản xuất acid quá mức từ nhiễm toan ceton. Loại nhiễm toan ceton phổ biến nhất là nhiễm toan ceton do đái tháo đường, xảy ra khi Glucose không thể đi vào tế bào để sản xuất đủ ATP. Trong bối cảnh glucose tế bào thấp (glucose huyết thanh thưởng khá cao trong nhiễm toan ceton do đái tháo đường), các acid béo sẽ bị oxy hóa để tạo ra các ketoacid để lấy năng lượng. Nhiễm toan ceton cũng có thể thấy ở người nhịn đói khi nồng độ glucose huyết tương thấp, và ở những bệnh nhân suy dinh dưỡng và nghiện rượu mạn tính.
Uống các acid ngoại sinh hoặc các chất tạo acid: salicylate, Ethanol, ethylene glycol, methanol, v.v.
- Bài tiết acid qua thận không đủ. Trong suy thận, tùy thuộc vào việc suy cầu thận hay ống thận, có thể xảy ra tích tụ H+ và/hoặc mất HCO3-. Vì toan do thận thường khởi phát chậm, tăng thông khí thường cung cấp sự bù trừ hô hấp để ngăn ngừa nhiễm toan máu trong giai đoạn đầu.
Sử dụng khoảng trống anion trong toan chuyển hóa. Khoảng trống anion (AG), đặc biệt khi tăng, có thể hữu ích trong việc chẩn đoán loại toan chuyển hóa và chỉ ra khả năng có rối loạn kiềm-toan hỗn hợp, như được trình bày trong Bảng 2.1.
Bảng 2.1. Những thay đổi của khoảng trống anion (AG) trong các rối loạn kiềm-toan khác nhau
| Rối loạn | Giảm | Tăng | Ảnh hưởng lên AG |
| Tiêu chảy | HCO3- | CI- | Ít thay đổi |
| Toan hóa ống thận | HCO3- | CI- | Ít thay đổi |
| Toan lactic | HCO3- | Lactat | Tăng |
Toan ceton | HCO3- | Ketoacid | Tăng |
| Rối loạn hỗn hợp: toan ceton + kiềm | HCO3- | Ketoacid và HCO3- | Tăng (ít thay đổi tổng CO2) |
Như đã mô tả trước đó, AG là sự khác biệt giữa các cation thường được đo (Na+ và đôi khi là K+) và các anion thường được đo (Cl- và HCO3-). Khoảng tham chiếu gần đúng cho AG là 8-16 mmol/L (8-16 mEq/L) khi AG = Na (CI + CO2) và 12-20 mmol/L (12-20 mEq/L) khi AG = (Na + K) - (Cl + CO2).
Albumin huyết thanh là một yếu tố quan trọng ảnh hưởng đến việc tính toán khoảng trống anion. Bởi vì albumin trong máu chiếm một tỷ lệ lớn các anion "không đo được", sự giảm hoặc tăng (ít phổ biến hơn) nồng độ albumin sẽ lần lượt làm giảm hoặc tăng việc tính toán khoảng trống anion. Cứ mỗi g/L giảm nồng độ albumin, AG giảm khoảng 0,25 mmol/L. Nếu phòng xét nghiệm báo cáo albumin theo g/dL thì mỗi g/dL giảm nồng độ albumin sẽ làm AG giảm khoảng 2,5 mmol/L. Điều này có thể che giấu một AG tăng do lactat tăng trong toan chuyển hóa. Nếu ghi nhận có giảm albumin máu, điều thường gặp ở bệnh nhân nặng, AG có thể được "hiệu chỉnh" bằng phương trình (2.1) để diễn giải AG tốt hơn. Độ nhạy của việc tăng khoảng trống anion trong việc phát hiện tăng lactat máu dường như được cải thiện bằng cách hiệu chỉnh AG theo nồng độ albumin.
AGcorr = AGmeas + 0.23 x (45 - Albmeas) (2.1)
AGcorr = AG đã hiệu chỉnh; AGmeas = AG đo được; Albmeas = albumin đo được tính bằng g/L.
Trong Bảng 2.2, AG đo được (thực ra là tính toán) trên một mẫu giả định có lactat tăng 5,0 mmol/L và albumin bình thường 45 g/L là 18 mmol/L, như mong đợi. Tuy nhiên, trên một mẫu có cùng lactat tăng 5,0 mmol/L, nhưng albumin giảm còn 25 g/L, AG đo được lại có vẻ bình thường ở mức 12 mmol/L. Hiệu chỉnh AG trong mẫu sau cho ra AG đã hiệu chỉnh là 18 mmol/L. Bảng 2.2 cũng cho thấy một mẫu giả định có albumin tăng 70 g/L và lactat bình thường có AG tăng giả tạo là 18 mmol/L. Hiệu chỉnh AG cho albumin tăng đã cho ra AG bình thường là 12 mmol/L. Một mối lo ngại tiềm tàng là việc hiệu chỉnh này yêu cầu sử dụng một giá trị albumin "bình thường" trong tính toán, chẳng hạn như giá trị trung bình của khoảng tham chiếu. Có lẽ sẽ tốt hơn nếu sử dụng albumin và AG ban đầu của bệnh nhân làm tham chiếu nếu có.
Bảng 2.2. Ảnh hưởng của nồng độ albumin lên khoảng trống anion (AG)
| Xét nghiệm hóa sinh | Albumin bình thường, Lactat tăng | Albumin thấp, Lactat tăng | Albumin tăng, Lactat bình thường |
| Na (mmol/L) | 140 | 138 | 140 |
| K (mmol/L) | 4,0 | 4,0 | 4,0 |
| Cl (mmol/L) | 104 | 108 | 98 |
| tCO2 (mmol/L) | 18 | 18 | 24 |
| Albumin (g/L) | 45 | 25 | 70 |
| Lactat (mmol/L) | 5,0 | 5,0 | 2,0 |
| AG đo được | 18 | 12 | 18 |
| AG hiệu chỉnh | 18 | 18 | 12 |
Theo dõi kết quả AG trong phòng xét nghiệm cũng là một kỹ thuật kiểm soát chất lượng phổ biến để phát hiện sự trôi dạt trong kết quả điện giải. Lưu ý rằng điều này được phát hiện bởi một loạt các khoảng trống anion bất thường, chứ không phải bởi một kết quả duy nhất. Đây có thể là lý do tại sao một báo cáo cho rằng nguyên nhân phổ biến nhất của khoảng trống anion thấp là lỗi phòng xét nghiệm trong các phép đo điện giải.
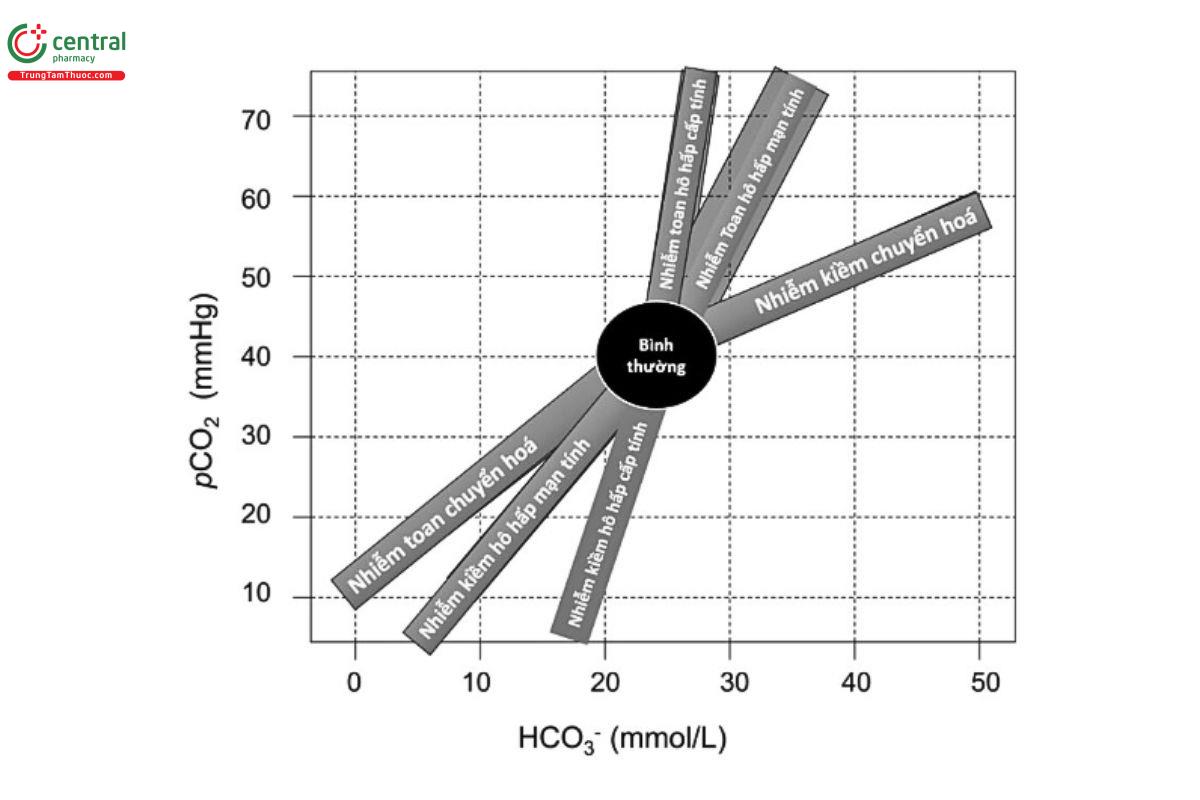
Bù trừ dự kiến trong toan chuyển hóa (Bảng 2.3 và Hình 2.1). Trong giai đoạn đầu của toan chuyển hóa (nhiễm toan máu với bicarbonate huyết tương thấp), cả pH và HCO3- đều giảm trong khi pCO2 vẫn bình thường. Bù trừ hồ hấp dự kiến là tăng thông khí, điều này sẽ bắt đầu làm giảm pCO2 máu trong vòng 30 phút, có tác dụng đáng kể sau 2 giờ, và đạt hiệu quả tối đa sau 12-24 giờ. Một quy tắc chung là bù trừ hô hấp làm giảm pCO2 1,2 mmHg cho mỗi 1,0 mmol/L giảm HCO3- dưới 24 mmol/L. Ví dụ, ở một bệnh nhân bị toan chuyển hóa và có pCO2 ban đầu là 40 mmHg và HCO3- ban đầu là 24 mmol/L, nếu HCO3- giảm 8 mmol/L từ 24 xuống 16 mmol/L, pCO2 sau khi bù trừ sẽ vào khoảng 30 mmHg (40-1,2 x 8).
Phương trình cho mối quan hệ này là:
PCO2 bù trừ = pCO2 ban đầu – 1.2 × [HCO3- ban đầu – HCO3- bù trừ] (2.2)
Do đó, nếu pCO2 cao hơn giá trị tính toán này hơn 3 mmHg, bệnh nhân có thể không có khả năng bù trừ hoàn toàn thông qua tăng thông khí và do đó cũng có thê có một tình trạng toan hô hấp tiềm ẩn. Nếu pCO2: thấp hơn giá trị tính toán này hơn 3 mmHg, có thể có một tình trạng kiềm hô hấp tiềm ẩn. Cả hai tình huống này đều cho thấy có một rối loạn hỗn hợp (toan chuyển hóa với toan hô hấp hoặc kiềm hô hấp).
Thận trọng: Các tính toán bù trừ dự kiến này nên được sử dụng như những hướng dẫn trong chẩn đoán và không nên được diễn giải quá mức như một chẩn đoán tuyệt đối.
Điều trị. Điều trị tối ưu cho toan chuyển hóa là khắc phục nguyên nhân cơ bản, chẳng hạn như dùng Insulin cho nhiễm toan ceton do đái tháo đường, cải thiện việc cung cấp oxy bằng cách tăng hàm lượng oxy trong máu và/hoặc cải thiện cung lượng tim. Mất dịch và điện giải nên được thay thế nếu thích hợp, lọc máu cho suy thận hoặc để loại bỏ một số nguyên nhân ngoại sinh gây toan chuyển hóa và có thể sử dụng bicarbonate. Tuy nhiên, việc sử dụng bicarbonate có thể gây hại và thường không được khuyến cáo ngoài trường hợp huyết động không ổn định thứ phát sau toan chuyển hóa nặng.
Bảng 2.3. pH, HCO3- và pCO2 trong các rối loạn nguyên phát, bù trừ và rối loạn hỗn hợp
| Rối loạn nguyên phát | pH | HCO3- | PCO2 | Tình trạng |
| Toan chuyển hóa | Giảm | Giảm | Bình thường | Giai đoạn sớm (<2 giờ) |
| Giảm -> gần bình thường | Giảm | Giảm | Bù trừ hô hấp dự kiến (26 giờ) | |
| Giảm | Giảm | Bình thường -> Giảm | Không có khả năng bù trừ | |
| Giảm nhiều | Giảm | Tăng | Toan chuyển hóa + Toan hô hấp hỗn hợp | |
| Kiềm chuyển hóa | Tăng | Tăng | Bình thường | Giai đoạn sớm (<2 giờ) |
| Tăng -> gần bình thường | Tăng | Tăng | Bù trừ hô hấp dự kiến (≥6 giờ) | |
| Tăng | Tăng | Bình thường -> Tăng | Không có khả năng bù trừ | |
| Tăng nhiều | Tăng | Giảm | Kiềm chuyển hóa + Kiềm hô hấp hỗn hợp | |
| Toan hô hấp | Giảm | Bình thường | Tăng | Giai đoạn đầu |
| Giảm -> gần bình thường | Tăng | Tăng | Bù trừ chuyển hóa dự kiến (≥ 24 giờ) | |
| Giảm | Bình thường -> Tăng | Tăng | Không có khả năng bù trừ | |
| Giảm nhiều | Giảm | Tăng | Toan hô hấp + Toan chuyển hóa hỗn hợp | |
| Kiềm hô hấp | Tăng | Bình thường | Giảm | Giai đoạn đầu |
| Tăng -> gần bình thường | Giảm | Giảm | Bù trừ chuyển hóa dự kiến (≥24 giờ) | |
| Tăng | Bình thường -> Giảm | Giảm | Không có khả năng bù trừ | |
| Tăng nhiều | Tăng | Giảm | Kiềm hô hấp + Kiềm chuyển hóa hỗn hợp |
2 Kiềm chuyển hóa
Kiềm chuyển hóa là một rối loạn kiềm-toan đặc trưng bởi sự tăng nồng độ bicarbonate trên 26 mmol/L và tăng pH. Nhiều tình trạng bệnh lý có thể gây ra kiềm chuyển hóa bao gồm mất ion hydro qua thận quá mức hoặc giữ lại bicarbonate, sự dịch chuyển ion hydro vào nội bảo, mất ion hydro qua đường tiêu hóa, và mất thể tích dịch qua việc sử dụng thuốc lợi tiểu mà không mất bicarbonate tương ứng, được gọi là "kiềm do cô đặc" (contraction alkalosis), thường liên quan đến suy giảm chức năng thận vì một quả thận khỏe mạnh có thể bài tiết một lượng lớn HCO3- khi nó dư thừa.
Cơ chế của kiềm chuyển hóa:
- Tăng nồng độ mineralocorticoid. Thận sử dụng một cơ chế trao đổi trong đó natri được tái hấp thu và hydro được bài tiết. Vi aldosterone làm tăng giữ natri, các tình trạng làm tăng aldosterone, chẳng hạn như cường aldosteron nguyên phát (hội chứng Conn) và thuốc lợi tiểu, có thể dẫn đến tăng natri máu và tăng mất ion hydro trong nước tiểu. Vì cortisol và các steroid khác như corticosterone có một số hoạt tính mineralocorticoid, cortisol dư thừa, như trong hội chứng Cushing, có thể dẫn đến bài tiết cả K+ và H+ ở ống thận xa với hậu quả là kiềm chuyển hóa và hạ kali máu.
- Mất acid qua đường tiêu hóa do nôn. Dịch dạ dày có tính acid cao, với pH khoảng 1,5-3,5. Do đó, việc mất acid dạ dày gây ra kiềm chuyển hóa với nồng độ bicarbonate trong máu tăng lên.
- Giảm clo máu (Hypochloremia). Thiếu hụt Cl- trong máu làm tăng cường tái hấp thu HCO3- ở ống thận. Khi các cation như Nat và Kẽ được tái hấp thu, một anion phải đi theo. Vì có ít Cl- hơn, nên nhiều HCO3- hơn được tái hấp thu.
- Hạ kali máu (Hypokalemia). Ha kali máu kích thích tái hấp thu ion HCO3- ở ống lượn xa. Trong cường mineralocorticoid nguyên phát, aldosterone làm tăng tái hấp thu Na ở ống thận và thúc đẩy mất ion K và H. Những sự di chuyển này dẫn đến kiềm ngoại bào với giảm clo máu, hạ kali máu, và tăng thể tích dịch ngoại bào.
- Sử dụng HCO3- quá mức. Mặc dù thường không cần thiết để điều trị toan chuyển hóa, việc truyền dung dịch natri bicarbonate đôi khi có thể được sử dụng. Nếu quá mức, việc sử dụng HCO3- có thể dẫn đến kiềm, đặc biệt nếu chức năng thận bị tổn thương.
- Kiềm do cô đặc. Điều này xảy ra khi một lượng lớn dịch có tương đối nhiều natri hơn bicarbonate bị mất khỏi cơ thể, sao cho nồng độ bicarbonate huyết tương tăng lên. Điều này có thể xảy ra với thuốc lợi tiểu, tiêu chảy, xơ nang, và các tình trạng khác.
- Giảm albumin máu (Hypoalbuminemia). Theo khái niệm hiệu số ion mạnh, sự giảm albumin huyết tương (là acid yếu chiếm ưu thế trong huyết tương) gây ra giảm nồng độ acid yếu, dẫn đến kiềm chuyển hóa.
Bù trừ dự kiến trong kiềm chuyển hóa (Bảng 2.3 và Hình 2.1). Vì thận hoạt động bình thường có thể bài tiết một lượng lớn bicarbonate, một lượng bicarbonate vừa phải có thể được bài tiết dễ dàng để điều chỉnh tình trạng kiềm chuyển hóa. Tuy nhiên, nếu việc bài tiết bicarbonate qua thận bị cản trở, bicarbonate có thể tăng trong máu dẫn đến tăng pH máu.
Những thay đổi trong pH máu được cảm nhận bởi cả các thụ thể hóa học ngoại biên và trung ương, do đó kiềm chuyển hóa luôn gây ra giảm thông khí và tăng pCO2 máu để bù trừ cho sự tăng bicarbonate. Tuy nhiên, trong khi giảm thông khí gần như luôn xảy ra khi có kiềm chuyển hóa, các yếu tố khác như đau, ví dụ do chọc động mạch, hoặc thiếu oxy máu có thể kích thích tăng thông khí và vượt qua tác nhân kích thích giảm thông khí của kiềm chuyển hóa.
Vì chúng có thể phần nào bù trừ cho nhau, sự kết hợp của các kích thích giảm thông khí do nhiễm kiềm và tăng thông khí do thiếu oxy máu có thể đặt ra những thách thức cả về chẩn đoán và điều trị. Những bệnh nhân có tăng CO2 máu do kiềm chuyển hóa và thiếu oxy máu do các nguyên nhân khác có thể bị bỏ sót tình trạng kiềm chuyển hóa. Trong những trường hợp như vậy, việc cung cấp oxy sẽ làm giảm kích thích tăng thông khí do thiếu oxy máu và bộc lộ tỉnh trạng giảm thông khí như một phản ứng bù trừ cho kiềm chuyển hóa.
Mặc dù bù trừ hô hấp tối đa bằng giảm thông khí từng được cho là không quá 55-60 mmHg, bù trừ có thể nâng pCO2 động mạch lên hơn 80 mmHg trong một số trường hợp.
Trong giai đoạn đầu của kiềm chuyển hóa, cả pH và HCO3- đều tăng và pCO2 vẫn bình thường. Trong vòng 2 giờ, bù trừ bằng giảm thông khí sẽ rõ ràng, với bù trừ tối đa xảy ra sau 12-24 giờ, làm tăng pCO2 máu để phù hợp với HCO3- tăng và khôi phục tỷ lệ HCO3-/pCO2 về bình thường. Nhìn chung, bù trừ hô hấp làm tăng pCO2 0,7 mmHg cho mỗi 1,0 mmol/L tăng HCO3-. Ví dụ, ở một bệnh nhân bị kiềm chuyển hóa, sau 24 giờ, nếu HCO, tăng từ 24 lên 32 mmol/L (tăng 8 mmol/L so với mức bình thưởng 24 mmol/L), pCO2 sẽ vào khoảng 46 mmHg (40 + 0,7 x 8). Phương trình cho điều này như sau:
PCO2 bù trừ = pCO2 ban đầu + 0.7 × [HCO3- bù trừ – HCO3- ban đầu] (2.3)
Nếu pCO2 thực tế chênh lệch so với pCO2 dự kiến này hơn 4 mmHg, bệnh nhân có thể có rối loạn hỗn hợp do toan hô hấp tiềm ẩn (nếu cao hơn 4 mmHg) hoặc kiềm hô hấp (nếu thấp hơn 4 mmHg).
Thận trọng: Các tính toán bù trừ dự kiến này nên được sử dụng như những hướng dẫn trong chẩn đoán và không nên được diễn giải quá mức như một chẩn đoán tuyệt đối.
Điều trị. Điều trị tối ưu cho kiềm chuyển hóa là khắc phục rối loạn cơ bản và bất kỳ yếu tố nào duy trì rối loạn. Trong một số trường hợp, chỉ cần bù nước đơn giản sẽ dần dần điều chỉnh kiềm chuyển hóa nếu chức năng thận bình thường. Vì tình trạng thiếu hụt Cl- thường gặp, Cl- có thể được thay thế bằng cách sử dụng dung dịch NaCl hoặc KCI khi thích hợp, có xem xét đến chức năng thận. Hiếm khi, HCl loãng có thể được truyền tĩnh mạch nếu cần thiết, và Brandis chỉ ra rằng việc điều chỉnh kiềm chuyển hóa sẽ gây ra sự dịch chuyển sang phải của đường cong phân ly oxy, làm tăng giải phóng oxy ngoại vi. Ở những bệnh nhân bị phù toản thân hoặc suy tim sung huyết vẫn trong tình trạng phù và tiếp tục cần lợi tiểu, có thể dùng acetazolamide, một chất ức chế carbonic anhydrase. Acetazolamide chủ yếu ức chế tái hấp thu natri bicarbonate ở ống lượn gần trong thận, do đó làm tăng bài tiết bicarbonate qua nước tiểu.
3 Toan hô hấp
pCO2 động mạch là sự cân bằng giữa sản xuất tế bào và loại bỏ qua thông khí phế nang. Toan hô hấp thường do thông khí không đủ dẫn đến dư thừa CO2 trong máu và đồng thời giảm pH máu dưới 7,35. Toan hô hấp cấp thường liên quan đến giảm thông khí, nhưng cũng có thể do tăng sản xuất CO2 của cơ thể, hoặc dư thừa CO2 trong khí hít vào. Bình thường, các trung tâm hô hấp ở cầu não và hành tủy kiểm soát thông khí phế nang bằng các thụ thể hóa học nhạy cảm với những thay đổi của pCO2, pO2, và pH, do đó bất kỳ sự tăng sản xuất CO2 nào cũng nhanh chóng kích thích tăng thông khí, duy trì pCO2 động mạch ở mức bình thường. Nếu pCO2 động mạch tăng, thường liên quan đến một vấn đề về thông khí.
Cơ chế của toan hô hấp cấp và mạn tính:
- Suy giảm thông khí do ức chế hệ thần kinh trung ương gây ra bởi chấn thương não, thuốc như opioid hoặc thuốc gây mê, hoặc suy yếu cơ hô hấp như trong các rối loạn thần kinh cơ, chẳng hạn như nhược cơ, xơ cứng teo cơ một bên, hoặc loạn dưỡng cơ.
- Suy giảm trao đổi khí ở phổi do tỷ lệ khoảng chết cao [(tổng thông khí - thông khí phế nang) / tổng thông khí]. Điều này có thể thấy trong một số bệnh phổi liên quan đến sự phá hủy không gian phế nang hoặc suy giảm lưu lượng máu đến một phân thùy của phổi. Trong những kịch bản này, thông khí phế nang hiệu quả chiếm một phần nhỏ hơn trong tổng thông khí phút.
- Giảm phản xạ đáp ứng mạn tính với tình trạng thiếu oxy và tăng CO2 máu thấy ở COPD, bệnh phổi hạn chế mạn tính, và hội chứng giảm thông khí do béo phì.
- Tắc nghẽn đường thở cấp tính do hít phải dị vật hoặc tắc ống nội khí quản.
- Suy tuần hoàn, gây ra việc cung cấp máu không đủ đến phối.
- Tăng chuyển hóa hoặc sản xuất CO2 ở bệnh nhân thở máy không tự thở. Nếu sản xuất CO2 tăng trong khi thông khí không đổi, pCO2 máu sẽ tăng.
Bù trừ dự kiến trong toan hô hấp (Bảng 2.3 và Hình 2.1). Để bù trừ cho lượng CO2 và acid dư thừa trong máu, thận bắt đầu bài tiết nhiều ion hydro và amoni hơn và tái hấp thu nhiều bicarbonate hơn. Trong giai đoạn cấp tính, sự đệm của huyết tương đối với CO2 tăng cao làm tăng nhẹ HCO3-, khoảng 1 mmol/L cho mỗi 10 mmHg tăng pCO2. Trong vài giờ tiếp theo, thận tăng tái hấp thu HCO3-, làm tăng HCO3- huyết thanh khoảng 2 mmol/L. Thận cũng có thể tăng giữ lại bicarbonate bằng cách bài tiết một nồng độ clorua (và ion amoni) cao trong nước tiểu so với natri, điều này sẽ làm giảm mất bicarbonate. Khi điều này tiếp diễn vào giai đoạn mạn tính (trên 24 giờ), bù trừ của thận xảy ra dần dần trong vài ngày để tăng HCO3- đạt đến trạng thái ổn định sau 2-5 ngày. Ngay cả sau vài ngày, bù trừ thường không đưa pH trở lại hoàn toàn bình thường. Vì bù trừ xảy ra theo hai giai đoạn, bù trừ dự kiến có hai thuật toán để dự đoán nồng độ HCO3- trong máu.
- Toan hô hấp cấp: Cứ mỗi 10 mmHg tăng pCO2 động mạch trên 40 mmHg, HCO3- sẽ tăng khoảng 1 mmol/L và pH sẽ giảm khoảng 0,07-0,08. Ví dụ, nếu nhịp thở của bệnh nhân chậm lại trong vài giờ và pCO2 tăng từ 40 lên 50 mmHg, HCO3- sẽ tăng khoảng 1 mmol/L (tức là 25 mmol/L) và pH sẽ giảm 0,08. Ví dụ, pH giảm từ 7,40 xuống khoảng 7,32.
HCO3- bù trừ = HCO3- ban đầu + 0.1× (pCO2 bù trừ – pCO2 ban đầu) (2.4)
Thay đổi pH = 0.008 × (40 - pCO2) = 0.008 × 10 = -0.08 (2.5)
- Toan hô hấp mạn: Phản ứng HCO3- tối đa xảy ra trong khoảng 3 ngày, với HCO3- tăng 3-4 mmol/L cho mỗi 10 mmHg tăng pCO2 động mạch. Ví dụ, nếu pCO2 đã tăng từ mức cơ bản của bệnh nhân là 40 mmHg lên trạng thái ổn định là 60 mmHg trong vài ngày, HCO3-sẽ tăng khoảng 6-8 mmol/L. Trong ví dụ của chúng ta, nếu HCO3- bình thường của bệnh nhân là 24 mmol/L, nó sẽ vào khoảng 30-32 mmol/L sau 3 ngày bù trừ chuyên hóa.
Do đó, đối với sự tăng pCO2 từ 40 đến 60 mmHg, bicarbonate dự kiến trong quá trình bù trừ có thể được tính bằng:
HCO3- bù trừ = HCO3- ban đầu + 0.35 × (pCO2 bù trừ - PCO2 ban đầu) (2.6)
Thay đổi pH dự kiến có thể được tính bằng:
Thay đổi pH = 0.003 x (40 - pCO2) = -0.06 (2.7)
Lưu ý rằng các tính toán này phụ thuộc vào thời gian. Nếu biết, các giá trị ban đầu của bệnh nhân được ưu tiên, nhưng nếu không biết, chúng ta có thể giả định bệnh nhân bắt đầu với pH rất bình thường (7,40), pCO2 (40 mmHg), và HCO3- (24 mmol/L).
Thận trọng: Các tính toán bù trừ dự kiến này nên được sử dụng như những hướng dẫn trong chẩn đoán và không nên được diễn giải quá mức như một chẩn đoán tuyệt đối.
Điều trị toan hô hấp. Tăng pCO2 máu nên được điều chỉnh dần dần đề ngăn ngừa sự kiềm hóa đột ngột của dịch não tủy có thể dẫn đến co giật. Mặc dù thông khí áp lực dương có thể cần thiết, liệu pháp dược lý ít xâm lấn hơn nhắm vào nguyên nhân cơ bản của toan hô hấp như thuốc giãn phế quản hoặc thuốc đối kháng opioid như Naloxone có thể là đủ. Việc sử dụng bicarbonate hiểm khi được thực hiện, vì HCO3- qua hàng rào máu não chậm, có thể làm tăng pH máu mà không ảnh hưởng đến pH của hệ thần kinh trung ương.
4 Kiềm hô hấp
Có lẽ đáng ngạc nhiên, kiềm hô hấp đã được coi là rối loạn kiềm-toan phổ biến nhất. Kiềm hô hấp có thể do bất kỳ tình trạng nào dẫn đến tăng thông khí và liên quan đến việc giảm pCO2 máu xuống dưới 35 mmHg và tăng pH máu. Từ thông khí phút bình thường 5-8 L/phút, kiềm hô hấp (tăng thông khí) là kết quả của việc tăng thông khí phút, trong đó CO2 bị mất nhanh hơn so với sản xuất, dẫn đến tăng pH và giảm pCO2. Bình thường, các trung tâm hô hấp ở cầu não và hành tủy kiểm soát thông khí, với nhiều yếu tố gây ra tăng thông khí.
Kiềm hô hấp có thể là một quá trình cấp tính hoặc mạn tính. Trong khi tăng thông khí có thể thay đổi nồng độ PCO2 rất nhanh, bù trừ chuyển hóa bằng cách tăng mất HCO3- và tăng giữ lại ion H là một quá trình chậm hơn nhiều và mất vài giờ đến vài ngày để bù trừ sự mất cân băng pH. Do đó, nồng độ HCO3- hầu như bình thường trong tăng thông khí cấp tính vì bài tiết qua thận chưa có đủ thời gian để làm giảm nồng độ HCO3-. Khi tăng thông khí bước vào giai đoạn mạn tính, nồng độ HCO3- sẽ giảm.
Cơ chế của kiềm hô hấp:
- Tăng thông khí do hệ thần kinh trung ương bởi chấn thương đầu, đột quỵ, đau, lo lắng, nhiễm trùng huyết, sợ hãi, căng thẳng, thuốc và dược phẩm.
- Tăng thông khí do thiếu oxy máu, như do thuyên tắc phổi, viêm phổi, tràn khí màng phổi, và các đợt cấp của bệnh phổi mạn tính.
- Thông khí phút quá mức với máy thở áp lực dương.
Bù trừ dự kiến trong kiềm hô hấp (Bảng 2.3 và Hình 2.1). Phản ứng chuyển hóa dự kiến đối với pCO2 máu giảm trong kiềm hô hấp là thận giảm tái hấp thu bicarbonate ở ống lượn gần, làm giảm HCO3- huyết tương và giảm pH huyết tương. Vì bù trừ chuyển hóa tương đối chậm, nó phụ thuộc vào thời gian và xảy ra theo hai giai đoạn. Do đó, bù trừ dự kiến có hai thuật toán để dự đoán nồng độ HCO3- trong máu:
Kiềm hô hấp cấp (<24 giờ): Cứ mỗi 10 mmHg giảm pCO2 động mạch dưới 40 mmHg, pH sẽ tăng khoảng 0,08, và HCO3- sẽ giảm ~2 mmol/L. Ví dụ, trong giai đoạn này, nếu pCO2 giảm từ 40 xuống 30 mmHg, sự giảm 10 mmHg này sẽ đi kèm với sự tăng pH 0,08 (pH ~7,48) và giảm bicarbonate 2 mmol/L từ 24 xuống ~22 mmol/L.
Phương trình cho điều này là:
HCO3- bù trừ = HCO3- ban đầu – 0.2 × (pCO2 ban đầu – pCO₂ bù trừ) (2.8)
Kiểm hô hấp mạn (2-5 ngày): Cứ mỗi 10 mmHg giảm pCO2, pH sẽ tăng khoảng 0,03 và HCO3- sẽ giảm khoảng 5 mmol/L. Ví dụ, nếu pCO2 giảm từ 40 xuống 30 mmHg sau 2 ngày tăng thông khí, pH sẽ tăng 0,03 (pH ~7,43) và HCO3-sẽ giảm khoảng 5, từ 24 xuống 19 mmol/L.
HCO3- bù trừ = HCO3- ban đầu – 0.5× (pCO2 ban đầu – pCO₂ bù trừ) (2.9)
Lưu ý: Giới hạn dưới cho bù trừ chuyển hóa trong tăng thông khí là HCO3- huyết tương ~12 mmol/L (~12 mEq/L). Nếu HCO3- huyết tương <12 mmol/L (<12 mEq/L), có thể có một tỉnh trạng toan chuyển hóa tiềm ẩn.
Thận trọng: Các tính toán bù trừ dự kiến này nên được sử dụng như những hướng dẫn trong chẩn đoán và không nên được diễn giải quá mức như một chẩn đoán tuyệt đối.
Điều trị kiềm hô hấp. Điều trị nhằm mục đích khắc phục hoặc làm giảm bớt tỉnh trạng cơ bàn, chẳng hạn như thuốc điều trị lo âu hoặc đau, kháng sinh cho nhiễm trùng huyết, hoặc thuốc chống đông cho thuyên tắc phối. Thiếu oxy máu phải được điều chỉnh bằng cách cung cấp oxy bổ sung. Tăng thông khí do lo lắng có thể được điều trị bằng cách trấn an hoặc đôi khi bằng cách hít thở lại không khí đã thở ra (có hàm lượng CO2 cao hơn) ở những người khỏe mạnh.
5 Phát hiện các rối loạn kiềm-toan hỗn hợp
Rối loạn kiềm-toan hỗn hợp xảy ra khi nhiều rối loạn kiềm-toan nguyên phát xảy ra cùng một lúc. Chúng phổ biến trong các quần thể bệnh viện, đặc biệt là ở khoa cấp cứu và đơn vị chăm sóc đặc biệt. Mặc dù các phương trình và Hình 2.1 và Hình 2.2 có thể hỗ trợ chẩn đoán, những mối quan hệ này có thể không hoàn toàn đúng ở những bệnh nhân có rối loạn kiềm-toan phức tạp và mạn tính thay đổi trong quá trình bệnh. Không có gì thay thế được việc xem xét cẩn thận bệnh sử và đánh giá lâm sàng của bệnh nhân.
Tầm quan trọng của việc xác định các rối loạn kiểm-toan hỗn hợp nằm ở ý nghĩa chẩn đoán và điều trị của chúng. Ví dụ, sự phát triển của một kiểm chuyển hóa nguyên phát ở một bệnh nhân mắc bệnh đường thở tắc nghẽn mạn tính đang được điều trị bằng thuốc lợi tiểu nên cảnh báo bác sĩ lâm sàng về khả năng thiếu hụt kali, và một bệnh nhân có kiểm hô hấp và toan chuyển hóa hỗn hợp nên được đánh giá về khả năng ngộ độc salicylate.
6 Bù trừ dự kiến có xảy ra không?
Một khái niệm đơn giản cần nhớ trong một rối loạn kiềm-toan nguyên phát là, nếu bù trừ dự kiến không xảy ra, nên nghi ngờ có rối loạn hỗn hợp. Ví dụ, trong toan chuyển hóa nguyên phát, phổi được kỳ vọng sẽ bù trừ cho lượng acid chuyển hóa dư thừa này bằng cách tăng thông khí (một quá trình kiểm hô hấp) để loại bỏ acid hô hấp CO2 và đưa pH trở lại bình thường. Nếu điều này không xảy ra như mong đợi, người đó được coi là có toan hô hấp tiềm ẩn.
Toan chuyển hóa: Phản ứng hô hấp để bù trừ toan chuyển hóa là tăng thông khí, làm bình thường hóa pH bằng cách giảm pCO2, để cân bằng sự thiếu hụt HCO3-. Phản ứng tăng thông khí bù trừ này bắt đầu trong vòng 30 phút và sẽ đạt tối đa sau 12-24 giờ. Phản ứng này sẽ làm giảm pCO2 máu 1,2 mmHg cho mỗi 1 mmol/L giảm HCO3- máu. Như đã suy ra trước đó, pCO2 (mmHg) dự kiến trong thời gian này sẽ nằm trong khoảng 3 mmHg của: \text{pCO2, bù trừ} = \text{pCO2 ban đầu} -1.2 \times [\text{HCO3-ban dầu} - \text{HCO3- bù trừ}] \quad (2.10)
Kiểm chuyển hóa: Phản ứng bù trừ cho kiểm chuyển hóa là giảm thông khí, làm tăng PCO2. Như đã mô tả trước đó, trong giai đoạn bù trừ này, pCO2 (mmHg) dự kiến sẽ nằm trong khoảng 3 mmHg của:
pCO₂ bù trừ = pCO2 ban đầu + 0.7 × [HCO3- bù trừ - HCO3- ban đầu] (2.11)
Toan hô hấp hoặc kiểm hô hấp: Nếu bệnh nhân có toan hô hấp đơn thuần, nồng độ HCO3-, bù trừ dự kiến có thể được dự đoán bằng phương trình (2.4) hoặc (2.5) cho toan hô hấp cấp và bằng phương trình (2.6) hoặc (2.7) cho toan hô hấp mạn. Nếu bệnh nhân có kiểm hô hấp đơn thuần, nồng độ HCO3-, bù trừ dự kiến có thể được dự đoán bằng phương trình (2.8) cho những thay đổi cấp tính và bằng phương trình (2.9) cho những thay đổi mạn tính. Ngoài ra, các quy tắc đơn giản dự đoán những thay đổi pH dự kiến so với sự thay đổi pCO2 trong các giai đoạn cấp và mạn tính. Trong giai đoạn cấp của các rối loạn hô hấp, cứ mỗi 10 mmHg tăng hoặc giảm pCO2, pH sẽ thay đổi 0,08. Khi điều này tiến triển vào giai đoạn mạn tính (1-2 ngày), cứ mỗi 10 mmHg tăng hoặc giảm pCO2, pH sẽ chỉ thay đổi 0,03. Bảng 2.4 minh họa mối quan hệ giữa pCO2, pH, và HCO3- cho những thay đổi hô hấp cấp và mạn tính:
Bảng 2.4. Những thay đổi dự kiến của pCO2, pH và HCO3- trong các tình trạng hô hấp cấp và mạn tính
| pCO2: (mmHg) | Tình trạng hô hấp cấp | Tình trạng hô hấp mạn | ||
| HCO3- (mmol/L) | pH | HCO3- (mmol/L) | pH | |
| 70 | 27 | 7.16 | 34.5 | 7.31 |
| 60 | 26 | 7.24 | 31.0 | 7.34 |
| 50 | 25 | 7.32 | 28.0 | 7.37 |
| 40 | 24 | 7.40 | 24.0 | 7.40 |
| 30 | 22 | 7.48 | 19.0 | 7.43 |
| 20 | 20 | 7.56 | 14.0 | 7.46 |
Khoảng trống Delta và Tỷ lệ Delta (tỷ lệ delta). "Khoảng trống Delta" là sự khác biệt giữa sự gia tăng AG và sự giảm HCO3-. Nó có thể giúp xác định xem toan chuyển hóa tăng khoảng trống anion có được giải thích hoàn toàn bởi sự giảm HCO3- hay không, hoặc liệu có khả năng có một rối loạn kiểm-toan hỗn hợp. Nếu Khoảng trống Delta gần bằng không, có khả năng là có một toan chuyển hóa đơn lẻ hoặc "thuần túy". Nếu khoảng trống Delta dương rõ rệt, điều đó cho thấy có nhiều HCO3- hơn trong máu (tức là ít HCO3- bị mất hơn) so với dự kiến từ AG tăng, do đó có thể có thêm một kiềm chuyển hóa. Nếu Khoảng trống Delta âm rõ rệt, điều đó cho thấy có ít HCO3- hơn (nhiều HCO, bị mất hơn) so với dự kiến từ AG tăng, do đó có thể có thêm một toan chuyển hóa không do AG.
Khoảng trống Delta = (AG - 12) - (24 - HCO3-) (2.12)
"Tỷ lệ Delta" dựa trên cùng một khái niệm để diễn giải một AG tăng, ngoại trừ việc nó sử dụng tỷ lệ của sự gia tăng AG (Na-CI-HCO3-) từ một giá trị trung bình bình thường là 12, so với sự giảm HCO3-, từ một giá trị bình thường là 24.
Một phương trình cho Tỷ lệ Delta như sau:
Tỷ lệ Delta = (AG - 12)/(24 - HCO3-) (2.13)
[Lưu ý rằng giá trị HCO3-, là 24 làm cho Tỷ lệ Delta không xác định vì mẫu số bằng không]
Trong một toan chuyển hóa điển hình, sự gia tăng AG từ 12 mmol/L và sự giảm HCO3- từ 24 mmol/L sẽ xấp xỉ bằng nhau, do đó "Tỷ lệ Delta" sẽ xấp xỉ 1. Nếu Tỷ lệ Delta lớn hơn 1 đáng kể, điều đó cho thấy có nhiều HCO3- hơn trong máu so với dự kiến từ AG tăng, do đó có thể có thêm một kiềm chuyển hóa. Nếu Tỷ lệ Delta nhỏ hơn 1 đáng kể, điều đó có nghĩa là có ít HCO3- hơn so với dự kiến từ AG tăng, do đó điều này cho thấy có thêm một toan chuyển hóa không do AG. Ví dụ về các Tỷ lệ Delta và Khoảng trống Delta khác nhau được minh họa trong Bảng 2.5, và các khoảng diễn giải được trình bày trong Bảng 2.6.
Bảng 2.5. Ví dụ về Tỷ lệ Delta và Khoảng trống Delta trong các toan chuyển hóa
| HCO3- (mmol/L) | Khoảng trống anion (AG, mmol/L) | Tỷ lệ Delta | Khoảng trống Delta | Tình trạng |
| 24 | 12 | Không xác định | 0 | Giá trị bình thường |
| 18 | 24 | Không xác định | +8 | Rối loạn hỗn hợp: Toan chuyển hóa AG + Kiềm chuyển hóa |
| 18 | 24 | 2.0 | +6 | Rối loạn hỗn hợp: Toan chuyển hóa AG + Kiềm chuyển hóa |
| 16 | 20 | 1.0 | 0 | Toan chuyển hóa AG thuần túy |
| 12 | 24 | 1.0 | 0 | Toan chuyển hóa AG thuần túy |
| 18 | 13 | 0.55 | -5 | Rối loạn hỗn hợp: Toan chuyển hóa AG + Toan chuyển hóa không do AG |
| 10 | 20 | 0.57 | -6 | Rối loạn hỗn hợp: Toan chuyển hóa AG + Toan chuyển hóa không do AG |
Ghi chú:
Tỷ lệ Delta = AG / HCO3-
Khoảng trống Delta = (AG đo - AG bình thường) – (HCO3- bình thường - HCO3- đo)
Dùng để phát hiện rối loạn hỗn hợp khi không phù hợp với toan chuyển hóa thuần túy.
Bảng 2.6. Diễn giải Khoảng trống Delta và Tỷ lệ Delta khi có toan chuyển hóa
| Khoảng trống Delta | Tỷ lệ Delta | Diễn giải |
| ≤-5 | ≈0,4 | Toan khoảng trống anion hỗn hợp: Toan chuyển hóa AG + Toan chuyển hóa không do AG |
| -4 đến +4 | 0,5-1,9 | Toan khoảng trống anion cao “thuần túy” |
| ≥+5 | ≥2,0 | Toan khoảng trống anion cao hỗn hợp + Kiểm chuyển hóa |
Như vậy:
- Khoảng trống Delta âm nhiều (≤ -5) → gợi ý có thêm toan chuyển hóa không do AG.
- Khoảng trống Delta gần 0 (-4 đến +4) → thường là toan AG cao thuần túy.
- Khoảng trống Delta dương cao (≥ +5) - cho thấy có kiểm chuyển hóa phối hợp.
Dưới đây là một số phát hiện gợi ý mạnh mẽ về các rối loạn kiểm-toan hỗn hợp:
- Nếu pH nằm trong giới hạn bình thường và cả HCO3-, và pCO2 đều bất thường.
- HCO3-, và pCO2 bất thường theo hướng ngược lại, ví dụ, HCO3- tăng với pCO2 giảm. Phản ứng bù trừ phải luôn cùng hướng với sự thay đổi do rối loạn nguyên phát gây ra.
- Các rối loạn kiểm-toan đơn thuần không bù trừ quá mức. Tức là, bù trừ sẽ không làm cho một tỉnh trạng nhiễm toan máu trở thành nhiễm kiềm máu. Thực tế, cơ chế bù trừ thường dừng lại một chút trước khi pH bình thường hóa.
7 Tiếp cận chẩn đoán các rối loạn kiềm-toan
Khoảng tham chiếu
Khoảng tham chiếu cho cả máu động mạch và tĩnh mạch được trình bày trong Bảng 1.1 cho các thông số khí máu và kiềm-toan phổ biến.
Tiếp cận từng bước để đánh giá tình trạng kiềm-toan
Lý tưởng nhất, việc đánh giá các rối loạn kiểm-toan, bao gồm cả các rối loạn kiểm-toan hỗn hợp, sẽ bao gồm thông tin đồng thời về bệnh sử lâm sảng, khám thực thể, kết quả điện giải, và kết quả khí máu của bệnh nhân. Với các máy phân tích khí máu hiện đại, kết quả khí máu thường có sẵn cùng với kết quả điện giải, chất chuyển hóa, và hemoglobin.
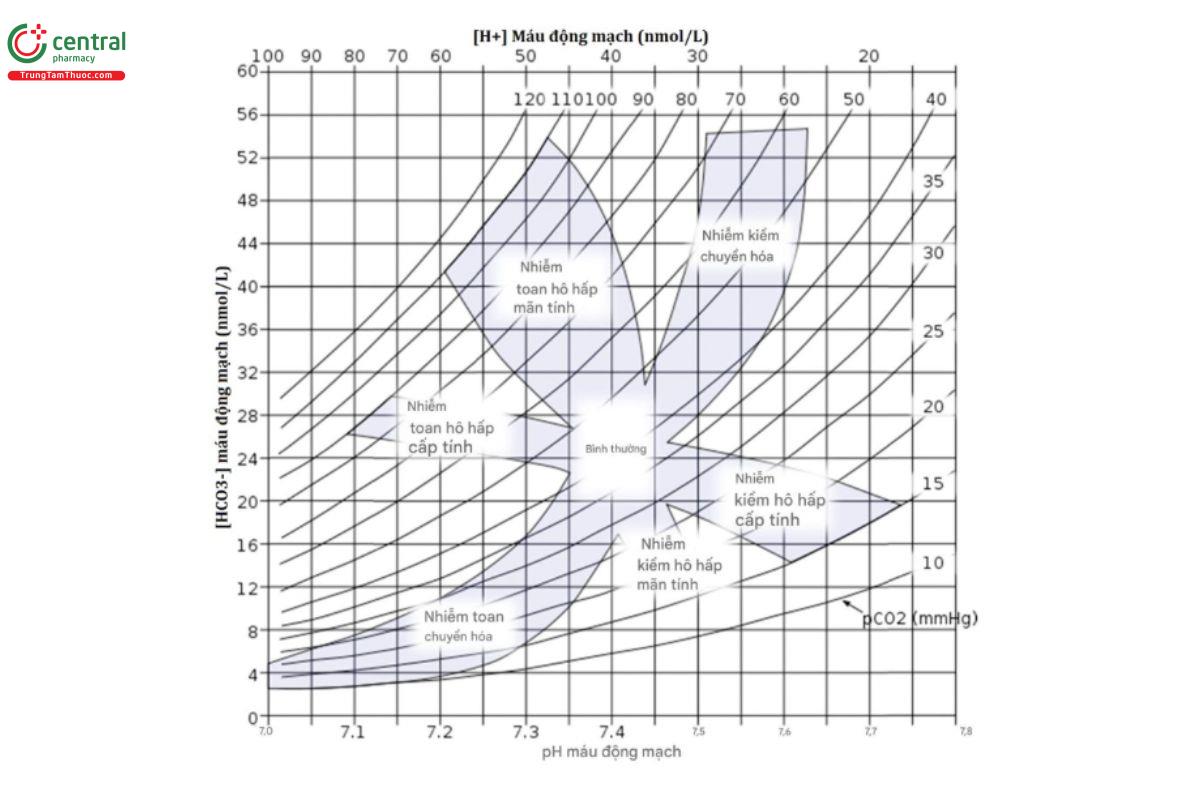
Hình 2.2 hữu ích như một hướng dẫn để đánh giá kết quả pH, pCO2, và HCO3- của bệnh nhân cho một rối loạn kiềm-toan tiềm tàng. Bảng kết quả khí máu (pH, pCO2, pO2, HCO3-, Na, K, lactat, v.v.) có thể được đánh giá theo nhiều bước, như sau:
1. Đánh giá bệnh sử lâm sàng và tỉnh trạng hiện tại của bệnh nhân để dự đoán các tỉnh trạng liên quan đến rối loạn kiềm-toan (xem Bảng 2.7).
2. Đánh giá pH.
3. Đánh giá tỉnh trạng thông khí (pCO2) và chuyển hóa (HCO3-) để có cái nhìn sâu sắc về việc liệu rối loạn kiểm-toan là đơn thuần hay có thể là một rối loạn hỗn hợp.
4. a. Đánh giá dữ liệu lâm sàng và xét nghiệm cho một rối loạn hỗn hợp có thể xảy ra và liệu bù trừ có phù hợp không. b. Các thông số như điện giải, lactat, AG, hoặc Khoảng trống/Tỷ lệ Delta có chỉ ra rằng có một rối loạn kiềm-toan khác không? c. Biểu hiện lâm sàng của bệnh nhân có phù hợp với kết quả khí máu không?
Việc đánh giá tình trạng oxy hóa hầu như độc lập với việc diễn giải kiềm-toan, và nó được thảo luận trong Chương 4.
Bảng 2.7. Ví dụ về các rối loạn kiểm-toan dự kiến trong các tình trạng lâm sàng
| Tình trạng lâm sàng | Rối loạn kiềm-toan dự kiến |
| Ngừng tim | Toan chuyển hóa |
| Ngừng thở | Toan hô hấp |
| Tăng thông khí (nhiều nguyên nhân) | Kiềm hô hấp |
| Tắc ống nội khí quản | Toan hô hấp |
| Nôn mửa | Kiềm chuyển hóa |
| Tiêu chảy | Toan chuyển hóa |
| Sốc (giảm tưới máu) | Toan chuyển hóa |
| Phù phổi cấp | Kiềm hô hấp (thiếu oxy → tăng thông khí) |
| Phù phổi nặng | Toan hô hấp |
| Điều trị lợi tiểu | Kiềm chuyển hóa |
| Ngộ độc thuốc | Toan hô hấp (ngừng thở) |
| Điều trị bicarbonate | Kiềm chuyển hóa |
| Tưới máu kém | Toan chuyển hóa |
Các bước tiếp cận đánh giá rối loạn kiềm - toan:
Bước 1. Đánh giá bệnh sử lâm sàng và tình trạng của bệnh nhân để dự đoán các rối loạn kiềm-toan có thể xảy ra
Có nhiều tỉnh trạng lâm sàng liên quan đến rối loạn kiểm-toan, như được liệt kê trong Bảng 2.7. Một đánh giá lâm sàng sâu sắc, cả ở lần đánh giá ban đầu và trong suốt quá trình lâm sàng, là một phần vô giá của việc đánh giá một bệnh nhân về các rối loạn kiềm-toan.
Bước 2. Đánh giá pH
Một pH bất thường cho thấy đã xảy ra một tỉnh trạng toan hoặc kiểm và mức độ của rối loạn kiểm-toan, và nó có thể gợi ý rằng đã có sự bù trừ. Tuy nhiên, chỉ riêng pH không cho biết liệu có một rối loạn hỗn hợp hay không. Hãy xem xét các ví dụ sau:
pH 7,20 xác nhận rằng có một tình trạng toan nặng và sự bù trừ hoặc đang ở giai đoạn đầu hoặc không hiệu quả trong việc kiểm soát tỉnh trạng toan. Cần điều tra thêm để xác định nguồn gốc chuyển hóa hoặc hô hấp của tình trạng toan và liệu có nhiều hơn một quá trình toan hay không.
pH 7,48 cho thấy một tình trạng kiểm nhẹ. Cần thêm thông tin để xác định nguyên nhân của tỉnh trạng kiềm và liệu tỉnh trạng kiềm đang ở giai đoạn đầu (và có thể trở nên tồi tệ hơn), đã được bù trừ gần như hoàn toàn, hay là một phần của một rối loạn hỗn hợp.
Một pH bình thường có thể cho thấy bệnh nhân không có rối loạn kiểm-toan. Tuy nhiên, bệnh nhân có thể có một sự kết hợp của các sự kiện toan và kiểm (nguyên phát hoặc bù trừ) đã bù trừ cho nhau. Ngoài bệnh sử của bệnh nhân, HCO3- và pCO2 phải được xem xét, như trong các ví dụ sau:
- pH 7,45 với HCO3- và pCO2 tăng cho thấy một kiểm chuyển hóa nguyên phát đã được bù trừ bởi một phản ứng toan hô hấp. Tương tự, một pH 7,45 với HCO3- và pCO2, giảm cho thấy một kiểm hô hấp nguyên phát đã được bù trừ bởi một phản ứng toan chuyển hóa.
- pH 7,40 với cả HCO3- và pCO2 bất thường cho thấy có một tình trạng toan và kiềm hỗn hợp đã tỉnh cờ bù trừ cho nhau để cho ra một pH bình thường.
Bước 3. Đánh giá tình trạng thông khí và chuyển hóa
Cách tiếp cận đơn giản nhất để đánh giá pCO2 và HCO3- là xem xét từng thông số riêng biệt như chỉ ra tình trạng toan, kiềm, hoặc bình thường, sau đó đánh giá chúng cùng với pH để xác định liệu rối loạn nguyên phát là hô hấp hay chuyển hóa và liệu có một rối loạn hỗn hợp hoặc bù trừ hay không.
Một pCO2, giảm cho thấy một quá trình kiểm hô hấp, có thể là nguyên phát hoặc bù trừ. Một pCO2 tăng cho thấy một quá trình toan hô hấp, có thể là nguyên phát hoặc bù trừ (Bảng 2.8).
Bảng 2.8. Đánh giá tình trạng thông khí bằng pCO2 động mạch
| pCO2 | Tình trạng thông khí |
| Giảm | Có một quá trình kiểm hô hấp (tăng thông khí) |
| Bình thường | Thông khí bình thường (cần xem xét có rối loạn hỗn hợp không) |
| Tăng | Có một quá trình toan hô hấp (giảm thông khí) |
Một HCO3- giảm cho thấy một tỉnh trạng toan chuyển hóa, có thể là nguyên phát hoặc bù trừ. Một HCO3- tăng cho thấy một tỉnh trạng kiểm chuyển hóa, có thể là nguyên phát hoặc bù trừ.
Bảng 2.9. Đánh giá tình trạng chuyển hóa bằng bicarbonate huyết tương (HCO3- )
| Bicarbonate (tổng CO2) | Tình trạng chuyển hóa |
| Giảm | Có một quá trình toan chuyển hóa (nguyên phát, bù trừ, hoặc hỗn hợp) |
| Bình thường | Không có rối loạn kiểm-toan chuyển hóa (nhưng vẫn có thể là rối loạn hỗn hợp) |
| Tăng | Có một quá trình kiểm chuyển hóa (nguyên phát, bù trừ, hoặc hỗn hợp) |
Bảng 2.8 (dựa vào pCO2) và bảng 2.9 (dựa vào HCO3-) thường đi kèm nhau để đánh giá trục hô hấp – chuyển hóa trong phân tích khí máu.
Lưu ý: Các thuật ngữ "kiềm hô hấp," "toan chuyển hóa," vv., để cập đến các quá trình bệnh lý và không phải là sự bù trừ. Tuy nhiên, tôi tin rằng việc tạm thời coi bất kỳ pCO2 giảm nào (ví dụ) là một quá trình kiểm hô hấp sẽ đơn giản hóa việc diễn giải. Liệu đó là một bất thường nguyên phát hay sự bù trừ phù hợp sẽ trở nên rõ ràng khi các yếu tố khác được xem xét.
Bước 4. Đánh giá dữ liệu lâm sàng và xét nghiệm cho một rối loạn hỗn hợp có thể xảy ra
Bước 4 có ba thành phần.
Bước 4a. Sự bù trừ có phù hợp với rối loạn nguyên phát không? Để đánh giá liệu sự bù trừ dự kiến có đang xảy ra đối với rối loạn kiểm-toan nguyên phát hay không, hãy tham khảo các mô tả "Bù trừ dự kiến" trong các phần khác nhau của các rối loạn kiềm-toan được mô tả trong chương này và phần "Phát hiện các Rối loạn Kiềm-Toan Hỗn hợp."
Bước 4b. Các kết quả xét nghiệm khác có gợi ý có thêm một rối loạn kiềm-toan không? Một số xét nghiệm thông thường có thể giúp xác định liệu có thêm các rối loạn kiểm-toan hay không.
- Kali. Hạ kali máu gợi ý có thể có kiểm chuyển hóa.
- pH. Một pH bình thường kết hợp với kết quả bất thường cho cả HCO3- và pCO2 cần xem xét một rối loạn kiểm-toan hỗn hợp.
- Clorua. Tăng clo máu có thể do nhiều nguyên nhân như đã mô tả trong phần toan chuyển hóa, chẳng hạn như toan hóa ống thận trong đó HCO3- bị mất trong nước tiêu, hoặc từ một toan chuyển hóa nguyên phát hoặc từ sự bù trừ toan chuyển hóa cho kiểm hô hấp. Giảm clo máu thúc đẩy thận giữ lại HCO3- dẫn đến kiểm chuyển hóa. Bù trừ cho toan hô hấp mạn tính làm tăng giữ lại HCO3-, của thận với việc mất CI-.
- Khoảng trống anion (AG). Một AG tăng >20 mmol/L cho thấy có toan chuyển hóa. AG cũng hữu ích trong việc phân biệt các nguyên nhân của toan chuyển hóa, như được trình bày trong Bảng 2.1.
- Khoảng trống Delta hoặc Tỷ lệ Delta. Các thông số này được thảo luận trước đó. Nếu Khoảng trống Delta dương rõ rệt hoặc Tỷ lệ Delta xấp xỉ hai hoặc lớn hơn, điều đó gợi ý có thể có thêm một kiểm chuyển hóa. Nếu Khoảng trống Delta âm rõ rệt hoặc Tỷ lệ Delta xấp xỉ 0,4-0,8, điều đó gợi ý có thể có thêm một toan chuyển hóa không do AG.
- Lactat. Một lactat máu tăng là một chỉ số nhạy cảm của toan chuyển hóa do nhiều rối loạn oxy hóa liên quan đến thông khí, trao đổi khí phế nang, vận chuyển tuần hoản, hấp thu tế bào, và/hoặc rối loạn chức năng ty thể.
- Creatinin. Một creatinin tăng cho thấy suy thận và có thể có toan chuyển hóa do urê huyết cao.
Bước 4c. Bệnh nhân có các tình trạng khác liên quan đến rối loạn kiềm-toan không? Như đã lưu ý trong Bước 1, việc đánh giá tình trạng kiềm-toan phải bao gồm các phát hiện từ bệnh sử và khám thực thể của bệnh nhân. Nhiều tỉnh trạng thường liên quan đến rối loạn kiềm-toan, với một số tỉnh trạng phổ biến được liệt kê trong Bảng 2.7. Đặc biệt nếu kết quả khí máu không giải thích rõ ràng rối loạn "nguyên phát" của bệnh nhân, điều này nên cảnh báo bác sĩ lâm sàng về khả năng có một rối loạn kiềm-toan hỗn hợp.
Tóm tắt diễn giải kiềm-toan (pH, PCO₂, và HCO3-)
Đánh giá pH: Trên 7,45 = Kiềm; Dưới 7,35 = Toan
Đánh giá tình trạng thông khí (pCO2) và chuyển hóa (HCO3-):
- pH và pCO2 thay đổi cùng chiều = Rối loạn chuyển hóa
- pH và pCO2 thay đổi ngược chiều = Rối loạn hô hấp
Xác định liệu có rối loạn hỗn hợp:
- Sự bù trừ của thận hoặc phổi có xảy ra khi mong đợi không? (Có: rối loạn đơn thuần; Không: rối loạn hỗn hợp)
- HCO3- và pCO2 có thay đổi ngược chiều không? (Có: rối loạn hỗn hợp)
- Các xét nghiệm khác có gợi ý có rối loạn kiểm-toan khác không? (K, CI, AG, Lactat, Creatinin, Khoảng trống/Tỷ lệ Delta)
- Bệnh sứ của bệnh nhân có chỉ ra có rối loạn kiềm-toan khác không?
Ví dụ ca lâm sàng kiềm-toan phức tạp
Đây là một ví dụ hay về cách một trường hợp kiềm-toan phức tạp có thể được đánh giá. Nó minh họa một số khái niệm: (1) thách thức của việc đánh giá phản ứng bù trừ trong các rối loạn kiềm-toan hô hấp vì chúng phụ thuộc vào thời gian; (2) các biểu đồ khác nhau có thể hữu ích như một hướng dẫn, nhưng phải được diễn giải một cách thận trọng trong các rối loạn kiềm-toan phức tạp; và (3) tầm quan trọng của việc đánh giá bệnh sử của bệnh nhân. Dưới đây là các kết quả kiểm-toan: pH: 7,27; pCO2: 70 mmHg (9,3 kPa); HCO3-: 31 mmol/L
pH thấp và pCO2, tăng cho thấy người này bị toan hô hấp. Theo Hình 2.2, đối với pCO2 70 mmHg, HCO3- bù trừ sẽ là ~27 mmol/L cho toan hô hấp cấp hoặc khoảng 36 mmol/L cho toan hô hấp mạn. Vì HCO3- đo được nằm giữa hai nồng độ này, có khả năng có một rối loạn kiểm-toan hỗn hợp. Dưới đây là bốn giải thích có thể:
- Toan hô hấp mạn + toan chuyển hóa. Đây có thể là một bệnh nhân mắc bệnh phổi tắc nghẽn mạn tính đã phát triển toan chuyển hóa do tiêu chảy hoặc suy giảm chuyển hóa oxy trong nhiễm trùng huyết.
- Một bệnh nhân bị toan hô hấp mạn đã phát triển thêm một toan hô hấp cấp chồng lên. Bệnh nhân có thể đã có pCO2 55 mmHg (7,3 kPa) với HCO3- được bù trừ phù hợp là 31 mmol/L, sau đó phát triển viêm phổi làm tăng cấp tính pCO2 lên 70 mmHg.
- Toan hô hấp cấp + kiểm chuyển hóa. Đây có thể là một người bị suy hô hấp cấp do dùng thuốc an thần, sau đó phát triển kiềm chuyển hóa do nôn hoặc dùng thuốc lợi tiều làm tăng HCO3- từ 27 lên 31 mmol/L.
- Toan hô hấp cấp đang tiến triển thành toan hô hấp mạn. Điều này có thể xảy ra khoảng 1-3 ngày sau khi đợt cấp bắt đầu.
8 TÀI LIỆU THAM KHẢO
1. Seifter, J. L.; Chang, H.-Y. Disorders of Acid-Base Balance: A New Perspective. Kidney Dis. 2017, 2 (4), 170-186.
2. Grogono, A. W. Acid-Base Tutorial: Metabolic Acidosis and Alkalosis. http:/www.acid-base. com. (accessed December 2008).
3. Brandis, K. Acid-Base Physiology: Metabolic Acidosis Causes. From http://www. anaesthesiaMCQ.com/AcidBaseBook. (accessed January 2009).
4. Robergs, R. A.; Ghiasvand, f, Parker, D. Biochemistry of Exercise-Induced Metabolic Acidosis. Am. J. Physiol. Regul. Integr. Comp. Physiol. 2004, 287, R502-R516.
5. Kraut, J. A.; Nagami, G. T. The Serum Anion Gap in the Evaluation of Acid-Base Disorders: What Are Its Limitations and Can Its Effectiveness Be Improved? Clin. J. Am. Soc. Nephrol. 2013, 8, 2018-2024.
6. Feldman, M.; Soni, N.; Dickson, B. Influence of Hypoalbuminemia or Hyperalbuminemia on the Serum Anion Gap. J. Lab. Clin. Med. 2005, 146, 317-320.
7. Brandis, K. Acid Base Physiology: 3.2 the Anion Gap. www.anaesthesiamcq.com/AcidBaseBook/ab3 2.php.
8. Hamm, L. L.; Nakhoul, N.; Hering-Smith, K. S. Acid-Base Homeostasis. Clin. J. Am. Soc. Nephrol. 2015, 10, 2232-2242.
9. Emmett, M.; Palmer, B. F. Simple and Mixed Acid-Base Disorders, 2020. www.uptodate. com. contents/simple-and-mixed-acid-base-disorders.
10.Burger, M.; Schaller, D. J. Metabolic Acidosis; NCBI Bookshelf, November 2020. https://www.ncbi.nlm.nih.gov/books/NBK482146/.
11. Brandis, K. Acid-Base Physiology: Metabolic Acidosis Correction. From http://www. anaesthesiaMCQ.com/AcidBaseBook/ab5 6.php. (accessed December 2020).
12.Brinkman, J. E.; Sharma, S. Physiology, Metabolic Alkalosis Stat Pearls, 2020. www.ncbi.nlm.nih.gov/books/NBK482291/.
13.Story, D. A.; Morimatsu, H.; Bellomo, R. Strong lons, Weak Acids and Base Excess: A Simplified Fencl-Stewart Approach to Clinical Acid-Base Disorders. Br. J. Anaesth. 2004, 92, 54-60.
14.Brandis, K. Acid-Base Physiology: Metabolic Alkalosis Causes. From http://www. anaesthesiaMCQ.com/AcidBaseBonyharassed November 2020).

