Các bệnh lý tiền ung thư, ung thư da và cách điều trị
Nguồn: Hình ảnh lâm sàng, chẩn đoán và điều trị trong chuyên ngành da liễu tập 2
Chủ biên: PGS.TS.Nguyên Văn Thường
1 Dày sừng ánh sáng (Actinic keratosis)
1.1 Đại cương
Dày sừng ánh sáng (actinic keratosis- AK) là một bệnh lý phổ biển với tổn thương đặc trưng là những dát, mảng hoặc sẩn đỏ, bong vảy xuất hiện trên nền da bị tổn thương do tiếp xúc mạn tính với tia tử ngoại.
Bệnh thường xuất hiện ở những người lớn tuổi có làn da sáng màu.
Bệnh hiện được coi là giai đoạn sớm của ung thư biểu mô tế bào vảy tại chỗ, mặc dù hiếm khi dày sừng ánh sáng tiến triển thành ung thư biểu mô tế bào vảy xâm lấn.
Yếu tố nguy cơ:
- Đặc trưng cá thể (tuổi cao, nam giới, da sáng, tóc vàng hoặc đỏ, màu mắt sáng).
- Tiếp xúc mạn tính với tia tử ngoại.
- Sống ở vùng có vĩ độ gần xích đạo, vùng khí hậu nhiệt đới, cận nhiệt đới.
- Tiền sử mắc dày sừng ánh sáng hoặc ung thư da khác.
- Suy giảm miễn dịch.
- Sử dụng một số thuốc gây tăng nhạy cảm ánh sáng.
- Hội chứng di truyền:
- Khô da sắc tố
- Hội chứng Bloom
- Hội chứng Rothmund-Thomson
1.2 Cơ chế bệnh sinh
Tia tử ngoại gây tác động trực tiếp hay gián tiếp lên các sợi ADN trong quá trình phân chia tế bào gây ra những sai lệch trong quá trình tổng hợp ADN, dẫn tới chết tế bào theo chương trình, những tế bào sừng chết theo chương trình này còn được gọi là tế bào “bỏng nắng” (sunburn cells).
Đột biến gen ức chế khối u p53 do tia uv gây ra trên các tế bào sừng lớp đáy gây ra đáp ứng bất thường với hiện tượng chết theo chương trình gây tăng sinh và phát triển bất thường các tế bào này.
Suy giảm miễn dịch cũng là một yếu tố nguy cơ, những bệnh nhân ghép tạng có tăng nguy cơ mắc dày sừng ánh sáng và ung thư biểu mô tế bào vảy (SCC), cơ chế bệnh sinh chưa rõ.
1.3 Lâm sàng
Thể điển hình: tổn thương thường xuất hiện ở những vùng tiếp xúc với ánh sáng (80%), phố biến nhất là mặt, tai, đỉnh đầu ở người hói, cổ, cánh tay và mặt mu bàn tay. Ở những bệnh nhân bị tổn thương nghiêm trọng, có thể phát hiện tổn thương ở vùng thân trên, chi dưới, mu bàn chân. Tổn thương AK điển hình ban đầu là những chấm nhỏ gồ ghề và thường được mô tả như giấy nhám. Theo thời gian tổn thương tăng dần kích thước (thường 3 - 10mm) trở nên đỏ và bong vảy, một số tổn thương lớn có thể tới vài centimet và thường có nhiều hơn một tổn thương.

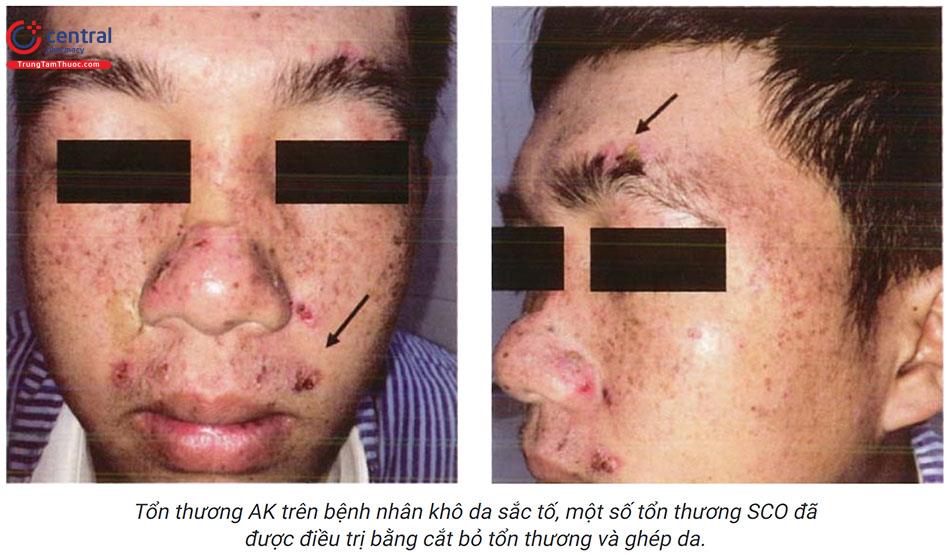
Một số biến thể khác của AK:
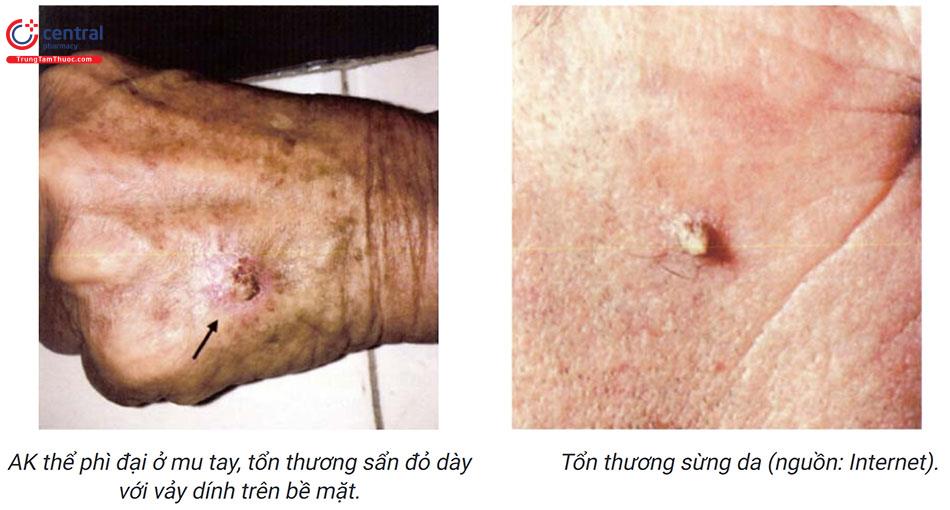
- AK thể phì đại (hypertrophic AK): những sẩn hoặc mảng xù xì, dày, vảy dính trên nền đỏ. Tổn thương có thể gặp ở bất cứ vị trí nào của cơ thể nhưng thường gặp hơn ở mu bàn tay, cánh tay, và da đầu. AK thể phì đại có thể tiến triển từ tổn thương AK điển hình và có thể khó phân biệt với scc, vì vậy cần có sinh thiết để chẩn đoán phân biệt.
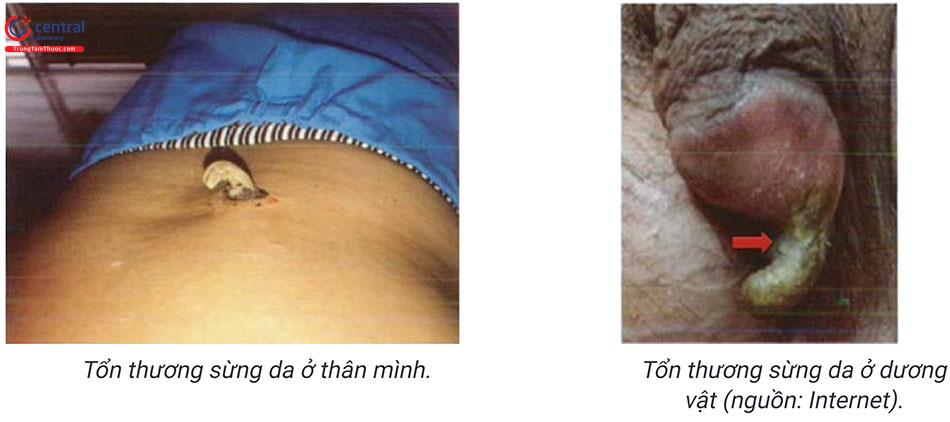
- Sừng da (cutaneous hom): không đặc hiệu cho AK và là một type của HAK, là khối sừng hình nón xuất hiện trên nền sẩn từ màu da tới đỏ. 38 - 40% tổn thương sừng đa là AK.
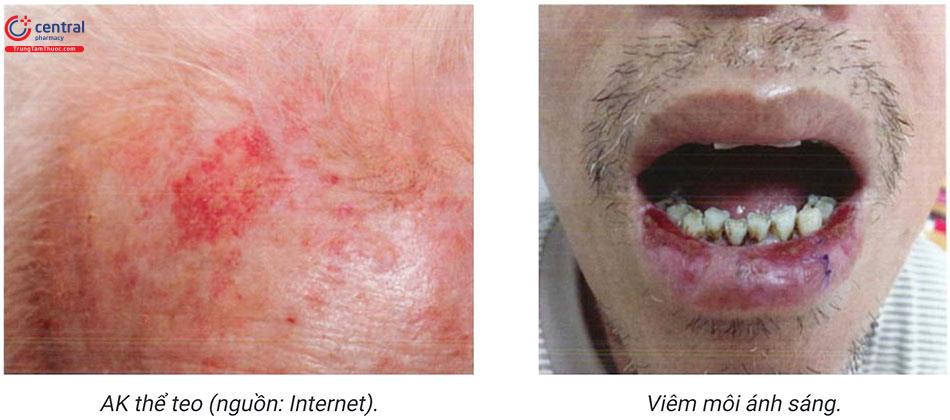
- AK thể teo: tổn thương là dát đỏ, bề mặt nhằn và không có vảy.
- Thể tăng sắc tố (pigmented AK): dát tăng sắc tố bong vảy, có thể khó phân biệt với lentigo ác tính.
- Viêm môi ánh sáng (actinic cheilitis): biểu hiện AK ở môi, tổn thương là vùng xù xì, bong vảy mạn tính, bệnh nhân thường than phiền là khô môi, đôi khi môi nứt nẻ, trợt và loét. Viền môi không rõ và dày sừng từng điểm hoặc bạch sản cũng có thể xuất hiện. Những tổn thương loét dai dẳng hoặc sùi cần yêu cầu sinh thiết để loại trừ scc. Cơ năng: thường không có triệu chứng.
1.4 Cận lâm sàng
1.4.1 Sinh thiết chẩn đoán
Giúp khẳng định chẩn đoán đặc biệt trong những trường hợp cần loại trừ scc khi tổn thương trên lâm sàng có những dấu hiệu sau: tổn thương >1 cm đường kính, thâm nhiễm, tiến triển nhanh, loét, đau khi sờ nắn, thất bại với điều trị AK thông thường (ví dụ: AK tổn tại dai dẳng 8-12 tuần sau điều trị nitơ lỏng).
Nếu chỉ có một phần tổn thương được cắt sinh thiết vì lý do tổn thương kích thước lớn hoặc liên quan tới biến chứng sẹo, điểm lựa chọn sinh thiết nên là nơi mà tổn thương dày nhất vì scc trên nền AK thường xuất hiện ở vị trí này. Độ sâu cắt sinh thiết ít nhất phải đạt tới trung bì lưới để loại trừ scc xâm lấn.
Mô bệnh học của AK phụ thuộc vào thể lâm sàng và đặc điểm tổn thương: thoái hoá sợi chun, á sừng, lớp tế bào đáy không điển hình, tăng sắc tố lớp đáy, xâm nhập viêm, dày đặc tế bào sừng không điển hình (nếu có dày đặc tế bào sừng không điển hình thì phải cân nhắc ung thư biểu mô tế bào vảy tại chỗ).
1.4.2 Dermoscopy
Dấu hiệu đặc trưng của AK thể không tăng sắc tố bao gồm:
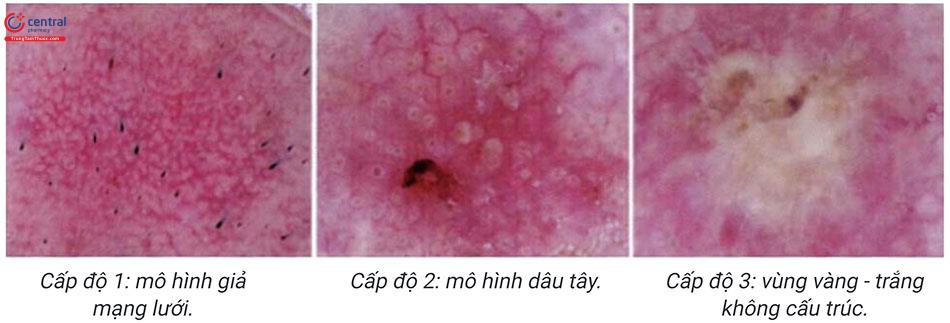
- Mô hình giả mạng lưới màu đỏ với vảy mỏng, rời rạc (cấp độ 1).
- Mô hình dâu tây (strawberry pat-term) được tạo thành bởi một nền đỏ xen kẽ bởi các lỗ mở của nang lông, dày sừng màu trắng - vàng tương tự bề mặt của một quả dâu tây (cấp độ 2).
- Vùng vàng - trắng không có cấu trúc (cấp độ 3).
1.5 Chẩn đoán
Chủ yếu dựa vào lâm sàng, trường hợp nghi ngờ chẩn đoán, như cần loại trừ scc hoặc điều trị thất bại, sinh thiết tổn thương là cần thiết.
Theo hướng dẫn của Hội Da liễu Anh (2017), AK được phân chia thành các cấp độ khác nhau:
- Cấp độ 1: mức độ nhẹ, tổn thương là các dát màu nâu, hồng với vảy mỏng hoặc sờ thấy lấm chấm.
- Cấp độ 2: mức độ trung bình: dày sừng nhiều hơn và dễ dàng phát hiện. + Cấp độ 3: nặng, phì đại, vảy dày.
- Mức thay đổi: các vùng hợp lại từ vài cm trở lên với sự thay đổi các cấp độ tổn thương khác nhau hoặc ở tất cả các cấp độ AK.
| AK kinh điển | Ak phi đại hoặc sừng da | AK tăng sắc tố |
| - SCC - Dày sừng dạng lichen mạn tính - Ung thư biểu mô tế bào đáy tại chỗ - Porokeratosis - Bệnh da viêm khác (vảy nến, viêm da dầu) | - SCC - Hạt cơm - Dày sừng da đầu | - Dày sừng da đầu - Lentigo ánh sáng - Lentigo ác tính |
1.6 Điều trị
Dày sừng ánh sáng có thể tiến triển theo các hướng: không đổi, tự thoái triển hoặc tiến triển thành ung thư biểu mô tế bào vảy. Thường không tiên đoán được chúng sẽ diễn tiến theo hướng nào mặc dù nguy cơ tiến triển của dày sừng ánh sáng thành ung thư biếu mô tế bào vảy là thấp, một bệnh nhân có thể có nhiều tổn thương và do đó, tỉ lệ này trở nên đáng kể, mặt khác tổn thương còn ảnh hưởng tới thẩm mỹ.
Hai nhóm phương pháp điều trị được đặt ra: điều trị phá huỷ tổn thương và điều trị bằng thuốc.
Hiệp hội chăm sóc ban đầu bệnh da liễu (primary care dermatology society) của Anh (2014) đã đưa ra hướng tiếp cận điều trị AK dưới đây:
| Mức độ tổn thương | Cấp độ 1 | Cấp độ 2 | Cấp độ 3 | Mức độ thay đổi | |
| Diện tích < 25cm2 | Diện tích > 25cm2 | ||||
| TẠI CHỖ | |||||
| Diclophenac 3% + hyaluronal gel | 2 | 1 | X | 2 | 2 |
| 5 - FU 5% | 1 | 2 | X | 2 | 1 |
| Imiquimod 5% | 1 | 1 | X | 1 | X |
| 5 - FU 0,5% + salicylic acid 10% | 2 | 2 | X | X | X |
| Imiquimod 3,75% | 1 | 1 | X | 1 | 2 |
| KHÁC | |||||
| Nitơ lỏng | 1 | 1 | 1 | X | X |
| PDT | 1 | 1 | X | 1 | 1 |
| Curet | 1 | 1 | 1 | X | X |
1: khuyến cáo tương đối, 2: khuyến cáo mạnh, x: không khuyến cáo điều trị đầu tiên
1.6.1 Điều trị phá huỷ tổn thương
Phương pháp áp lạnh: sử dụng nitơ lỏng (-196 °C) dạng xịt.
- Là phương pháp sử đụng rộng rãi nhất, thời gian đóng băng tuỳ thuộc vào vị trí tổn thương, chiều rộng và độ dày tổn thương.
- Với tổn thương mỏng, tỷ lệ đáp ứng lên tới 99%. Tổn thương dày và những tổn thương ở cánh tay, bàn tay đáp ứng kém hơn.
- Thời gian lành vết thương thay đổi từ 5 - 10 ngày ở mặt, 3-4 tuần ở bàn tay, 6 tuần hoặc lâu hơn ở chân. Nguy cơ sẹo, giảm sắc tố sau điều trị.
Phương pháp phẫu thuật: chủ yếu dựa vào các nghiên cứu nhỏ và kinh ng-hiệm.
- Cắt bỏ tổn thương: thường không được sử dụng trong điều trị dày sừng ánh sáng, thường chỉ áp dụng cho trường hợp tổn thương hay tái phát hoặc thâm nhiễm, đảm bảo tổn thương được kiểm tra trên mô bệnh học để loại trừ scc xâm lấn.
- Nạo bằng curet có sấy điện (elec-trodesiccation), bào (shave) và dao điện: có thể áp dụng với trường hợp tổn thương dày sừng nhiều, sừng da (cutaneous hom), mẫu bệnh phẩm không đánh giá hết được độ xâm lấn.
Liệu pháp quang động lực (PDT): hiệu quả vượt trội hơn phương pháp áp lạnh và đùng 5-FU trong một số nghiên cứu, ít tác dụng phụ. Thích hợp cho trường hợp có nhiều tổn thương.
1.6.2 Điều trị bằng thuốc
5-fluorouracil (5-FU) tại chỗ: thường dùng kem 5-FU 5%. Với tổn thương không dày sừng, hiệu quả lên tới 90%. Kem thường được áp dụng 1 - 2 lần/ngày trong 2-8 tuần. Đôi khi thuốc được kết hợp với Acid salicylic hoặc mỡ cal-cipotriol làm tăng hiệu quả.
Imiquimod 5% cream: thường áp dụng 2-3 lần/tuần trong 12-16 tuần, kết quả sạch tổn thương 50%. Kem nồng độ 3,75% có hiệu quả thấp hơn nhưng ít tác dụng phụ hơn.
Diclofenac gel bôi: là một loại thuốc chống viêm, dùng 2 lần/ngày trong 3 tháng, thuốc dung nạp tốt nhưng hiệu quả kém hơn các thuốc trên.
Retinoid bôi: hiệu quả không rõ.
1.7 Tiên lượng và phòng tránh
Dày sừng ánh sáng có thể tiến triển thành ung thư biểu mô tế bào vảy xâm lấn, tuy nhiên ung thư biểu mô tế bào vảy xâm lấn liên quan tới dày sừng ánh sáng ít có nguy cơ di căn, vậy nên bệnh nhân có tổn thương dày sừng ánh sáng cần theo dõi và khám da định kỳ 6 - 12 tháng.
Tổn thương có thể tái phát sau vài tháng hoặc nhiều năm điều trị.
Phòng tránh bằng cách sử dụng kem chống nắng phổ rộng (SPF 50+) hàng ngày tại vùng da tổn thương và vùng da hở, dùng quanh năm, che chắn ánh nắng bằng trang phục.
2 Dày sừng do Arsen (Arsenical keratosis)
2.1 Đại cương
Arsen là một nguyên tố kim loại được tìm thấy trong nhiều loại đá, arsen được giải phóng xâm nhập vào nước ngầm và có thể gây ô nhiễm nguồn nước cũng như thức ăn. Nồng độ arsen cao gây độc với nhiều tế bào đã được biết đến là một tác nhân gây ung thư.
Nhiều báo cáo xác nhận rằng arsen có thể gây bệnh Bowen, ung thư biểu mô tế bào vảy (SCC), ung thư biểu mô tế bào đáy (BCC) và các ung thư nội tạng (phổi, thận, bàng quang và gan).
Arsen cũng gây các tổn thương da như thay đổi sắc tố, tổn thương dày sừng. Tổn thương dày sừng là tổn thương da đặc trưng nhất sau phơi nhiễm arsen trong thời gian dài.
2.2 Cơ chế bệnh sinh
Cơ chế chưa rõ ràng, một số nghiên cứu cho thấy arsen làm tăng khả năng gây đột biến gen của các tác nhân gây tổn thương ADN khác thông qua làm suy yếu việc sửa chữa cắt nucleotide, ảnh hưởng tới biểu hiện gen bàng cách tăng hoặc giảm quá trình methyl hoá DNA. Ái tính cao của arsen với các nhóm sylfhydryl làm cho các tế bào giàu keratin (tế bào biểu bì) nhạy cảm với độc tính của arsen, từ đó gây ra các biểu hiện dày sừng do arsen.
Nguyên nhân: ba nguồn chính có thể tiếp xúc với arsen là thuốc, nước uống và nghề nghiệp:
- Thuốc: thuốc chứa arsen được sử dụng trong điều trị nhiều bệnh khác nhau (trứng cá, tiêu chảy, loét dạ dày, hen, sốt rét, lupus, vảy nến, viêm da thần kinh, chàm, thấp khớp). Ở châu Á, một số loại thuốc thảo dược đã được báo cáo chứa nồng độ arsen cao.
- Nước: nước giếng khoan là nguồn tiếp xúc chủ yếu chứa arsen.
- Nghề nghiệp: nghề thợ hàn, công nhân nhà máy sản xuất thuốc trừ sâu, sản xuất thuỷ tinh và thợ mỏ, đốt gồ ép có thể gây khói chứa arsen, công nghiệp sử dụng galium arsenide trong chế tạo chíp bán dẫn.
2.3 Lâm sàng
Tổn thương cơ bản:
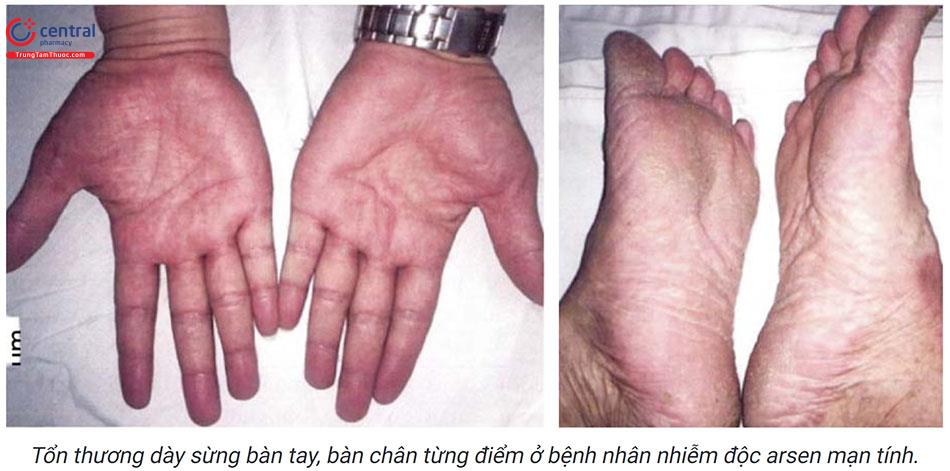
- Điểm dày sừng nhỏ ở lòng bàn tay, bàn chân, kích thước 2 – 10mm, cứng, màu vàng, thường đối xứng hai bên. Theo thời gian, tổn thương có thể phát triển rộng ra, liên kết với nhau thành các mảng sùi hoặc mảng chai chân, có thể lan lên mặt mu bàn tay, bàn chân. Biểu hiện dày sừng xuất hiện muộn, thường sau khi nhiễm ar-sen từ 10 - 30 năm.
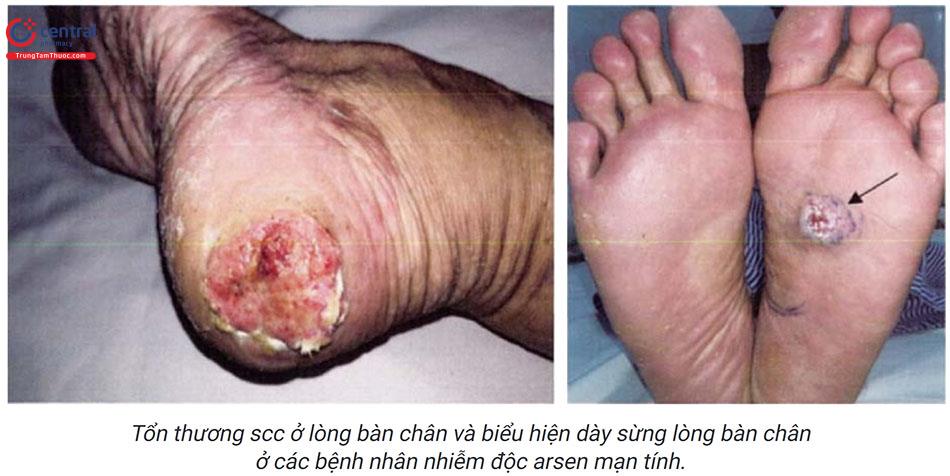
- Loét thường xuất hiện khi tổn thương bắt đầu trở nên ác tính.
Tổn thương khác:
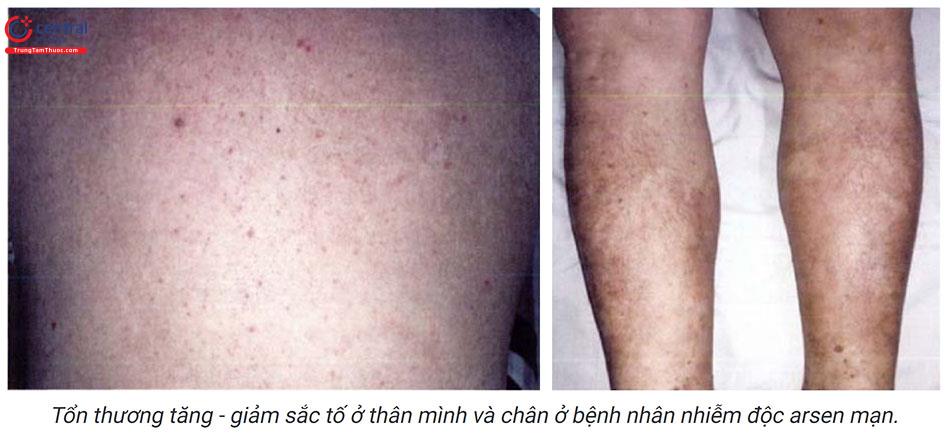
- Dát tăng, giảm sắc tố ở thân trên và chi, phân bố hai bên, đối xứng. Tăng sắc tố ở núm vú, nách, bẹn hoặc vùng tỳ đè.
- Bệnh Bowen, ung thư tế bào vảy ở vùng dày sừng hoặc vùng da không tiếp xúc ánh sáng.
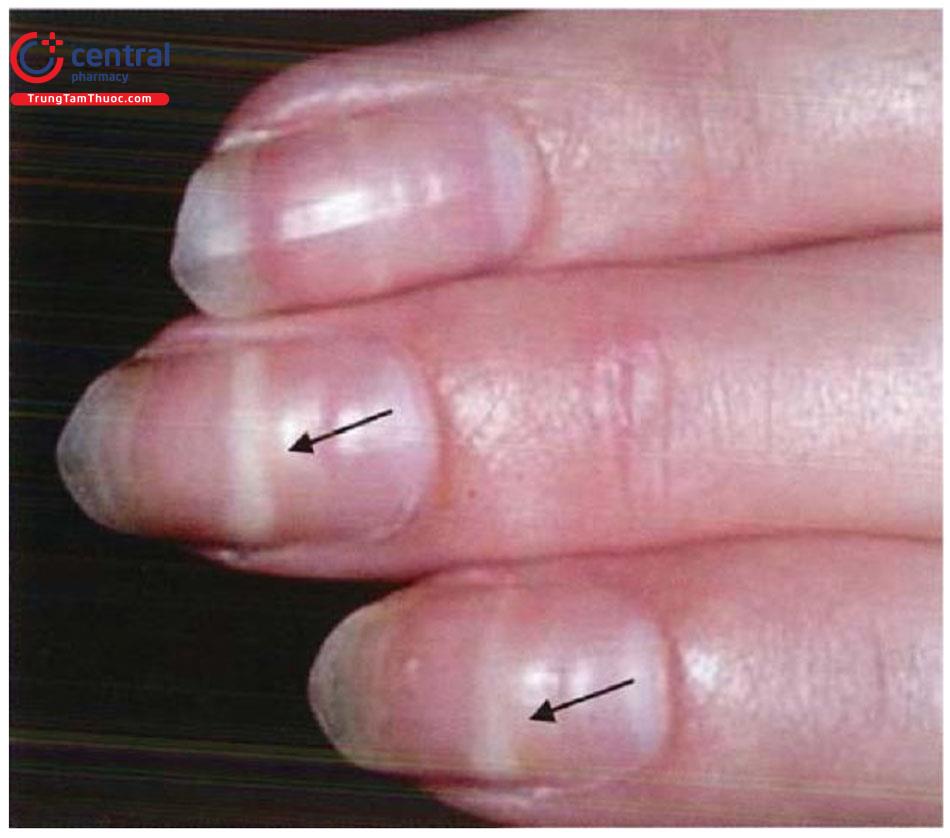
- Rụng tóc lan toả, đường Mee: dải ngang hẹp màu trắng ở móng tay.
- Nhiễm arsen mạn tính có thể lắng đọng ở tạng như gan, thận, tim, phổi, tiêu hoá, cơ, thần kinh gây nhiều bệnh lý khác nhau và hậu quả nghiêm trọng nhất là u ác tính.
2.4 Chẩn đoán phân biệt
Chai chân
Hạt cơm
Dày sừng lòng bàn tay, bàn chân
2.5 Xét nghiệm
Xét nghiệm phát hiện arsen:
- Phân tích hoá học hàm lượng arsen trong mô, tóc, móng giúp phát hiện được nồng độ arsen tích lũy trước đó 3 - 6 tháng. Mức độ có thể bình thường nếu bệnh nhân không tiếp xúc với arsen gần đây.
- Nồng độ arsen trong máu hoặc định lượng arsen trong nước tiểu 24 giờ giúp phát hiện ngộ độc arsen. Tuy nhiên, nồng độ arsen sẽ giảm xuống nhanh theo thời gian.
- Đo nồng độ arsen trong nguồn nước nếu nghi ngờ.
Xét nghiệm máu:
- Tổng phân tích tế bào máu: có thể phát hiện giảm ba đòng hồng cầu, bạch cầu, tiểu cầu.
- Phát hiện đái tháo đường liên quan tới arsen.
Xét nghiệm chức năng gan, thận.
Mô bệnh học: dày sừng, á sừng tương tự dày sừng ánh sáng, tuy nhiên sự xuất hiện của nhiều tế bào sừng có không bào và sự vắng mặt của thoái hoá sợi chun do ánh sáng là gợi ý của dày sừng do ars-en nhưng không phải là tiêu chuẩn tuyệt đối.
2.6 Điều trị
Không có điều trị đặc hiệu với nhiễm độc arsen mạn tính.
Các thuốc bôi tại chỗ:
- Dưỡng ẩm, bạt sừng: salicylic 5 - 20%, Acid Lactic 10%, ure 10 - 40%, tuỳ theo mức độ dày sừng, cổ thể băng bịt qua đêm để tăng hiệu quả, đặc biệt với tổn thương khu trú.
- Retinoid tại chỗ: cũng cho thấy hiệu quả nhưng dễ gây kích ứng.
Phẫu thuật loại bỏ hoặc phá huỷ tổn thương dày sừng (cắt bỏ, curet, phẫu thuật lạnh, bào da).
Phát hiện và điều trị sớm các tổn thương ung thư da và các khối u nội tạng.
2.7 Tiên lượng
Dày sừng do arsen không gây tử vong nhưng thường gây khó chịu do đau, chảy máu, nứt, loét và triệu chứng kéo dài.
Bệnh có thể tiến triển thành bệnh Bow-en, SCC xâm lấn, với nguy cơ di căn cao hơn sec do ánh nắng và các khối u nội tạng có thể gây tử vong. Nguy cơ này có liên quan tới liều lượng arsen tiếp xúc và thời gian tiếp xúc.
Cần hướng dẫn phát hiện sớm và tránh phơi nhiễm arsen (nguồn nước, gỗ ép, thuốc thảo dược).
3 Sừng da (Cutaneous horn)
3.1 Đại cương
Sừng da (cutaneous hom) là bệnh có tổn thương hình nón xuất hiện trên bề mặt da, được cấu tạo từ chất sừng (kera-tin). Sừng da là một bệnh khá hiếm gặp, có thể xuất hiện ở người lớn tuổi, nhất là trong độ tuổi 60 - 79. Tỷ lệ gặp ở nam và nữ là như nhau, tuy nhiên nguy cơ ác tính cao hơn ở nam.
Đa số sừng da là tổn thương lành tính, chỉ khoảng dưới 20% phát triển thành ác tính. Nguyên nhân gây bệnh cho đến nay vẫn chưa rõ ràng, nhưng nhiều tác giả cho rằng nó có liên quan đến ánh nắng mặt trời và HPV.
3.2 Lâm sàng
Sừng da chủ yếu bao gồm keratin và giống với sừng của động vật nhưng không có xương ở trung tâm. Tổn thương thường cứng và có màu nâu vàng, có thể có các nếp gấp theo chiều dọc hay chiều ngang, da xung quanh bình thường. Đáy của sừng da có thể bằng phẳng, nhô ra hoặc giống như một miệng núi lửa. Có thể có hiện tượng viêm do chấn thương tái diễn.
Sừng da thường xuất hiện đơn độc. Chúng có thể gặp ở bất cứ nơi nào trên cơ thể, nhưng phổ biến hơn trên các khu vực tiếp xúc với ánh nắng mặt trời, đặc biệt là đầu và tai, lưng, bàn tay, cẳng tay. Chúng cũng có thể xuất hiện ở các vị trí không tiếp xúc ánh nắng mặt trời như dương vật, niêm mạc môi dưới, và tiền đình mũi.
Sừng da có thể phát triển với nhiều kích thước khác nhau, từ vài millimet đến vài centimet và có thể có nhiều hình dạng khác nhau, bao gồm cả hình trụ, hình nón, thẳng, cong và nhọn.
Các sừng da có kích thước lớn hoặc khổng lồ thường xuất hiện trên nền tổn thương ác tính, chiếm tỷ lệ 30% các trường hợp.
Năm 1941, Montgomery đã phân loại sừng da dựa trên nguyên nhân, lâm sàng và các đặc điểm mô học, bao gồm:
- Sừng da phát triển từ u nang biểu bì.
- Sừng phát triển từ niêm mạc.

3.3 Điều trị
Lựa chọn hàng đầu: cắt bỏ tổn thương, làm xét nghiệm mô bệnh học. Tùy theo kết quả chẩn đoán mô bệnh học để quyết định hướng xử trí tiếp theo.
- Nếu tổn thương là lành tính, chỉ cần theo dõi chặt chẽ.
- Nếu tổn thương là tiền ung thư hoặc ác tính, cần cắt rộng tổn thương và theo dõi sau đó.
Lựa chọn thay thế: laser CO2, laser Nd:YAG...
4 Sẩn dạng Bowen (Bowenoid papulosis)
4.1 Đại cương
Sẩn dạng Bowen (bowenoid papulo-sis) là một dạng hiếm gặp của u quá sản biểu mô và là một tổn thương tiền ung thư. Virus gây u nhú ở người (HPV) có liên quan mật thiết với sẩn dạng Bowen, trong đó type HPV 16 hay gặp nhất.
Hầu hết các trường hợp sẩn dạng Bow-en đều lành tính và tự thoái triển sau vài tháng, tuy nhiên một tỷ lệ nhỏ <1% phát triển thành ung thư biểu mô tế bào vảy (SCC) vì thế cần theo dõi chặt.
4.2 Lâm sàng
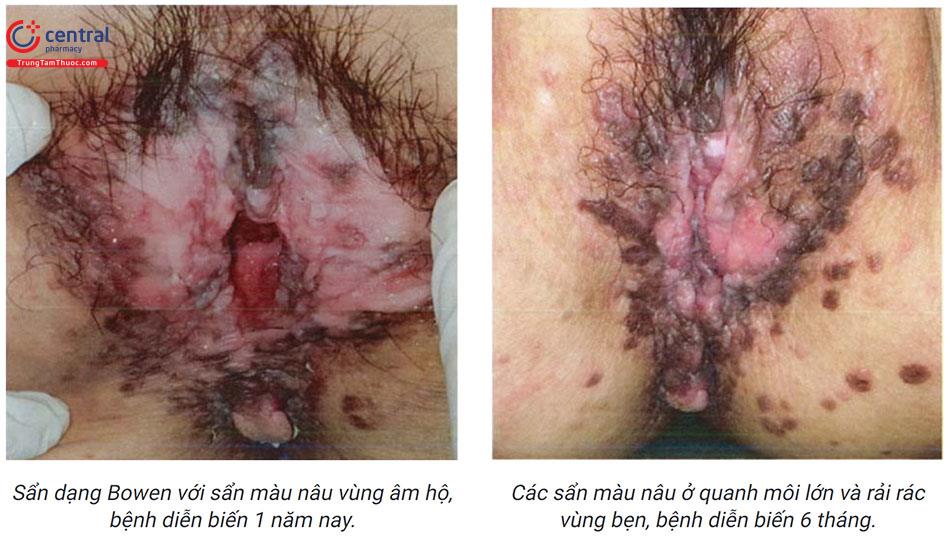
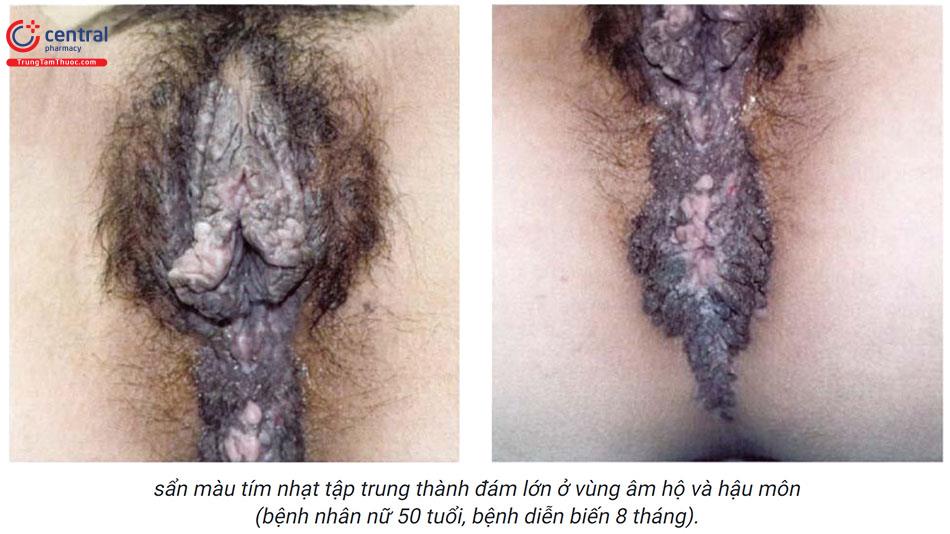
Tổn thương cơ bản là sẩn dạng mụn cơm màu nâu, xuất hiện chủ yếu ở thân dương vật hoặc môi lớn. Có thể gặp hình thái khác như mảng, dát màu nâu hoặc màu tím, hồng.
Thường không có triệu chứng cơ năng nhưng một số trường hợp tổn thương có thể bị viêm gây ngứa và đau.
Sẩn dạng Bowen có thể tự hết sau vài tháng. Phụ nữ đang mang thai, tổn thương có thể hết sau khi sinh. Trường hợp tổn thương tồn tại dai dẳng, cân điều trị vì nó có khả năng triến triển thành ung thư biểu mô tế bào vảy (SCC).
4.3 Chẩn đoán phân biệt
Bệnh Bowen
Ung thư biểu mô tế bào vảy
Sùi mào gà thể tăng sắc tố
Lichen phẳng sinh dục
4.4 Cận lâm sàng
Xét nghiệm định type HPV, sẩn dạng Bowen thường liên quan đến HPV type 16.
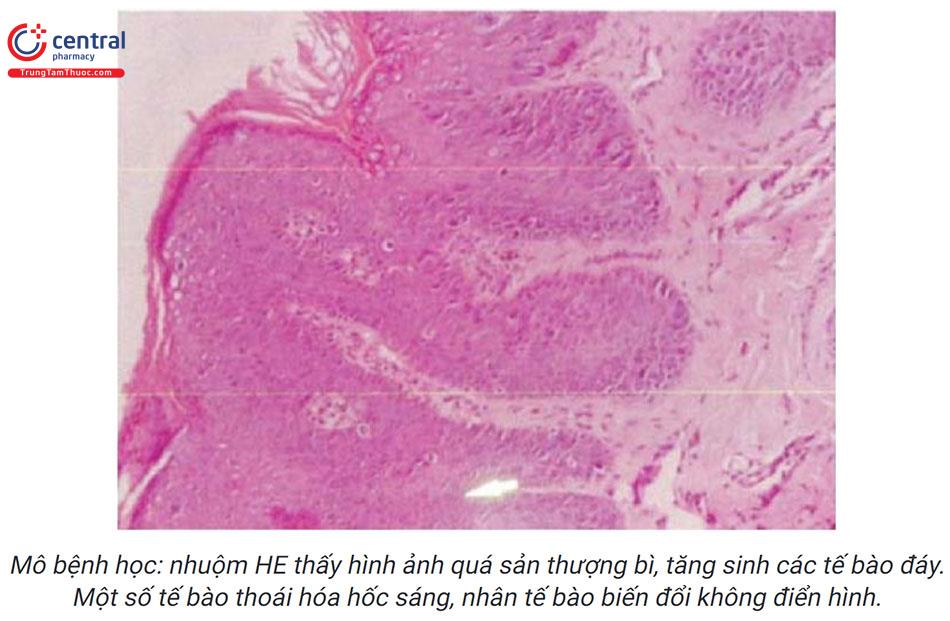
4.5 Chẩn đoán xác định
Dựa vào lâm sàng và mô bệnh học.
4.6 Điều trị
Sẩn dạng Bowen có thể tự thoái lui dù không điều trị, thời gian trung bình là 8 tháng.
Điều trị hiệu quả nhất đối với sẩn dạng Bowen là phá hủy tổn thương tại chỗ. Các phương pháp khác nhau có thể sử dụng bao gồm phẫu thuật, cắt lạnh, laser CO2 hoặc sử dụng các thuốc bôi như 5-floro-uracil, imiquimod 5%, podophyllin.
Các chất điều hòa miễn dịch cũng đã được báo cáo là có hiệu quả trong điều trị sẩn dạng Bowen và hạn chế tái phát bệnh. Trong đó, thường được sử dụng nhất là imiquimod 5% và interferon.
Một báo cáo mô tả 2 trường hợp sẩn dạng Bowen sinh dục đã được điều trị thành công với tazaroten 0,05% ngày 1 lần buổi tối, sau 2 tuần tổn thương giảm hết, 1 bệnh nhân tái phát sau đó nhưng đáp ứng với thuốc trở lại.
Một báo cáo khác cho thấy một trường hợp sẩn dạng Bowen cải thiện sau 8 tuần điều trị với Acitretin uống kết hợp và tại chỗ 5% imiquimod.
5 U quá sản sừng (Keratoacanthoma)
5.1 Đại cương
Keratoacanthoma (KA) là một tổn thương da thường xuất hiện ở vùng da tiếp xúc với ánh nắng mặt trời, trông giống hình ảnh núi lửa.
Tổn thương thường xuất hiện nhanh trong vòng vài tuần đến vài tháng.
Tổn thương bắt nguồn từ các tế bào nang lông, thực tế, nó được coi như một loại ung thư biểu mô tế bào vảy (SCC).
5.2 Lâm sàng
5.2.1 Keratoacanthoma đơn độc
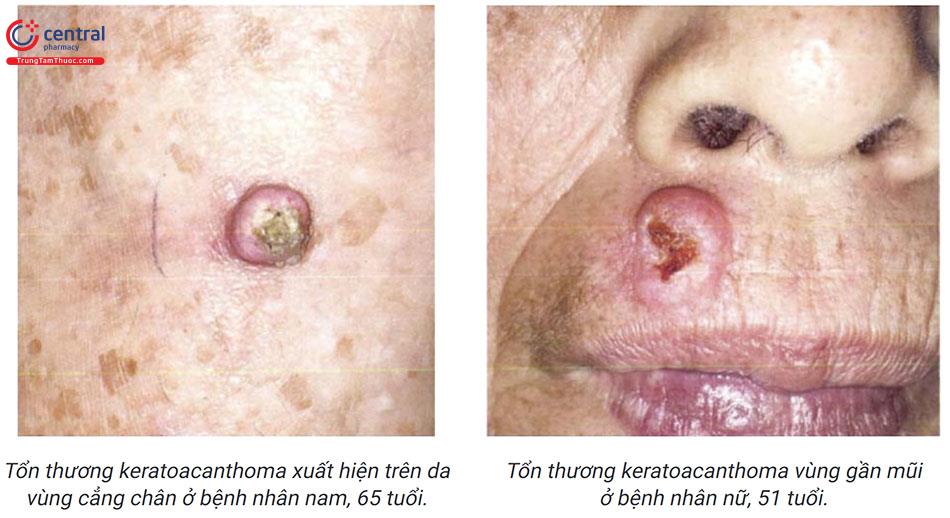
Hình thái thường gặp nhất của KA là tổn thương đơn độc.
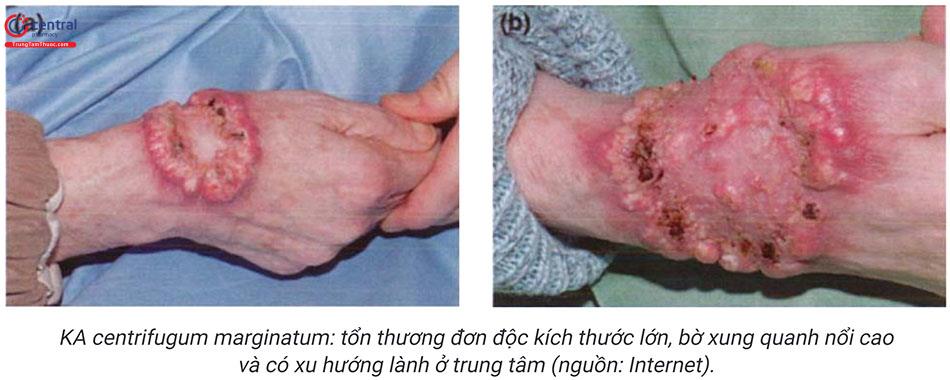
Tổn thương thường là u màu đỏ, trung tâm có tổ chức sừng giống miệng núi lửa, có đường kính khoảng 1 - 2cm và nối cao khoảng 0,5cm so với bề mặt da. Tuy nhiên, kích thước của nó có thể thay đổi, ví dụ trong trường hợp KA centrifugum marginatum, tổn thương đơn độc có bờ ngoài nổi cao, trung tâm lành và lõm xuống, đường kính có thể lên đến 20cm.
Tổn thương thường gặp ở vùng da tiếp xúc nhiều với ánh nắng, các trường hợp hiếm có thể gặp KA ở niêm mạc miệng hoặc vùng chuyển tiếp ở âm hộ.
5.2.2 Keratoacanthoma thể nhiều tổn thương
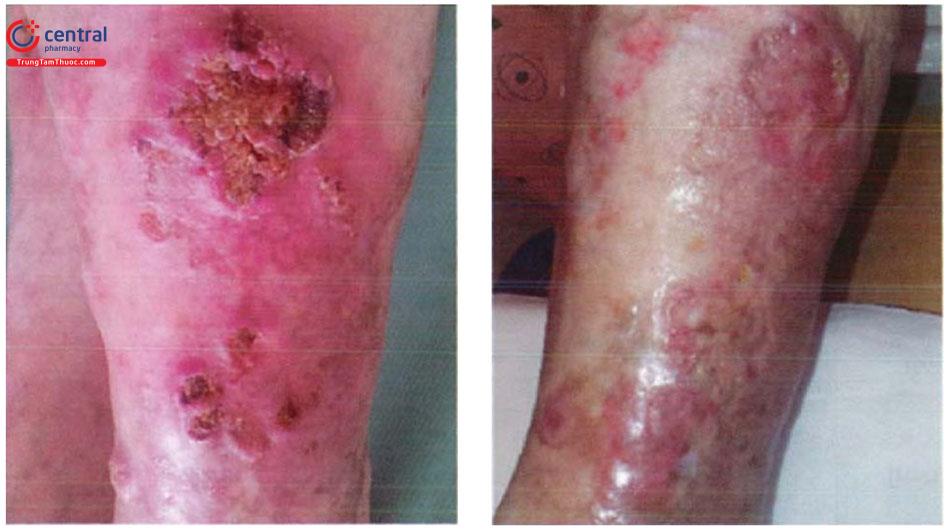
KA thể nhiều tổn thương thường hiếm gặp, tổn thương có thể rời rạc hoặc tập trung thành nhóm. Một số trường hợp có thể liên quan đến các tổn thương sẩn cục, thường gặp tại các vùng da tiếp xúc ánh nắng ở người già.
KA thể nhiều tổn thương khu trú gặp trong thể Ferguson-Smith, còn được gọi là quá sản biểu mô vảy tự giới hạn (MSHSE) đã được mô tả lần đầu ở một gia đình người Scotland. Sau này, các trường hợp di truyền tương tự cũng đã được xác nhận và mô tả trên toàn thế giới. Có một số lượng nhỏ những người mang gen không biểu hiện triệu chứng.
KA lan tỏa (GEKAs) được mô tả lần đầu tiên năm 1950 bởi Marian Grzybowski, cho đến nay chỉ có khoảng 30 trường hợp được mô tả trên y văn. Các tiêu chuẩn chẩn đoán thể bệnh này bao gồm:
| Tiêu chuẩn chính | Tiêu chuẩn phụ |
| - Khởi phát ở người lớn (thường 50 - 70 tuổi) - Tổn thương sần nhỏ, ranh giỡi rõ, sừng hóa trung tâm, số lượng vài trăm đến hàng nghìn, phân bố rải rác toàn thân - Cơ năng: ngứa nhiều và dai dẳng - Tiến triển từng đợt - Mô bệnh học khẳng định KA - Không có tiền sử gia đình | - Dấu hiệu "đeo mặt nạ" (dấu hiệu "mask of Zorro") - Tổn thương KA điển hình |
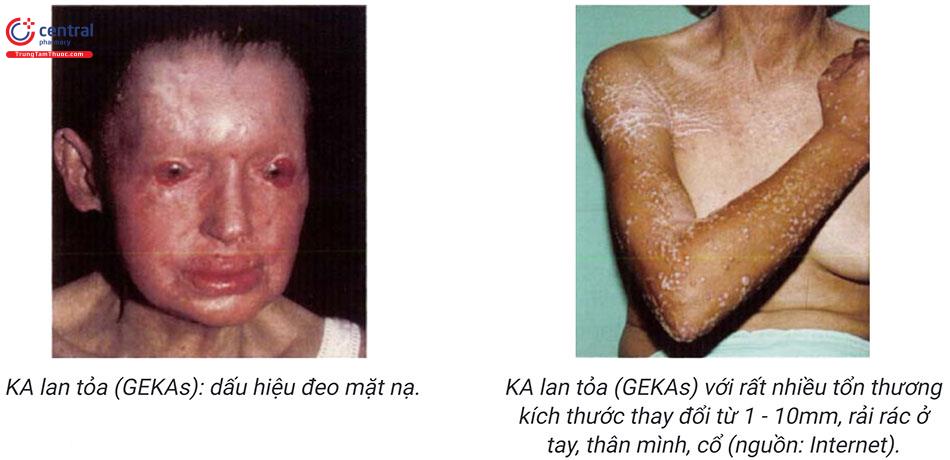
Dưới đây là bảng so sánh hai thể MSHSE và GEKA:
| Đặc điểm | Thể Ferguson - Smith (MSHSE) | Thể Grzybowski (GEKAs) |
| Tiền sử gia đình | Di truyền nội nhiễm sắc thể thường | Không |
| Khởi phát | Phân bố từ 10 - 70 tuổi | 50 - 70 tuổi |
| Tiến triển | Tổn thương phát triển chậm và tự khỏi sau vài tháng, các tổn thương mới vẫn tiếp tục xuất hiện | Khởi phát và tiến triển cấp tính |
| Tổn thương | - Số lượng tùy bệnh nhân - Các sẩn lớn (khoảng 1cm ở vùng mặt và lớn hơn ở các chi) với nút sừng hoặc loét ở trung tâm. | - Số luuwongj từ vài trăm đến hàng nghìn - Kích thước nhỏ (1 - 2mm) - Sẩn nang lông hình vòm có hoặc không có sừng hóa ở trung tâm |
| Phân bố | - Tay, chân và mặt - Ít gặp ở thân mình - Không có tổn thương ở lòng bàn tay, bàn chân | - Lan tỏa toàn thân - Các vùng tiếp xúc ánh sáng: nửa thân trên, mặt, các chi |
| Sẹo | Sẹo rỗ, thường thấy ở mặt nhiều hơn | Không rõ |
| Ngứa | Không | Ngứa nhiều |
5.3 Cận lâm sàng
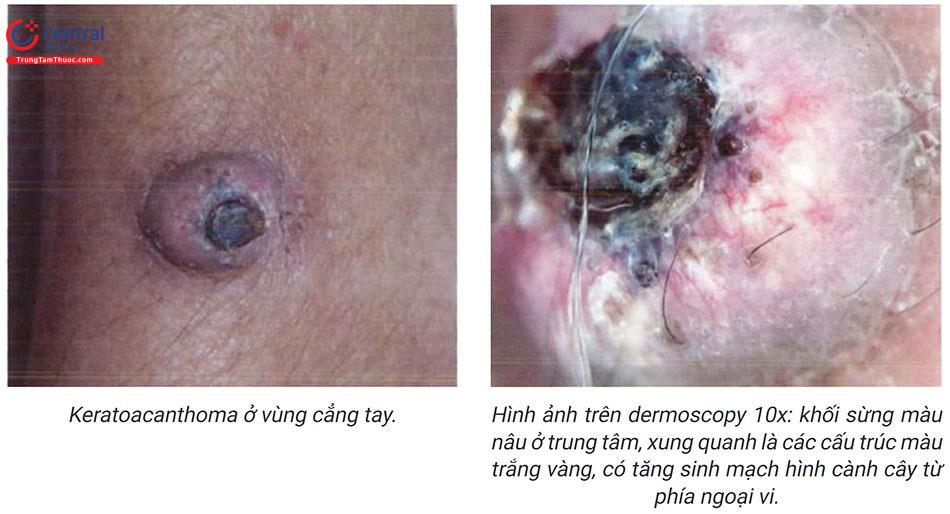
Dermoscopy: hình ảnh khối chất sừng màu trắng vàng đến vàng nâu ở trung tâm, xung quanh là vùng có cấu trúc hình nhẫn có màu trắng ở nang lông, có thể có tăng sinh mạch máu hình dải hoặc hình cành cây.
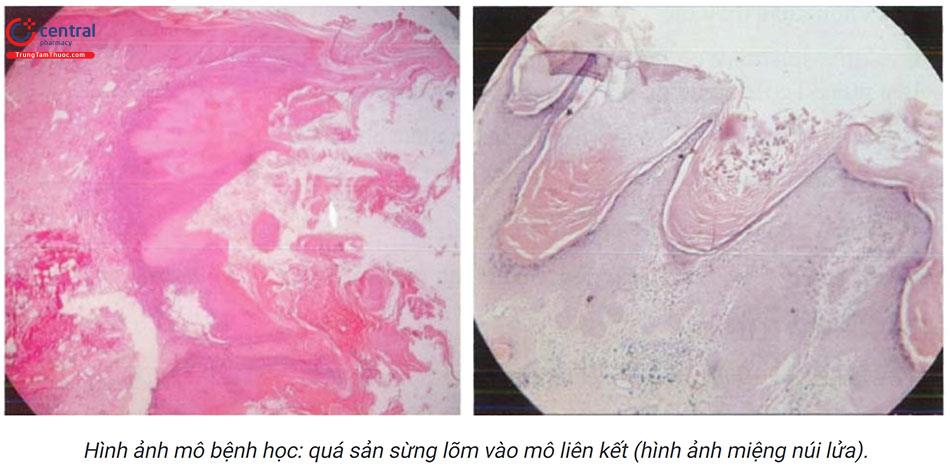
Giải phẫu bệnh: hiện tượng quá sản lớp sừng lõm xuống dưới như một miệng núi lửa ăn sâu vào mô liên kết bên dưới. Trung bì có sự xâm nhập viêm mạn tính của các tế bào lympho.
5.4 Chẩn đoán phân biệt
Dày sừng ánh sáng
Sừng da (cutaneous hom)
Sẩn cục
Sporotrichosis
U mềm lây
5.5 Điều trị
5.5.1 Keratoacanthoma thể tổn thương đơn độc
Lựa chọn đầu tiên: phẫu thuật loại bỏ tổn thương, thường chỉ định cho những tổn thương nhỏ.
Lựa chọn thứ 2: tiêm nội tổn thương một trong các loại thuốc sau: methotrex-ate, 5fluorouracil, bleomycin, interferon. Đối với các tổn thương lớn có thể tiêm nội tổn thương trước phẫu thuật, tổn thương có thể nhỏ lại đến 50 - 80%.
Một số phương pháp khác:
- Laser bề mặt
- Liệu pháp lạnh
- Liệu pháp quang động lực
- Thuốc bôi: 5-FU, imiquimod, podo-phyllin. Thuốc được dùng nhiều nhất là imiquimod, sử dụng hàng ngày hoặc cách ngày trong vòng 4-11 tuần.
- Thuốc uống: Erlotinib, retinoid
5.5.2 Keratoacanthoma thể nhiều tổn thương
Lựa chọn đầu tiên: acitretin đường toàn thân hoặc một retinoid khác.
- Sử dụng đơn độc hoặc kết hợp với phẫu thuật, các lựa chọn khác như KA đơn độc.
- Liều dùng: acitretin 0,5 - 1 mg/kg/ngày, sau đó có thể giảm liều dần.
- Việc sử dụng liều thấp acitretin 10 - 20mg/ngày hoặc sử dụng liều cao ngắn hạn từng đợt có thể làm hạn chế việc tái phát tổn thương.
Các lựa chọn khác thay thế:
- Cyclophosphamid: có hiệu quả trong trường hợp không đáp ứng với reti-noid. Sử dụng với liều pulse 1g/tháng để giảm liều tích lũy và nguy cơ độc tính lâu dài của thuốc.
- Erlotinib, corticoid, cyclosporin cũng có thể cân nhắc chỉ định.
5.5.3 Theo dõi sau điều trị
Tỷ lệ tái phát khoảng 1 - 8% sau 1 tuần đến 8 tháng.
Tránh các yếu tố kích thích, bao gồm tia cực tím, ánh nắng mặt trời, chấn thương.
6 Ung thư biểu mô tế bào đáy (Basal cell carcinoma - BCC)
6.1 Đại cương
Ung thư biểu mô tế bào đáy (basal cell carcinoma-BCC) là loại u ác tính của da, gồm những tế bào giống với những tế bào ở lớp đáy của thượng bì. Nguồn gốc thực sự của ung thư biểu mô tế bào đáy còn chưa rõ ràng. Đây là loại ung thư da hay gặp nhất, chiếm khoảng 75% các loại ung thư da. Bệnh bao gồm nhiều thể khác nhau, thường gặp ở người trên 50 tuổi.
Các yếu tố nguy cơ:
- Ánh nắng mặt trời: nhiều nghiên cứu đã xác định tia cực tím là nguyên nhân chủ yếu gây ung thư da, nhất là ung thư biểu mô tế bào đáy. Những người làm việc ngoài trời có tỉ lệ mắc ung thư biểu mô tế bào đáy rất cao. Khoảng 80% các thương tổn ung thư biểu mô tế bào đáy ở vùng da hở.
- Những biến đổi về gen:
- Gen p53: mã hóa cho protein p53, là gen được biết đến nhiều nhất có liên quan tới ung thư da. Những biến đối ở các gen do tia uv gây ra luôn được kiểm soát bởi p53. Ở những bệnh nhân có gen p53 không hoạt động, thì 50% số bệnh nhân này mắc ung thư da ở tuổi 30 và 90% mắc ung thư da ở tuổi 70. •
- Gen BRAF, gen “patched” cũng có vai trò trong cơ chế bệnh sinh của BCC.
6.2 Lâm sàng
6.2.1 Thể u
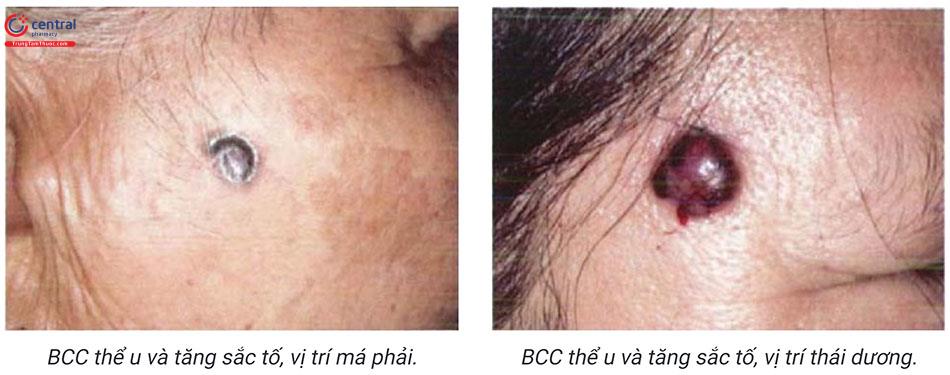
Là thể hay gặp nhất, chủ yếu gặp ở vùng đầu, cổ và nửa trên lưng. Biểu hiện lâm sàng thường bắt đầu là u kích thước từ 1 đến vài centimet, mật độ chắc, trên có giãn mạch, không ngứa, không đau, tiến triển chậm lan ra xung quanh, có thể có thâm nhiễm, loét, dễ chảy máu, đóng vảy tiết đen, bờ nổi cao với các sẩn bóng, chắc được gọi là “hạt ngọc ung thư”. Hình ảnh mô bệnh học biểu hiện lớp thượng bì bị phá hủy. Các tế bào ung thư có nhân thẫm màu, hình bầu dục sắp xếp thành khối, giới hạn rõ, được bao bọc xung quanh bởi các bó xơ.
6.2.2 Thể nông
Tổn thương dát hoặc sẩn màu hồng hoặc đỏ nâu, có vảy da, trung tâm tổn thương thường lành.
Bờ hơi nổi cao giống như sợi chỉ.
Vị trí thường gặp ở vùng thân và ít có xu hướng xâm lấn.
Trên mô bệnh học, tế bào ung thư khu trú ở thượng bì, có thể xâm lấn xuống trung bì nông.
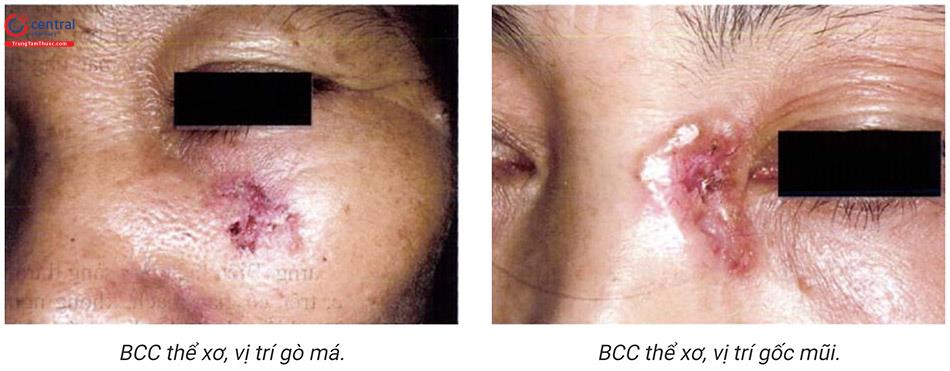
6.2.3 Thể xơ
Thường gặp ở vùng mũi hoặc trán, biểu hiện là thương tổn bằng phẳng với mặt da đôi khi thành sẹo lõm, thâm nhiễm, trên có các mạch máu giãn, giới hạn không rõ ràng với da lành.
Hình ảnh mô bệnh học cho thấy các tế bào ung thư thẫm màu xen kẽ các tế bào xơ, giới hạn không rõ, đôi khi xâm lấn sâu xuống trung bì sâu.
Thể này có tỉ lệ tái phát rất cao sau điều trị.
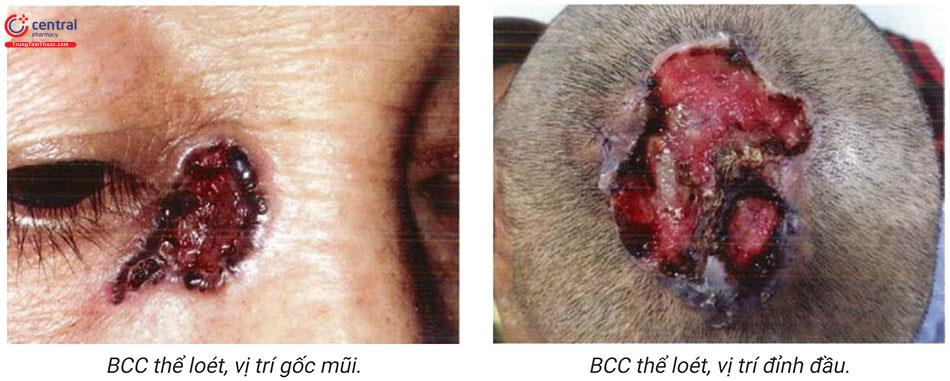
6.2.4 Thể loét
Thể loét rất thường gặp, các thể phía trên đều có thể loét hoặc tăng sắc tố và không phụ thuộc vào kích thước khối u.
Loét thường ở trung tâm tổn thương, bờ không đều, nham nhở, đáy bẩn, trên có vảy tiết màu nâu đen và dễ chảy máu.
Vết loét thường rất lâu lành, có thể tiến triển lành tạo sẹo gây co kéo đôi khi làm biến dạng các hốc tự nhiên như miệng, mũi, mắt...
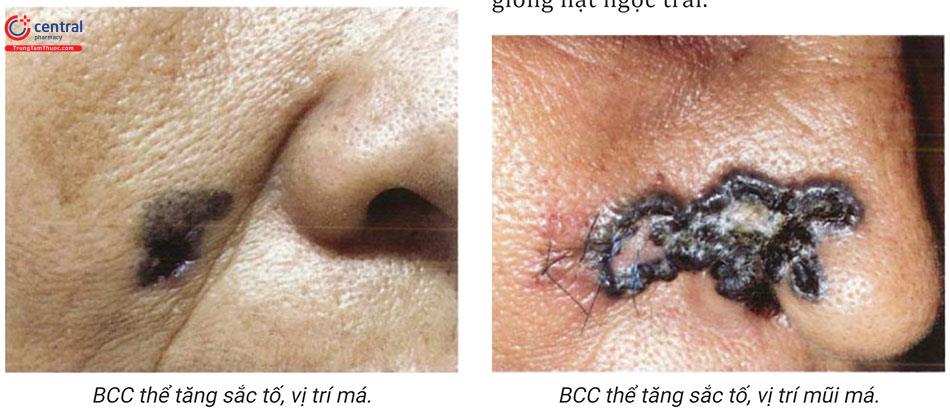
6.2.5 Thể tăng sắc tố
Thể tăng sắc tố cũng rất thường gặp. Đôi khi rất khó chẩn đoán với ung thư tế bào hắc tố.
Trong ung thư biểu mô tế bào đáy thường có màu đen đồng nhất xen kẽ với các vảy tiết màu đen hoặc các u nhỏ giống hạt ngọc trai.
6.2.6 Một số bệnh liên quan tới ung thư biểu mô tế bào đáy
Khô da sắc tố (xeroderma pigmen-tosum): bệnh do rối loạn gen lặn trên nhiễm sắc thể thường, được đặc trưng bởi tình trạng tăng nhạy cảm với ánh sáng, thay đổi sắc tố da, lão hóa da sớm và xuất hiện các khối u ác tính, các tổn thương da ác tính (ung thư biểu mô tế bào đáy, ung thư biểu mô tế bào vảy, ung thư hắc tố) thường xuất hiện sớm lúc 4 - 5 tuổi.
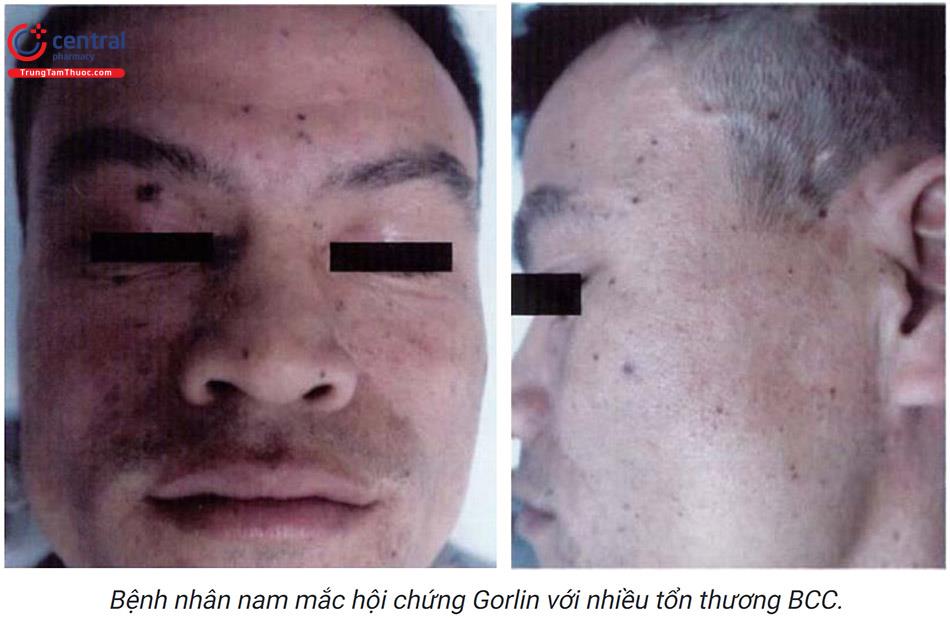
Hội chứng Gorlin (Gorlin’s syndrome hoặc nevoid bacal cell carcinoma syn-drome): là rối loạn gen trội trên nhiễm sắc thể thường, đặc trưng bởi tình trạng quá mẫn với bức xạ ion hoá. Biểu hiện lâm sàng gồm: số lượng tổn thương nhiều, thường gặp ở người trẻ tuổi, có tiền sử gia đình, kén ở xương hàm, kén tuyến bã, các khối u lành tính ở cơ quan khác (thận, buồng trứng, xương, mắt, mô thần kinh), dày sừng thành điểm ở lòng bàn tay, bàn chân.
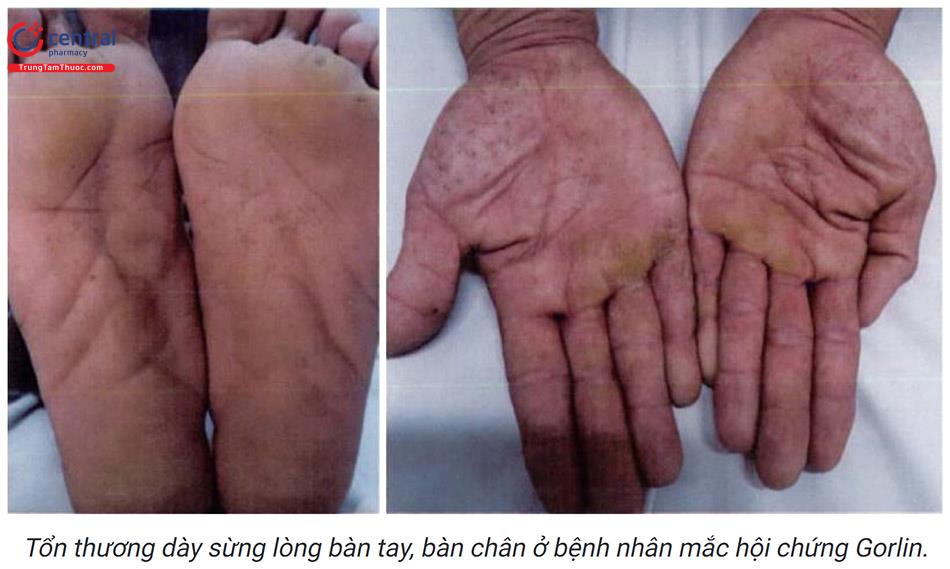
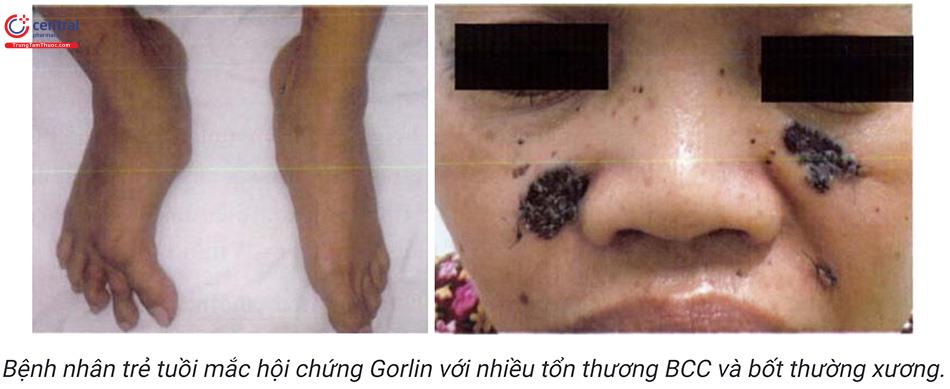
6.3 Cận lâm sàng
6.3.1 Xét nghiệm mô bệnh học
Cần được thực hiện trên tất cả các bệnh nhân nghi ngờ. Trên hình ảnh giải phân bệnh với nhuộm Hematoxyline
Eosine (HE): xác định các tế bào ác tính: bào tương bắt màu kiềm, nhân quái, nhân chia, tập trung thành đám, bao quanh bởi tổ chức xơ, phá vỡ cấu trúc của thượng bì và màng đáy; xác định mức độ biệt hóa; mức độ xâm lấn xuống trung bì; loét.
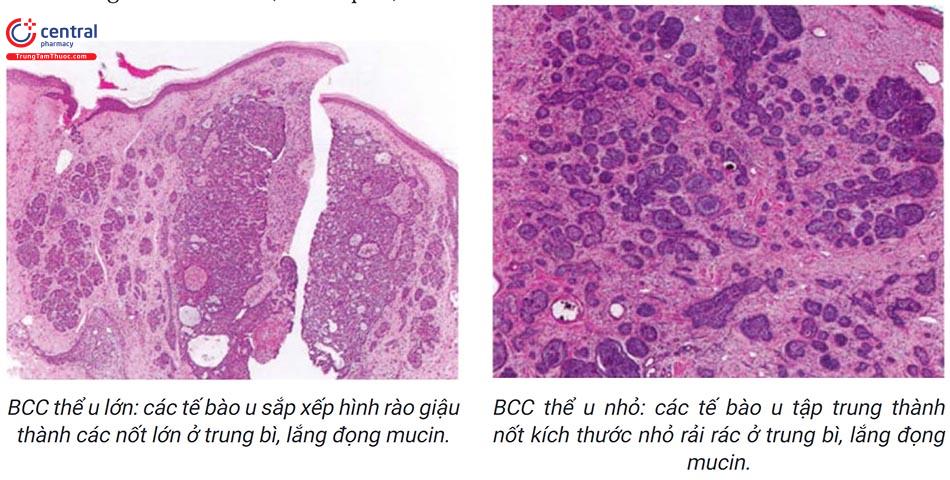
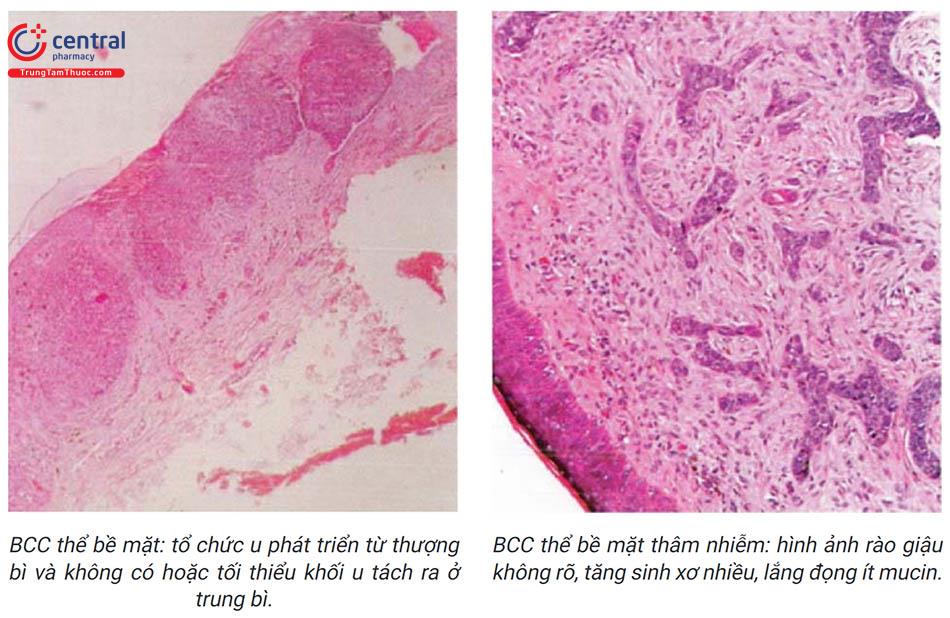
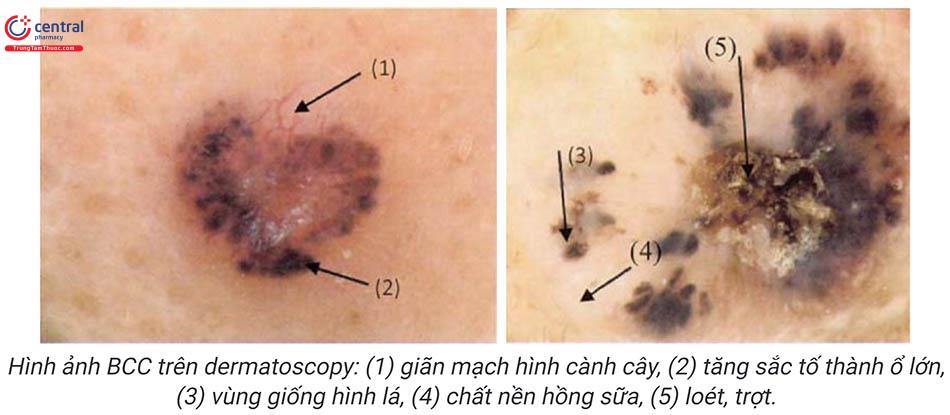
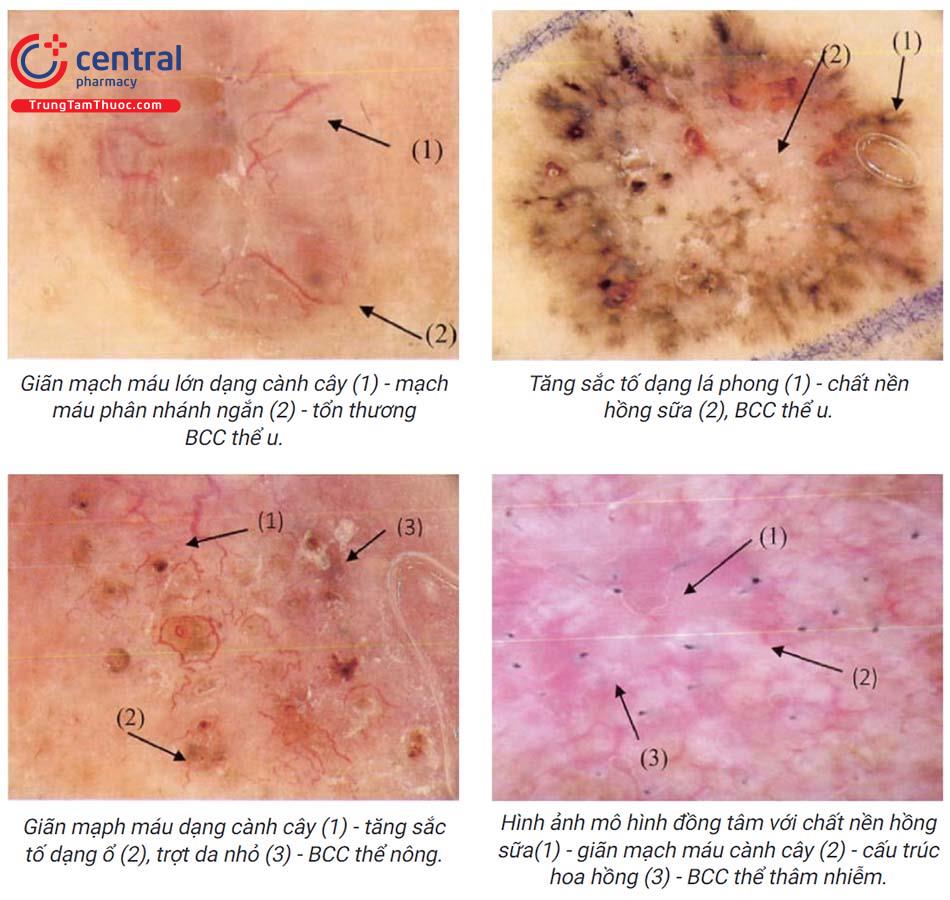
6.3.2 Dermoscopy
Có thể thấy các hình ảnh: giãn mạch hình cành cây, tăng sắc tố dạng ổ, cấu trúc giống nan hoa bánh xe, vùng giống hình lá, loét.
6.3.3 Các xét nghiệm phát hiện di căn
X-quang, cắt lớp vi tính (CT-scan), PET- CT.
6.4 Chẩn đoán xác định
Chẩn đoán xác định ung thư biểu mô tế bào đáy chủ yếu dựa vào:
Triệu chứng lâm sàng:
- Tổn thương ở người có tuổi, biểu hiện là các u chắc, bóng, trên có giãn mạch hoặc tổn thương nổi gờ cao, bóng và hình ảnh “hạt ngọc trai”.
- Vùng da hở.
- Không ngứa, không đau.
- Tiến triển chậm, xâm lấn tổ chức xung quanh có thể loét, dễ chảy máu.
Xét nghiệm mô bệnh học.
6.5 Chẩn đoán phân biệt
Lupus lao.
Ung thư tế bào gai.
Lupus đỏ kinh.
Ung thư tế bào hắc tố.
Sarcoidosis.
Paget ngoài vú.
6.6 Chẩn đoán giai đoạn bệnh
Xác định giai đoạn của ung thư theo phân loại TNM của AJCC (American Joint Commitee on cancer: T (Tumour), N (Lymph node), M (Distant metastases).
Giai đoạn I: T1N0M0.
Giai đoạn II: T bất kỳ, Nl-3, MO.
Giai đoạn III: T bất kỳ, N bất kỳ, Ml.
6.7 Tiến triển
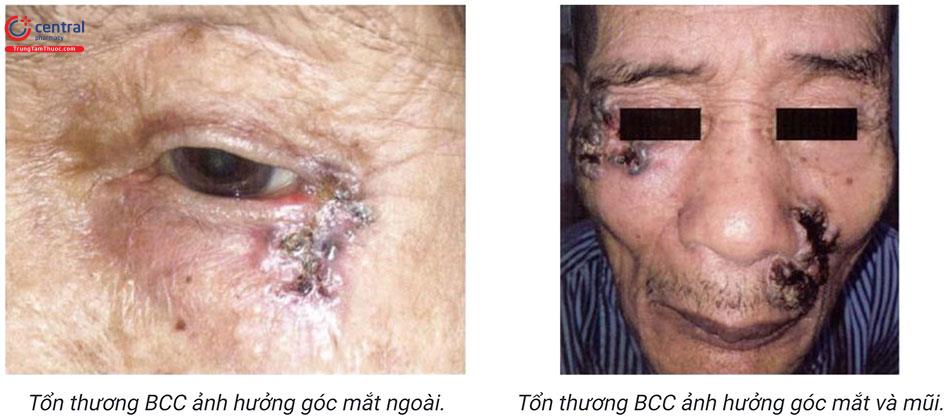
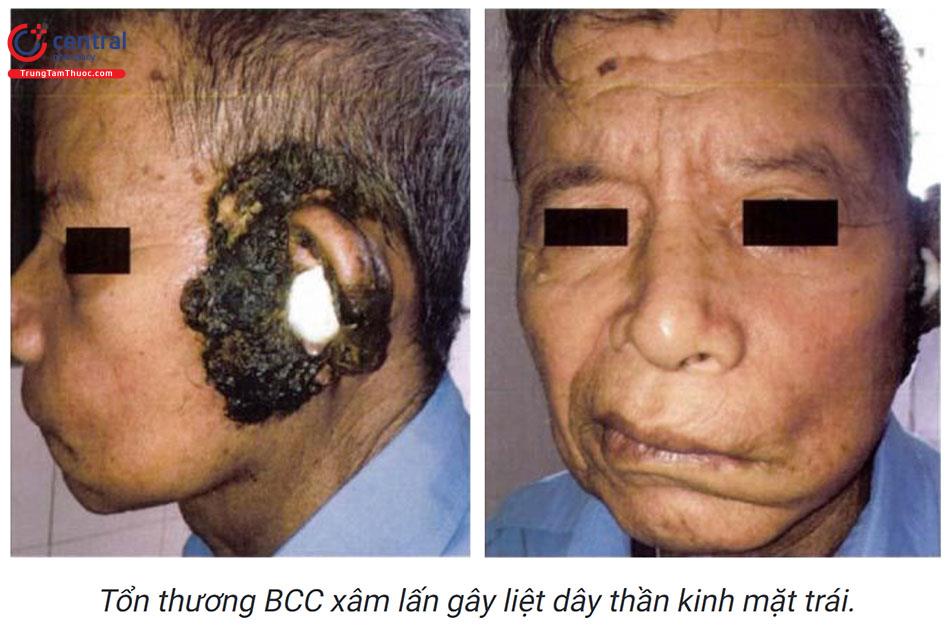
Ung thư biểu mô tế bào đáy tiến triển chậm, tổn thương có thể lan rộng, xâm lấn tổ chức xung quanh gây biến dạng và làm rối loạn chức năng của một số cơ quan bộ phận như mũi, miệng và mắt. Nếu được phát hiện sớm và điều trị kịp thời cắt bỏ rộng thương tổn, tiên lượng của bệnh rất tốt.
BCC di căn là cực kỳ hiếm gặp, với tỷ lệ thay đổi từ 0,0028% đến 0,55%.
6.8 Điều trị
6.8.1 Nguyên tắc điều trị
Loại bỏ triệt để tổ chức ung thư.
Điều trị phủ tổn khuyết, đảm bảo chức năng và thẩm mỹ sau khi cắt bỏ thương tổn u.
6.8.2 Điều trị cụ thể
Loại bỏ tổ chức ung thư: có nhiều phương pháp khác nhau để loại bỏ tổ chức ung thư tùy thuộc vào hoàn cảnh cụ thể của từng bệnh nhân và điều kiện trang thiết bị.
- Các lựa chọn ưu tiên:
- Phẫu thuật cắt bỏ rộng thương tổn: đây là biện pháp được chỉ định nhiều nhất, đường rạch da cách bờ tổn thương từ 3 - 5mm.
- Phẫu thuật Mohs: là phương pháp cho kết quả tốt, đạt tỷ lệ khỏi tới 99% cho ung thư biểu mô tế bào đáy nguyên phát và 90 - 95% ung thư biểu mô tế bào đáy tái phát. Tuy nhiên, phẫu thuật Mohs đòi hỏi các trang thiết bị hiện đại. Bệnh nhân phải trải qua nhiều lần phẫu thuật, tốn kém về thời gian và kinh phí.
- Điều trị phủ tổn khuyết:
- Phẫu thuật tạo hình phủ tổn khuyết sử dụng các vạt da tại chỗ hoặc từ xa, vá da toàn bộ hay da mỏng.
- Lành sẹo tự nhiên: trường hợp thương tổn nhỏ ở một số vị trí đặc biệt như ở mũi, góc mắt... hoặc thể trạng bệnh nhân quá yếu không thể phẫu thuật phủ tốn khuyết, sau khi cắt bỏ tổ chức ung thư, tiến hành thay băng hàng ngày để tổn khuyết lên tổ chức hạt và tự lành sẹo.
- Các lựa chọn khác: thường được chỉ định trong các trường hợp bệnh nhân có tuổi, thể trạng kém, mắc một số bệnh mạn tính không có chỉ định phẫu thuật cắt bỏ thương tổn.
- Nạo và đốt điện: nên áp dụng với trường hợp bệnh nhân không có chỉ định phẫu thuật, tổn thương nhỏ, giới hạn rõ. o Áp lạnh: sử dụng nitơ lỏng nhiệt độ - 196°c hoặc tuyết car-bon. Phương pháp này chủ yểu áp dụng cho điều trị thể nông. Có thể kết hợp phương pháp nạo bỏ tổn thương và áp lạnh đế cho kết quả tốt hơn.
- Quang động lực (PDT): phương pháp mang tính thẩm mỹ hơn và không để lại sẹo, tuy nhiên tỷ lệ tái phát cao, thường áp dụng cho trường hợp nhiều tổn thương như hội chứng Gorlin.
- Xạ trị: áp dụng cho những bệnh nhân không có chỉ định phẫu thuật hoặc có tình trạng da không thể phẫu thuật, những trường hợp tổn thương không cắt bỏ được hoàn toàn, ung thư biểu mô tế bào đáy thâm nhiễm thần kinh trên mô bệnh học.
- Laser CO2: áp dụng cho bệnh nhân không có chỉ định phẫu thuật, hoặc ung thư biểu mô tế bào đáy thể nông. Sử dụng laser phá huỷ tổ chức u tới vùng da lành cách bờ tổn thương 3 -5mm. Nguy cơ sẹo xấu (sẹo lồi, sẹo quá phát) cao kèm theo tình trạng rối loạn sắc tố.
- Thuốc bôi tại chỗ: 5-FU, imiquimod chỉ định cho thể nông, nhất là khi có nhiều tổn thương, những người già yếu không có khả năng phẫu thuật. Kết quả điều trị có thể đạt 60 - 100%.
- Tiêm nội tổn thương interferon: kết quả khỏi 70 - 100% sau thời gian điều trị 8-16 tuần.
6.9 Dự phòng
Tránh ánh sáng mặt trời: che chắn, sử dụng kem chống nắng.
Chẩn đoán và điều trị sớm các ung thư biểu mô tế bào đáy mới xuất hiện.
Khám định kỳ 1 - 2 lần/năm để phát hiện tình trạng tái phát hoặc các tổn thương ung thư mới.
7 Ung thư biểu mô tế bào vảy (Squamous cell carcinoma)
7.1 Đại cương
Ung thư biểu mô tế bào vảy ở da (squa-mous cell carcinoma - SCC) là ung thư khởi phát từ tế bào sừng của da và niêm mạc. Ung thư biểu mô tế bào vảy chiếm khoảng 20% các ung thư da và đứng hàng thứ hai sau ung thư biểu mô tế bào đáy. Khác với ung thư biểu mô tế bào đáy, ung thư biểu mô tế bào vảy nguy hiểm hơn vì nguy cơ xâm lấn, tái phát và di căn xa.
Dịch tễ học: trên thế giới, ung thư biểu mô tế bào vảy hay gặp ở những người da trắng với tỷ lệ mới mắc ở Mỹ khoảng hơn 100/100.000 dân, ở Úc là 250/100000 dân, ở Pháp là 30/100.000 dân. scc ít gặp hơn ở những người có da type IV-V theo phân loại của Fitzpatrick.
Yếu tố nguy cơ:
- Yếu tố môi trường:
- Ánh nắng mặt trời: tiếp xúc với tia tử ngoại (UV) mạn tính như tắm nắng, điều trị bằng uv hoặc tiếp xúc ánh sáng với liều tích luỹ cao là yếu tố quan trọng nhất cho sự phát triển của scc. Tia uv là tác nhân gây đột biến vì có khả năng gây tổn thương DNA dẫn tới biến đổi tế bào sừng. Ngoài ra, tia uv cũng được chứng minh là làm thay đổi đáp ứng miễn dịch của da khiến da dễ phát sinh khối u.
- Bức xạ ion hoá: tổng liều không quan trọng bằng liều cách quãng lớn, liều cách quãng > 12 - 15G đủ để hình thành khối u.
- Chất hoá học: nguy cơ cao nhất là thuốc trừ sâu, Nhựa đường, hy-drocarbon thơm nhiều vòng. Các nguyên nhân trên thường gây tổn thương khu trú ở tay do tiếp xúc trực tiếp. Arsen được biết đến từ lâu là nguyên nhân gây scc, với biểu hiện nhiễm độc arsen mạn tính như dày sừng lòng bàn tay, bàn chân và nhiều tổn thương scc, bệnh Bowen.
- Nhiễm HPV: gồm hai nhóm chính là các virus nguy cơ thấp như type 1, 6, 11... và type nguy cơ cao gây ung thư như type 8, 16, 18, 38. Các type 16, 18, 31, 33, 35 và 58 liên quan đến ung thư cổ tử cung còn các type 36, 38, và 8 liên quan đến scc ở da.
- Suy giảm miễn dịch: ngày càng được công nhận là yếu tố nguy cơ cho phát sinh ung thư, điều này đúng với cả trường hợp suy giảm miễn dịch do điều trị (ghép tạng, sử dụng các thuốc ức chế miễn dịch) hoặc không do điều trị (HIV/AIDS).
- Hội chứng di truyền làm tăng nguy cơ SCC: khô da sắc tố là bệnh di truyền gen lặn trên nhiễm sắc thể thường, được biết đến nhiều nhất với nguy cơ xuất hiện tổn thương ung thư BCC, scc sớm (trung bình 8 tuổi), nguy cơ mắc ung thư này tăng gấp 4800 lần người bình thường ở độ tuổi > 20. Ngoài ra các bệnh lý di truyền khác như bạch biến, loạn sản thượng bì dạng hạt cơm, ly thượng bì bọng nước thể loạn dưỡng cũng làm tăng nguy cơ.
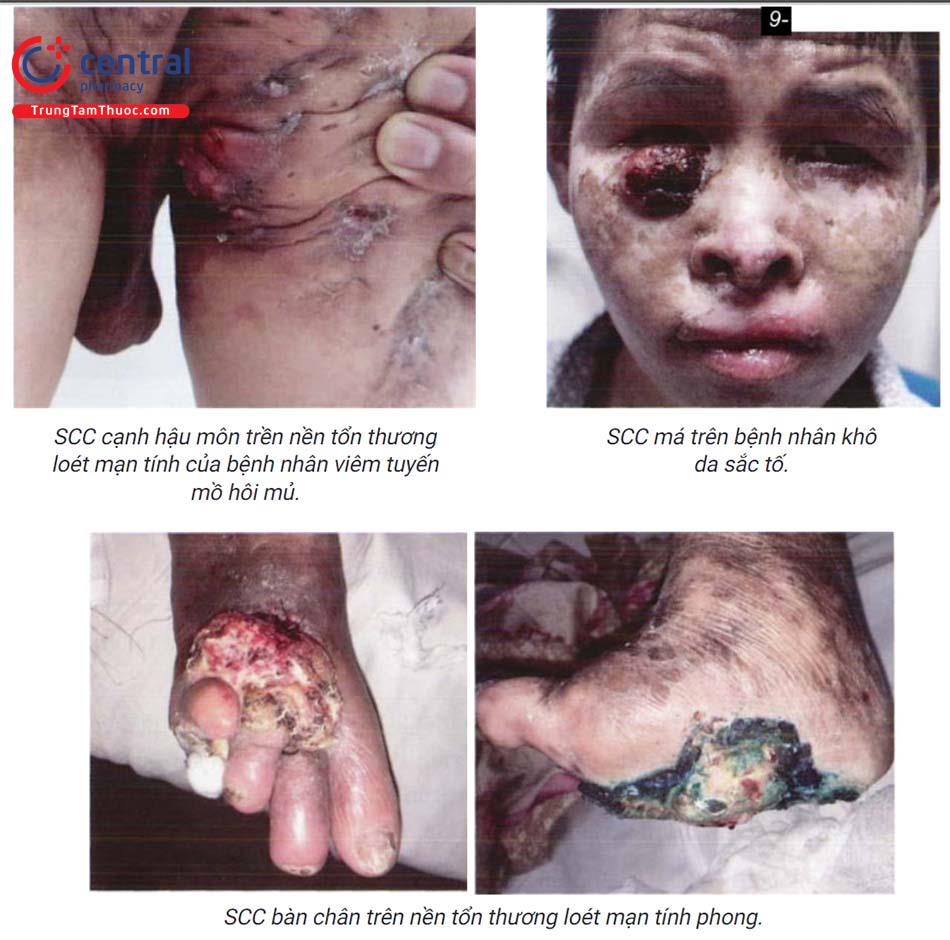
- Yếu tố nguy cơ khác: loét mạn tính, sẹo bỏng, sử dụng thuốc lá (đặc biệt scc ở môi).
Điều trị bệnh chủ yếu hiện nay vẫn là phẫu thuật cắt bỏ khối u, phẫu thuật nạo vét hạch được chỉ định trong một số trường hợp di căn hạch. Điều trị tia xạ và hoá chất có tác dụng hỗ trợ cho phẫu thuật và dự phòng tái phát, di căn.
7.2 Lâm sàng và mô bệnh học
Bệnh thường biểu hiện rất đa dạng với hai dạng chính:
Ung thư biểu mô tế bào vảy tại chỗ (in-situ): bao gồm dày sừng ánh sáng, bệnh Bowen, bạch sản miệng, hồng sản Queyrat. Tổn thương ung thư chỉ giới hạn ở lớp thượng bì, thường điều trị khỏi, ít khi di căn hạch và nội tạng (xem thêm bài dày sừng ánh sáng, bệnh Bowen).
Ung thư biểu mô tế bào vảy xâm nhập (invasive): ung thư xâm nhập qua màng đáy. Tỷ lệ di căn phụ thuộc vào độ biệt hoá tế bào, mức độ xâm lấn mô học, xâm lấn thần kinh, mạch máu.
7.2.1 Ung thư biểu mô tế bào vảy tại chỗ
Tham khảo bài dày sừng ánh sáng, bệnh Bowen.
7.2.2 Ung thư biểu mô tế bào vảy xâm lấn
7.2.2.1 Ung thư thế bào vảy xâm lấn thể thông thường
Bao gồm phần lớn trường hợp scc, thường phát triển trên nền tổn thương tiền ung thư như dày sừng ánh sáng, bạch sản, bệnh Bowen. Tổn thương do ánh sáng thường xuất hiện ở vùng da hở: đầu, mặt, cổ, mu tay và cẳng chân; tổn thương là các sẩn, nốt, có thể ở dạng mảng, u nhú, bề mặt bong vảy ở các mức độ khác nhau, một số tổn thương dày sừng nhanh, một số tổn thương sùi, trợt, loét và đóng vảy tiết.
Có thể phát triển trên một tổn thương mạn tính như loét, sẹo, tổn thương do tia xạ. Trên nền tổn thương ban đầu xuất hiện khối sùi, tăng kích thước, vượt quá bờ tổn thương, thâm nhiễm, loét bờ không đều, chảy máu, mùi hôi thối. Trường hợp không điều trị kịp thời, khối ung thư phát triển nhanh, xâm lấn xuống tổ chức xung quanh và di căn xa (hạch và nội tạng).
Khám hạch có thể phát hiện hạch bạch huyết khu vực to.
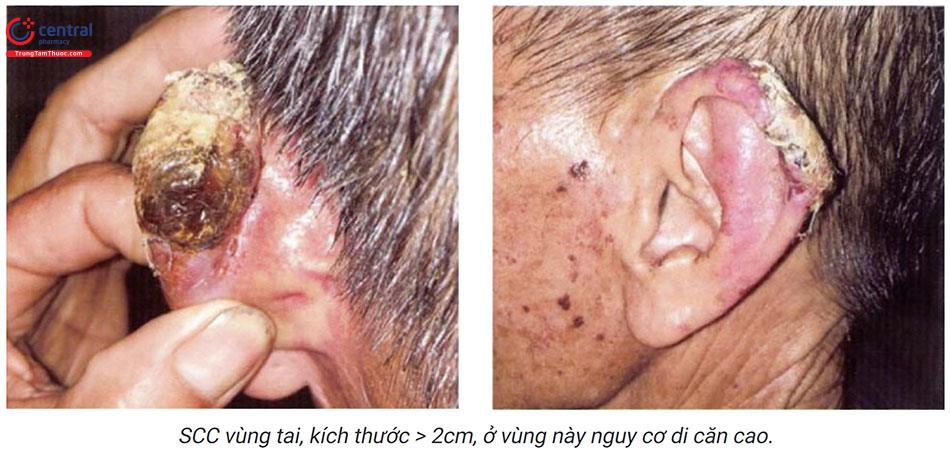
Tiến triển tự nhiên của khối u thay đổi khác nhau. Tổn thương do ánh sáng thường ở giai đoạn sớm, tổn thương scc trên nền dày sừng ánh sáng (AK) tỷ lệ di căn thấp (0,5%), những tổn thương có kích thước > 2cm và ở các vị trí như môi, tai, sinh dục (âm hộ, dương vật) có nguy cơ di căn cao hơn.
Cơ năng: thường không có triệu chứng, những trường hợp xuất hiện dị cảm, tê và đau có thể là dấu hiệu của khối u xâm lấn thần kinh.
Một số trường hợp đặc biệt:
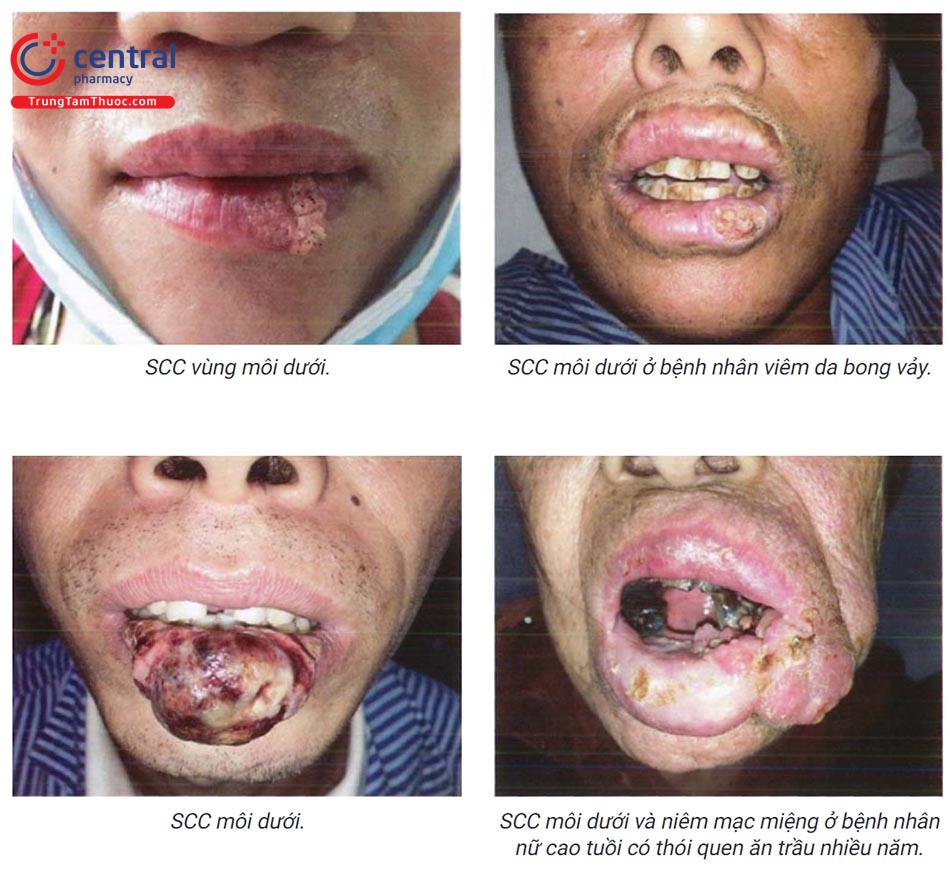
- SCC quanh miệng: thường gặp ở môi dưới với biểu hiện sẩn, sùi đỏ, cứng, thâm nhiễm, trợt. Tổn thương thường phát triển trên một tình trạng viêm môi ánh sáng trước đó, bạch sản ở người hút thuốc lá, thuốc lào, ăn trầu.
- SCC quanh móng: thương tổn dễ nhầm với hạt cơm, thường chỉ chẩn đoán ra khi có sinh thiết và thường liên quan tới HPV16.
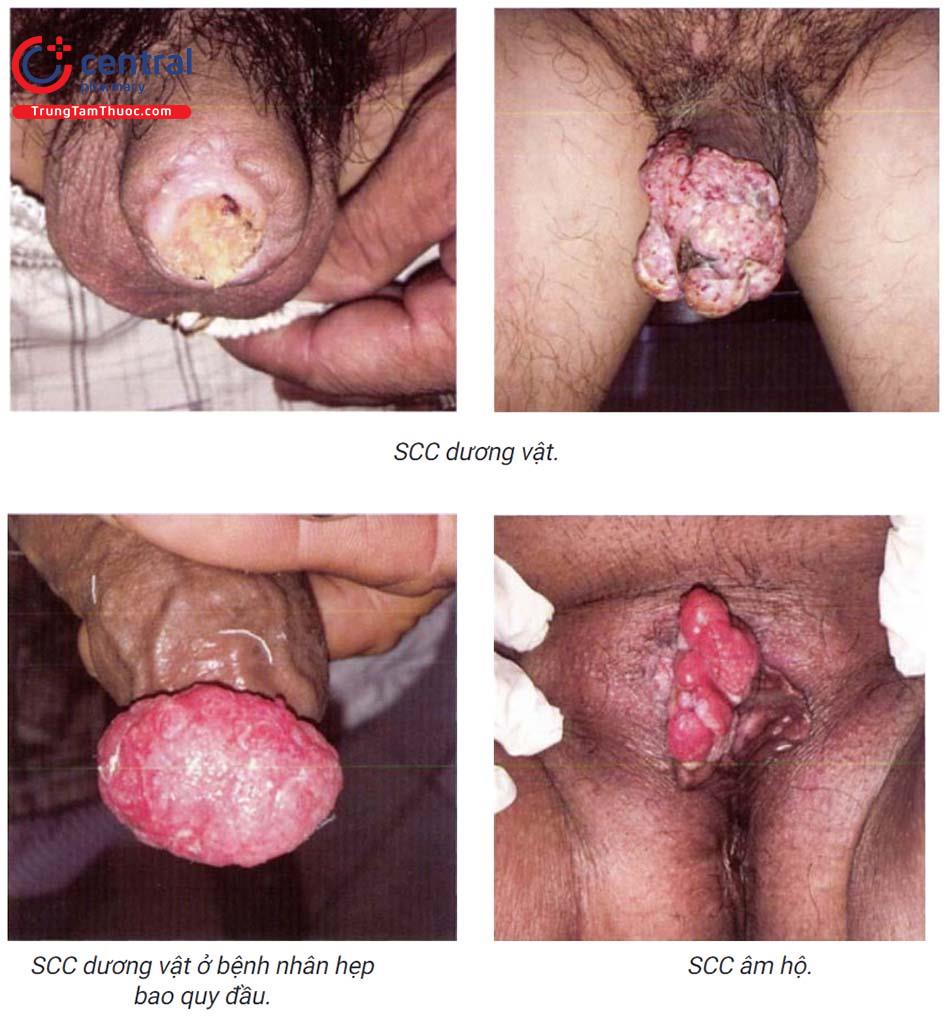
- SCC sinh dục, hậu môn: SCC âm hộ thường xuất phát ở môi lớn, thường trên một nền lichen xơ teo, ban đầu là một tổn thương dạng nốt, dạng hạt cơm nhỏ hoặc mảng đỏ trợt, tổn thương không triệu chứng nhưng thường liên quan tới ngứa và chảy máu. scc cổ tử cung chủ yếu liên quan tới nhiễm HPV, đặc biệt là HPV type 16. scc vùng bìu xuất phát từ một tổn thương sẩn nhỏ sùi ngứa, sau đó tổn thương tăng kích thước, scc dương vật thường xuất hiện ở bệnh nhân hẹp bao quy đầu, những bệnh nhân vệ sinh vùng sinh dục kém (10%), trên nền tổn thương hồng sản Quey-rat, sùi mào gà hay lichen xơ teo.
Mô bệnh học: tăng sinh ác tính các tế bào sừng thành các trụ kéo dài từ thượng bì hoặc các đảo xâm nhập sâu vào trung bì. Các tế bào ác tính nhân đa hình thái, bắt màu kiềm, tỷ lệ nhân/bào tương tăng, có thể rõ hoặc không rõ các cầu sừng.
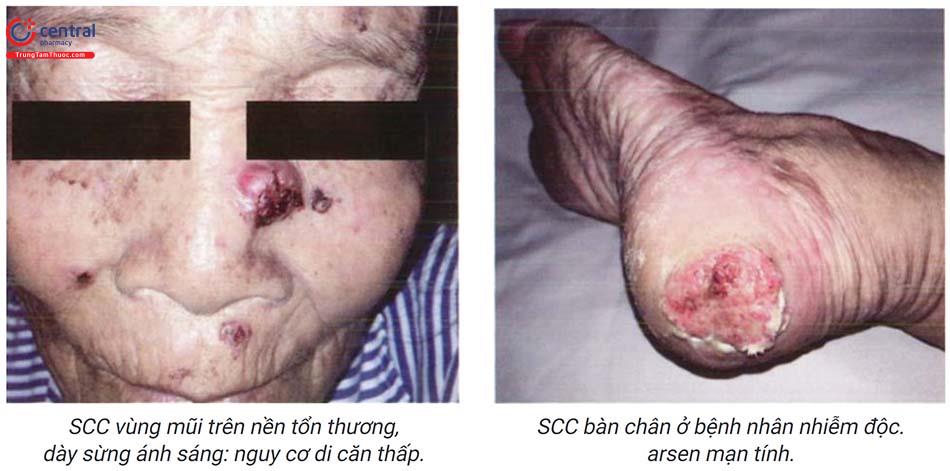
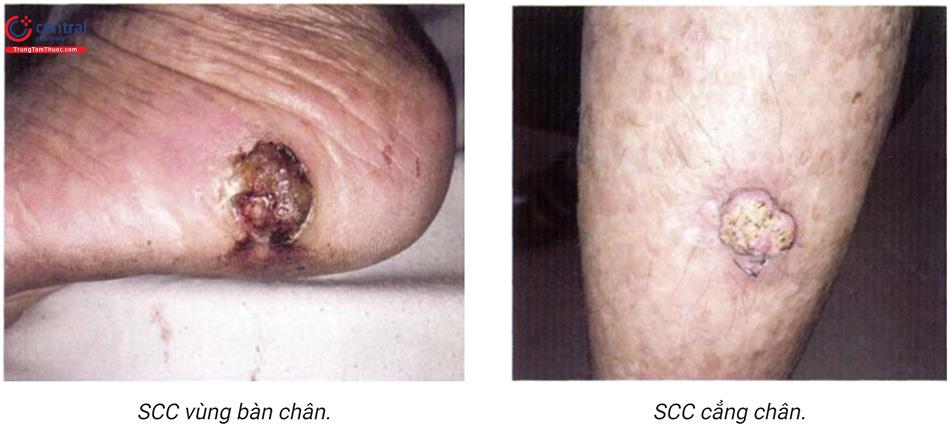
7.2.2.2 Biến thể khác của SCC với nguy cơ di căn thắp
Ung thư biểu mô tế bào vảy thê sùi (ver-rucous carcinomas):
- Là biến thể hiếm gặp, có xu hướng xảy ra ở người trung niên và cao tuổi. Nó được coi là khối u ác tính mức độ thấp với 3 loại chính: carcinoma cu-niculatum (cẳng chân và bàn chân), oral papillomatosis (niêm mạc miệng hầu) và u Buschke-Lowenstein (sinh dục và quanh hậu môn). Bệnh thường liên quan tới HPV.
- Tổn thương trên lâm sàng là những khối sùi lớn, đôi khi là khổng lồ với bề mặt có nhiều nhú hoặc như hạt cơm, tổn thương tiến triển và xâm lấn chậm, dần dần khối u xâm nhập vào các mô bên dưới và phá huỷ mô dưới da, cân và xương. Việc phân biệt giữa u Buschke-Lowenstein và sùi mào gà khổng lồ đôi khi rất khó khăn.
- U cũng có thể phát triển từ tổn thương sẹo hay mỏm cụt chi và có thể dẫn tới đường rò tuỷ xương.
- Bệnh hay tái phát nhưng thường không di căn trừ trường hợp bị biến đổi do chiếu xạ.
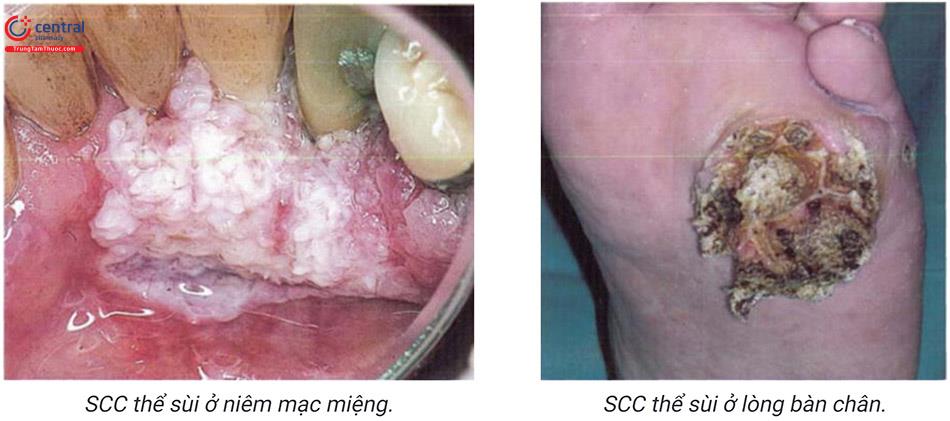
Ung thư biếu mô tế bào vảy - đáy (ba-sosquamous carcinoma)
- Là một dạng hiếm gặp với biểu hiện trên mô bệnh học của cả ung thư biểu mô tế bào đáy và ung thư biểu mô tế bào vảy mặc dù trên lâm sàng có thể biểu hiện những đặc trưng của BCC, đôi khi triệu chứng không đặc hiệu và vì vậy làm chậm chẩn đoán. Tổn thương thường phổ biến ở đầu và cổ nhưng có thể xuất hiện ở bất cứ vị trí nào bao gồm cả vùng sinh dục. Tổn thương có xu hướng xâm lấn và di căn cao hơn BCC. Hiện tại không có triệu chứng đặc hiệu để phân biệt ung thư biểu mô tế bào vảy đáy với BCC, chẩn đoán xác định cần phải dựa vào mô bệnh học. Hiện nay, nhiều tác giả ủng hộ việc coi ung thư biểu mô tế bào vảy - đáy là một biến thể của scc.
- Mô bệnh học: ngoài các khối u của các tế bào dạng đáy, các tế bào vảy với bào tương bắt màu hồng, sự sừng hoá và một vùng chuyển tiếp với các tế bào trung gian.
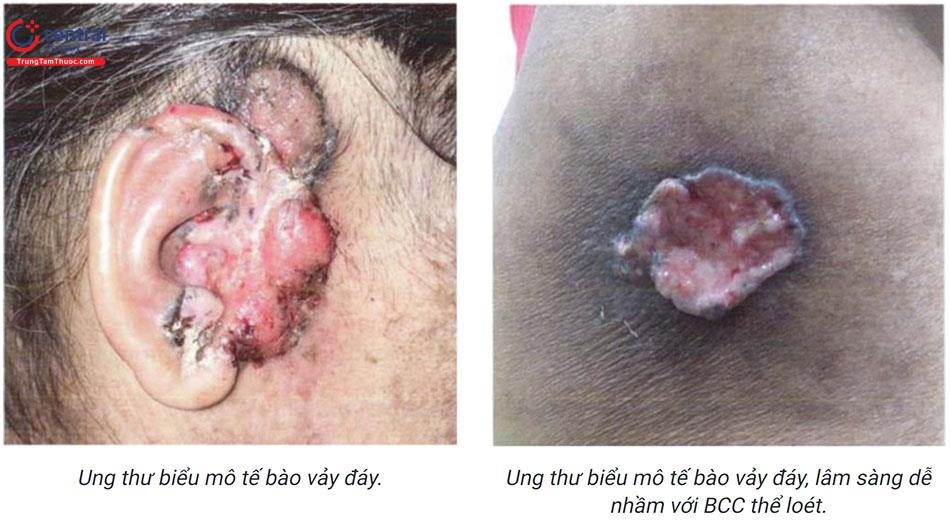
Ung thư dạng biểu bì hình thoi (fusi-form or sarcomatoid epidermoid carci-noma):
- Là một dạng hiếm gặp được quan sát thấy ở những vùng tổn thương do ánh sáng hoặc do tia xạ, thường gặp ở người lớn tuổi. Tổn thương là mảng loét ở trung tâm, sùi, chảy dịch hôi, dễ chảy máu ở vùng đầu mặt cổ. Điều quan trọng là phân biệt được tổn thương trên vùng bị nhiễm xạ vì tổn thương này có nguy cơ di căn cao hơn.
- Mô bệnh học biểu hiện sự xâm lấn dày đặc của các tế bào thượng bì không điển hình, hình thoi đứng riêng lẻ có thể có hoặc không liên kết với thượng bì. Các tế bào khổng lồ đa hình thái, nhân chia, thâm nhiễm sâu có thể tới xương, xâm lấn thần kinh.
7.2.2.3 Biến thể khác của scc với nguy cơ di căn cao hơn
Ung thư biểu mô tế bào vảy xâm nhập tủy gai (acanthoỉytỉc epidermoid carci-noma):
- Gặp 2 - 4% SCC, đặc biệt vùng đầu và cổ, thường xuất hiện trên nền tổn thương dày sừng ánh sáng ly gai. Tỷ lệ di căn tương đối cao, một nghiên cứu đã chỉ ra 19% trường hợp trên 49 bệnh nhân có di căn và tử vong, có tương quan với tổn thương kích thước > 1,5cm.
- Trên mô bệnh học còn được gọi là ung thư biểu mô tế bào vảy giả tuyến hay adenoid với hình ảnh của ung thư biểu mô tế bào vảy điển hình kèm theo hình ảnh ly gai, dị sừng xâm lấn giống tuyến vào trung bì.
Ung thư biểu mô tế bào vảy thê tuyến (adenosquamous carcinoma):
- Hiếm gặp, tổn thương thường gặp ở vùng đầu-mặt-cổ với biểu hiện là các mảng sừng cứng, nổi cao trên mặt da, đường kính 1 - 6 em. Bệnh thường ở người lớn tuổi. Đây là một thể xâm lấn với nguy cơ tái phát và di căn cao. Một nghiên cứu tổng kết 13 bệnh nhân ung thư biểu mô tế bào vảy thể tuyến, tổn thương khối u từ 0,5 - 5cm, với tỷ lệ tử vong (trung bình 32 tháng) 5/13 bệnh nhân và tái phát 6/13 bệnh nhân.
- Mô bệnh học: khối u sắp xếp theo theo dạng tuyến khu trú hay lan toả xâm nhập sâu vào trung bì. Hình ảnh các tế bào tuyến từ hình đa diện tới tế bào trụ thấp. Phân biệt với ung thư biểu mô tế bào vảy ly gai vì chỉ có hình ảnh giả tuyến chứ không có tuyến thực sự.
Ung thư biểu mô tế bào vảy xâm lấn tạo xơ (desmoplastic squamous cell): Là một dạng được phân biệt trên mô bệnh học bởi các tiêu chuẩn sau: các tế bào khối u bao gồm biệt hoá vảy và hình thành các chuỗi phân nhánh xơ phong phú (tỷ lệ ít nhất 30% khối u). Nghiên cứu của Breuninger và cộng sự trên 594 trường hợp SCC, trong đó 44 trường hợp đủ tiêu chuẩn mô bệnh học của ung thư biểu mô tế bào vảy tạo xơ, thời gian theo dõi trung bình 5,3 năm, tỷ lệ di căn của nhóm này cao gấp 6 lần và tỷ lệ tái phát tại chỗ gấp 10 làn 550 trường hợp còn lại.
7.2.3 Keratoacanthoma (tham khảo chi tiết tại bài keratoacanthoma)
7.3 Tiên lượng
Tiên lượng của SCC tốt cho hầu hết các trường hợp. Nguy cơ di căn là 2,3% trong vòng 5 năm và 5,2% sau 5 năm với sec do ánh sáng. Tần số tái phát hoặc di căn và tỷ lệ sống liên quan tới SCC thường do khối u được điều trị sai hoặc do khối u xâm lấn.
Hội đồng nghiên cứu y khoa và sức khoẻ quốc gia Úc (NHMRC) đưa ra 7 yếu tố nguy cơ :
- Phân độ TNM: đối với phân độ T, đường kính bên ngoài xác định giai đoạn từ T1-T3 và không phân biệt mức độ xâm lấn da và trong khi T4 được xác định là khi xâm lấn sâu tới cơ và xương.
- Sự xuất hiện của di căn hạch vùng hoặc thần kinh.
- Tái phát tại chỗ hoặc điều trị không triệt để: hai yếu tố này đi cùng nhau vì phụ thuộc nhau.
- Phân độ mô bệnh học: biệt hoá tốt, biệt hoá vừa, biệt hoá kém, không biệt hoá.
- Vị trí tiên phát của khối u: vị trí nguy cơ cao bao gồm đầu, tai, môi.
- SCC không do ánh sáng ở bệnh nhân miễn dịch bình thường (SCC trên đường rò tuỷ xương mạn tính, sẹo bỏng, tia xạ).
- SCC trên người suy giảm miễn dịch.
Hội da liễu Anh 2007 (BAD) đề xuất thêm 2 tiêu chuẩn tiên lượng kém khi đo lường trên kính hiển vi: khối u dày hơn 4 mm và xâm lấn hạ bì mức độ V (tham khảo phân độ ung thư hắc tố của Clark).
Mạng lưới ung quốc gia của Mỹ 2007 (NCCN) phân biệt nguy cơ lâm sàng và mô bệnh học như bảng dưới đây. Tuy nhiên phân độ của NCCN về vị trí nguy cơ (H, I, B) không được chấp nhận vì các chuyên gia xác định vùng nguy cơ này chỉ dựa trên tỷ lệ tái phát của hàng loạt trường hợp điều trị BCC.
| Nguy cơ thấp | Nguy cơ cao | |
| Lâm sàng | ||
| Vị trí/kích thước | Vùng B < 20mm Vùng I < 10mm Vùng H < 6mm | Vùng B > 20mm |
| Bờ | Giới hạn rõ | Giới hạn không rõ |
| Tiên phát và tái phát | U tiên phát | Tái phát |
| Suy giảm miễn địch | Không | Có |
| SCC trên tổn thương tia xạ hoặc tổn thương viêm | Không | Có |
| SCC tiến triển nhanh | Không | Có |
| Triệu chứng của thần kinh | Không | Có |
| Mô bệnh học | ||
| Mức độ biệt hóa | Biệt hóa tốt | Biệt hóa kém đến trung bình |
| Thể: thể ly gai, thể tuyến, thể tạo xơ | Không | Có |
| Độ sâu: độ dày hoặc phân độ Clark | I, II, III hoặc < 4mm | IV, V hoặc > 4mm |
| Xâm lấn mạch máu hoặc thần kinh | Không | Có |
B: Vùng nguy cơ thấp (thân mình, chi)I: Vùng nguy cơ trung bình (má, trán, đỉnh đầu, cổ) H: Vùng nguy cơ cao (vùng trung tâm mặt như mi mắt, lông mày, quanh mắt, mũi, môi, cằm, quai hàm, tai và quanh tai, thái dương, sinh dục, bàn tay, bàn chân).
7.3.1 Yếu tố tiên lượng trên lâm sàng
7.3.1.1 Vị trí khối u
Nguy cơ tái phát tại chỗ hoặc di căn thay đổi tùy theo vị trí của khối u ban đầu, nhưng nguy cơ này rất khó đánh giá vì chỉ có một số ít các nghiên cứu nhỏ lẻ hoặc không báo cáo về mối tương quan giữa độ dày khối u và mức độ xâm lấn.
Tổn thương ở vùng da tiếp xúc với ánh nắng (trừ môi và tai) có nguy cơ tái phát thấp nhất.
Các vị trí được báo cáo là có nguy cơ tái phát hoặc di căn cao nhất là:
- Khu vực quanh các hốc tự nhiên (mũi, môi, tai ngoài và mí mắt), và da đầu.
- Các khối u có nguồn gốc ở vùng da không tiếp xúc với ánh nắng mặt trời (đáy chậu, vùng cùng cụt, lòng bàn chân) hoặc trên nền viêm da do bức xạ, sẹo bỏng, viêm loét mạn tính (mức độ bằng chứng 4).
7.3.1.2 Đường kính tổn thương
Mặc dù thông số này không phản ánh chính xác kích thước thực tế của khối u, tuy nhiên nó vẫn được xem như một yếu tố tiên lượng trong hướng dẫn của NHMRC, BAD và NCCN. Đây là một tiêu chí được sử dụng trong phân loại TNM. Có hai ngưỡng để phân loại đường kính khối u: 2cm và 5cm (từ T1 đến T3). Sự phân loại này không liên quan đến độ sâu xâm lấn ngoại trừ T4: xâm nhập vào cơ, xương hoặc sụn.
Theo đánh giá của Rowe, các khối u có đường kính từ 2cm trở lên có nguy cơ tái phát tại chỗ gấp đôi và nguy cơ di căn xa gấp 5 lần so với các khối u có đường kính nhỏ hơn 2cm. Tỷ lệ tái phát và di căn trong 5 năm tương ứng là 7,4% và 9,1%. - Do vậy, kích thước khối u trên 2cm có thể được coi là một yếu tố tiên lượng đáng kể. Tuy nhiên các số liệu tái phát liên quan đến đường kính khối u cho thấy ngưỡng đường kính an toàn trên thực tế thấp hơn, đặc biệt là các vị trí có nguy cơ cao (mức độ bằng chứng 4). Đối với các vị trí này, các nghiên cứu đều cho thấy đường kính tổn thương không phải là yếu tố tiên lượng phù hợp nhất mà phải tính đến các yếu tố khác.
7.3.1.3 Tái phát tại chỗ
Tái phát tại chỗ là một yếu tố nguy cơ đáng kể đối với di căn hạch hoặc di căn xa. Nó là hậu quả của việc không tuân thủ các nguyên tắc về việc cắt bỏ và kiểm tra mô bệnh học rìa tổn thương. Trong một nghiên cứu hồi cứu trên 193 bệnh nhân bị scc ở vùng đầu cổ, kết quả cho thấy có một mối tương quan đáng kể giữa tái phát và di căn hạch. Các nghiên cứu khác cũng cho thấy tỷ lệ di căn cao hơn sau tái phát, dao động từ 25% đến 45% tùy vị trí. Nguy cơ tái phát tại chỗ cũng phụ thuộc vào kích thước và mức độ lan rộng của tổn thương ban đầu, vì các yếu tố đó quyết định mức độ khó khăn trong việc cắt bỏ tổn thương đến mô lành, do đó việc kiểm soát tại chỗ là quan trọng (mức độ bằng chứng 4).
7.3.1.4 Suy giảm miễn dịch
Tỷ lệ bị scc tăng sau ghép tạng đã được chứng minh, mặc dù vẫn còn nhiều ý kiến trái chiều. Trong một nghiên cứu trên 5356 bệnh nhân sau ghép tạng, nguy cơ ung thư da (ngoại trừ melanoma và BCC) cao gấp 100 lần so với dân số nói chung (mức độ bằng chứng 2).
Nguy cơ SCC trên các bệnh nhân ghép tạng còn liên quan đến mức độ suy giảm miễn dịch do việc dùng thuốc lâu dài. Ở cùng độ tuổi, các bệnh nhân ghép thận dùng ciclosporin, azathioprin và pred-nisolon có nguy cơ cao hơn đáng kể so với những bệnh nhân điều trị bằng aza-thioprin và prednosolon. Mức độ xâm lấn của SCC ở các bệnh nhân ghép tạng có vẻ cao hơn so với những người có đáp ứng miễn dịch bình thường. Một nghiên cứu bệnh chứng trên 60 bệnh nhân SCC có ghép tạng và 40 bệnh nhân SCC có hệ miễn dịch bình thường, kết quả cho thấy các bệnh nhân ghép tạng có tiên lượng xấu hơn (mức độ bằng chứng 3).
7.3.2 Các yếu tố tiên lượng về mô học của SCC tiên phát
7.3.2.1 Độ dày và mức độ xâm lấn
Độ dày của khối u và độ sâu xâm lấn là yếu tố có giá trị tiên đoán tốt nhất, nhưng thông tin này thường không có trong các báo cáo về mô bệnh học. Do đó nó không được xem xét trong tất cả các trường hợp.
Theo đánh giá của Rowe, các khối u có độ dày trên 4mm và những khối u mở rộng hoặc xâm lấn xuống lớp trung bì lưới (Clark độ IV hoặc V) có nguy cơ tái phát tại chỗ cao gấp 3 lần, và nguy cơ di căn cao gấp 5 lần so với các khối u có độ dày hoặc phân độ Clark thấp hơn. Tỷ lệ tái phát và di căn sau 5 năm tương ứng là 5,3% và 6,7%. Tuy nhiên trên thực tế, ngưỡng an toàn có thể thấp hơn, đặc biệt là với những vị trí có nguy cơ cao.
Trong một loạt các nghiên cứu hồi cứu phân tích mô bệnh học trên 673 trường hợp SCC và ung thư biểu mô ở môi dưới, không thấy di căn sau phẫu thuật 3 năm đối với các khối u có độ dàỵ < 2mm (n=325). Tỷ lệ di căn là 4,5% đối với khối u có độ dày 2 - 6mm và 12% đối với khối u có độ dày > 6mm. Mối tương quan với mức độ xâm lấn cũng đã được chứng minh: không có trường hợp nào di căn khi khối u chỉ xâm lấn đến % độ dày trung bì, 4,5% khi khối u đã xâm lấn đến hạ bì, và 12,5% khi khối u xâm lấn cơ hoặc xương (mức độ bằng chứng 2).
Có thể áp dụng các nguyên tắc sau:
- Các khối u có độ dày < 2 (hoặc 3) mm hoặc Clark độ < III (hoặc IV) hiếm khi có di căn. Các khối u có độ dày 2 - 5mm có nguy cơ trung bình (tỷ lệ di căn 3 - 5%). Các khối u có độ dày trên 5mm hoặc phân độ Clark > V, nguy cơ di căn có thể vượt quá 15% và đôi khi cao tới 45% (mức độ bằng chứng 2).
- Cần lưu ý rằng khi xác định độ dày của khối u cần loại trừ lớp á sừng. Độ dày của khối u loét cần phải đo từ đáy vết loét.
7.3.2.2 Xâm lấn thần kinh (PNI)
Tỷ lệ xâm lấn thần kinh của SCC ước tính là 4,5 - 14%. Khối u ở vị trí đầu mặt thường có nguy cơ xâm lấn các dây thần kinh nội sọ, hay gặp nhất là thần kinh sinh ba (V) và thần kinh mặt (VII), với mức độ tái phát và di căn cao. Trong một nghiên cứu trên 967 trường hợp SCC ở 520 bệnh nhân, tỷ lệ PNI là 14%. Trong nhóm này, người ta quan sát thấy có sự gia tăng tỷ lệ di căn hạch (35% so với 15%; p <0,0005) và di căn xa (15% so với 3%; p < 0,0005) so với các bệnh nhân không có PNI. Nghiên cứu gần đây của úc trên 1177 bệnh nhân SCC đã được phẫu thuật Mohs, 336 bệnh nhân trong số đó được theo dõi sau 5 năm. PNI được báo cáo trong 70 trường hợp (5,95%), 25 trong số đó được theo dõi sau 5 năm. Tỷ lệ tái phát trong nhóm có PNI và nhóm không có tương ứng là 8% và 3,7% (p=0,02) (mức độ bằng chứng 2).
7.3.2.3 Mức độ biệt hóa tế bào
Phân loại scc theo mức độ biệt hóa tế bào đã được lấy làm yếu tố tiên lượng trong các hướng dẫn trước đó. Dựa trên tỷ lệ của các tế bào biệt hóa và không biệt hóa, người ta chia ra 4 mức độ: độ 1 = 3:1, độ 2 - 1:2, độ 3 = 1:3, độ 4 = không biệt hóa, cách phân loại này ít được sử dụng. Trên thực tế, phần lớn các nhà nghiên cứu sử dụng một phân loại đơn giản hơn mô tả sự biệt hóa của khối u như: “biệt hóa tốt”, “biệt hóa kém”, “không biệt hóa”. Theo đánh giá của Rowe, trong trường hợp khối u biệt hóa kém hoặc không biệt hóa, scc có nguy cơ tái phát gấp đôi và nguy cơ di căn gấp ba lần so với các khối u biệt hóa tốt (mức độ bằng chứng 4).
7.3.2.4 Thể mô bệnh học
Phân biệt các thể scc theo mô bệnh học được đưa ra trong hướng dẫn NCCN, với các thể hỗn hợp, thể ly gai, scc thể tuyến, và thể tạo xơ.
Nghiên cứu về phân loại scc theo mô bệnh học của Cassarino và cộng sự dựa trên sự tổng hợp của nhiều nghiên cứu trước đó. Theo đó, nhóm scc nguy cơ thấp (tỷ lệ di căn < 2%) bao gồm các thể scc thông thường, scc thể sùi, scc dạng biểu bì hình thoi (ngoại trừ scc ở vùng chiếu xạ) cũng như nhóm ung thư biểu mô hỗn hợp. Nhóm có nguy cơ trung bình (tỷ lệ di căn 3 - 10%) bao gồm thể ly gai. Nhóm có nguy cơ cao (tỷ lệ di căn >10%) bao gồm dạng xâm lấn của bệnh Bowen và scc thể tuyến (mức độ bằng chứng 4).
7.3.3 Phân loại tiên lượng cho scc tiên phát
Cho đến nay, không có phân loại tiên lượng thỏa đáng cho scc tiên phát. Phân loại TNM được phát triển bởi AJCC/IUAC/UICC và được áp dụng cho tất cả các dạng ung thư da ngoại trừ melano-ma, không phù hợp với scc. Nó sử dụng đường kính lớn nhất của khối u làm tiêu chí duy nhất cho TI đến T3, với ngưỡng là 2 và 5 cm, và xác định giai đoạn T4 dựa trên sự xâm lấn các cấu trúc dưới da: sụn, cơ vân hoặc xương.
| Khối u nguyên phát (T) | Hạch vùng (N) | Di căn xa (M) |
| TX: u nguyên phát không đánh giá được TO: không xác định được u nguyên phát Tis: ung thư tại chỗ T1: khối u < 2cm T2: 2cm < khối u 5cm T3: khối u > 5cm T4: khối u xâm lấn vào các tổ chức như sụn, cơ vân, xương Chú ý: nếu có nhiều khối u thì phân loại dựa trên khối u có T cao nhất | Nx: không đánh giá được hạch vùng NO: không có di căn hạch vùng N1: di căn hạch vùng (a) micrometastasis (b) di căn hạch cùng bên đơn độc, < 3cm N2: (a) di căn hạch cùng bên đơn độc, đường kính 3 - 6cm, (b) nhiều hạch di căn cùng bên, đường kính > 6cm, (c) di căn mạch bạch huyết vùng N3: (a) di căn hạch đối bên hoặc cả hai bên (b) di căn hạch xâm lấn vùng mặt hoặc nền sọ | MX: không đánh giá được di căn xa MO: không có di căn xa M1: có di căn xa |
| Giai đoạn 0 | Tis | NO | MO |
| Giai đoạn I | T1 | NO | MO |
| Giai đoạn II | T2 | NO | MO |
| T3 | NO | MO | |
| Giai đoạn III | T4 | NO | MO |
| T bất kỳ | N1 | MO | |
| Giai đoạn IV | T bất kỳ | N bất kỳ | M1 |
7.3.4 Phân loại mức độ di căn
SCC có thể tại chỗ, di căn vùng hoặc di căn xa, có thể gây tử vong. 80% di căn theo con đường bạch huyết.
7.3.4.1 Di căn mạch bạch huyết
Di căn nội mạch tại chỗ: đây là những vi thuyên tắc thấy trong các mô bị cắt bỏ gần khối u nguyên phát. Nếu không được điều trị từ đầu, chúng có thể dẫn đến tái phát tại chỗ hoặc di căn vệ tinh sau đó.
Di căn di chuyển (intransit metastases): tiên lượng tương tự di căn hạch.
7.3.4.2 Di căn hạch
Vị trí thường gặp nhất của scc là vùng đầu cổ, các hạch bạch huyết vùng này thường bị ảnh hưởng như hạch dưới hàm, dưới cằm, hạch trong tuyến mang tai.
Tình trạng hạch vùng có ảnh hưởng lớn đến tiên lượng, vì tỷ lệ sống sau 5 năm đối với di căn hạch là 40%, trong khi đó, tái phát tại hạch sau khi nạo vét hạch triệt để gây tử vong trong hầu hết các trường hợp.
Dựa trên số lượng hạch di căn trên mô bệnh học, có thể tiên lượng nguy cơ tử vong.
| Số lượng hạch di căn | Tỷ lệ sống sau 5 năm |
| 1 | 49% |
| 2 | 30% |
| > 3 | 13% |
| Sự mở rộng ngoài bao hạch | |
| Không | 47% |
| Có | 23% |
Khuyến cáo: đánh giá tiên lượng về tình trạng hạch bạch huyết phải tính đến hai yếu tố: số lượng và kích thước hạch di căn, có hay không lan ra ngoài bao hạch.
Do phần lớn các di căn hạch đều thấy trong trường hợp scc ở đầu và cổ, khuyến cáo nên sử dụng các tiêu chí phân loại trên cho những trường hợp này.
7.4 Chẩn đoán xác định
Dựa trên lâm sàng và mô bệnh học như đã mô tả.
7.5 Chẩn đoán phân biệt
Dày sừng ánh sáng
Ung thư biểu mô tế bào đáy
Tổn thương da lành tính
Sẩn dạng Bowen
Viêm da mủ hoại thư
Loét mạn tính
7.6 Điều trị
7.6.1 Điều trị scc tại chỗ
Tham khảo bài dày sừng ánh sáng, bệnh Bowen.
7.6.2 Điều trị scc xâm lấn
7.6.2.1 Phẫu thuật điều trị ung thư
Là tiêu chuẩn vàng trong điều trị scc được nhất trí trong hướng dẫn của BAD, NCCN, NHMRC, nó cho phép cung cấp một mô được cắt bỏ, cho phép xác nhận chẩn đoán và xác nhận chất lượng cắt bỏ cũng như đạt được tỷ lệ kiểm soát tại chỗ cùng như điều trị khỏi ở đa số trường hợp.
Mục tiêu điều trị
- Mục đích chính của điều trị phẫu thuật cho scc là đạt dược kết quả cắt bỏ u hoàn toàn trên mô bệnh học.
- Ngoài ra cần chú ý hai mục tiêu khác: duy trì chức năng bình thường và đảm bảo thẩm mỹ đặc biệt ở vị trí khuôn mặt.
- Cắt bỏ khối u tiên phát khi được thực hiện đúng, tỷ lệ chữa khỏi trên 90%.
Nguyên tắc điều trị
- Bệnh nhân phải được thông báo rằng mô bị cắt bỏ sẽ được làm giải phẫu bệnh, và có thể cần phẫu thuật thêm tùy thuộc vào kết quả trong trường hợp cắt bỏ không hoàn toàn khối u.
- Nếu có nghi ngờ lâm sàng về chẩn đoán, cần xác nhận bằng mô bệnh học. Điều này sẽ yêu cầu sinh thiết (bằng punch hoặc cắt) trước mổ, hoặc cắt bỏ hoàn toàn trong trường hợp tổn thương nhỏ.
- Sinh thiết chỉ cho phép nghiên cứu một phần tổn thương, các bệnh phẩm hậu phẫu cần được làm xét nghiệm mô bệnh học.
- Quy trình phẫu thuật phải được lên kế hoạch theo các thông số khối u. Bờ và độ sâu (mức độ xâm nhập) của tổn thương phải được đánh giá lâm sàng cẩn thận. Rìa cắt bỏ phải được đánh dấu trước khi tiêm tê cục bộ, vì sau đó có thể làm cho bờ khối u khó phân biệt hơn.
- Cắt bỏ khối u rộng ở các khu vực nhạy cảm về thẩm mỹ hoặc chức năng (cắt đi một phần của mí mắt hoặc ống dẫn lệ, các hoạt động liên quan đến khuôn mặt, môi, mũi và nói chung là bất kỳ trường hợp nào dẫn đến mất mô nhiều sau khi cắt bỏ) yêu cầu sự thành thạo về phẫu thuật trong quán lý ung thư da.
- Xạ trị sau phẫu thuật có thể cần thiết trong một số trường hợp.
Bờ và độ sâu
- Hướng dẫn BAD và NCCN đề cập đến nghiên cứu của Brodland và Zitelli, dựa trên một nghiên cứu tiền cứu liên quan đến 141 trường hợp scc nguyên phát được loại bỏ bằng phẫu thuật Mohs, lưu ý rằng:
- Khoảng cách với rìa khối u từ 4mm là đủ để loại bỏ 95% khối u đường kính dưới 2cm.
- Khoảng cách với rìa khối u > 6mm thậm chí tới l0mm là cần thiết để có được kết quả tương tự đối với các khối u có đường kính > 2cm hoặc đối với các khối u có yếu tố nguy cơ, chẳng hạn như scc biệt hoá kém, scc xâm lấn hạ bì hoặc scc nằm trong khu vực có nguy cơ (mức độ bằng chứng 2).
- Độ sâu cắt bỏ phải tới lớp hạ bì miễn là khối u không xâm lấn vào cân, màng xương, màng sụn.
7.6.2.2 Phẫu thuật Mohs
Thực hiện ở những vùng cần tiết kiệm tổ chức và chỉ nên sử dụng trong trường hợp không thấy hạch trên lâm sàng hoặc trên siêu âm, kỹ thuật này có thể kiểm soát tốt 95% tổn thương tại chỗ.
Phẫu thuật Mohs được ưu tiên chỉ định trong các trường hợp có nguy cơ cao sau: + Khó xác định bờ tổn thương trên lâm sàng.
- Thương tổn ở vị trí nguy cơ tái phát cao (trung tâm mặt, đầu, môi, trụ mũi, tai, chi dưới, trán, giường móng, niêm mạc), vị trí cần bảo tồn tổ chức (đầu mũi, cánh mũi, mi mắt, quanh mắt, góc mắt, sinh dục).
- Ung thư biếu mô tế bào vảy thâm nhiễm, có thâm nhập thần kinh, xương, cơ.
- Ung thư biểu mô tế bào vảy trên một sẹo mạn tính, loét mạn tính, sẹo bỏng, viêm tuỷ xương mạn tính, lupus đỏ hình đĩa, bệnh Bowen, lichen xơ teo.
Nguyên cứu của Leibovitch I và cộng sự báo cáo kết quả của một nghiên cứu tiến cứu đa trung tâm liên quan đến 1263 trường hợp scc (1993-2002), trong đó 61,1% là scc nguyên phát và 38,9% scc tái phát. Sau mổ Mohs, tỷ lệ tái phát trong 5 năm đối với 381/1263 bệnh nhân là 2,6% đối với scc nguyên phát và 5,9% đối với scc tái phát (mức độ bằng chứng 2).
Malhotra R và cộng sự đã báo cáo tỷ lệ tái phát là 3,64% (2/56) ở 71 bệnh nhân trải qua phẫu thuật Mohs cho scc quanh mắt. Tỷ lệ này thấp hơn so với tất cả các phương pháp điều trị thay thế khác cho những khối u có tiên lượng xấu.
7.6.2.3 Điều trị bằng dao điện và curet
Phương pháp này nhanh chóng, tiết kiệm mô da, cho phép cầm máu, ngay cả ở những bệnh nhân đang điều trị các thuốc chống đông máu và không tốn kém.
Sử dụng curette có thể giúp cung cấp thông tin mô bệnh học để chẩn đoán, nhưng không cho phép kiểm soát bờ của tổn thương. Phương pháp này đòi hỏi sư chắc chắn của chẩn đoán lâm sàng, bờ khối u được phân định rõ, phẫu thuật viện được đào tạo.
Hướng dẫn NCCN đưa ra hai lưu ý khi sử dụng kỹ thuật này:
- Vùng lông/tóc không phù hợp vì các khối u lan rộng dọc theo vỏ không phải lúc nào cũng loại bỏ được bởi curet.
- Kỹ thuật này không phù hợp với các tổn thương liên quan tới hạ bì, bởi vì trong khu vực này, người phẫu thuật không thể phân biệt được sự khác nhau của khối u và mô lành.
7.6.2.4 Xạ trị
Xạ trị đã được sử dụng trong tất cả các dạng scc, và cho thấy hiệu quả tương đương với phẫu thuật, nhưng vì phần lớn scc bao gồm các tổn thương nhỏ, phẫu thuật có ưu điểm là dễ sử dụng, lành vết thương nhanh, cùng với kết quả thẩm mỹ tốt. Do đó, các hướng dẫn NHM-RC khuyến nghị xạ trị là điều trị bậc hai, dựa trên lời khuyên của chuyên gia và chỉ trong các trường hợp sau:
- Bệnh nhân có chống chỉ định phẫu thuật, bệnh nhân từ chối phẫu thuật hoặc phẫu thuật sẽ dẫn đến kết quả không thể chấp nhận được.
- scc tái phát, xạ trị có thể được kết hợp với phẫu thuật để cải thiện kiểm soát khối u. + Khối u còn sót lại sau điều trị và phẫu thuật là không khả thi.
- Quản lý di căn.
Chống chỉ định:
- Bệnh nhân dưới 60 tuổi, tổn thương có thể phẫu thuật được.
- Tổn thương trên da đầu hoặc tiếp xúc với ống dẫn nước mắt.
- Tổn thương tiến triển xâm lấn gân, khớp hoặc xương.
- Tổn thương ở những khu vực nghèo mạch máu và dễ bị thương (ví dụ: tổn thương trước xương chày).
- Tổn thương ở những vùng đã chiếu xạ.
- Tổn thương sát xương dễ bị chấn thương, chi dưới, mi mắt trên hoặc bất cứ vị trí nào kém dung nạp.
- Bệnh da di truyền có nguy cơ ung thư da, hội chứng Gorlin, khô da sắc tố.
Trong trường hợp có sự liên quan với hạch bạch huyết, phẫu thuật cắt bỏ được đề xuất là điều trị đầu tay. Mức độ kiểm soát tại chỗ sau điều trị kết hợp (phẫu thuật và xạ trị bổ trợ ngoài) trong trường hợp xâm lấn hạch bạch huyết là khoảng 80% so với 30% 50% sau đơn trị liệu (phẫu thuật hoặc xạ trị ngoài, sống sót không tái phát tại thời điểm 5 năm là 70% so với 50%.
Trường hợp SCC tái phát sau phẫu thuật và khi không thể phẫu thuật thêm, tỷ lệ kiểm soát tại chỗ sau khi chiếu xạ được ước tính là từ 65% đến 80% sau 5 năm, đồng thời trong trường hợp khối u còn sót lại dưới kính hiển vi, xạ trị bổ trợ chỉ được chỉ định khi không thể phẫu thuật thêm.
7.6.2.5 Hoá trị liệu toàn thân
Hóa trị có giá trị hạn chế, chỉ được sử dụng trong trường hợp phẫu thuật hoặc xạ trị thất bại, điều trị không đầy đủ hoặc bệnh giai đoạn muộn. Trong hướng dẫn của NHRMC, Cisplatin là hóa trị liệu tham khảo. Các tài liệu về hóa trị rất ít, chủ yếu là các nghiên cứu nhỏ lẻ. Các nghiên cứu có kiểm soát duy nhất liên quan đến SCC vùng đầu và cổ (miệng, hầu và thanh quản), nhưng chúng không thể đồng nhất hoàn toàn với SCC.
Một số cách khác nhau được lựa chọn:
- Hoá trị bổ trợ trước mổ: đã được sử dụng trong các khối u rất lớn để giúp phẫu thuật thuận lợi. Vì phần lớn các nghiên cứu đã cho thấy không có sự cải thiện trong kiểm soát khối u hoặc tỷ lệ sống sót, vì vậy phương pháp điều trị này hiếm khi được sử dụng.
- Hoá trị sau mổ: nghiên cứu của Ber-nier J và cộng sự (2004) chỉ ra kết hợp xạ trị sau phẫu thuật và cisplatin đã giúp cải thiện khả năng sống sót so với xạ trị đơn thuần cho trường hợp di căn. Không có nghiên cứu nào chứng minh tỷ lệ sống tăng lên đối với đa hóa trị liệu so với chỉ dùng cis-platin.
- Điều trị giảm nhẹ: một số nghiên cứu và phân tích tổng hợp về liệu pháp kết hợp liên quan đến hóa trị liệu giảm nhẹ - xạ trị trong SCC niêm mạc ở đầu và cổ đã cho thấy tỷ lệ sống vượt trội so với xạ trị đơn thuần, nhưng tăng nguy cơ độc tính (niêm mạc, thần kinh, đường tiêu hóa, tủy và thận).
Liệu pháp điều trị đích:
- Cetuximab là một kháng thể đơn dòng của người và có ái lực mạnh với EGFR (thụ thể yếu tố tăng trưởng thượng bì) dẫn tới ức chế sự tăng trưởng của tế bào. Thuốc thường được sử dụng trong trường hợp ung thư đường hô hấp, đường tiêu hóa và ung thư đại trực tràng di căn, độ dung nạp tương đối tốt. Thuốc được được nghiên cứu sử dụng trong trường hợp SCC của mặt và thân, cũng như trong di căn hạch bạch huyết của SCC.
- Một nghiên cứu ngẫu nhiên pha III trên 117 bệnh nhân bị SCC di căn ở hầu họng, môi hoặc mặt cho thấy hiệu quả vượt trội của cetuximab-cispla-tin so với cisplatin đơn thuần, nhưng không tăng đáng kể thời gian sống. Nghiên cứu pha II không được kiểm soát với 103 bệnh nhân bị SCC di căn hoặc tái phát ở đầu và cổ, được điều trị bằng cetuximab, tỷ lệ đáp ứng là 13%.
- Hiện tại không thể khẳng định rằng cetuximab là một lựa chọn điều trị có giá trị.
7.6.3 Điều trị SCC di căn
7.6.3.1 Di căn tại chỗ (in-transit)
Sự xuất hiện của di căn có thể quan sát được trên lâm sàng xung quanh SCC nguyên phát hoặc tái phát, có thể cắt bỏ bằng phẫu thuật nếu số lượng, kích thước, sự lan rộng và vị trí của tổn thương phù hợp. Bổ sung xạ trị bổ trợ nếu có thể.
7.6.3.2 Di căn hạch lympho
Tỷ lệ sống sau 5 năm của bệnh nhân di căn hạch bạch huyết là 30%.
Vét hạch thường quy
- Vét hạch thường quy hiện đang được tiến hành với SCC vùng da, niêm mạc của đầu và cổ vì có nguy cơ di căn hạch cao (nguy cơ di căn tiềm ẩn > 20%), mặc dù về mặt sống sót, giá trị của vét hạch thường quy chưa được chứng minh.
- Nó đã được đề xuất cho các tổn thương môi có độ dày > 6mm và cho các vị trí khác có độ dày vượt quá 8mm, mặc dù mức độ bằng chứng thấp.
- Hiện tại không được khuyến cáo do tỷ lệ về lợi ích trên nguy cơ tử vong thấp.
Vét hạch chọn lọc
- Cách tiếp cận này cũng được đề xuất cho các trường hợp SCC có nguy cơ cao ở đầu và cổ mà không sờ thấy hạch. Điều trị được giới hạn ở vị trí của các hạch bạch huyết dẫn lưu từ tổn thương ban đầu với sự kiểm soát tạm thời của các hạch bạch huyết xa. Vét hạch toàn bộ chỉ được thực hiện nếu hạch kiểm tra sau đó dương tính.
- Vét hạch chọn lọc bằng cách sử dụng kỹ thuật hạch gác đã được chứng minh không có giá trị và hiện không được khu-yến nghị.
Vét hạch toàn bộ
- Được thực hiện trong trường hợp phát hiện hạch di căn rõ ràng trên lâm sàng hoặc sinh thiết hạch dương tính. Chưa có hướng dẫn cụ thể nào về phương pháp phẫu thuật và mức độ nạo vét hạch, số lượng trung bình của các hạch bạch huyết liên quan đến khu vực phẫu thuật là:
- 15 hạch bạch huyết ở vùng nách
- 10 hạch bạch huyết ở vùng bẹn
- 15 hạch bạch huyết ở vùng mặt cổ
- Những số liệu này có thể thay đổi tùy theo từng cá nhân và theo mức độ sàng lọc các hạch bạch huyết trong mô bị cắt bỏ.
8 Ung thư tế bào hắc tố (Malignant melanoma)
8.1 Đại cương
Ung thư tế bào hắc tố là khối u ác tính có nguồn gốc từ các tế bào hắc tố chủ yếu xuất phát từ các tế bào hắc tố ở da. Ngoài ra, ung thư tế bào hắc tố có thể xuất phát từ các tế bào hắc tố nằm ở màng bồ đào, biểu mô sắc tố võng mạc, niêm mạc ống tiêu hóa hay màng não mềm. Ung thư tế bào hắc tố có thể là tổn thương tiên phát hoặc phát triển trên nền tổn thương trước đó (như bớt sắc tố).
Tỷ lệ mắc bệnh ngày càng tăng trên thế giới, đặc biệt là nơi mà tầng ozone có xu hướng mỏng đi (như ở Úc, Mỹ).
Độ tuổi khoảng 40 - 50 tuổi.
Yếu tố nguy cơ của ung thư tế bào hắc tố được chia thành ba nhóm chính: do gen, do môi trường và do kiểu hình.
| YẾU TỐ NGUY CƠ CỦA UNG THƯ TẾ BÀO HẮC TỐ |
| Do gen |
| Tiền sử gia đình có người bị ung thư tế bào hắc tố |
| Da tối màu |
| Dễ bị bỏng nặng, da khó bị ngăm đen |
| Tóc màu đỏ |
| Các bệnh lý khiếm khuyết trong sửa chữa sai sót của DNA (khô da sắc tố) |
| Do môi trường |
| Tiếp xúc ánh sáng cường độ mạnh, đột ngột |
| Tiếp xúc với ánh sáng mặt trời thường xuyên |
| Sống ở vùng gần xích đạo |
| PUVA |
| Tắm nắng, đạc biệt là trước 35 tuổi |
| Suy giảm miễn dịch mắc phải hoặc do điều trị bằng các liệu pháp ức chế miễn dịch |
| Sự biểu hiện của kiểu hình trong mối liên quan giữa gen và môi trường |
| Bớt sắc tố và đồi mồi: Số lượng bớt sắc tố mắc phải: > 100 bớt sắc tố làm tăng nguy cơ ung thư tế bào hắc tố 8 - 10 lần. Bớt sắc tố không điển hình: > 5 bớt sắc tố không điển hình làm tăng nguy cơ ung thư tế bào hắc tố lên 4 - 6 lần Đồi mồi: nhiều tổn thương đồi mồi làm tăng nguy cơ ung thư tế bào hắc tố lên 3 - 4 lần. Nguy cơ tương đối của ung thư hắc tố khi phối hợp tất cả các yếu tố nguy cơ trên: ví dụ một người có > 100 bớt sắc tố, > 5 bớt sắc tố không điển hình và nhiều tổn thương đồi mồi thì nguy cơ của người này bị ung thư tế bào hắc tố khoảng 10x5x3 = 150 lần so với người bình thường. |
| Bản thân từng bị ung thư tế bào hắc tố da. |
8.2 Lâm sàng
Biểu hiện lâm sàng của ung thư tế bào hắc tố hết sức đa dạng.
Tiêu chuẩn “ABCDE” thường được sử dụng trên lâm sàng để nhận biết khối u tế bào hắc tố. Trong đó: Asymmetry: không đối xứng. Borders (Irregular bor-ders): ranh giới không rõ. Color (Color variegation): màu sắc không đồng nhất. Diameter: đường kính > 6mm (Differ-ence). Evolve (Evolving over time): tiến triển theo thời gian.
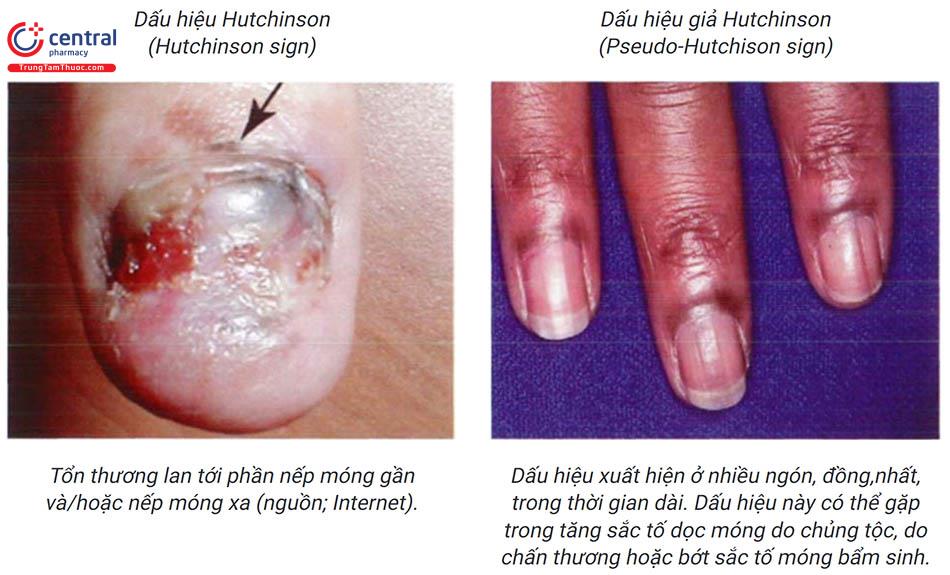
Để không bỏ sót chẩn đoán ung thư tế bào hắc tố thể nốt và thể không tăng sắc tố, người ta thêm vào tiêu chuẩn “ABC-DE” 3 tiêu chuẩn nữa là “EFG”. Trong đó: Elevated: gồ lên mặt da. Firm: chắc. Growing: tiến triển. Dấu hiệu Hutchin-son: là dấu hiệu quan trọng trong chẩn đoán ung thư hắc tố móng.
Ung thư tế bào hắc tố được phân loại dựa vào hình thái trên lâm sàng và trên mô bệnh học. Trong đó có 4 thể chính của ung thư tế bào hắc tố (thường gặp nhất):
- Ung thư tế bào hắc tố lan tỏa thể nông (superficial spreading melanoma).
- Ung thư tế bào hắc tố thể nốt (nodu-lar melanoma).
- Ung thư tế bào hắc tố thể Dubreuilh (Dubreuilh melanoma hay lentigo maligna melanoma).
- Ung thư tế bào hắc tố thể đầu cực (acral lentiginous melanoma): đây là thể thường gặp nhất ở người châu Á và châu Phi.
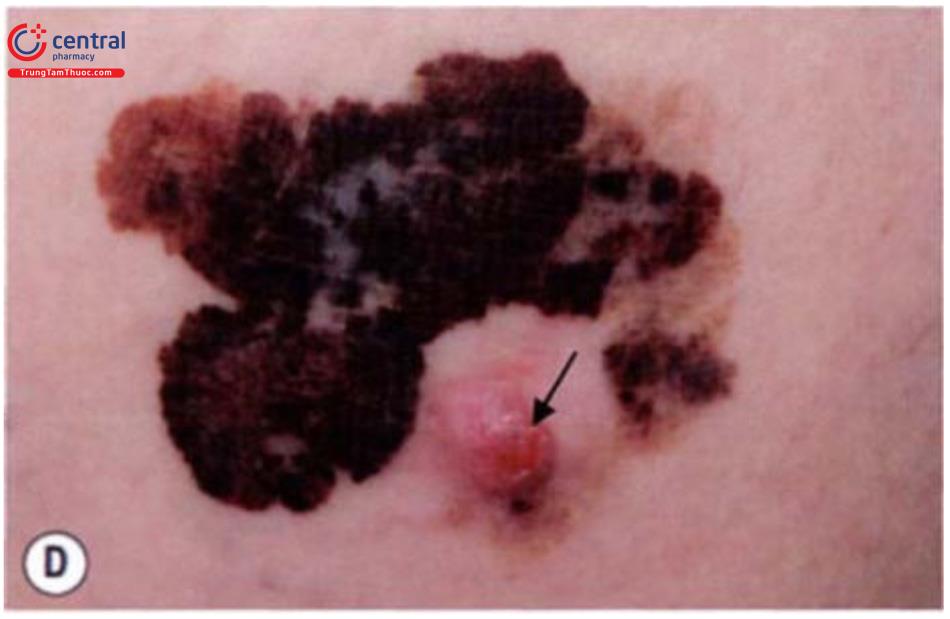
Ung thư tế bào hắc tố lan tỏa thể nông (superficial spreading melanoma) Ban đầu là tổn thương dạng dát với những đặc điểm của ung thư hắc tố, sau đó lan rộng ra xung quanh, xuất hiện nốt (mũi tên), cục, loét và chảy máu, khi đó tổn thương đã ở giai đoạn xâm nhập sâu.
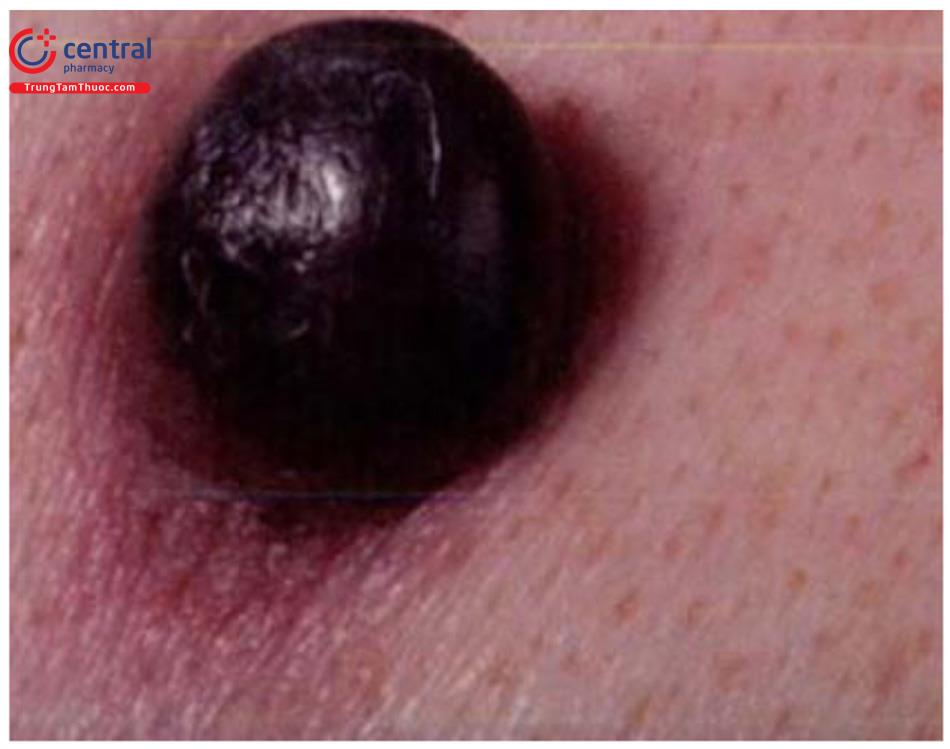
Ung thư tế bào hắc tố thể nốt (nodular melanoma) Tổn thương cơ bản là u nhỏ nổi cao trên mặt da, hình vòm đôi khi có cuống, có thể loét, chảy máu. Thường có màu nâu đỏ, tăng sắc tố rải rác trên bề mặt tổn thương, không đều. Tổn thương thường xuất hiện ở thân mình.
Ung thư tế bào hắc tố thể Dubreuilh (Dubreuỉlh melanoma hay lentigo ma-ligna melanoma) Dát màu nâu hoặc đen, lan rộng dần ra xung quanh, đôi khi lành ở giữa, sau đó xuất hiện u trên tổn thương (xâm lấn sâu). Đây là dưới thể của ung thư tế bào hắc tố tại chỗ (in situ), thông thường tổn thương thường phát triển nông trong nhiều năm trước khi tiến triển xâm lấn xuống sâu.

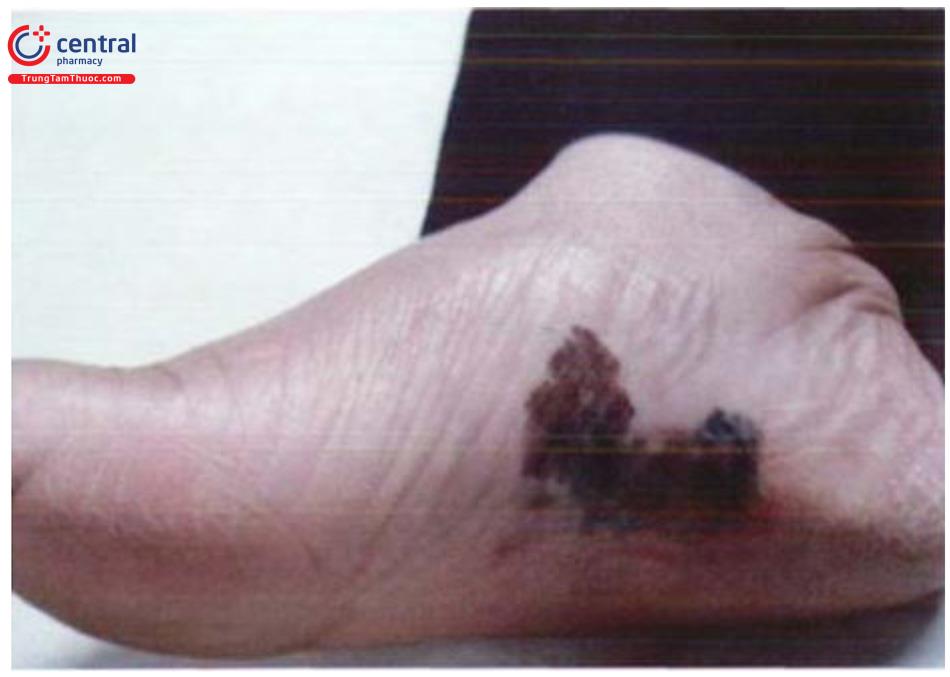
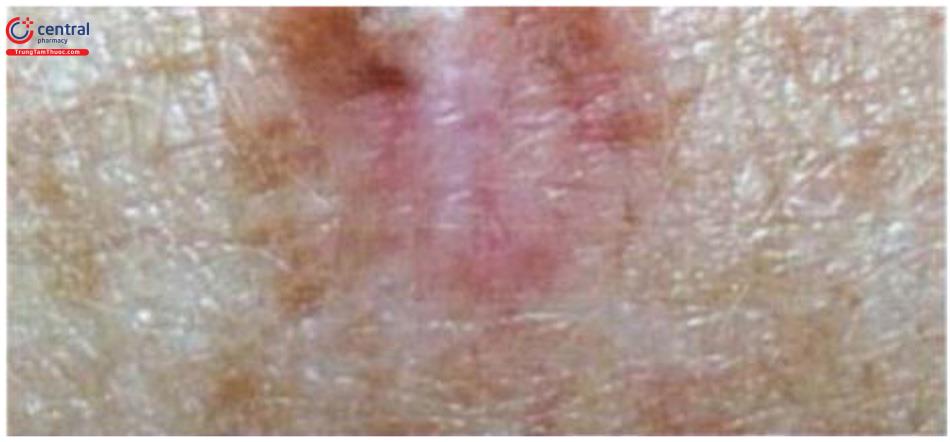
Ung thư tế bào hắc tố thể đầu cực (acral lentiginous melanoma) Ban đầu là dát tăng sắc tố, sau đó lan rộng ra xung quanh, xuất hiện loét hoặc khối u nổi cao. Đây là thể thường gặp nhất ở người châu Á, trong đó có Việt Nam.
Các thể khác ít gặp hơn:
- Ung thư hắc tố thể không tăng sắc tố (amelanotic melanoma)
- Ung thư hắc tố móng (nail matrix melanoma)
- Ung thư hắc tố niêm mạc (mucosal melanoma)
- Ung thư hắc tố thể xơ (desmoplastic melanoma)
Ung thư tế bào hắc tố thể không tăng sắc tố (amelanotic melanoma)
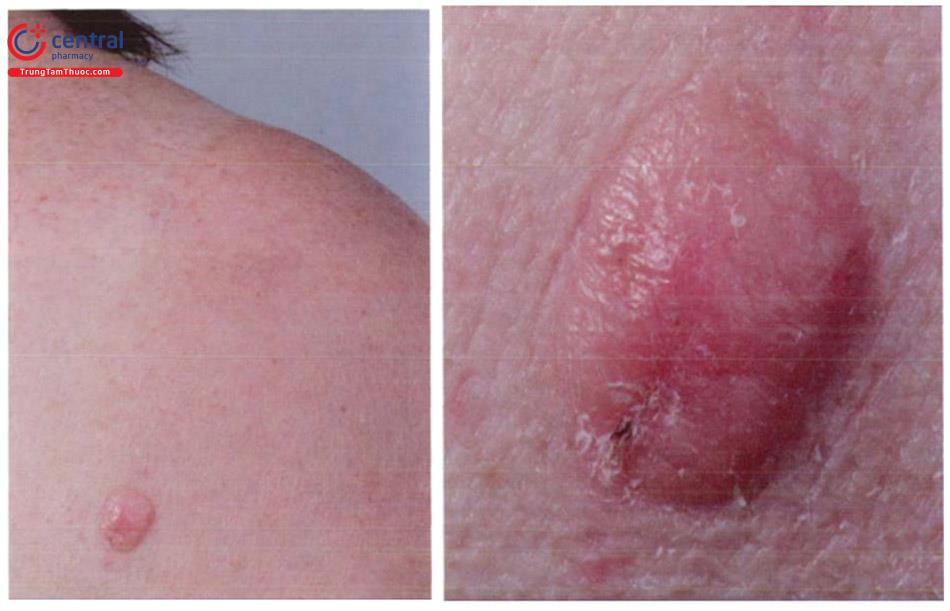
Tổn thương cơ bản là tổn thương dạng nốt màu từ hồng tới đỏ. Tuy nhiên, tất cả các thể của ung thư tế bào hắc tố đều có thể không tăng sắc tố. Ở trẻ em có thể xuất hiện tổn thương ung thư hắc tố thể không tăng sắc tố mà lâm sàng cần phải phân biệt với côn trùng đốt hoặc u hạt nhiễm khuẩn.
Ung thư hắc tố móng (nail matrix mel-anoma)
“ABCDE” cho ung thư hắc tố móng
A: Age: 50 - 70 tuổi African-Ameri-cans, Native Americans Asians (Mỹ gốc Phi, châu Mỹ bản địa, châu Á)
B: Brown to Black (nâu đến đen) Breadth (rộng > 3mm) Borders (ranh giới loang lổ)
C: Change in nail band (dải sắc tố móng thay đổi màu sắc hoặc kích thước)
D: Digit (móng thường gặp là ngón tay cái và ngón chân cái)
E: Extension into the proximal/later-al nail fold (Tổn thương lan tới nếp móng gần/bên). Dấu hiệu Hutchinson.
F: Family (gia đình hoặc bản thân có tiền sử ung thư hắc tố).
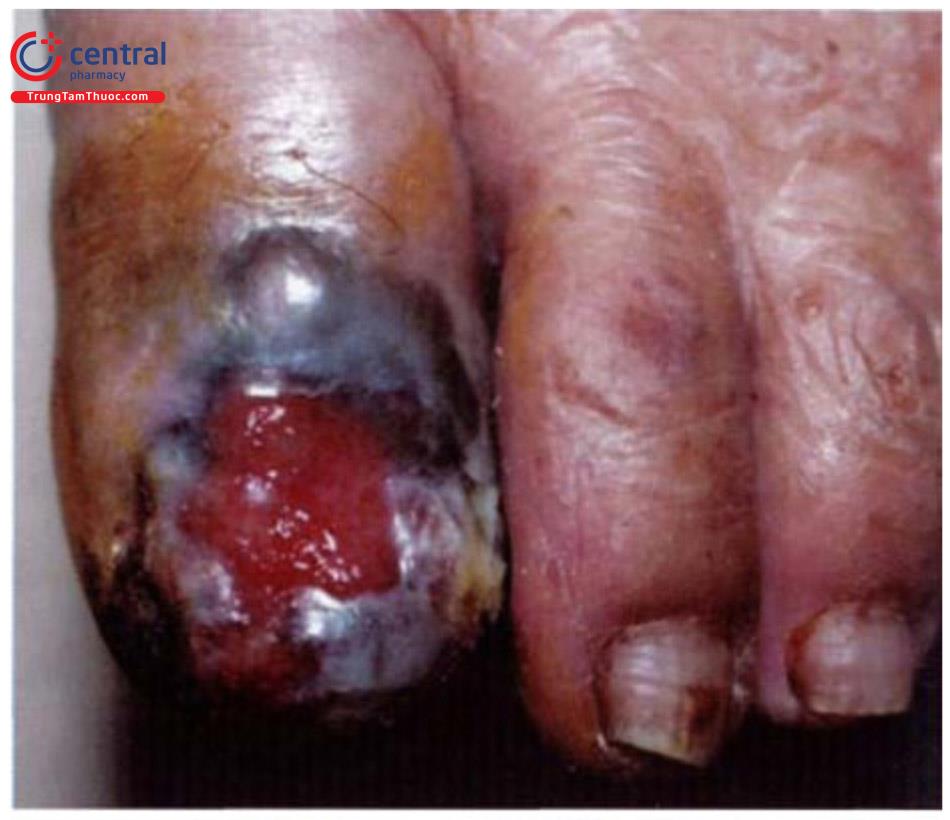
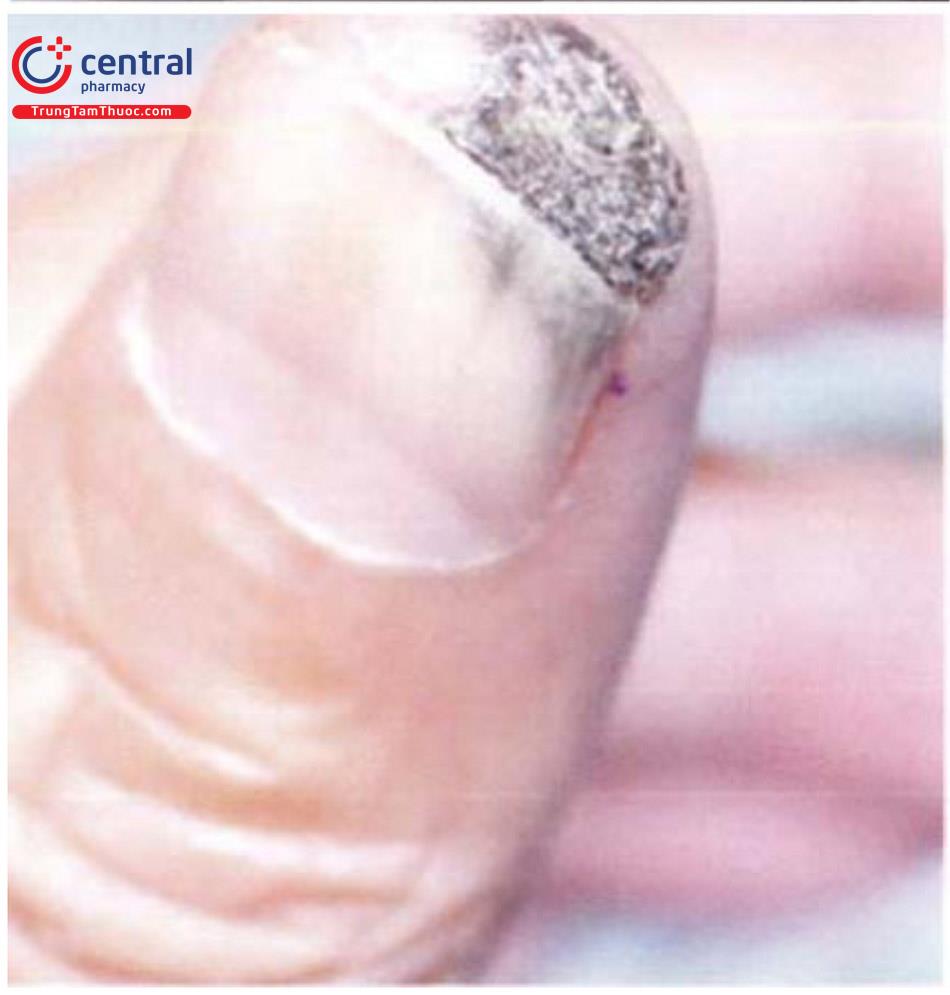
Ung thư tế bào hắc tố niêm mạc (mucosal melanoma)
Tổn thương cơ bản là tổn thương dát tăng sắc tố với các đặc điểm của ung thư tế bào hắc tố. Tuy nhiên có khoảng 35% các trường hợp không có tăng sắc tố. Tổn thương có thể gặp ở miệng (vòm miệng, lợi), hậu môn. Mũi họng, thanh quản, âm hộ ít gặp hơn.
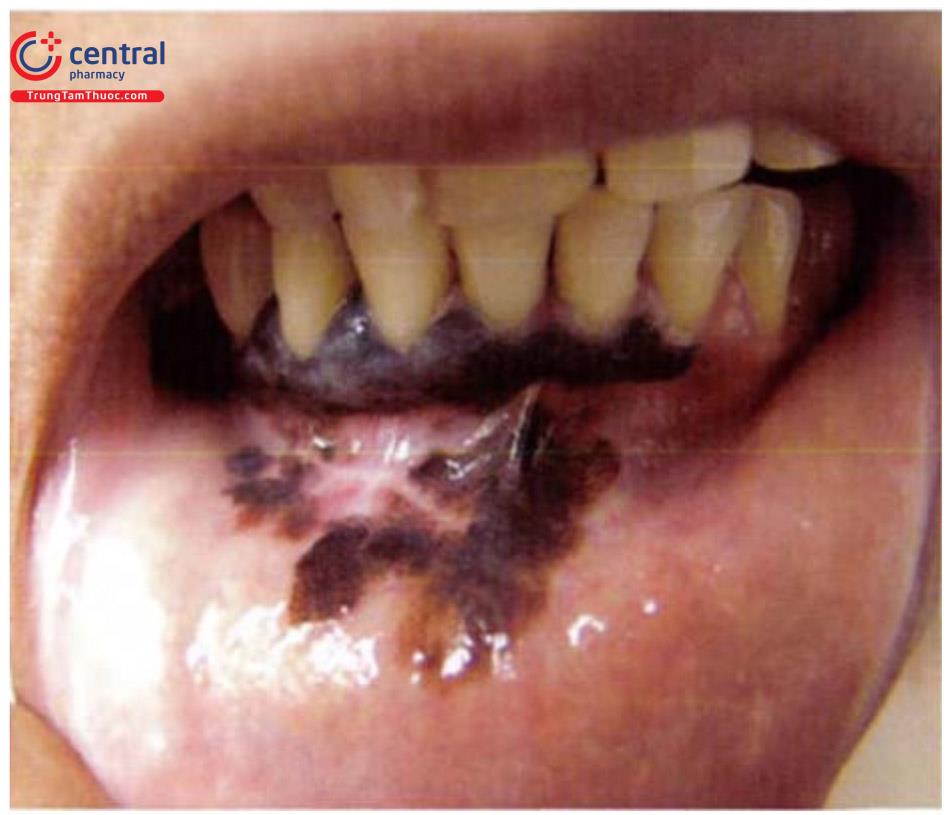
Ung thư hắc tố thể xơ (desmoplastic melanoma)
Là thể hiếm gặp của ung thư tế bào hắc tố xâm nhập. Tổn thương trên mô bệnh học được bao quanh bởi mô xơ ở trung bì. Tổn thương thường ảnh hưởng tới sợi thần kinh nên còn có tên gọi khác là neurotrophic melanoma.
Khái niệm ung thư hắc tố tại chỗ (mela-noma in situ - MIS): là khối u chỉ khu trú ở thượng bì và/hoặc biểu mô nang lông. Tất cả các thể của ung thư hắc tố (trừ ung thư hắc tố thể nốt) đều có giai đoạn ung thư tế bào hắc tố tại chỗ. Trong đó, ung thư hắc tố thể Dubreuilh là dưới thể của ung thư hắc tố tại chỗ phát triển ở vùng tiếp xúc với ánh sáng mạn tính nhưng không tiến triển xâm lấn sâu trong nhiều năm.
Ung thư tế bào hắc tố ở trẻ em rất hiếm gặp. Tổn thương thường có xu hương dày hơn do đó rất khó phân biệt với bớt spitz trên mô bệnh học, tuy nhiên tiền lượng tương đối tốt.
8.3 Mô bệnh học
Trên mô bệnh học, ung thư tế bào hắc tố đặc trưng bởi: tăng sinh, thâm nhập các tế bào hắc tố ở thượng bì và trung bì; tế bào chưa biệt hóa, nhân to, bắt màu đậm; rối loạn phân bào, tăng tỷ lệ nhân chia. Ngoài ra có thể gặp: tăng sinh mạch máu, thâm nhiễm bạch cầu, có thể có loét.
Đánh giá mức độ xâm lấn của ung thư tế bào hắc tố trên mô bệnh học có vai trò quan trọng trong điều trị và tiên lượng bệnh. Chỉ số Breslow (Breslow’s depth) và thang Clark (Clark’s level) là hai chỉ số thường được sử dụng, trong đó:
- Chỉ số Breslow: là khoảng cách tính từ lớp hạt của thượng bì tới điểm mà khối u xâm lấn sâu nhất (mm).
- Thang Clark: là mức độ xâm lấn của khối u trên mô bệnh học tính theo các lớp của da: thượng bì, trung bì nông, trung bì sâu, giữa trung bì nông và sâu, hạ bì tương ứng với thang Clark là 1, 2, 3, 4 và 5 điểm.
Trong nhiều trường hợp để phân biệt tế bào ác tính có nguồn gốc từ tế bào hắc tố (ung thư tế bào hắc tố) và có nguồn gốc từ loại tế bào khác, có thể phải sử dụng các marker đặc trưng cho tế bào hắc tố. Trong đó, các marker thường được sử dụng nhất là HMB45, S100, Melan-A.
8.4 Dermoscopy
Dermoscopy là một trong những công cụ hồ trợ rất quan trọng trong chẩn đoán ung thư tế bào hắc tố, đặc biệt có ý ng-hĩa hơn trong việc chẩn đoán bệnh ở giai đoạn sớm.
Ung thư tế bào hắc tố qua dermoscopy có nhiều biểu hiện đa dạng và đã được đưa vào sử dụng trong chẩn đoán theo nhiều thang điểm. Trong đó, có hai thang điểm thường được sử dụng:
| Tiêu chuẩn 7 điểm (1998) | ||
| Tiêu chuẩn chính | Mạng lưới sắc tố không điển hình | 2 |
| Mạng xanh trắng | 2 | |
| Mạng lưới mạch máu không điển hình | 2 | |
| Tiêu chuẩn phụ | Đường sọc không đồng đều | 1 |
| Đốm bất thường (về màu sắc, hình dạng) | 1 | |
| Sắc tố hình chấm và hình cầu bất thường (do hiện tượng tập trung sắc tố) | 1 | |
| Cấu trúc thoái hóa (vùng trắng như sẹo và/hoặc cấu trúc xanh hoặc xanh xám) | 1 | |
| *Chẩn đoán ung thư tế bào hắc tố khi tổng điểm > 3 điểm | ||
TIÊU CHUẨN 3 ĐIỂM Không đối xứng về màu sắc và cấu trúc theo trục thẳng đứng hoặc trục ngang Mạng lưới sắc tố không điển hình với những lỗ khuyết và đường kẻ dày, phân bố bất thường Cấu trúc màu xanh trắng *Chẩn đoán ung thư tế bào hắc tố khi có cả 3 tiêu chuẩn, nghi ngờ ung thư tế bào hắc tố khi tổn thương thỏa mãn 1 tiêu chuẩn
Chẩn đoán xác định
Những dấu hiệu nghi ngờ ung thư tế bào hắc tố trên lâm sàng cần được phát hiện càng sớm càng tốt để không làm chậm trễ quá trình điều trị. Yếu tố quan trọng nhất trong chẩn đoán ung thư tế bào hắc tố là dấu hiệu lâm sàng. Mô bệnh học mục đích chính là để khẳng định chẩn đoán.
Khi tiến hành sinh thiết tổn thương nên cố gắng cắt bỏ toàn bộ tổn thương, khẳng định ung thư hắc tố trên mô bệnh học và tính chỉ số Breslow. Trừ trường hợp tổn thương quá lớn để có thể cắt bở ngay lập tức khi đó cắt một phần tổn thương làm mô bệnh học có thể được cân nhắc. Khi thăm khám toàn bộ các tổn thương da trên cơ thể, có hai dấu hiệu cần được lưu ý để phát hiện sớm ung thư tế bào hắc tố:
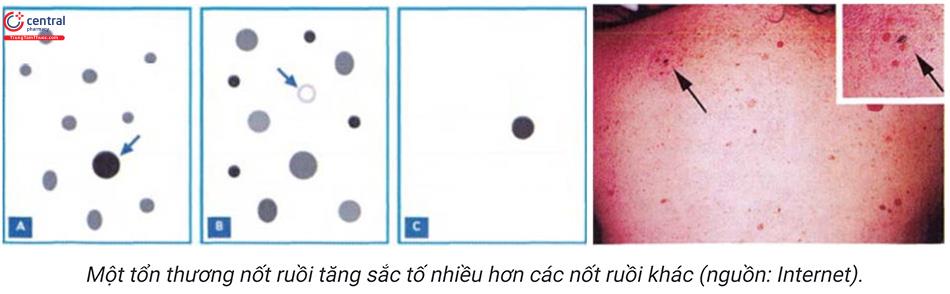
Dấu hiệu “vịt xấu xí” (“ugly duckling” sign)
Là dấu hiệu nhằm phát hiện tổn thương nốt ruồi có biểu hiện khác lạ hơn so với các nốt ruồi khác (vị trí được đánh dấu mũi tên) hoặc chỉ một nốt ruồi duy nhất nhưng xuất hiện bất thường. Giống như “chú vịt” khác thường so với con khác trong đàn vịt. Áp dụng với trường hợp có nhiều tổn thương nốt ruồi.
Dấu hiệu “cô bé quàng khăn đỏ” (“little red riding hood” sign) Chủ yếu giúp phát hiện ung thư tế bào hắc tố không tăng sắc tố ở người da trắng, biểu hiện là viền dát đỏ xung quanh tổn thương.

8.5 Phân loại giai đoạn bệnh ung thư tế bào hắc tố theo AJCC năm 2010
| Phân loại theo TNM | ||
| T | Độ dày của khối u | Loét/Phân bào |
| Tis | Không xác định | Không xác định |
| T1 | < 1,0 mm | a: có/không có loét và phân bào < 1/mm2 |
| b: có loét hoặc phân bào > 1/mm2 | ||
| T2 | 1,01 - 2,0 mm | a: có/không có loét |
| b: có loét | ||
| T3 | 2,01 - 4,0 mm | a: có/không có loét |
| b: có loét | ||
| T4 | > 4,0mm | a: có/không có loét |
| b: có loét | ||
| N | Di căn hạch | Tình trạng di căn hạch |
| NO | 0 hạch | |
| N1 | 1 hạch | a: di căn vi thể* |
| b: di căn đại thể** | ||
| N2 | 2 - 3 hạch | a: di căn vi thể* |
| b: di căn đại thể** | ||
| c: không có di căn hạch vùng nhưng có tổn thương vệ tinh | ||
| N3 | > 4 hạch hoặc hạch dính nhau, hoặc có tổn thương vệ tinh kèm theo di căn hạch vùng | |
| M | Di căn xa | LDH huyết thanh |
| MO | Chưa di căn xa | |
| M1a | Di căn xa ở da, lớp dưới da, hoặc di căn hạch | Bình thường |
| M1b | Di căn phổi | Bình thường |
| M1c | Di căn cơ quan nội tạng khác ngoài phổi | Bình thường |
| Di căn xa vị trí bất kỳ | Tăng | |
| *di căn hạch được xác định sau khi sinh thiết hạch gác hoặc vét hạch vùng **di căn hạch sờ được hạch to trên lâm sàng và được khẳng định lại bằng sinh thiết hạch | ||
| Phân loại giai đoạn lâm sàng | Phân loại giai đoạn mô bệnh học | ||||||
| 0 | Tis | NO | MO | 0 | Tis | NO | MO |
| IA | T1a | NO | MO | IA | T1a | NO | MO |
| IB | T1b, T2a | NO | MO | IB | T1b, T2a | NO | MO |
| IIA | T2b, T3a | NO | MO | IIA | T2b, T3a | NO | MO |
| IIB | T3b, T4a | NO | MO | IIB | T3b, T4a | NO | MO |
| IIC | T4b | NO | MO | IIC | T4b | NO | MO |
| III | T bất kỳ | N>0 | MO | IIIA | T1 - 4a | N1a, N2a | MO |
| IIIB | T1 - 4b | N1a, N2a | MO | ||||
| T1 - 4a | N1b, N2b, N2c | MO | |||||
| NIC | T1 - 4b | N1b, N2b, N2c | MO | ||||
| T bất kỳ | N3 | MO | |||||
| IV | T bất kỳ | N bất kỳ | M1 | IV | T bất kỳ | N bất kỳ | M1 |
8.6 Chẩn đoán phân biệt
| Dựa vào tình trạng tăng sắc tố | Dựa vào vị trí phân bố cuả tổn thương |
Tăng sắc tố màu đen Không tăng sắc tố màu đen (hồng, đỏ) | Ung thư hắc tố thể Dubreuilh Ung thư hắc tố móng Ung thư hắc tố niêm mạc Ung thư hắc tố thể đầu cực |
8.7 Điều trị
Ung thư tế bào hắc tố có thể được chữa khỏi nếu được chẩn đoán và điều trị khi khối u còn nông và vẫn chưa xâm lấn sâu vào da. Nếu u hắc tố không được cắt bỏ ở giai đoạn sớm, tế bào ung thư có thể phát triển từ bề mặt da sâu xuống dưới, xâm lấn vào mô lành. Khi u hắc tố trở nên dày và sâu, bệnh thường lan sang các bộ phận khác của cơ thể và khó kiếm soát.
8.8 Phẫu thuật
Phẫu thuật để cắt bỏ u hắc tố là phương pháp điều trị chính cho loại ung thư này. cần phải cắt bỏ không chỉ có khối u mà còn phải cắt cả một phần mô lành xung quanh nó đế giảm khả năng tế bào ung thư còn sót lại xuống mức thấp nhất. Độ rộng và chiều sâu của lớp da xung quanh cần phải cắt bỏ phụ thuộc vào độ sâu của khối u xâm nhập vào da. Giới hạn của đường rạch cách bờ tổn thương dựa vào chỉ số Breslow:
- Chỉ số Breslow < lmm thì đường rạch da cách bờ tổn thương lcm.
- Chỉ so Breslow > 1mm và < 2 thì đường rạch da cách bờ tổn thương 2cm.
- Chỉ số Breslow > 2mm thì đường rạch da cách bờ tổn thương 3 cm.
Nạo vét hạch: đối với các tổn thương có chỉ số Breslow trên 10mm thì nên nạo vét hạch. Phẫu thuật hạch gác (phẫu thuật hạch chọn lọc) cho phép lấy hạch chọn lọc đế làm tổ chức học để đánh giá sự di căn đầu tiên đến hạch gác. Chất chỉ thị màu hoặc chất có gắn phóng xạ được tiêm vào tổn thương ở da, sau đó dựa vào sự hiện diện của chất chỉ thị màu hay chất gắn phóng xạ tại các hạch vùng để cắt bỏ chọn lọc những hạch đó và làm giải phẫu bệnh.
Sau phẫu thuật cắt bỏ, bệnh nhân cần được theo dõi 3 tháng một lần trong 3 đến 5 năm. cần lưu ý hiện tượng tái phát tại chỗ hay di căn hạch và cơ quan khác, đặc biệt ở phối và não.
Nói chung phương pháp phẫu thuật không còn hiệu quả đối với ung thư tế bào hắc tố đã di căn. Trong những trường hợp này, bác sĩ có thể sử dụng các phương pháp khác như hóa trị liệu, liệu pháp sinh học, xạ trị hoặc phối hợp các phương pháp.
8.8.1 Xạ trị
Xạ trị được chỉ định trong những trường hợp có di căn hoặc không có chỉ định phẫu thuật. Khoảng 50% hạch di căn hay u ở tổ chức phần mềm có đáp ứng tốt với xạ trị. Tuy nhiên, chỉ có 30% các u di căn ở não đáp ứng tốt với xạ trị. Điều trị xạ trị liều thấp kết hợp với cor-ticosteroid liều thấp có tác dụng tốt để giảm đau đối với những ung thư đã di căn ở não, xương.
8.8.2 Điều trị hóa chất
Có nhiều hóa chất có tác dụng trong điều trị ung thư tế bào hắc tố; bao gồm dacar-bazin, carmustin, lomustin, cisplatin, te-mozolomid và Vincristin, tất cả đều dung nạp tương đối tốt và có tỷ lệ đáp ứng từ 15 đến 20%. Tùy theo từng bệnh nhân, có thể dùng đơn hóa trị liệu hay phối hợp nhiều thuốc để điều trị. Đơn hóa trị dùng dacarbazin với liều 700 mg/m²/ngày trong thời gian 1 đến 5 ngày, sau đó ngừng điều trị. Tháng tiếp theo lặp lại như vậy. Ngoài ra có thể sử dụng các thuốc khác như fotemustin với liều 100 mg/m² vào các ngày 1,8, 15, 50; sau đó 3 tuần tiêm một lần. Với những bệnh nhân có di căn, một số phác đồ đa hóa trị đã được thử nghiệm như phác đồ Dart-mouth - là sự kết hợp 4 thuốc dacarba-zin, cisplatin, carmustin và Tamoxifen. Sự kết hợp này đã được báo cáo với tỷ lệ đáp ứng điều trị cao hơn so với kết quả điều trị một loại thuốc duy nhất hoặc kết hợp một vài loại thuốc thử nghiệm trước đó. Đối với những bệnh nhân không thể dùng cisplatin vì tình trạng thận của họ hoặc vì lý do khác thì có thể thay phác đồ gồm dacarbazin, vincristin, bleomycin, carmustin và interferon alpha cho thấy kết quả đầy hứa hẹn.
8.8.3 Điều trị miễn dịch
Interferon alpha có tác dụng ức chế sự tăng trưởng của tế bào hắc tố ác tính và cũng có tác dụng miễn dịch. Tỷ lệ đáp ứng trong khối u ác tính là 15 - 20%. Interferon alpha - 2b đã được sử dụng với liều 3 triệu đơn vị tiêm dưới da, 3 lần trong một tuần, trong thời gian 18 tháng, cho kết quả khả quan.
Ipilimumab là kháng thể đơn dòng gắn với tế bào lympho T độc có liên quan antigen 4 (CTLA-4), ức chế CTLA-4 với CD80 và CD86, từ đó làm tăng đáp ứng của tế bào T chống lại tế bào ung thư. Pembrolizumab cũng là kháng thể đơn dòng gắn kết với PD-1 (là một loại protein trên tế bào T). Khi pembroli-zumab gắn với các ptotein này, làm cho các protein do các tế bào ung thư tiết ra không còn tác động đến các tế bào T, cho phép các tế bào T phát huy tác dụng miễn dịch. Từ năm 2014, pembrolizumab đã được FDA cho phép sử dụng để điều trị ung thư tế bào hắc tố ở Mỹ.
Vaccin tiêm phòng ung thư tế bào hắc tố, phương pháp điều trị nhắm đích bằng kháng thể đơn dòng, liệu pháp tế bào nuôi hay liệu pháp gen hiện nay vẫn đang trong giai đoạn thử nghiệm.
8.9 Các yếu tố tiên lượng trong ung thư tế bào hắc tố
| Yếu tố chính tiên lượng trong ung thư tế bào hắc tố | |
| Yếu tố tiên lượng | Ý nghĩa |
| Độ dày của khối u | < 1mm -> nguy cơ thấp; > 1mm -> nguy cơ cao |
| Loét | Có loét nguy cơ cao (trên lâm sàng hoặc trên mô bệnh học) |
| Tỷ lệ nhân chia | > 1 nhân chia/mm2 -> nguy cơ cao |
| Tuổi | Tuổi càng cao tiên lượng càng kém |
| Giới | Nam giới tiên lượng kém hơn |
| Vị trí tổn thương | Tổn thuwong vùng thân mình, đầu và cổ tiên lượng kém hơn tổn thương ở chi |
| Số hạch di căn | Tiên lượng kém khi có hoặc 1; 2 - 3 và > 4 hạch di căn |
| Tình trạng di căn hạch | Di căn hạch sờ được trên lâm sàng tiên lượng kém hơn là di căn trên mô bệnh học không sờ được trên lâm sàng |
| Di căn xa | Di căn tạng hoặc di căn xa không phải tạng (da, dưới da, hạch xa) đều có tiên lượng kém. |

Chỉ số Breslow và thang Clark đánh giá mức độ xâm lấn của khối u trên mô bệnh học cũng thường được sử dụng để tiên lượng bệnh, mức độ xâm lấn của khối u càng sâu thì tiên lượng càng kém. Dưới đây là tỷ lệ sống trên 10 năm của bệnh nhân ung thư tế bào hắc tố ước tính theo chỉ số Breslow và thang Clark trên mô bệnh học.
9 Bệnh Paget (Paget’s disease)
9.1 Đại cương
Paget là một bệnh ung thư biểu mô tuyến, liên quan đến tuyến appocrin và gặp ở người trên 50 tuổi. Bệnh gồm hai loại là Paget vú và Paget ngoài vú.
Bệnh Paget vú gặp ở nữ giới, tuổi hay gặp 50 - 60 tuổi, chiếm khoảng 1 - 3% các ung thư vú.
Bệnh Paget ngoài vú hiếm gặp hon, thường gặp ở âm hộ, quanh hậu môn, bìu và sinh dục. Tuổi thường gặp từ 60 - 80 tuổi.
9.2 Lâm sàng
Thương tổn da của Paget vú là dát, mảng đỏ ở trên hoặc xung quanh núm vú một bên, tổn thương ranh giới rõ, trên có vảy, gây đau, rát, chảy dịch, máu, có thể loét hoặc làm tụt núm vú. Bệnh thường dễ chẩn đoán nhầm với các viêm da khác.
Với Paget ngoài vú, thương tổn cơ bản cũng giống với Paget vú, hay gặp ở vùng giàu tuyến appocrin như sinh dục, nách, hậu môn, bìu. Có thể có hiện tượng tăng, giảm sắc tố. Paget ngoài vú được chia thành hai loại: paget ngoài vú tiên phát và thứ phát, phụ thuộc vào nguồn gốc tế bào. Paget ngoài vú tiên phát có nguồn gốc từ thượng bì còn paget ngoài vú thứ phát có nguồn gốc từ ung thư biểu mô tuyến di căn tới da.
Khám các bộ phận khác có thể phát hiện khối u ở đại tràng, khối u vú, hạch nách, hạch bẹn to.
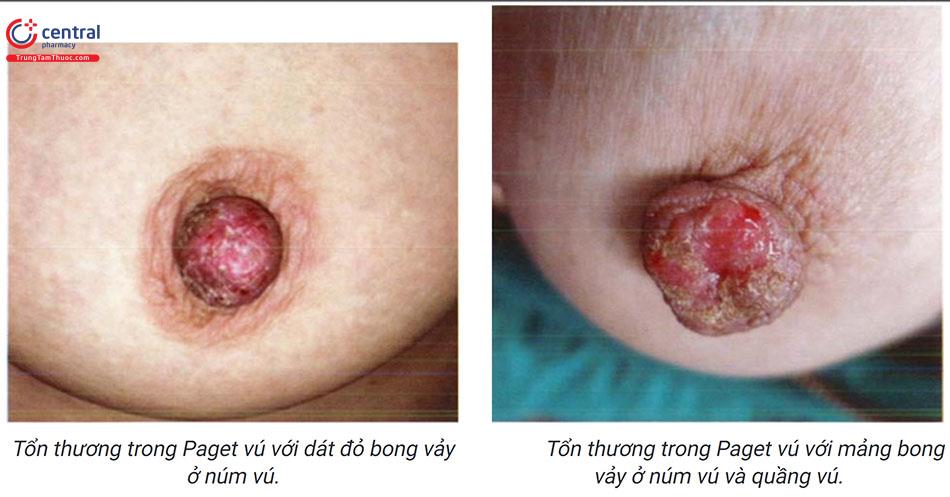
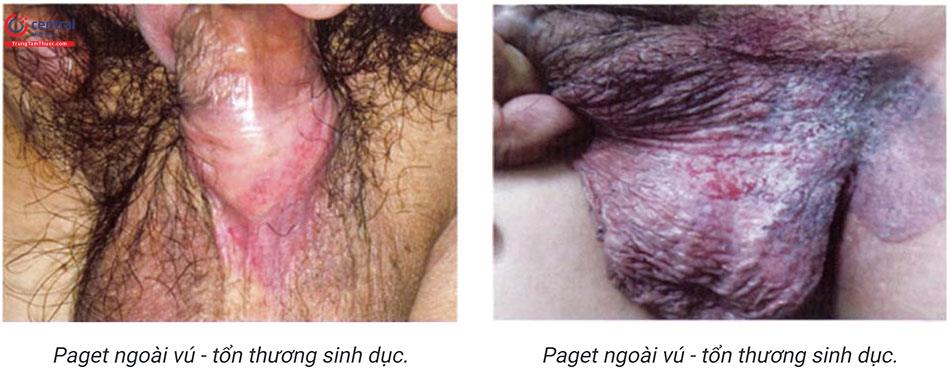
9.3 Cận lâm sàng
Sinh thiết với nhuộm HE, PAS: các tế bào Paget với nhân rộng chiếm ưu thế, bào tương nhạt màu, không có cầu nổi liên tế bào, có thể đứng đơn độc hoặc thành nhóm. Các tế bào này xâm lấn hết thượng bì, có thể vào cả nang lông và ống tuyến mồ hôi. Có hiện tượng ly gai, dầy sừng và á sừng.
Hóa mô miễn dịch: CK7 và anti-cytoker-atin (CAM 5,2) là các dấu ấn nhạy trong cả Paget vú và ngoài vú. CK20 dương tính trong các trường hợp Paget ngoài vú thứ phát. Các dấu ấn khác để chẩn đoán phân biệt như EMA, S100, Melan-A (MART-1), HMB-45...
Các xét nghiệm khác nhằm tìm các khối u nội tạng: chụp Mammo vú, MRI vú, nội soi đại tràng, soi bàng quang, chụp tiết niệu cản quang, X quang phổi. Chụp PET-CT có tác dụng trong tầm soát di căn.
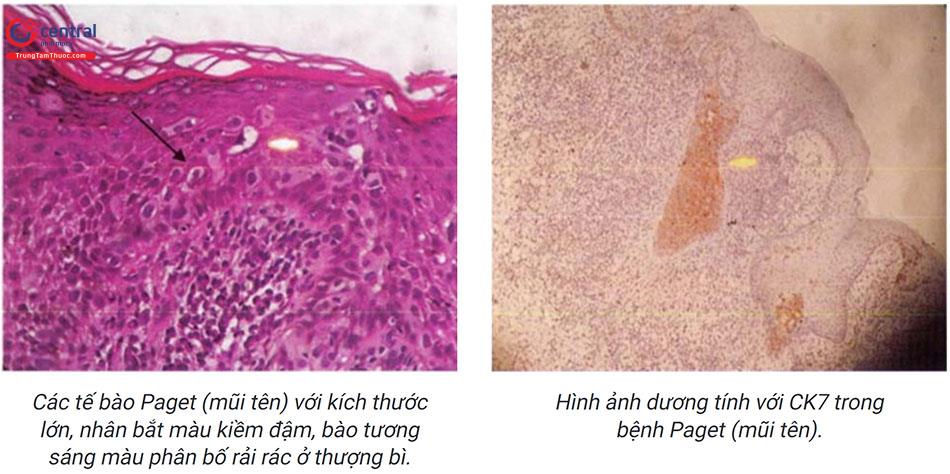
9.4 Chẩn đoán xác định
Dựa vào lâm sàng và mô bệnh học, trong đó quan trọng là hóa mô miễn dịch để khẳng định nguồn gốc tế bào.
9.5 Chẩn đoán phân biệt
Paget vú: cần phân biệt với chàm vú, vảy nến, nấm da, pemphigus, bệnh Bow-en, ung thư biểu mô tế bào đáy...
Paget ngoài vú: cần phân biệt với nấm da, vảy nến, viêm da dầu, chàm đồng xu, pemphigus, lichen phẳng, lichen đơn mạn tính, dị ứng thuốc, bệnh Bowen, hồng sản Queyrat...
9.6 Điều trị
Lựa chọn số 1: phẫu thuật
- Cắt rộng cách bờ tổn thương 2cm và chiều sâu 0,5cm hoặc phẫu thuật Mohs: làm giảm tỷ lệ tái phát của bệnh.
- Với Paget vú, nếu phát hiện khối u vú (trên lâm sàng hoặc chẩn đoán hình ảnh): cắt vú, nạo vét hạch nách và tia xạ.
- Với Paget ngoài vú, trường hợp có liên quan tới các khối u sâu: phẫu thuật triệt để có/không kết hợp xạ trị.
Các phương pháp khác: lựa chọn thay thế hoặc kết hợp với phẫu thuật
- Xạ trị: dùng khi không có khả năng phẫu thuật hoặc ảnh hưởng đến chức năng nếu cắt bỏ rộng. Hỗ trợ điều trị sau phẫu thuật để giảm tỉ lệ di căn.
- Hoá chất bôi tại chỗ: hiệu quả thay đổi tuỳ thuốc và ít tác dụng vì khả năng xâm lấn của khối u. Các thuốc được sử dụng là 5 fluorouracil (5FU), bleomycin, imiquimod.
- Hoá trị toàn thân: trường hợp không có chỉ định xạ trị hoặc phẫu thuật, tác dụng hạn chế.
- Quang động liệu pháp: có hiệu quả nhất định, giúp giảm tỉ lệ tái phát hoặc những trường hợp khó khăn khi phẫu thuật rộng và nguy cơ tái phát cao.
10 U sùi dạng nấm (Mycosis fungoides)
10.1 Đại cương
U lympho T da là một bệnh u lympho không Hodgkin có tăng sinh các tế bào lympho T, là thể hay gặp nhất của u lym-pho tại da (80%). Trong đó, mycosis fun-goides (MF) là thể hay gặp nhất.
Bệnh thường tiến triển nhiều giai đoạn, biểu hiện đa dạng về lâm sàng, mô bệnh học, vì vậy chẩn đoán khó ở giai đoạn đầu. Tên bệnh là u sùi dạng nấm bởi tổn thương có hình ảnh giống nấm da trên lâm sàng.
Trên thế giới u lympho T tăng ở những người có nhiễm HTLV-1 (Human T-cell lymphotrophic virus type 1) như ở các vùng Nhật Bản, Caribe, Nam Mỹ... Bệnh thường gặp ở tuổi trung niên và người già. Tỉ lệ nam giới gấp đôi nữ giới.
10.2 Lâm sàng
MF là thể hay gặp nhất trong u lym-pho T với lứa tuổi thường gặp 50 - 60 tuổi. Tùy từng giai đoạn mà có những biểu hiện da khác nhau như dát, mảng thâm nhiễm hay các khối u. Trên một bệnh nhân có thể có cùng lúc nhiều loại tổn thương ở các giai đoạn khác nhau.
10.2.1 Giai đoạn đám (patch stage)
Thương tổn cơ bản là một hoặc nhiều đám màu đỏ trên có vảy da mỏng, kích thước đa dạng, ranh giới rõ. Ở người da sẫm màu tổn thương có xu hướng tăng hoặc giảm sắc tố. Vị trí thường ở vùng kín như phần dưới của bụng, mông, đùi.
Thương tổn ngứa nhiều hoặc không có triệu chứng, tồn tại nhất thời, có thể thuyên giảm tự nhiên mà không để lại sẹo. Đa số sau nhiều năm tiến triển thành giai đoạn mảng.
Chẩn đoán ở giai đoạn này thường khó khăn và có thể nhầm với một số bệnh da mạn tính khác, do đó với các thương tổn da mạn tính nhưng không đáp ứng với điều trị thông thường cần được sinh thiết làm mô bệnh học nhiều lần để khẳng định chẩn đoán.
Mô bệnh học có hình ảnh thâm nhiễm các tế bào lympho không điển hình xung quanh mạch, phần phụ và hướng thượng bì. Không thấy hình ảnh xốp bào là đặc điểm quan trọng để phân biệt với chàm ở giai đoạn này.
10.2.2 Giai đoạn mảng (plaque stage)
Thông thường giai đoạn mảng xuất hiện từ tổn thương đám sau nhiều tháng, nhiều năm, đôi khi tổn thương mảng cũng có thể xuất hiện ngay từ đầu.
Tổn thương cơ bản giống nấm: các mảng hình nhẫn hoặc hình rắn bò màu đỏ, ranh giới rõ với da lành, bờ không đều, lành ở giữa ở bờ nổi cao, bong vảy mỏng ở rìa hoặc trên tổn thương. Tổn thương thường ở vùng da kín như thân mình, mông, gốc chi. Nếu tổn thương xuất hiện trên da đầu có thể thấy hình ảnh rụng tóc.
Mô bệnh học ở giai đoạn này điển hình với thâm nhiễm dày đặc các tế bào lym-pho ác tính ở thượng bì và dưới thượng bì. Hiện tượng hướng thượng bì rõ ràng hơn với vi áp-xe Pautrier.
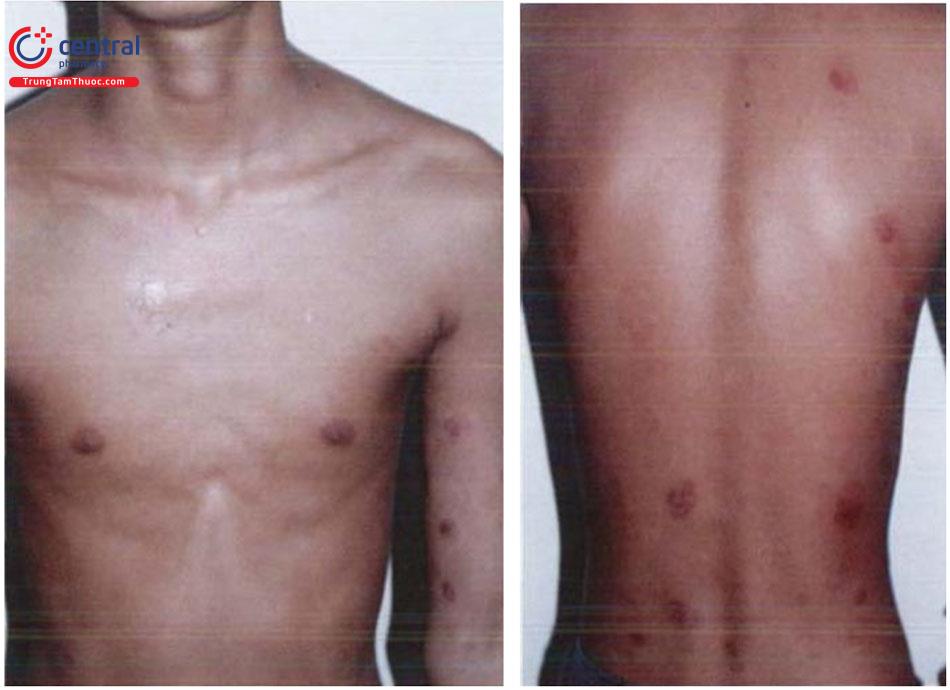
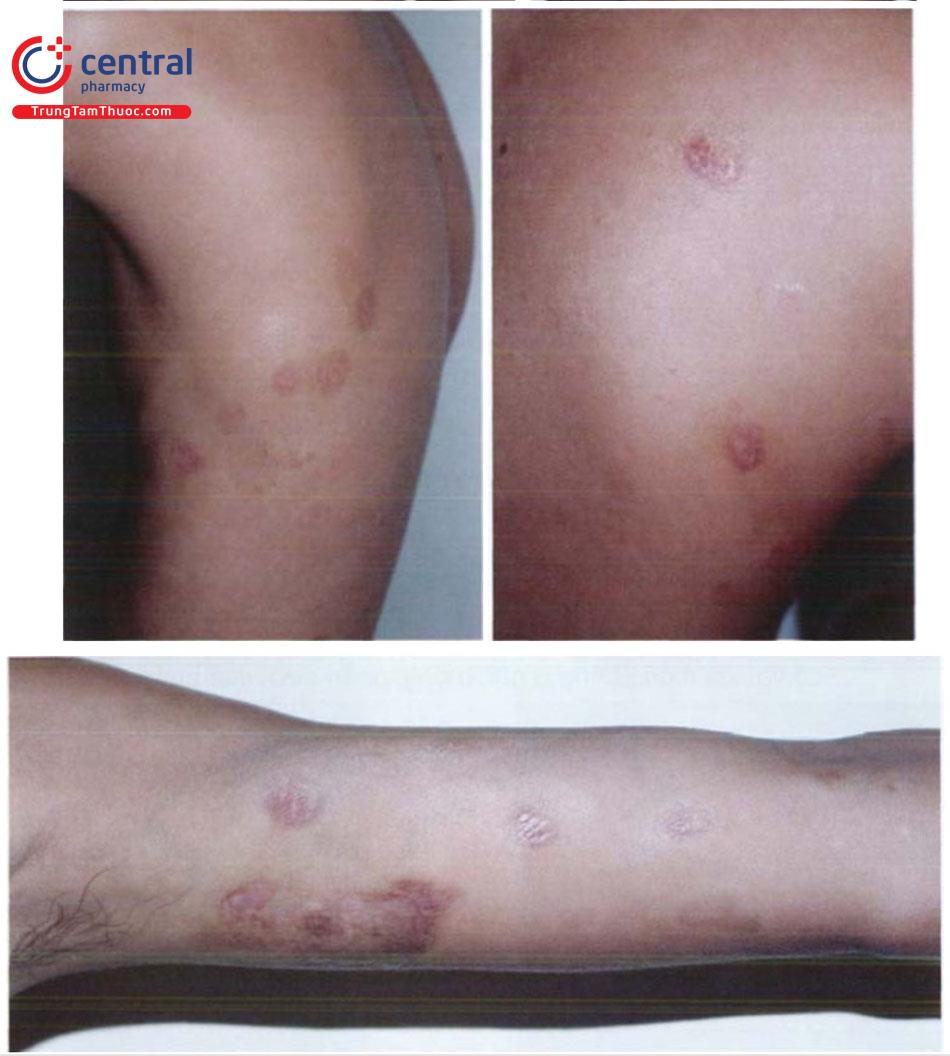
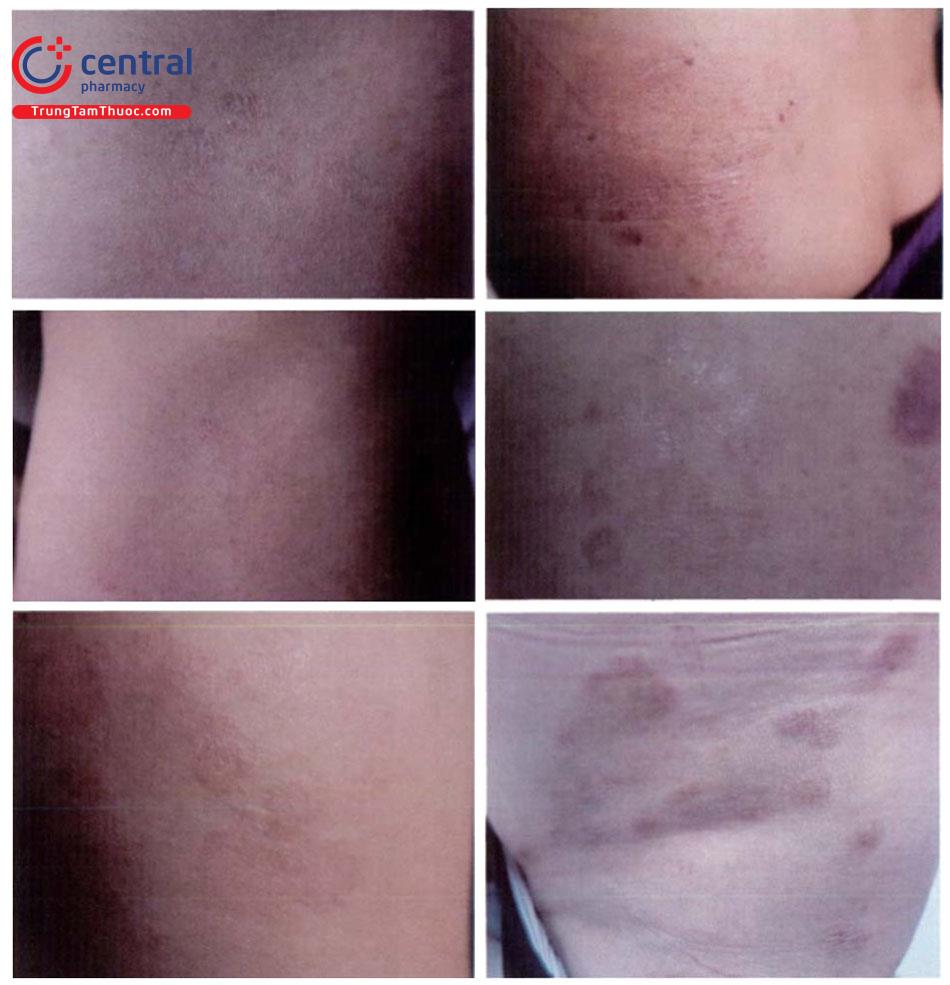
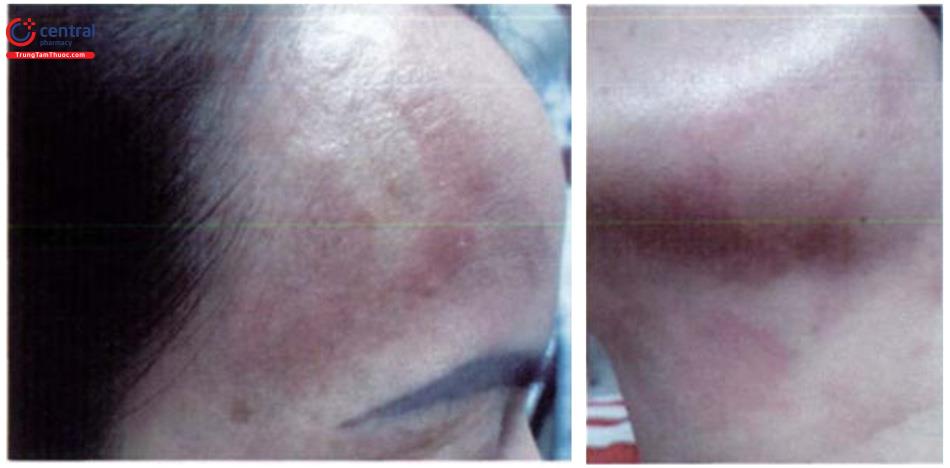
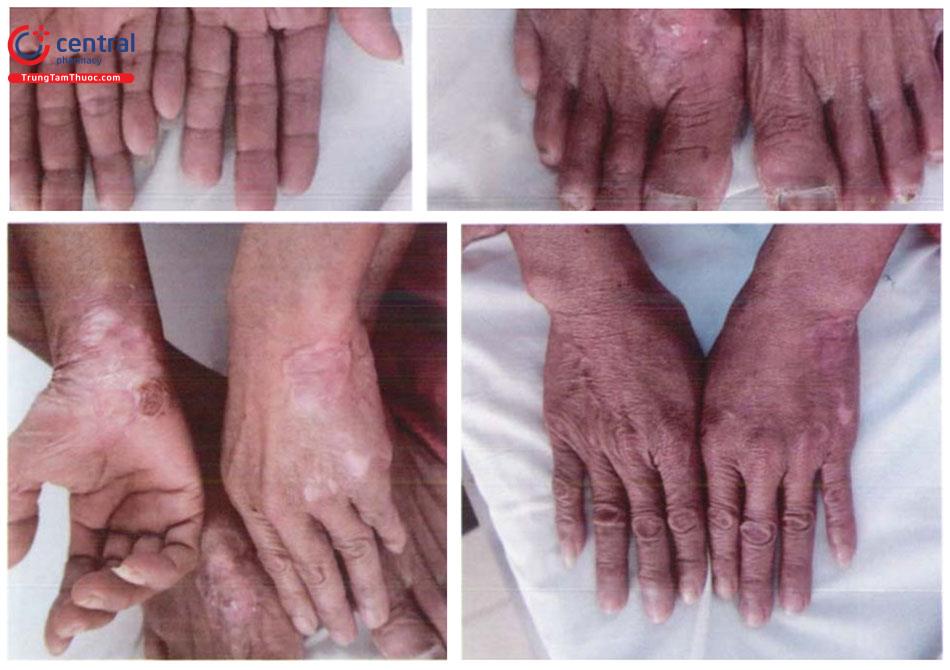
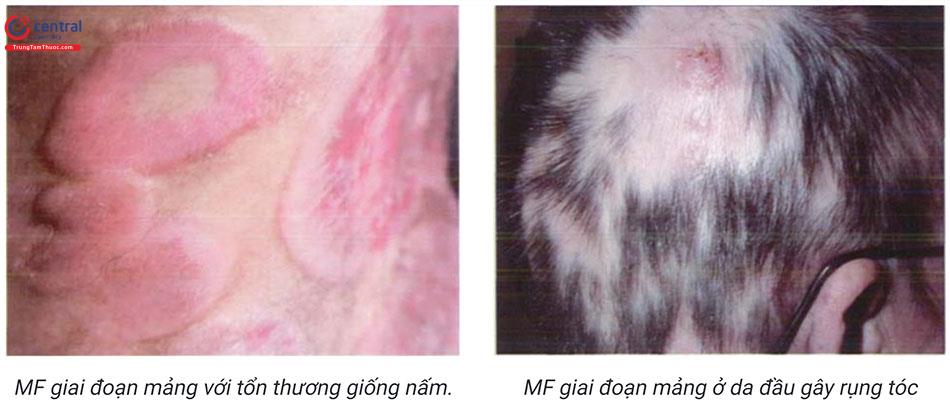
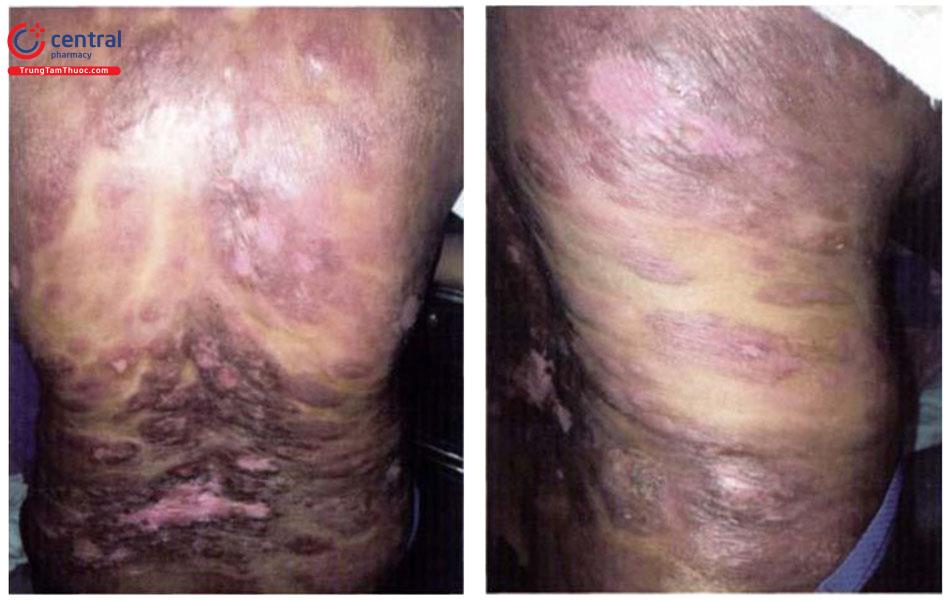
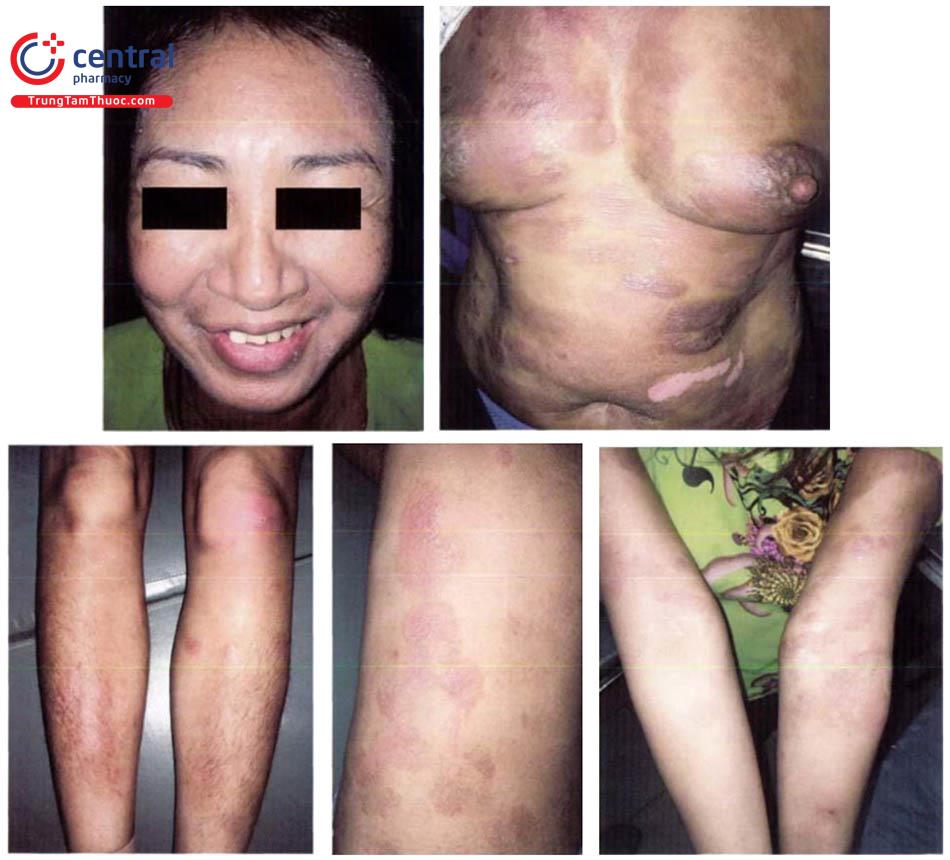
10.2.3 Giai đoạn u (tumor stage)
Giai đoạn u thường xuất hiện trên dát hoặc mảng. Trong trường hợp xuất hiện trên da lành là thương tổn di căn. Các u màu đỏ nâu hoặc đỏ tím bề mặt mềm và thường xuất hiện loét, có thể nhiễm trùng thứ phát. Có thể gặp bất cứ vị trí nào, tuy nhiên thường gặp hơn ở vùng mặt, các nếp gấp lớn như nách, nếp vú.
Mô bệnh học có hình ảnh tăng sinh các tế bào lympho dày đặc ở trung bì sâu, lan tỏa hơn các giai đoạn trước đó, giảm hoặc mất tính chất hướng thượng bì. Các tế bào lympho không điển hình với nhân giãn rộng, hạt nhân lớn và không đều, tăng nhiễm sắc.
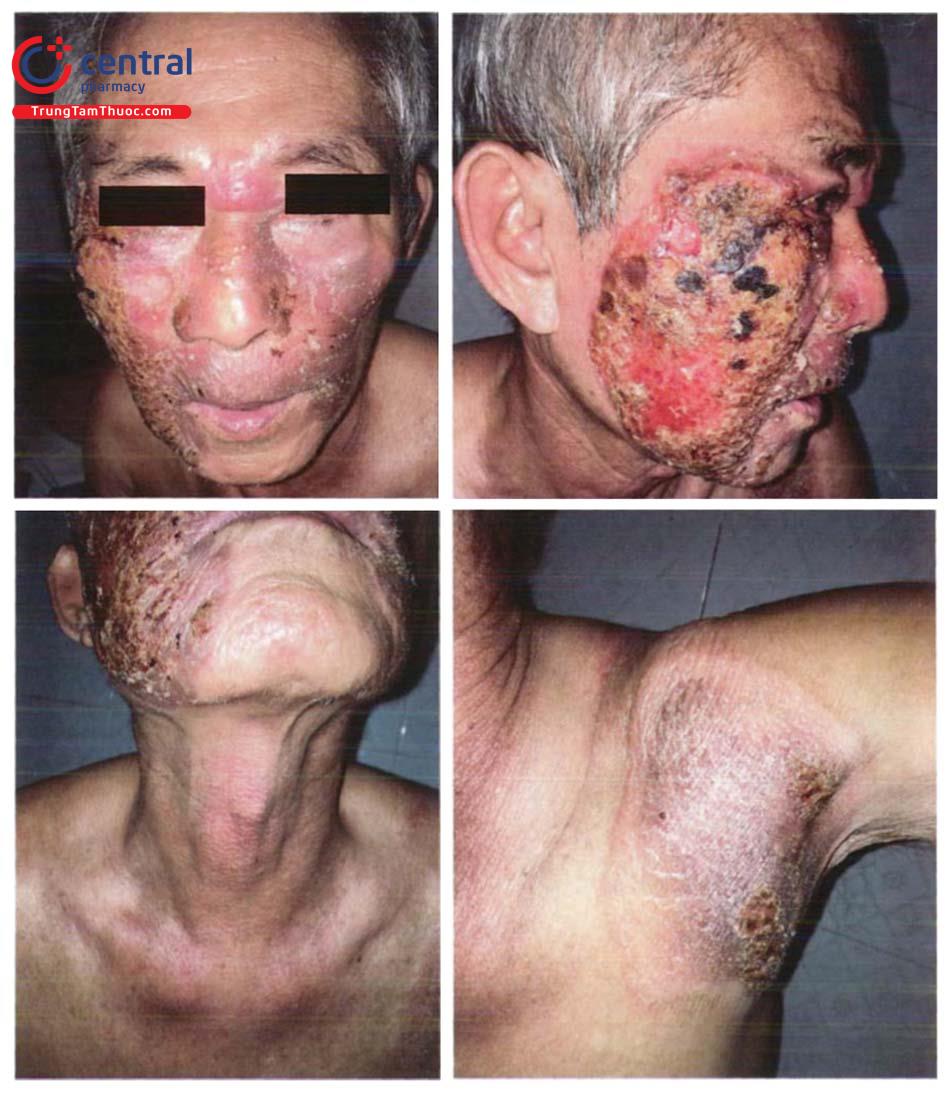
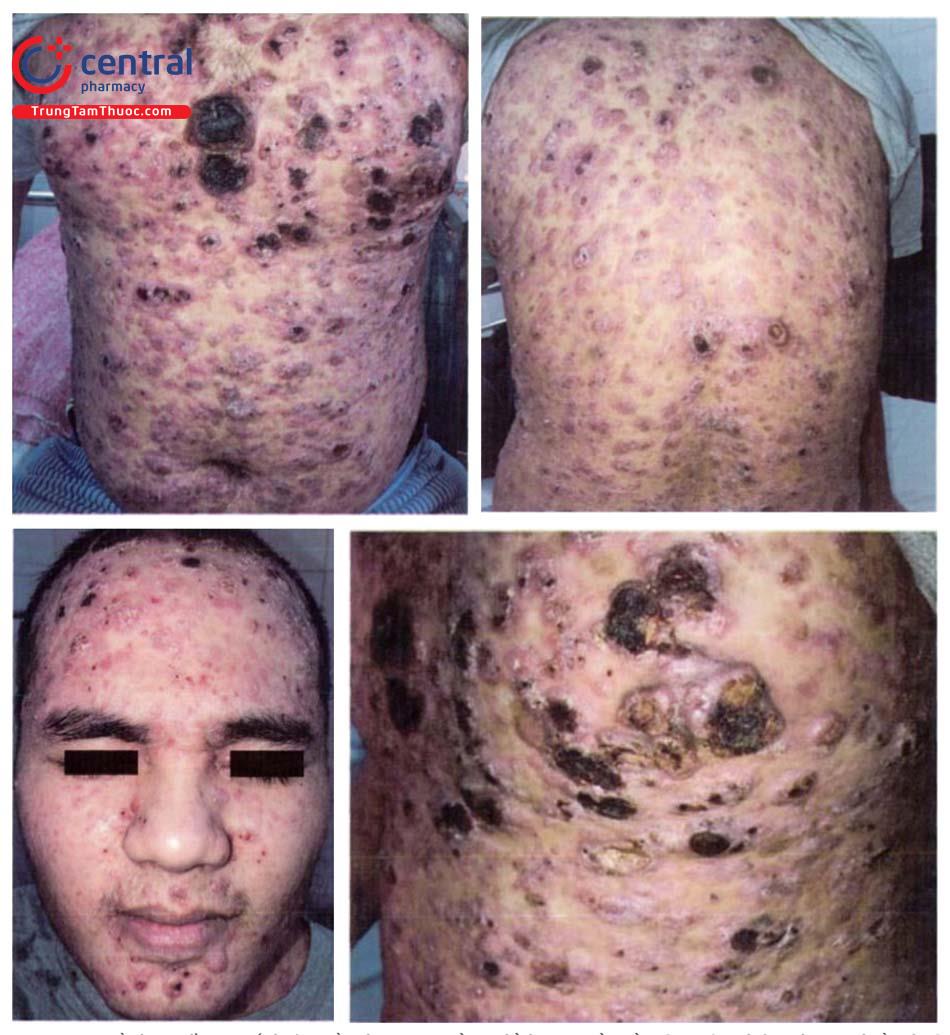
10.2.4 Đỏ da toàn thân do u sùi dạng nấm
Đỏ da toàn thân có thể phát triển ngay từ đầu hoặc từ những bệnh nhân bị u sùi dạng nấm từ trước. Thương tổn là các mảng đỏ tươi, bong vảy, chiếm phần lớn diện tích cơ thế. Thương tổn thường ở các vùng gấp như bụng, nách, khuỷu tay được gọi là dấu hiệu cái ghế gấp.
Một số triệu chứng khác có thể gặp như sốt, mệt mỏi, giảm cân, loạn dưỡng móng, dày sừng lòng bàn tay, bàn chân, các vết nứt. Ngứa rất nhiều làm bệnh nhân gãi gây ra các vết trợt, xước, chảy dịch và gây mất ngủ.
Mô bệnh học giống với giai đoạn mảng hoặc u.
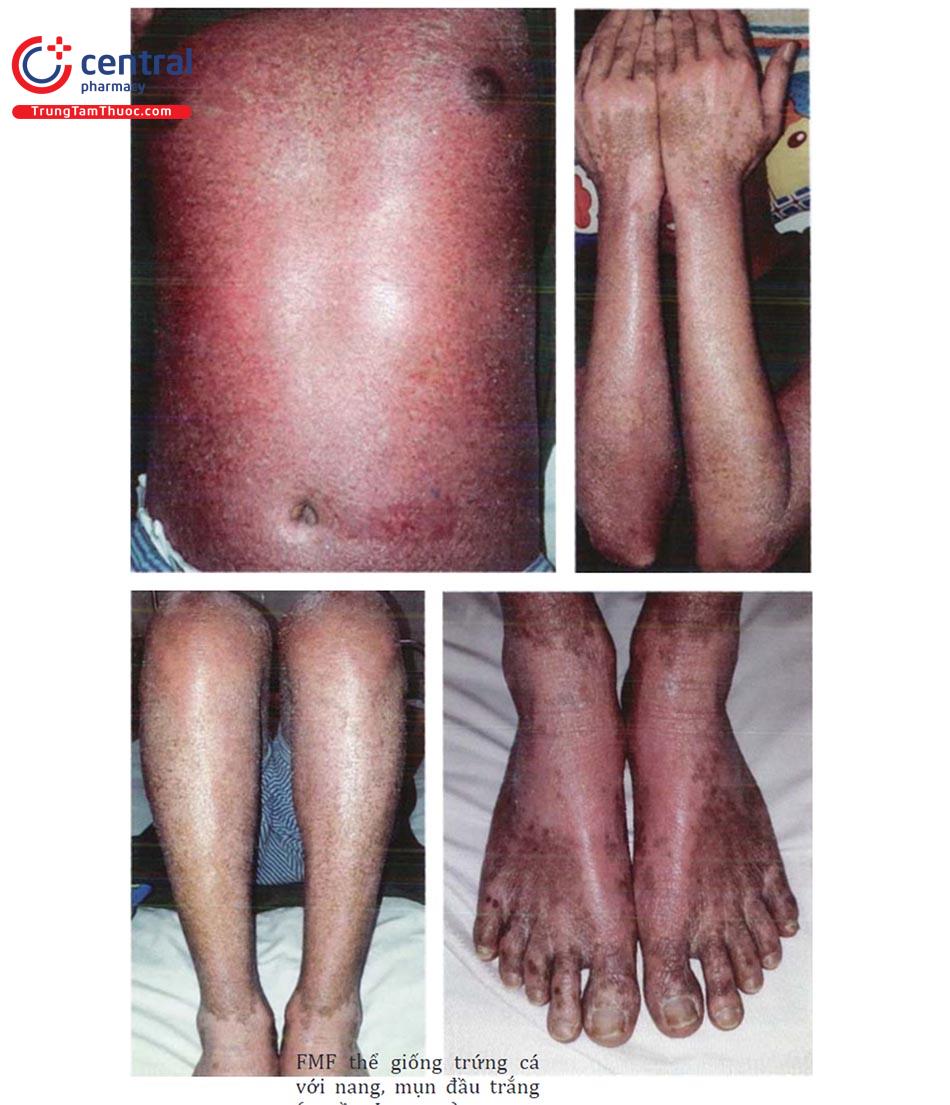
10.2.5 Các dạng khác của u sùi dạng nấm
10.2.5.1 U sùi dạng nấm hướng nang lông (folliculotropic mycosis fungoides, FMF)
Trước kia còn gọi là bệnh mucin nang lông (follicular mucinosis) hoặc rụng tóc mucin (alopecia mucinosa). Hay gặp ở người lớn, ít khi gặp ở trẻ em và thanh thiếu niên.
Thương tổn gồm: sẩn đỏ ở nang lông, dạng trứng cá (nang, mụn nhân), có thể có các u, mảng thâm nhiễm phối hợp với rụng tóc mảng chủ yếu ở đầu và cổ. Thường kèm rụng lông và tóc, nhất là vùng lông mày. cần phân biệt hai FMF giai đoạn sớm hay FMF tiến triển.
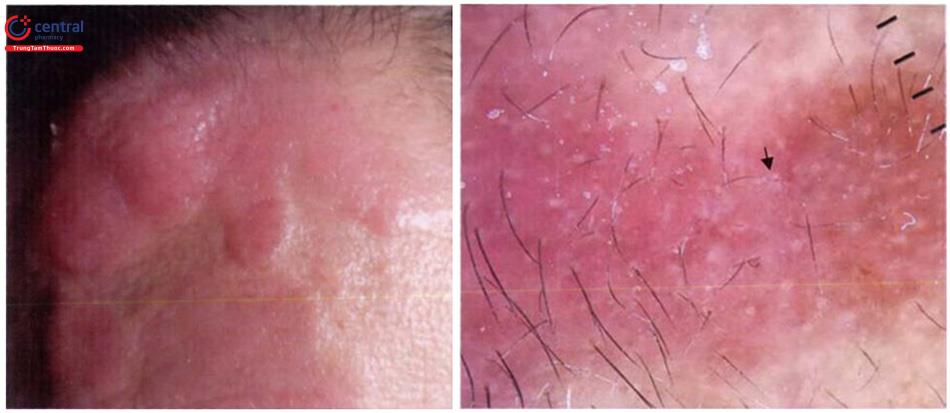
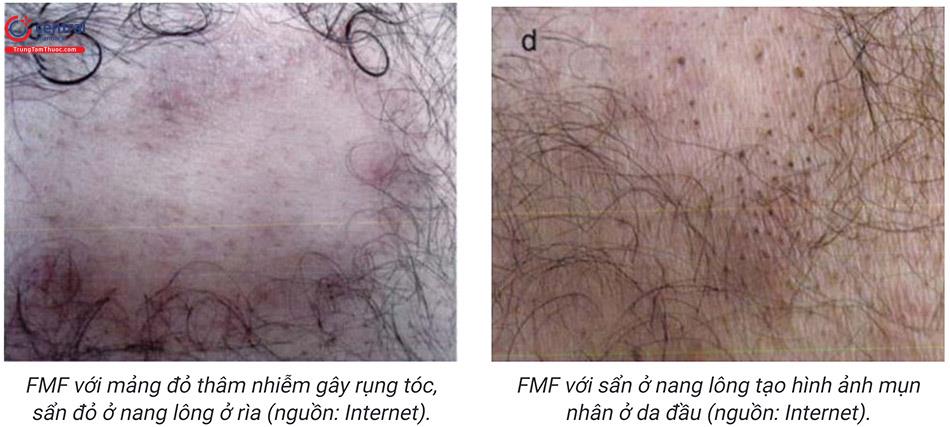
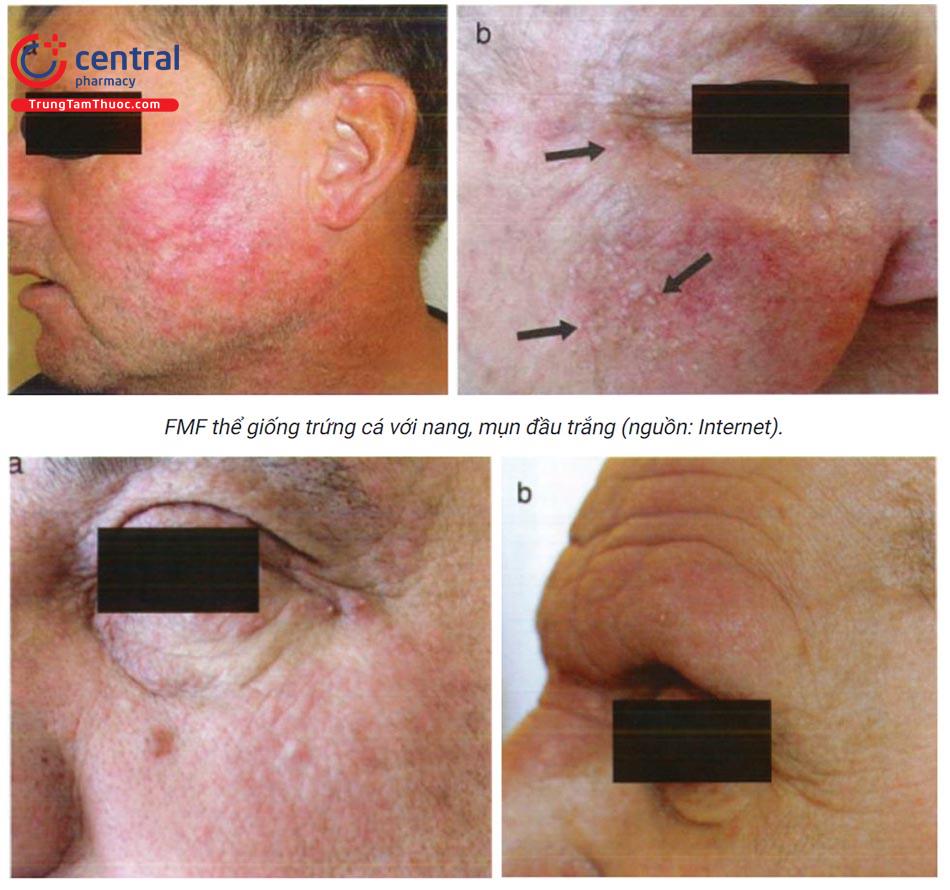
| FMF sớm | FMF tiến triển | |
| Vị trí phân bố | Thân mình, chi, có thể kết hợp tổn thương ở đầu | Đầu cổ là chủ yếu |
| Ngứa | 47% | 80% |
| Mức độ xâm nhập quanh nang lông | Thấp đến trung bình | Trung bình đến dày đặc |
| Độ sâu của thâm nhiễm | 1,77 mm | 3,06 mm |
| Hướng tuyến mồ hôi | 25,6% | 56,3% |
| Bạch cầu ưa acid | 11,3% | 61,5% |
| Tế bào Plasma | 1,9% | 23% |
Tiên lượng của FMF giai đoạn sớm khá tốt với tỉ lệ sống sau 5 năm là 92%, tuy nhiên giai đoạn tiến triển chỉ khoảng 55%. Với giai đoạn sớm có thể đáp ứng tốt với điều trị ít xâm lấn như bôi corti-coid tại chỗ hoặc ánh sáng trị liệu, giai đoạn tiến triển cần phối hợp các phương pháp điều trị toàn thân (tiên lượng đáp ứng kém với điều trị).
10.2.5.2 U lympho dạng Paget (pagetoid reticulosis, PR)
Bệnh còn gọi là bệnh Woringer-Kolopp, thường tiến triển chậm và không thấy thương tổn ở nơi khác ngoài ở da. Tiên lượng bệnh tốt, điều trị khỏi ít tái phát. Các phương pháp điều trị chủ yếu tại chỗ: cắt bỏ, bôi corticoid, bôi nitrogen mustard, imiquimod, ánh sáng, xạ trị...
Thương tổn cơ bản là dát, mảng dạng vảy nến, dày sừng thường khu trú ở các chi. Mô bệnh học đặc trưng với tổn thương hướng thượng bì, có xâm nhập tế bào giống Paget (tế bào lympho với quầng sáng quanh nhân) vì thế có tên gọi là u lympho dạng Paget.

10.2.5.3 U lympho có phản ứng u hạt thừa da (granulomatous slack skin)
Là một thể hiếm gặp của mycosis fun-goid. Thương tổn cơ bản là mảng/dát với da chảy nhão, thường ở vùng hõm nách, khoeo. - Mô bệnh học thấy thâm nhiễm dạng u hạt dày đặc chiếm hết trung bì, các tế bào u loại CD3+, CD4+, CD8+ các tế bào đơn nhân, đại thực bào, các tế bào đa nhân khổng lồ, mất sợi chun.
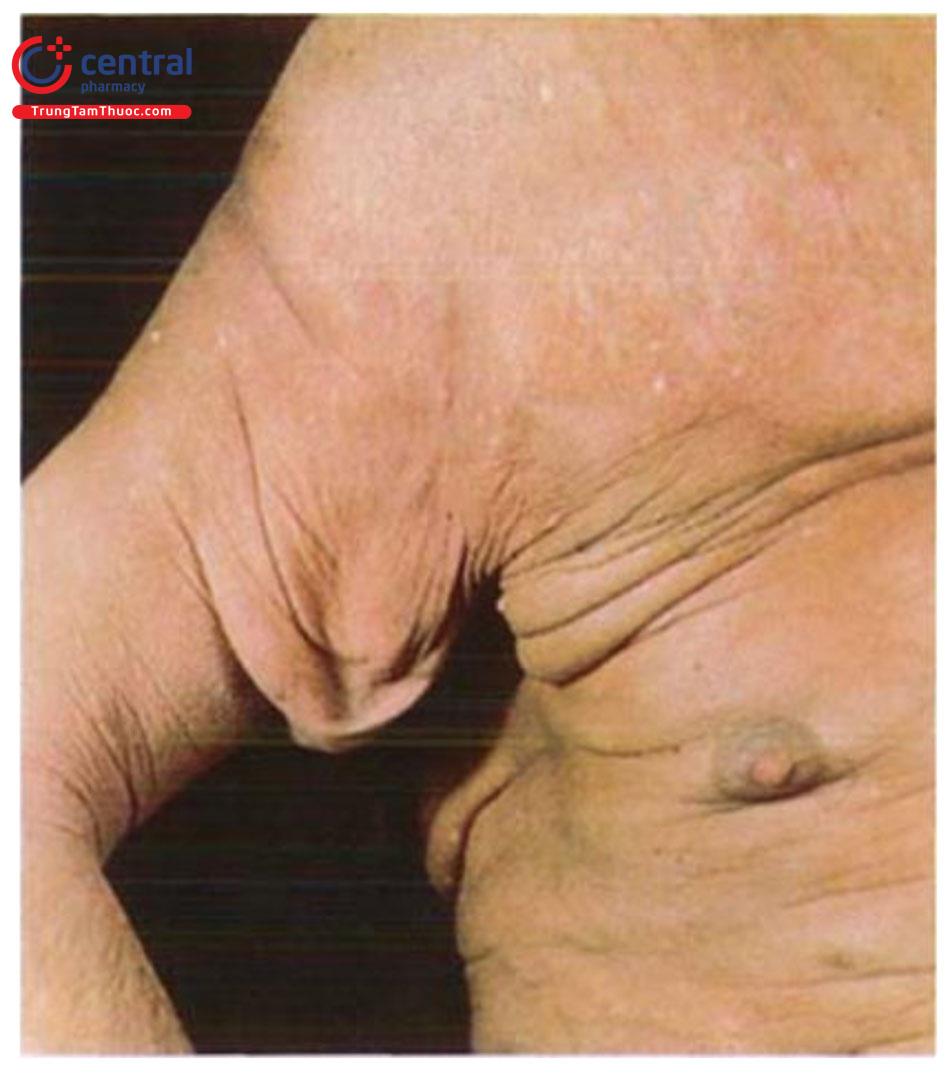
10.2.5.4 U sùi dạng nấm thể giảm sắc tố (hypopigmented MF)
Là một biến thể hiếm gặp của MF giai đoạn dát, đặc trưng bởi sự xâm nhập tế bào lympho T CD8+ ở lớp thượng bì. Thương tổn cơ bản là những dát giảm sắc tố không teo da, vị trí tổn thương thường gặp ở thân mình, mông, chi, ít gặp ở mặt và bàn tay bàn chân.
Thường gặp ở độ tuổi dưới 30, là thể lâm sàng chủ yếu của MF ở trẻ em, tỷ lệ nam/nữ theo các nghiên cứu từ 1,2/1 đến 2,8/1. Biến thể này có tiên lượng tốt hơn MF thông thường, đáp ứng với điều trị tốt, đặc biệt là ánh sáng trị liệu.
Cơ chế giảm sắc tố chưa được hiểu rõ, các tác giả cho rằng sự xâm nhập của tế bào lympho đã ảnh hưởng đến quá trình tạo sắc tố và vận chuyển sắc tố đến tế bào sừng.
Giải phẫu bệnh đặc trưng bởi thâm nhiễm lympho ở lớp thượng bì, nhuộm hóa mô miễn dịch cho thấy giảm bắt màu với CD7 và tăng các tế bào Langerhans CDla+.
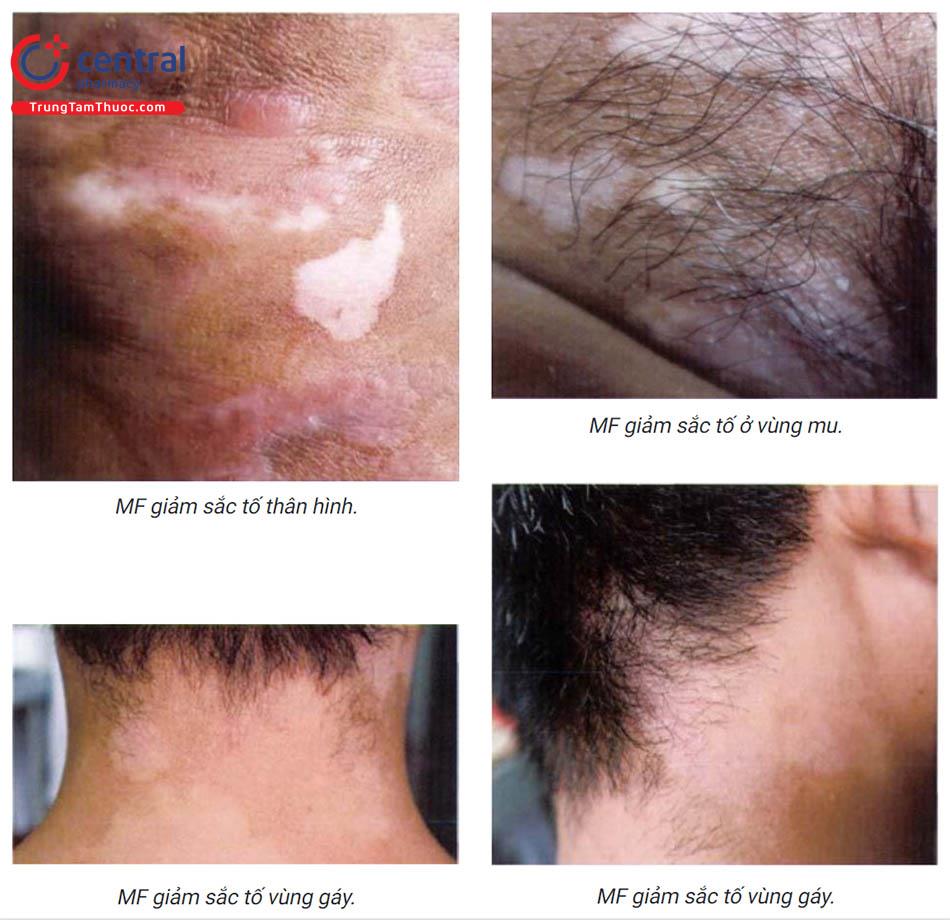
10.2.5.5 MF thể u hạt (granulomatous MF)
Thể u hạt (GMF) là một biến thể mô bệnh học hiếm gặp của MF được xác định bởi sự hiện diện của tổn thương u hạt dạng sarcoid. Thương tổn cơ bản tương tự như MF cổ điển, không có các túi da nhão vùng nếp gấp như u lympho có phản ứng u hạt thừa da.
Mô bệnh học thâm nhiễm lan tỏa tế bào lympho vừa và nhỏ và u hạt dạng sarcoid trên khắp lớp hạ bì.
10.2.5.6 MF thể bọng nước (bullous MF)
Là một biến thể ít gặp của MF, có tiên lượng xấu, đáp ứng với điều trị kém, tỷ lệ tử vong trong năm đầu lên tới 50% trong nghiên cứu của Bowman.
Tổn thương cơ bản là bọng nước, mềm hoặc căng, rải rác thân mình, tay chân, thường xuất hiện sau các tổn thương điển hình của MF. Chúng có thể nằm trên nền tổn thương cũ hoặc vùng da lành.
Mô bệnh học: hình ảnh bọng nước trong hoặc dưới thượng bì kèm theo biểu hiện khác của MF như thâm nhiễm tế bào lympho không điển hình, hướng thượng bì, vi áp-xe Pautrier.
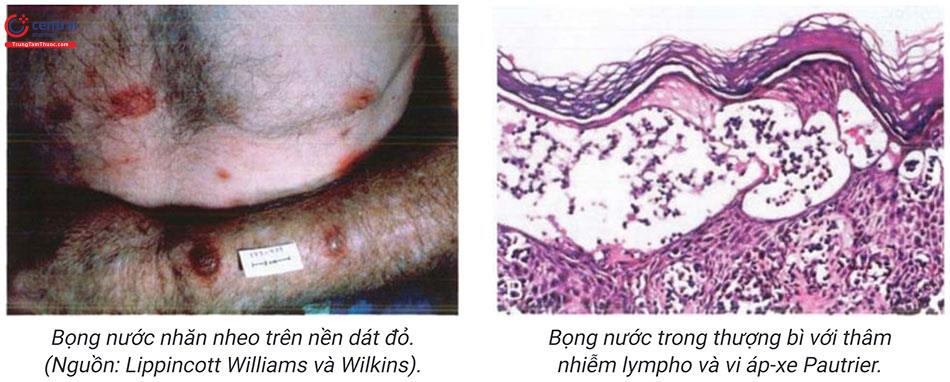
10.2.5.7 MF thể đốm da (poikilodermatous MF)
Là một biến thể của MF, xuất hiện với các mảng lớn màu đỏ đậm hoặc nâu, có vảy da, xen kẽ tăng giảm sắc tố, teo da, giãn mạch dưới da ở các khu vực uốn cong (ngực, mông) và thân mình.
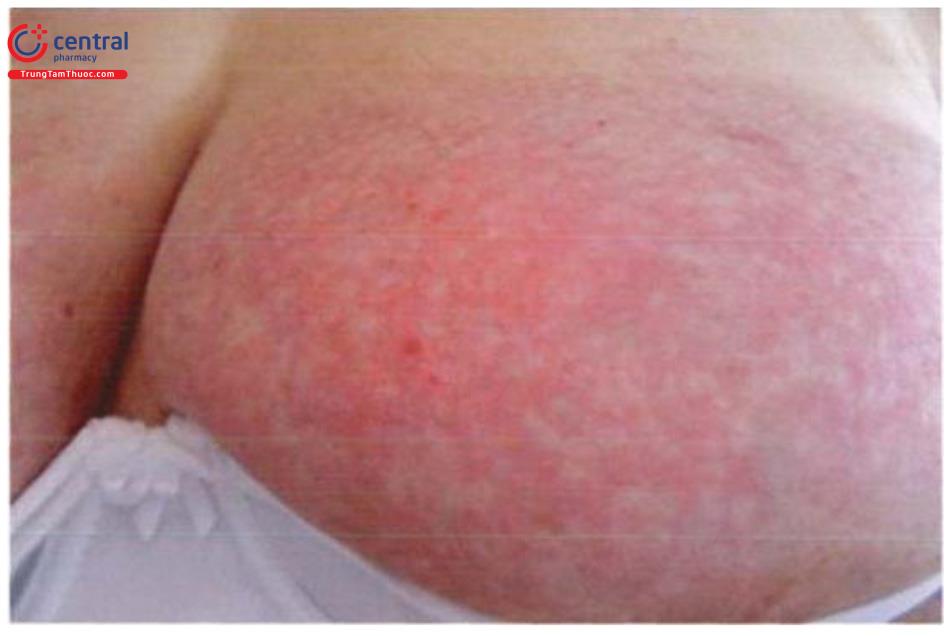
10.2.5.8 MF thể khu trú gan bàn tay, bàn chân (MF palmaris et plantaris)
Biến thể hiếm gặp, trong đó tổn thương MF chỉ giới hạn ở gan bàn tay hoặc gan bàn chân.
Tổn thương cơ bản đa dạng: dát, mảng tăng sắc tố, u, mụn mủ, loét, loạn dưỡng móng. Thường khó xác định và dễ nhầm lẫn với các bệnh khác, cần có mô bệnh học để chẩn đoán. Hình ảnh sinh thiết giống như MF điển hình nhưng chỉ khu trú ở gan bàn tay và gan bàn chân.
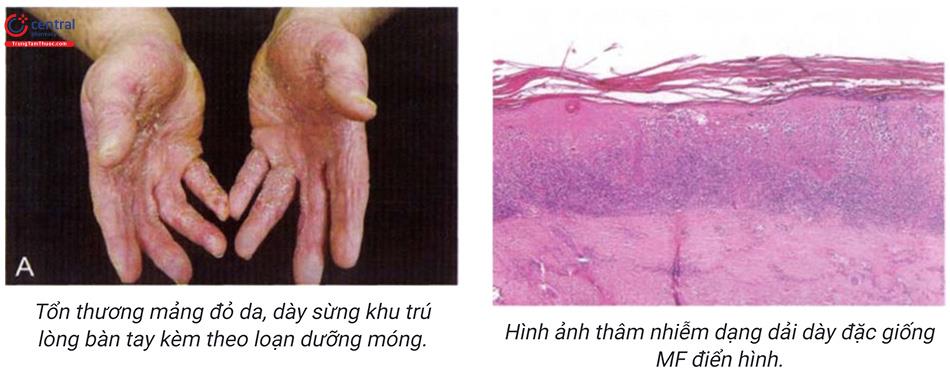
10.2.5.9 MF thể đơn độc
Là một biến thể hiếm gặp của MF, với đặc điểm tổn thương và mô bệnh học giống như MF điển hình nhưng chỉ xuất hiện ở một vị trí duy nhất.
Biến thể này được cho là có tiên lượng tốt.
Ngoài ra, MF còn nhiều biến thể hiếm gặp khác: teo da, thể sẩn, thể mụn mủ, thể hạt cơm...
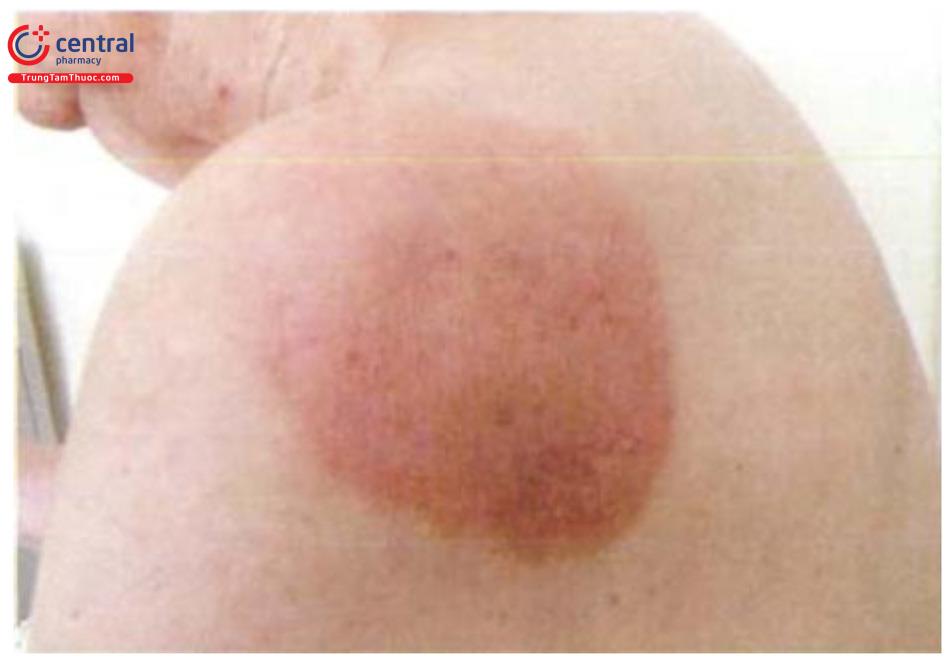
10.3 Mô bệnh học
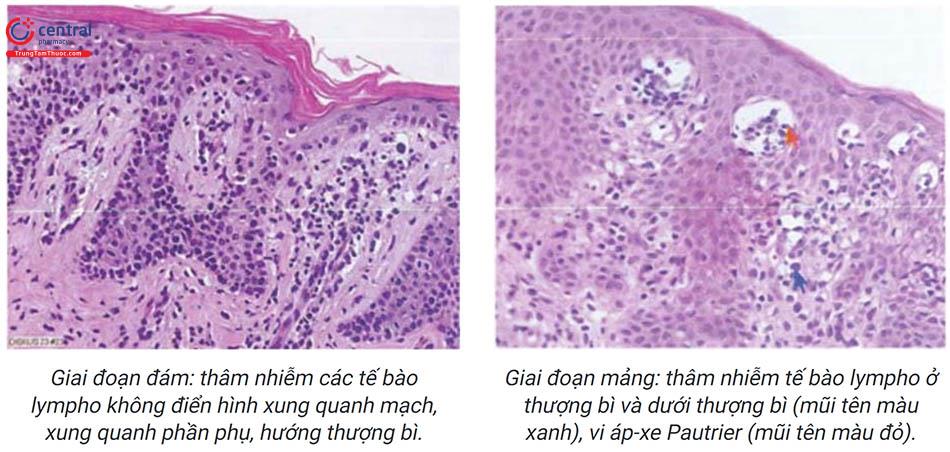
Hóa mô miễn dịch: dương tính với CD2, CD3, CD5, CD7, CD45RO.
Chẩn đoán phân biệt
Tùy vào từng giai đoạn bệnh mà cần phải chẩn đoán phân biệt với các bệnh lý khác nhau: -
Giai đoạn đám/mảng:
- Vảy nến
- Viêm da tiếp xúc mạn tính
- Nấm da
- Chàm
- Viêm da dầu
- Nhiễm mycobacteria không điển hình
- Bệnh phong
- Bệnh leishmania (leishmaniasis)
Giai đoạn u:
Giai đoạn đỏ da toàn thân:
- U lympho B
- Ung thư da
- Bệnh sarcoid (sarcoidosis)
- Vảy phấn đỏ nang lông
- Vảy nến
- Viêm da cơ địa
- Nấm sâu
10.4 Chẩn đoán xác định
10.4.1 Chẩn đoán sớm bệnh MF
Chẩn đoán MF giai đoạn sớm thường khó do triệu chứng lâm sàng và mô bệnh học chưa điển hình, dễ nhầm với các bệnh da khác.
Hiệp hội quốc tế về u lympho da (ISCL) năm 2005 đã đưa ra thang điểm để chẩn đoán MF giai đoạn sớm, dựa trên lâm sàng, mô bệnh học và sinh học di truyền: > 4 điểm dưới đây:
| Tiêu chuẩn | Điểm |
| Lâm sàng Tiêu chuẩn cơ bản: đám/mảng phẳng dai dẳng hoặc tiến triển Yếu tố cộng thêm: + Vị trí không phơi nắng + Kích thước/hình dạng biến đổi + Poikiloderma | - 2 điểm: tiêu chuẩn cơ bản và 2 yếu tố cộng thêm - 1 điểm: tiêu chuẩn cơ bản và 1 yếu tố cộng thêm |
| Mô bệnh học Tiêu chuẩn cơ bản: thâm nhiễm lympho ở lớp nông. Yếu tố cộng thêm: + Có bạch cầu huwosng thượng bì, không có hiện tượng xốp bào (spongiosis) + Tế bào lympho bất thường: nhân to, không đều. | - 2 điểm: tiêu chuẩn cơ bản và 2 yếu tố cộng thêm - 1 điểm: tiêu chuẩn cơ bản và 1 yếu tố cộng thêm |
| Sinh học phân tử Sự sắp xếp lại dòng gen TCR | 1 điểm |
| Hóa mô miễn dịch Dưới 50% tế bào T CD2+, CD3+, và/hoặc CD5+ Dưới 10% tế bào T CD7+ Thượng bì/trung bì không hòa hợp giữa CD2, CD3, CD5 hoặc CD7 | 1 điểm: 1 hoặc nhiều tiêu chuẩn |
10.4.2 Chẩn đoán giai đoạn bệnh theo TNM
Da:
- TI: đám, sẩn hoặc mảng chiếm diện tích < 10% bề mặt da. Chia thành TIa (chỉ có tổn thương đám) và Tlb (mảng ± đám).
- T2: đám hoặc mảng chiếm > 10% bề mặt da. Gồm T2a (chỉ có tổn thương đám) và T2b (mảng ± đám).
- T3: một hoặc nhiều khối u (đường kính > 1cm).
- T4: tổng diện tích tổn thương chiếm > 80% bề mặt cơ thể....
Hạch:
- N0: không có hạch bạch huyết ngoại vi bất thường trên lâm sàng, không yêu cầu sinh thiết.
- N1: lâm sàng có hạch ngoại vi bất thường, mô bệnh học Dutch độ 1. Bao gồm: N1a clone âm tính, N1b clone dương tính.
- N2: lâm sàng hạch ngoại vi bất thường, mô bệnh học Dutch độ 2. Gồm N2a clone âm tính, N2b clone dương tính.
- N3: lâm sàng hạch bạch huyết ngoại vi bất thường, mô bệnh học Dutch độ 3 - 4; nhân bản tích cực hoặc tiêu cực.
- Nx: lâm sàng hạch ngoại vi bất thường, không có xác nhận mô bệnh học.
Tổn thương tạng: MO không có tổn thương cơ quan nội tạng, Ml có tổn thương tạng.
Máu:
- BO < 5% tế bào lympho máu ngoại vi là tế bào không điển hình (tế bào Sezary). Gồm BOa clone âm tính, BOb clone dương tính.
- BI > 5% tế bào lympho máu ngoại biên là các tế bào không điển hình (Sezary) nhưng không đáp ứng tiêu chí của B2. Gồm Bia clone âm tính, Bib clone dương tính.
- B2 > 1000/pl tế bào Sezary với clone dương tính.
| Giai đoạn | T | N | M | B | Tỷ lệ sống 5 năm (%) |
| IA | 1 | 0 | 0 | 0, 1 | 98 |
| IB | 2 | 0 | 0 | 0, 1 | 89 |
| IIA | 1, 2 | 1, 2 | 0 | 0, 1 | 89 |
| IIB | 3 | 0 - 2 | 0 | 0, 1 | 56 |
| IIIA | 4 | 0 - 2 | 0 | 0 | 54 |
| IIIB | 4 | 0 - 2 | 0 | 1 | 48 |
| IVA1 | 1 - 4 | 0 - 2 | 0 | 2 | 41 |
| IVA2 | 1 - 4 | 3 | 0 | 0 - 2 | 23 |
| IVB | 1 - 4 | 0 - 3 | 1 | 0 - 2 | 18 |
10.5 Điều trị
10.5.1 Lựa chọn điều trị theo khuyến cáo châu Âu 2017
| Giai đoạn bệnh | Lựa chọn đầu tay | Mức độ bầng chứng | Lựa chọn thứ 2 | Mức độ bằng chứng |
| IA, IB, IIA | - Chờ đợi, theo dõi (IA) - Corticoid tại chỗ - UVB (chủ yếu IA và IIA) - PUVA - Xạ trị tại chỗ (cho MF tại chỗ và u lym pho thể Paget) | 4 2 2 2 4 | - Toàn thân: retinoids hoặc IFN-CC thường kết hợp với PUVA - TSEB (chủ yếu cho T2b) - MTX liều thấp - Liệu pháp sử dụng chùm tia electron (Total skin electron beam therapy) | 2 2 2 4 |
| IIB | - Liệu pháp toàn thân* + Retinoids + IFN-a - TSEB (Chủ yếu cho T2b) - Đơn hóa trị liệu (gemcitabin, doxorubicin) - MTX liều thấp - Xạ trị tại chỗ** * Thường kết hợp với PUVA, hoặc các phương pháp khác. ** Như một biện pháp hỗ trợ cho liệu pháp toàn thân và liệu pháp da trực tiếp khác. | 2 2 2 4 4 4 | - Đa hóa trị liệu* - Ghép tế bào gốc** *: phác đồ CHOP được sử dụng rộng rãi nhất **: nên hạn chế với bệnh nhân không ổn định | 3 3 |
| IIIA, IIIB | - Liệu pháp toàn thân* **: ECP đơn độc hoặc phối hợp toàn thân và tại chỗ | 2 2 3 4 2 | Đa hóa trị liệu* Ghép tế bào gốc** *: phác đồ CHOP được sử dụng rộng rãi nhất **: nên hạn chế với bệnh nhân không ổn định | 3 3 |
| IVA, IVB | - Hóa trị (gemcitabin, doxorubicin, CHOP and CHOP-like) - Xạ trị (Xạ electron và xạ tại chỗ) - Alentuzumab - Ghép tế bào gốc | 3 4 3 3 | ||
| Hội chứng Sezary | - ECP - Chlorambucil + prednison - Liệu pháp toàn thân kết hợp với ECP hoặc: + PUVA + Retinoid + IFN-0 + MTX liều thấp | 3 3 3 0 3 4 | - Hóa trị (gemcitabin, doxorubicin, CHOP and CHOP-like) - Alentuzumab - Ghép tế bào gốc | 3 4 3 |
10.5.2 Điều trị cụ thể
10.5.2.1 Theo dõi
Bệnh nhân giai đoạn IA có nguy cơ tiến triển bệnh thấp, ước tính 10% trong vòng 10 năm. Vì thế có thể khuyến cáo theo dõi không cần điều trị đối với người bệnh ở giai đoạn bệnh IA. Tuy nhiên, cần theo dõi chặt chẽ và tái khám định kì để phát hiện bệnh tiến triển.
10.5.2.2 Điều trị tại chỗ
Corticoid tại chỗ:
- Là biện pháp được sử dụng rộng rãi và có hiệu quả trong điều trị giảm bệnh ở những bệnh nhân có tổn thương đám/mảng giai đoạn sớm.
- Nghiên cứu năm 1998 bởi Zackheim đánh giá hiệu quả điều trị bằng corti-coid loại mạnh bôi tại chỗ 2 lần/ngày trên 79 bệnh nhân giai đoạn bệnh IA/B cho thấy tỷ lệ đáp ứng 94%.
Mechlorethamin (HN2):
- Mechlorethamine là một tác nhân kiềm hóa được Mỹ chấp thuận lần đầu điều trị MF vào năm 1949. Gần đây, thuốc dưới dạng gel 0,02% được FDA chấp thuận trong điều trị MF giai đoạn IA và IB. Thuốc dùng một lần/ngày, bôi trên tất cả các tổn thương.
- Tác dụng không mong muốn hay gặp là kích ứng da tại chỗ. Không có bằng chứng về tác dụng độc khi dùng lâu dài cũng như xuất hiện các ung thư da thứ phát.
Bexaroten tại chỗ: dẫn xuất retinoid, gắn chọn lọc và hoạt hóa receptor retinoid X:
- Thuốc dạng gel 1% được FDA chấp thuận trong điều trị bôi tại chỗ tổn thương da MF giai đoạn IA và IB ở người bệnh kháng trị với các biện pháp khác hoặc bệnh dai dẳng hoặc không dung nạp với các điều trị khác.
- Tỷ lệ đáp ứng từ 44% đến 63% tùy nghiên cứu. Tác dụng không mong muốn nhẹ, chủ yếu là kích ứng da. Thuốc có thể gây quái thai, chống chỉ định ở phụ nữ có thai và thận trọng ở phụ nữ trong độ tuổi sinh đẻ.
Chùm tia electron: điều trị sử dụng chùm tia electron được tạo ra trong máy gia tốc thẳng để đâm xuyên vào da với một độ sâu nhất định, ảnh hưởng không đáng kể đến các tạng bên trong cơ thể bao gồm cả tủy xương. Điều trị tiêu chuẩn bao gồm tổng liều 30 - 36Gy trong thời gian 8-10 tuần với tỷ lệ lui bệnh cao, đặc biệt giai đoạn T2, T3. Gần đây, phương pháp điều trị với liều thấp hơn (từ 10 - 12Gy) được nghiên cứu có độ an toàn cao hơn, tuy nhiên hiệu quả so với liều điều trị tiêu chuẩn chưa được đánh giá.
Xạ trị tại chỗ: xạ trị nông, cục bộ cho kết quả điều trị giảm bệnh tốt đối với những tổn thương đơn độc, thậm chí đạt lui bệnh trong thời gian dài. Điều trị có thể đơn thuần hoặc kết hợp với các phương pháp điều trị toàn thân hoặc tại chỗ khác. Với MF thể đơn độc (unilesional) và thể dạng Paget (pagetoid reticulosis) khuyến cáo dùng liều 20 - 24Gy. Trường hợp bệnh nặng với tổn thương mảng hoặc u đơn độc có thể điều trị giảm nhẹ với liều thấp (2 - 4Gy).
10.5.2.3 Ánh sáng trị liệu
Ánh sáng trị liệu đặc biệt là UVB dải hẹp (NB-UVB) và PUVA luôn là lựa chọn ưu tiên trong MF giai đoạn I - III. Với giai đoạn III cần phối hợp với phương pháp toàn thân.
NB-UVB là lựa chọn ưu tiên trong điều trị MF giai đoạn sớm, đặc biệt là TIa và T2a (đặc trưng là thể đám). PUVA được lựa chọn điều trị MF giai đoạn T1b và T2b (các tổn thương dạng mảng) và người có type da sẫm màu. PUVA: thường được dùng đường uống, không khuyến cáo đường tắm. PUVA bôi tại chỗ chỉ dùng ở bệnh nhân có một tổn thương đơn độc và tổn thương dạng Paget.
Điều trị tương tự như điều trị vảy nến. Tỉ lệ đáp ứng cao 70 - 100%, tuy nhiên tỉ lệ tái phát cao chủ yếu sau 1 - 2 năm. Vì thế cần điều trị duy trì sau khi đạt lui bệnh hoàn toàn hoặc gần hoàn toàn phòng tái phát.
Những bệnh nhân đáp ứng không đầy đủ hoặc tái phát nhanh, hoặc MF giai đoạn III ưu tiên điều trị phối hợp thêm với thuốc toàn thân như retinoid và INF-a.
10.5.2.4 Điều trị toàn thân
Retinoid: retinoid là các dẫn xuất của vi-tamin A, các thuốc đã được dùng để điều trị u lympho T ở da bao gồm Isotretinoin, etretinate, acitretin, bexaroten và ali-tretinoin:
- Bexaroten là thuốc tốt nhất trong các retinoid để điều trị MF. Được chỉ định điều trị các tổn thương da trong các trường hợp bệnh nặng đã kháng trị với ít nhất một phương pháp điều trị toàn thân trước đó, tỉ lệ đáp ứng là 45%. Phối hợp với ánh sáng được khuyến cáo.
- Thuốc thường được dung nạp tốt, các tác dụng không mong muốn thường gặp bao gồm khô da, niêm mạc, tăng lip-id máu và trong trường hợp dùng bex-aroten, thường có nhược giáp trung ương cần bổ sung hormon tuyến giáp ở hầu hết bệnh nhân. Tất cả các thuốc reti-noid đều có khả năng gây quái thai.
Interferon a: IFN-a là interferon duy nhất được chấp thuận trong điều trị u lympho T ở da. Thuốc có thể dùng đơn trị liệu từ 3 triệu đơn vị cho đến 18 triệu đơn vị tiêm dưới da 3 lần/tuần hoặc hàng ngày. Thuốc có thể bắt đầu với liều 3 triệu đơn vị X 3 lần/tuần, tăng liều dần dựa trên đáp ứng và giảm liều dần để duy trì. Tuy nhiên, phối hợp với ánh sáng được khuyến cáo. Tác dụng không mong muốn phụ thuộc liều, bao gồm triệu chứng giống cúm, tăng transaminase, hạ bạch cầu, hạ tiểu cầu, giảm nhận thức, rối loạn nhịp tim, rối loạn hormon tuyến giáp.
IFN-a kết hợp với retinoid: retinoid (etretinat, isotretinoin) được sử dụng kết hợp với IFN-a cho thấy có hiệu quả đạt lui bệnh và duy trì đáp ứng tốt mà không tăng tác dụng độc. Mặc dù IFN-a kết hợp với PUVA cho hiệu quả tốt hơn IFN-a kết hợp với retinoid, IFN-a kết hợp với retinoid vẫn là điều trị kết hợp được lựa chọn tốt ở những bệnh nhân đáp ứng kém với đơn trị liệu cộng với tiếp cận với PUVA hạn chế.
Điều trị hóa chất: công thức CHOP [(C)yclophosphamid-(H)ydroxydaunorubi-cin-(O)ncovin(P)rednison or (P)rednis-olon] vẫn là lựa chọn tiêu chuẩn. Một trong những thuốc có tác dụng điều trị có độc tính chấp nhận được là pegylated liposomal doxorubicin và gemcitabin.
- Trong một nghiên cứu đa trung tâm thực hiện bởi Dummer, tiến hành điều trị doxorubicin 20 mg/m2 mỗi 2 tuần trên 49 bệnh nhân MF giai đoạn muộn (IIB, IVA hay IVB) đã được điều trị trước đó thấy tỉ lệ đáp ứng là 40,8% với thời gian đáp ứng trung bình là 6 tháng.
- Chlorambucil được giới thiệu điều trị hội chứng Sezary vào những năm 1970 bởi Winkelmann. Thuốc có thể được dùng đường uống: liều 2-6 mg/ngày liên tục kết hợp Prednisone khởi đầu 20 mg/ngày, giảm liều dần đến 0-10 mg/ngày. Do thuốc có thể gây ức chế tủy xương, leukemia; không khuyến cáo dùng thuốc kéo dài.
- Methotrexate khuyến cáo dùng liều 5 - 25mg một lần/tuần.
Điều trị miễn dịch nhắm đích:
- Denileukin diftitox: là protein tái tổ hợp gồm có IL-2 liên kết với nhánh xúc tác của độc tố bạch hầu, thuốc nhắm vào các tế bào có receptor IL-2. Thuốc đang được nghiên cứu.
- Alemtuzumab: là kháng thể đơn dòng IgGl người tái tổ hợp chống lại glycopro-tein bề mặt tế bào CD52, có trên các lym-pho B và T bình thường và ác tính nhưng không có ở các tế bào gốc tạo máu. Liều tiêu chuẩn 30mg tiêm tĩnh mạch 3 lần/tuần trên bệnh nhân MF cho tỷ lệ đáp ứng hơn 50%. Tác dụng không mong muốn thường gặp là suy giảm miễn dịch, nhiễm trùng cơ hội... Thuốc hiệu quả đối với đỏ da toàn thân (T4) và biểu hiện trong máu (B >1). Một số bệnh nhân có thể đạt được lui bệnh lâu dài. Liều thấp hơn với độc tính ít hơn: tiêm dưới da 15mg, tiêm cách ngày cho thấy tỉ lệ đáp ứng tương tự phác đồ điều trị trước đó. Đồng thời, không có những nhiễm khuẩn liên quan ở liều thấp hơn 10mg.
- Brentuximab vedotin: là kháng thể liên hợp, bao gồm IgGl kháng CD30 gắn với monomethyl auristatin E (một tác nhân phá hủy vi ống). Thuốc thâm nhập vào các tế bào biểu hiện CD30, giải phóng monomethyl auristatin E gây ngừng chu kỳ tế bào. Thuốc có hiệu quả tổt ở những ung thư có biểu hiện CD30 cao trên hóa mô miễn dịch và ngược lại, hiệu quả thấp ở những ung thư có biểu hiện CD30 thấp trên hóa mô miễn dịch. Tác dụng không mong muốn hay gặp bao gồm bệnh lý thần kinh ngoại vi, giảm bạch cầu, mệt mỏi, buồn nôn, rụng tóc. Hiện tại thuốc chưa được chấp thuận điều trị MF. Thuốc có thể được lựa chọn theo chỉ định của bác sĩ trong trường hợp CD30 dương tính cao.
- Mogamulizumab: là kháng thể đơn dòng người, kháng CCR4 (CC chemokine receptor 4). Hiện tại, thuốc được chấp thuận ở Nhật trong điều trị u lympho T ngoại vi CCR4+ tái phát/kháng trị. Tác dụng không mong muốn nhẹ, gồm có sốt, ớn lạnh, phát ban, buồn nôn, đau đầu, các phản ứng liên quan tới truyền thuốc.
Quang hóa trị liệu ngoài cơ thể: (ex-tracorporeal photochemotherapy/pho-topheresis) là phương pháp điều trị bằng ánh sáng đối với máu của người bệnh bên ngoài cơ thể có mặt psoralen. Là phương pháp có độ an toàn rất cao. Trong một nghiên cứu bởi Edelson và cộng sự, tác giả báo cáo tỉ lệ đáp ứng lên tới 73%, các bệnh nhân mang bệnh chủ yếu là T4. Phương pháp này được dùng phối hợp với các phương pháp khác bao gồm retinoid, interferon, PUVA...
Ghép tế bào gốc tạo máu: là phương pháp mới, có nhiều hứa hẹn. Ghép tế bào gốc allogeneic (alloSCT) hiện là lựa chọn duy nhất mang ý nghĩa chữa khỏi bệnh đối với MF. Việc chọn lựa bệnh nhân khó khăn, cần tư vấn kỹ và nên thực hiện chủ yếu trên những người trẻ, bệnh giai đoạn muộn, khối lượng u thấp, nguy cơ tiến triển cao, tiên lượng xấu tại thời điểm ghép.
Các thuốc ức chế histone deacetyl-ase: hiện tại có ba thuốc là vorinostat, romidepsin và belinostat được FDA chấp thuận trong một số trường hợp u lym-pho ở da. Tác dụng không mong muốn thường gặp bao gồm tác dụng phụ trên đường tiêu hóa, giảm tiểu cầu, kéo dài QTc và huyết khối tĩnh mạch sâu (với vorinostat).
10.5.2.5 Điều trị duy trì
MF là bệnh lý mạn tính, điều trị duy trì sau khi đã đạt được lui bệnh nhằm duy trì đáp ứng và ngăn tái phát, tiến triển. Thông thường, điều trị duy trì bằng trị liệu ánh sáng, retinoid, IFN-a...
Điều trị duy trì nên được cân nhắc chủ yếu ở những bệnh nhân MF giai đoạn > IB (T2b) với nguy cơ tái phát và hoặc tiến triển cao.
11 Ung thư mạch máu ở da (Cutaneous angiosarcoma)
11.1 Đại cương
Angiosarcoma là một khối u ác tính, có nguồn gốc từ tế bào nội mô mạch máu. Là một bệnh hiếm gặp, chiếm tỉ lệ khoảng 1% sarcoma, thường gặp ở độ tuổi trên 70. Angiosarcoma ở người trẻ thường liên quan đến các bệnh phù mạch bạch huyết mạn tính, viêm da do tia xạ hay suy giảm miễn dịch, làm tăng nguy cơ ung thư nội tạng.
Bệnh hay gặp ở người da trắng, tỉ lệ nam/nữ = 3/1. Tiên lượng xấu, tỉ lệ sống trên 5 năm khoảng 15%. Angiosarcoma có thể gặp ở bất cứ bộ phận nào trên cơ thể nhưng hay gặp ở da và mô mềm (chiếm 50 - 60%), ngoài ra có ở gan, lách, xương, vú, tim, phổi... Các yếu tố xạ trị, phơi nhiễm với các chất gây ung thư, phù bạch huyết... làm tăng nguy cơ mắc bệnh.
11.2 Cơ chế bệnh sinh
Cơ chế chưa thực sự được biết rõ. Đối với angiosarcoma phát triển trên vùng phù mạch bạch huyết mạn tính, có giả thuyết cho ràng sự thay đổi tạo u là do tích luỹ các chất sinh u (chưa rõ) trong dịch bạch huyết.
Một nghiên cứu cho thấy biểu hiện về sự liên quan giữa nội mạch bạch huyết với kháng nguyên VEGFR-3 ở 8/16 bệnh nhân ung thư mạch (ngoại trừ những bệnh nhân có phù mạch bạch huyết hoặc có chiếu xạ trước đó).
Một số các nghiên cứu khác đã tìm thấy sự có mặt đồng thời của hai chất podo-planin và podocalyxin trong hầu hết các ung thư mạch máu, người ta cho rằng podoplanin là marker của mạch bạch huyết, còn podocalyxin là marker của tế bào nội mô mạch máu. Điều này gợi ý rằng bệnh ung thư mạch máu liên quan tới gen.
11.3 Lâm sàng
11.3.1 Angiosarcoma vùng đầu mặt
Là thể phổ biến nhất.
Tổn thương cơ bản: mảng hơi tím ở trung tâm mặt, trán, da đầu giống như là vết tụ máu hoặc bầm tím đơn thuần, có thể sưng nề hay phù mặt. Tổn thương tiến triển thành cục nổi cao màu tím dễ chảy máu, có thể có loét, xuất hiện các thương tổn vệ tinh. Tổn thương có thể lan rộng thành những mảng thâm nhiễm hay những cục tím, chắc, liên kết lại và lan tỏa gây phù mạch mạn tính bao phủ phần lớn đầu cổ. Tổn thương ban đầu có thể đơn độc hoặc nhiều.
Phân bố: hay gặp ở da đầu, nửa trên phần mặt, ít gặp hơn ở cổ.
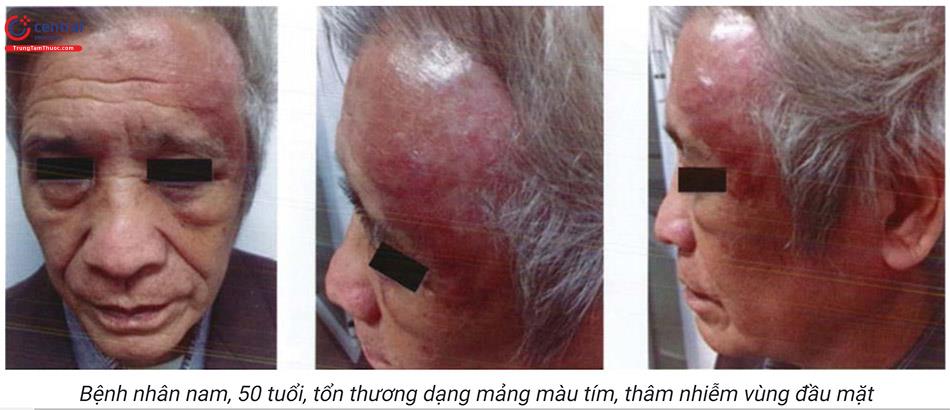
11.3.2 Angiosarcoma phát triển trên vùng phù mạch bạch huyết mạn tính (Lymphedema - associated angiosarcoma - LAS)
Bệnh nhân có phù mạch bạch huyết mạn tính do các nguyên nhân khác: phù mạch bẩm sinh, phù mạch do chấn thương, phù mạch tự phát, phù mạch do giun chỉ.
Thời gian phù mạch mạn tính xuất hiện trước angiosarcoma từ 4 đến 27 năm.
Di căn phổi là nguyên nhân gây tử vong thường gặp nhất.
11.3.3 Angiosarcoma sau tia xạ
Tổn thương là những cục, mảng thâm nhiễm tại hoặc xung quanh vị trí chiếu xạ. Tiên lượng kém nhất trong các loại angiosarcoma. Xâm nhập, tiến triển không ngừng, đa vị trí. Hay di căn hạch bạch huyết, phổi.
11.3.4 Ung thư mạch dạng thượng bì (epithelioid angiosarcoma)
Tổn thương cơ bản: thường gặp ở mô mềm ở sâu hay ở hạ bì. Tổn thương ở mô dưới da, có thể xâm lấn đến gân, sụn khớp, mạch máu và thần kinh lớn. Bề mặt tổn thương thường có loét. Có thể gây chèn ép thần kinh gây yếu cơ và tê bì. Phân bố: hay gặp ở tay, sau đó đến phần xa của chi dưới.
Di căn: thường gặp ở hạch, phổi, da đầu.
Angiosarcoma ở da, mô mềm cũng được báo cáo là có liên quan đến các bệnh như: + U bao thần kinh lành tính hay ác tính.
- U nang buồng trứng hai bên.
- Mất chức năng shunt động - tĩnh mạch thận sau cấy ghép thận.
- Tiếp xúc lâu dài với các chất độc hai.
- Khô da sắc tố.
11.4 Cận lâm sàng
11.4.1 Giải phẫu bệnh
Angiosarcoma vùng đầu mặt:
- Tổn thương lan rộng hơn so với tổn thương nhìn thấy trên lâm sàng.
- Xoang mạch máu bất thường về hình dạng và kích thước thông với nhau thành mạng lưới.
- Các xoang được lót bởi lớp tế bào nội mô không điển hình có thể là một hàng duy nhất hay một lớp dày cấu trúc lộn xộn.
- Các tế bào nội mô có hạt nhân lớn chứa nhiều chất nhiễm sắc, sắp xếp thành các nhú nhô vào lòng mạch làm giảm không gian mạch máu.
- Có thể thâm nhiễm bạch huyết hay xuất huyết.
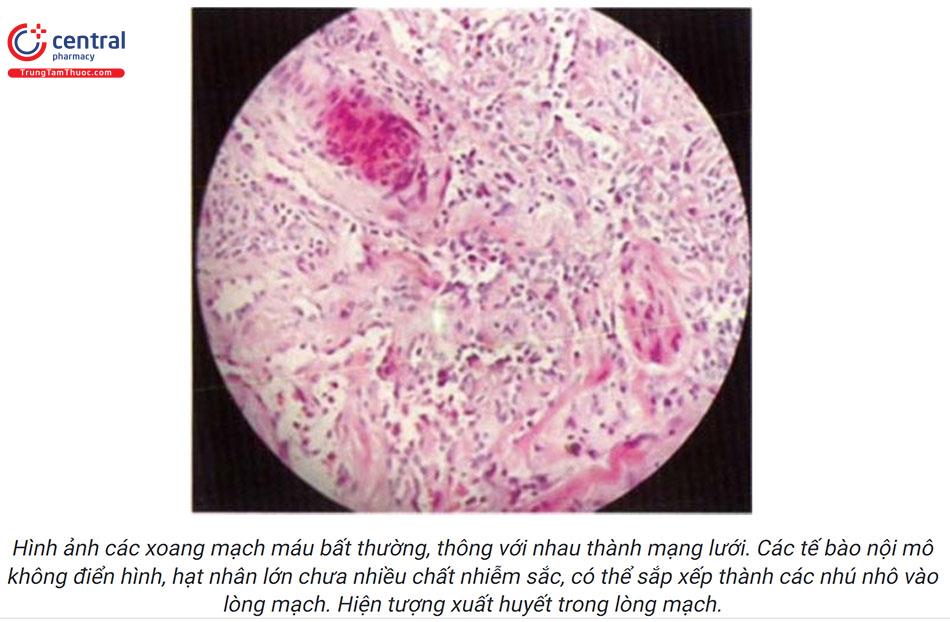
| Biệt hóa cao | Biệt hóa thấp |
| Mạng lưới mạch máu nghèo nàn Tế bào nội mô có nhân từ nhỏ đến trung bình, nhân không điển hình | Tăng sinh mạch hỗn loạn, hiện tượng xuất huyết, có nhiều khoang hồ máu. Tế bào nội mô có nhân hình khía. |
Angiosarcoma liên quan đến phù bạch huyết mạn tính:
- Mạng lưới mạch máu nghèo nàn.
- Tế bào nội mô có nhân từ nhỏ - trung bình, nhân không điển hình.
- Ung thư mạch máu dạng thượng bì.
- Gồm những tế bào hình tròn lớn, có nhân ưa acid chiếm ưu thế, có nhiều hốc bào trong tế bào chất là chứng minh sự biệt hoá mạch máu.
- Các tế bào xung quanh vùng trung tâm hoại tử.
11.4.2 Hóa mô miễn dịch
Dương tính với CD31, CD34 (CD31 có độ nhạy và độ đặc hiệu cao hon so với tế bào nội mô).
Kháng nguyên liên quan đến yếu tố VIII (độ đặc hiệu cao tuy nhiên độ nhạy không cao: phản ứng âm tính hay dương tính nhẹ với u mạch máu biệt hóa cao). Cytokeratin: dương tính ở 1/3 số trường hợp u mạch dạng thượng bì, kết hợp với CD31 để chẩn đoán phân biệt các dạng khác của ung thư biểu mô da.

11.5 Giai đoạn
11.5.1 Phân loại TNM
Khối u (tumor):
- Tx: khối u không thể đánh giá được
- TO: không có bằng chứng của khối u
- T1: khối u lớn nhất < 5cm
- T1A: khối u ở bề mặt
- T1B: khối u thâm nhiễm sâu
- T2: khối u lớn nhất > 5cm
- T2A: khối u ở bề mặt
- T2B: khối u thâm nhiễm sâu
Hạch (node)
- Nx: không đánh giá được
- NO: không có di căn hạch
- Nl: có di căn hạch
Di căn xa (metastatis)
- M0: không có di căn xa
- M1: có di căn xa
11.5.2 Giai đoạn
| Giai đoạn | Phân độ TNM | Nguy cơ |
| IA | T1a NO, Nx, MO T1b NO, Nx, MO | Nguy cơ thấp Nguy cơ thấp |
| IB | T2a NO, Nx, MO T2b NO, Nx, MO | Nguy cơ thấp Nguy cơ thấp |
| IIA | T1a NO, Nx, MO T1b NO, Nx, MO | Nguy cơ cao Nguy cơ cao |
| IIB | T2a NO, Nx, MO T2b NO, Nx, MO | Nguy cơ cao Nguy cơ cao |
| III | T2b NO, Nx, MO | Nguy cơ cao |
| IV | Mọi T, N1, MO Mọi T, Nx, M1 | Nguy cơ rất cao Nguy cơ rất cao |
11.6 Chẩn đoán phân biệt
U mạch bạch huyết lành tính: dễ nhầm với u mạch máu biệt hoá cao.
Các giả ung thư mạch khác:
- U nội mô mạch dạng lưới giống Dabska
- U nội mô mạch dạng thượng bì
- U mạch dạng búi
- Sarcoma
- Kaposi
11.7 Điều trị
11.7.1 Nguyên tắc điều trị
Nên kết hợp các biện pháp hơn là dùng đơn độc.
Giai đoạn I.
Khối u < 5cm có thể điều trị bằng cắt bỏ tổn thương đơn độc. cắt rộng xung quanh tổn thương.
Đối với khối u lớn hơn, xạ trị sau phẫu thuật có thể được áp dụng nhằm giảm tỉ lệ tái phát.
Giai đoạn II và III.
Khối u giai đoạn này có xu hướng phát triến và lan rộng nhanh chóng. Một số khối u giai đoạn III đã lan đến các hạch bạch huyết gần đó. Ngay cả khi những sarcom này chưa lan đến các hạch bạch huyết, nguy cơ lây lan (đến các hạch bạch huyết hoặc các vị trí khác xa hơn) là rất cao. Những khối u này cũng có xu hướng phát triển trở lại ở cùng vị trí sau khi được loại bỏ (tái phát cục bộ).
Phẫu thuật: là phương pháp điều trị chính. Có thể xạ trị sau phẫu thuật.
Nếu khối u lớn hoặc ở nơi phẫu thuật khó khăn (nhưng không phải trong các hạch bạch huyết), bệnh nhân có thể được điều trị bằng hóa trị và/hoặc xạ trị trước khi phẫu thuật. Mục đích là thu nhỏ khối u, giúp loại bỏ dễ dàng hơn. Hóa trị và/hoặc xạ trị cũng có thể được đưa ra sau phẫu thuật.
Trong một số ít trường hợp, cắt cụt chi là cần thiết để loại bỏ toàn bộ chi với khối u.
Hóa trị và/hoặc xạ trị mà không phẫu thuật: khi vị trí hoặc kích thước của khối u hay sức khỏe của bệnh nhân không thích hợp để tiến hành phẫu thuật.
Giai đoạn IV
Angiosarcom giai đoạn IV hiếm khi có thể chữa được. Một số bệnh nhân có thể được chữa khỏi nếu khối u nguyên phát và tất cả các khối u di căn được loại bỏ bằng phẫu thuật. Tỷ lệ thành công cao nhất là khi ung thư chỉ di căn đến phổi.
Ở những bệnh nhân này, khối u nguyên phát được điều trị như ở giai đoạn II hoặc III, đồng thời khối u di căn phải được loại bỏ hoàn toàn nếu có thể.
Đối với những bệnh nhân có khối u nguyên phát và các khối u di căn không thể loại bỏ hoàn toàn bằng phẫu thuật, xạ trị và/hoặc hóa trị thường được sử dụng để làm giảm các triệu chứng. Các loại thuốc hóa học doxorubicin và ifosf-amid thường là lựa chọn đầu tiên, cùng với nhau hoặc cùng với các loại thuốc khác. Doxorubicin có thể được dùng cùng với thuốc nhắm trúng đích olara-tumab. Gemcitabin và Docetaxel có thể được dùng khi lựa chọn đầu tiên thất bại.
11.7.2 Một số phác đồ hóa trị liệu được áp dụng Kết hợp:
AD (doxorubicin, dacarbazin)
Gemcit abin, docetaxel
AIM (doxorubicin, ifosfamid, Mesna)
Gemcitabin, vinorelbin
MAID (mesna, doxorubicin,ifosfamid, dacarbazin)
Doxorubicin, olaratuma
Ifosfamid, epirubicin, mesna
Gemcitabin, dacarbazin
Đơn độc:
Doxorubicin
Ifosfamid
Epirubicin
Gemcitabin
Dacarbazin
Liposomal doxorubicin
Temozolomid
Vinorelbin
Eribulin
Trabectedin
Pazopanib

