Nhiễm nấm nông bôi thuốc gì cho hết? Phác đồ điều trị, hình ảnh mô tả bệnh

Tác giả: Kiran Motaparthi
Dịch: Bs. Trương Tấn Minh Vũ
Tải PDF TẠI ĐÂY
1 Nhiễm nấm dermatophyte (Dermatophytosis)
1.1 Đặc điểm lâm sàng
Nhiễm nấm dermatophyte (dermatophytosis, tinea), do ba loại nấm sợi, Trichophyton, Microsporum và Epidermophyton gây ra, là bệnh nhiễm nấm nông phổ biến nhất ở trẻ em. Nhiễm nấm dermatophyte được phân loại dựa trên vị trí giải phẫu. Tùy thuộc vào loài, sự lây nhiễm có thể là ưa người (tiếp xúc với người bị nhiễm bệnh), ưa động vật (tiếp xúc với động vật bị nhiễm bệnh) hoặc ưa địa chất (tiếp xúc với đất).
Nấm thân mình (tinea corporis) dùng để chỉ nhiễm nấm dermatophyte ở thân hoặc tứ chi ngoại trừ lòng bàn tay và lòng bàn chân; những đặc điểm đặc trưng là các mảng ngứa có vùng trung tâm sạch, có vảy ở vùng xung quanh và đôi khi có mụn mủ (Hình 16.1). U hạt Majocchi là một biến thể của nấm thân mình, với sự ảnh hưởng chủ yếu ở các nang lông tạo ra các mụn mủ hoặc sẩn quanh nang lông trên lâm sàng (Hình 16.2) [1, 2].
.jpg)
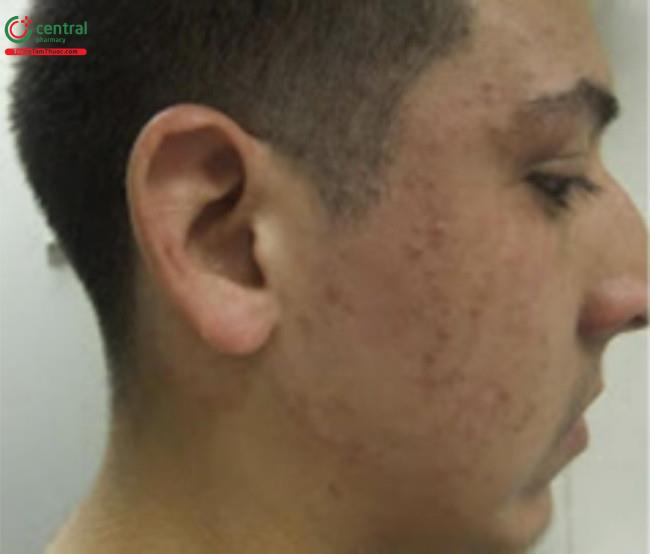
lan rộng trên má của một nam thiếu niên.
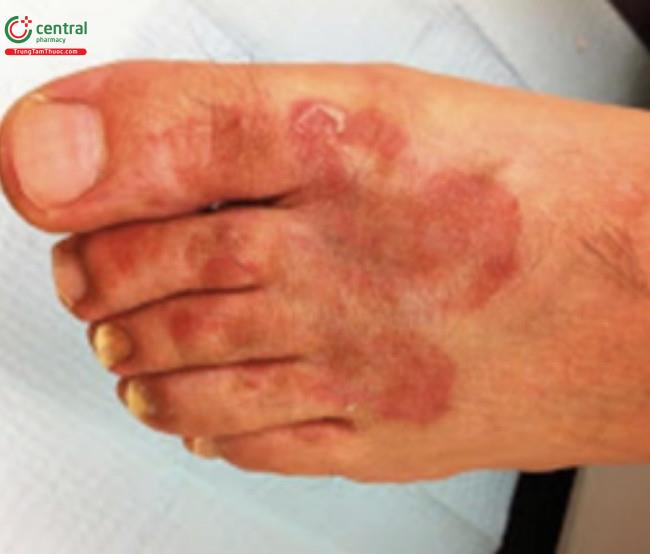
Nấm bàn chân (tinea pedis) thường gặp ở thanh thiếu niên nhưng rất hiếm gặp ở trẻ em trước tuổi dậy thì và thường biểu hiện dưới dạng ban đỏ, tróc vảy, ngâm nước hoặc vết trợt ở vùng kẽ ngón. Ban đỏ và tróc vảy ở bề mặt lòng bàn chân, đôi khi có mụn mủ và mụn nước (nấm bàn chân viêm hoặc bọng nước) cũng được nhìn thấy. Nấm bẹn (tinea cruris) đi kèm với nấm bàn chân và biểu hiện với các dát hoặc mảng mỏng, ngứa, có ranh giới rõ, ảnh hưởng vùng háng nhưng thường không có ở bìu.
Nấm lòng bàn tay (tinea manuum), giống như nấm móng, hiếm gặp ở trẻ em và thường biểu hiện dưới dạng ban đỏ tróc vảy một bên.
Nấm da mặt (tinea faciei) ảnh hưởng khuôn mặt, với các đặc điểm lâm sàng tương tự như nấm thân mình (Hình 16.3 và 16.4). Nấm vùng râu (tinea barbae) là một biến thể ảnh hưởng vùng râu hoặc lông trên khuôn mặt của nam thanh thiếu niên.
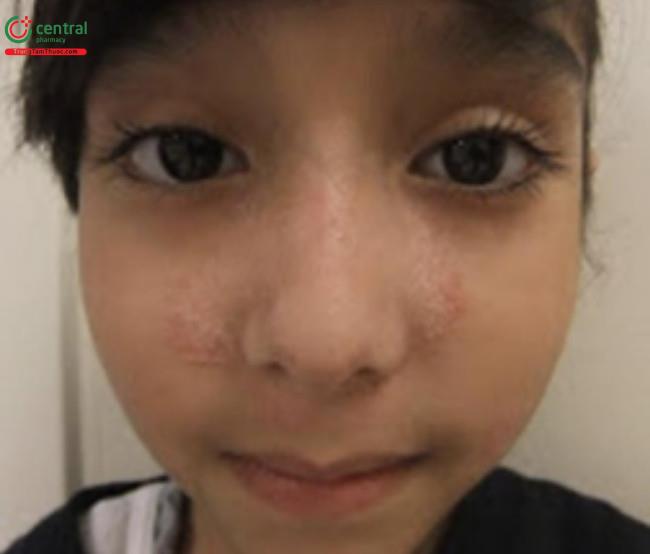
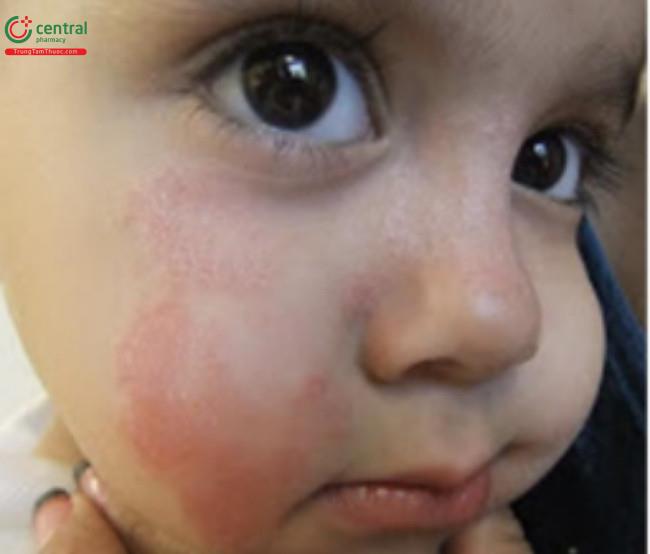
Nấm da đầu (tinea capitis) rất phổ biến ở trẻ em và có thể gặp ở 8% trẻ em trong độ tuổi đi học. Biểu hiện điển hình là các mảng rụng tóc giới hạn có vảy, ban đỏ và tóc gãy (“chấm đen” của nhiễm nấm). Có thể có mụn mủ. Sưng hạch vùng cổ hoặc chẩm là đầu mối hữu ích cho chẩn đoán. Kerion là một biến thể được đặc trưng bởi mảng hoặc nốt viêm rõ rệt với mụn mủ và lớp mài dày đặc (Hình 16.5 và 16.6).
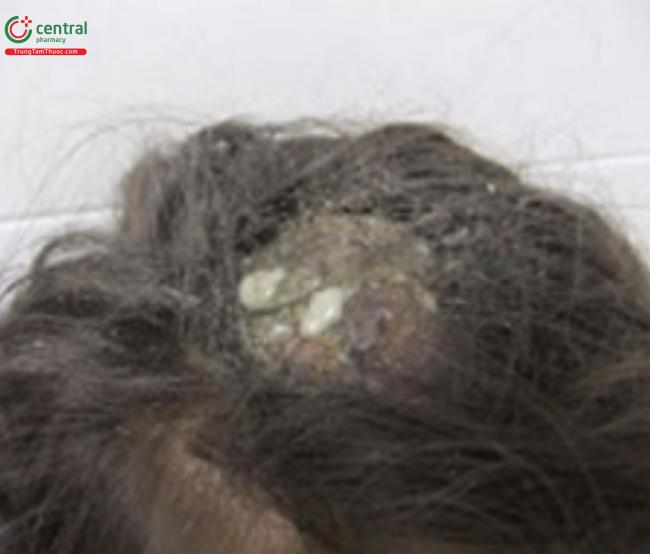
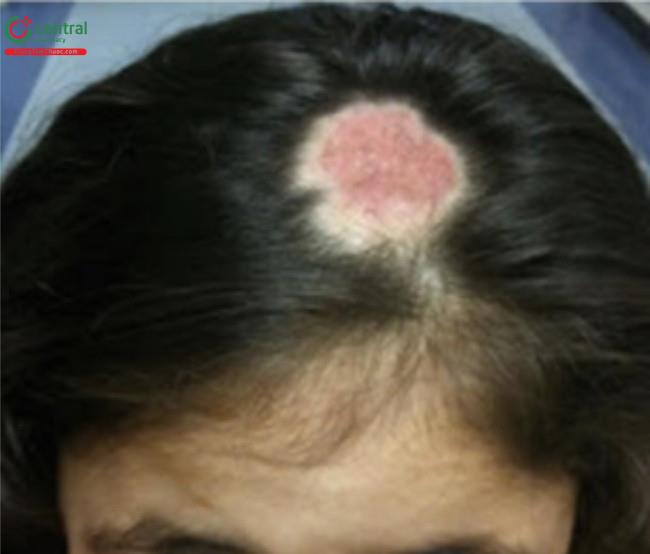
Tóc mọc lại được thấy trong lần khám tiếp theo.
Nấm móng (onychomycosis) có thể do nấm dermatophyte, nấm men như Candida hoặc nấm mốc không phải dermatophyte. Mặc dù hiếm gặp ở trẻ em, nấm dermatophyte là nguyên nhân phổ biến nhất gây bệnh nấm móng ở trẻ em. Vùng dưới móng ở đầu xa và đầu gần được đặc trưng bởi sự đổi màu từ vàng sang trắng và các mảnh vụn dưới móng (Hình 16.7). Bệnh nấm móng trắng nông là một bệnh nhiễm nấm chỉ ở phiến móng.
1.2 Cận lâm sàng được đề xuất
| Để chẩn đoán |
| Cạo và soi tươi với KOH |
| Nuôi cấy nấm |
| Đèn Wood (nấm da đầu) |
| Soi da (nấm da đầu) |
| Mô bệnh học |
| Để điều trị (với thuốc chống nấm toàn thân) |
| Công thức máu toàn phần (CBC) |
| Xét nghiệm chức năng gan (LFT) |
Đối với nhiễm nấm dermatophyte ở da và tóc, có thể soi tươi với KOH bằng cách cạo vảy bằng một phiến kính và cho thấy độ nhạy cao để chẩn đoán. Đáng chú ý, KOH không nhạy cảm trong u hạt Majocchi do khả năng thiếu các yếu tố sợi nấm trong lớp sừng. Nuôi cấy nấm cho phép xác nhận nhiễm nấm trong vòng vài ngày và xác định loài, nhưng kém nhạy hơn KOH và mất vài tuần để phát triển trên môi trường thạch Sabouraud dextrose, thạch Mycosel hoặc môi trường thử nghiệm dermatophyte. Chúng thu được bằng cách cạo vảy hoặc tóc bằng bàn chải đánh răng dùng một lần, bàn chải tế bào hoặc tăm bông vô trùng. Dựa trên các nghiên cứu trên bệnh nhân bị nấm móng, soi tươi với KOH cho thấy độ nhạy 76–94% và độ đặc hiệu trên 70% trong khi nuôi cấy cho thấy độ nhạy 53–59% và độ đặc hiệu trên 80%. Kiểm tra mô bệnh học (cắt móng bằng PAS) là tiêu chuẩn vàng để chẩn đoán nấm móng, với độ nhạy 80–98% và độ đặc hiệu trên 70%. Sinh thiết da (đối với mô bệnh học, có hoặc không có PAS) hiếm khi cần thiết, nhưng có thể hữu ích trong các trường hợp u hạt Majocchi hoặc trong các trường hợp mô phỏng bệnh da viêm [3–5].
Đối với nấm da đầu, kiểm tra bằng đèn Wood rất hữu ích trong trường hợp nhiễm Microsporum, cho thấy huỳnh quang màu xanh lục sáng trong phòng tối. Do việc nuôi cấy nấm phải mất vài tuần để xác định loài, nên liệu pháp kháng nấm toàn thân theo kinh nghiệm được khuyến cáo trong các trường hợp nghi ngờ lâm sàng về nấm da đầu ở trẻ em, và terbinafine tốt hơn đối với các loài Trichophyton trong khi Griseofulvin tốt hơn đối với các loài Microsporum, đèn Wood là một phương pháp chẩn đoán bổ trợ rất hữu ích cho phép lựa chọn liệu pháp theo kinh nghiệm đối với viêm da đầu do nấm. Soi da đầu và tóc (trichoscopy) có thể là một biện pháp bổ trợ hữu ích. Các dấu hiệu bao gồm tóc gãy, tóc loạn dưỡng, tóc hình xoắn ốc, tóc dấu phẩy, chấm đen, dải trắng nằm ngang trong thân tóc và đục, tóc dễ biến dạng [6–8]
Ở những trẻ khỏe mạnh khác, không cần phải đánh giá xét nghiệm cơ bản trước khi điều trị bằng thuốc chống nấm toàn thân đối với nhiễm nấm dermatophyte. Tuy nhiên, ở trẻ em có rối loạn chức năng gan từ trước hoặc các bất thường về huyết học, nên đánh giá LFT hoặc CBC tương ứng. Ngoài ra, các xét nghiệm này nên được thực hiện ở những trẻ khỏe mạnh với các đợt điều trị kéo dài: trên 8 tuần với griseofulvin, 6 tuần với terbinafine hoặc 4 tuần điều trị với azole [9].
1.3 Nấm da đầu, vùng có râu (Tinea Capitis, Barbae)
1.3.1 Chiến lược quản lý
Việc điều trị cần sử dụng thuốc kháng nấm đường uống; thuốc kháng nấm bôi tại chỗ không thể thâm nhập đầy đủ vào nang lông và nên tránh sử dụng. Terbinafine và griseofulvin là hai loại thuốc duy nhất được FDA phê duyệt để điều trị nấm da đầu.
Cả terbinafine và griseofulvin đều cho thấy hiệu quả trong điều trị nấm da đầu, trong đó terbinafine hiệu quả hơn đối với các loài Trichophyton và griseofulvin hiệu quả hơn đối với các loài Microsporum. Một nghiên cứu sử dụng cả hai loại thuốc trong 6 tuần cho thấy tỷ lệ khỏi bệnh hoàn toàn và khỏi bệnh về mặt nấm cao hơn ở nhóm terbinafine so với nhóm griseofulvin (45,1% so với 39,2% và 61,5% so với 55,5%); tuy nhiên, trong hai phân tích tổng hợp, không thấy sự khác biệt đáng kể về hiệu quả. Tuy nhiên, cả hai phân tích tổng hợp đều cho thấy terbinafine hiệu quả hơn trong điều trị các loài Trichophyton trong khi griseofulvin hiệu quả hơn đối với các loài Microsporum. Ngoài ra, terbinafine được sử dụng trong thời gian trung bình ngắn hơn (4 tuần) so với griseofulvin (8 tuần).
Trong một thử nghiệm ngẫu nhiên có đối chứng, fluconazole trong 3 tuần (6 mg/kg/ ngày), fluconazole trong 6 tuần (6 mg/kg/ ngày) và griseofulvin trong 6 tuần (11 mg/kg/ ngày dạng vi hạt) đều cho tỷ lệ khỏi bệnh về mặt nấm (44,5%, 49,6% và 52,2%) và lâm sàng tương tự nhau và thấp. Trong một thử nghiệm ngẫu nhiên khác, fluconazole trong 4 tuần có hiệu quả 78%, trong khi griseofulvin trong 6 tuần có hiệu quả 76% trong việc điều trị khỏi nấm da đầu. Trong một nghiên cứu so sánh nhiều loại thuốc kháng nấm đường uống trong điều trị T. tonsurans hoặc T. violaceum, tỷ lệ hiệu quả là 92% đối với griseofulvin (6 tuần), 94% đối với terbinafine, 86% đối với itraconazole và 84% đối với fluconazole (mỗi loại dùng trong 2 tuần). Sáu tuần điều trị bằng itraconazole 100 mg mỗi ngày và griseofulvin vi hạt 500 mg mỗi ngày cho tỷ lệ khỏi bệnh 88% trong một nhóm bệnh nhân mà 90% trường hợp nấm da đầu do M. canis gây ra.
Cả dầu gội Selenium sulfide và ciclopirox, khi được sử dụng kết hợp với griseofulvin, đã cho thấy tỷ lệ khỏi bệnh về mặt nấm trên 90%. Trong khi một nghiên cứu trên ba trẻ em bị kerion [19] chứng minh lợi ích của việc sử dụng steroid đường uống, một nghiên cứu hồi cứu lớn hơn [20] không thấy lợi ích nào từ steroid đường uống hoặc tiêm trong tổn thương.
1.3.2 Liệu pháp điều trị
Bảng 16.1 Các liệu pháp điều trị đầu tiên
| Thuốc | Liều lượng | |
| Terbinafine | Dạng hạt: điều trị 6 tuần | A |
| <25 kg: 125 mg/ngày | ||
| 25–35 kg: 187,5 mg/ngày | ||
| >35 kg: 250 mg/ngày | ||
| Viên nén: điều trị 6 tuần | A | |
| 10–20 kg: 62,5 mg/ngày | ||
| 20–40 kg: 125 mg/ngày | ||
| >40 kg: 250 mg/ngày | ||
| Griseofulvin | Dạng rất nhỏ (viên nén hoặc hỗn dịch) | A |
| 20–25 mg/kg/ngày x 6–12 tuần với liều tối đa hàng ngày là 1.000 mg | ||
| Dạng cực nhỏ (chỉ viên nén) | A | |
| 10–15 mg/kg/ngày x 6–12 tuần với liều tối đa hàng ngày là 750 mg |
Bảng 16.2 Các liệu pháp điều trị thứ hai
| Thuốc | Liều lượng | |
| Fluconazole | 6 mg/kg/ngày × 3–6 tuần với liều tối đa hàng ngày là 400 mg | A |
| 6 mg/kg/tuần × 6–12 tuần (phác đồ theo nhịp) | B | |
| Itraconazole | 3–5 mg/kg/ngày × 4–6 tuần với liều tối đa hàng ngày là 400 mg | A |
| 3–5 mg/kg/ngày × 1 tuần mỗi tháng x 2–3 tháng (phác đồ theo nhịp) | B |
Bảng 16.3 Các liệu pháp điều trị thứ ba
| Thuốc | Liều lượng | |
| Dầu gội chống nấm | Bệnh nhân và người tiếp xúc gần trong gia đình: 2 lần một tuần trong 8 tuần | A |
| Selenium sulfide 1 % | ||
| Ciclopirox 1 % | ||
| Ketoconazole 2 % | B | |
| Glucocorticoid toàn thân (kerion) | Prednisone 0,5–1 mg/kg/ngày trong 1 tuần | E |
1.4 Nấm da thân mình, mặt, bẹn (Tinea Corporis, Faciei, Cruris)
Trong một phân tích tổng hợp, naftifine và terbinafine hiệu quả nhất trong việc đạt được sự khỏi bệnh về nấm và lâm sàng, hiệu quả là tương tự giữa azole và allylamine. Đối với nấm bẹn, sau 2 tuần điều trị tại chỗ, butenafine có hiệu quả khỏi bệnh về lâm sàng trên 79% trong khi terbinafine có hiệu quả 62%. Tỷ lệ khỏi bệnh về nấm của butenafine cũng cao hơn so với terbinafine (lần lượt là 94% và 62%). Ngoài ra, đáp ứng điều trị nhanh hơn với butenafine. Trong một nghiên cứu về điều trị toàn thân cho nấm thân mình, terbinafine hiệu quả hơn griseofulvin (87% so với 73%). Một nghiên cứu khác về nấm thân mình so sánh itraconazol với griseofulvin cho thấy tỷ lệ đáp ứng là 91% với itraconazol so với 64% đối với griseofulvin. Itraconazol cũng hữu ích hơn đáng kể trong đạt được sự khỏi bệnh về mặt nấm (87% so với 57%).
Liệu pháp điều trị
Bảng 16.4 Các liệu pháp điều trị đầu tiên
| Thuốc | Liều lượng | |
| Thuốc bôi allylamine | 1 -2 lần/ngày x 2–4 tuần | A |
| Terbinafine 1% | ||
| Kem hoặc gel Naftifine 1% | ||
| Thuốc bôi benzylamine | 1 lần/ngày x 2 tuần | B |
| Butenafine 1% | ||
| Terbinafine đường uống | Thời gian điều trị: 1–2 tuần | A |
| Dạng hạt | ||
| <25 kg: 125 mg/ngày | ||
| 25–35 kg: 187,5 mg/ngày | ||
| >35 kg: 250 mg/ngày | ||
| Viên nén | ||
| 10–20 kg: 62,5 mg/ngày | ||
| 20–40 kg: 125 mg/ngày | ||
| >40 kg: 250 mg/ngày | ||
| Itraconazole | Thời gian điều trị: 1 tuần | A |
| 3–5 mg/kg/ngày với liều tối đa hàng ngày là 200 mg |
Bảng 16.5 Các liệu pháp điều trị thứ hai
| Thuốc | Liều lượng | |
| Thuốc bôi azole: | Thời gian: 2–4 tuần | A |
| Kem Clotrimazole 1% | 2 lần/ngày | |
| Kem Econazol 1% | 1 lần/ngày | |
| Kem Ketoconazol 2% | 1 lần/ngày | |
| Kem Oxiconazol 1% | 1-2 lần/ngày | |
| Kem Sertaconazol 2% | 2 lần/ngày | |
| Kem Ciclopirox 0,77% | 2 lần/ngày | A |
| Kem Tolnaftate 1% | 2 lần/ngày | A |
| Fluconazol | Thời gian: 2–4 tuần | A* |
| 6 mg/kg 1lần/ tuần | ||
| Griseofulvin | Thời gian: 2–4 tuần | A |
| Dạng rất nhỏ: 10–20 mg/kg/ngày | ||
| Dạng cực nhỏ: 5–15 mg/kg/ngày |
1.5 Nấm da bàn chân, bàn tay (Tinea Pedis, Manuum)
Allylamines và butenafine là những thuốc bôi tại chỗ hiệu quả nhất trong điều trị nấm bàn chân. Tuy nhiên, allylamine chỉ hiệu quả hơn azole một chút. Ciclopirox, tolnaftate và undecanoates ít hiệu quả hơn azole và allylamine.
Một đánh giá hệ thống cho thấy allylamines có hiệu quả hơn một chút so với azole trong điều trị nấm bàn chân, và azole có hiệu quả hơn tolnaftate.
Itraconazol và terbinafine đường uống có hiệu quả như nhau trong điều trị nấm bàn chân. Terbinafine có hiệu quả hơn đáng kể so với griseofulvin, trong khi không thấy sự khác biệt đáng kể giữa fluconazole và itraconazole.
Bảng 16.6 Các liệu pháp điều trị đầu tiên
| Thuốc | Liều lượng | |
| Thuốc bôi allylamine | 1 - 2 lần/ngày trong 4 tuần | A |
| Terbinafine 1% | ||
| Kem hoặc gel Naftifine 1% | ||
| Thuốc bôi benzylamine | 2 lần/ngày trong 4 tuần | A |
| Butenafine 1% | ||
| Terbinafine đường uống | Thời gian điều trị: 2 tuần | A |
| Dạng hạt | ||
| <25 kg: 125 mg/ngày | ||
| 25–35 kg: 187,5 mg/ngày | ||
| >35 kg: 250 mg/ngày | ||
| Viên nén | ||
| 10–20 kg: 62,5 mg/ngày | ||
| 20–40 kg: 125 mg/ngày | ||
| >40 kg: 250 mg/ngày | ||
| Itraconazole | Thời gian điều trị: 1 tuần | A |
| 3–5 mg/kg/ngày với liều tối đa hàng ngày 200 mg |
Bảng 16.7 Các liệu pháp điều trị thứ hai
| Thuốc | Liều lượng | |
| Thuốc bôi azole | Thời gian: 4 tuần | A |
| Kem Clotrimazole 1% | 2 lần/ngày | |
| Kem Econazole 1% | 1 lần/ngày | |
| Kem Ketoconazole 2% | 1 lần/ngày | |
| Kem Oxiconazole 1% | 1 -2 lần/ngày | |
| Kem Sertaconazole 2% | 2 lần/ngày | |
| Kem Ciclopirox 0,77% | 2 lần/ngày | A |
| Kem Tolnaftate 1% | 2 lần/ngày | A |
| Fluconazole | 2–4 tuần | A |
| 6 mg/kg 1lần/tuần | ||
| Griseofulvin | 4–8 tuần | A |
| Dạng rất nhỏ: 10– 20 mg/kg/ngày | ||
| Dạng cực nhỏ: 5– 15 mg/kg/ngày |
1.6 Nấm móng do dermatophyte (Tinea Unguium)
1.6.1 Chiến lược quản lý
Nấm móng phổ biến ở người lớn nhưng ít gặp hơn ở trẻ em dưới 18 tuổi, nên các bằng chứng đến từ các thử nghiệm trên bệnh nhân người lớn. Tỷ lệ phần trăm khỏi bệnh về nấm (theo thứ tự giảm dần), dựa trên phác đồ liều thuốc tiêu chuẩn cho người lớn, là 76% đối với terbinafine, 63% đối với itraconazole liệu pháp xung, 60% đối với griseofulvin, 59% đối với itraconazole liệu pháp liên tục và 48% đối với fluconazole [31].
Một đánh giá tiến cứu về nấm móng ở trẻ em chứng minh sự hiếm gặp của tình trạng này ở trẻ dưới 18 tuổi. Trong một nghiên cứu cỡ mẫu nhỏ gồm 17 bệnh nhân, cho thấy thuốc uống tốt hơn thuốc bôi tại chỗ. Trong số các thuốc uống, terbinafine tốt hơn itraconazole, là loại tốt hơn fluconazole. Mức độ bằng chứng là A đối với việc sử dụng đường uống các thuốc này ở người lớn bị nấm móng.
Trong một nghiên cứu trên trẻ em dưới 18 tuổi sử dụng dung dịch sơn móng tay ciclopirox 8%, 77% đạt được khỏi bệnh về nấm và 71% có đáp ứng lâm sàng. Ở người lớn, dung dịch efinaconazol 10% cho thấy tỷ lệ khỏi bệnh về nấm lên tới 55,2% và khỏi bệnh hoàn toàn lên tới 17,8% sau 48 tuần điều trị hàng ngày trong các nghiên cứu đa trung tâm, ngẫu nhiên, mù đôi.
Một thử nghiệm với mỡ Bạc Hà Vicks Vaporub (dầu Khuynh Diệp, Long Não, tinh dầu bạc hà, thymol và dầu nhựa thông, nhục đậu khấu và lá tuyết tùng) cho thấy 27,8% bệnh nhân khỏi bệnh về lâm sàng và nấm sau 48 tuần bôi hàng ngày. Laser Nd:Yag 1.064 nm, được thực hiện trong 4 hoặc 8 lần điều trị hàng tuần, có hiệu quả lên tới 68% về mặt đáp ứng lâm sàng. Cả hai nghiên cứu chỉ được thực hiện ở bệnh nhân người lớn.
1.6.2 Liệu pháp điều trị
Bảng 16.8 Các liệu pháp điều trị đầu tiên
| Thuốc | Liều lượng | |
| Terbinafine | Móng chân: 12 tuần | C/A* |
| Móng tay: 6 tuần | ||
| 10–20 kg: 62,5 mg/ngày | ||
| 20–40 kg: 125 mg/ngày | ||
| >40 kg: 250 mg/ngày | ||
| Itraconazole | Móng chân: 12–16 tuần | C/A* |
| Móng tay: 18–26 tuần | ||
| <20 kg: 5 mg/kg/ngày | ||
| 20–40 kg: 100 mg mỗi ngày | ||
| 40–50 kg: 200 mg mỗi ngày | ||
| >50kg: 200 mg x 2 lần/ngày | ||
| Fluconazole | Móng chân: 18–26 tuần | C/A* |
| Móng tay: 12–16 tuần | ||
| 3–6 mg/kg 1lần/ tuần |
Bảng 16.9 Các liệu pháp điều trị thứ hai
| Thuốc | Liều lượng | |
| Dung dịch sơn móng tay Ciclopirox 8% | Hàng ngày trong 32 tuần | A |
| Dung dịch Efinaconazol 10% | Hàng ngày trong 48 tuần | A* |
Bảng 16.10 Các liệu pháp điều trị thứ ba
| Thuốc | Liều lượng | |
| Mỡ bạc hà (Vicks VapoRub) | Hàng ngày trong 48 tuần | C* |
| Liệu pháp laser | B* |
2 Lang ben (Tinea Versicolor)
2.1 Đặc điểm lâm sàng
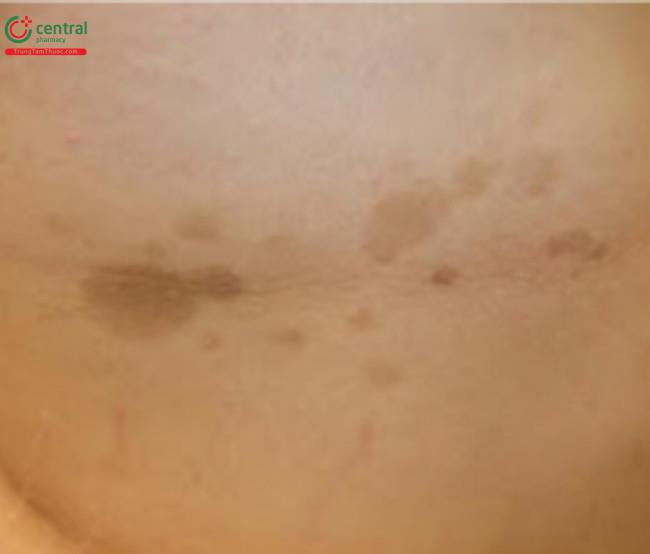
Lang ben do nấm men Malassezia gây ra, loại nấm sống hội sinh bình thường trên da, nhưng trở thành bệnh lý khi dạng nấm men biến đổi thành sợi nấm dưới điều kiện nhiệt, mồ hôi, da nhờn hoặc ức chế miễn dịch. Biểu hiện phổ biến là các dát và mảng nhỏ, tróc vảy, tăng sắc tố hoặc giảm sắc tố, thường gặp nhất là ở thân mình và vai (Hình 16.8). Đôi khi, có thể thấy tổn thương ở các vùng kẽ, và ở đầu và cổ ở trẻ nhỏ hơn (Hình 16.9). Sự thay đổi sắc tố sau viêm có thể trở thành mãn tính.
2.2 Cận lâm sàng được đề xuất
| Để chẩn đoán |
| Soi tươi với KOH |
| Nuôi cấy nấm |
| Mô bệnh học |
| Để điều trị (với thuốc chống nấm toàn thân) |
| CBC |
| LFT |
Soi tươi với KOH cho thấy sợi nấm ngắn và các cụm bào tử (“dạng mì spaghetti và thịt viên”). Nuôi cấy nấm không đặc hiệu để chẩnđoán và không được khuyến khích vì Malassezia là vi sinh vật bình thường trên da. Sinh thiết da để xác định mô bệnh học có hoặc không có PAS thường không cần thiết nhưng lại rất chính xác trong việc khẳng định chẩn đoán, cho thấy nhiều vi sinh vật ở lớp sừng, đi kèm không viêm hoặc viêm ít.
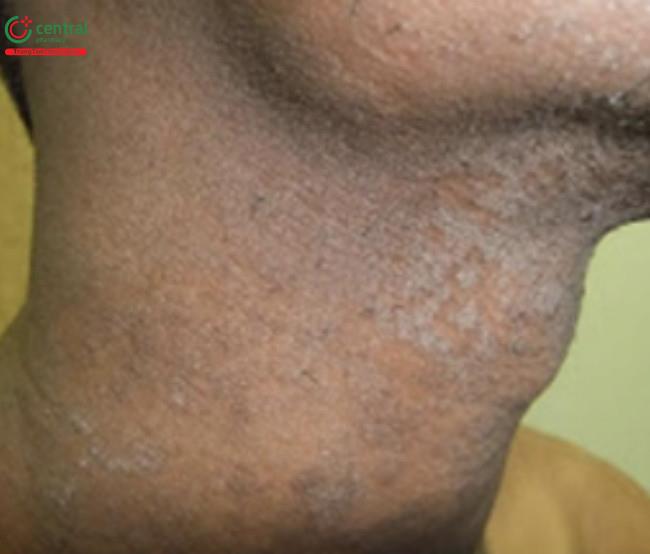
có vảy mịn trên vùng cổ của một nam thanh niên.
Do thời gian điều trị bằng thuốc chống nấm toàn thân rất ngắn nên làm xét nghiệm đánh giá là không cần thiết. Ở những bệnh nhân có bất thường về huyết học và gan từ trước hoặc ở những bệnh nhân cần điều trị nhiều đợt cho bệnh kháng trị, nên đánh giá CBC và LFT.
2.3 Chiến lược quản lý
Nói chung, liệu pháp bôi tại chỗ là phương pháp điều trị được lựa chọn cho lang ben. Tuy nhiên, một đánh giá hệ thống về các thử nghiệm có đối chứng cho thấy hầu hết các nghiên cứu đều thiếu phát hiện về sự khác biệt có ý nghĩa thống kê, mặc dù hầu hết các thuốc bôi tại chỗ đều có hiệu quả so với giả dược. Liệu pháp toàn thân có hiệu quả cao nhưng thường dành cho người lớn với bệnh kháng trị hoặc tái phát, bằng chứng từ các thử nghiệm đánh giá điều trị toàn thân ở trẻ em vẫn chưa có. Phác đồ hiệu quả nhất dựa trên đánh giá các nghiên cứu ở người lớn là itraconazole (200 mg/ngày trong 5–7 ngày), fluconazole (300 mg/tuần trong 2 tuần) và pramiconazole (200 mg/ngày trong 2 ngày) [37, 38].
Trong các nghiên cứu gồm cả bệnh nhân người lớn và trẻ em lớn tuổi, kem ketoconazol cho kết quả đáp ứng lâm sàng 98% và tỷ lệ khỏi bệnh về nấm là 84% so với giả dược. Dầu gội ketoconazol cũng có hiệu quả, với đáp ứng lâm sàng tương đương giữa việc dùng một lần và phác đồ điều trị 3 ngày (hiệu quả 73% so với 69%). Kem terbinafine 1% bôi tại chỗ chứng minh khả năng làm sạch nấm ở 81% bệnh nhân và đáp ứng lâm sàng ở 72% bệnh nhân lang ben. 77% bệnh nhân được điều trị bằng kem ciclopirox, so với 45% bệnh nhân được điều trị bằng clotrimazole, đã khỏi bệnh về lâm sàng và về nấm.
Trong một nghiên cứu ngẫu nhiên cho thấy lotion selen sulfide 2,5% tốt hơn giả dược; trong thực hành lâm sàng, dầu gội selen sulfide 2,5% thường được kê đơn hơn. Một nghiên cứu khác cho thấy dầu gội Kẽm pyrithione tốt hơn so với dầu gội thường, tất cả các bệnh nhân được điều trị đều cho thấy đáp ứng lâm sàng.
Những phương pháp sau không được dùng phổ biến để điều trị lang ben nhưng các nghiên cứu cũ cho thấy hiệu quả tốt. Trong một thử nghiệm, thuốc mỡ Whitfield có hiệu quả tương đương so với kem clotrimazole 1%, với tỷ lệ khỏi bệnh về nấm là 80%. Dầu gội sulfur-salicylic giúp khỏi bệnh về nấm ở 86% bệnh nhân lang ben. Một nghiên cứu nhỏ hơn trên 20 bệnh nhân sử dụng propylene glycol 50% trong nước 2 lần/ngày cho thấy tất cả bệnh nhân đều có đáp ứng lâm sàng, chỉ 10% có cảm giác bỏng rát nhẹ sau khi bôi.
2.4 Liệu pháp điều trị
Bảng 16.11 Các liệu pháp điều trị thứ nhất
| Thuốc | Liều lượng | |
| Kem Ketoconazole 2% | 1 lần / ngày × 11–22 ngày | A |
| Dầu gội Ketoconazole 2% | Dùng một lần hoặc hàng ngày × 3 ngày | A |
| Kem Terbinafine 1% | 2 lần / ngày × 1 tuần | A |
| Kem Ciclopirox olamine 1% | 2 lần / ngày × 14 ngày | A |
Bảng 16.12 Các liệu pháp điều trị thứ hai
| Thuốc | Liều lượng | |
| Lotion Selenium sulfide 2,5% | 1 lần / ngày × 7 ngày | A* |
| Dầu gội Selenium sulfide 2,5% | 1 lần / ngày × 7 ngày | E |
| Dầu gội kẽm pyrithione 1% | 1 lần / ngày × 14 ngày | A* |
Bảng 16.13 Các liệu pháp điều trị thứ ba
| Thuốc | Liều lượng | |
| Thuốc mỡ Whitfield (axit salicylic 3% và axit benzoic 6%) | 2 lần/ngày × 4 tuần | A |
| Dầu gội lưu huỳnh- axit salicylic | 1 lần/ngày × 7 ngày | A |
| Propylene glycol 50% trong nước | 2 lần/ngày × 2 tuần | B |
| Dầu gội Selenium sulfide 1% (không kê đơn) | 1 lần/ngày × 7 ngày | E |
3 Nấm da đen (Tinea Nigra)
3.1 Đặc điểm lâm sàng
Nấm da đen là một bệnh nhiễm nấm không triệu chứng hiếm gặp ở lòng bàn tay hoặc lòng bàn chân, do nấm men đen Hortaea werneckii gây ra, biểu hiện dưới dạng các dát hoặc mảng sắc tố, thường phân bố một bên, và phổ biến hơn ở các vùng nhiệt đới [48].
3.2 Cận lâm sàng được đề xuất
| Để chẩn đoán |
| Soi tươi với KOH |
| Soi da |
| Mô bệnh học |
| Để điều trị |
| Không cần xét nghiệm cụ thể |
Khám lâm sàng và soi tươi với KOH là đủ để chẩn đoán trong hầu hết các trường hợp, mối lo ngại lâm sàng phổ biến nhất là nevus acral hoặc u hắc tố (melanoma). Soi da là một phương pháp không xâm lấn hữu ích để hỗ trợ phân biệt các tổn thương tế bào hắc tố và gợi ý chẩn đoán trong hơn 50% trường hợp. Dấu hiệu với soi da gồm các sợi mịn, màu nâu nhạt ở bề mặt tạo thành một mảng dạng lưới có màu nâu đồng nhất; không giống như các tổn thương tế bào hắc tố, các rãnh và đường gờ không được theo dõi [49]. Sinh thiết da thường được thực hiện để loại trừ tân sinh tế bào hắc tố và mang tính chẩn đoán xác định, cho thấy nhiều sợi nấm sắc tố trong lớp sừng.
3.3 Chiến lược quản lý
Điều trị nhiễm nấm nông này phần lớn dựa trên các báo cáo trường hợp, thiếu các nghiên cứu và thử nghiệm dựa trên bằng chứng.
3.4 Liệu pháp điều trị
Bảng 16.14 Các liệu pháp điều trị đầu tiên
| Thuốc | Liều lượng | |
| Gel Ciclopirox olamine 0,77 % | 3 lần / ngày × 3 ngày | E* |
Bảng 16.15 Các liệu pháp điều trị thứ hai
| Thuốc | Liều lượng | |
| Kem isoconazol | 2 lần / ngày × 20-30 ngày | E* |
| Kem Terbinafine 1% | 1 lần / ngày × 15 ngày | E* |
| Kem Ketoconazol 2% | 2 lần / ngày × 15 ngày | D |
| Thuốc mỡ Whitfield (axit salicylic 3% và axit benzoic 6%) | 2 lần / ngày × 18 ngày | D |
Bảng 16.16 Các liệu pháp điều trị thứ ba
| Thuốc | Liều lượng | |
| Không điều trị (theo dõi) | D |
4 Nấm tóc Piedra (Piedra)
4.1 Đặc điểm lâm sàng
Nấm tóc Piedra là một nhiễm nấm nông không có triệu chứng, giới hạn ở thân tóc. Piedra đen do nấm đen Piedraia hortae gây ra, có đặc điểm là các nốt cứng màu đen hoặc kết tụ của tóc trên da đầu, và phổ biến nhất ở các vùng nhiệt đới. Ngược lại, piedra trắng do loài Trichosporon gây ra, tạo ra các kết tụ trắng mềm ở da đầu cũng như lông mu, nách và mặt, phổ biến nhất ở vùng khí hậu ôn đới.
Một số loài Trichosporon như T. asahii có liên quan đến nhiễm nấm xâm lấn ở bệnh nhân suy giảm miễn dịch; các biểu hiện ở da được thấy ở 1/3 số bệnh nhân, bao gồm các nốt xuất huyết, các sẩn lan tỏa và bọng nước. Bối cảnh lâm sàng phổ biến nhất của nhiễm nấm xâm lấn là giảm bạch cầu; các tình trạng khác gồm AIDS, bỏng, đặt ống thông tiểu, liệu pháp corticosteroid và phẫu thuật van tim, là những yếu tố nguy cơ. Nhiễm nấm xâm lấn thường gây tử vong [53–55].
4.2 Cận lâm sàng được đề xuất
| Để chẩn đoán |
| Soi tươi với KOH |
| Nuôi cấy nấm |
| Để điều trị |
| Không cần xét nghiệm cụ thể |
Những sợi tóc bị nhiễm nấm được xử lý với KOH và được kiểm tra dưới kính hiển vi [53]. Ở Piedra trắng, các khối kết tụ lỏng lẻo được nhuộm tối màu hình thành bởi các sợi nấm có vách ngăn, bào tử nấm. Ở Piedra đen, thấy các nốt màu nâu đen, là các khối chặt gồm các sợi nấm có vách ngăn, thành dày, và bào tử.
Nuôi cấy nấm thường không cần thiết trong các trường hợp nhiễm nấm nông, nhưng rất quan trọng trong các trường hợp nhiễm nấm xâm lấn do loài Trichosporon [56]. P. hortae phát triển trên môi trường thạch Sabouraud dextrose, cũng như môi trường chứa cycloheximide (môi trường thạch Mycosel và môi trường thử nghiệm dermatophyte). Tuy nhiên, loài Trichosporon bị ức chế bởi cycloheximide và do đó nên nuôi cấy trên môi trường thạch Sabouraud dextrose ở 28–30 °C.
4.3 Piedra trắng (White Piedra)
Hướng dẫn của Học viện Da liễu Hoa Kỳ công bố năm 1996 nêu rõ phương pháp điều trị được lựa chọn cho cả nấm tóc Piedra trắng và đen là loại bỏ tất cả tóc bị nhiễm nấm bằng cách cạo hoặc cắt. Tuy nhiên, đây thường không phải là lựa chọn điều trị được bệnh nhân chấp nhận, và do đó, các phương pháp điều trị bằng thuốc kháng nấm đường uống và bôi tại chỗ được nghiên cứu. Trong một nghiên cứu hồi cứu trên 8 trẻ em, tất cả đều cho thấy sạch tổn thương nấm da đầu khi sử dụng kết hợp thuốc kháng nấm đường uống và dầu gội ketoconazole 2%, mà không cần cạo tóc. Trong một thử nghiệm với itraconazole đường uống 100 mg/ngày, 11 trong số 12 bệnh nhân nữ cho thấy sạch tổn thương về mặt lâm sàng và nấm của nhiễm nấm da đầu sau 8 tuần điều trị với itraconazole đường uống. Không cần phải cạo tóc.
Hướng dẫn của Học viện Da liễu Hoa Kỳ cũng báo cáo về các phương pháp điều trị tại chỗ bên cạnh việc loại bỏ tóc. Ở những bệnh nhân dị ứng với azole, các thuốc chống nấm bôi tại chỗ thay thế bao gồm kem ciclopirox olamine, bọt selenium sulfide 2%, Lưu Huỳnh kết tủa 6% trong Vaseline trắng, dung dịch amphotericin B và thuốc bôi Castellani. Việc loại bỏ hoàn toàn thường khó khăn với tỉa hoặc cạo tóc, và các xét nghiệm nuôi cấy tiếp theo có thể vẫn dương tính mặc dù đã sạch tổn thương trên lâm sàng.
Liệu pháp điều trị
Bảng 16.17 Các liệu pháp điều trị đầu tiên
| Thuốc | Liều lượng | |
| Cạo hoặc cắt tóc | D* | |
| Dầu gội Itraconazole và Ketoconazole 2% | Itraconazole: 100 mg /ngày × 1 tháng | D |
| Ketoconazole: mỗi ngày × 2 tháng | ||
| Itraconazole | 100 mg/ngày × 4–8 tuần (cho đến khi kết quả nuôi cấy âm tính) | C* |
Bảng 16.18 Các liệu pháp điều trị thứ hai
| Thuốc | Liều lượng | |
| Dầu gội hoặc kem Ketoconazole 2% trên vùng da bị ảnh hưởng đã cạo hoặc cắt tóc trước đó | 1 lần / ngày trong vài tháng cho đến khi sạch hoàn toàn | D |
| Kem Miconazole 2%, kem isoconazole hoặc kem econazole nitrate 1%, trên vùng da bị ảnh hưởng đã cạo hoặc cắt tóc trước đó | 1 lần / ngày trong vài tháng cho đến khi sạch hoàn toàn | D |
4.4 Piedra đen (Black Piedra)
4.4.1 Liệu pháp điều trị
Bảng 16.19 Các liệu pháp điều trị đầu tiên
| Thuốc | Liều lượng | |
| Cạo hoặc cắt tỉa tóc | D* |
Bảng 16.20 Các liệu pháp điều trị thứ hai
| Thuốc | Liều lượng | |
| Terbinafine đường uống | 250 mg/ngày × 6 tuần | E |
| Thuốc chống nấm bôi tại chỗ sau khi cạo hoặc cắt tóc | 1 lần/ ngày trong vài tháng cho đến khi sạch hoàn toàn | E |
5 Nhiễm nấm Candida (Candidiasis)
5.1 Đặc điểm lâm sàng
Nhiễm nấm Candida ở trẻ em biểu hiện với nhiều triệu chứng khác nhau, từ nhiễm nấm niêm mạc khu trú đến lan rộng toàn thân [62– 64]. Các loài Candida là một phần của hệ vi sinh bình thường, nhưng trở nên gây bệnh khi chúng phát triển quá mức trong bối cảnh mất cân bằng của các vi sinh vật khác, suy giảm miễn dịch hoặc lây lan qua đường máu ở những bệnh nhân có van tim nhân tạo hoặc đặt ống thông hệ thần kinh trung ương.
Nhiễm nấm Candida vùng hầu họng (tưa miệng) phổ biến ở trẻ nhỏ, nhưng cũng có thể gặp ở trẻ lớn hơn sau một đợt điều trị với kháng sinh hoặc steroid, hoặc trong bối cảnh suy giảm miễn dịch như HIV/AIDS hoặc hóa trị. Các mảng giả màng màu trắng trên vòm miệng và lưỡi là phổ biến nhất. Ít phổ biến hơn, viêm lưỡi teo cấp tính có thể dẫn đến lưỡi đau, đỏ và nhẵn. Nhiễm nấm có thể không có triệu chứng hoặc đi kèm với chứng khó nuốt. Viêm góc miệng gây ra vết nứt, đau ở khóe miệng, thường do độ ẩm quá mức hoặc liếm.
Viêm da vùng tã do Candida cũng rất phổ biến ở trẻ nhỏ, biểu hiện là ban đỏ hợp lưu kèm theo sẩn, mụn mủ và các tổn thương vệ tinh ở vùng đùi. Viêm da vùng tã dai dẳng hoặc khó trị có thể là dấu hiệu của tình trạng thiếu hụt miễn dịch, suy giảm miễn dịch tiềm ẩn, hoặc nhiễm nấm Candida niêm mạc mạn tính (CMCC).
Viêm vùng kẽ do Candida xảy ra ở các vùng gấp dễ tích tụ độ ẩm, và có các bề mặt tiếp xúc gần nhau như cổ, nách và nếp gấp giữa hai mông. Tương tự như viêm da vùng tã, các mảng đỏ và bị ngâm nước với các tổn thương vệ tinh, mụn mủ và vết trợt là phổ biến.
Viêm âm hộ âm đạo có thể xảy ra ở trẻ nhỏ hoặc thanh thiếu niên [64]. Ở trẻ nhỏ, tã, thuốc kháng sinh và suy giảm miễn dịch đều là các yếu tố nguy cơ. Ở thanh thiếu niên, dụng cụ tránh thai, thuốc tránh thai đường uống và mang thai là các yếu tố dẫn đến. Các đặc điểm lâm sàng bao gồm ban đỏ, sưng tấy và dịch tiết màu trắng đặc hoặc loãng như nước. Các triệu chứng kèm theo bao gồm đau, ngứa và tiểu khó. Tương tự, viêm bao quy đầu có thể được thấy ở trẻ nhỏ hoặc thanh thiếu niên và biểu hiện dưới dạng các mảng trắng hoặc đỏ, đôi khi có vết trợt, trên dương vật.
Trẻ sơ sinh, trẻ em bị suy giảm miễn dịch và trẻ em nhập viện tại các đơn vị chăm sóc tích cực (ICU) có nguy cơ bị nhiễm nấm Candida máu và nhiễm nấm Candida toàn thân [65]. Ở trẻ sơ sinh, các yếu tố nguy cơ bao gồm cân nặng khi sinh cực thấp hoặc rất thấp (dưới 1000 g hoặc dưới 1500 g), sinh non, sử dụng kháng sinh phổ rộng hoặc các thủ thuật xâm lấn. Lây truyền dọc là do viêm âm đạo của mẹ, lây nhiễm âm đạo nặng hoặc cho con bú. Lây truyền ngang là do lây lan từ nhân viên y tế và thường liên quan đến các bề mặt bị nhiễm. Các yếu tố đưa đến nhiễm nấm Candida máu ở người suy giảm miễn dịch bao gồm bệnh ác tính về huyết học, giảm bạch cầu trung tính, hóa trị và kháng sinh. Bệnh nhân trong ICU có nguy cơ đặc biệt cao trong trường hợp bỏng, chấn thương, đặt ống thông, sử dụng kháng sinh, chạy thận nhân tạo và thở máy.
Các dấu hiệu và triệu chứng của nhiễm trùng huyết ngoài suy tạng cũng có thể được nhìn thấy. Biểu hiện ngoài da bao gồm các cụm mụn mủ không đau trên nền đỏ, có hoặc không có hoại tử, phát ban dạng dát, áp xe da và nốt xuất huyết do tắc mạch nhiễm trùng [66].
Nhiễm nấm Candida bẩm sinh biểu hiện với các dát hoặc sẩn nhỏ lan rộng trên nền đỏ, tiến triển thành mụn mủ hoặc mụn nước [67]. Thường gặp ở lòng bàn tay, lòng bàn chân và dây rốn. Ở trẻ nhỏ khỏe mạnh, các tổn thương da sẽ tự khỏi trong vòng một tuần và có thể được điều trị bằng thuốc bôi tại chỗ. Tuy nhiên, trẻ sơ sinh sinh non có nguy cơ nhiễm trùng toàn thân và nên được điều trị theo kinh nghiệm đối với nhiễm nấm Candida máu cho đến khi loại trừ được nhiễm trùng toàn thân.
CMCC là một nhóm các rối loạn không đồng nhất được đặc trưng bởi các khiếm khuyết miễn dịch di truyền dẫn đến nhiễm Candida không xâm lấn mạn tính, dai dẳng và khó trị ở da, niêm mạc và móng. Bệnh nội tiết tự miễn thường đi kèm. Các đột biến liên quan bao gồm AIRE (bộ điều hòa tự miễn dịch) [68], STAT1 [69], IL17RA (thụ thể alpha Interleukin 17) [70], Lyp [71], Dectin-1 [72] và TLR3 (thụ thể giống toll 3).
Các đột biến trong AIRE có liên quan đến bệnh đa nội tiết tự miễn -nhiễm nấm Candida loạn sản ngoại bì (APECED), đặc trưng bởi suy tuyến cận giáp, suy tuyến thượng thận, tiểu đường loại 1, bạch biến và rụng tóc từng vùng trong số các vấn đề tự miễn tiềm ẩn liên quan. CMCC thường khởi phát ở thời thơ ấu, mặc dù điều này thường thay đổi [68].
5.2 Cận lâm sàng được đề xuất
| Để chẩn đoán |
| Soi tươi với KOH |
| Nuôi cấy nấm |
| Mô bệnh học |
| Xét nghiệm di truyền (đối với CMCC) |
| Để điều trị |
| Công thức máu toàn phần (CBC) |
| Xét nghiệm chức năng gan (LFTs) |
| Các xét nghiệm khác: chức năng thận (nitơ urê máu và creatinin) và xét nghiệm chuyển hóa (đường huyết, kali), điện tâm đồ (ECG) |
Các loài Candida khác nhau nói chung đều có khả năng gây ra tất cả các hội chứng lâm sàng, dù nhiễm C. albicans là phổ biến nhất.
Đối với các trường hợp nhiễm nấm da và niêm mạc không phức tạp, có thể thực hiện soi tươi với KOH để xác nhận sự hiện diện của nấm men đang nảy chồi có hoặc không có sợi nấm. Nuôi cấy trong trường hợp này không bắt buộc, nhưng nên được thực hiện trong trường hợp nhiễm nấm niêm mạc da khó điều trị hoặc kháng thuốc để xác định các loài có khả năng kháng nhóm azole. C. glabrata và C. krusei ít nhạy cảm hơn với thuốc kháng nấm azole, và C. lusitaniae có thể kháng amphotericin B.
Sinh thiết da không bắt buộc đối với các trường hợp nhiễm trùng niêm mạc không phức tạp, nhưng cho kết quả chính xác, và thường cho thấy nhiều vi sinh vật trong lớp sừng và đôi khi cả biểu mô. Sinh thiết bấm lỗ cũng có thể hữu ích trong các trường hợp nhiễm trùng xâm lấn hoặc lan rộng, thường cho thấy áp xe, nấm men và sợi nấm, và có thể được sử dụng để lấy mô nuôi cấy [63].
Candida trong nuôi cấy máu không nên được coi là chất gây nhiễm và luôn phải thúc đẩy việc tìm kiếm nguồn gốc của nhiễm nấm máu. Ở một số bệnh nhân, nhiễm Candida máu là biểu hiện của nhiễm nấm Candida lan tỏa, trong khi ở những bệnh nhân khác, nó phản ánh sự xâm nhiễm của ống thông tĩnh mạch đặt cố định. Vì độ nhạy của một lần cấy máu là thấp trong việc phát hiện nhiễm nấm Candida lan tỏa, nên cần thực hiện nhiều lần hoặc lặp lại cấy máu. Nếu có ống thông đặt cố định, cần lấy mẫu cấy qua ống thông và mạch máu ngoại vi để phân biệt giữa nhiễm trùng lan tỏa và nhiễm nấm Candida liên quan đến ống thông. Cần lưu ý rằng, các loài Candida thường cần 1-4 ngày để phát triển trên môi trường nuôi cấy [73].
Các xét nghiệm kháng thể và kháng nguyên không đủ nhạy để sử dụng trong lâm sàng. Xét nghiệm Beta-D-glucan chứng minh độ nhạy cao, và PCR có độ đặc hiệu cao và nhạy như nuôi cấy máu, nhưng kinh nghiệm với các xét nghiệm này ở trẻ em còn hạn chế [74, 75].
Phân tích di truyền các đột biến gây bệnh có thể được sử dụng để xác nhận các trường hợp nghi ngờ mắc CMCC, nhưng không phải tất cả các đột biến di truyền đều được biết đến. Chẩn đoán dựa trên tập hợp các dấu hiệu lâm sàng hiện có. Kháng thể Candida trong huyết thanh không có giá trị trong chẩn đoán CMCC, cũng như các xét nghiệm IgE trên da hoặc huyết thanh đối với Candida.
Trước khi điều trị ngắn hạn bằng thuốc kháng nấm azole toàn thân ở trẻ em khỏe mạnh, không cần thiết phải thực hiện các xét nghiệm cận lâm sàng. Ở những bệnh nhân trải qua nhiều đợt điều trị, hoặc có tiền sử rối loạn chức năng gan hoặc bất thường về huyết học, nên thực hiện xét nghiệm chức năng gan (LFT) và công thức máu toàn phần (CBC). Các tác dụng phụ của amphotericin B bao gồm phản ứng truyền dịch, suy thận, hạ Kali máu và viêm cơ tim. Do đó, đối với những bệnh nhân đang điều trị bằng amphotericin, cần theo dõi chức năng thận (nitơ urê máu và creatinine), các chỉ số chuyển hóa (đường huyết, kali) và điện tâm đồ (ECG).
5.3 Nhiễm nấm Candida vùng hầu họng (Oropharyngeal Candidiasis)
Nystatin từ lâu được coi là phương pháp điều trị đầu tiên cho nhiễm nấm Candida vùng hầu họng, với dạng hỗn dịch cho thấy tỷ lệ chữa khỏi lên đến 80%. Các nghiên cứu về các thuốc điều trị tại chỗ khác (hỗn dịch, viên ngậm, gel) thường cho thấy hiệu quả tương tự hoặc tốt hơn. Trong một nghiên cứu, gel miconazole cho thấy hiệu quả vượt trội hơn đáng kể so với hỗn dịch nystatin trong khả năng chữa khỏi về lâm sàng (99% so với 54%) ở trẻ sơ sinh có hệ miễn dịch bình thường. Miconazole cũng vượt trội hơn trong việc tiêu diệt nấm men. Trong một nghiên cứu khác, hỗn dịch uống fluconazole cho thấy tỷ lệ chữa khỏi 100%, so với chỉ 32% chữa khỏi với hỗn dịch nystatin. Tuy nhiên, do hạn chế tự nhiên của nhiễm nấm Candida hầu họng ở trẻ sơ sinh có hệ miễn dịch bình thường, nystatin và clotrimazole được ưu tiên sử dụng làm thuốc điều trị đầu tiên. Cần lưu ý, không nên sử dụng viên ngậm nystatin và clotrimazole cho trẻ em dưới 4 tuổi vì chúng có thể gây nghẹn.
Ở trẻ nhỏ và trẻ em suy giảm miễn dịch, fluconazole cho tỷ lệ khỏi bệnh về lâm sàng là 91% và tỷ lệ khỏi bệnh về nấm là 76%, so với 51% khỏi bệnh về lâm sàng và 11% khỏi bệnh về nấm với nystatin. Fluconazole cũng vượt trội hơn nystatin trong đạt được sự khỏi bệnh về lâm sàng và nấm ở trẻ em nhiễm HIV và nhiễm nấm Candida hầu họng. Viên ngậm clotrimazole cho tỷ lệ khỏi bệnh tương tự như hỗn dịch fluconazole, nhưng fluconazole vượt trội hơn về tỷ lệ khỏi bệnh về nấm. Thuốc Tím gentian vượt trội hơn nystatin trong đạt được sự khỏi bệnh về lâm sàng, nhưng được ưu tiên sử dụng như liệu pháp điều trị thứ ba, do nguy cơ làm nhuộm màu môi và quần áo cũng như khả năng gây kích ứng và loét.
Liệu pháp điều trị
Bảng 16.21 Các liệu pháp điều trị đầu tiên
| Thuốc | Liều lượng | |
| Hỗn dịch Nystatin | Trẻ nhỏ: | A |
| <30 ngày tuổi: 50.000 đơn vị mỗi bên má, 4 lần / ngày x 7–14 ngày | ||
| >30 ngày tuổi: 100.000 đơn vị mỗi bên má, 4 lần / ngày x 7–14 ngày | ||
| Trẻ em trên 4 tuổi: | A | |
| 600.000 đơn vị, 4 lần / ngày x 7-14 ngày | ||
| 1 đến 2 viên ngậm (mỗi viên 200.000 đơn vị), 4 lần / ngày x 7-14 ngày | ||
| Clotrimazole | Trẻ em >4 tuổi: | A |
| Viên ngậm (10 mg), 5-6 lần / ngày x 7-14 ngày | ||
| Gel Miconazole (25 mg) | Gel Miconazole (25 mg) 4 lần / ngày trong 14 ngày | A |
Bảng 16.22 Các liệu pháp điều trị thứ hai
| Thuốc | Liều lượng | |
| Fluconazole | 6 mg/kg vào ngày 1, sau đó 3 mg/kg mỗi ngày trong 14 ngày, liều tối đa hàng ngày 200 mg | A |
Bảng 16.23 Các liệu pháp điều trị thứ ba
| Thuốc | Liều lượng | |
| Dung dịch tím gentian 0,5% hoặc 1% | Bôi 1 hoặc 2 lần/ngày trong 3 ngày | A |
5.4 Viêm da vùng kẽ và tã lót do nấm Candida (Candidal Intertrigo and Diaper Dermatitis)
Trong một thử nghiệm ngẫu nhiên trên hơn 90 trẻ nhỏ bị viêm da vùng tã do nhiễm nấm Candida, clotrimazole có hiệu quả khỏi bệnh ở 68% bệnh nhân, trong khi nystatin khỏi bệnh ở 47% bệnh nhân. Tuy nhiên, tỷ lệ khỏi bệnh về mặt nấm là 100% đối với cả hai loại thuốc. Trong một nghiên cứu mở, kem sertaconazole mang lại hiệu quả khỏi bệnh cả về lâm sàng và nấm ở hơn 88% trẻ nhỏ bị viêm da vùng tã do nấm Candida.
Miconazole cho thấy tỷ lệ khỏi bệnh về lâm sàng là 38% so với 11% ở nhóm đối chứng (giả dược), dù tỷ lệ khỏi bệnh về mặt nấm cao hơn. Ciclopirox, trong một nghiên cứu mở, cho hiệu quả khỏi bệnh về lâm sàng ở 50% trẻ nhỏ bị viêm da vùng tã do nấm Candida.
Trong trường hợp bệnh nặng hoặc kháng trị, liệu pháp kháng nấm azole đường uống có thể được sử dụng. Ketoconazole có hiệu quả nhưng không nên sử dụng do nguy cơ gây độc cho gan.
Liệu pháp điều trị
Bảng 16.24 Các liệu pháp điều trị đầu tiên
| Thuốc | Liều lượng | |
| Clotrimazole 1% | 2 lần / ngày x 14 ngày | A |
| Sertaconazole 2% | 2 lần / ngày x 14 ngày | B |
| Nystatin 100.000 IU | 2 lần / ngày x 14 ngày | A |
Bảng 16.25 Các liệu pháp điều trị thứ hai
| Thuốc | Liều lượng | |
| Miconazole 0,25% trong kẽm oxit/petrolatum | 2 lần / ngày x 7 ngày | A |
| Ciclopirox 0,77% | 2 lần / ngày x 7 ngày | B |
Bảng 16.26 Các liệu pháp điều trị thứ ba
| Thuốc | Liều dùng (thời gian: 2–6 tuần hoặc cho đến khi khỏi bệnh) | |
| Fluconazole | 6 mg/kg một lần, sau đó 3 mg/kg/ngày | E |
| Itraconazole | 5–10 mg/kg/ngày, chia làm hai liều | E |
5.5 Viêm âm hộ âm đạo do nấm Candida (Candidal Vulvovaginitis)
Trong một đánh giá hệ thống, không thấy sự khác biệt đáng kể về tỷ lệ khỏi bệnh về mặt nấm học hoặc lâm sàng giữa liệu pháp kháng nấm azole tại chỗ (đặt âm đạo) và toàn thân (uống) ngắn hạn. Trong các nghiên cứu mở và thử nghiệm ngẫu nhiên, fluconazole đường uống liều đơn và liệu trình clotrimazole đặt âm đạo trong 1 tuần đã cho thấy hiệu quả tương đương về tỷ lệ khỏi bệnh về lâm sàng (83–97%) và tỷ lệ khỏi bệnh về mặt nấm (70– 80%). Các thử nghiệm đối chứng ngẫu nhiên cũng cho thấy các liệu trình terconazole và miconazole ngắn, dưới dạng viên đặt âm đạo hoặc kem bôi tại chỗ, có hiệu quả tương đương trong đạt được sự khỏi bệnh về lâm sàng và nấm so với fluconazole đường uống liều đơn. Tuy nhiên, fluconazole vẫn là liệu pháp điều trị đầu tay được ưu tiên, do liều lượng thuận tiện, chi phí thấp và dễ sử dụng.
Trong bối cảnh viêm âm hộ âm đạo nặng, nhiễm các loài Candida khác ngoài C. Albicans như là C. glabrata, suy giảm miễn dịch hoặc tiền sử bệnh tái phát (hơn bốn lần mỗi năm), cần dùng liệu pháp tích cực hơn. Với bệnh nhân không thể dùng fluconazole, lựa chọn thay thế cho bệnh tái phát là dùng azole bôi tại chỗ trong 10-14 ngày và sau đó là viên đặt âm đạo clotrimazole 200 mg hàng tuần trong 6 tháng. Fluconazole liều đơn có hiệu quả 85%, phác đồ hai liều có hiệu quả 94% ở bệnh nhân bị viêm âm hộ âm đạo nặng nhưng không tái phát. Với bệnh nhân bị viêm âm hộ âm đạo tái phát, điều trị hàng tuần bằng fluconazole liều đơn có hiệu quả phòng ngừa trên 90% sau 6 tháng điều trị, và không gây ra tình trạng kháng thuốc ở các chủng phân lập lâm sàng. Những kết quả này, cùng với dữ liệu từ các nghiên cứu tương tự, đã được xác nhận thêm trong một đánh giá hệ thống.
Liệu pháp điều trị
Bảng 16.27 Các liệu pháp điều trị đầu tiên
| Thuốc | Liều lượng | |
| Fluconazole | 150 mg uống một lần | A |
Bảng 16.28 Các liệu pháp điều trị thứ hai
| Thuốc | Liều lượng | |
| Clotrimazole | Viên đặt âm đạo 200 mg mỗi ngày x 7 ngày | A |
| Viên đặt âm đạo 500 mg hoặc kem 10% liều đơn | B | |
| Terconazole | Kem 0,4–0,8% mỗi ngày x 7 ngày | A |
| Viên đặt âm đạo 80 mg mỗi ngày x 3 ngày | A | |
| Miconazole | Kem 2% mỗi ngày x 7 ngày | A |
| Thuốc đặt âm đạo cũng có sẵn |
Bảng 16.29 Các liệu pháp điều trị thứ ba
| Thuốc | Liều dùng (thời gian: 2–6 tuần hoặc cho đến khi khỏi bệnh) | |
| Fluconazole | Bệnh nặng: | A |
| 150 mg uống mỗi 3 ngày, tổng cộng 3 liều | ||
| Bệnh tái phát: | A | |
| 150 mg uống mỗi 3 ngày, tổng cộng 3 liều, sau đó: | ||
| 150 mg uống mỗi tuần, trong 6 tháng |
5.6 Nhiễm nấm Candida sơ sinh và toàn thân (Neonatal and Systemic Candidiasis)
5.6.1 Chiến lược quản lý
Điều quan trọng là, các thiết bị y tế nghi ngờ là ổ nhiễm trùng cần được loại bỏ ngay lập tức sau khi phát hiện nhiễm nấm Candida máu. Trong một nghiên cứu hồi cứu về trẻ sơ sinh bị nhiễm nấm Candida máu, việc không loại bỏ ống thông tĩnh mạch trung tâm đặt cố định có liên quan đến việc tăng gần 40% tỷ lệ tử vong [96].
Amphotericin B là thuốc được sử dụng phổ biến nhất dựa trên kinh nghiệm sử dụng, nhạy cảm với hầu hết các loài Candida trong ống nghiệm, và khả năng dung nạp ở trẻ sơ sinh bị nhiễm nấm Candida toàn thân hoặc lan tỏa.
Trong hai nghiên cứu mở, không có sự khác biệt đáng kể về mặt thống kê về tỷ lệ tử vong sau điều trị bằng fluconazole so với amphotericin B đối với nhiễm nấm Candida xâm lấn ở trẻ nhỏ. Tuy nhiên, một số loài như C. krusei, C. glabrata và C. parapsilosis thường kháng fluconazole. Vì lý do này, fluconazole không nên được sử dụng làm liệu pháp đơn trị đầu tiên hoặc theo kinh nghiệm. Thay vào đó, amphotericin B nên được sử dụng cho đến khi có kết quả nuôi cấy và độ nhạy cảm. Các chế phẩm amphotericin B gốc lipid được coi là ít gây độc cho thận hơn, nhưng dữ liệu hồi cứu cho thấy tỷ lệ tử vong cao hơn ở trẻ nhỏ bị nhiễm nấm Candida toàn thân được điều trị bằng amphotericin B gốc lipid so với những trẻ được điều trị bằng amphotericin B deoxycholate thông thường.
Dựa trên các đánh giá hồi cứu, caspofungin là một liệu pháp thay thế hiệu quả cho trẻ sơ sinh bị nhiễm nấm Candida máu dai dẳng hoặc nhiễm nấm Candida xâm lấn kháng trị. Trong một đánh giá hệ thống các thử nghiệm gồm 30 trẻ sinh non và không sinh non bị nhiễm nấm Candida xâm lấn, tỷ lệ điều trị thành công là 73% với micafungin.
Flucytosine không hữu ích khi dùng đơn trị liệu do gây ra tình trạng kháng thuốc nhanh chóng, nhưng hữu ích khi kết hợp với amphotericin B để điều trị nhiễm nấm Candida hệ thần kinh trung ương. Tuy nhiên, nồng độ thuốc phải được theo dõi chặt chẽ do nguy cơ ức chế tủy xương.
5.6.2 Liệu pháp điều trị
Bảng 16.30 Các liệu pháp điều trị đầu tiên
| Thuốc | Liều lượng | |
| Amphotericin B deoxycholate | Liều khởi đầu: 0,5 mg/kg, sau đó là 1 mg/kg/ngày tiêm tĩnh mạch | A |
| Thời gian điều trị: 14 ngày sau khi loại bỏ nấm hoặc cho đến khi đạt tổng liều tích lũy 25–30 mg/kg |
Bảng 16.31 Các liệu pháp điều trị thứ hai
| Thuốc | Liều dùng (thời gian: 14 ngày sau khi loại bỏ nấm) | |
| Fluconazole | Liều khởi đầu 25 mg/kg, sau đó là 12 mg/kg/ngày tiêm tĩnh mạch | B |
| Amphotericin B gốc lipid | 3–5 mg/kg/ngày tiêm tĩnh mạch | D |
Bảng 16.32 Các liệu pháp điều trị thứ ba
| Thuốc | Liều dùng (thời gian: 14 ngày sau khi loại bỏ nấm) | |
| Echinocandins | ||
| Caspofungin | Liều khởi đầu 70 mg/m2, sau đó 50 mg/m2/ngày tiêm tĩnh mạch, liều tối đa hàng ngày là 70 mg | D |
| Micafungin | 2–4 mg/kg/ngày tiêm tĩnh mạch | C |
| Flucyotosine (chỉ dùng đường uống) | Tổng cộng 50–150 mg/kg/ngày, chia làm 4 liều | D |
5.7 Nhiễm Candida mạn tính ở da niêm (Chronic Mucocutaneous Candidiasis)
Fluconazole là thuốc điều trị đầu tiên được ưu tiên, vì chủng được phân lập phổ biến nhất trong CMCC là C. Albicans. Tuy nhiên, tình trạng kháng fluconazole có thể xảy ra, đặc biệt là trong bối cảnh điều trị ức chế mạn tính.
Nếu tình trạng kháng fluconazole phátntriển, thì itraconazole,voriconazole hoặc posaconazole có thể được sử dụng để điều trị nhiễm nấm da.
Liệu pháp điều trị
Bảng 16.33 Các liệu pháp điều trị đầu tay
| Thuốc | Liều lượng (thời gian điều trị thay đổi tùy thuộc vào loại nhiễm nấm) | |
| Fluconazole | Liều khởi đầu 6 mg/kg đường uống (tối đa 200 mg), sau đó là 3 mg/kg/ngày đường uống (liều tối đa hàng ngày 100 mg) | D |
Bảng 16.34 Các liệu pháp điều trị thứ hai
| Thuốc | Liều lượng (thời gian điều trị thay đổi tùy thuộc vào loại nhiễm nấm) | |
| Itraconazole | 2,5 mg/kg/ngày uống 2 lần / ngày, liều tối đa hàng ngày là 200 mg | B |
| Voriconazole | 9 mg/kg uống 2 lần / ngày, liều tối đa hàng ngày là 350 mg | D |
| Posaconazole | 800 mg/ngày uống chia làm 2- 4 liều | D |
6 Tài liệu tham khảo
1. Hawkins DM, Smidt AC. Superficial fungal infections in children. Pediatr Clin North Am. 2014;61(2):443–55.
2.Kelly BP. Superficial fungal infections. Pediatr Rev. 2012;33(4):e22–37.
3. Weinberg JM, Koestenblatt EK, Tutrone WD, Tishler HR, Najarian L. Comparison of diagnostic methods in the evaluation of onychomycosis. J Am Acad Dermatol. 2003;49(2):193–7.
4. Lilly KK, Koshnick RL, Grill JP, Khalil ZM, Nelson DB, Warshaw EM. Cost-effectiveness of diagnostic tests for toenail onychomycosis: a repeated-measure, single-blinded, cross-sectional evaluation of 7 diagnostic tests. J Am Acad Dermatol. 2006;55(4):620–6.
5. Karimzadegan-Nia M, Mir-Amin-Mohammadi A, Bouzari N, Firooz A. Comparison of direct smear, culture and histology for the diagnosis of onychomycosis. Australas J Dermatol. 2007;48(1):18–21.
6. Ekiz O, Sen BB, Rifaioglu EN, Balta I. Trichoscopy in paediatric patients with tinea capitis: a useful method to differentiate from alopecia areata. J Eur Acad Dermatol Venereol. 2014;28(9): 1255–8.
7. Slowinska M, Rudnicka L, Schwartz RA, Kowalska-Oledzka E, Rakowska A, Sicinska J, et al. Comma hairs: a dermatoscopic marker for tinea capitis: a rapid diagnostic method. J Am Acad Dermatol. 2008;59(5 Suppl):S77–9.
8. Lacarrubba F, Verzi AE, Micali G. Newly described features resulting from high magnification dermoscopy of tinea capitis. JAMA Dermatol. 2015;151(3):308–10.
9. Gupta AK. Chapter 9: systemic antifungals. In: Wolverton SE, editor. Comprehensive dermatologic drug therapy. 3rd ed. Philadelphia: Elsevier; 2012.
10. Elewski BE, Cáceres HW, DeLeon L, El Shimy S, Hunter JA, Korotkiy N, et al. Terbinafine hydrochloride oral granules versus oral griseofulvin suspension in children with tinea capitis: results of two randomized, investigator blinded, multicenter, international, controlled trials. J Am Acad Dermatol. 2008;59(1):41.
11. Tey HL, Tan AS, Chan YC. Meta-analysis of randomized, controlled trials comparing griseofulvin and terbinafine in the treatment of tinea capitis. J Am Acad Dermatol. 2011;64(4):663.
12. Gupta AK, Drummond-Main C. Meta-analysis of randomized, controlled trials comparing particular doses of griseofulvin and terbinafine for the treatment of tinea capitis. Pediatr Dermatol. 2013;30(1):1–6.
13. Foster KW, Friedlander SF, Panzer H, Ghannoum MA, Elewski BE. A randomized controlled trial assessing the efficacy of fluconazole in the treatment of pediatric tinea capitis. J Am Acad Dermatol. 2005;53(5):798.
14. Dastghaib L, Azizzadeh M, Jafari P. Therapeutic options for the treatment of tinea capitis: griseofulvin versus fluconazole. J Dermatolog Treat. 2005;16(1):43–6.
15. Gupta AK, Dlova N, Taborda P, Morar N, Taborda V, Lynde CW. Once weekly fluconazole is effective in children in the treatment of tinea capitis: a prospective, multicentre study. Br J Dermatol. 2000;142(5):965–8.
16. Gupta AK, Adam P, Dlova N, Lynde CW, Hofstader S, Morar N, et al. Therapeutic options for the treatment of tinea capitis caused by Trichophyton species: griseofulvin versus the new oral antifungal agents, terbinafine, itraconazole, and fluconazole. Pediatr Dermatol. 2001;18(5):433–8.
17. López-Gómez S, Del Palacio A, Van Cutsem J, Soledad Cuétara M, Iglesias L, Rodriguez Noriega A. Itraconazole versus griseofulvin in the treatment of tinea capitis: a double-blind randomized study in children. Int J Dermatol. 1994;33(10):743–7.
18. Gupta AK, Cooper EA. Update in antifungal therapy of dermato- phytosis. Mycopathologia. 2008;166(5–6):353.
19. Chen C, Koch LH, Dice JE, Dempsey KK, Moskowitz AB, Barnes-Eley ML. A randomized, double-blind study comparing the efficacy of selenium sulfide shampoo 1% and ciclopirox sham- poo 1% as adjunctive treatments for tinea capitis in children. Pediatr Dermatol. 2010;27(5):459–62. Epub 2010 Aug 24.
20. Keipert JA. Beneficial effect of corticosteroid therapy in micros- porum canis kerion. Australas J Dermatol. 1984;25(3):127–30.
21. Proudfoot LE, Higgins EM, Morris-Jones R. A retrospective study of the management of pediatric kerion in Trichophyton tonsurans infection. Pediatr Dermatol. 2011;28(6):655–7.
22. El-Gohary M, van Zuuren EJ, Fedorowicz Z, Burgess H, Doney L, Stuart B. Topical antifungal treatments for tinea cruris and tinea corporis. Cochrane Database Syst Rev. 2014;8:CD009992.
23. Das S, Barbhuniya JN, Biswas I, Bhattacharya S, Kundu PK. Studies on comparison of the efficacy of terbinafine 1% cream and butenafine 1% cream for the treatment of Tinea cruris. Indian Dermatol Online J. 2010;1(1):8–9. doi:10.4103/2229-5178.73249.
24. Cole GW, Stricklin G. A comparison of a new oral antifungal, terbinafine, with griseofulvin as therapy for tinea corporis. Arch Dermatol. 1989;125(11):1537.
25. Bourlond A, Lachapelle JM, Aussems J, Boyden B, Campaert H, Conincx S, et al. Double-blind comparison of itraconazole with griseofulvin in the treatment of tinea corporis and tinea cruris. Int J Dermatol. 1989;28(6):410.
26. Faergemann J, Mörk NJ, Haglund A, Odegård T. A multicentre (double-blind) comparative study to assess the safety and efficacy of fluconazole and griseofulvin in the treatment of tinea corporis and tinea cruris. Br J Dermatol. 1997;136(4):575.
27. Bogaert H, Cordero C, Ollague W, Savin RC, Shalita AR, Zaias N. Multicentre double-blind clinical trials of ciclopirox olamine cream 1% in the treatment of tinea corporis and tinea cruris. J Int Med Res. 1986;14(4):210–6.
28. Crawford F, Hollis S. Topical treatments for fungal infections of the skin and nails of the foot. Cochrane Database Syst Rev. 2007;18:CD001434.
29. Hart R, Bell-Syer SE, Crawford F, Torgerson DJ, Young P, Russell I. Systematic review of topical treatments for fungal infections of the skin and nails of the feet. BMJ. 1999;319(7202):79– 82.
30. Bell-Syer SE, Khan SM, Torgerson DJ. Oral treatments for fungal infections of the skin of the foot. Cochrane Database Syst Rev. 2012;10:CD003584.
31. Gupta AK, Ryder JE, Johnson AM. Cumulative meta-analysis of systemic antifungal agents for the treatment of onychomycosis. Br J Dermatol. 2004;150(3):537.
32. Gupta AK, Sibbald RG, Lynde CW, Hull PR, Prussick R, Shear NH, et al. Onychomycosis in children: prevalence and treatment strategies. J Am Acad Dermatol. 1997;36(3 Pt 1):395.
33. Friedlander SF, Chan YC, Chan YH, Eichenfield LF. Onychomycosis does not always require systemic treatment for cure: a trial using topical therapy. Pediatr Dermatol. 2013; 30(3):316–22.
34. Elewski BE, Rich P, Pollak R, Pariser DM, Watanabe S, Senda H, et al. Efinaconazole 10% solution in the treatment of toenail onychomycosis: two phase III multicenter, randomized, double-blind studies. J Am Acad Dermatol. 2013;68(4):600.
35. Derby R, Rohal P, Jackson C, Beutler A, Olsen C. Novel treatment of onychomycosis using over the-counter mentholated ointment: a clinical case series. J Am Board Fam Med. 2011;24(1):69.
36. Zhang RN, Wang DK, Zhuo FL, Duan XH, Zhang XY, Zhao JY. Long-pulse Nd:YAG 1064- nm laser treatment for onychomycosis. Chin Med J (Engl). 2012;125(18):3288–91.
37. Hu SW, Bigby M. Pityriasis versicolor: a systematic review of interventions. Arch Dermatol. 2010;146(10):1132.
38. Gupta AK, Lane D, Paquet M. Systematic review of systemic treatments for tinea versicolor and evidence-based dosing regimen recommendations. J Cutan Med Surg. 2014;18(2):79–90.
39. Savin RC, Horwitz SN. Double-blind comparison of 2% ketoconazole cream and Placebo in the treatment of tinea versicolor. J Am Acad Dermatol. 1986;15(3):500.
40. Lange DS, Richards HM, Guarnieri J, Humeniuk JM, Savin RC, Reyes BA, et al. Ketoconazole 2% shampoo in the treatment of tinea versicolor: a multicenter, randomized, double-blind, placebo controlled trial. J Am Acad Dermatol. 1998;39(6):944.
41. Vermeer BJ, Staats CC. The efficacy of a topical application of terbinafine 1% solution in subjects with pityriasis versicolor: a placebo-controlled study. Dermatology. 1997;194 Suppl 1:22.
42. Treatment of tinea versicolor with a new antifungal agent, ciclopirox olamine cream 1%. Clin Ther. 1985;7(5):574.
43. Sánchez JL, Torres VM. Double-blind efficacy study of selenium sulfide in tinea versicolor. J Am Acad Dermatol. 1984;11(2 Pt 1):235.
44. Fredriksson T, Faergemann J. Double-blind comparison of a zinc pyrithione shampoo and its shampoo base in the treatment of tinea versicolor. Cutis. 1983;31(4):436–7.
45. Clayton R, Du Vivier A, Savage M. Double blind trial of 1% clotrimazole cream and Whitfield ointment in the treatment of pityriasis versicolor. Arch Dermatol. 1977;113(6):849–50.
46. Bamford JT. Treatment of tinea versicolor with sulfur-salicylic shampoo. J Am Acad Dermatol. 1983;8(2):211–3.
47. Faergemann J, Fredriksson T. Propylene glycol in the treatment of tinea versicolor. Acta Derm Venereol. 1980;60(1):92–3.
48. Bonifaz A, Badali H, de Hoog GS, Cruz M, Araiza J, Cruz MA, et al. Tinea nigra by Hortaea werneckii, a report of 22 cases from Mexico. Stud Mycol. 2008;61:77–82.
49. Piliouras P, Allison S, Rosendahl C, Buettner PG, Weedon D. Dermoscopy improves diagnosis of tinea nigra: a study of 50 cases. Australas J Dermatol. 2011;52(3):191–4.
50. Rosen T, Lingappan A. Rapid treatment of tinea nigra palmaris with ciclopirox olamine gel, 0.77%. Skinmed. 2006;5(4):201–3.
51. Rossetto AL, Cruz RC, Haddad JV. Double blind study with topical Isoconazole and Terbinafine for the treatment of one patient with bilateral Tinea nigra plantaris and suggestions for new differential diagnosis. Rev Inst Med Trop Sao Paulo. 2013; 55(2):125–8.
52. Bonifaz A, Badali H, de Hoog GS, Cruz M, Araiza J, Cruz MA, et al. Tinea nigra by Hortaea werneckii, a report of 22 cases from Mexico. Stud Mycol. 2008;61:77–82. doi:10.3114/sim.2008.61.07.
53. Bonifaz A, Gómez-Daza F, Paredes V, Ponce RM. Tinea versicolor, tinea nigra, white piedra, and black piedra. Clin Dermatol. 2010;28(2):140–5. doi:10.1016/j.clindermatol.2009.12.004.
54. Pierard GE, Read D, Pierard-Franchimont C, Lother Y, Rurangirwa A, Arrese EJ. Cutaneous manifestations in systemic trichosporonosis. Clin Exp Dermatol. 1992;17(2):79–82.
55. Nahass GT, Rosenberg SP, Leonardi CL, Penneys NS. Disseminated infection with Trichosporon beigelii. Report of a case and review of the cutaneous and histologic manifestations. Arch Dermatol. 1993;129(8):1020–3.
56. Richini-Pereira VB, Camargo RM, Bagagli E, Marques SA. White piedra: molecular identification of Trichosporon inkin in members of the same family. Rev Soc Bras Med Trop. 2012;45(3):402–4.
57. Guidelines/Outcomes Committee. Guidelines of care for superficial mycotic infections of the skin: Piedra. Guidelines/Outcomes Committee. American Academy of Dermatology. J Am Acad Dermatol. 1996;34(1):122–4.
58. Kiken DA, Sekaran A, Antaya RJ, Davis A, Imaeda S, Silverberg NB. White piedra in children. J Am Acad Dermatol. 2006;55(6): 956– 61.
59. Khandpur S, Reddy BS. Itraconazole therapy for white piedra affecting scalp hair. J Am Acad Dermatol. 2002;47(3):415–8.
60. Kalter DC, Tschen JA, Cernoch PL, McBride ME, Sperber J, Bruce S, et al. Genital white piedra: epidemiology, microbiology, and therapy. J Am Acad Dermatol. 1986;14(6):982–93.
61. Gip L. Black piedra: the first case treated with terbinafine (Lamisil). Br J Dermatol. 1994;130 Suppl 43:26–8.
62. Hacimustafaoglu M, Celebi S. Candida infections in non-neutropenic children after the neonatal period. Expert Rev Anti Infect Ther. 2011;9(10):923–40.
63. Rowen JL. Mucocutaneous candidiasis. Semin Perinatol. 2003; 27(5):406–13.
64. Koumantakis EE, Hassan EA, Deligeoroglou EK, Creatsas GK. Vulvovaginitis during childhood and adolescence. J Pediatr Adolesc Gynecol. 1997;10(1):39–43.
65. Lopez Sastre JB, Coto Cotallo GD, Fernandez Colomer B, Grupo de Hospitales C. Neonatal invasive candidiasis: a prospective multicenter study of 118 cases. Am J Perinatol. 2003;20(3):153–63.
66. Bodey GP, Luna M. Skin lesions associated with disseminated candidiasis. JAMA.1974;229(11):1466–8.
67. Darmstadt GL, Dinulos JG, Miller Z. Congenital cutaneous candidiasis: clinical presentation, pathogenesis, and management guidelines. Pediatrics. 2000;105(2):438–44.
68. Ahonen P, Myllarniemi S, Sipila I, Perheentupa J. Clinical variation of autoimmune polyendocrinopathy-candidiasis-ectodermal dystrophy (APECED) in a series of 68 patients. N Engl J Med. 1990;322(26):1829–36.
69. van de Veerdonk FL, Plantinga TS, Hoischen A, Smeekens SP, Joosten LA, Gilissen C, et al. STAT1 mutations in autosomal dominant chronic mucocutaneous candidiasis. N Engl J Med. 2011;365(1):54–61.
70. Puel A, Cypowyj S, Bustamante J, Wright JF, Liu L, Lim HK, et al. Chronic mucocutaneous candidiasis in humans with inborn errors of interleukin-17 immunity. Science. 2011;332(6025):65–8.
71. Nahum A, Bates A, Sharfe N, Roifman CM. Association of the lymphoid protein tyrosine phosphatase, R620W variant, with chronic mucocutaneous candidiasis. J Allergy Clin Immunol. 2008;122(6):1220–2.
72. Ferwerda B, Ferwerda G, Plantinga TS, Willment JA, van Spriel AB, Venselaar H, et al. Human dectin-1 deficiency and mucocutaneous fungal infections. N Engl J Med. 2009;361(18):1760–7.
73. Schelonka RL, Moser SA. Time to positive culture results in neonatal Candida septicemia. J Pediatr. 2003;142(5):564–5.
74. Karageorgopoulos DE, Vouloumanou EK, Ntziora F, Michalopoulos A, Rafailidis PI, Falagas ME. beta-D-glucan assay for the diagnosis of invasive fungal infections: a metanalysis. Clin Infect Dis. 2011;52(6):750–70.
75. Tirodker UH, Nataro JP, Smith S, LasCasas L, Fairchild KD. Detection of fungemia by polymerase chain reaction in critically ill neonates and children. J Perinatol. 2003;23(2):117–22.
76. Hoppe JE. Treatment of oropharyngeal candidiasis in immunocompetent infants: a randomized multicenter study of miconazole gel vs. nystatin suspension. The Antifungals Study Group. Pediatr Infect Dis J. 1997;16(3):288.
77. Boon JM, Lafeber HN, Mannetje AH, van Olphen AH, Smeets HL, Toorman J, et al. Comparison of ketoconazole suspension and nystatin in the treatment of newborns and infants with oral candidosis. Mycoses. 1989;32(6):312.
78. Goins RA, Ascher D, Waecker N, Arnold J, Moorefield E. Comparison of fluconazole and nystatin oral suspensions for treatment of oral candidiasis in infants. Pediatr Infect Dis J. 2002;21(12):1165.
79. Flynn PM, Cunningham CK, Kerkering T, San Jorge AR, Peters VB, Pitel PA, et al. Oropharyngeal candidiasis in immunocompro mised children: a randomized, multicenter study of orally administered fluconazole suspension versus nystatin. The Multicenter Fluconazole Study Group. J Pediatr. 1995;127(2):322.
80. Pienaar ED, Young T, Holmes H. Interventions for the prevention and management of oropharyngeal candidiasis associated with HIV infection in adults and children. Cochrane Database Syst Rev. 2010;10:CD003940.
81. Hoeger PH, Stark S, Jost G. Efficacy and safety of two different antifungal pastes in infants with diaper dermatitis: a randomized, controlled study. J Eur Acad Dermatol Venereol. 2010;24(9): 1094–8.
82. Bonifaz A, Tirado-Sanchez A, Graniel MJ, Mena C, Valencia A, Ponce-Olivera RM. The efficacy and safety of sertaconazole cream (2%) in diaper dermatitis candidiasis. Mycopathologia. 2013;175(3–4):249–54.
83. Spraker MK, Gisoldi EM, Siegfried EC, Fling JA, de Espinosa ZD, Quiring JN, et al. Topical miconazole nitrate ointment in the treatment of diaper dermatitis complicated by candidiasis. Cutis. 2006;77(2):113–20.
84. Gallup E, Plott T, Ciclopirox TSI. A multicenter, open-label study to assess the safety and efficacy of ciclopirox topical suspension 0.77% in the treatment of diaper dermatitis due to Candida albicans. J Drug Dermatol. 2005;4(1):29–34.
85. American Academy of Pediatrics. Antimicrobial agents and related therapy. In: Pickering LK, editor. Red book: 2009 report of the committee on infectious diseases, 28th. Elk Grove Village: American Academy of Pediatrics; 2009. p. 737.
86. Watson MC, Grimshaw JM, Bond CM, Mollison J, Ludbrook A. Oral versus intra-vaginal imidazole and triazole anti-fungal treatment of uncomplicated vulvovaginal candidiasis (thrush). Cochrane Database Syst Rev. 2001;4:CD002845.
87. Sobel JD, Brooker D, Stein GE, Thomason JL, Wermeling DP, Bradley B, et al. Single oral dose fluconazole compared with conventional clotrimazole topical therapy of Candida vaginitis. Fluconazole Vaginitis Study Group. Am J Obstet Gynecol. 1995;172(4 Pt 1):1263–8.
88. Sekhavat L, Tabatabaii A, Tezerjani FZ. Oral fluconazole 150mg single dose versus intra vaginal clotrimazole treatment of acute vulvovaginal candidiasis. J Infect Public Health. 2011;4(4): 195–9.
89. Mendling W, Krauss C, Fladung B. A clinical multicenter study comparing efficacy and tolerability of topical combination therapy with clotrimazole (Canesten, two formats) with oral single dose fluconazole (Diflucan) in vulvovaginal mycoses. Mycoses. 2004;47(3– 4):136–42.
90. Slavin MB, Benrubi GI, Parker R, Griffin CR, Magee MJ. Single dose oral fluconazole vs intravaginal terconazole in treatment of Candida vaginitis. Comparison and pilot study. J Fla Med Assoc. 1992;79(10):693–6.
91. Corson SL, Kapikian RR, Nehring R. Terconazole and miconazole cream for treating vulvovaginal candidiasis. A comparison. J Reprod Med. 1991;36(8):561–7.
92. Pappas PG, Kauffman CA, Andes D, Benjamin Jr DK, Calandra TF, Edwards Jr JE, et al. Clinical practice guidelines for the management of candidiasis: 2009 update by the Infectious Diseases Society of America. Clin Infect Dis. 2009;48(5):503–35.
93. Sobel JD, Kapernick PS, Zervos M, Reed BD, Hooton T, Soper D, et al. Treatment of complicated Candida vaginitis: comparison of single and sequential doses of fluconazole. Am J Obstet Gynecol. 2001;185(2):363–9.
94. Sobel JD, Wiesenfeld HC, Martens M, Danna P, Hooton TM, Rompalo A, et al. Maintenance fluconazole therapy for recurrent vulvovaginal candidiasis. N Engl J Med. 2004;351(9): 876–83.
95. Rosa MI, Silva BR, Pires PS, Silva FR, Silva NC, Silva FR, et al. Weekly fluconazole therapy for recurrent vulvovaginal candidiasis: a systematic review and meta-analysis. Eur J Obstet Gynecol Reprod Biol. 2013;167(2):132–6.
96. Karlowicz MG, Hashimoto LN, Kelly Jr RE, Buescher ES. Should central venous catheters be removed as soon as candidemia is detected in neonates? Pediatrics. 2000;106(5):E63.
97. Butler KM, Rench MA, Baker CJ. Amphotericin B as a single agent in the treatment of systemic candidiasis in neonates. Pediatr Infect Dis J. 1990;9(1):51–6.
98. Hall JE, Cox F, Karlson K, Robertson A. Amphotericin B dosage for disseminated candidiasis in premature infants. J Perinatol. 1987;7(3):194–8.
99. Ascher SB, Smith PB, Watt K, Benjamin DK, Cohen-Wolkowiez M, Clark RH, et al. Antifungal therapy and outcomes in infants with invasive Candida infections. Pediatr Infect Dis J. 2012;31(5): 439–43.
100. Le J, Adler-Shohet FC, Nguyen C, Lieberman JM. Nephrotoxicity associated with amphotericin B deoxycholate in neonates. Pediatr Infect Dis J. 2009;28(12):1061–3.
101. Driessen M, Ellis JB, Cooper PA, Wainer S, Muwazi F, Hahn D, et al. Fluconazole vs. amphotericin B for the treatment of neonatal fungal septicemia: a prospective randomized trial. Pediatr Infect Dis J. 1996;15(12):1107–12.
102. Wainer S, Cooper PA, Gouws H, Akierman A. Prospective study of fluconazole therapy in systemic neonatal fungal infection. Pediatr Infect Dis J. 1997;16(8):763–7.
103. Wade KC, Benjamin Jr DK, Kaufman DA, Ward RM, Smith PB, Jayaraman B, et al. Fluconazole dosing for the prevention or treatment of invasive candidiasis in young infants. Pediatr Infect Dis J. 2009;28(8):717–23.
104. Baley JE, Meyers C, Kliegman RM, Jacobs MR, Blumer JL. Pharmacokinetics, outcome of treatment, and toxic effects of amphotericin B and 5-fluorocytosine in neonates. J Pediatr. 1990; 116(5):791–7.
105. Manzoni P, Wu C, Tweddle L, Roilides E. Micafungin in prema- ture and non-premature infants: a systematic review of 9 clinical trials. Pediatr Infect Dis J. 2014;33(11):e291–8.
106. Odio CM, Araya R, Pinto LE, Castro CE, Vasquez S, Alfaro B, et al. Caspofungin therapy of neonates with invasive candidiasis. Pediatr Infect Dis J. 2004;23(12):1093–7.
107. Natarajan G, Lulic-Botica M, Rongkavilit C, Pappas A, Bedard M. Experience with caspofungin in the treatment of persistent fungemia in neonates. J Perinatol. 2005;25(12):770–7.
108. Kirkpatrick CH. Chronic mucocutaneous candidiasis. Pediatr Infect Dis J. 2001;20(2):197– 206.
109. Kamai Y, Maebashi K, Kudoh M, Makimura K, Naka W, Uchida K, et al. Characterization of mechanisms of fluconazole resistance in a Candida albicans isolate from a Japanese patient with chronic mucocutaneous candidiasis. Microbiol Immunol. 2004;48(12): 937–43.
110. Rautemaa R, Richardson M, Pfaller MA, Perheentupa J, Saxen H. Activity of amphotericin B, Anidulafungin, caspofungin, micafungin, posaconazole, and voriconazole against Candida albicans with decreased susceptibility to fluconazole from APECED patients on long-term azole treatment of chronic mucocutaneous candidiasis. Diagn Microbiol Infect Dis. 2008; 62(2):182–5.

