Các phương pháp theo dõi cung lượng tim: Lợi ích, hạn chế của từng phương pháp

Tác giả: Nathan BetteridgeFiona, Armstrong
Dịch: BS Nguyễn Thanh Tuấn - Khoa ICU BV HNĐK Nghệ An
Tải file PDF TẠI ĐÂY
1 Tóm tắt
Theo dõi cung lượng tim ngày càng phổ biến trong theo dõi chăm sóc chuẩn đối với gây mê ở bệnh nhân đại phẫu và chăm sóc tích cực. Nhiều kỹ thuật đã được sử dụng và các mô hình khác nhau để tính toán cung lượng - thứ không thể đo trực tiếp.
Mỗi phương pháp đều có ưu điểm và nhược điểm khác nhau, do đó, việc lựa chọn thiết bị nên cân đối giữa tính xâm lấn, tính khả dụng, độ tin cậy và tính hợp lý. Theo dõi xu hướng thay đổi thường được nhấn mạnh hơn các giá trị tuyệt đối.
Keywords Aortie Doppler; bioimpedanee; cardiac output; echocar-diography; indicator dilution; oesophageal Doppler; pulse contour analysis; pulse waveform analysis; thermodilution
Royal College of Anaesthetists CPD Skills Framework: Scientific prineiples.
2 Giới thiệu
Cung lượng tim (CO) là 1 thông số quan trọng, biểu thị tổng lưu lượng máu trong hệ tuần hoàn đi qua tim. Nó được định nghĩa là thể tích máu được bơm ra từ thất phải hoặc thất trái theo mỗi đơn vị thời gian, thường được mô tả bằng đơn vị lít/phút.
CO = Thể tích nhát bóp (SV) x tần số tim (HR)
Cung cấp oxy là 1 vấn đề sống còn, đặc biệt là ở bệnh nhân nặng hoặc sau mổ, những trường hợp tăng nhu cầu oxy do đáp ứng viêm. Để đảm bảo chức năng cơ quan thích hợp và hô hấp hiểu khí trong bối cảnh này, phải duy trì tưới máu và cung cấp oxy. Cung cấp oxy là hệ quả của cung lượng tim và lượng oxy trong máu động mạch:
DO2 [ml/phút] = Cung lượng tim [lít/phút] x tổng lượng oxy động mạch [ml/dl] x 10
Do đó, bằng cách sử dụng các kỹ thuật đề tính toán CO và kết hợp với đo tổng lượng oxy động mạch, chúng ta có thể ước tính chính xác cung cấp oxy mô, từ đó tác động đến cách điều trị bệnh nhân.
Trong gần 1 thế kỷ, có 1 số cách để tính toán cung lượng tim, mỗi cách đều có vần đề về các lỗi tiềm ẩn, chi phí hoặc hạn chế sử dụng. Hầu hết các hình thức đo CO đều giới hạn ở các khu vực được kiểm soát như chăm sóc tích cực hoặc phòng mổ do bản chất xâm lấn của chúng. Mỗi kỹ thuật có thể được phân loại thành 3 loại chính:
- Xâm lân: Sử dụng 1 catheter tĩnh mạch trung tâm, catheter động mạch hoặc catheter động mạch phổi.
- Xâm lấn tối thiểu: Siêu âm động mạch chủ qua thực quản.
- Không xâm lấn: 1 số kỹ thuật, như đo trở kháng.
Tất cả các phương pháp này đều nhằm mục đích tính toán chính xác thể tích nhát bóp (SV) của bệnh nhân để đưa ra giá trị CO.
Bài viết này giải thích các nguyên tắc và cơ chế sinh lý học đằng sau mỗi phương pháp và những hạn chế của từng phương pháp.
3 Phương pháp xâm lấn
3.1 Nguyên Lý Fick
Nguyên lý này nói rằng sự hấp thụ hoặc bài tiết một chất của một cơ quan bằng với sự chênh lệch giữa lượng chất đi vào và lượng chất đi ra khỏi cơ quan đó. (hình 1).
Dòng máu tới cơ quan = [O2 tiêu thụ (tỉ lệ 1 chất bị loại bỏ hoặc thêm vào)] / [Chênh lệch nông độ (động mạch-tĩnh mạch)]
Điều quan trọng phải nhận ra đó là toàn bộ thể tích máu đi qua phổi nên những thay đổi về nồng độ oxy có thể cung cấp hình ảnh chính xác về CO ở bệnh nhân. Tuy nhiên, việc sử dụng oxy không thực tế vì nó đòi hỏi phải có ống thông động mạch phổi (PA) và phương pháp này cũng đưa ra những thông số kết quả về hệ thống mà nó đang ước tính sự khác biệt nồng độ (ví dụ: Thể tích phổi và thể tích toàn thân bằng nhau). Ngoài ra, để đảm bảo đo oxy chính xác, cần có 1 sealed hood (bình kín) để đo khí, điều này một lần nữa làm tăng thêm sự phức tạp khi sử dụng oxy làm chất được đo trong nguyên lý Fick. Sau đó, các kỹ thuật sử dụng chất chỉ thị hoặc pha loãng nhiệt được sử dụng thay thế và giả định rằng tốc độ phân hủy nồng độ chất/thay đổi nhiệt độ tỷ lệ thuận với tốc độ dòng chảy qua cơ quan.
3.2 Kỹ Thuật Pha Loãng Bằng Cách Sử Dụng Chất Chỉ Thị
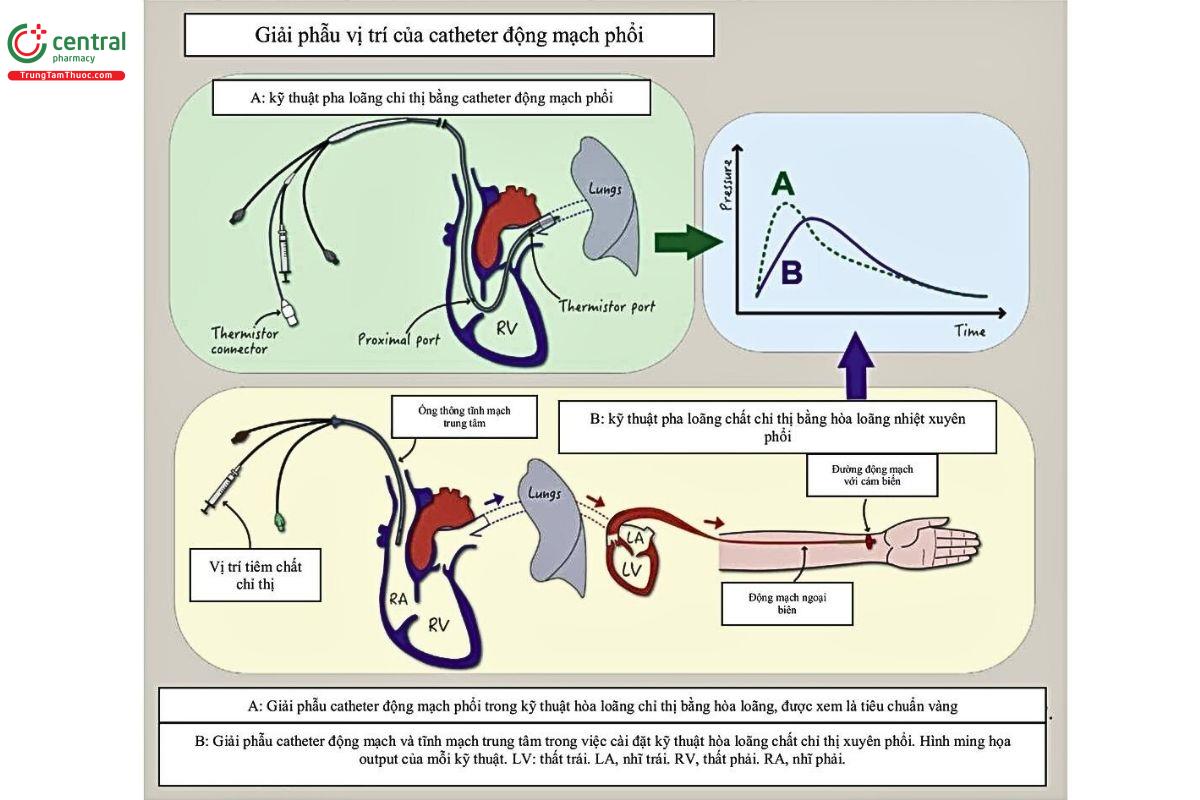
Phương pháp sử dụng: Trong trường hợp này, 1 thể tích/lượng chất đánh dấu đã biết được chọn và tiêm vào động mạch phổi hoặc tĩnh mạch trung tâm (do đó, cần phải có ống thông tĩnh mạch trung tâm (CVC) hoặc ống thông động mạch phổi PA). Sau đó, một đường động mạch ngoại vi được sử dụng đề lấy mẫu nồng độ chất chỉ thị liên tục. Điều này có thể tạo ra một biểu đồ đo nồng độ theo thời gian (hình 2).
.jpg)
Theo truyền thống, indocyanine green là 1 chất chỉ thị được sử dụng vì nó có độc tính thấp và thời gian bán thải ngắn. Điều này hạn chế lượng tuần hoàn trở lại sau khi đi qua hệ thống mạch máu toàn thân lần đầu tiên. Ngày nay, Lithium được sử dụng phổ biến hơn vì nó không phải là ion có sẵn trong huyết tương bình thường, nên chỉ cần liều rất nhỏ để đạt được tỷ lệ tín hiệu cao trên mức nhiễu, điều này một lần nữa đảm bảo bệnh nhân không tiếp xúc với liều độc hại hoặc có ý nghĩa dược lý.
Sau đó, CO thể được tính toán từ đồ thị được tạo ra bằng cách sử dụng Diện tích dưới đường cong (tích phân của đường cong) và phương trình Fick hiệu chỉnh, được gọi là phương trình Stewarte Hamilton (Hình 1).
3.2.1 Hạn chế
- Cần hiệu chỉnh logarit của nồng độ để đưa ra ước tính chính xác hơn về diện tích đưới đường cong và giảm thiểu sự tái tuần hoàn của chất chỉ thị.
3.3 Hòa Loãng nhiệt
Để tránh vấn đề chất chỉ thị bị tái tuần hoàn, kỹ thuật hòa loãng nhiệt đã được phát triển. Sau đó, điều nảy trở thành “tiêu chuẩn vàng" đề so sánh với các biện pháp đo CO khác. Nó sử dụng cùng 1 nguyên tắc như pha loãng chất chỉ thị, ngoại trừ việc nó sử dụng 10 - I5 ml nước muối lạnh tiêm qua ống thông động mạch phổi (PA).
Sau đó, sự thay đổi nhiệt độ máu được đo từ Cổng gần (Proximal Port) - nơi nó được tiêm qua điện trở nhiệt ở phần xa của ống thông. Một phương trình Stewarte-Hamilton sửa đổi được sử dụng để tính toán CO (Hình 1 và 2).
3.3.1 Phương pháp thực hiện
Nó được đưa vào bằng cách làm căng quả bóng ở đầu ống thông PA và luồn ống thông qua nhĩ phải, thất phải và để nó nằm
trong động mạch phổi (hình 2). Sau đó, bơm nước muối lạnh và đo CO.
3.3.2 Lợi ích
- Không cần lấy mẫu máu và không có vấn đề tái tuần hoàn vì máu đã ấm trở lại bình thường khi đến tuần hoàn phổi.
- Hệ thống này vẫn chính xác trong bối cảnh có bóng chèn hoặc rối loạn nhịp, và có thể giảm sai số bằng cách thực hiện đo nhiều lần.
3.3.3 Biến chứng
- Liên quan với việc đặt catheterr động mạch phổi, bao gồm: Rối loạn nhịp, nhiễm trùng, tồn thương van, vỡ động mạch phổi.
1 nghiên cứu năm 2005 (nghiên cứu PAC-MAN) nhằm đánh giá tỷ lệ tử vong liên quan với đặt ống thông động mạch cảnh ở những bệnh nhân nguy kịch.
Mặc dù nghiên cứu ngẫu nhiên đối chứng này không tìm ra bằng chứng lợi ích hoặc tác hại, thực tế lâm sàng không chỉ có sự chuyển sang các phương pháp đo CO kém chính xác hơn mà còn có xu hướng ngừng sử dụng chúng có nhiều yếu tố tác động đến sự thay đổi này và vượt ra ngoài phạm vi của bài viết; tuy nhiên, việc công nhận hình thức theo dõi CO này là "tiêu chuẩn vàng" để đo lường các hình thức khác là rất quan trọng.
3.4 Phân tích sóng áp lực
Việc sử dụng áp lực mạch trong lâm sàng, gồm đánh giá đặc tính và thể tích của nó, đã được sử dụng từ lâu trước khi có nhiều biện pháp định lượng hơn trong thực hành hiện tại bằng cách sử dụng ống thông động mạch để đánh giá dạng sóng áp lực mạch và hiện nay hình thành các kỹ thuật được sử dụng rộng rãi nhất để theo dõi CO.
Hiệu ứng Windkessel: Thất trái (LV) co tạo nên huyết áp tâm thu và bơm trung bình 70 ml (gọi là thể tích nhát bóp) máu vào động mạch chủ.
Máu trong động mạch chủ làm cho thành mạch trở nên mở rộng và kéo dãn ra để chứa thể tích này, nâng áp lực từ 80 mmHg lên 120 mmHg. Máu được đẩy ra có động năng đẩy nó về phía trước, vào hệ thống mạch máu, có các thành động mạch chủ đàn hồi và căng ra, chứa thế năng.
Sau đó, thế năng này được chuyển thành động năng khi các thành mạch co lại và giúp đảm bảo máu tiếp tục di chuyển xuyên suốt hệ thống mạch máu toàn thân trong thời kỳ tâm trương, giúp duy trì huyết áp tâm trương. Hiệu ứng này được gọi là Hiệu ứng Windkessel: Là cách áp lực hình sin này được tạo ra trong tìm sau đó được chuyển thành áp lực đường và không đổi tại các mô.
Otto Frank, nhà sinh lý học người Đức, người đầu tiên mô tả Hiệu ứng này, ví von nó như buồng khí 'Windkessel' được sử dụng trong xe cứu hỏa vào thời điểm đó, thứ chuyển áp lực bơm hình sin tạo ra thành dòng nước liên tục (hình 3). 2
Khả năng tạo ra Áp lực hằng định, không đổi nảy trở khó khăn hơn khi tuổi cao đi kèm với mất sợi Elastin và Collagen trong thành động mạch. Mất khả năng giãn nở và kéo giãn đồng nghĩa với tuần hoàn hệ thống phải vật lộn để bù đắp cho SV và sự gia tăng áp lực lớn trong quá trình tâm thu. Điều này giúp giải thích tại sao tăng huyết áp tâm thu trở nên phổ biến hơn ở nhóm dân số lớn tuổi.
Sóng áp lực động mạch cho thấy điều gì? Có sự khác biệt giữa sóng áp lực động mạch và sóng lưu lượng máu. Khi cảm thấy mạch đập, người ta sẽ cảm nhận được sóng áp lực và cho rằng đó là lưu lượng máu. Tương tự như vậy, đồ thị được tạo ra bằng cách sử dụng ống thông động mạch cho thấy sóng áp suất và từ đó suy ra lưu lượng máu (hình 3).
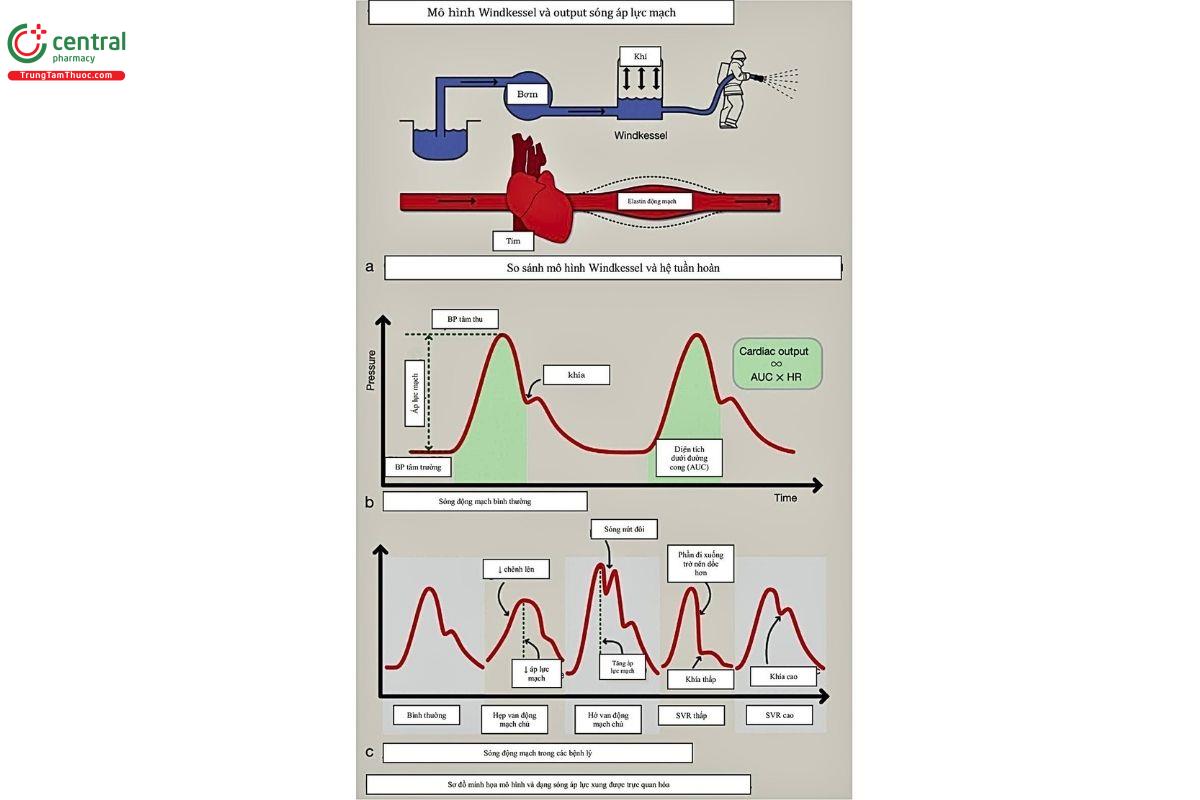
Vì thất trái bơm 1 thể tích vào động mạch chủ, áp lực trong động mạch chủ tăng lên đạt đỉnh 120mmHg (SBP), khi quá trinh bơm ngừng lại và sự đàn hồi mạch máu xảy ra, huyết áp giảm xuống 80 mmHg (DBP). Sự gián đoạn của đường cong áp lực này xảy ra khi van động mạch chủ đóng lại. Có sự gia tăng ngắn về áp suất bên trong động mạch chủ; gọi là Khía hai nhánh. (dicrotic notch)
Dạng sóng nhìn thấy sẽ thay đổi tùy thuộc vào vị trí của động mạch mà nó được đo, ví dụ như bên trong động mạch chủ so với động mạch ngoại vi hơn. Thông tin nào chúng ta có thể thu được từ sóng áp lực mạch? Biến thiên áp lực mạch (PPV) là thước đo áp lực mạch tối đa và tối thiểu trong 1 chu kỳ hô hấp. Điều này chỉ có thể được sử dụng ở những bệnh nhân thở máy vì hồi lưu tĩnh mạch bị ảnh hưởng bởi việc thông khí áp lực dương ở những bệnh nhân giảm thể tích máu/hoặc giảm đổ đầy, làm thay đổi tiền gánh với mỗi lần thở. Điều này gây ra sự "dao động" hoặc thay đổi theo thời gian trong áp lực mạch. Theo dõi cụ thể có thể tính toán % PPV hoặc thay vào đó bạn có thể cố gắng hình dung sự biến đổi PPV. Biến đổi > 10% gợi ý bệnh nhân giảm thể tích/giảm khả năng đổ đầy.
Độ dốc của hình dạng sóng cho thấy khả năng co bóp của tim, vì độ dốc tăng lên cho thấy áp lực do tim tạo ra lớn hơn theo thời gian. Thông thường, điều này có thể xem như sức co bóp tăng, nhưng trong bối cảnh bệnh van động mạch chủ, điều này có thể không chính xác. Hẹp động mạch chủ có thể làm giảm độ dốc lên vì có tắc nghẽn cố định dòng chảy vào động mạch chủ, trong khi ở tình trạng hở van động mạch chủ, khả năng co bóp bình thường có thể biểu hiện dạng sóng đôi (hình 3).
Sức cản mạch hệ thống (SVR) được biểu thị ở phần sóng đi xuống (downstroke). SVR thấp biểu hiện bằng phần sóng đi xuống dốc hơn với Khía thấp, tạo ra hình dạng sóng dày và nhọn, Ngược lại, Khía cao và phần xuống ít đốc hơn chỉ ra SVR cao hơn (hình 3).
3.5 Phân tích xung sóng mạch
Do đó, thông tin được mô tả ở trên cho phép đánh giá liên tục cung lượng tim bằng điện tích dưới đường cong x nhịp tim. Sau đó, thuật toán máy tính dành riêng cho hệ thống đang sử dụng sẽ tính cung lượng tìm cùng với một số biến số khác được đo hoặc suy ra, bao gồm SV, chỉ số tim (CI) và biến thiên thể tích nhát bóp (SVV). SVV khác với PPV. Chỉ số này này bị ảnh hưởng bởi hồi lưu tĩnh mạch trong chu kỳ hô hấp, khi áp lực trong lồng ngực thay đổi, SV thực tế được tính toán bằng thuật toán và sự khác biệt giữa SV tối đa và tối thiểu theo thời gian được xác định. Điều này cho phép đánh giá đáp ứng với truyền dịch dựa trên giá thiết: Nếu bạn “đầy đủ dịch” hơn thì hồi lưu tĩnh mạch sẽ ít thay đổi hơn, và điều này cũng được chuyển sang SV, Trong thực hành, bệnh nhân với SVV >15% sẽ tăng CO khi bolus dịch, và ngược lại nếu <10%.
Hệ thống phân tích này có thể chia làm 2 loại khác nhau: Hiệu chỉnh (calibrated) và không hiệu chỉnh (uncalibrated). Hệ thống hiệu chỉnh sử dụng nguyên lý Fick được mô tả trong phần trước để ước tính cung lượng tim bằng cách hiệu chỉnh sóng xung áp lực theo lưu đồ. Hệ thống không hiệu chỉnh sử dụng dữ liệu dựa trên nhân khẩu học đề tính toán các giá trị có thể có trong thuật toán.
3.6 Hiệu Chỉnh
3.6.1 Tính cung lượng tim theo đường viền xung (PiCCO)
Hệ thống nảy sử dụng phương pháp hòa loãng nhiệt xuyên phổi để hiệu chỉnh thuật toán của nó (hình 2).
Phương pháp sử dụng: Cần 1 đường tĩnh mạch trung tâm thông thường và 1 đường động mạch có điện trở cảm biến nhiệt — thường đặt ở động mạch đùi hoặc cánh tay. Nước muối lạnh được bơm vào đường tĩnh mạch trung tâm và sự thay đổi nhiệt độ được đo ở đường động mạch. Những thông tin này được hệ thống sử dụng để phân tính sóng áp lực mạch để tính toán cung lượng tim và đảm bảo thuật toán chính xác.
3.6.2 Hạn chế
- Có 1 Biên độ sai số (so với kỹ thuật pha loãng nhiệt ống thông động mạch phổi) vì nhiệt bị mất và tản ra khi đi qua tuần hoàn phổi.
3.6.3 Đo cung lượng tim bằng hòa loãng Lithium (LiDCO)
Hệ thống này sử dụng phương pháp hòa loãng lithium để hiệu chỉnh thuật toán của nó và chỉ cần đường động mạch.
Phương pháp: Lithium chloride được bơm qua đường tĩnh mạch trung tâm hoặc thậm chí là tĩnh mạch ngoại vi. Sự thay đổi nồng độ được đo bởi điện cực ở đường động mạch. Điều này loại bỏ nhược điểm mà PiCCO gặp phải khi mất nhiệt ở phổi, tuy nhiên, nó đòi hỏi phải hiệu chỉnh lại sau mỗi 8 giờ hoặc sau khi bệnh nhân có sự thay đổi trạng thái huyết động lớn.
3.6.4 Hạn chế
- Không thể sử dụng cho bệnh nhân đang dùng lithium điều trị vì không thể hiệu chỉnh được.
- Thuốc giãn cơ có thể phản ứng chéo với điện cực đo lithium và làm cho nó không chính xác.
- Cần hiệu chỉnh thường xuyên theo thời gian khi nhắc lại liều lithium, điều này một lần nữa làm giảm độ chính xác của hệ thống.
3.7 Không Hiệu Chỉnh
3.7.1 FloTrac/Vigileo
Trong hệ thống này, 1 cảm biến áp suất chuyên dụng gọi là FloTrac được sử dụng.
Phương pháp: Cảm biến FloTrac được gắn với đường động mạch tiêu chuẩn, sau đó kết nối với máy theo dõi Vigileo, thứ sử dụng dữ liệu dựa trên nhân khẩu học (ví dụ: Tuổi, giới tính, cân nặng, chiều cao) để ước tính độ đàn hồi động mạch chủ. Thông tin này sau đó được nhập vào thuật toán phân tích áp lực mạch Flotrac/Vigileo đề tính CO.
3.7.1.1 Hạn chế
- Không được hiệu chỉnh và dựa vào dữ liệu nhân khẩu học dân số. Do đó, một số giả định về thông số giải phẫu và sinh lý dựa trên dữ liệu "trung bình" có thể không áp dụng được hoặc không chính xác ở 1 số bệnh nhân.
3.7.2 LiDCOrapid
Hệ thống này sử dụng thuật toán áp lực mạch để tính CO giống như hệ thống LiDCO, nhưng sử dụng biểu đồ dựa trên nhân khẩu học hơn là hòa loãng lithium. Điều này có thể dẫn đến ước tính CO không chính xác hoặc lỗi. Nhìn chung, phân tích dạng sóng áp lực mạch cho thấy mối tương quan tốt với phương pháp pha loãng nhiệt “tiêu chuẩn vàng” PAC để đo CO. Điều quan trọng là có 1 số điều kiện và tình huống nhất định mà điều này không đúng và có thể khiến phân tích áp lực mạch không chính xác.
3.7.2.1 Hạn chế trong phân tích đường viền xung áp lực
- Phân tích xung áp lực không chính xác trong 1 số tình trạng lâm sàng và bối cảnh:
Đường sóng động mạch bị under-damped (dạng sóng tròn trịa, không có Khía) hoặc over-damped (dạng sóng dao động quá mức)
Rối loạn nhịp tim
Hở van động mạch chủ
Sự có mặt của Bơm bóng trong động mạch chủ.
3.7.2.2 Lợi ích của phân tích đường viền xung áp lực
- Biện pháp phản ánh khá chính xác quá trình hoà loãng nhiệt 3 trong khi tránh được các biến chứng xâm lấn của ống thông PA.
- Dễ dàng tiếp cận trong môi trường phòng mổ hoặc chăm sóc đặc biệt.
- Thiết bị sử dụng thường có sẵn, cụ thể là ống thông động mạch giúp tiết kiệm chi phí hơn.
3.7.2.3 Biển chứng
- Thường liên quan đến ống thông động mạch.
4 PHƯƠNG PHÁP XÂM LẤN TỐI THIỂU VÀ KHÔNG XÂM LẤN
4.1 Doppler động mạch chủ
Nguyên lý của siêu âm và hiệu ứng Doppler: Doppler động mạch chủ là 1 phương pháp đo cung lượng tim dựa trên vận tốc của hồng cầu trong động mạch chủ, từ đó đánh giá lưu lượng máu động mạch chủ. 1 đầu dò được đưa vào thực quản và hướng về phía đoạn xuống của Động mạch chủ. Phương pháp này sử dụng siêu âm và nguyên lý Doppler. Đầu dò siêu âm chứa các tinh thể điện áp phát ra sóng âm ở tần số cố định (4-5Hz trong Doppler thực quản) khi có dòng điện tác động vào chúng. Những sóng âm tần số cao này có thể xuyên qua các mô, từ đó phản ảnh các cấu trúc có mật độ khác nhau. Một tỷ lệ sau đó được phản xạ trở lại và đến các tinh thể điện áp trong đầu dò, chuyển đổi năng lượng phản xạ lại thành tín hiệu điện. Máy siêu âm tiếp nhận tín hiệu và chuyển đổi thành hình ảnh siêu âm. Khi một vật liệu chứa các bộ phận chuyển động so với nguồn, chẳng hạn như máu chảy qua đầu dò thì sẽ xảy ra sự dịch chuyển tần số được gọi là nguyên lý Doppler. Điều này có nghĩa là sóng phản xạ có tần số cao hơn nếu vật thể di chuyển về phía đầu dò và thấp hơn nếu vật thể di chuyển ra xa. Mức độ dịch chuyển tỷ lệ thuận với tốc độ của vật thể và có thể được đầu dò siêu âm phát hiện. Việc thay đổi tần số có thể được sử dụng để tính vận tốc tế bào hồng cầu và sau đó được biểu diễn dưới dạng đồ thị thể hiện vận tốc theo thời gian (hình 4). Vào đầu kỳ tâm thu, vận tốc của các tế bào hồng cầu cao hơn gây ra sự thay đổi tần số cao hơn so với cuối kỳ tâm thu và kỳ tâm trương.
Công thức Doppler được sử dụng để tính vận tốc tế bào hồng cầu trong động mạch chủ. Nó cần thông tin về tần số dẫn truyền (Ft) và tần số phản xạ (Fd), tốc độ truyền âm trong mô và huyết tương (C). Hệ số hiệu chỉnh (Cos q) được dùng để bù trừ cho góc độ đầu dò (độ chính xác lên tới 20°) so với trục của dòng máu. Chỉ nên sử dụng sự dịch chuyển tần số phản xạ để tính toán vận tốc. Điều này có nghĩa là cần đưa một yếu tổ vào phương trình để giảm một nửa vận tốc để tính đến sự dịch chuyển tần số dẫn truyền và phản xạ đều được thu nhận.
Fd = (2 Ft V Cos∅)/C
Để chuyển đổi vận tốc thành lưu lượng, cần phải sử dụng diện tích mặt cắt ngang của động mạch chủ. Hầu hết các màn hình output Doppler sử dụng biểu đồ để ước tính điều này dựa trên chiều cao, tuổi, giới tính và cân nặng. Siêu âm M-mode cũng có thể được sử dụng.
Đo cung lượng tim: Siêu âm Doppler thực quản (hình 4) có thể sử dụng để suy ra các thông số hữu ích trong việc đánh giá cung lượng tim. Tích phân của đường cong vận tốc/thời gian tống máu (VTI) cho chúng ta “chiều dài” nhát bóp, nhân tích phân này với diện tích động mạch chủ cắt ngang ước tính (LVOT) cho chúng ta thể tích nhát bóp. Cung lượng tim = thể tích nhát bóp x tần số tim.
Độ dốc trung bình của đồ thị vận tốc - thời gian biểu thị gia tốc trung bình của các tế bào hồng cầu như một dấu hiệu của khả năng co bóp, không phụ thuộc vào trương lực mạch máu (không giống như vận tốc). Một trong những giá trị hữu ích nhất được suy ra từ biểu đồ thời gian vận tốc là thời gian lưu lượng được hiệu chỉnh (FTc) vì đây là dấu hiệu của tiền gánh và có thể được sử dụng để hướng dẫn liệu pháp truyền dịch. Thời gian thực hiện toàn bộ đỉnh tống máu được chuẩn hóa theo nhịp tim là 60 nhịp/phút. Nếu điều này giảm thì nó cho thầy giảm tiền tải và truyền dịch có thể cải thiện cung lượng tim. Hình dạng đường sóng giúp suy ra bệnh lý và nguyên nhân gây giảm cung lượng tim (hình 4).
Phương pháp sử dụng: Chọn đầu dò chính xác cho thời gian cần thiết (thường tính bằng giờ hoặc ngày) và bôi trơn. Đưa vào miệng hoặc mũi cách răng 35-40 cm và thao tác cho đến khi nghe thấy tiếng Doppler "vù vù" với đường sóng trên màn hình. Điều chỉnh độ khuếch đại và độ dài chu kỳ để có hình ảnh tối ưu cho việc phân tích.
4.1.1 Hạn chế
- Vị trí của đầu dò rất quan trọng, phụ thuộc vào người làm và có thể di chuyển trong quá trình sử dụng, dẫn đến thay đổi giá trị.
- Việc ước tính diện tích mặt cắt ngang động mạch chủ có biên độ sai số.
- Dòng chảy hỗn loạn làm mất hiệu, lực của phương trình được sử dụng để ước tính dòng chảy từ vận tốc và diện tích mặt cắt ngang.
- Khó sử dụng ở bệnh nhân tỉnh.
4.1.2 Lợi ích
- Về mặt nghiên cứu và sử dụng, phương pháp này có xu hướng tương quan tốt với ống thông động mạch phổi, mặc dù các giá trị tuyệt đối kém thuyết phục hơn.4
.jpg)
- Ít xâm lấn hơn các phương pháp xâm lấn.
4.1.3 Biến chứng
- Chấn thương hoặc hẹp thực quản.
- Lệch đầu dò.
4.2 Trở Kháng Sinh Học (Bioimpedance)
Định luật Ohm và trở kháng: Dòng điện có thể được dẫn bởi các hạt tích điện (ion). Định luật Ohm mô tả mối quan hệ giữa hiệu điện thế, cường độ dòng điện (dòng ion) và điện trở (với dòng chảy).
Hiệu điện thế (V) = cường độ dòng điện (I) × điện trở (R)
Do đó, công thức này có thể viết lại: Cường độ dòng điện = hiệu điện thế chia cho điện trở.
I = V/R
Điện trở với dòng điện được gọi là Trở kháng khi dòng điện xoay chiều. Thuật ngữ trở kháng sinh học mô tả việc sử dụng định luật Ohm để xác định trở kháng và đo hiệu điện thể khi có dòng điện đi qua mô hữu cơ. Trở kháng sử dụng ký hiệu Z và nếu dòng điện không đổi thì sự thay đổi về điện trở và điện áp sẽ tương ứng.
Các các mô khác nhau trong cơ thể được cấu tạo từ các vật chất có trở kháng khác nhau. Mô hình trở kháng sinh học phân biệt các mô có trở kháng cao như không khí (1274 U/cm) và các mô có trở kháng thấp như máu (150 U/cm). Trong trở kháng sinh học ngực (được sử dụng phổ biến nhất), ngực được biểu diễn như một hình trụ, máu được xem như một hình trụ nhỏ hơn bên trong, có trở kháng thấp và một hình trụ lớn hơn với các mô cơ thể có trở kháng cao hơn. Sau đó, nó được hiệu chỉnh thành hình nón hơn, đại diện cho khoang ngực nhiều hơn.
1 dòng điện có tần số cao, biên độ thấp đi từ điện cực đặt ở ngoài cố, qua ngực đến cơ hoành, trong khi các điện cực bên trong đo sự biến đổi. Bên trái và phải được tính trung bình để đưa ra các giá trị trung bình. Nguyên tắc là dòng điện sẽ tìm đến nơi có trở kháng ít nhất để đến máu (biểu thị bằng hình trụ có trở kháng thấp bên trong). Hình trụ này sẽ gia tăng trong thì tâm thu khi động mạch chủ giãn ra, làm tăng thể tích máu, dẫn đến sụt giảm trở kháng và tăng độ dẫn điện. Bộ điện cực chuyển đổi bên trong đo cả trở kháng cơ bản (tỷ lệ nghịch với thể tích dịch trong lồng ngực) và sự thay đổi trở kháng. Chúng được xác định thời gian theo dạng sóng ECG cho phép suy ra nhiều thông số khác nhau (hình 5). Trở kháng đo được có thể được vẽ cùng với ECG để tìm ra sự thay đổi trở kháng, từ đó tính được sự thay đổi trở kháng. Bạn sẽ thấy sự thay đổi trở kháng lớn nhất sau khi khử cực tâm thất, khi thất tống máu và động mạch chủ giãn nở.
.jpg)
Phần dốc xuống từ đỉnh (maximum descending slope) được gọi là (dZ/dt) và được sử dụng để tính toán chỉ số co bóp của pha tống máu (EPCI) bằng cách nhân với tổng độ dẫn điện của chất lỏng.
Chỉ số này sau đó được sử dụng để ước tính thể tích nhát bóp. Điều này cần tỉnh khoảng R-R trên ECG để xác định thời gian thất tống máu (VET) và thể tích của mô tham gia dẫn điện (hoặc thể tích lồng ngực) (VEPT) – thứ được dự đoán dựa trên chiều cao, cân nặng và giới tính của bệnh nhân.
SV=VEPT x VET × EPCI
SV ở đây có thể dùng để tính CO.
4.3 Bioreactance
Trở kháng sinh học chỉ có thể đo sự thay đổi cường độ dòng điện. Bioreactance là một công nghệ cải tiến phân tích sự dịch chuyển pha tương đối của dao động dòng điện và kết quả tín hiệu điện áp.
Điều này ít bị ảnh hưởng bởi nhiễu ảnh chuyển động, sự thay đổi cơ thể bệnh nhân và vị trí điện cực và nó cho kết quả tốt hơn trong các nghiên cứu so sánh.4
Phương pháp sử dụng: 8 điện cực được đặt - 2 điện cực đặt ở mỗi bên cổ bộ nối cổ - ngực (thoracic inlet: nằm ở giữa xương sườn 1 và xương đòn) và 2 điện cực đặt mỗi bên cơ hoành (2 điện cực ghi lại điện áp nằm ở bên trong (inner transducing) và 2 điện cực phát ra dòng điện nằm ở bên ngoài (outer current electrode)). 1 dòng điện tần số cao, biên độ thấp truyền qua các điện cực này và hiệu điện thế được ghi lại. (hình 7)
4.3.1 Hạn chế
- Phụ thuộc vào vị trí điện cực.
- Dễ bị nhiễu và giả ảnh. (do chuyển động, dòng điện sinh nhiệt (electric diathermy))
- Dịch bất thường trong lồng ngực (dịch màng phổi) gây ra sai lệch kết quả.
- Giả định trong các phép tính (điện dung mạch máu không thay đổi khi hô hấp, sinh trở kháng thay đổi do lưu lượng máu động mạch chủ) dẫn đến sai số.
- Có sự tương quan dao động khi so sánh với tiêu chuẩn vàng - điều này được cải thiện bằng công nghệ Bioreactance.4
4.3.2 Lợi ích
- Không xâm lấn.
4.3.3 Biến chứng
Không có báo cáo đáng kể.
4.4 Siêu Âm Tim
Đây có thể được coi là phương pháp không xâm lấn hoặc bán xâm lấn để đánh giá cả giải phẫu và chức năng của tim.
Phương pháp sử dụng: Các phương pháp phổ biến được sử dụng trong thực hành lâm sàng bao gồm: Sử dụng đầu dò siêu âm đặt trên thành ngực để siêu âm qua thành ngực (TTE) hoặc trong thực quản để siêu âm qua thực quản (TOE). Cả 2 hình thức đánh giá này đều cung cấp hình ảnh tim để thể thực hiện các phép đo 1 số cấu trúc bao gồm: Diện tích mặt cắt ngang của động mạch chủ lên, đường ra thất trái (LVOT) và thậm chí cả thể tích thất trái (hình 6). Có thể quan sát Khoảng vận tốc - thời gian (VTi) hoặc Doppler xung bằng cách sử dụng mặt cắt 5 hoặc 3 buồng ở đỉnh tim. Về bản chất, sau khi tính toán diện tích của LVOT, Doppler sóng xung VTi sẽ cung cấp kết quả tốc độ máu di chuyển qua LVOT. Điều này tạo ra 1 biểu đồ vận tốc - thời gian. Bằng cách sử dụng diện tích bên dưới đường cong, biểu đồ này sẽ cho bạn biết khoảng cách mà dòng máu đã di chuyển. Thể tích nhát bóp (hay SV) có thể được tính = Diện tích LVOT x VTi, từ đó tính toán ra CO.
.jpg)
4.4.1 Lợi ích
- Phương pháp này nhanh chóng, hiệu quả và tương đối không xâm lấn (với TTE) để xác định CO của bệnh nhân.
- Có những tranh luận về việc liệu siêu âm tim có đạt đến "tiêu chuẩn vàng" của phương pháp pha loãng nhiệt hay không, nhưng 1 phân tích tổng hợp gần đây cho thấy không có sự khác biệt đáng kể giữa 2 hình thức đo đạc này 5 và các kỹ thuật này có thể thay thế cho nhau trong một số trường hợp nhất định.
4.4.2 Hạn chế
- Việc sử dụng công cụ này bị hạn chế ở một số nhóm bệnh nhân, ví dụ những bệnh nhân có chỉ số khối cơ thể cao có thể sẽ không tạo ra được hình ảnh tốt và phụ thuộc rất nhiều vào người siêu âm. Người siêu âm cần được đào tạo và thực hành quét đáng kể để đảm bảo đủ năng lực sử dụng - điều này có thể hạn chế tính khả dụng và tốc độ đánh giá của nó.
- Chỉ cung cấp 1 cửa sổ 'cắt nhanh' cung lượng tim của bệnh nhân tại 1 thời điểm cụ thể, do đó cần đánh giá lại nếu có sự thay đổi hoặc can thiệp vào trạng thái huyết động của bệnh nhân.
- TOE cần gây mê hoặc an thần để bệnh nhân dung nạp đầu dò và do đó hạn chế khả năng sử dụng của nó. Nó thường được sử dụng trong khi phẫu thuật tim hoặc trong đơn vị chăm sóc tim mạch đặc biệt.
4.4.3 Biến chứng
- TTE tương đối ít biến chứng, ngoài phản ứng với gel siêu âm.
- TOE xâm lấn hơn nhiều, không chỉ gây ra rủi ro gây mê, v.v. mà còn có thể dẫn đến nguy cơ tổn thương từ răng, môi và khoang miệng đến thực quản và dạ dày. 1 số yếu tố nguy cơ gồm: Rối loạn nhịp, chảy máu, thủng thực quản hoặc vỡ thực quản có thể cần can thiệp phẫu thuật để khắc phục.
.jpg)
5 References
1. Harvey S, Harrison DA, Singer M, et al. Assessment of the clinical effectiveness of pulmonary artery catheters in management of patients in intensive care (PAC-Man): a randomised controlled trial. Lancet 2005; 366: 472e7.
2. Frank O. The basic shape of the arterial pulse. First treatise:mathematical analysis. J Mol Cell Cardiol 1990; 22: 255e77.
3. Weber T, Wassertheurer S, Hametner B, et al. Noninvasive methods to assess pulse wave velocity: comparison with theinvasive gold standard and relationship with organ damage J Hypertens 2015; 33: 1023e31.
4. Saugel B, Cecconi M, Wagner JY, et al. Noninvasive continuouscardiac output monitoring in perioperative and intensive care medicine. Br J Anaesth 2015; 114: 562e75.
5. Zhang Y, Wang Y, Shi J, et al. Cardiac output measurements via echocardiography versus thermodilution: a systematic review andmeta-analysis. PLoS One 2019; 14: e0222105.
6 Further Reading
Chambers D, Huang C, Matthews G. Basic physiology for anaesthe-tists. 2nd edn. Cambridge: Cambridge University Press, 2019.
Deltex omega education on Doppler. https://www.deltexmedical.com/ decision_tree/doppler-specific-parameters/ (accessed 15 November2024). Kolb B, Kapoor V. Cardiac output measurement. Anaesth Intensive Care Med 2019; 20: 193e201.
LIDCO education pages. https://www.lidco.com/archives/LiDCOplus_brochure_1914.pdf (accessed 15 November 2024).
Squara P, Burkhoff D. Bioreactance. In: Vincent JL, Hall JB, eds. Ency- clopedia of intensive care medicine. Berlin, Heidelberg: Springer, 2012.

