Hỗ trợ hô hấp không xâm lấn tại khoa cấp cứu: Các tranh cãi và khuyến nghị hiện tại

Trungtamthuoc.com - Suy hô hấp cấp tính là lý do phổ biến khiến người bệnh phải đến khoa cấp cứu và nhập viện. Hiện nay, các chiến lược hỗ trợ hô hấp không xâm lấn đang là các phương pháp được sử dụng ngày càng nhiều. Bài viết này sẽ xem xét sinh lý học của suy hô hấp và các phương thức hỗ trợ hô hấp không xâm lấn, đồng thời đưa ra dữ liệu và khuyến nghị theo hướng dẫn trong bối cảnh có những tranh cãi lâm sàng quan trọng.
Bản dịch của Bác sĩ Đặng Thanh Tuấn – Bệnh viện Nhi Đồng 1
Tải PDF bản dịch TẠI ĐÂY
1 Tóm tắt
Suy hô hấp cấp tính là lý do phổ biến khiến người bệnh phải đến khoa cấp cứu và nhập viện. Những bất thường sinh lý cơ bản đa dạng dẫn đến những khía cạnh độc đáo về nguyên nhân phổ biến nhất của suy hô hấp cấp tính: suy tim mất bù cấp tính, đợt cấp của bệnh phổi tắc nghẽn mạn tính và suy hô hấp thiếu oxy cấp tính mới mắc. Các chiến lược hỗ trợ hô hấp không xâm lấn đang là các phương pháp được sử dụng ngày càng nhiều để hỗ trợ công thở và cải thiện các bất thường về trao đổi khí nhằm cải thiện kết quả liên quan đến liệu pháp oxy thông thường hoặc thở máy xâm lấn. Hỗ trợ hô hấp không xâm lấn bao gồm thông khí áp lực dương không xâm lấn và thở lưu lượng cao qua mũi, mỗi loại có cơ chế sinh lý riêng. Bài viết này sẽ xem xét sinh lý học của suy hô hấp và các phương thức hỗ trợ hô hấp không xâm lấn, đồng thời đưa ra dữ liệu và khuyến nghị theo hướng dẫn trong bối cảnh có những tranh cãi lâm sàng quan trọng.
2 Giới thiệu
Suy hô hấp cấp tính xảy ra ở 1275 người trên 100.000 người trưởng thành ở Hoa Kỳ. Lý do phổ biến nhất phải nhập viện cấp cứu (emergency department - ED) do suy hô hấp cấp là do đợt cấp của các bệnh mãn tính, phổ biến nhất là suy tim mất bù cấp tính (acute decompensated heart failure - ADHF) và bệnh phổi tắc nghẽn mạn tính (chronic obstructive pulmonary disease - AECOPD), tiếp theo là suy hô hấp thiếu oxy cấp tính mới mắc (acute de novo hypoxemic respiratory failure - AHRF) do nhiễm trùng cấp tính hoặc tổn thương phổi. Các chiến lược hỗ trợ hô hấp không xâm lấn (noninvasive respiratory support - NIRS) ngày càng được sử dụng nhiều trong phòng cấp cứu cho bệnh nhân suy hô hấp cấp tính, tăng hơn 400% từ năm 2002 đến năm 2017. Con số chính xác về việc sử dụng NIRS hàng năm không được theo dõi rõ ràng, nhưng ước tính tốt nhất cho thấy rằng hàng trăm nghìn số bệnh nhân mỗi năm được bắt đầu sử dụng NIRS tại ED, con số đã tăng đáng kể trong đại dịch COVID-19. Do nhận thức của bác sĩ ngày càng tăng và cuộc khủng hoảng nội trú ED ngày càng tồi tệ, việc sử dụng3 ED NIRS có thể sẽ tăng lên.
Đánh giá này sẽ mô tả các phương thức NIRS và các cơ chế sinh lý hỗ trợ suy hô hấp cấp tính, tóm tắt những tranh cãi, tài liệu và hướng dẫn hiện có, nêu bật những lỗ hổng kiến thức quan trọng và đưa ra các khuyến nghị thực tế cho việc sử dụng NIRS trong ED.
3 Nền tảng cơ bản của NIRS
3.1 Phương thức NIRS
Các phương thức NIRS bao gồm hỗ trợ dựa trên áp lực và hỗ trợ dựa trên lưu lượng.
NIRS dựa trên áp lực, còn được gọi là thông khí áp lực dương không xâm lấn (noninvasive positive pressure ventilation - NIPPV), bao gồm áp lực đường thở dương liên tục (continuous positive airway pressure - CPAP) và áp lực đường thở dương hai mức (bilevel positive airway pressure - BiPAP), và sử dụng mặt nạ mũi, mặt nạ mặt hoặc hệ thống dựa trên mũ bảo hiểm. Đặc điểm chung trên tất cả các giao diện này là mục đích cung cấp áp lực dương trong toàn bộ chu kỳ hô hấp (tức là CPAP) và tất cả chúng đều cung cấp áp lực dương cuối thì thở ra (PEEP). Áp lực hỗ trợ có thể được tạo ra bởi (1) lưu lượng liên tục qua van được thiết kế đặc biệt, (2) van thở ra hoặc (3) máy thở không xâm lấn. Để tạo ra áp lực bằng các van CPAP tạo lưu lượng liên tục, lưu lượng được phân chia thông qua các vi lỗ tạo ra một biến van PEEP ảo tương ứng với lượng lưu lượng qua nó. Một ví dụ nổi bật về van dựa trên lưu lượng là hệ thống Boussignac CPAP. Với các van thở ra, chẳng hạn như những van được gắn vào bóng giúp thở qua mặt nạ, PEEP được tạo ra thông qua lực cản vật lý đối với dòng thở ra, thường là thông qua việc siết chặt lò xo gắn vào màng ngăn một chiều. Với máy thở không xâm lấn, máy thổi/máy nén tạo ra áp lực dương cài đặt mong muốn.
Có sự khác biệt tinh tế giữa các phương thức hỗ trợ áp lực. Van Boussignac và PEEP cung cấp áp lực trong suốt giai đoạn thở ra, nhưng áp lực đường thở có thể giảm trong thì hít vào, đặc biệt nếu nỗ lực hô hấp cao. Ngược lại, máy thở không xâm lấn phải bù trừ cho áp lực đường thở giảm để tạo áp lực cho hệ hô hấp ở áp lực cài đặt trong suốt chu kỳ hô hấp (Hình 1). BiPAP giống như CPAP, nhưng mức áp lực khác nhau khi hít vào và thở ra, được gọi là áp lực đường thở dương thì hít vào (inspiratory positive airway pressure - IPAP) và áp lực đường thở dương thì thở ra (expiratory positive airway pressure - EPAP).

NIRS dựa trên lưu lượng được cung cấp bởi hệ thống lưu lượng cao qua mũi (nasal high flow - NHF) được thiết kế đặc biệt, cung cấp khí được làm nóng và làm ẩm với FiO2 có thể chuẩn độ thông qua hệ thống ống thông mũi được thiết kế đặc biệt. Các mức độ khít kín lỗ mũi khác nhau và tốc độ lưu lượng cố định mang lại hiệu quả sinh lý tương tự như hiệu quả đạt được với NIPPV (Hình 2). Khí được làm nóng và làm ẩm giúp cải thiện khả năng thanh thải chất nhầy, kiểm soát bài tiết và tạo cảm giác thoải mái. Khi tốc độ lưu lượng đạt đến hoặc vượt quá nhu cầu hít vào, công thở hít vào sẽ giảm. Cùng với nhau, những tác động này giúp cải thiện quá trình trao đổi khí và giảm công thở. Tuy nhiên, sinh lý NHF vẫn chưa được hiểu đầy đủ cũng như cơ học hô hấp thay đổi như thế nào theo tốc độ lưu lượng cũng như sự khác biệt giữa các hệ thống lưu lượng cao. Các nghiên cứu sinh lý học cho thấy công thở ra giảm bằng cách kéo dài thời gian thở ra do sức cản thở ra tăng lên khi thở ngược với lưu lượng không đổi, tương tự như tác động của hơi thở đối với PEEP.

3.2 Suy hô hấp và công thở
Suy hô hấp cấp tính xảy ra do bất kỳ tình trạng nào dẫn đến không thể thông khí hoặc cung cấp oxy hiệu quả. Suy hô hấp xảy ra khi có bất kỳ sự mất cân bằng nào trong việc sản xuất CO2 ngoại vi và sự thở ra CO2 ở phổi dẫn đến pH máu giảm. Thiếu oxy xảy ra chủ yếu thông qua shunt và thông khí: tưới máu không phù hợp do vô số nguyên nhân. Con đường cuối cùng phổ biến dẫn đến suy hô hấp cấp tính là thay đổi cơ học hô hấp, mệt mỏi và trao đổi khí bất thường. Tuy nhiên, sinh lý bệnh cơ bản dẫn đến hội chứng lâm sàng của suy hô hấp khác nhau giữa các nguyên nhân, tạo ra các cơ chế hỗ trợ NIRS khác nhau trong từng bệnh (Bảng 1).
Bảng 1. Đặc điểm của các kiểu hình suy hô hấp cấp.
Đặc trưng | ADHF | AECOPD | AHRF |
Lợi ích của NIRS | Cải thiện hiệu suất cơ tim | Giảm công hít vào của hơi thở Bù trừ PEEP tự động và xẹp đường thở động | Giảm sự không phù hợp V/Q Cải thiện trao đổi khí Giảm công thở |
Tỷ lệ tử vong | Thấp | Thấp | Cao |
Hiệu quả NIPPV so với NHF | Không rõ | Không thua kém | Không rõ |
Thể tích phổi lúc nghỉ | Bình thường đến giảm | Tăng | Giảm |
Tỷ lệ thất bại | Thấp | Thấp | Cao |
Thời gian hỗ trợ NIRS | Giờ | Giờ | Ngày |
Sinh lý bệnh | Phù phổi Áp lực đổ đầy tim cao Khả năng co bóp kém Trương lực mạch máu cao | Siêu lạm phát động, co thắt phế quản, mất nhu mô | Mất dung tích cặn chức năng, xẹp phổi hoặc thâm nhiễm phế nang, tính thấm nội mô, dòng viêm |
Chữ viết tắt: ADHF, suy tim mất bù cấp tính; AECOPD, đợt cấp của COPD; AHRF, suy hô hấp thiếu oxy cấp tính; NHF, lưu lượng mũi cao; NIPPV, thông khí áp lực dương không xâm lấn; NIRS, hỗ trợ hô hấp không xâm lấn.
Mục tiêu tổng thể khi sử dụng NIRS là giảm công thở, đây là một khái niệm phức tạp. Theo nghĩa đơn giản nhất, hơi thở cần năng lượng (công) để vượt qua: (1) lực đàn hồi của phổi (tức là độ giãn nở của phổi) để bơm phổi từ thể tích nghỉ ngơi (dung tích cặn chức năng) đến thể tích cuối thì hít vào tạo thể tích khí lưu thông, (2) lực của thành ngực (độ giãn nở của thành ngực) và (3) sức cản đối với luồng không khí. Tổng công thở là công mỗi hơi thở nhân với số lần thở mỗi phút. Bất cứ điều gì làm tăng khoảng chết (thông khí/tưới máu cao [V/Q]) đều dẫn đến thở nhanh và tăng thông khí phút để bù trừ cho thông khí phế nang hiệu quả bị suy giảm. Các bệnh lý làm giảm thể tích hoặc độ giãn nở của phổi khi nghỉ ngơi (ví dụ: ARDS, béo phì) sẽ làm tăng nỗ lực mỗi nhịp thở và dẫn đến tăng shunt trong phổi (V/Q thấp) sẽ gây ra tình trạng thiếu oxy máu, dẫn đến thở nhanh. Những gì chúng tôi quan sát được trên lâm sàng là nỗ lực và nhịp thở.
3.3 Hệ thống NIRS nào và khi nào?
Các bác sĩ lâm sàng nên ghi nhớ những điểm tổng quát này khi lựa chọn hệ thống NIRS dựa trên áp lực hoặc dựa trên lưu lượng để chăm sóc hô hấp tại ED.
1. Cả hệ thống NIPPV và NHF đều làm giảm công thở nhưng cần được sử dụng một cách thận trọng khi xem xét hiệu quả mong muốn và đáp ứng của bệnh nhân dựa trên nguyên nhân cơ bản (Bảng 3).
2. Cần có hệ thống máy thở để đạt được CPAP thực sự. Việc nâng cấp lên BiPAP có thể làm giảm công thở hơn nữa.
3. Đối với hệ thống NHF, tốt hơn nên cai máy khi bệnh nhân cải thiện hơn là điều chỉnh khi bệnh nặng hơn. Bắt đầu với lưu lượng cao hơn để giảm strain phổi nhiều nhất (thể tích khí lưu thông liên quan đến thể tích lúc nghỉ) và công thở, ngay cả khi trao đổi khí được cải thiện ở lưu lượng thấp hơn.
4 Tranh cãi về NIRS
4.1 Tranh cãi số 1: Có nên điều trị bệnh nhân mắc ADHF bằng NIPPV thay vì NHF?
Phù phổi do tim do ADHF xảy ra do áp lực tĩnh mạch phổi cao, dẫn đến xung huyết kẽ và phù phế nang. Khi áp lực tĩnh mạch phổi vượt quá áp lực phế nang (tức là các tình trạng của vùng West III), sự mất thể tích từ nước phổi ngoài mạch làm tăng diện tích shunt trong phổi và sự không phù hợp V/Q trở nên trầm trọng hơn. Kết hợp lại, điều này tạo ra hội chứng suy hô hấp lâm sàng với tình trạng thiếu oxy máu và tăng công thở.
NIPPV cải thiện tình trạng phù phổi do tim chủ yếu thông qua tác động hô hấp và huyết động của PEEP.8 Một quan niệm sai lầm phổ biến là PEEP “đẩy” phù nề ra khỏi phế nang, nhưng điều này không chính xác. Mặc dù có một số tác động nhỏ của sự chênh lệch áp lực từ phế nang vào hệ bạch huyết quanh phế nang, phù phổi chủ yếu được cải thiện thông qua cải thiện hoạt động của cơ tim. PEEP cải thiện dung tích cặn chức năng và giảm cả tiền tải và hậu tải thất trái, dẫn đến cải thiện nhanh tình trạng khó thở, nhịp thở và thiếu oxy máu.
Các bác sĩ lâm sàng thường sử dụng NIPPV cho ADHF, đặc biệt là CPAP. NHF cũng được sử dụng để điều trị ADHF nhưng ở mức độ thấp hơn. Tuy nhiên, bằng chứng so sánh trực tiếp NIPPV và NHF còn hạn chế và các nghiên cứu về NIPPV thường so sánh nó với oxy thông thường hơn là NHF. Mặc dù có những thử nghiệm đang diễn ra, nhưng bằng chứng gần đây ủng hộ NHF như một giải pháp thay thế khả thi cho NIPPV trong điều trị ADHF. So sánh NHF với NIPPV chỉ mang tính chất quan sát. Một nghiên cứu tiền cứu ở những bệnh nhân tăng CO2 bị phù phổi do tim không tìm thấy sự khác biệt về độ thanh thải CO2 hoặc công thở, trong khi một nghiên cứu hồi cứu cho thấy tỷ lệ thất bại tăng lên ở những bệnh nhân bị phù phổi do tim hoặc tăng CO2 máu khi điều trị bằng NHF. Thử nghiệm duy nhất được công bố so sánh NHF với NIPPV cho thấy CPAP qua mũ bảo hiểm có sự cải thiện lớn hơn về tình trạng suy hô hấp sau 1 giờ.
Người ta biết rất ít về tác dụng sinh lý của NHF đối với chứng phù phổi cấp do tim. Tuy nhiên, do NHF làm tăng thể tích phổi cuối thì thở ra mà không cần áp lực dương trong lồng ngực cần thiết, lợi ích cho bệnh nhân ADHF có thể là do cơ học phổi và trao đổi khí được cải thiện hơn là hiệu suất của cơ tim.
Ý nghĩa đối với thực hành ED
Mặc dù các hướng dẫn khuyến cáo mạnh NIPPV cho ADHF, nhưng bằng chứng ủng hộ khuyến nghị này chỉ có chất lượng vừa phải (Bảng 2). Do đó, các bác sĩ lâm sàng nên coi cả NIPPV và NHF là phương pháp điều trị ban đầu tiềm năng cho ADHF. Đối với NIPPV, điều hợp lý là bắt đầu CPAP/EPAP ở mức vừa phải (8–10 cm H2O) và điều chỉnh tăng dần tùy theo khả năng dung nạp, đồng thời thêm IPAP để giảm thêm công thở. Đối với NHF, cách tiếp cận ngược lại—bắt đầu ở lưu lượng cao để tối đa hóa thể tích phổi cuối thì thở ra và cai máy dựa trên công thở—có thể là cách tiếp cận tối ưu (Bảng 3).
4.2 Tranh cãi số 2: Bệnh nhân mắc AECOPD hoặc tăng CO2 máu có nên được điều trị bằng NIPPV thay vì NHF?
Đối với AECOPD, xẹp đường thở động dẫn đến bẫy khí, PEEP tự động, siêu bơm phồng và tăng công thở do các cơ hô hấp bị căng quá mức và dẫn đến thở nhanh. NIPPV có thể hỗ trợ từng hiệu ứng này. Nếu EPAP được đặt dưới mức PEEP tự động thì EPAP sẽ làm giảm tình trạng xẹp đường thở động, giảm PEEP tự động và công thở ra mà không đóng góp vào tổng PEEP. IPAP làm giảm nỗ lực hít vào (giảm công thở) trên các cơ hô hấp vốn đã căng quá mức và mệt mỏi.
Bảng 2. Hướng dẫn thực hành lâm sàng thích hợp.
Hướng dẫn | Dân số bệnh nhân | Tuyên bố | Sức mạnh của khuyến nghị | Sự chắc chắn của bằng chứng |
Hiệp hội Y học Chăm sóc Chuyên sâu Châu Âu Nhóm làm việc về Áp lực màng phổi | AHRF | “Chúng tôi khuyến nghị sử dụng HFNC so với COT cho bệnh nhân suy hô hấp thiếu oxy” | Mạnh | Vừa phải |
Hiệp hội Hô hấp Châu Âu/Hiệp hội Lồng ngực Hoa Kỳ | AeCOPD | “Chúng tôi đề nghị không sử dụng NIV ở những bệnh nhân tăng CO2 máu không bị nhiễm toan trong bối cảnh đợt cấp của COPD.” | Có điều kiện | Thấp |
AeCOPD | “Chúng tôi khuyến nghị NIV hai mức áp lực cho bệnh nhân mắc ARF dẫn đến nhiễm toan hô hấp cấp tính hoặc cấp tính trên nền mãn tính (pH ⩽ 7,35) do đợt cấp của COPD.” | Mạnh | Cao | |
| “Chúng tôi khuyến nghị thử nghiệm NIV hai mức áp lực ở những bệnh nhân được coi là cần đặt nội khí quản và thở máy, trừ khi tình trạng bệnh nhân xấu đi ngay lập tức.” | Mạnh | Vừa phải | |
ADHF | “Chúng tôi khuyên dùng NIV hai mức áp lực hoặc CPAP cho bệnh nhân mắc ARF do phù phổi do tim.” | Mạnh | Vừa phải | |
ADHF | “Chúng tôi đề nghị sử dụng CPAP hoặc NIV hai mức áp lực cho bệnh nhân mắc ARF do phù phổi do tim ở môi trường trước bệnh viện.” | Có điều kiện | Thấp | |
Hen suyễn | “Do bằng chứng không chắc chắn, chúng tôi không thể đưa ra khuyến nghị về việc sử dụng NIV cho ARF do hen suyễn.” |
|
| |
Suy giảm miễn dịch | “Chúng tôi đề nghị NIV sớm cho những bệnh nhân suy giảm miễn dịch mắc ARF.” | Có điều kiện | Vừa phải | |
AHRF | “Do bằng chứng không chắc chắn, chúng tôi không thể đưa ra khuyến nghị về việc sử dụng NIV cho ARF mới bắt đầu.” |
|
| |
Chấn thương | “Chúng tôi đề xuất NIV cho bệnh nhân chấn thương ngực mắc ARF.” | Có điều kiện | Vừa phải | |
Hiệp hội Y học Chăm sóc Chuyên sâu Châu Âu | AHRF | “Chúng tôi khuyến nghị những bệnh nhân mắc AHRF không có thở máy không phải do phù phổi do tim hoặc đợt cấp của COPD nên sử dụng HFNO so với liệu pháp oxy thông thường để giảm nguy cơ đặt nội khí quản.” | Mạnh | Vừa phải |
“Chúng tôi không thể đưa ra khuyến nghị ủng hộ hay phản đối việc sử dụng HFNO thay vì liệu pháp oxy thông thường để giảm tỷ lệ tử vong.” | Không có |
| ||
“Chúng tôi không thể đưa ra khuyến nghị ủng hộ hay phản đối việc sử dụng HFNO so với áp lực đường thở dương liên tục (CPAP)/NIV để giảm đặt nội khí quản hoặc tử vong trong điều trị những bệnh nhân không được lựa chọn bị suy hô hấp thiếu oxy cấp tính không phải do phù phổi do tim”. hoặc đợt cấp của bệnh COPD.” | Khôngb |
| ||
“Chúng tôi đề nghị có thể xem xét CPAP/NIV thay vì HFNO trong điều trị AHRF do COVID-19 nhằm giảm nguy cơ đặt nội khí quản (khuyến cáo yếu, mức độ bằng chứng cao), nhưng không thể đưa ra khuyến nghị nào về việc có nên sử dụng CPAP/NIV hay không”. có thể làm giảm tỷ lệ tử vong so với HFNO trong COVID-19.” | Không có | Cao | ||
“Chúng tôi không thể đưa ra khuyến nghị ủng hộ hay phản đối việc sử dụng CPAP/NIV so với liệu pháp oxy thông thường để điều trị AHRF (không liên quan đến phù phổi do tim hoặc đợt cấp của COPD) để giảm tỷ lệ tử vong hoặc ngăn ngừa đặt nội khí quản.” | Khôngc |
| ||
“Chúng tôi đề nghị sử dụng CPAP thay vì liệu pháp oxy thông thường để giảm nguy cơ đặt nội khí quản ở những bệnh nhân bị suy hô hấp thiếu oxy cấp tính do COVID-19.” | Yếu | Thấp | ||
“Trong nhóm đối tượng này, chúng tôi không thể đưa ra khuyến nghị ủng hộ hay phản đối việc sử dụng CPAP thay vì liệu pháp oxy thông thường để giảm tử vong.” | Không cód |
| ||
“Chúng tôi không thể đưa ra khuyến nghị ủng hộ hay phản đối việc sử dụng giao diện mũ bảo hiểm cho CPAP/NIV so với mặt nạ để ngăn ngừa đặt nội khí quản hoặc giảm tỷ lệ tử vong suy hô hấp thiếu oxy cấp tính.” | Khôngai | Rất thấp | ||
“Chúng tôi không thể đưa ra khuyến nghị ủng hộ hay phản đối việc sử dụng NIV so với CPAP để điều trị AHRF.” | Không có | Không có bằng chứng |
aMức độ cao của bằng chứng không có tác dụng.
bMức độ bằng chứng trung bình về tỷ lệ tử vong, mức độ bằng chứng thấp về việc đặt nội khí quản, không ủng hộ cũng không phản đối.
cMức độ bằng chứng cao về tỷ lệ tử vong, mức độ bằng chứng trung bình về việc đặt nội khí quản.
dMức độ vừa phải của bằng chứng không có tác dụng.
eBằng chứng ủng hộ ở mức độ rất thấp.
Bảng 3. Cài đặt bắt đầu và những gì cần theo dõi NIRS trong ED
| NHF | CPAP | NIPPV | Hiệu ứng mong muốn | Khi nào nên đặt nội khí quản |
Suy tim mất bù cấp tính | FiO2 = 100% Lưu lượng = dựa trên sự thoải mái/khó thở và SpO2 | FiO2 = 100% CPAP = 8–10 cm H2O, dựa trên mức độ thoải mái/khó thở và khả năng chịu đựng | FiO2 = 100% EPAP = 8–10 cm H2O dựa trên dung nạp IPAPa = 5+ điều chỉnh dựa trên mức độ thoải mái/khó thở | Áp lực dương cuối thì thở ra là cần thiết để cải thiện hiệu suất cơ tim. PEEP, cũng như EELV với NHF sẽ cải thiện cơ học hô hấp. | Vào lúc 1–2 giờ nếu: Sốc tim Trạng thái trầm cảm Mệt mỏi hô hấp mặc dù hỗ trợ NIRS tối ưu Cân nhắc ở bệnh nhân cần chụp động mạch vành |
Đợt cấp của bệnh COPD | FiO2 = tăng 50% để giữ SpO2 ở mức 88–90% Lưu lượng = mức tối đa khả dụng cho hệ thống được sử dụng. | FiO2 = tăng 50% để giữ SpO2 ở mức 88– 90% CPAP = 5–8 cm H2O, dựa trên công thở | FiO2 = 100% EPAPb = 5–8 cm H2O IPAP = 10–12 cm H2O điều chỉnh dựa trên công thở | Bù trừ autoPEEP, giảm công thở và cải thiện thông khí. | Vào lúc 1–2 giờ nếu: Mệt mỏi hô hấp mặc dù NIRS tối ưu Trạng thái trầm cảm Nhiễm toan hô hấp nặng (pH < 7,2) |
Suy hô hấp thiếu oxy cấp tính | FiO2 = 100% Lưu lượng = mức tối đa khả dụng cho hệ thống được sử dụng. | FiO2 = 100% CPAP = 10cmH2O | FiO2 = 100% EPAPc = 10 cm H2O IPAPd = 5 cm H2O, điều chỉnh dựa trên thể tích khí lưu thông | Cải thiện sự không phù hợp giữa FRC và V/Q, giảm nỗ lực hô hấp và công thở tổng thể | Trong vòng 3–4 giờ nếu: Nỗ lực hô hấp cao mặc dù lưu lượng tối đa với NHF hoặc PEEP 10+ với NIPPV Chỉ số ROX không thuận lợie (tỷ lệ SF thấp trên nhịp thở cao) Thở nhanh (RR > 30) mặc dù được hỗ trợ tối đa Giảm oxy máu (SpO2 < 90%) |
aIPAP trong ADHF chỉ nhằm mục đích tạo sự thoải mái và hỗ trợ cho công thở khi cần thiết.
bEPAP trong AECOPD bù trừ cho tình trạng xẹp đường thở động và autoPEEP, nhưng IPAP cần thiết cho công thở để giúp giảm tải cho các cơ hô hấp bị căng quá mức.
cEPAP trong AHRF là cần thiết để huy động bất kỳ nhu mô phổi nào có thể huy động được nhằm giảm tính không đồng nhất tổng thể, cải thiện dung tích cặn chức năng và giảm sự không phù hợp V/Q.
dIPAP trong AHRF làm giảm công thở vào, nhưng có nguy cơ gây tổn thương thể tích khí lưu thông. Sự khác biệt giữa IPAP và EPAP là áp lực đẩy đường thở để hỗ trợ thông khí. Tuy nhiên, đó là một mối quan hệ phức tạp với nỗ lực hô hấp. Nếu thể tích khí lưu thông thấp, EPAP có thể cần phải tăng lên để vượt quá áp lực mở tới hạn của các đơn vị phổi phụ thuộc, đặc biệt ở những bệnh nhân béo phì hoặc độ giãn nở của thành ngực kém.
eChỉ số ROX là (SpO2:FiO2)/nhịp thở và là đánh giá mối quan hệ giữa mức độ thiếu oxy (SpO2:FiO2) với công thở (nhịp thở).
NHF có thể hỗ trợ AECOPD thông qua các cơ chế khác nhau, chủ yếu bằng cách xả sạch khoảng chết, giúp loại bỏ CO2 hiệu quả hơn và cung cấp khí sạch khi bắt đầu hít vào.20 Giải phóng khoảng chết và hỗ trợ thể tích phổi cuối kỳ thở ra tăng lên với NHF (có khả năng có thể bù trừ PEEP tự động), làm giảm nỗ lực hít vào và giảm công thở, và đã được chứng minh là tương đối hiệu quả trong AECOPD.
NIPPV hiện được coi là tiêu chuẩn chăm sóc cho AECOPD, tuy nhiên dữ liệu cho thấy có lợi ích cho NHF. Một nghiên cứu quan sát, đánh giá hệ thống và phân tích tổng hợp gần đây cho thấy không có sự khác biệt về thất bại điều trị hoặc tử vong giữa NHF và NIPPV trong AECOPD. NHF không thua kém về mặt thống kê so với NIPPV trong một thử nghiệm đa trung tâm dựa trên mức giảm tương tự về PaCO2 sau 2 giờ. Mặc dù tỷ lệ chéo cao từ NHF sang NIPPV, một phân tích phân nhóm theo kế hoạch cho thấy tác động lên PCO2 và pH, tỷ lệ đặt nội khí quản và tỷ lệ thất bại điều trị là tương tự ở bệnh nhân tăng CO2 máu. NHF làm giảm PaCO2 một cách hiệu quả ở những bệnh nhân tăng CO2 máu chủ yếu bị viêm phổi và COPD. Những dữ liệu này cho thấy NHF là hợp lý ở bệnh nhân AECOPD và bệnh nhân suy hô hấp nguyên nhân hỗn hợp và tăng CO2 máu, nhưng cần có nhiều thử nghiệm lâm sàng hơn ở nhóm đối tượng này.
Ý nghĩa đối với thực hành ED
Các hướng dẫn khuyến nghị mạnh NIPPV cho bệnh nhân mắc AECOPD, tăng CO2 máu và nhiễm toan (Bảng 2). Tuy nhiên, cách tiếp cận tốt nhất đối với AECOPD, tăng CO2 máu mà không nhiễm toan, vẫn chưa rõ ràng. Vì nguyên nhân gây suy hô hấp cấp ở hầu hết bệnh nhân cấp cứu có thể không được xác định khi bắt đầu NIRS, NHF là cách tiếp cận ban đầu hợp lý đối với AECOPD. Nếu bệnh nhân có biểu hiện toan máu với công thở cao ở mức NHF tối đa, các bác sĩ lâm sàng có thể cân nhắc chuyển sang NIPPV. Không giống như ADHF trong đó PEEP/CPAP là áp lực cải thiện tình trạng suy hô hấp nhiều nhất, trong AECOPD, IPAP làm giảm công thở nhiều nhất. Vì vậy, khi sử dụng NIPPV, hãy giữ EPAP ở mức PEEP tự động (5–8 cm H2O) và tăng hỗ trợ áp lực hít vào cho đến khi công thở và thông khí phút được cải thiện (Bảng 3).
4.3 Tranh cãi số 3: Có nên điều trị bệnh nhân mắc AHRF bằng NHF thay vì NIPPV?
Ở những bệnh nhân mắc AHRF, viêm phổi, nhiễm trùng hoặc viêm dẫn đến mất thể tích do bệnh nhu mô đường thở làm giảm dung tích cặn chức năng và làm tình trạng mất cân bằng V/Q trầm trọng hơn. Những thay đổi này dẫn đến thở nhanh và thiếu oxy. Trái ngược với những bệnh nhân mắc AECOPD bị giảm lực hít vào do phổi quá giãn nở, bệnh nhân mắc AHRF đã tăng lực hít vào thông qua cơ chế Starling nếu nỗ lực hô hấp được bảo toàn. Ngoài ra, không giống như những bệnh nhân mắc AECOPD hoặc ADHF khi NIRS thường chỉ được yêu cầu trong thời gian ngắn, AHRF thường yêu cầu hỗ trợ hô hấp trong thời gian dài hơn và thường trở nên tồi tệ hơn trong quá trình điều trị nguyên nhân cơ bản.
NIPPV là con dao hai lưỡi ở bệnh nhân AHRF. Thở tự nhiên với áp lực dương có thể cải thiện thông khí vùng đến các vùng phổi phụ thuộc (cải thiện sự không phù hợp V/Q), giúp cải thiện chức năng tim phổi và ngăn ngừa teo cơ hoành. Những lợi ích này có liên quan đến việc ít ngày thở máy hơn và có khả năng giảm các chất trung gian gây viêm trong phân tích rửa phế quản phế nang. Mặt khác, lực hít vào tăng lên khi có bệnh khoảng không (airspace) đồng nhất dẫn đến sự khuếch đại áp lực xuyên phổi theo vùng (sự khác biệt giữa áp lực phế nang và áp lực màng phổi xung quanh), dẫn đến sự phân phối lại thể tích trong khí lưu thông theo vùng (tức là pendelluft))—có nguy cơ xảy ra các khu vực trọng tâm của chấn thương khí áp và thể tích khí lưu thông gây tổn thương tổng thể (tổn thương phổi do bệnh nhân gây ra [patient-self-induced lung injury - P-SILI]).
NHF có một số tác dụng có lợi đối với cơ học hô hấp ở bệnh nhân mắc AHRF, giúp cung cấp thông khí và hỗ trợ oxygen hóa ngoài việc chỉ đơn giản làm sạch khoảng chết giải phẫu bằng oxy tươi. NHF cung cấp các hiệu ứng phụ thuộc vào lưu lượng lên cơ học phổi tương tự như NIPPV nhưng không có áp lực. Những lợi ích này bao gồm dao động áp lực thực quản thấp hơn (giảm nỗ lực hít vào), cải thiện độ giãn nở phổi động (thay đổi thể tích khí lưu thông/áp lực thực quản), tích số áp lực theo thời gian thấp hơn và giảm tổng thể tích phổi (tức là thể tích khí lưu thông)/dung tích cặn chức năng). Có sự phân bổ sai phổ biến về một lượng nhỏ PEEP do NHF tạo ra. Mặc dù NHF tạo ra một số áp lực dương ở hầu họng, nhưng có sự gia tăng phụ thuộc vào lưu lượng trong thể tích phổi cuối thì thở ra (EELV, tức là dung tích cặn chức năng), được bảo tồn tương đối mặc dù mất gần như hoàn toàn áp lực dương ở mũi họng (tức là “PEEP”) khi miệng mở ra vào cuối thì thở ra. Sự tăng EELV này, hay hiệu ứng giống PEEP, làm giảm tình trạng xẹp phổi và tăng lượng oxygen hóa. Những phát hiện này cho thấy rằng tác động lên quá trình oxygen hóa khó có thể xảy ra thông qua bất kỳ áp lực họng dương nào. Ngoài ra, NHF có thể làm giảm khả năng điều hòa hô hấp và công thở mà không làm tăng thể tích khí lưu thông có hại. Tác dụng có lợi đối với công thở (nhịp thở) và oxygen hóa (độ bão hòa oxy) có thể được thấy ngay sau 15 phút sau khi bắt đầu NHF, với sự cải thiện về PaO2 và tỷ lệ PaO2/FiO2 xảy ra trong vòng 1 giờ. Nếu tốc độ dòng khí NHF đủ hỗ trợ nhu cầu lưu lượng hít vào của bệnh nhân, bệnh nhân sẽ thở FiO2 do hệ thống cài đặt và không bị pha loãng bởi khí phòng.
Dữ liệu lâm sàng về AHRF rất phức tạp để giải thích. Các chiến lược NIRS ngày càng được sử dụng làm phương pháp điều trị đầu tay cho AHRF, bao gồm cả ARDS. NIPPV và NHF đều có kết quả tốt hơn (giảm tỷ lệ đặt nội khí quản, viêm phổi, thời gian nằm ICU và tử vong) so với liệu pháp oxy thông thường, nhưng có rất ít so sánh trực tiếp giữa NHF và NIPPV, ít nhất cho đến khi xảy ra đại dịch COVID-19. Các nghiên cứu quan sát báo cáo tỷ lệ thất bại NIPPV cao ở bệnh nhân mắc AHRF, có liên quan đến tỷ lệ tử vong tăng lên và thời gian nằm ICU lâu hơn. NIPPV là phương thức điều trị đầu tiên ở 15% bệnh nhân trong một nghiên cứu quan sát lớn, với tỷ lệ thất bại chung là 32%, tăng tuyến tính theo mức độ nghiêm trọng của ARDS (22% ở ARDS nhẹ, 42% ở mức độ trung bình, 47% ở mức độ nặng) và tỷ lệ tử vong tăng 30% (45 so với 16%).
Thử nghiệm FLORALI mang tính bước ngoặt cho thấy tỷ lệ tử vong trong 90 ngày do NHF giảm ở các bệnh nhân ICU khác bị AHRF do viêm phổi, một kết quả thứ cấp, nhưng không có sự khác biệt về tỷ lệ đặt nội khí quản. Tuy nhiên, những bệnh nhân được chọn điều trị FLORALI đều đến từ phòng ICU và có chẩn đoán rõ ràng. Những kết quả này rất khó ngoại suy cho ED, trong đó nguyên nhân gây ARF của bệnh nhân ban đầu thường không được phân biệt và chiến lược NIRS phải được lựa chọn trước khi chẩn đoán rõ ràng. Doshi và cộng sự đã chỉ ra rằng NHF không thua kém NIPPV về tỷ lệ đặt nội khí quản trên diện rộng, trong một thử nghiệm nhỏ trên các bệnh nhân ED không phân biệt.
Các nghiên cứu của NIRS về AHRF do COVID-19 cho thấy kết quả rất khác nhau. Một số cho thấy kết quả được cải thiện với NHF so với oxy thông thường hoặc NIPPV. Một số cho thấy kết quả được cải thiện với NIPPV so với oxy thông thường hoặc NHF. Một số không có sự khác biệt khi so sánh với oxy thông thường hoặc với nhau. Tuy nhiên, việc sử dụng NIRS ngày càng tăng trong đại dịch COVID-19 đã nâng cao kiến thức của chúng ta về sinh lý học liên quan đến NIRS trong AHRF và dẫn đến việc phải suy nghĩ lại về định nghĩa ARDS.
Các đánh giá hệ thống và phân tích tổng hợp gần đây cho thấy NIRS có liên quan đến việc giảm đặt nội khí quản và tỷ lệ tử vong, nhưng lợi ích bị sai lệch bởi NIPPV qua mũ bảo hiểm. Một phân tích tổng hợp cho thấy cả NIPPV và NHF đều làm giảm tỷ lệ đặt nội khí quản và tỷ lệ tử vong so với thở oxy thông thường, nhưng không có sự khác biệt giữa mặt nạ NIPPV và NHF. Ba nghiên cứu cho thấy không có sự khác biệt về đặt nội khí quản và tử vong giữa NIPPV và NHF. Tuy nhiên, phân tích dưới nhóm cho thấy NHF có liên quan đến tỷ lệ đặt nội khí quản thấp hơn NIPPV ở những bệnh nhân có tỷ lệ PaO2:FiO2 thấp < 150), nhưng không có ở tỷ lệ PaO2:FiO2 [tương đối] cao. Một số hướng dẫn thực hành lâm sàng đã cố gắng tổng hợp bằng chứng thành hướng dẫn trong những năm gần đây và các khuyến nghị thích hợp được tóm tắt trong Bảng 2. Nhìn chung, cần có nhiều thử nghiệm chất lượng cao hơn đối với bệnh nhân mắc AHRF, như được nhấn mạnh trong hướng dẫn gần đây nhất của Hiệp hội Y học Chăm sóc Chuyên sâu Châu Âu.
Ý nghĩa đối với thực hành ED
Các hướng dẫn này tương đối thiếu thông tin đối với bệnh nhân ED do sự phức tạp trong việc diễn giải các dữ liệu khác nhau (Bảng 2). Dữ liệu tổng thể cho thấy có sự cân bằng giữa NHF và NIPPV ở bệnh nhân mắc AHRF. Vì mục tiêu của cả hai phương thức NIRS trong AHRF là giảm công thở, nên hãy bắt đầu với lưu lượng tối đa khi sử dụng NHF và PEEP cao hơn (10 cm H2O) khi sử dụng NIPPV để tối đa hóa thể tích phổi cuối kỳ thở ra, dung tích cặn chức năng và giảm sự không phù hợp của V/Q và lực hít vào (Bảng 3). Chúng tôi khuyên bạn nên sử dụng máy thở không xâm lấn cho NIPPV, thay vì các lựa chọn thay thế như van PEEP hoặc van CPAP tạo lưu lượng trừ khi ở các cơ sở trước khi nhập viện hoặc nguồn lực hạn chế.
4.4 Tranh cãi số 4: Thất bại NIRS có làm tăng nguy cơ tử vong không?
Thất bại của NIRS, đặc biệt là NIPPV, có liên quan đến tỷ lệ tử vong quá mức, đặt ra câu hỏi liệu có yếu tố gây nhiễu nào không (tức là, “bệnh nhân nặng hơn thất bại và tỷ lệ tử vong của họ cao hơn”) hoặc liệu một hoặc tất cả các phương thức NIRS có thể gây tổn thương do điều trị hay không. Bằng chứng gần đây cho thấy có những rủi ro tiềm ẩn đối với việc thở tự nhiên ở áp lực dương ở một số bệnh nhân mắc AHRF và điều hòa hô hấp cao có thể làm tổn thương phổi nặng hơn. Có một mối quan hệ phức tạp giữa sự đóng góp của thần kinh và ngoại biên đối với hoạt động điều hòa hô hấp và nỗ lực. Nỗ lực hô hấp cao trong khi thở tự nhiên với áp lực dương sẽ duy trì thể tích khí lưu thông có hại. Ngoài ra, sự khuếch đại không đồng nhất của áp lực xuyên phổi được tạo ra từ nhịp thở gắng sức hô hấp cao được cho là góp phần tạo ra P-SILI, đây là một cơ chế bị nghi ngờ gây ra tỷ lệ thất bại cao và tỷ lệ tử vong vượt mức được quan sát thấy với sự cố NIRS. Mức tăng cao này có thể giảm khi mức PEEP cao hơn, nhưng điều này thường cần mũ bảo hiểm. Điều này ít nhất có thể giải thích một phần kết quả được cải thiện khi sử dụng mũ bảo hiểm NIPPV so với mặt nạ NIPPV. Như vậy, NIRS vẫn là con dao hai lưỡi. Việc sử dụng thành công NIRS giúp cải thiện kết quả (giảm tỷ lệ tử vong, số ngày thở máy, v.v.), trong khi thử nghiệm NIRS không thành công có thể làm tăng tỷ lệ tử vong. Do đó, việc xác định các cơ chế gây ra lỗi và các phương pháp dự đoán lỗi đáng tin cậy được cho là lỗ hổng kiến thức quan trọng nhất cho tương lai của NIRS.
Dự đoán thất bại bằng cách sử dụng dữ liệu lâm sàng có sẵn rộng rãi là một thách thức. Một số nghiên cứu đã xác định các yếu tố liên quan hoặc dự đoán sự thất bại của cả NIPPV và NHF, tất cả thường liên quan đến các chỉ số về công thở hoặc mức độ nghiêm trọng của tình trạng thiếu oxy máu ở dạng này hay dạng khác. Chỉ số ROX [(SpO2/FiO2)/nhịp thở] được lấy và xác nhận để xác định xem bệnh nhân có khả năng thành công hay thất bại NHF. Giá trị > 4,88 có giá trị tiên đoán khá tốt khi không cần đặt nội khí quản, trong khi các giá trị < 2,85 lúc 2 giờ, < 3,47 lúc 6 giờ và < 3,85 lúc 12 giờ là những yếu tố dự báo thất bại NHF, để lại một khoảng giá trị lớn không có thông tin đầy đủ. Ngoài ra, chỉ số ROX chỉ được xác nhận cho một loại hệ thống lưu lượng cao cụ thể và phần lớn phụ thuộc vào lưu lượng, với sự gia tăng chỉ số ROX khi lưu lượng từ 30 đến 60 L mỗi phút có khả năng phản ánh mức độ nghiêm trọng cao hơn của bệnh phổi hơn là nỗ lực. Công việc gần đây hơn đã sử dụng các mô hình học sâu để phát triển các thuật toán dự đoán nhằm xác định bệnh nhân có nguy cơ cần thở máy ở bệnh nhân COVID-19 nhập viện và dự đoán thất bại NIRS ở bệnh nhân suy hô hấp cấp, với kết quả hứa hẹn.
Ý nghĩa đối với thực hành ED
Xác định sớm thất bại là rất quan trọng. Mặc dù bệnh nhân có thể được cung cấp oxy hoặc thông khí đầy đủ, nhưng nếu nỗ lực hô hấp không giảm, những bệnh nhân đó có nguy cơ cao bị suy hô hấp, phải đặt nội khí quản và tỷ lệ tử vong cao hơn. Cần đặc biệt chú ý đến việc đánh giá nỗ lực hô hấp mặc dù đã thở oxy. Về mặt khái niệm, chỉ số ROX có thể đánh giá mức độ thiếu oxy máu và shunt (SpO2/FiO2) đối với công thở (nhịp thở) bất kể phương thức NIRS (Hình 3). Nếu được cung cấp đủ oxy và công thở thấp thì nguy cơ thất bại sẽ thấp. Nếu có đủ oxy và công thở cao, hoặc shunt cao và công thở cao thì không nên trì hoãn đặt nội khí quản. Với những trường hợp ngoại lệ hiếm gặp ở bệnh nhân mắc AHRF, việc một phương thức NIRS không làm giảm công thở nên được coi là một dấu hiệu để đặt nội khí quản, chứ không phải chuyển sang phương thức NIRS khác.
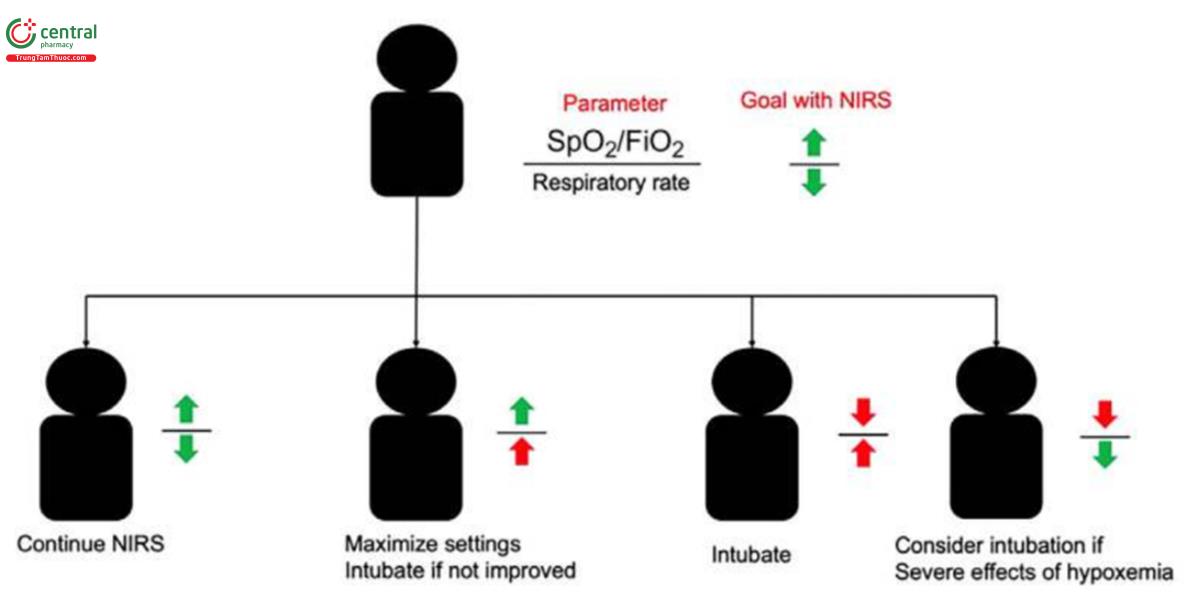
4.5 Tranh cãi số 5: Bệnh nhân được điều trị bằng NIPPV có nguy cơ mắc P-SILI cao hơn NHF không?
Cho đến nay, P-SILI phần lớn là một rủi ro về mặt lý thuyết mà không có bằng chứng rõ ràng, tuy nhiên hai nghiên cứu gần đây đã cho thấy bằng chứng trực tiếp ủng hộ giả thuyết P-SILI. Grieco và cộng sự đã so sánh nỗ lực hô hấp (∆P thực quản) giữa NHF và NIPPV mũ bảo hiểm ở bệnh nhân mắc AHRF trong một thử nghiệm chéo. Sự dao động áp lực xuyên phổi (∆PL) nhìn chung cao hơn với NIPPV, đặc biệt khi nỗ lực hít vào thấp ở bệnh nhân mắc NHF. Tuy nhiên, những người có nỗ lực hô hấp cao khi sử dụng NHF có mức giảm nỗ lực lớn nhất khi chuyển sang mũ bảo hiểm NIPPV, cho thấy rằng NIPPV có tác dụng bảo vệ đối với một số bệnh nhân và gây tổn hại cho những người khác. Nỗ lực hít vào cao và dao động áp lực xuyên phổi có liên quan đến việc cần đặt nội khí quản muộn hơn 12 giờ ở những người được điều trị bằng NIPPV, nhưng mối liên quan đó không có ý nghĩa đối với NHF.98 Những phát hiện này đã được hỗ trợ thêm trong nghiên cứu thứ hai, trong đó Tonelli và cộng sự105 ghi danh bệnh nhân mắc AHRF đến NIPPV bằng mặt nạ có PEEP được đặt ở 4–8 cm H2O và hỗ trợ áp lực được điều chỉnh để giữ thể tích khí lưu thông < 9,5 mL/kg. Những bệnh nhân thất bại với NIPPV sau 24 giờ đã tăng đáng kể nỗ lực hít vào (∆P thực quản) và áp lực xuyên phổi (∆PL) sau 2 giờ so với những bệnh nhân được điều trị thành công bằng NIPPV.105 Những bệnh nhân này cũng có hình ảnh ngực xấu đi sau 24 giờ, trong khi những bệnh nhân giảm nỗ lực hít vào lúc 2 giờ lại có hình ảnh ngực được cải thiện sau 24 giờ. Thay đổi ∆P thực quản <10 cm H2O sau 2 giờ NIPPV dự đoán chính xác nhất tình trạng NIPPV thất bại sau 24 giờ.
Về cơ bản, mối tương quan nghịch giữa nỗ lực hít vào (∆P thực quản) và độ giãn nở của phổi (VT/∆PL) có nghĩa là khi có nỗ lực tự phát mạnh, thể tích phổi ban đầu giảm theo tỷ lệ sẽ tăng sức mạnh của nỗ lực tự phát do lực co cơ hoành lớn hơn thông qua cơ chế Starling. Ngoài ra, nỗ lực tự phát cao hơn có liên quan đến nhiều thất bại hơn, bất chấp áp lực căng thẳng tương tự. Nỗ lực tự phát tăng lên dẫn đến hiện tượng pendelluft và căng quá mức cục bộ ở vùng lưng phổi, gây ra P-SILI.
Hỗ trợ dựa trên áp lực bằng NIPPV cũng có khả năng làm tăng nguy cơ mắc P-SILI thông qua sự dao động áp lực xuyên phổi cao, được phân bổ không đồng nhất và phóng đại nếu nỗ lực hô hấp được duy trì. Hỗ trợ dựa trên lưu lượng với NHF làm tăng thể tích phổi lúc nghỉ mà không tăng thể tích khí lưu thông hoặc áp lực như trường hợp của NIPPV, về mặt lý thuyết làm giảm nguy cơ mắc PSILI. Tuy nhiên, NHF có một số tác dụng sinh lý có thể làm tăng hoặc giảm nguy cơ thất bại và/hoặc P-SILI ở bệnh nhân mắc AHRF tùy thuộc vào yếu tố nào chiếm ưu thế. Lưu lượng cao hơn, đặc biệt là khi ngậm miệng, làm tăng sức cản đường thở, đòi hỏi phải tăng co cơ hít vào để tạo ra thể tích khí lưu thông tương đương. Điều này làm tăng công việc tổng thể trên mỗi nhịp thở và việc khuếch đại theo khu vực của công việc tăng lên trên mỗi nhịp thở sẽ làm tăng sức căng khu vực dẫn đến lưu lượng pendelluft nhiều hơn. Tuy nhiên, sự gia tăng thể tích phổi cuối thì thở ra và thể tích khí lưu thông không thay đổi sẽ làm giảm cả sức căng tổng thể và khu vực cũng như công trên mỗi nhịp thở, dẫn đến giảm lưu lượng thở ra, giả sử nỗ lực giảm. Sức cản thở ra tăng lên có thể làm giảm tích số áp lực-thời gian bằng cách kéo dài giai đoạn thở ra để giảm nhịp thở và công thở tổng thể. Trong cả hai nghiên cứu của Grieco và cộng sự và Tonelli và cộng sự, nỗ lực hít vào không tương quan đáng kể với mức độ nghiêm trọng của tình trạng thiếu oxy máu (PaO2:FiO2), hạn chế khả năng của PaO2:FiO2 để xác định bệnh nhân có nỗ lực hô hấp có hại— một lỗ hổng kiến thức quan trọng khác để tìm ra các phương pháp lâm sàng đáng tin cậy để đo và theo dõi nỗ lực hô hấp.
Ý nghĩa đối với thực hành ED
Có dữ liệu hạn chế về rủi ro của P-SILI đối với từng phương thức, mặc dù về mặt lý thuyết rủi ro thấp hơn với NHF dựa trên các cơ chế được đề xuất. Cho đến khi các nghiên cứu trong tương lai có thể cung cấp thông tin về những rủi ro này và làm sáng tỏ sinh lý cơ bản, việc cảnh giác theo dõi sự thất bại là cực kỳ quan trọng. Những cạm bẫy dựa trên bằng chứng hiện tại bao gồm trì hoãn đặt nội khí quản ở bệnh nhân có công thở cao do trao đổi khí sai lầm và chuyển từ phương thức NIRS này sang phương thức NIRS khác.
5 Kết luận
Việc sử dụng NIRS trong ED sẽ tiếp tục tăng, đặc biệt khi số lượt thăm khám và thời gian lưu trú tại ED tiếp tục tăng sau đại dịch.3 ED quản lý suy hô hấp mang lại động lực ảnh hưởng đến quá trình nhập viện và kết quả tiếp theo đối với bệnh nhân suy hô hấp cấp tính.115-118 Do đó, điều quan trọng là bác sĩ cấp cứu phải hiểu cách hoạt động của từng phương thức NIRS, mục tiêu của từng dạng suy hô hấp và thậm chí quan trọng hơn là cách theo dõi và hành động khi thất bại.

